Rinita alergică: de la ghiduri la practica medicală
Allergic rhinitis: from guidelines to clinical practice
Abstract
Allergic rhinitis (AR) is a symptomatic disorder induced by the hyperreactivity of the nasal mucosa after allergen exposure. Ever since the first ARIA guideline was published in 2001, the approach of patients with allergic rhinitis has evolved, thanks to new studies and new technologies. In the century of computerization, mobile applications have also emerged in medicine, in order to make life easier for patients and healthcare professionals. The selection of pharmacotherapy for the patient with allergic rhinitis depends on several factors, including age, prominent symptoms, AR control, patient preferences and cost. In the future, clinical decision support systems may be a useful tool based on algorithms for choosing the best treatment for each patient. This article focuses on the current therapeutic options and the recommendations of the European and US guidelines.Keywords
allergic rhinitisARIA guidelinemobile applicationsRezumat
Rinita alergică (RA) este o afecţiune caracterizată prin apariţia de simptome din cauza hiperreactivităţii mucoasei nazale ca urmare a expunerii la un alergen sensibilizant. De la apariţia primului ghid ARIA în 2001, abordarea pacienţilor cu rinită alergică a evoluat, datorită noilor studii şi noilor tehnologii. În secolul informatizării, aplicaţiile mobile şi-au făcut loc şi în medicină, cu scopul de a uşura viaţa pacienţilor şi a personalului medical. Alegerea farmacoterapiei pentru pacientul cu rinită alergică depinde de mai mulţi factori, printre care: vârsta, simptomul principal, controlul RA, preferinţele pacientului şi costul medicaţiei. Sistemele de suport pentru decizia clinică pot reprezenta în viitor o unealtă bazată pe algoritme, utilă în alegerea unui tratament optim pentru fiecare pacient. Articolul este centrat pe opţiunile terapeutice existente în prezent şi pe recomandările în vigoare ale ghidurilor europene şi americane.Cuvinte Cheie
rinită alergicăghid ARIAaplicaţii mobileRinita alergică (RA) este o afecţiune caracterizată de simptome ce apar din cauza hiperreactivităţii mucoasei nazale ca urmare a expunerii la un alergen sensibilizant. Mecanismul fiziopatologic este de cele mai multe ori IgE-mediat. Simptomatologia include rinoree, obstrucţie nazală, prurit nazal şi strănut. Simptomele se remit spontan sau sub tratament. RA se poate însoţi deseori de conjunctivită alergică, manifestată prin prurit şi hiperemie conjunctivală, şi de hiperlăcrimare(1).
RA reprezintă o problemă globală de sănătate, afectând 10% până la 20% din populaţie. Deoarece mulţi pacienţi îşi subestimează afecţiunea, probabil că incidenţa este subapreciată. Deşi de obicei nu este o boală severă, RA afectează viaţa socială, performanţa şcolară şi productivitatea la serviciu(2).
RA şi astmul au caracteristici comune epidemiologice, patologice, fiziologice şi terapeutice. Deseori coexistă, astfel încât 15% până la 38% din pacienţii cu RA suferă şi de astm, iar 6% până la 85% din pacienţii astmatici prezintă şi simptome nazale(3).
Pentru a facilita diagnosticul şi a emite recomandări cu privire la tratamentul RA, în 2001 a fost publicat primul ghid ARIA (Allergic Rhinitis and its Impact on Asthma; Rinita alergică şi impactul ei asupra astmului)(4). Ulterior au fost publicate actualizări şi revizuiri, dintre care cel din 2008 rămâne un reper important pentru clinicieni, cuprinzând date referitoare la epidemiologie, clinică, evaluarea pacientului cu rinită alergică, algoritmul de diagnostic şi tratament(2). Ghidul ARIA a fost preluat de numeroase societăţi naţionale şi a fost tradus în peste 30 de limbi(5). Acesta reprezintă şi în prezent o resursă utilă pentru clinicieni.
Din punctul de vedere al severităţii şi persistenţei simptomatologiei, precum şi al afectării calităţii vieţii, a fost propusă o clasificare a RA în intermitentă/persistentă, respectiv uşoară/moderat-severă. Pentru evaluarea severităţii rinitei, cât şi pentru evaluarea eficienţei tratamentului, a fost propusă o scală analoagă vizuală (VAS; Visual Analogue Scale). VAS a fost validată pe scară largă în multe afecţiuni, fiind un instrument cantitativ. În rinita alergică, VAS a fost validată pentru severitatea simptomatologiei, evaluarea răspunsului la tratament, cât şi pentru scorul global al simptomatologiei. VAS poate avea valori de la 0 la 10 cm, unde 0 reprezintă lipsa simptomatologiei nazale, iar 10 este alocat simptomatologiei nazale foarte supărătoare. Astfel, în funcţie de valoarea VAS aleasă de pacient, RA poate fi clasificată în uşoară (VAS între 0 şi 3), moderată (3,1-7) şi severă (7,1-10)(2,6).
La fel ca şi în alte afecţiuni, abordarea terapeutică a RA trece în prezent de la „un tratament ce se potriveşte tuturor” („one size fits all”) la medicină personalizată şi medicină de precizie. Strategia de tratament se bazează pe combinaţia dintre îngrijire personalizată, predictibilitate a răspunsului favorabil la tratament, prevenţie şi participare a pacientului la elaborarea planului terapeutic. Până la 50% din pacienţii trataţi pentru RA ar dori să fie informaţi cu privire la opţiunile terapeutice disponibile. Astfel, medicul curant ar trebui să prezinte pacientului debutul estimat al acţiunii şi beneficiul opţiunilor terapeutice, evoluţia, siguranţa şi posibilele reacţii adverse ale diferitelor molecule, precum şi informaţii cu privire la impactul terapiei RA asupra comorbidităţilor, cum ar fi astmul, otita medie şi eczema. Participarea pacientului la stabilirea planului terapeutic ar trebui avută în vedere în ceea ce priveşte alegerea căii de administrare (intranazală versus orală), a terapiei combinate versus monoterapie, a preferinţelor legate de corticoterapie şi, nu în ultimul rând, a alegerii imunoterapiei alergen-specifice. Medicina personalizată trebuie aplicată ţinând cont de simptomul/simptomele predominante, de comorbidităţi, endotipul afecţiunii (inflamaţie de tip Th2, inflamaţie mixtă, inflamaţie neurogenică sau afectarea barierei)(7).
Utilizarea tehnologiei informatice şi de comunicaţii în medicină a introdus aplicaţii pentru telefoanele mobile sau tabletele consumatorilor. Aceste aplicaţii au devenit în scurt timp foarte populare în rândul pacienţilor. Au fost create sisteme ce obţin informaţii şi le procesează în vederea îmbunătăţirii accesibilităţii la tratament. Mobile Airways Sentinel networK (MASK) reprezintă a treia fază a iniţiativei ARIA şi a fost inţiată pentru a reduce povara globală a multimorbidităţilor din rinită şi astm, oferind pacienţilor şi profesioniştilor din domeniul medical unelte simple pentru a preveni şi trata mai corect afecţiunile respiratorii alergice. Aplicaţia MASK (the allergy diary) este disponibilă pentru descărcare în anumite ţări ale Uniunii Europene şi este combinată cu o funcţie interoperabilă pe o tabletă a unui medic sau a unui profesionist din domeniul medical. Pacientul introduce zilnic scorul VAS în aplicaţie şi medicaţia utilizată. Sistemele de suport pentru decizia clinică (SSDC) sunt algoritmi software care ajută personalul medical în privinţa diagnosticului şi abordării pacienţilor prin interacţiunea datelor pacienţilor şi a informaţiei medicale, precum prescrierea medicamentelor. SSDC ar trebui să se bazeze pe dovezile şi algoritmii cei mai buni pentru a ajuta pacienţii şi medicii să descopere împreună tratamentul optim şi strategia de step-up sau step-down pentru un control eficient al bolii(8).
Alegerea farmacoterapiei pentru pacienţii cu RA depinde de mai mulţi factori, inclusiv vârsta, simptomele predominante, severitatea lor, nivelul de control al RA, preferinţele pacientului şi cost. SSDC poate fi util prin evaluarea controlului bolii şi al răspunsului la tratament. Bousquet şi colab. fac o analogie între strategia de tratament al pacientului astmatic bazată pe controlul bolii şi opţiunile de step-up sau step-down. Ca şi în cazul astmului, se recomandă ca cel mai bun control al RA să fie obţinut cât mai curând posibil pentru a îmbunătăţi satisfacţia pacientului şi aderenţa la tratament şi pentru a reduce consecinţele RA, precum simptomele, afectarea calităţii vieţii şi absenteismul de la şcoală/serviciu(9).
Acest algoritm pentru controlul simptomatologiei RA se bazează pe recomandările ghidului ARIA 2016(3), care formulează recomandări cu nivel de evidenţă ridicat pentru anumite situaţii clinice. De asemenea, există recomandări în funcţie de existenţa anterioară a unui tratament al RA, făcând analogii cu terapia astmului (figurile 1 şi 2).
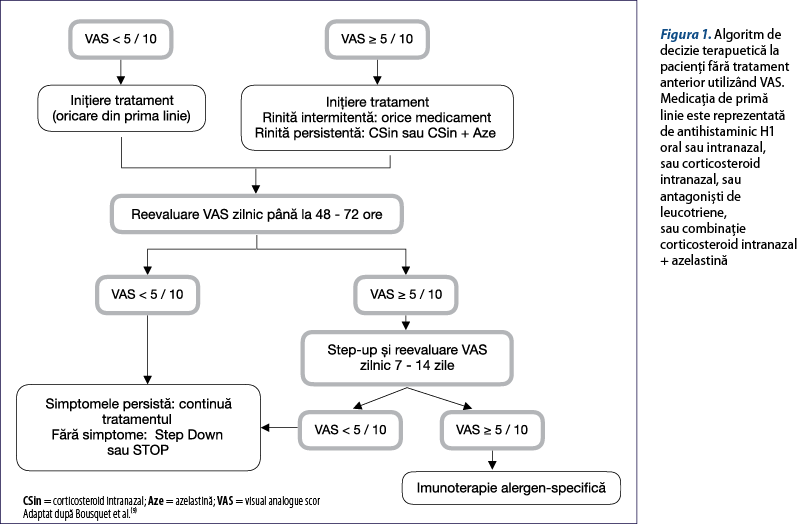
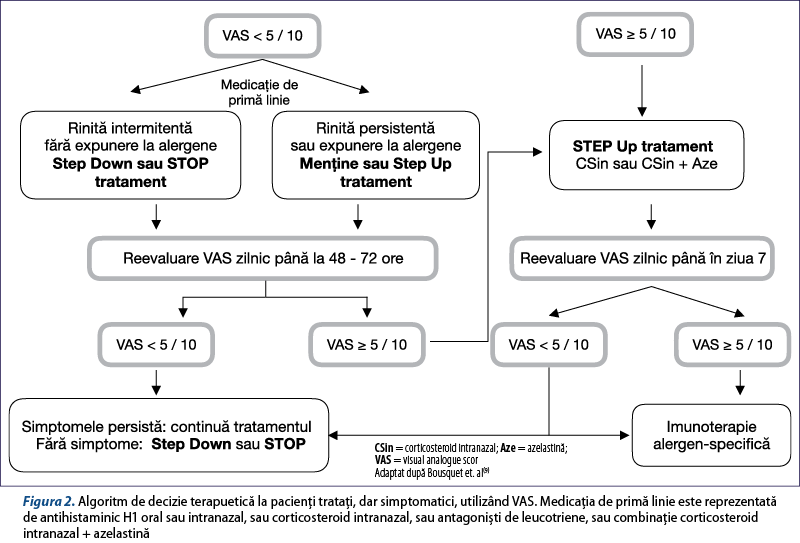
Treptele de tratament în funcţie de severitatea simptomelor sunt:
-
Pentru simptome uşoare se recomandă antihistaminic H1 oral sau intranazal.
-
Pentru simptome moderat-severe şi/sau rinită persistentă, terapia de primă intenţie este reprezentată de corticosteroizii intranazali. Doza pentru anumite molecule de corticosteroizi intranazali poate fi crescută conform prospectului.
-
Pacienţii cu simptome necontrolate în treapta 2 au indicaţie pentru combinaţia corticosteroid intranazal şi antihistaminic intranazal. Cu toate acestea, în funcţie de experienţa medicului, pot fi folosite şi alte strategii terapeutice.
-
Este posibil ca o cură scurtă de corticosteroizi orali să poată ajuta la obţinerea rapidă a controlului şi apoi să se continue cu treapta 3.
Reevaluarea pacientului trebuie făcută la 1-7 zile după iniţierea tratamentului pentru a confirma controlul sau a creşte treapta de tratament(9).
În mod similar, se poate utiliza un algoritm de step-down, iar treapta 3 poate fi considerată primul nivel de tratament la pacienţi cu răspuns anterior slab la monoterapie.
Dykewicz şi colab., într-un update al ghidului de tratament al RA sezoniere (US Practice Parameters), recomandă ca tratament iniţial la pacienţii cu vârsta de peste 12 ani corticosteroid intranazal ca monoterapie, afirmând că nu există dovezi asupra eficacităţii superioare a combinaţiei corticosteroid intranazal şi antihistaminic H1 oral. De asemenea, este subliniată superioritatea tratamentului cu corticosteroid intranazal faţă de antagonist de receptori pentru leucotriene la pacienţii cu vârsta de peste 15 ani. Pentru formele moderat-severe, recomandarea de primă intenţie este combinaţia corticosteroid intranazal cu antihistaminic H1 intranazal(10). Pentru a îmbunătăţi controlul iniţial al simptomelor, combinaţia de corticosteroid intranazal cu antihistaminic intranazal este superioară monoterapiei cu oricare dintre cele două substanţe(11). Cele mai frecvente reacţii adverse ale acestei combinaţii sunt reprezentate de gustul amar, epistaxis şi cefalee. Cu toate acestea, studiul amintit a demonstrat, ca obiective secundare, o reducere a simptomelor oculare şi ameliorarea calităţii vieţii. De asemenea, experţii recomandă ca atunci când un pacient este sub tratament cu corticosteroid intranazal şi simptomele nu sunt complet anulate, trebuie avută în vedere adăugarea în schema de tratament a unui antihistaminic H1 intranazal în defavoarea unuia oral(10). În prezent nu există studii care să compare eficacitatea tratamentului antihistaminic H1 intranazal cu cel oral. Ghidul ARIA 2016 recomandă utilizarea oricărui preparat în formele uşoare de RA sezonieră sau perenă.
Imunoterapia alergen-specifică este indicată la pacienţi cu simptomatologie de rinită, cu sau fără conjunctivită. Simptomatologia trebuie să fie indusă de expunerea la un alergen sensibilizant, sensibilizare dovedită prin teste cutanate prick sau IgE specifice. Identificarea alergenului sau alergenelor responsabile de apariţia simptomelor este primul pas în alegerea corectă a produsului pentru imunoterapie. În cazurile în care testarea cutanată prick sau a IgE specifice nu este concludentă, poate fi utilizat diagnosticul bazat pe componente moleculare. Conform ghidului ARIA, imunoterapia alergen-specifică trebuie recomandată pacienţilor cu simptome moderat-severe, intermitente sau persistente, ce nu pot fi controlate de măsurile de profilaxie şi terapia farmacologică standard. De asemenea, imunoterapia poate fi folosită la pacienţi cu simptome mai uşoare care vor să beneficieze de efectul pe termen lung asupra simptomelor de rinită şi de potenţialul modificator al bolii, de a preveni astmul. Ghidul EAACI pentru imunoterapie recomandă utilizarea doar a extractelor standardizate, a căror eficienţă a fost dovedită prin studii clinice. Pacienţii polisensibilizaţi, cu sensibilizare relevantă la alergene omoloage înrudite taxonomic, pot primi tratament cu un singur alergen sau un amestec de alergene omoloage din acea familie biologică ce acoperă alergenele majore. Pacienţii polisensibilizaţi la alergene neomoloage pot primi recomandare de iniţiere a imunoterapiei cu alergenul ce produce majoritatea simptomelor rinoconjunctivale sau două tratamente separate cu două dintre alergenele cele mai importante(12).
Utilizarea aplicaţiilor pe dispozitivele mobile ale pacienţilor a permis obţinerea de date pe loturi mari de pacienţi, în afara studiilor, cu dovezi din viaţa reală. Un prim studiu care urmăreşte aderenţa la tratament a pacienţilor cu RA a arătat că există o diferenţă semnificativă între teorie şi practică. Toate recomandările de tratament al RA sunt pentru o continuitate a medicaţiei, pe când studiul a arătat că aderenţa la tratament este scăzută, adică pacienţii au tendinţa de a utiliza tratamentul la nevoie. Este necesară o consiliere mai atentă a pacienţilor. În viaţa reală, pacienţii urmează foarte rar ghidurile. Aproximativ 70% dintre pacienţii cu RA care au completat datele în aplicaţie nu urmează tratamentul prescris întocmai. Doar 11,3% urmau tratamentul prescris complet şi pe durata prescrisă. Utilizarea unei aplicaţii mobile ar putea îmbunătăţi aderenţa la tratament şi selecţiona pacienţii care au nevoie de îngijire într-un centru terţiar sau pot beneficia de imunoterapie alergen-specifică(13).
O formă particulară de RA este rinita alergică locală, caracterizată de un răspuns inflamator, mediat de IgE, limitat la nivelul mucoasei nazale. Valoarea IgE serice este în limite normale, iar testele cutanate prick la aeroalergenele posibil incriminate sunt negative. Studiile au arătat că RA locală ar reprezenta aproximativ 26% din toate cazurile de rinită şi până la 70% din cazurile de rinită non-alergică. Acest diagnostic ar trebui suspicionat atunci când anamneza este înalt sugestivă pentru RA, dar evaluarea alergologică obişnuită nu relevă o sensibilizare clinică. Standardul de aur pentru diagnosticul acestei forme este testul de provocare nazală, deşi în prezent se cercetează şi alte modalităţi de evaluare, precum testul de activare a bazofilului(14).
Tratamentul pacienţilor diagnosticaţi cu rinită alergică trebuie personalizat, pornind de la ghiduri, aplicând principiile medicinei de precizie şi ţinând cont de preferinţele individuale. Aplicaţiile pe telefoane sau tablete pot furniza informaţii ce pot ajuta la alegerea celui mai bun tratament pentru fiecare pacient.
Bibliografie
- Brozek JL, Bousquet J, Baena-Cagnani CE, Bonini S, Canonica GW, Casale TB, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines: 2010 revision. J Allergy Clin Immunol. 2010; 126:466-76.
- Bousquet J, Khaltaev N, Cruz AA, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 update (in collaboration with the World Health Organization, GA(2)LEN and AllerGen). Allergy. 2008; 63(Suppl 86):8-160.
- Brozek JL, Bousquet J, Agache I, Agarwal A, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines – 2016 revision. J Allergy Clin Immunol. 2017; 140:950-8.
- Bousquet J, Van Cauwenberge P, Khaltaev N. Allergic rhinitis and its impact on asthma. J Allergy Clin Immunol. 2001; 108(Suppl. 5):S147– S334.
- Bousquet J, Schunemann HJ, Samolinski B, Demoly P, et al. Allergic Rhinitis and its Impact on Asthma (ARIA): Achievements in 10 years and future needs. J Allergy Clin Immunol. 2012; 130:1049-62.
- Bousquet PJ, Combescure C, Neukirch F, Klossek JM, Mechin H, Daures JP, et al. Visual analog scales can assess the severity of rhinitis graded according to ARIA guidelines. Allergy. 2007; 62:367–372.
- Hellings PW, Fokkens WJ, Bachert C, Akdis CA, et al. Positioning the principles of precision medicine in care pathways for allergic rhinitis and chronic rhinosinusitis – A EUFOREA-ARIA-EPOS-AIRWAYS ICP statement. Allergy. 2017; 72:1297–1305.
- Bousquet J, Arnavielhe S; MASK study group. MASK 2017: ARIA digitally-enabled, integrated, person-centred care for rhinitis and asthma multimorbidity using real-world-evidence. Clin Transl Allergy. 2018; 8:45.
- Bousquet J, Schunemann HJ, Hellings PW, Arnavielhe S, Bachert C, Bedbrook A, et al. MACVIA clinical decision algorithm in adolescents and adults with allergic rhinitis.
- J Allergy Clin Immunol. 2016; 138(2):367–74 (e2).
- Dykewicz MS, Wallace DV, Baroody F, Bernstein J, et al. Treatment of seasonal allergic rhinitis. An evidence-based focused 2017 guideline update. Ann Allergy Asthma Immunol. 2017; 119; 489e511.
- Meltzer EO, LaForce C, Ratner P, Price D, Ginsberg D, Carr W. MP29-02 (a novel intranasal formulation of azelastine hydrochloride and fluticasone propionate) in the treatment of seasonal allergic rhinitis: a randomized, double-blind, placebo-controlled trial of efficacy and safety. Allergy Asthma Proc. 2012; 33:324e332.
- Roberts G, Pfaar O, Akdis CA, et al. EAACI Guidelines on Allergen Immunotherapy: Allergic rhinoconjunctivitis. Allergy. 2018; 73:765–798.
- Menditto E, Costa E, Midão L, et al., the MASK group. Adherence to treatment in allergic rhinitis using mobile technology. The MASK Study. Clin Exp Allergy. 2019; 49: 442-460.
- Duarte Ferreira R, Ornelas C, Silva S, Morgado R, et al. Contribution of In Vivo and In Vitro Testing for The Diagnosis of Local Allergic Rhinitis. J Investig Allergol Clin Immunol. 2019; Vol. 29(1): 46-48.



