Metode de prezervare a fertilităţii la femeile supuse terapiei gonadotoxice sau chirurgiei gonadoreductoare
Fertility preservation methods in women subjected to gonadotoxic treatment or gonadoreducing surgery
Abstract
All patients in whom gonadotoxic treatment or gonadal resection is recommended and also present future reproductive intentions should be referred to a specialist in infertility and endocrinology to be detailed fertility preservation options. The gold standard in these cases is the cryopreservation of embryos, being superior to the freezing of oocytes or other techniques. For the cases where freezing embryos it is not possible, cryopreservation of mature oocytes is reasonable. Maturation of oocytes in vitro is an experimental method, with implantation and pregnancy rates lower than if using oocytes matured in vivo. Ovarian tissue cryopreservation is an investigational technique not recommended in patients with ovarian cancer or at increased risk for this pathology, with still uncertain eficacy, but more and more increasingly used. If cryopreservation of embryos or oocytes is not feasible, alternative methods are needed to protect fertility. For cases which are to undergo pelvic radiotherapy, but not to chemotherapy, ovarian transposition outside the field of radiation may be an option. The use of GnRH agonists in women following chemotherapy is not recommended, having unproven benefits and theoretical risks. Alternative methods (ovarian tissue transplantation, donation of oocytes or embryos, the use of surrogate mothers, adoption) are the last choices for cases where the other methods are not available.Keywords
gonadotoxic treatmentgonadoreducing surgeryfertility preservationRezumat
Toate pacientele la care se recomandă tratament gonadotoxic sau rezecţie gonadală şi prezintă totodată intenţii reproductive pentru viitor trebuie îndrumate către un specialist în infertilitate şi endocrinologie, pentru a li se detalia opţiunile de prezervare a fertilităţii. Standardul de aur în aceste cazuri este reprezentat de criogenarea de embrioni, fiind superioară congelării de ovocite sau altor tehnici. Pentru cazurile în care congelarea embrionilor nu este posibilă, criogenarea de ovocite mature este rezonabilă. Maturarea ovocitelor in vitro este o metodă experimentală, cu rate de implantare şi obţinere a unei sarcini inferioare utilizării de ovocite maturate in vivo. Crioprezervarea ţesutului ovarian este o tehnică investigaţională, nerecomandată la pacientele cu cancer ovarian sau cu risc crescut pentru această patologie, cu eficacitate încă incertă, dar din ce în ce mai utilizată. Dacă criogenarea de embrioni sau ovocite nu este fezabilă, sunt necesare metode alternative de protejare a fertilităţii. Pentru cazurile care urmează să fie supuse radioterapiei pelviene, dar nu chimioterapiei, transpoziţia ovariană în afara câmpului de iradiere poate fi o opţiune. Utilizarea de agonişti de GnRH la femeile urmând chimioterapie nu este recomandată, având beneficii nedovedite şi riscuri teoretice. Metodele alternative (transplantul de ţesut ovarian, donarea de ovocite sau embrioni, utilizarea de mame-surogat, adopţia) reprezintă alegeri de ultimă intenţie pentru cazurile la care celelalte metode nu sunt disponibile.Cuvinte Cheie
tratament gonadotoxicchirurgie gonadoreductoareprezervarea fertilităţiiIntroducere
Necesitatea apariţiei şi dezvoltării metodelor de conservare a fertilităţii pacientelor supuse tratamentelor citotoxice sau chirurgiei gonadoreductoare a apărut odată cu creşterea ratelor de supravieţuire în patologia malignă şi autoimună şi totodată a fost susţinută de progresul medicinei reproductive. Opţiunea alegerii unei metode de prezervare a potenţialului fertil trebuie oferită oricărei paciente cu vârsta sub 40 de ani, conform majorităţii studiilor, sau 35 de ani, conform altora, care prezintă risc crescut de insuficienţă ovariană prematură(1). Având în vedere complexitatea şi particularitatea acestor metode, este imperativă opinia unui specialist în medicina reproductivă, infertilitate şi endocrinologie, care, în funcţie de caracteristicile pacientei (afecţiunea malignă sau autoimună, tratamentul citotoxic sau chirurgia gonadoreductivă planificate, vârsta pacientei, dorinţa de reproducere ulterioară, existenţa unui partener, costuri), va individualiza managementul(2).
Consilierea pacientei pre-tratament este extrem de importantă în aceste cazuri, planificarea sa fiind optimă imediat după comunicarea diagnosticului(3). Recomandările Societăţii Americane de Oncologie Clinică şi ale Societăţii Americane de Medicină Reproductivă includ dorinţa femeii în alegerea metodei de prezervare a funcţiei reproductive, aceste paciente prezentând provocări reproductive atât din punct de vedere medical, cât şi social. Aceste măsuri trebuie demarate cu două săptămâni înainte de iniţierea tratamentului citotoxic, iar riscurile lor au fost apreciate ca minime pe studii prospective de dimensiuni medii (figura 1)(4).
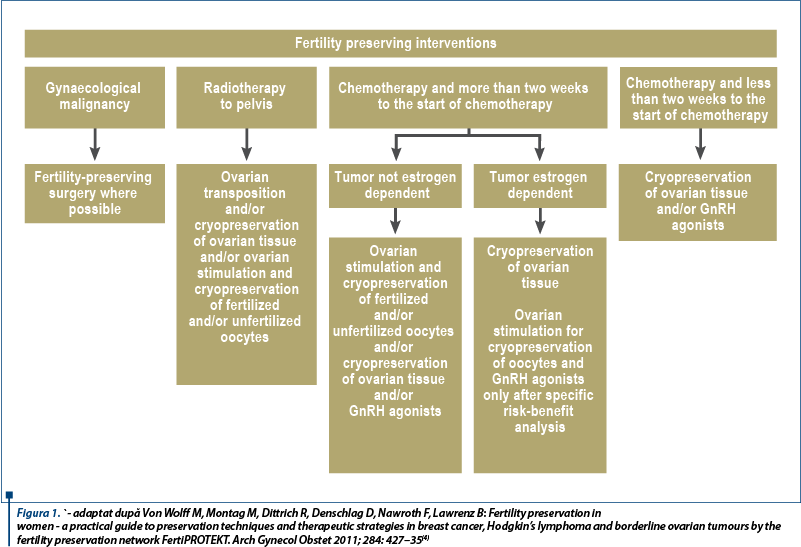
Metode de prezervare a fertilităţii
Nu au fost efectuate încă studii randomizate pentru compararea intervenţiilor terapeutice detaliate mai jos în ceea ce priveşte impactul asupra infertilităţii sau supravieţuirea pe termen lung. Singura recomandare comună este reprezentată de atenţionarea asupra riscurilor procedurilor de reproducere umană asistată în cazul pacientelor cu cancere estrogen-dependente, din cauza nivelurilor estrogenice crescute generate în cursul acestor terapii.
Crioprezervarea
Reprezintă o metodă de păstrare a potenţialului reproductiv cu rezultate dovedite, a cărei eficienţă a fost dovedită clinic, aproximativ un sfert din toate procedurile de reproducere umană asistată utilizând embrioni crioprezervaţi(5). Se pot congela embrioni, ovocite mature sau imature, ţesut ovarian sau ovarul integru cu pedicul vascular intact, ca metodă experimentală. Embrionii şi ovocitele congelate pot rămâne viabile câţiva ani, însă embrionii crioprezervaţi au o rezistenţă superioară la decongelare comparativ cu ovocitele nefertilizate.
Crioprezervarea embrionilor
Crioprezervarea embrionilor este o procedură standardizată, utilizată frecvent în cadrul ciclurilor de fertilizare in vitro. La pacientele diagnosticate cu malignităţi care urmează să fie supuse tratamentului citotoxic există însă particularităţi. În primul rând, există un interval scurt de timp de la diagnostic şi până la iniţierea chimioterapiei sau radioterapiei, în care poate fi efectuată. Astfel, stimularea ovariană, pentru care este necesar un interval liber de două-trei săptămâni, nu poate fi efectuată în toate cazurile, uneori tratamentul gonadotoxic fiind iniţiat imediat. Din cauza acestor restricţii temporale, s-a încercat recoltarea de ovocite în timpul fazei luteale fără stimulare prelabilă, cu maturarea şi fertilizarea lor in vitro şi ulterior crioprezervarea acestor embrioni(6). O altă modalitate prin care se scurtează intervalul de timp necesar stimulării ovariene este reprezentată de iniţierea sa indiferent de momentul ciclului menstrual, de obicei cu asociere de hCG şi analog de GnRH. Odată începută chimioterapia, este contraindicată stimularea ovariană, din cauza alterărilor la nivelul ADN-ului ovocitar, fiind necesare cel puţin şase luni de la întreruperea agenţilor citotoxici, mai ales dacă aceştia sunt alchilanţi (de exemplu, ciclofosfamida) pentru a demara acţiunile reproductive(7). În cazul pacientelor fără partener, opţiunea unei fertilizări in vitro poate fi oferită doar apelând la o bancă de spermă. Există de asemenea şi ţări în care legislaţia interzice crioprezervarea embrionilor, apărând astfel probleme etico-legale. O situaţie particulară este reprezentată de femeile care prezintă tumori estrogen-dependente, la care stimularea ovariană este controversată, din cauza riscului de creştere tumorală(8).
Crioprezervarea ovocitelor
Reprezintă o opţiune viabilă pentru femeile care nu au un partener şi refuză ideea de donator de spermă în vederea fertilizării in vitro. Şansele de supravieţuire a ovocitelor mature la decongelare sunt mai mici comparativ cu embrionii, deoarece conţinutul lor în apă este mai mare şi astfel rezistenţa la criogenare este mai mică, din cauza formării cristalelor de gheaţă. Există două modalităţi de congelare, şi anume lentă şi, respectiv, vitrificarea, care este o metodă de criogenare foarte rapidă, utilizând agenţi crioprotectori, şi pare a avea rezultate superioare(9). Probabilitatea de a da naştere unui făt viu utilizând ovocite mature criogenate depinde de: vârsta pacientei, metoda de congelare, numărul de ovocite congelate şi, respectiv, care au rezistat la decongelare şi numărul de embrioni transferaţi. S-au ridicat şi probleme legate de posibilitatea apariţiei anomaliilor cromozomiale fetale cauzate de afectarea fusului de diviziune ovocitar în timpul crioprezervării(10).
Ca metodă investigaţională a fost folosită şi recoltarea de ovocite imature atât de la nivel in situ, cât şi din ţesut ovarian excizat, cu maturarea lor in vitro fie înainte de congelare, fie după decongelare. Ovocitele proaspete prezintă însă o rată de succes superioară pentru maturare in vitro comparativ cu cele criogenate. Metoda prezintă numeroase avantaje: sunt evitate stimularea ovariană şi astfel prelungirea timpului până la iniţierea tratamentului, poate fi utilizată în cazul tumorilor estrogen-dependente, iar ovocitele imature sunt mai rezistente la procesul congelare/decongelare, pentru că nu prezintă fus de diviziune(11). Totuşi, fiind încă o metodă în curs de standardizare, ratele de obţinere a unei sarcini sunt inferioare folosirii de ovocite mature sau embrioni criogenaţi.
Crioprezervarea ovarului
Crioprezervarea ovarului cu pedicul vascular integru este o tehnică experimentală, dificil de efectuat tehnic. Are însă avantajul de a evita pierderea foliculară masivă care apare odată cu ischemia tranzitorie post-transplantare.
Crioprezervarea ţesutului ovarian
Congelarea de fragmente ovariene cu implantarea lor ulterioară heterotopică - la nivelul peretelui abdominal, al antebraţului sau al toracelui - ori ortotopică, la nivelul ţesutului ovarian restant sau al peritoneului pelvian, reprezintă o altă metodă în curs de investigaţie. Această abordare poate fi utilă la paciente la prepubertate sau atunci când tratamentul citotoxic trebuie iniţiat imediat. Ca metodă suplimentară de siguranţă, pot fi recoltate de la nivelul acestor fragmente ovocite imature şi ulterior congelate. Este important ca partea exterioară a ovarului să fie prezervată, întrucât toţi foliculii care conţin ovocite sunt situaţi în porţiunea de 1 milimetru de la suprafaţa ovariană(12).
Indicaţiile crioprezervării ovariene
Selectarea pacientelor care sunt candidate pentru crioprezervare ovariană conform criteriilor Edinburgh este restrictivă şi include femei cu vârsta sub 35 de ani, care nu au copii şi la care riscul apreciat de insuficienţă ovariană post-tratament este de cel puţin 50%. Aceste criterii stricte necesită adaptare individualizată, deoarece există femei cu vârsta peste 35 de ani care prezintă o rezervă ovariană bună, femei care, deşi au copii, îşi doresc să mai conceapă după tratamentul gonadotoxic sau femei care, dimpotrivă, îşi doresc să amâne planurile reproductive mai mult timp după chimio- sau radioterapie(13).
Contraindicaţiile şi riscurile crioprezervării ovariene
O contraindicaţie pentru prezervarea ovariană o reprezintă prezenţa sau riscul de a dezvolta cancer ovarian. În acest sens, femeile purtătoare de mutaţii la nivelul genelor BRCA1 şi BRCA2 au un risc de dezvoltare a unei malignităţi ovariene de 60%, respectiv 10-20% pe parcursul vieţii. Pentru aceste paciente, recomandarea de ooforectomie bilaterală profilactică după încheierea planului reproductiv este optimă(14). Atunci când această procedură este efectuată însă la vârste tinere sau la paciente care nu au procreat, problema prezervării ţesutului ovarian este delicată, din cauza riscului crescut de cancer ovarian ocult (2-18,5%). În cazul în care se optează pentru criogenarea ovariană, analiza histopatologică detaliată prealabilă este imperativă, testarea imunohistochimică suplimentară fiind recomandată. Pentru cancerele extraovariene există riscul de autotransplant al fragmentelor ovariene conţinând micrometastaze pentru malignităţile sangvine, limfomul Burkitt, neuroblastom sau carcinomul lobular mamar(15).
Protejarea funcţiei ovariene native
Consultarea unui specialist în fertilitate este recomandată pentru toate pacientele diagnosticate cu afecţiuni maligne sau care necesită tratament gonadotoxic înaintea iniţierii acestuia, pentru a stabili strategia de protejare a potenţialului reproductiv. Aceste metode protective depind în mare măsură şi de tipul de tratament citotoxic la care urmează să fie supusă pacienta, de obicei radioterapie, chimioterapie sau ambele(16).
Protejarea funcţiei ovariene la paciente supuse radioterapiei
Ţesutul ovarian este susceptibil la efectul radiaţiilor ionizante prin alterările la nivelul ADN-ului, generând astfel atrofie şi reducerea semnificativă a numărului de foliculi ovarieni. Efectul nociv al radioterapiei asupra ovarului depinde de vârsta pacientei, de doza de radiaţie şi de asocierea posibilă cu chimioterapia(17).
Transpoziţia ovariană
Ovaropexia cu mutarea ovarelor în afara câmpului de radiaţie este o metodă simplă, uşor de realizat şi cu costuri reduse, cu eficienţă în limitarea efectelor adverse ale radioterapiei. Procedura poate fi realizată laparoscopic înaintea iniţierii terapiei, pentru a evita posibilitatea migrării ovarului către câmpul de radiaţie. Au fost descrise şi metode combinate de prezervare a fertilităţii: crioprezervarea unui ovar cu pexia celuilalt la distanţă de aria de radioterapie. Factorii de prognostic negativ ai acestei metode sunt reprezentaţi de radiaţia dispersată în afara câmpului stabilit, afectarea vascularizaţiei şi doza totală iradiantă(18). Printre posibilele complicaţii ale metodei se numără durerea pelviană cronică, infarctul tubar, apariţia chisturilor ovariene şi migrarea ovarului către poziţia anatomică.
Ecranarea
Pentru a minimiza efectul radiaţiei dispersate în cazul iradierii tumorilor non-pelviene se poate folosi ecranarea ovarelor cu şorţ de protecţie situat la nivelul pelvisului(19).
Autotransplantul
Pentru cazurile de tumori situate la nivel pelvian care necesită iradiere, o soluţie de protejare a fertilităţii este recoltarea ovarului şi autotransplantul acestuia la nivelul porţiunii superioare a corpului (braţ, perete toracic). Deşi reprezintă o modalitate facilă şi eficientă teoretic, realizarea sa practică întâmpină dificultăţi tehnice(20).
Protejarea funcţiei ovariene la paciente supuse chimioterapiei
Pentru femeile care urmează să fie tratate cu agenţi citotoxici sunt disponibile ca modalităţi de protejare a fertilităţii tehnicile de crioprezervare descrise mai sus, la care poate fi asociată administrarea de agonişti GnRH, metodă larg dezbătută, pentru care nu s-a stabilit încă un consens.
Agoniştii GnRH
Recomandările specialiştilor privind tratamentul cu agonişti GnRH la pacientele care nu pot beneficia de crioprezervare, în vederea menţinerii potenţialului reproductiv, sunt încă în dezbatere, beneficiile acestuia fiind încă nedovedite. Studiile randomizate pe loturi mari de paciente nu au arătat efecte benefice semnificative după utilizarea agoniştilor GnRH pentru prezervarea fertilităţii, cuantificate prin nivelul hormonului antimüllerian şi numărarea foliculilor antrali. Mecanismul lor protectiv se presupune a fi prin inhibarea funcţiei ovariene şi astfel evitarea acţiunii nocive a chimioterapiei sau a radioterapiei la nivelul gonadelor. Însă efectul distructiv la nivel de ADN este independent de funcţia ovariană şi, mai mult de atât, foliculii primordiali care ar trebui protejaţi nu exprimă receptori pentru gonadotropine(21,22).
În general, studiile care au arătat o rată mai mică de insuficienţă ovariană prematură la pacientele care au primit agonişti GnRH au prezentat criterii de includere foarte flexibile, femeile primind regimuri chimioterapice diferite, iar loturile de studiu au fost de mică amploare. Această linie terapeutică este foarte eficientă pentru pacientele care prezintă menometroragii sau risc crescut de menoragii cauzate de trombocitopenia severă indusă de medicaţia citotoxică. Ideal, medicaţia trebuie iniţiată cu două-trei săptămâni înaintea chimioterapiei, efectele sale adverse incluzând uscăciunea mucoasei vaginale şi bufeurile. Siguranţa utilizării agoniştilor GnRH este de asemenea dezbătută, întrucât receptorii GnRH sunt exprimaţi de o serie de celule maligne şi au roluri biologice, existând riscul de a scădea efectul chimioterapiei atunci când sunt administraţi concomitent cu aceasta(23).
Metode alternative
Transplantul de ţesut ovarian
Transplantul poate fi de tip autolog heterotopic, utilizând ţesut ovarian proaspăt sau criogenat, ori non-autolog ortotopic, cu ovar sau ţesut ovarian de la o donatoare compatibilă. Transplantul autolog heterotopic poate fi indicat la pacientele care urmează să fie iradiate la nivel pelvian sau după chimioterapie, un ovar integru cu pedicul sau o fâşie de ţesut ovarian putând fi implantate subcutanat la nivelul antebraţului, al peretelui abdominal sau al toracelui(21). Au fost raportate cazuri de naşteri de feţi vii consecutive acestei proceduri, după metode de reproducere asistată, deşi există o perioadă limitată de funcţionalitate a ţesutului ovarian transplantat, evaluată la trei ani, din cauza injuriei ischemice post-implantare. Transplantul non-autolog ortotopic a fost raportat prima dată în cazul a două surori gemene monozigote, însă acesta are riscul major de a putea cauza insuficienţă ovariană prematură la pacienta donatoare. Având în vedere şi faptul că necesită o donatoare identică imunologic, este preferată de cele mai multe ori donarea de ovocite în detrimentul acestei metode.
Trachelectomia radicală
Pentru cazurile de cancer de col uterin stadializate până la Ib inclusiv, trachelectomia radicală practicată în detrimentul histerectomiei poate menţine potenţialul reproductiv cu prognostic bun în ceea ce priveşte evoluţia unei viitoare sarcini.
Donarea de ovocite
Pentru pacientele care prezintă uter intact, dar nu deţin ovocite proaspete sau criogenate ori ţesut ovarian care să le producă, băncile de ovocite pot reprezenta o opţiune. Dacă sperma partenerului poate fi folosită, poate fi obţinută o sarcină prin fertilizare in vitro.
Donarea de embrioni
Femeile care au uter, dar nu au nici partener, nici rezervă ovariană, pot apela la donarea de embrioni congelaţi, donaţi cel mai frecvent de cuplurile care apelează la proceduri de fertilizare in vitro în care rămân în exces.
Mame-surogat
Utilizarea unei mame-surogat este utilă în cazul pacientelor care deţin ovocite native sau criogenate, dar nu au uter, care doresc să evite o sarcină din cauza riscului crescut de cancer de sân recurent sau din cauza tratamentului cronic cu inhibitori de aromatază, ori nu vor să aştepte până la finalul tratamentului cu letrozol sau tamoxifen pentru neoplasm mamar. Există şi posibilitatea ca mama-surogat să fie totodată şi donatoare de ovocite la femeile care nu au posibilitatea de a utiliza propriile ovocite, ea având în acest caz şi o legătură genetică, nu doar gestaţională cu fătul.
Adopţia
Dacă celelalte metode descrise mai sus sunt indisponibile sau pacienta preferă acest lucru, adopţia reprezintă o opţiune valabilă.
Transplantul uterin
Transplantul uterin este în curs de investigare, fiind util la pacientele cu histerectomie, cu afectare a funcţionalităţii uterului post-iradiere pelviană sau cu anomalii congenitale. Tehnica este încă la nivel experimental, cu numeroase riscuri.
Concluzii
Toate pacientele la care este necesar tratamentul gonadotoxic sau rezecţia gonadală şi au totodată intenţii reproductive pentru viitor trebuie îndrumate către un specialist în infertilitate şi endocrinologie, pentru a li se detalia opţiunile de prezervare a fertilităţii. Acest aspect este extrem de important pentru asigurarea respectării dreptului reproductiv al femeii şi, astfel, a unei calităţi a vieţii optime. Standardul de aur în aceste cazuri este reprezentat de criogenarea de embrioni, fiind superioară congelării de ovocite sau altor tehnici.
Bibliografie
1. Loren AW, Mangu PB, Beck LN, et al. Fertility preservation for patients with cancer: American Society of Clinical Oncology clinical practice guideline update. J Clin Oncol 2013;31:2500.
2. The Practice Committee of the American Society for Reproductive Medicine. Fertility preservation in patients undergoing gonadotoxic therapy or gonadectomy: a committee opinion. Fertil Steril 2013;100:1214.
3. The Ethics Committee of the American Society for Reproductive Medicine. Fertility preservation and reproduction in patients facing gonadotoxic therapies: a committee opinion. Fertil Steril 2013;100:1224.
4. Von Wolff M, Montag M, Dittrich R, Denschlag D, Nawroth F, Lawrenz B: Fertility preservation in women - a practical guide to preservation techniques and therapeutic strategies in breast cancer, Hodgkin’s lymphoma and borderline ovarian tumours by the fertility preservation network FertiPROTEKT. Arch Gynecol Obstet 2011; 284:427–35.
5. Das M, Shehata F, Moria A, et al. Ovarian reserve, response to gonadotropins, and oocyte maturity in women with malignancy. Fertil Steril 2011;96:122.
6. Knopman JM, Noyes N, Talebian S, et al. Women with cancer undergoing ART for fertility preservation: a cohort study of their response to exogenous gonadotropins. Fertil Steril 2009; 91:1476.
7. Robertson AD, Missmer SA, Ginsburg ES. Embryo yield after in vitro fertilization in women undergoing embryo banking for fertility preservation before chemotherapy. Fertil Steril 2011; 95:588.
8. Pal L, Leykin L, Schifren JL, et al. Malignancy may adversely influence the quality and behaviour of oocytes. Hum Reprod 1998;13:1837.
9. Quintero RB, Helmer A, Huang JQ, Westphal LM. Ovarian stimulation for fertility preservation in patients with cancer. Fertil Steril 2010; 93:865.
10. Domingo J, Guillén V, Ayllón Y, et al. Ovarian response to controlled ovarian hyperstimulation in cancer patients is diminished even before oncological treatment. Fertil Steril 2012; 97:930.
11. Barton SE, Missmer SA, Berry KF, Ginsburg ES. Female cancer survivors are low responders and have reduced success compared with other patients undergoing assisted reproductive technologies. Fertil Steril 2012; 97:381.
12. Soleimani R, Heytens E, Oktay K. Enhancement of neoangiogenesis and follicle survival by sphingosine-1-phosphate in human ovarian tissue xenotransplants. PLoS One 2011;6:e19475.
13. Borini A, Levi Setti PE, Anserini P, et al. Multicenter observational study on slow-cooling oocyte cryopreservation: clinical outcome. Fertil Steril 2010; 94:1662.
14. Scaravelli G, Vigiliano V, Mayorga JM, et al. Analysis of oocyte cryopreservation in assisted reproduction: the Italian National Register data from 2005 to 2007. Reprod Biomed Online 2010; 21:496.
15. Huang JY, Tulandi T, Holzer H, et al. Combining ovarian tissue cryobanking with retrieval of immature oocytes followed by in vitro maturation and vitrification: an additional strategy of fertility preservation. Fertil Steril 2008;89:567.
16. Prasath EB, Chan ML, Wong WH, et al. First pregnancy and live birth resulting from cryopreserved embryos obtained from in vitro matured oocytes after oophorectomy in an ovarian cancer patient. Hum Reprod 2014;29:276.
17. Dolmans MM, Marinescu C, Saussoy P, et al. Reimplantation of cryopreserved ovarian tissue from patients with acute lymphoblastic leukemia is potentially unsafe. Blood 2010;116:2908.
18. Meirow D, Hardan I, Dor J, et al. Searching for evidence of disease and malignant cell contamination in ovarian tissue stored from hematologic cancer patients. Hum Reprod 2008;23:1007.
19. Elassar A, Oktem O, Oktay K. Fertility preservation with ovarian cryopreservation: a decade of experience. Fertil Steril 2007;88:S12.
20. Oktay KH, Yih M. Preliminary experience with orthotopic and heterotopic transplantation of ovarian cortical strips. Semin Reprod Med 2002;20:63.
21. Vitale AM, Abramovich D, Peluffo MC, et al. Effect of gonadotropin-releasing hormone agonist and antagonist on proliferation and apoptosis of human luteinized granulosa cells. Fertil Steril 2006;85:1064.
22. Emons G, Gründker C, Günthert AR, et al. GnRH antagonists in the treatment of gynecological and breast cancers. Endocr Relat Cancer 2003;10:291.

