Modificări metabolice şi structurale descoperite prin rezonanţă magnetică la feţii cu restricţie de creştere intrauterină
Metabolic and structural changes detected by magnetic resonance in IUGR fetuses
Abstract
Intrauterine growth restriction (IUGR) due to placental insufficiency affects 5-10% of all pregnancies and induces cognitive disorders in a substantial proportion of all newborns and is associated with a high risk of abnormal neurodevelopment. Magnetic resonance imaging (MRI) studies have consistently demonstrated brain structural changes on IUGR fetuses: decreased volume in gray matter (GM) and hippocampus; major delays in cortical development have been reported in neonates; reduced GM volumes and decreased fractal dimension of both GM and white matter in infants. MR spectroscopy (MRS) has become a powerful diagnostic tool in the detection of specific brain abnormalities, such as hypoxic-ischemic encephalopathy. Therefore, it is of great interest to explore the possibilities of proton MR spectroscopy as a tool to examine the human fetal brain in situ. This is a technique with which the chemical composition of in vivo tissue can be assessed noninvasively. It has been reported that impaired fetal brain development associated with ventriculomegaly, intrauterine growth restriction (IUGR), and small for gestational age fetuses can be shown by MRS signal changes. Normative values for the levels of the fetal brain metabolites, Inositol, Choline, Creatine, N-Acetylaspartate and their ratios are available and can be used as references to examine changes in MRS spectra due to pathological conditions of the fetal brain, for example, neuronal damage due to hypoxia. MRI has the potential to become an important tool in studying normal and abnormal fetal brain development.Keywords
intauterine growth restrictionfetusproton spectroscopybrain metabolitesRezumat
Restricţia de creştere intrauterină (RCIU) afectează 5-10% dintre sarcini şi include tulburări cognitive la copii într-o proporţie substanţială, asociindu-se cu o rată crescută a întârzierii neurodezvoltării. Există o serie de modificări cerebrale reale în cazul feţilor cu RCIU şi acestea au putut fi descoperite cu ajutorul rezonanţei magnetice (RM): volume scăzute de substanţă cenuşie şi dimensiunea fractală diminuată atât a substanţei cenuşii, cât şi a celei albe, precum şi întârzieri majore în dezvoltarea corticală. Mai recent apărută, spectroscopia cu protoni permite achiziţia de informaţii in vivo despre statusul metabolic al ţesutului fetal cerebral. Spectroscopia RM (RMS) a devenit o modalitate diagnostică importantă în detectarea unor anomalii cerebrale specifice, cum ar fi encefalopatia hipoxic ischemică. De aceea, reprezintă un interes major explorarea posibilităţilor spectroscopiei IRM cu protoni ca o metodă de examinare a creierului uman fetal in situ. Reprezintă o tehnică prin care compoziţia chimică a ţesuturilor vii poate fi evaluată non-invaziv. Valorile normative pentru nivelurile de metaboliţi cerebrali fetali (Inozitol, Colină, Creatina şi N-acetil), cât şi raporturile dintre ele sunt disponibile şi pot fi folosite ca referinţă pentru a evalua schimbările în spectrul IRMS datorate condiţiilor patologice ale creierului fetal, de exemplu distrucţia neuronală datorată hipoxiei. Sincronizarea şi modelul reorganizării cerebrale în cadrul RCIU sunt încă slab documentate, IRM fetal poate fi folosit pentru a achiziţiona informaţii funcţionale şi metabolice de la făt şi placentă.Cuvinte Cheie
restricţie de creştere intrauterinăfătmetaboliţi cerebralispectroscopia cu protoniIntroducere
În ultimi ani, rezonanţa magnetică a crescut ca importanţă, devenind a doua modalitate imagistică în diagnosticul prenatal, completând examinarea ultrasonografică. Evaluarea sistemului nervos central (SNC) este aplicaţia principală a RM fetale. Dintre indicaţiile principale ale RM în imagistica SNC amintim: ventriculomegalia, agenezia de corp calos, anomalii cerebeloase, infecţii congenitale, edemul cerebral, malformaţii corticale, evenimente acute hipoxice.
RCIU adevărată este asociată cu fenomenul de „brain sparing”, care se defineşte ca o creştere a fluxului sanguin spre cord şi creier în detrimentul altor organe, cum ar fi rinichii şi tractul gastrointestinal. Mecanismul presupus neuroprotector nu este compensator în întregime, aceasta evidenţiindu-se prin incidenţa mai crescută a paraliziei cerebrale şi a neurodezvoltării tardive la copiii cu RCIU. Sincronizarea şi modelul reorganizării cerebrale în cadrul RCIU sunt slab documentate. Reducerea fluxului placentar rezultă prin expunere cronică la hipoxie şi subnutriţie, ce are consecinţe asupra dezvoltării cerebrale(1-4).
RM - RCIU
Imaginile cerebrale pot fi normale la feţii cu RCIU. Un grup de cercetători britanici a studiat o cohortă de 40 de feţi cu RCIU (greutatea fetală estimată <percentila 5; indexul de pulsatilitate pe artera ombilicală >percentila 95; indexul de pulsatilitate <percentila 5 pe artera cerebrală medie; flux rezidual diastolic absent pe artera ombilicală; flux rezidual diastolic inversat pe artera ombilicală; unda „a” absentă sau inversată pe ductul venos şi/sau pulsatilitate pe vena ombilicală) şi s-a urmărit dacă volumele organelor feţilor cu RCIU sunt mai mici decât volumele organelor feţilor normali. S-a constatat că: volumul corpului feţilor cu RCIU este mai mic faţă de cel al feţilor normali; volumul placentar la feţii cu RCIU este redus; alveolele feţilor cu RCIU sunt mai puţine şi cu septuri groase; volumul timic al feţilor cu RCIU este scăzut faţă de cel al feţilor normali. La nivelul SNC s-au decelat următoarele modificări: reducere cerebrală crescută cu severitate accentuată pentru RCIU; volumul ventricular scăzut la feţii cu RCIU; feţii RCIU au diferenţe regionale în organizarea creierului: lob frontal mai mic, metabolism şi microstructură diferită(5).
RM fetal - spectroscopia cu protoni
Este o tehnică imagistică non-invazivă, ce permite achiziţia de informaţii in vivo despre statusul metabolic al ţesutului fetal cerebral şi analizează diferenţa absorbţiei de protoni pe radiofrecvenţe specifice într-un câmp magnetic static.
În timp ce RM fetal a fost folosit de mai mult de o decadă pentru vizualizarea morfologică a maturării normale sau patologice fetale, a structurilor extrafetale intrauterine, aspectele metabolice şi funcţionale au fost luate în considerare doar de puţină vreme.
Spectroscopia se poate realiza şi fără sedare, totuşi premedicaţia maternă cu flunitrazepam administrat oral cu 15 min.-1 oră înaintea examinării RM este recomandată.
Spectroscopia RM a devenit o modalitate diagnostică importantă în detectarea unor anomalii cerebrale specifice, cum ar fi encefalopatia hipoxic ischemică. De aceea, reprezintă un interes major explorarea posibilităţilor spectroscopiei RM cu protoni ca o metodă de examinare a creierului uman fetal in situ. Reprezintă o tehnică prin care compoziţia chimică a ţesuturilor vii poate fi evaluată non-invaziv. S-a raportat că dezvoltarea anormală a creierului fetal se asociază cu ventriculomegalie şi RCIU, care se evidenţiază prin schimbarea de semnal a RMS.
Metaboliţi cerebrali vizualizaţi prin RMS
În creierul nou-născutului la termen apar patru grupe principale de metaboliţi: N-acetil aspartat (NAA), Creatina (Cr), Colina (Cho), Inositol (Ino). Valorile normative pentru nivelurile de metaboliţi cerebrali fetali, Ino, Cho, Cr şi NAA, cât şi raporturile dintre ele sunt disponibile şi pot fi folosite ca referinţă pentru a evalua schimbările în spectrul IRMS datorate condiţiilor patologice ale creierului fetal, de exemplu distrucţia neuronală datorată hipoxiei.
S-a arătat că nivelurile de metaboliţi din creierul fetal se schimbă cu creşterea vârstei gestaţionale, începând cu trimestrul al treilea. Această descoperire se pare că reflectă maturarea, în concordanţă cu imaginile RMS realizate la nou-născuţii prematur. La 22 de săptămâni de gestaţie, RMS este caracterizat de două rezonanţe atribuite Ino şi Cho. Ino rezonanţa domină spectrul de la 22 până la 28 de săptămâni de gestaţie şi este redus semnificativ odată cu progresia vârstei gestaţionale la feţi. Cho este crescută şi pe spectrul RMS între 22 şi 28 de săptămâni. Cho este implicată în sinteza de acetilcolină şi a membranelor fosfolipidice, fiind preluată atât de neuroni, cât şi de celulele gliale. Cho şi raportul Cho:Cr scad semnificativ cu creşterea vârstei gestaţionale. NAA apare, de asemenea, în spectru cel mai devreme la 22 de săptămâni; deşi intensitatea vârfului este slabă, se crede că se asociază cu dezvoltarea dendritelor şi a sinapselor şi cu proliferarea şi diferenţierea oligodendrocitelor. Semnalul NA creşte semnificativ cu progresia vârstei gestaţionale. Ino nu arată nici o schimbare semnificativă în corelaţie cu vârsta gestaţională. Creşterea nivelului de NAA şi Cr din ţesutul cerebral şi scăderea nivelului de Cho şi Ino se observă odată cu dezvoltarea creierului fetal. La 34 de săptămâni de gestaţie, spectrul metaboliţilor este similar cu cel al nou-născutului.
Recent, s-a evidenţiat în studiile IRMS prezenţa lactatului la feţii RCIU, cât şi la cei cu gastroschizis. Totuşi, deşi lactatul poate fi parte a metabolismului normal al nou-născutului prematur, semnificaţia patologică a vârfului acestuia observat în creierul fetal rămâne neclară. La feţii RCIU cu morfologie normală, RMS a creierului fetal evidenţiază prezenţa lactatului şi un index NAA:Cho scăzut, markeri metabolici de subnutriţie/hipoxie. Acest model se corelează cu schimbările metabolice prezente în suferinţa hipoxic ischemică a nou-născutului. Studii recente au arătat o creştere semnificativă a raportului Ino:Cho şi o valoare semnificativ crescută a coeficientului de difuzie în tractul piramidal la feţii RCIU, comparativ cu cei normal dezvoltaţi pentru vârsta gestaţională(6).
NAA este sintetizat de mitocondriile neuronale şi apoi transportat în oligodendrocite. NAA redus poate fi semn de imaturitate, dar poate reflectă şi o disfuncţie mitocondrială. Modele pe şobolani cu RCIU demonstrează disfuncţia mitocondrială în creier şi în alte organe (ex.: pancreas).
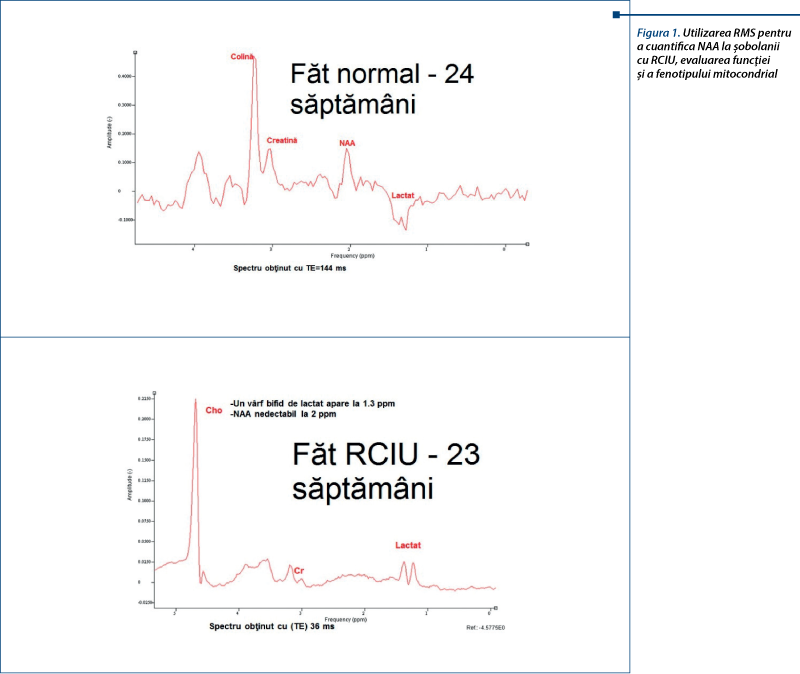
S-au comparat nivelurile de Colină, NAA, lactat, Creatină detectate în creierul feţilor normali şi ai celor cu IUGR şi s-a observat, comparativ cu feţii normali, că, în creierul feţilor cu IUGR, NAA este nedetectabil, iar lactatul este mai crescut, în timp ce Colina şi Creatina sunt mai scăzute (figurile 1 şi 2).
Concluzii
RM are potenţialul de a deveni o unealtă importantă în studierea dezvoltării cerebrale fetale normale şi patologice.
Acesta relevă nu doar condiţiile ce duc la o alterare cerebrală severă (paralizie cerebrală), ci şi pe cele care implică o afectare minoră (RCIU). Poate fi relevant şi în elucidarea mecanismelor implicate în funcţionarea creierului adult. În completarea morfologiei fetale, aceste metode diagnostice ne aduc informaţii suplimentare despre dezvoltarea prenatală normală şi patologică. Când există suspiciunea unei anomalii fetale la examinarea ecografică, RM este folosită ca o metodă eficientă de examinare adiţională. Investigaţii suplimentare sunt necesare pentru a dovedi potenţialul diagnostic al acestor noi tehnici imagistice.
Menţiune: Această lucrare este parţial sprijinită de către Programul Operaţional Sectorial Dezvoltarea Resurselor Umane (POSDRU) finanţat din Fondul Social European şi de către Guvernul României prin contractul nr. POSDRU 141531.
Bibliografie
1. Pugash D, Krssak M, Kulemann V, et al. Magnetic resonance spectroscopy of the fetal brain. Prenat Diagn 2009;29:434-441.
2. Huppi PS, Amato M. Advanced magnetic resonance imaging techniques in perinatal brain injury. Biol Neonate 2001;80:7 14.
3. Toft PB, Leth H, Lou HC, et al. Metabolite concentrations in the developing brain estimated with proton MR spectroscopy. J Magn Reson Imaging 1994;4:674-680.
4. Cady EB, Amess P, Penrice J, et al. Early cerebral-metabolite quantification in perinatal hypoxic-ischemic encephalopathy by proton and phosphorus magnetic resonance spectroscopy. Magn Reson Imaging 1997;15:605-611.
5. Am J Obstet Gynecol. 2011 Nov;205(5):483.e1-8. doi: 10.1016/j.ajog.2011.06.032. Epub 2011 Jun 15.
6. Story L, Damodaram MS, Allsop JM, et al. Brain metabolism in fetal intrauterine growth restriction: a proton magnetic resonance spectroscopy study. Am J Obstet Gynecol 2011;205:483.e1-8.
