Factori care influenţează acoperirea vaccinală în România
Factors influencing the vaccination coverage in Romania
Abstract
In Romania, the vaccination coverage has dropped to levels that oscillate at around 60%. The factors contributing to this decline are: the ignorance of preventable disease, cross-border migration, antivaccine campaigns, the discontinuity of supply. Meanwhile, the vaccination schedule was changed by the introduction of newer products in the program with very good safety and efficacy profile. There are also available optional vaccines for clinicians, who have the responsability of providing information to parents about the benefits. Often, it is required the adaptation of the vaccination schedule, according to history, in order to upgrade it.Keywords
coveragevaccine-preventable diseasesvaccinationRezumat
În România, acoperirea vaccinală a scăzut până la valori ce oscilează în jurul procentului de 60%. Factorii care contribuie la această scădere sunt: necunoaşterea bolii prevenibile, migraţia transfrontalieră, campaniile antivaccinare, discontinuitatea în aprovizionare. În acelaşi timp, schema de vaccinare s-a modificat prin introducerea în program a produsele mai noi cu profil de siguranţă şi eficacitate foarte bună. Clinicienii au la dispoziţie şi vaccinuri opţionale, lor revenindu-le sarcina informării părinţilor privind beneficiile administrării. De multe ori, se impune adaptarea schemei de vaccinare pentru recuperare, în funcţie de istoric, pentru completarea acesteia.Cuvinte Cheie
acoperire vaccinalăboli prevenibile prin vaccinarevaccinareÎn România, Programul Naţional de Vaccinare (PNV) se desfăşoară preponderent în cabinetele medicilor de familie, doar vaccinurile administrate în maternităţi constituind excepţia. Acest lucru determină o imensă responsabilizare pentru medicii de familie, dar nu numai. Activitatea de vaccinare este strâns dependentă de activitatea de consiliere, datorită caracterului neobligatoriu al administrării vaccinurilor din PNV, astfel încât toate specialităţile care abordează curricular vârsta pediatrică participă la efortul de atingere a unei acoperiri vaccinale (AV) optime.
De-a lungul timpului, România s-a situat în rândul ţărilor care atingeau acoperiri vaccinale optimale, pentru anumite antigene, chiar la valori de 99%. Conform datelor raportate de către România la Organizaţia Mondială a Sănătăţii (OMS), acoperirea vaccinală pentru difterie, tetanos, tuse convulsivă şi poliomielită a fost de 99% în 2000, a scăzut la 89% în 2013(1), pentru ca raportul Centrului Naţional de Supraveghere şi Control al Bolilor Transmisibile (CNSCBT) să raporteze în anul 2016 o AV de numai 60,7% pentru 4 doze de DTP şi VPI(2).
Cifrele publicate anul trecut în februarie constituiau un puternic semnal de alarmă şi vin să întărească atenţionarea OMS, care a plasat România în rândul ţărilor la risc înalt pentru transmiterea virusului poliomielitei, alături de Ucraina şi Bosnia-Herţegovina, încă din anul 2013. Atenţionarea a fost determinată în special de contextul general creat de detectarea şi apoi confirmarea circulaţiei virusului polio sălbatic de tip 1 (WPV1) în mai multe regiuni din Israel(3). Ulterior, evoluţiile din Siria şi Ucraina au confirmat acest lucru, cazurile de circulaţie a virusului polio vaccinal din Ucraina fiind cu atât mai importante pentru ţara noastră, în urma apariţiei acestora în localităţi situate la graniţa comună(4).
Scăderea acoperirii vaccinale şi-a pus însă amprenta pe evoluţia unei noi epidemii de rujeolă, care până la data de 10.03.2017 s-a soldat cu 3446 de cazuri, dar şi cu 17 decese(5). Studii viitoare vor trebui să aducă argumente pentru această mortalitate foarte crescută (4,93 decese la 1000 de cazuri, în condiţiile în care mortalitatea ar trebui să fie de 1-2 la 1.000 de cazuri).
Cauzele care stau la baza acestei scăderi a AV sunt sintetizate de Ministerul Sănătăţii şi preluate de mai mulţi autori, astfel: lipsa de percepţie a riscului (nu s-au mai raportat cazuri de difterie, poliomielită etc.), influenţa campaniilor antivaccinare, întârzierile în aprovizionarea cu vaccin, migraţia transfrontalieră a copiilor împreună cu familiile, unde primesc scheme diferite adaptate specificului epidemiologic local(6).
O altă provocare încă întâlnită în România o constituie contextul epidemiologic legat de tuberculoză, copiii născuţi în ţara noastră fiind expuşi în continuare riscului de a dezvolta forme grave de tuberculoză în absenţa vaccinării BCG. Acest lucru se datorează persistenţei unui număr de cazuri-sursă destul de important, incidenţa tuberculozei menţinându-se la valori mai ridicate decât în alte ţări din Uniunea Europeană. În anul 2014, ea a fost de 67 la 100.000 de locuitori, în scădere faţă de anii anteriori, în timp ce în Franţa a fost 7 la 100.000 de locuitori, în Marea Britanie şi Spania a fost de 10 la 100.000 de locuitori, iar în Italia şi Germania, de 5 la 100.000 de locuitori(1).
Pe lângă aspectele semnalate mai sus, vaccinatorii sunt puşi în faţa schimbărilor survenite în programul naţional de vaccinare, prin care România se aliniază la schemele de vaccinare din majoritatea ţărilor occidentale. Acestea vizează atât introducerea de vaccinuri noi, cât şi modificări ale schemei de vaccinare. În ultimii ani au fost introduse vaccinuri noi, începând cu înlocuirea vaccinului polio oral (VPO) cu vaccin polio inactivat (VPI), componenta pertussis celulară a fost înlocuită cu componenta pertussis acelular, a fost introdusă componenta Haemophillus influenzae de tip B (Hib), s-a preferat vaccinul hexavalent şi pentavalent, astfel încât acceptarea vaccinării să crească, dar şi să permită aducerea de vaccinuri noi. De asemenea, s-a trecut la vaccinarea cu vaccinul trivalent rujeolă - oreion - rubeolă (ROR), dar şi la modificarea schemei de vaccinare pentru DTP şi VPI de la schema 3+1 la schema 2+1, odată cu aprobarea acesteia de către Comisia Europeană la data de 5.03.2015(7). La 1.04.2015, România a adoptat imediat schema 2+1.
Înlocuirea VPO cu VPI a dus la dispariţia riscului de apariţie a poliomielitei paralitice asociate vaccinării (risc de 2-4 cazuri la 1 milion de doze) produse de virusul derivat din vaccin, precum şi de circulaţie a virusului polio derivat din vaccin (responsabil de apariţia celor două cazuri din Ucraina). Totuşi, VPI este mai puţin eficient decât OPV în a induce apărare la nivelul mucoasei intestinale la copiii care nu au fost vaccinaţi anterior. Copiii vaccinaţi cu VPI se pot infecta şi elimina virusul prin materiile fecale, dar nu vor dezvolta boala datorită anticorpilor protectori sistemici. Totuşi, VPI poate reduce cantitatea şi durata eliminării, contribuind în mai mică măsură la împiedicarea circulaţiei virusului(8,9). Trecerea la schema cu VPI a fost posibilă datorită faptului că România a asigurat pentru multă vreme valori optime ale AV, recomandările OMS referindu-se la administrarea doar a schemei cu VPI în ţările în care se menţin AV cu valori înalte şi risc scăzut de import şi transmitere(9).
Folosirea pertussisului acelular în schema naţională reprezintă încă un beneficiu suplimentar, în special pentru bebeluşi, deoarece numărul şi intensitatea reacţiilor adverse locale, dar şi sistemice sunt cu mult reduse comparativ cu pertussisul celular. Dificultăţile de producţie şi tulburările sistematice în aprovizionare împiedică administrarea cât mai precoce a produselor care conţin pertussis acelular, inclusiv hexavalentul din PNV. Consecinţa o poate constitui creşterea numărului de cazuri de tuse convulsivă la sugarii şi copiii mici nevaccinaţi, dar şi de boli produse de Haemophilus influenzae de tip b(10). Beneficiul uriaş îl reprezintă reducerea numărului de determinanţi antigenici de la circa 3000 cuprinşi în produsele care conţin pertussis celular la un număr de 2, 3 sau 5 determinanţi antigenici, în funcţie de produs, conţinuţi în pertussisul acelular(11).
Peste problemele de producţie apărute, s-au adăugat şi problemele provocate de dificultăţile survenite în procesul de achiziţionare a vaccinurilor de către Ministerul Sănătăţii. Se impune, astfel, în majoritatea cazurilor, realizarea unor scheme de recuperare a acestora care necesită cunoştinţe avansate privind principiile generale de recuperare şi chiar colaborarea interdisciplinară.
A fost introdusă în PNV şi vaccinarea antipneumococică, încă din anul 2012, însă Ministerul Sănătăţii nu a reuşit încă achiziţia vaccinului, fapt inacceptabil, având în vedere importanţa administrării acestuia.
De asemenea, vaccinul împotriva virusului papilloma uman (HPV) împărtăşeşte aceeaşi soartă cu vaccinul antipneumococic, fiind introdus în PNV, dar neachiziţionat.
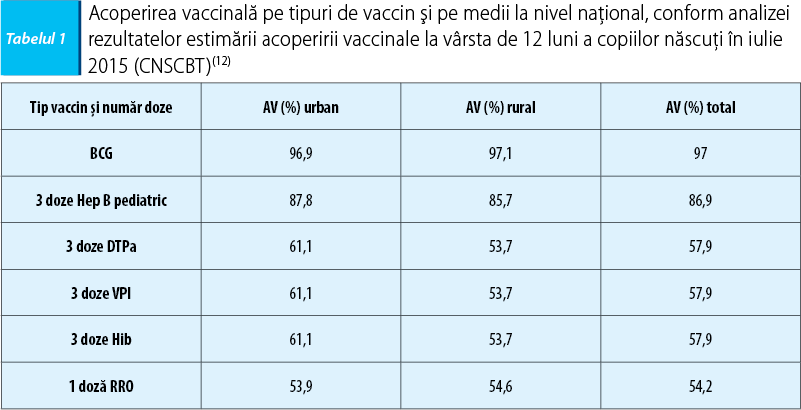
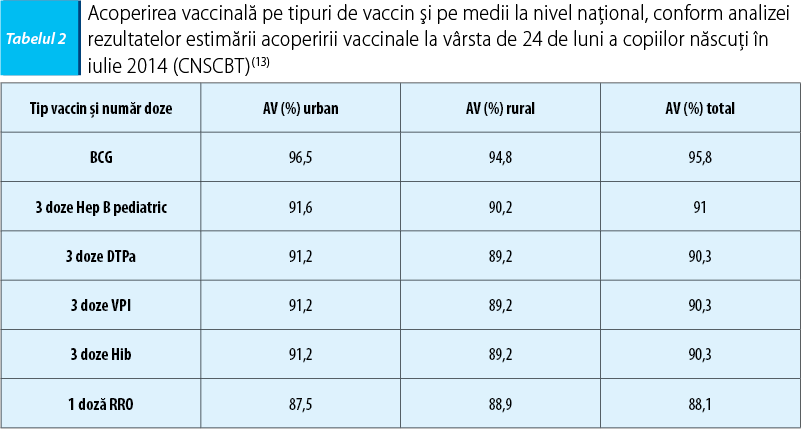
Analizând diferenţele majore dintre tabelul 1 şi tabelul 2, putem constata următoarele:
1. Valorile optime ale AV sunt atinse cu mare dificultate şi la mare distanţă de vârsta optimă.
2. Vaccinarea ROR nu atinge AV mai mare de 95% nici măcar la un an de la vârsta indicată în PNV.
3. AV în mediul rural este nesemnificativ mai mică decât în urban, diferenţele dintre medii fiind în favoarea urbanului pentru DTPa, VPI, Hib şi vacinului hepatitic B (Hep B) şi în favoarea ruralului pentru ROR.
4. Singurul vaccin la care încă atingem 95% din acoperirea vaccinală este BCG.
Datele sunt culese prin metodologia clasică şi nu rezultă din evaluarea datelor din Registrul Electronic Naţional de Vaccinări (RENV). Analizând concordanţa acestor date cu cele din RENV, rezultă o suprapunere de date pentru 85,1% dintre medicii de familie, raportându-ne la cohorta născută în iulie 2014 şi evaluată la 24 de luni(13).
Acest lucru se datorează atât dificultăţilor de înregistrare în RENV de către medicii de familie, dar şi fenomenului de vaccinare a copiilor abordat şi de alte specialităţi medicale din sfera pediatrică. Practic, există un procent de copii pe care nu îl cunoaştem care se vaccinează în sistem privat, sistem nesupus procesului de raportare a vaccinărilor realizate şi evaluare a AV. În opinia autorului, acest proces trebuie acceptat şi legalizat prin reglementarea fenomenului şi integrarea serviciilor de vaccinare la alţi furnizori de servicii medicale decât cei prevăzuţi în PNV, inclusiv cel de raportare a vaccinării în RENV. Consider că este o necesitate care vine să ajute la cunoaşterea cât mai aproape de realitate a AV, în special în context epidemiologic provocator.
România a asigurat multă vreme o acoperire vaccinală optimală şi datorită existenţei unui personal obişnuit cu activitatea de vaccinare, cu mare încredere în siguranţa şi eficacitatea vaccinării. O mare parte din medicii vaccinatori şi asistentele acestora sunt acum la procesul de ieşire naturală din sistem. Locul lor este luat de către medici tineri, fără experienţa participării în situaţii epidemiologice speciale, dar şi fără siguranţa profesională oferită de propria activitate. Fenomenul se observă la o paletă largă de specialităţi, inclusiv de medicină de familie şi pediatrie, personal primind chiar şi telefonic sfatul de a fi mai precaut faţă de siguranţa şi eficienţa vaccinării, de la un coleg mai tânăr din altă specialitate. Se impune astfel acordarea unei atenţii sporite programului de pregătire din facultate, rezidenţiat şi postuniversitară a tuturor specialităţilor medicale implicate în procesul de vaccinare. Apariţia de noi surse de informare, în special în social media, şi deplasarea preferinţelor de achiziţie a informaţiilor noi impun adaptarea metodelor de învăţare şi a platformelor de educare către zona online, fiind astfel obligatorie abordarea de tehnologii moderne care astfel eficientizează fluxul informaţional educaţional.
O nevoie resimţită acut în activitatea de vaccinare o constituie dezvoltarea capacităţilor de comunicare între vaccinatori şi părinţi. Este absolut necesară deprinderea de abilităţi de comunicare din partea medicilor de familie vaccinatori, dar şi deprinderea de tehnici de consiliere provaccinare. În cadrul procesului de consiliere, livrarea mesajului este esenţială pentru a creşte nivelul de încredere al familiei şi pentru obţinerea, din nou, a unor acoperiri vaccinale optimale.
Un alt element cu impact asupra AV îl constituie fenomenul de migraţie transfrontalieră, ce cunoaşte valenţe bidirecţionale. Întâlnim atât copii care se nasc în România şi care primesc o doză în cabinetele noastre, părăsind apoi ţara, continuând schema în alte ţări, cât şi copii care se nasc în alte ţări şi se întorc apoi împreună cu familiile. În afara dezavantajelor cauzate de pierderea contactului cu familia şi de necunoaşterea antecedentelor vaccinale, fenomenul poate fi privit şi din perspectivă pozitivă. Folosirea în PNV a aceluiaşi vaccin ca în alte ţări sporeşte încrederea părinţilor în vaccin, ba chiar se încurajează achiziţionarea de vaccinuri opţionale precum vaccinul pneumococic conjugat sau vaccinul rotaviral.
Refuzul vaccinării de către părinţi este puternic încurajat de informaţiile din mediul online. De cele mai multe ori, informaţia cu caracter medical rezultată dintr-o consultaţie medicală este verificată de către pacienţi sau părinţi pe reţele de socializare sau pe diferite site-uri nereglementate. Informaţiile sunt în majoritatea cazurilor insuficiente sau chiar eronate, îndeajuns pentru a induce atitudini diverse, de suspiciune sau teamă, ducând în final la refuzarea vaccinării. Este necesară o atitudine proactivă în acest domeniu, societăţile profesionale, dar şi autorităţile fiind obligate să ofere alternative informaţionale care să conţină date validate ştiinţific.
Concluzii
1. Acoperirea vaccinală este în scădere, din cauza unui cumul de condiţii favorizante.
2. Sunt necesare colaborarea şi sprijinul reciproc între furnizorii de servicii medicale aparţinând tuturor specialităţilor implicate în abordarea pediatrică.
3. Se impune identificarea de soluţii adaptate condiţiilor noi create de migraţia transfrontalieră, de accesul la informaţii nevalidate ştiinţific şi de înlocuirea naturală a personalului medical.
4. Se impune reglementarea clară a procesului de achiziţie de vaccinuri, care să preîntâmpine aprovizionarea deficitară.
5. Personalul medical trebuie să îşi adapteze mesajul provaccinare la contextul general, puternic modificat.
Bibliografie
1. World Health Organization. Country Profile on regional site [internet]. 2017 [cited 15.03.2017]. Available from: http://www.euro.who.int/en/countries
2. Centrul Naţional de Control al Bolilor Transmisibile. Analiza rezultatelor estimarii acoperirii vaccinale la vârsta de 18 luni a copiilor născuti în iulie 2014. 2016 [cited 15.03.2017]. Available from: http://cnscbt.ro/index.php/analiza-date-supraveghere/evaluarea-acoperirii-vaccinale/397-analiza-rezultate-av-18-luni-feb-2016/file
3. World Health Organization. Report of the 28th Meeting of the European Regional Certification Commission for Poliomyelitis Eradication Copenhagen, Denmark 3-5 June 2014 [internet]. 2014 [cited 15.03.2017]. Available from: http://www.euro.who.int/__data/assets/pdf_file/0008/256949/Report-of-the-28th-Meeting-of-the-European-Regional-Certification-Commission-for-Poliomyelitis-Eradication.pdf?ua=1
4. European Centre for Disease Prevention and Control. Outbreak of vaccine-derived poliovirus type 1 (cVDPV1) in Ukraine, August 2015 - 2 September, Stockholm, 2015. Available from: http://ecdc.europa.eu/en/publications/Publications/Poliomyelitis-Ukraine-rapid-risk-assessment-September-2015.pdf
5. Centrul Naţional de Control al Bolilor Transmisibile. Situaţia rujeolei în România la data de 10.03.2017. 2017 [cited 15.03.2017]. Available from: http://cnscbt.ro/index.php/informari-saptamanale/rujeola-1/649-situatia-rujeolei-in-romania-la-data-de-10-03-2017/file
6. Vlădescu C, Scîntee SG, Olsavszky V, Hernández-Quevedo C, Sagan A. Romania: Health system review. Health Systems in Transition, 2016; 18(4):1–170. Available from: http://www.euro.who.int/__data/assets/pdf_file/0017/317240/Hit-Romania.pdf
7. European Medicines Agency. Hexyon. 2016 [cited 15.03.2017]. Available from: http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/002796/human_med_001641.jsp&mid=WC0b01ac058001d124
8. World Health Organization. Planification de l’introduction du VPI - martie 2014. [cited 15.03.2017]. Available from: http://www.who.int/immunization/diseases/poliomyelitis/inactivated_polio_vaccine/ipv_implementation_facts_mar14_fr.pdf
9. World Health Organization. Weekly epidemiological record. Polio vaccines: WHO position paper, January 2014. No. 9, 2014, 89, 73–92. [cited 15.03.2017]. Available from: http://www.who.int/wer/2014/wer8909.pdf
10. European Centre for Disease Prevention and Control. Shortage of acellular pertussis-containing vaccines and impact on immunisation programmes in the EU/EEA - 8 October 2015. Stockholm: ECDC; 2015. [cited 15.03.2017]. Available from: http://ecdc.europa.eu/en/publications/Publications/vaccine-shortage-rapid-risk-assessment-october-2015.pdf
11. Offit P. et al. Addressing Parents’ Concerns: Do Multiple Vaccines Overwhelm or Weaken the Infant’s Immune System? Pediatrics 2002; 109;124.
12. Centrul Naţional de Control al Bolilor Transmisibile. Analiza rezultatelor estimării acoperirii vaccinale la vârsta de 12 luni pentru copiii născuţi în luna iulie 2015. 2016 [cited 15.03.2017]. Available from: http://cnscbt.ro/index.php/analiza-date-supraveghere/evaluarea-acoperirii-vaccinale/593-analiza-rezultatelor-estimarii-acoperirii-vaccinale-la-varsta-de-12-luni-a-copiilor-nascuti-in-luna-iulie-2015/file
13. Centrul Naţional de Control al Bolilor Transmisibile. Analiza rezultatelor estimării acoperirii vaccinale la vârsta de 24 de luni pentru copiii născuţi în luna iulie 2014, 2016 [cited 15.03.2017]. Available from: http://cnscbt.ro/index.php/analiza-date-supraveghere/evaluarea-acoperirii-vaccinale/594-analiza-rezultatelor-estimarii-acoperirii-vaccinale-la-varsta-de-24-luni-a-copiilor-nascuti-in-luna-iulie-2014/file
