Eosinophilic esophagitis is a chronic, immune‑mediated, antigen‑induced disease characterized clinically by variable digestive symptoms indicative of upper gastrointestinal dysfunction and histologically by eosinophilic predominant inflammation. The elimination diets have been proved to be efficient, provideing a therapeutic solution free of drugs adverse reactions. Until now, a range of different antigen restrictive diets have been used, with clinical and histologic remission. Regardless of the chosen elimination diet, patients require a carefull nutritional management because these diets are not without risks and may impact children's growth and development and the quality of life în general.
Rolul dietelor de excludere în esofagita eozinofilică
The role of exclusion diets in eosinophilic esophagitis
First published: 24 decembrie 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Aler.2.4.2018.2132
Abstract
Rezumat
Esofagita eozinofilică este o afecţiune cronică, mediată imunologic, alergen indusă, caracterizată din punct de vedere clinic prin manifestări digestive variate atribuite disfuncţiei esofagiene şi, din punct de vedere histologic, prin inflamaţie predominant de tip eozinofilic. Dietele de restricţie antigenică şi-au dovedit eficacitatea în tratamentul acestei afecţiuni, oferind o soluţie terapeutică lipsită de efectele adverse ale medicaţiei alopate. Până în prezent au fost abordate câteva alternative terapeutice de diete restrictive antigenic, cu inducerea remisiunii clinice şi histologice. Dincolo de tipul de dietă abordat, pacienţii necesită un management nutriţional atent, întrucât dietele de eliminare nu sunt lipsite de riscuri, putând avea impact asupra creşterii şi dezvoltării la copil şi asupra calităţii vieţii, în general.
Esofagita eozinofilică, cunoscută şi ca „astmul esofagian”, este o afecţiune inflamatorie a esofagului, alergen indusă, interleukina (IL)13 dependentă, mediată imunologic prin Th2. Histopatologic, esofagita eozinofilică este definită ca o inflamaţie predominant de tip eozinofilic (>15 eozinofile/câmp), însă şi cu recrutarea de alte celule inflamatorii, cum ar fi celule mastocitare, limfocite, bazofile şi celule înnăscute limfoide(1,2).
La copii, esofagita eozinofilică se prezintă clinic prin dureri abdominale, stare de greaţă, vărsături, regurgitări frecvente, alimentaţie dificilă şi retard de creştere. Adulţii acuză adesea disfagie şi impactarea bolului alimentar.
Esofagita eozinofilică aproape invariabil progresează către fibrostenoză esofagiană, în condiţiile lipsei de tratament, conducând la rigiditate, distensibilitate redusă şi dismotilitate(1). Controlată suboptimal, inflamaţia persistentă conduce la formarea de stricturi, contribuind la disfagie şi impactarea bolului alimentar.
Managementul acestei afecţiuni presupune o abordare terapeutică multimodală, multidisciplinară şi cuprinde tratament topic cronic cu corticosteroizi (budesonidă, fluticazonă), inhibitori de pompă de protoni (IPP), restricţie antigenică dietetică, modificarea stilului de viaţă, însoţit de diagnostic endoscopic repetat cu reevaluare terapeutică. La aceste metode deja însuşite de clinicieni, studii extinse au încercat abordarea şi a altor alternative terapeutice, cum ar fi azatioprina şi 6-mercaptopurina, cromoglicatul de sodiu, montelukast – însă cu rezultate nesatisfăcătoare, cele mai promiţătoare fiind cu agenţi biologici – anticorpi anti-IL-5 (mepolizumab, reslizumab) şi anticorpi monoclonali anti-IL-13 QAX576, dar care necesită cercetări suplimentare(2).
În situaţiile de urgenţă, precum fibrostenoza esofagiană, intervenţia endoscopică de dilatare a esofagului este terapia salvatoare.
Ţinta tratamentului în esofagita eozinofilică este atât remiterea manifestărilor clinice, cât şi a inflamaţiei esofagiene de tip eozinofilic, cu stoparea remodelării tisulare şi menţinerea remisiunii, prevenind astfel progresia către fibrostenoză şi, în consecinţă, eliminarea necesitaţii terapiilor de salvare.
În ultimii ani, eforturile cercetătorilor s-au concentrat tot mai mult asupra utilizării dietelor de restricţie antigenică, în scopul atingerii acestui deziderat. În acest sens, articolul de faţă se va centra în principal pe rezultatele obţinute şi publicate în 2016 într-un raport al Grupului de Lucru al Academiei Americane de Alergologie, Astm şi Imunologie referitor la managementul esofagitei eozinofilice folosind dietele de eliminare, dar şi provocările potenţiale ale implementării unor astfel de regimuri alimentare(3).
În primul rând, trebuie menţionat că ele nu sunt fără riscuri, putând avea impact major asupra statusului nutriţional, asupra plăcerii de a mânca şi, în general, asupra calităţii vieţii. Totuşi, sub o îndrumare adecvată, aceste terapii pot fi eficiente, dar şi echilibrate nutriţional, cu minimizarea impactului asupra stilului de viaţă. Dietele pot fi folosite fie ca terapie de primă intenţie, fie în cazul eşecului celorlalte terapii, putând oferi remisiune atât clinică, cât şi histologică, cel mai adesea de lungă durată, fără efectele adverse date de medicamente.
Implementarea unei diete poate fi cu adevărat provocatoare, întrucât nu există în prezent teste care să identifice cu acurateţe triggerii alimentari în esofagita eozinofilică.
Alegerea unui regim dietetic terapeutic specific este individualizată şi orientată de preferinţele pacientului şi de fezabilitatea lui din punct de vedere terapeutic şi nutriţional(4).
Există trei tipuri de abordare a dietelor de restricţie antigenică:
1. Dieta elementală, bazată pe formule de aminoacizi, care elimină alergenele alimentare. Această dietă, după o administrare de minimum 6 săptămâni, a dus la remisiune clinică şi ameliorare histologică la 95-98% dintre pacienţii cu esofagită eozinofilică, în alte studii, cu eficienţă clinică şi histologică de 90,8%, atât la copii, cât şi la adulţi, fiind la fel de eficientă în remiterea manifestărilor clinice ca şi tratamentul corticosteroid. În prezent, societăţile de alergologie şi gastroenterologie recomandă aceste formule bazate pe aminoacizi în detrimentul celor extensiv hidrolizate(5-8). Dintre dezavantajele acestor formule menţionăm costurile mari şi gustul neplăcut, care le fac greu de acceptat, afectând calitatea vieţii pacienţilor. Un aspect important care trebuie urmărit este legat de conţinutul nutritiv al formulei, care diferă în funcţie de producător. Sugarii şi preşcolarii necesită atenţie specială, întrucât principalele achiziţii în dezvoltarea neuromotorie sunt însuşite în primii trei ani de viaţă şi aptitudinile necesare alimentaţiei se dobândesc şi se perfecţionează prin modul de prezentare a alimentelor. Înlăturarea tuturor alimentelor în această perioadă poate avea consecinţe dramatice asupra dezvoltării neuromotorii, împiedicând dobândirea achiziţiilor motorii legate de alimentaţie, dar şi modificarea preferinţelor de gust(9,10). Adăugarea de una‑două alimente (ex.: ou, măr sau cartof dulce) poate ajuta în conservarea sau dezvoltarea aptitudinilor motorii şi să ducă la îmbunătăţirea acceptabilităţii dietei.
Ajutorul unui dietetician poate fi necesar în această etapă, arătând părinţilor felul cum un număr limitat de alimente poate fi oferit în diferite moduri de preparare. Amelioratori ai gustului, precum vanilia, sau potenţiatori artificiali de gust consideraţi siguri, bazaţi pe siropuri din zahăr/porumb, oţet, sare, sirop de arţar, uleiuri vegetale, pot fi folosiţi pentru a da varietate gustului. La adulţi este permis ceaiul negru sau cel verde.
2. Dieta de eliminare empirică este cea mai îmbrăţişată de cercetători; ea exclude alergenele alimentare comune, fără a fi necesare investigaţii prealabile, precum testele cutanate prick sau patch la alimente sau testele in vitro – IgE specifice pentru alimente.
În cadrul acestei diete există mai multe abordări: unele studii au exclus un număr de şase alimente din dietă, altele, patru. În studiile care au exclus şase alimente considerate ca fiind cei mai mari potenţiali triggeri incriminaţi în esofagita eozinofilică, acestea au fost: laptele, oul, făina, soia, arahidele/alunele de pădure şi peştele/fructele de mare. În urma eliminării acestor alergene din dietă, s-a observat ameliorarea semnificativă clinică şi răspuns histologic în 74% dintre cazuri, iar într-un alt studiu, similar, în 70% din cazuri(11). După perioada de excludere, investigatorii au reintrodus secvenţial alimentele excluse, repetând şi endoscopia esofagiană cu prelevare de biopsii, pentru a verifica prezenţa modificărilor histologice, a eozinofilelor. Astfel, s-a constatat că alimentele cele mai implicate în apariţia recăderilor au fost: laptele de vacă (74% dintre copii şi 50% dintre adulţi), făina de grâu (26%, respectiv 60%), oul (17%, respectiv 10%), soia (10%, respectiv 10%) şi arahidele (6%, respectiv 5%)(12,13).
Studiile care au restricţionat la adulţi folosirea unui grup mai restrâns de alimente – patru, pentru şase săptămâni – au exclus laptele, oul, făina şi leguminoasele, cu obţinerea remisiunii în 54% dintre cazuri. Un studiu prospectiv din 2017 efectuat la copii, care a exclus de asemenea patru alimente (laptele, făina, oul şi soia) pentru opt săptămâni, a obiectivat remisiune histologică la 64% dintre pacienţi. După reintroducerea secvenţială a posibililor triggeri alimentari, inducerea inflamaţiei histologice a apărut după consumul de lapte de vacă (85%), ou (35%), făină (33%) şi soia (19%)(14).
3. Dieta de restricţie antigenică ţintită (ghidată de teste) se bazează pe identificarea alergenelor alimentare prin testare cutanată prick/patch/IgE serice specifice. Aceste teste nu doar că sunt consumatoare de timp, însă pot da rezultate fals pozitive sau fals negative. O revizuire a 14 studii cu acest tip de dietă a găsit remisiune histologică în total în 45,5% din cazuri, cu o mare variabilitate a ratei de răspuns între studii (35,4-55,7%)(15).
Singura cale sigură de a afla dacă un aliment este trigger pentru esofagita eozinofilică constă în excluderea alimentului, urmată de remisiune clinică şi histologică, apoi reintroducerea alimentului, cu recurenţa simptomatologiei şi apariţia modificărilor histologice.
Provocările acestor diete restrictive rezidă din faptul că ele solicită un management nutriţional profund, având în vedere că pacienţii diagnosticaţi cu esofagită eozinofilică pot fi deja la risc din punct de vedere nutriţional, atât înainte de iniţierea terapiei restrictive, cât şi după excluderea multiplelor alimente cu valoare nutriţională bogată. Mukkada şi colaboratorii au evaluat 200 de copii cu esofagită eozinofilică, cu media de vârstă de 34 de luni, şi au constatat că 16,9% se confruntau cu tulburări ale alimentaţiei majore, iar 93,9% se învăţaseră cu administrarea parentală a alimentaţiei, primeau cu greu, în cantităţi variabile nesatisfăcătoare, sau refuzau alimentele oferite, nu prezentau un program al meselor sau erau refractari la a încerca noi alimente(10).
Pentru o mai bună evaluare a severităţii simptomelor şi a comportamentului adaptativ s-a conceput pentru adulţi Indexul de activitate a esofagitei eozinofilice, care urmăreşte activitatea pacientului într-un interval de şapte zile. Cel mai frecvent comportament adaptativ pentru pacienţii adulţi cu esofagită eozinofilică a fost timpul prelungit necesar administrării de alimente cu consistenţă crescută (carne, pâine, alimente neprelucrate). La adulţi, disfagia la administrarea de hrană solidă cu impactarea bolului alimentar este cel mai frecvent simptom (50%), necesitând intervenţie endoscopică pentru dezimpactare. Alte simptome: dureri toracice, arsuri retrosternale şi dureri abdominale.
Implementarea unei astfel de diete presupune evaluarea amănunţită a statusului nutriţional al copilului/adultului prin calculul indicilor antropometrici, cu urmărirea curbelor de creştere.
Administrarea slabă, inadecvată a caloriilor, a proteinelor, poate duce la deficite ponderale, la topirea ţesutului celular subcutanat sau a musculaturii, rezultând într-un status funcţional diminuat. Totuşi, pierderea în greutate sau retardul de creştere nu constituie o contraindicaţie a iniţierii terapiei dietetice, însă necesită un plan nutriţional adiţional pentru a furniza caloriile, proteinele, vitaminele şi mineralele necesare recuperării deficitelor la copii şi pentru evitarea pierderilor involuntare la adult.
Atât la copii, cât şi la adulţi se impune investigarea abilităţilor şi comportamentelor alimentare (ex.: tăierea în bucăţele mici, administrarea solidelor în acelaşi timp cu lichidele pentru a facilita înghiţirea, evitarea anumitor alimente cum ar fi carnea, mestecatul prelungit etc.). Pentru a întocmi o dietă cât mai echilibrată nutriţional, pacientul este rugat să ţină un jurnal alimentar de trei zile, din care să se poată determina aportul zilnic, tipul alimentaţiei şi dacă pacientul este capabil să îşi asigure necesarul de macro‑ şi micronutrienţi. Există situaţii când barierele (nutriţionale, financiare, cognitive, lipsa suportului social sau lipsa motivaţiei) sunt atât de semnificative, încât tratamentul dietetic nu e fezabil sau se poate dovedi a fi dăunător.
Aşadar, în unele situaţii, terapia bazată pe dietele de eliminare nu este în beneficiul pacientului şi opţiuni alternative trebuie luate în considerare, cum ar fi tratamentul topic cu corticosteroizi.
După cum am mai menţionat anterior, alegerea tratamentului necesită o abordare individualizată, centrată pe pacient.
Odată iniţiată dieta, în rutina zilnică a pacientului trebuie să se regăsească în mod esenţial citirea ingredientelor de pe ambalajul produselor, cu menţiunea că derivate din unele alimente considerate alergene majore nu sunt uneori specificate pe ambalaj, făcând evicţia alergenelor o provocare.
Dincolo de educaţia de evicţie, familia pacientului trebuie să se adapteze la dieta necesară pacientului şi, după eliminarea alimentelor interzise din locuinţă, să facă o listă a preparatelor alternative nealergenice care sunt preferate de pacient. Este important ca substituenţii aleşi să acopere nevoile nutriţionale pierdute prin alimentele înlocuite (tabelul 1). Fiecare produs alimentar înlocuit furnizează un set unic de micronutrienţi şi înlocuirea lui trebuie să se facă cu produse la fel de bogate nutritiv. Dacă sunt tolerate de către pacienţi, alimente precum carne, cereale (inclusiv cele îmbogăţite cu vitamine de la micul dejun), vegetale verzi sau portocalii şi seminţe pot fi adăugate în dietă pentru a da valoare nutritivă meselor. Oferirea unor modele de meniuri poate fi de folos(3).

Tranziţia la noua dietă se poate face progresiv, în 1-2 săptămâni, pentru a fi mai uşor de asimilat şi mai puţin intimidantă pentru pacienţi.
Sfaturi practice în procesul de înlocuire a alimentelor
Eliminarea produselor din grâu. Faţă de produsele bazate pe făină de grâu, care sunt îmbogăţite cu vitamine, majoritatea produselor din cereale care nu conţin grâu nu au adaosuri de vitamine, multe dintre ele fiind obţinute din cereale rafinate, aşadar sărace în fibre, vitamine din clasa B-urilor şi minerale. Utilizarea de substituenţi precum hrişcă, amaranth, quinoa, mei egiptean, produse din ovăz fără gluten, orez brun şi mei este recomandată.
Eliminarea laptelui de vacă şi a produselor lactate. Laptele de vacă poate fi înlocuit cu produse îmbogăţite cu calciu, vitamină D şi alţi micronutrienţi. Între alternative enumerăm băuturile pe bază de orez, ovăz (dacă e fără gluten), in, cartof. Cele din soia, migdale şi caju de obicei sunt excluse din dieta de eliminare din esofagita eozinofilică. Laptele de cocos este totuşi cel mai adesea tolerat. Aceste băuturi pot fi folosite pentru copt şi gătit, dar sunt mai slab nutritive (mai puţine proteine şi calorii decât laptele de vacă), de aceea ele nu pot fi folosite la copilul mic ca echivalent al laptelui de vacă. Au fost raportate cazuri de kwashiorkor şi rahitism nutriţional la sugarii care au consumat substituenţi inadecvaţi ai laptelui. Copiii sub doi ani, nealăptaţi, ar trebui să aibă prescrisă o formulă pe bază de aminoacizi până la vârsta de 2 ani(16).
Eliminarea oului. Deşi nutrienţii din ou sunt uşor de înlocuit (tabelul 2), totuşi ouăle acţionează ca un liant, dând consistenţă unor produse coapte şi textură preparatelor importante pentru copiii mici.
Arahidele, alunele de pădure, peştele şi fructele de mare. Seminţele şi untul de seminţe sunt buni înlocuitori, oferind nutrienţi similari. Deficitul de vitamine A, D şi de Omega-3 provocat de eliminarea peştelui sau a arahidelor/alunelor de pădure poate fi oferit de seminţele de rapiţă sau de uleiul de in.
Dietele restrictive antigenic sunt mult mai uşor de implementat dacă pacientul primeşte o listă cu alimentele alternative şi cantităţile necesare per porţie, pentru a avea o dietă cât mai echilibrată nutriţional (tabelul 2).
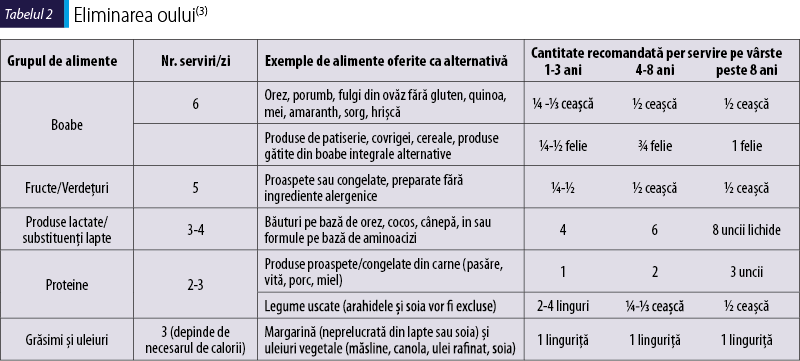
Porţiile şi unităţile de măsură sunt pentru alimente din SUA. Echivalente europene pentru o ceaşcă = 237 ml; o uncie de lichide = 29,5 ml; o linguriţă = 15 ml; o lingură = 15 ml; o uncie solidă = 28,31 g; o ceaşcă de fructe = o banană mare, 8 căpşuni, două prune mari; o ceaşcă de vegetale = 10 căpăţâni broccoli, 12 morcovi baby, un cartof dulce mare.
Consulturile periodice e necesar să cuprindă monitorizarea creşterii la copii, a greutăţii la adulţi şi o evaluare a dietei, care poate include un jurnal alimentar pe trei zile sau chestionare alimentare.
Reintroducerea alimentelor. În cazul în care dieta s-a dovedit un succes (remisiune a manifestărilor clinice şi histologice), se recomandă reintroducerea secvenţială a alimentelor, urmărind cu atenţie care dintre alimentele eliminate sunt de fapt triggeri ai esofagitei eozinofilice.
Totuşi, există o serie de provocări cu care se confruntă atât pacienţii, cât şi clinicienii în procesul de reexpansionare a dietei. Rolul alergologului este esenţial în această etapă, pentru a fi evitată o reacţie de hipersensibilitate IgE‑mediată la un aliment după excluderea îndelungată a acestuia din dietă, în condiţiile în care a preexistat o sensibilizare demonstrată la acel aliment (testare cutanată prick sau IgE serice specifice). Foarte rar pot apărea reacţii IgE‑mediate de novo la alimente.
Întrucât cele mai frecvente recăderi apar după lapte, ou, grâu şi soia, fiind cu mai mare probabilitate triggeri pentru esofagita eozinofilică, reintroducerea acestora în alimentaţie ar trebui să fie făcută într-o etapă cât mai tardivă. De aceea, de obicei, reintroducerea se face cu nuci şi peşte/fructe de mare, abordând progresiv şi alimentele cu riscuri mai mari.
În cazul recăderii, alimentul identificat ca fiind unul dintre triggerii pentru esofagita eozinofilică va fi evitat pe termen lung.
O altă provocare este dată de abilităţile deficitare de alimentare ale pacientului (aversiune faţă de mâncare, alimentare adaptativă sau texturile modificate ale dietei).
Concluzii
Dieta de restricţie antigenică poate induce remisiunea la majoritatea pacienţilor cu esofagită eozinofilică, oferind o alternativă pentru tratamentul pe termen lung. Cu toate acestea, dietele nu sunt lipsite de riscuri, putând avea impact asupra statusului nutriţional, a plăcerii de a mânca şi asupra calităţii vieţii în general.
Sub o îndrumare adecvată şi o monitorizare atentă, aceste riscuri pot fi minimizate, tot mai mulţi pacienţi putând beneficia de această opţiune nemedicamentoasă de tratament.
Bibliografie
- Nhu QM, Aceves SS. Medical and dietary management of eosinophilic esophagitis. Annals of Allergy, Asthma and Immunology. 2018 Aug; Volume 121, Issue 2, pages 156-161.
- Monjur A. Eosinophilic esophagitis in adults: An update. World J Gastrointest Pharmacol Ther. 2016 May 6; 7(2): 207-213.
- Groetch M, Venter C, Skypala I. Eosinophilic Gastrointestinal Disorders Committee of the American Academy of Allergy, Asthma and Immunology. Dietary Therapy and Nutrition Management of Eosinophilic Esophagitis: A Work Group Report of the AAAAI. J Allergy Clin Immunol Pract. 2017 Mar-Apr; 5(2):312-324.e29. doi: 10.1016/j.jaip.2016.12.026.
- Greenhawt M, Aceves SS, Spergel JM, Rothenberg ME. The management of eosinophilic esophagitis. J Allergy Clin Immunol Pract. 2013; 1:332-40.
- Kelly KJ, Lazenby AJ, Rowe PC, Yardley JH, Perman JA, Sampson HA. Eosinophilic esophagitis attributed to gastroesophageal reflux: improvement with an amino acid-based formula. Gastroenterology. 1995; 109:1503‑1512. [
- Papadopoulou A, Koletzko S, Heuschkel R, Dias JA, Allen KJ, Murch SH, et al. Management guidelines of eosinophilic esophagitis in childhood. J Pediatr Gastroenterol Nutr. 2014; 58:107-18.
- Boyce JA, Assa’ad A, Burks AW, Jones SM, Sampson HA, Wood RA, et al. Guidelines for the diagnosis and management of food allergy in the United States: summary of the NIAID-Sponsored Expert Panel Report. J Allergy Clin Immunol. 2010; 126:1105-18.
- Dellon ES, Gonsalves N, Hirano I, Furuta GT, Liacouras CA, Katzka DA. ACG clinical guideline: evidenced based approach to the diagnosis and management of esophageal eosinophilia and eosinophilic esophagitis (EoE). Am J Gastroenterol. 2013; 108:679-92.
- Delaney AL, Arvedson JC. Development of swallowing and feeding: prenatal through first year of life. Dev Disabil Res Rev. 2008; 14:105-17.
- Mukkada VA, Haas A, Maune NC, Capocelli KE, Henry M, Gilman N, et al. Feeding dysfunction in children with eosinophilic gastrointestinal diseases. Pediatrics. 2010; 126:e672-7.
- Lucendo AJ, Arias A, Gonzalez-Cervera J, Yague-Compadre JL, Guagnozzi D, Angueira T, et al. Empiric 6-food elimination diet induced and maintained prolonged remission in patients with adult eosinophilic esophagitis: a prospective study on the food cause of the disease. J Allergy Clin Immunol. 2013; 131:797-804.
- Kagalwalla AF, Sentongo TA, Ritz S, Hess T, Nelson SP, Emerick KM, et al. Effect of six-food elimination diet on clinical and histologic outcomes in eosinophilic esophagitis. Clin Gastroenterol Hepatol. 2006; 4:1097-102.
- Gonsalves N, Yang GY, Doerfler B, Ritz S, Ditto AM, Hirano I. Elimination diet effectively treats eosinophilic esophagitis in adults; food reintroduction identifies causative factors. Gastroenterology. 2012; 142:1451-1459.e1.
- Kagalwalla AF, Wechsler JB, Amsden K, Schwartz S. Efficacy of a 4-food elimination diet for children with eosinophilic esophagitis. Clin Gastroenterol Hepatol. 2017 Nov; 15(11):1698-1707.e7. doi: 10.1016/j.cgh.2017.05.048. Epub 2017, Jun 8.
- Arias A, Gonzalez-Cervera J, Tenias JM, Lucendo AJ. Efficacy of dietary interventions for inducing histologic remission in patients with eosinophilic esophagitis: a systematic review and meta-analysis. Gastroenterology. 2014; 146:1639-48.
- Awazuhara H, Kawai H, Baba M, Matsui T, Komiyama A. Antigenicity of the proteins in soy lecithin and soy oil in soybean allergy. Clin Exp Allergy. 1998; 28:1559-64.
Articole din ediţiile anterioare
Proctocolita alergică indusă de proteine alimentare – actualităţi de diagnostic şi tratament
Proctocolita alergică indusă de proteine alimentare (PAIPA) este o entitate benignă caracterizată de modificări inflamatorii la nivelul porţiunii d...
Etiologii multiple ale eozinofiliei sangvine
Deşi reprezintă o subpopulaţie mai restrânsă în sângele circulant, eozinofilele generează un interes din ce în ce mai mare din partea comunităţii ş...
Rinita alergică locală în populaţia pediatrică
Rinita alergică locală se caracterizează prin sinteza la nivelul mucoasei nazale de imunoglobuline E specifice, în absenţa sensibilizării sistemice...
Utilitatea probelor funcţionale în diagnosticul astmului alergic
Astmul este o afecțiune eterogenă, caracterizată prin inflamația cronică a căilor respiratorii şi prin hiperreactivitate bronşică la stimuli dire...