During the last decade, the ingestion of gluten, a composite of storage proteins, has been linked to various diseases, such as celiac disease, wheat allergy, nonceliac gluten sensitivity or gluten intolerance, that have an estimated global prevalence around 5%. Different mechanisms are involved in the pathogenesis of gluten-related disorders: allergic, immune-mediated and non-immune/non-allergic. Regarding wheat allergy and celiac disease we have strong diagnosis criteria and therapeutic algorithms. It is well established that ω-5 gliadine is the major allergen involved in wheat-dependent exercise-induced anaphylaxis. In genetically susceptible individuals (carriers of HLA class II DQ2 or DQ8) the ingestion of gluten can cause celiac disease. It is frequently associated with type I diabetes, autoimmune thyroiditis and primary biliary cirrhosis. In nonceliac gluten-sensitivity, intestinal and extraintestinal symptoms appear after the ingestion of gluten. The diagnosis can be established following negative tests for wheat allergy and celiac disease. Positive response to gluten-free diet for a limited period of time, followed by the reappearance of symptoms after gluten challenge, at this moment, is the best approach for confirming the diagnosis, because there are no objective criteria or specific biomarkers. Gluten sensitivity can be associated with irritable bowel syndrome, when besides gluten, fermentable oligo-, di-, and monosaccharides and polyols can contribute to the symptoms. When evaluating a patient with symptoms triggered by the ingestion of wheat, the doctor should consider besides wheat allergy and celiac disease, a less-well known disease, nonceliac gluten sensitivity, whose prevalence seems to be increasing.
Sensibilitatea la gluten – adevăr sau tendinţe?
Sensitivity to gluten: true or trend?
First published: 25 martie 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Aler.3.1.2019.2266
Abstract
Rezumat
În ultima decadă, ingestia glutenului, un complex de componente proteice de origine vegetală, a fost asociată cu diverse afecţiuni, cum sunt boala celiacă, alergia la grâu, sensibilitatea nonceliacă la gluten sau intoleranţa la gluten, estimându-se o prevalenţă globală a acestora de 5%. Din punct de vedere fiziopatologic, acestea pot fi împărţite în alergice, mediate autoimun şi afecţiuni determinate prin mecanism nonautoimun/nonalergic. Alergia la grâu şi boala celiacă sunt bine definite din punctul de vedere al criteriilor de diagnostic şi abordare terapeutică. Fracţiunea ω-5 gliadină a grâului este cel mai frecvent implicată în anafilaxia indusă de efort. Boala celiacă este o afecţiune complexă, a cărei apariţie este determinată de asocierea între factori genetici (HLA-DQ2 şi HLA-DQ8) şi de mediu (ingestia glutenului). Se asociază frecvent cu afecţiuni autoimune cum sunt diabetul zaharat de tip 1, tiroidita autoimună şi ciroza biliară primară. Sensibilitatea nonceliacă la gluten poate avea manifestări gastrointestinale şi extraintestinale, simptome debutate după ingestia de produse cu conţinut de gluten. Diagnosticul este de obicei unul de eliminare, după excluderea alergiei la grâu şi a bolii celiace. Deoarece nu există criterii obiective şi biomarkeri specifici, răspunsul terapeutic la o dietă fără gluten, urmat de reapariţia simptomatologiei la reintroducerea glutenului, confirmă prezenţa sensibilităţii nonceliace la gluten. Se poate asocia cu sindromul de intestin iritabil, când afecţiunea poate fi agravată şi de fermentarea oligozaharidelor, dizaharidelor, monozaharidelor şi a poliolilor. Pe lângă cele două afecţiuni bine cunoscute, alergia la grâu şi boala celiacă, în evaluarea pacienţilor cu simptome determinate de ingestia de grâu trebuie avută în vedere şi această nouă entitate, sensibilitatea nonceliacă la gluten, a cărei incidenţă este în creştere.
De la începuturile agriculturii în Mesopotamia, în urmă cu aproximativ 10000 de ani, grâul (Triticum aestivum) a susţinut dezvoltarea şi sănătatea omului până în prezent. În ultima decadă, glutenul şi alergia la grâu au reprezentat unul dintre cele mai mediatizate subiecte despre nutriţie. Majoritatea articolelor şi a reportajelor aparţin unor persoane din afara specialităţii medicale şi se referă la adoptarea unei diete fără gluten ca terapie pentru diverse semne şi simptome care nu pot fi încadrate într-un diagnostic precis. Studii efectuate la populaţia generală au arătat că procentul persoanelor care adoptă o dietă fără gluten este cu mult mai mare faţă de incidenţa afecţiunilor induse de gluten, ajungând până la 13%(1).
Proteinele din grâu au fost clasificate în funcţie de solubilitatea lor în apă (tabelul 1). Fracţiunile solubile în apă sau în soluţie salină sunt reprezentate de albumine şi globuline. Fracţiunile insolubile în apă, prolaminele, includ gliadinele şi gluteninele. Acestea reprezintă proteinele de stocaj majore din bobul de grâu, iar rolul lor în reacţiile alergice a fost stabilit, dar nu există un consens asupra calităţii de alergen major sau minor. Până în prezent au fost descrise 27 de alergene din bobul de grâu, începând cu Tri a 12 (profilina) până la Tri a 45(2).

În prezent sunt definite trei entităţi clinice distincte induse de componentele grâului: alergia la grâu, boala celiacă şi sensibilitatea nonceliacă la gluten (SNCG) sau intoleranţa la gluten. Sub umbrela alergiei la grâu sunt descrise alergia la grâu, anafilaxia dependentă de grâu indusă de efort, astmul brutarilor şi dermatita de contact.
Alergia la grâu este relativ rară, afectând mai puţin de 0,5% din populaţia generală(3). Majoritatea reacţiilor sunt IgE-mediate, iar sensibilizarea are loc la nivelul tractului digestiv. Simptomatologia este comună tuturor alergiilor alimentare, pornind de la urticarie şi angioedem, vărsături, dureri abdominale, diaree, afectarea tractului respirator până la anafilaxie. Afectează mai frecvent copiii şi, în marea majoritate a cazurilor, dispare odată cu înaintarea în vârstă, până la 16 ani. Diagnosticul se bazează pe suspiciunea clinică, testele cutanate prick şi/sau dozarea IgE specifice, iar standardul de aur este reprezentat de testul de provocare dublu orb, placebo-controlat(4).
În anafilaxia dependentă de grâu indusă de efort, alergenul incriminat este ω-5 gliadina (Tri a 19). Simptomatologia debutează de obicei la 1-3 ore (până la 6 ore) după ingestia unei mese care a conţinut şi preparate pe bază de grâu, urmată de efort fizic intens. De asemenea, au fost identificaţi cofactori ai reacţiei: consumul de medicamente antiinflamatoare nesteroidiene, alcoolul, infecţiile. Mecanismul nu a fost complet desluşit; se pare că efortul fizic creşte permeabilitatea pentru alergene la nivelul peretelui intestinal şi osmolaritatea, redistribuie fluxul sangvin sau scade pragul pentru degranularea mastocitară determinată de IgE(5).
Astmul brutarilor apare la persoane expuse ocupaţional la făina de grâu. Au fost identificate valori ale IgE specifice la făina de grâu care au o valoare predictivă pozitivă de 100%, 2,32 KU/l, respectiv, în cazul testelor cutanate prick, 5 mm. În centrele de referinţă, diagnosticul este stabilit ca urmare a unui test de provocare bronşică. Se utilizează soluţii apoase de făină administrate prin nebulizare cu concentraţii crescătoare (0,01; 0,1; 1; 10 şi 100 mg/ml) la intervale de 10 minute. Funcţia pulmonară se evaluează prin spirometrie sau pletismografie. Testul este pozitiv în cazul diminuării cu 20% a volumului expirator maxim pe secundă(6).
În cazul dermatitei de contact la făina de grâu, sensibilizarea are loc prin expunerea repetată la cosmetice care conţin fracţiuni proteice ale acestei cereale.
Boala celiacă este o afecţiune autoimună mediată de limfocitul T. Prevalenţa în populaţia generală este de 1 la 100 de indivizi, iar în rândul pacienţilor cu alergie alimentară severă este de cinci ori mai frecventă(7). Ingestia glutenului de către indivizi predispuşi genetic care sunt purtători ai alelei HLA DQ2/DQ8 poate determina o reacţie imună mediată de celula T împotriva transglutaminazei tisulare, o enzimă a matricei extracelulare, ceea ce conduce la afectare mucoasei şi, în cele din urmă, la atrofie a vilozităţilor intestinale. Vârsta de debut a bolii variază, dar de obicei apare la aproximativ 6 luni după introducerea cerealelor cu conţinut de gluten în alimentaţie. Afectează mai frecvent sexul feminin. Manifestările clinice sunt eterogene şi variază de la sindromul „clasic”, cu diaree, scădere ponderală şi malnutriţie, până la malabsorbţie selectivă a micronutrienţilor (fier, vitamina B12, calciu). Manifestările nespecifice includ simptome caracteristice sindromului de intestin iritabil, creşterea marcată a transaminazelor serice, ataxie cerebelară şi neuropatie periferică. Boala celiacă se poate asocia cu alte afecţiuni autoimune, precum diabet zaharat de tip 1, tiroidită autoimună, hepatită autoimună, infertilitate sau dermatită herpetiformă(8).
Pentru stabilirea diagnosticului de boală celiacă se recomandă dozarea anticorpilor antitransglutaminază tisulară IgA şi IgG, în paralel cu excluderea unei deficienţe de IgA. Sensibilitatea şi specificitatea testelor este de 95%, efectuate în timp ce pacientul consumă produse cu gluten(9). Astfel, în prezenţa simptomatologiei sugestive şi a anticorpilor antitransglutaminază tisulară pozitivi, se recomandă biopsia duodenală. Chiar şi în absenţa semnelor clinice, se recomandă screeningul pentru boală celiacă la rudele de gradul I ale pacienţilor cu boală celiacă, ale celor cu diabet zaharat de tip 1 sau cu sindrom Down(10). Singura metodă de tratament al bolii celiace în prezent este reprezentată de dieta fără gluten.
Sensibilitatea nonceliacă la gluten (SNCG) este o afecţiune relativ recent descrisă. Este caracterizată din punct de vedere clinic de simptome gastrointestinale şi extradigestive, care sunt corelate cu ingestia de gluten, la pacienţi la care s-au exclus alergia alimentară şi boala celiacă(8). În prezent, prevalenţa afecţiunii este dificil de estimat. Astfel, într-un studiu realizat în Marea Britanie, bazat doar pe un chestionar adresat populaţiei generale, s-a raportat o incidenţă de 13%, doar 1% având un diagnostic stabilit de medic(1). Incidenţa este mult mai mare în rândul pacienţilor cu sindrom de intestin iritabil, ajungând până la 28%(11). Cu toate acestea, afecţiunea este mai frecventă în rândul persoanelor de sex feminin de vârstă medie(8).
Fiziopatologia bolii este incomplet descifrată. Se pare că glutenul are unele proprietăţi biologice intrinseci care determină alterarea morfologiei şi motilităţii celulare, precum şi organizarea citoscheletului şi a contactului intercelular la nivelul proteinelor joncţiunilor strânse. Unele peptide din structura gliadinei se leagă de receptorul TLR2, care creşte producţia de interleukină 1, o citokină proinflamatorie, prin intermediul Myd88. Aceasta este o proteină-cheie care reglează eliberarea de zonulină ca răspuns la ingestia de gluten, iar aceasta creşte permeabilitatea intestinală. Pacienţii cu boală nonceliacă indusă de gluten au niveluri mai mari ale TLR2 faţă de cei cu boală celiacă, ceea ce determină disbioză similară cu cea din boala intestinală inflamatorie(12).
De asemenea, componentele nonproteice ale grâului, oligozaharidele, dizaharidele, monozaharidele şi poliolii fermentabili produc simptome nespecifice la pacienţii cu SNCG, în special meteorism abdominal. Aceşti carbohidraţi cu absorbţie scăzută fermentează la nivelul colonului, eliberând gaze care produc distensia colonului(13). Unii autori au lansat ipoteza că aceşti polioli ar sta la baza simptomatologiei, glutenul fiind doar un cofactor. Se pare că o dietă cu un conţinut scăzut de polioli ar conduce la dispariţia simptomatologiei(14).
Manifestările clinice sunt variate, astfel încât un grup de experţi a întocmit o serie de criterii de diagnostic (Criteriile de diagnostic Salerno). Simptomele pot fi împărţite în funcţie de frecvenţa cu care sunt întâlnite şi de organul sau sistemul afectat (tabelul 2)(15).
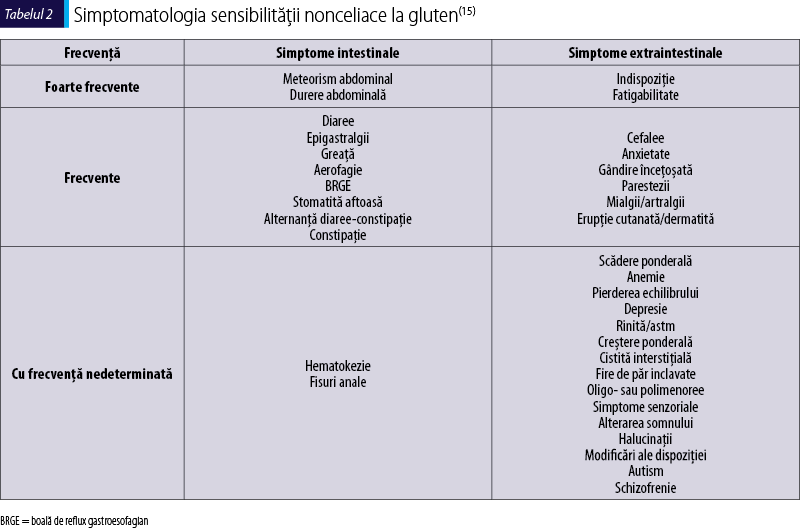
În octombrie 2014, la a treia Întâlnire Internaţională a Experţilor în Afecţiuni Gluten-Induse de la Salerno, Italia, s-a elaborat un ghid pentru diagnosticul SNCG. S-a stabilit că, în absenţa biomarkerilor, o evaluare atentă şi standardizată a pacienţilor în timpul dietei de eliminare a glutenului şi după reintroducerea acestuia în alimentaţie reprezintă cea mai bună metodă de diagnostic. SNCG ar trebui avută în vedere la pacienţii cu simptome digestive sau extradigestive, cu teste negative pentru alergia alimentară sau boala celiacă, ce afirmă agravarea simptomatologiei după ingestia de alimente cu conţinut de gluten. Pentru cuantificarea simptomatologiei se recomandă utilizarea Scalei de Evaluare a Simptomelor Gastrointestinale. Aceasta reprezintă un instrument validat pentru evaluarea simptomatologiei gastrointestinale(16). Având în vedere că o parte din simptomatologia SNCG nu aparţine tractului gastrointestinal, autorii recomandă acelaşi instrument şi pentru evaluarea acuzelor extraintestinale.
Ca demers diagnostic, primul pas este reprezentat de evaluarea completă pentru excluderea bolii celiace şi a alergiei la grâu. La momentul iniţial pacientul trebuie să aibă o dietă cu alimente cu conţinut de gluten de cel puţin şase săptămâni. Se completează un chestionar cu două săptămâni şi o săptămână înainte de începerea dietei fără gluten şi la momentul zero i se cere pacientului să aleagă unul, două sau trei simptome din lista din tabelul 2 şi să le cuantifice pe fiecare cu o valoare între 1 şi 10, unde 1 reprezintă afectare uşoară, 5 medie, iar 10 severă. La momentul zero se iniţiază dieta fără gluten, a cărei durată recomandată este de minimum şase săptămâni. Deşi ameliorarea simptomatologiei ar trebui să apară după o perioadă relativ scurtă, se recomandă observarea mai îndelungată, în special pentru simptomele fluctuante (de exemplu, cefaleea). În fiecare săptămână, pacientul va cuantifica severitatea acuzelor. Sunt considerate semnificative cele cu valoare de peste 3. Se consideră o probă terapeutică pozitivă diminuarea cu cel puţin 30% din scorul iniţial a unuia sau a tuturor celor trei simptome sau doar a unuia dintre simptome, în absenţa agravării celorlalte, pentru cel puţin 50% din perioada de supraveghere. Diagnosticul SNCG este infirmat de lipsa îmbunătăţirii simptomatologiei după şase săptămâni de dietă fără gluten(15).
Simptomele gastrointestinale care trebuie evaluate în chestionar sunt: durerea sau disconfortul abdominal, pirozisul, refluxul acid, meteorismul, greaţa şi vărsăturile, borborigmele, distensia abdominală, eructaţiile, flatulenţa, încetinirea sau accelerarea tranzitului intestinal, scaunele de consistenţă scăzută sau crescută, nevoia urgentă de defecaţie, senzaţia de evacuare incompletă. Simptomele extraintestinale care ar putea însoţi SNCG sunt: dermatita, cefaleea, gândirea înceţoşată, fatigabilitatea, paresteziile la nivelul membrelor, durerile articulare sau musculare, leziunile mucoasei bucale sau ale limbii ori altele.
La pacienţii care urmează o dietă fără gluten la momentul evaluării se recomandă testul de provocare cu gluten, de preferinţă dublu-orb placebo-controlat. Acesta este de obicei rezervat centrelor de cercetare. În practica de zi cu zi se recomandă testul de provocare placebo-controlat, pacientul primind o dietă cu minimum 8 g de gluten pe zi, completând acelaşi chestionar la sfârşitul fiecăreia dintre cele două săptămâni de urmărire. În cazul în care reapar simptomele, se poate întrerupe mai repede testul de provocare(15).
În figura 1 este schematizată o propunere de algoritm pentru diagnosticul SNCG, adaptat după cel propus de Elli et al(8).
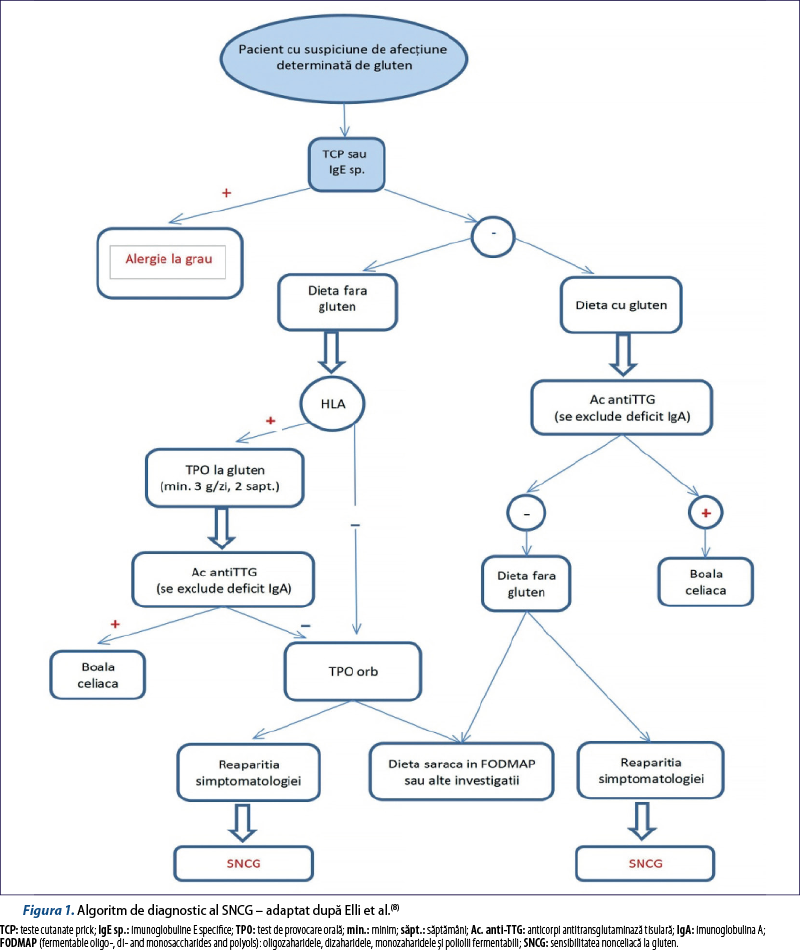
În ceea ce priveşte populaţia pediatrică, există mai puţine studii. Incidenţa la copii este mai mică faţă de cea de la adulţi (0,29:1)(17). Cu toate acestea, într-o cohortă de copii, procentul celor care urmau o dietă fără gluten era de 5 ori mai mare decât al celor diagnosticaţi cu boală celiacă(18). Principalele simptome sunt, în cazul copiilor, durerea abdominală şi diareea cronică. De asemenea, pot asocia fatigabilitate, meteorism abdominal, dureri la nivelul membrelor, vărsături, constipaţie, cefalee şi retard al creşterii(19). Ca şi în cazul adulţilor, nu există teste diagnostice sau biomarkeri.
Recomandarea terapeutică în cazul pacienţilor cu SNCG este reprezentată de dieta fără gluten. Unii autori recomandă o perioadă de eliminare completă a glutenului (chiar şi a produselor cu urme de gluten) de şase luni, urmată apoi de reintroducerea treptată a alimentelor cu conţinut de gluten. Aceasta se va face iniţial cu cereale cu conţinut scăzut de gluten – de exemplu, ovăz. Pe timp îndelungat, dietele fără gluten pot fi recomandate ca terapie „la nevoie” în perioadele de recădere a simptomatologiei(13).
Din cauza creşterii numărului de persoane care adoptă o dietă fără gluten în lipsa unui diagnostic cert, Societatea Germană de Alergologie şi Imunologie Clinică (DGAKI) a publicat un document care recomandă precauţie în evaluarea acestor pacienţi. Dintre aceştia, cei care continuă să îşi restricţioneze dieta în absenţa unui diagnostic confirmat vor fi îndrumaţi către personal specializat în boli de nutriţie(19).
SNCG este o entitate cu multiple faţete, a cărei patogeneză nu a fost încă pe deplin elucidată şi al cărei diagnostic este unul de excludere. În prezent, din ce în ce mai multe studii susţin dieta de eliminare a glutenului la pacienţi selecţionaţi, în absenţa bolii celiace sau a alergiei la grâu. Clinicienii trebuie să aprofundeze diferenţele între afecţiunile induse de gluten, pentru un diagnostic precis şi o abordare terapeutică adecvată.
Bibliografie
- Aziz I et al. A UK study assessing the population prevalence of selfreported gluten sensitivity and referral characteristics to secondary care. Eur J Gastroenterol Hepatol 2014; 26: 33-39.
- Matricardi PM, et al. EAACI Molecular Allergology User's Guide. Pediatr Allergy Immunol. 2016;27(suppl23):1-250.
- Zuidmeer L et al. The prevalence of plant food allergies: a systematic review. J Allergy ClinImmunol. 2008;121:1210-1218.
- Cianferoni A. Wheat allergy: diagnosis and management. Journal of Asthma and Allergy. 2016;9 13–25.
- Scherf KA et al. Wheat-dependent exercise-induced anaphylaxis. Clin Exp Allergy. 2016; 46(1):10-20.
- Kampen AN et al. Prediction of challenge test results by flour-specific IgE and skin prick test in symptomatic bakers. Allergy. 2008;63(7):897–902.
- Pillon R et al. Prevalence of celiac disease in patients with severe food allergy. Allergy. 2015; 70: 1346–1349.
- Elli L et al. Diagnosis of gluten related disorders: Celiac disease, wheat allergy and nonceliac gluten sensitivity. World J Gastroenterol. 2015; 21(23): 71107119.
- van der Windt DA et al. Diagnostic testing for celiac disease among patients with abdominal symptoms: a systematic review. JAMA 2010; 303: 17381746.
- Rubio-Tapia A et al. ACG clinical guidelines: diagnosis and management of celiac disease. Am J Gastroenterol. 2013; 108: 656-676.
- Biesiekierski JR et al. Gluten causes gastrointestinal symptoms in subjects without celiac disease: a doubleblind randomized placebocontrolled trial. Am J Gastroenterol. 2011; 106: 508-514.
- Casella G et al. Non celiac gluten sensitivity and diagnostic challenges. Gastroenterol Hepatol Bed Bench. 2018;11(3):197-202).
- Elli L et al. Nonceliac gluten sensitivity: Time for sifting the grain. World J Gastroenterol. 2015; 21(27): 8221-8226.
- Biesiekierski JR et al. No effects of gluten in patients with self-reported non-celiac gluten sensitivity after dietary reduction of fermentable, poorly absorbed, short-chain carbohydrates. Gastroenterology. 2013; 145: 320-328.
- Catassi C et al. Diagnosis of Nonceliac Gluten Sensitivity (NCGS): The Salerno Experts’ Criteria. Nutrients. 2015; 7: 4966-4977.
- Kulich KR et al. Reliability and validity of the Gastrointestinal Symptom Rating Scale (GSRS) and Quality of Life in Reflux and Dyspepsia (QOLRAD) questionnaire in dyspepsia: A six-country study. Health Qual. Life Outcomes. 2008; 6:12.
- Volta U et al. An Italian prospective multicenter survey on patients suspected of having nonceliac gluten sensitivity. BMC Medicine. 2014; 12:85.
- Tanpowpong P et al. Coeliac disease and gluten avoidance in New Zealand children. Arch Dis Child. 2012, Jan;97(1):12-6.
- Reese I et al. Nonceliac gluten/wheat sensitivity (NCGS) – a currently undefined disorder without validated diagnostic criteria and of unknown prevalence. Position statement of the task force on food allergy of the German Society of Allergology and Clinical Immunology (DGAKI). Allergo J Int. 2018; 27:147–151.
Articole din ediţiile anterioare
Urticaria cronică spontană în practica clinică
Urticaria cronică spontană (UCS) este o patologie care afectează 1-2% din populaţie. Infecţia cronică subiacentă şi stresul mental şi emoţional pot...
Actualităţi privind potenţiali markeri de răspuns la tratamentul cu omalizumab în urticaria cronică spontană
Urticaria este definită de apariţia papulelor urticariene, a angioedemului sau a ambelor timp de mai mult de şase săptămâni în urticaria cronică sa...
Hiperimunoglobulinemia E în imunodeficienţele primare
Această lucrare reprezintă o trecere în revistă a imunodeficienţelor primare care evoluează cu niveluri înalte ale imunoglobulinei E (IgE) serice. ...
Alergia alimentară la mazăre şi corelaţiile acesteia cu procesarea termică
Alergiile produse de leguminoase ocupă unul dintre primele cinci locuri în topul alergiilor alimentare, deoarece leguminoasele reprezintă principal...