Inflammatory bowel diseases (IBD) are a group of conditions characterized by chronic inflammation of the digestive tract segments. These diseases are multifactorial conditions with an increased prevalence in modern society, a consequence of genetic and environmental factors. The main IBD are ulcerative colitis and Crohn’s disease, which have many similarities but differ by localization in the digestive tract and by the degree of histopathological damage. The groups of drugs used in the treatment of IBD are: aminosalicylates, corticosteroids, antibiotics, immunomodulators and biological agents. Although there has been a lot of progress in the treatment of these diseases, currently there is no curative treatment.
Abordări farmacoterapeutice ale bolilor inflamatorii intestinale
Pharmacotherapeutic approaches of inflammatory bowel disease
First published: 22 martie 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/FARM.186.1.2019.2252
Abstract
Rezumat
Bolile inflamatorii intestinale (BII) reprezintă un grup de afecţiuni care se caracterizează printr-o inflamaţie cronică, la nivelul segmentelor tubului digestiv. Aceste boli sunt afecţiuni multifactoriale, cu o răspândire crescută în societatea modernă, fiind o consecinţă a factorilor genetici şi de mediu. Principalele BII sunt colita ulcerativă şi boala Crohn, care prezintă numeroase asemănări, dar care diferă prin localizarea la nivelul segmentelor tubului digestiv şi prin gradul de afectare histopatologică. Dintre grupele de medicamente utilizate în tratamentul BII enumerăm: aminosalicilaţi, corticosteroizi, antibiotice, imunomodulatoare şi agenţi biologici. Cu toate că au fost înregistrate numeroase progrese în tratamentul acestor boli, nu există în acest moment un tratament curativ.
Ce sunt bolile inflamatorii intestinale?
Bolile inflamatorii intestinale (BII) reprezintă un grup de afecţiuni care se caracterizează printr-o reactivitate anormală a sistemului imunitar, cu producerea unei inflamaţii cronice la nivelul segmentelor tubului digestiv. Acest grup de afecţiuni digestive include două afecţiuni principale: boala Crohn (BC) şi rectocolita ulcero-hemoragică (colită hemoragică – CU), însă există pacienţi care pot prezenta o formă intermediară(1).
Care sunt cauzele BII?
Etiologia BII nu este încă pe deplin cunoscută, dar se presupune că mai mulţi factori sunt implicaţi. Probabil, boala apare la indivizii predispuşi genetic, sub influenţa unor diferiţi factori de mediu.
Dintre factorii de risc enumerăm:
Vârsta. De obicei, BII sunt diagnosticate până la vârsta de 30 de ani.
Rasa. Incidenţa cea mai crescută a fost observată la populaţia albă, iar riscul este şi mai crescut pentru evreii Ashkenazi.
Istoricul familial. Riscul creşte când o rudă apropiată (părinţi, fraţi, copii) are o BII.
Fumatul. Există un paradox al fumatului în BII. Fumătorii prezintă un risc cu 50% mai mare de a dezvolta BC. Pentru CU însă, se poate observa un efect protector al fumatului, incidenţa fiind mult crescută în cazul nefumătorilor şi în special al foştilor fumători. O perioadă s-a crezut că nicotina este responsabilă de acest efect protector, care însă a fost confirmat în studiile pe animale de laborator.
Medicamentele. Unele medicamente precum antiinflamatoarele nesteroidiene (ibuprofen, naproxen, diclofenac etc.), contraceptivele orale sau antibioticele (utilizate mai ales în primul an de viaţă) cresc riscul apariţiei BII sau pot agrava simptomele acestora.
Factorii de mediu. Prezintă un risc crescut de BII persoanele care:
-
trăiesc în zone industrializate cu un grad ridicat de poluare;
-
trăiesc în zonele nordice şi prezintă o expunere deficitară la lumina soarelui. Această teorie este în concordanţă cu cele care afirmă că niveluri scăzute de vitamină D sunt asociate cu un risc crescut de dezvoltare a BII;
-
au o dietă bogată în grăsimi sau alimente rafinate(2,3,4).
Care este incidenţa BII?
Primul caz de colită ulcerativă a fost descris în 1875, numărul pacienţilor crescând considerabil începând cu primii ani ai secolului XX, în zonele industrializate precum Europa de Vest, America de Nord, Australia şi Noua Zeelandă. În zilele noastre este estimat că aproximativ 0,5% din populaţia acestor ţări suferă de o formă de BII. De remarcat faptul că în ultimii ani a fost observată o creştere a numărului de cazuri de BII în ţările în curs de dezvoltare, nou industrializate, precum China şi India, preconizându-se că în următoarele decenii numărul pacienţilor din aceste zone va fi similar cu al celor din Europa de Vest(5,6).
Care sunt principalele diferenţe între BC şi CU?
Cele două tipuri de BII prezintă numeroase asemănări, precum:
-
pot apărea la orice vârstă, dar în special în primele decade de viaţă;
-
afectează în mod egal atât femeile, cât şi bărbaţii;
-
simptomele şi etiologia sunt asemănătoare.
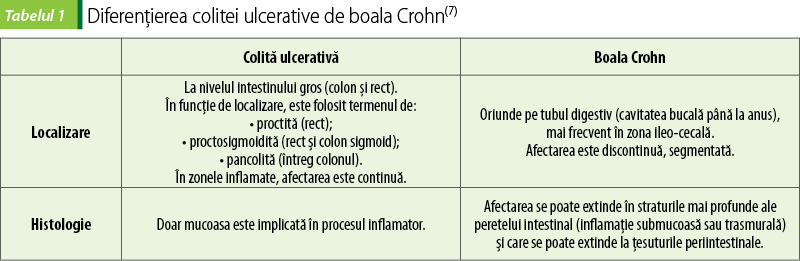
Diferenţele principale constau în localizare şi gradul de afectare histopatologică (tabelul 1).
Care sunt simptomele BII?
Simptomele BII variază în funcţie de severitatea inflamaţiei. Există episoade de acutizare, când simptomele se manifestă mai intens, şi perioade de remisiune, când simptomele sunt diminuate sau chiar dispar.
Simptomele comune celor două tipuri de BII includ:
-
diaree;
-
febră şi oboseală;
-
crampe şi durere abdominală;
-
sânge în fecale (care apare frecvent în CU şi mai rar în BC);
-
apetit scăzut;
-
pierdere în greutate;
-
artrită şi artralgie;
-
anemie;
-
erupţii cutanate;
-
uveită(2,8).
Principalul simptom al CU este diareea sangvinolentă. În trecut, CU prezenta o rată mare de mortalitate, dar care a scăzut datorită progreselor făcute în domeniul medical. Majoritatea pacienţilor suferă un episod acut o dată pe an, dar pentru un procent însemnat acestea sunt mult mai frecvente. Dintre pacienţii cu pancolită severă, 20-30% trebuie să fie supuşi operaţiei de colectomie(9). Un simptom frecvent al CU este formarea unor pseudopolipi inflamatori benigni. Aceştia apar ca urmare a perioadelor repetate de inflamaţie şi ulceraţie, urmate de un proces intensiv de vindecare. Aceştia pot provoca complicaţii precum sângerări şi obstrucţie şi sunt consideraţi un factor de risc pentru cancerul colorectal, necesitând monitorizare endoscopică frecventă(10).
Pentru BC, durerea abdominală, diareea şi pierderea în greutate sunt mai frecvente. Ca urmare a inflamaţiei severe poate apărea un proces de fibrozare, cu formarea de stricturi care în cazuri grave pot produce ocluzie intestinală. Frecvent pot apărea fistule (ulceraţii adânci), de obicei perianale, şi abcese. În funcţie de prezenţa acestor modificări histopatologice, se poate clasifica în:
-
BC fără stricturi şi nepenetrantă;
-
BC penetrantă;
-
BC cu stricturi.
Aproximativ 70-80% dintre pacienţi necesită tratament chirurgical. BC produce un grad de dizabilitate mai mare decât CU, doar 75% dintre pacienţi fiind capabili să muncească la un an după punerea diagnosticului(9).
Care sunt clasele de medicamente utilizate în tratamentul BII?
Nu există în acest moment tratament curativ pentru BII. Scopul tratamentului este de a elimina simptomele, a îmbunătăţi calitatea vieţii, a evita spitalizările şi intervenţiile chirurgicale. Alegerea tratamentului se face în funcţie de stadiul, localizarea şi severitatea bolii.
Principalele clase de medicamente utilizate în prezent sunt:
-
Aminosalicilaţi
-
Corticosteroizi (CS)
-
Antibiotice şi chimioterapice
-
Imunomodulatoare
-
Agenţi biologici.
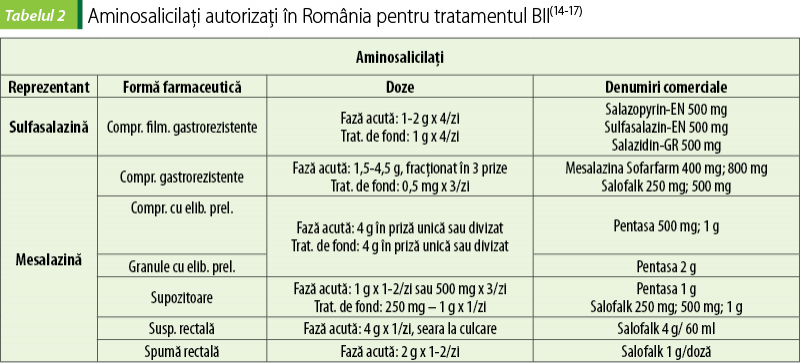
1. Aminosalicilaţi
Aminosalicilaţii fac parte dintr-o clasă de compuşi care conţin în moleculă acidul 5 amino-salicilic (mesalazina; 5-ASA). Acţionează la nivelul celulelor epiteliale, scăzând eliberarea mediatorilor lipidici, celulelor inflamatoare, a citokinelor şi a speciilor reactive de oxigen.
Se pot administra oral şi rectal, pentru tratamentul episoadelor acute uşoare şi moderate ale BC şi CU, precum şi ca tratament de fond al CU. Utilizarea lor ca tratament de fond al BC este limitată, din cauza eficacităţii scăzute(11).
Pentru ca substanţa activă, mesalazina, să ajungă la locul de acţiune, se folosesc:
-
forme farmaceutice orale cu eliberare modificată, care pot elibera mesalazina la nivelul intestinului subţire şi/sau intestinului gros;
-
forme farmaceutice rectale, care sunt active la nivelul rectului (supozitoare), rectului şi sigmoidului (spume rectale) şi la nivelul rectului, sigmoidului şi colonului descendent (clisme);
-
prodroguri care eliberează substanţa activă sub influenţa bacteriilor din colon (sulfasalazina, olsalazina, balsalazina)(12).
Primul reprezentant al acestei clase a fost sulfasalazina. Aceasta eliberează în colon 5-ASA şi sulfapiridină, responsabilă de majoritatea reacţiilor adverse (RA), precum oligospermie reversibilă, cefalee, greaţă, erupţii cutanate, care apar la aproximativ 45% dintre pacienţi. Dintre reacţiile idiosincratice ale sulfasalazinei enumerăm: sindrom Stevens-Johnson, pancreatită, agranulocitoză, alveolită. Ceilalţi aminosalicilaţi sunt mult mai bine toleraţi. Toţi aminosalicilaţii produc nefrotoxicitate, inclusiv nefrită interstiţială şi sindrom nefrotic(9,13).
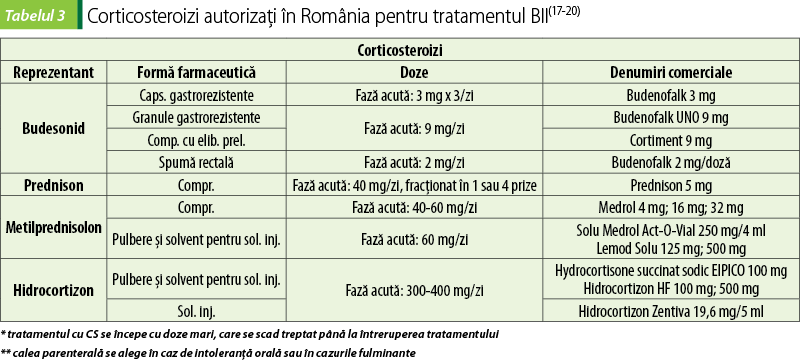
2. Corticosteroizi (CS)
CS sunt antiinflamatoare potente utilizate în faza acută a formelor moderate şi severe de BC şi CU. Nu se utilizează ca tratament de fond, din cauza lipsei de eficacitate şi a RA care apar la utilizare îndelungată. Tratamentul este cuprins de obicei între 7 şi 28 de zile(11).
Mecanismul lor de acţiune constă în suprimarea transcripţiei interleukinelor şi a metabolismului acidului arahidonic, precum şi stimularea apoptozei limfocitelor de la nivelul mucoasei tubului digestiv(9).
Administrarea lor se poate face pe mai multe căi:
-
oral – budesonid, prednison, prednisolon etc.;
-
intravenos – hidrocortizon, metilprednisolon etc.;
-
intrarectal – budesonid, betametazonă, hidrocortizon, prednisolon metasulfobenzoat.
Dintre CS, budesonidul se remarcă printr-o absorbţie scăzută şi un efect de prim pasaj hepatic intens, ceea ce îi conferă avantajul de a avea efecte locale la nivel digestiv, utile în BII, şi toxicitate sistemică scăzută.
Aproximativ 50% dintre pacienţi raportează RA la utilizarea CS. Acestea se pot clasifica astfel:
-
RA datorate dozelor suprafiziologice – acnee, edeme, tulburări de somn şi dispoziţie, dispepsie, intoleranţă la glucoză;
-
RA asociate tratamentelor mai lungi de 12 săptămâni – cataractă, osteoporoză, osteonecroză, miopatie, creşterea riscului de infecţii;
-
RA care apar la întreruperea tratamentului – insuficienţă corticosuprarenală (la întreruperea bruscă), mialgie, artralgie, stare generală proastă, presiune intracraniană crescută(9).
3. Antibiotice
Antibioticele se folosesc în tratamentul complicaţiilor infecţioase consecutive BII, precum abcesele şi fistulele, sau al diverticulitei, care poate apărea după colectomie.
Cele mai utilizate antibiotice sunt metronidazol (10-20 mg/kg/zi) şi ciprofloxacina (500 mg x 2/zi) sau o combinaţie între cele două.
Substanţele antimicrobiene nu sunt recomandate pentru tratamentul formelor uşor-moderate de CU, cu toate că există studii care le susţin eficacitatea(9).
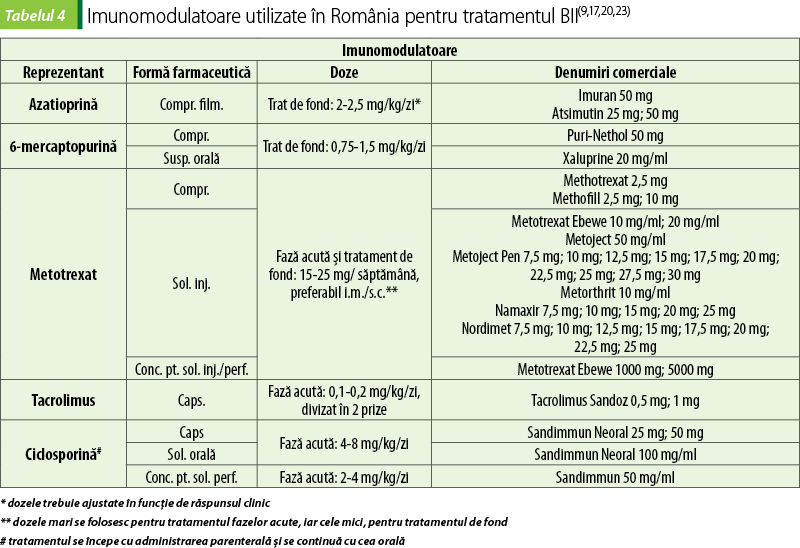
4. Imunomodulatoare
Imunomodulatoarele sunt substanţe care modifică activitatea sistemului imunitar, cu scăderea răspunsului inflamator. Imunomodulatoare care se folosesc pentru tratamentul BII sunt:
-
tiopurinele: azatioprina (AZA), 6-mercaptopurina (MP);
-
metotrexat (MTX);
-
inhibitori de calcineurină: tacrolimus, ciclosporina.
-
Se utilizează în caz de:
-
intoleranţă sau ineficienţă a tratamentului cu aminosalicilaţi, antibiotice sau CS;
-
boală dependentă de CS;
-
complicaţii (ex.: fistule);
-
pentru a preveni recăderile după intervenţiile chirurgicale.
Principalul factor limitativ al terapiei cu aceste substanţe este toxicitatea lor sau lipsa studiilor pe termen lung în tratamentul BII.
Tiopurinele constituie o clasă de substanţe care acţionează ca antimetaboliţi ai purinelor şi care se folosesc în tratamentul leucemiei, al bolilor autoimune şi pentru prevenirea rejecţiei de transplant.
Se folosesc atât în CU, cât şi în BC, în special ca tratament de fond, deoarece efectul terapeutic are o latenţă mare. Se pot utiliza şi în fazele acute ale bolii, dar doar asociate cu alte medicamente cu efect imediat. Mecanismul de acţiune constă în inhibarea sintezei ribonucleotidelor şi creşterea apoptozei celulelor T.
Prezintă numeroase RA, care apar la aproximativ 20% dintre pacienţi, cele mai importante fiind: creşterea riscului apariţiei limfomului, reacţii gastrointestinale precum greaţă şi hepatotoxicitate, mielosupresie, alopecie, pancreatită şi leucopenie(21).
Metotrexatul este un inhibitor al dihidrofolat-reductazei, care se foloseşte când pacienţii nu tolerează sau sunt rezistenţi la tratamentul cu tiopurine. Se foloseşte pentru tratamentul fazelor acute şi ca terapie de menţinere pentru ambele tipuri de BII.
Reacţiile adverse apar frecvent şi sunt greu de suportat de către pacienţi, motiv pentru care aceştia renunţă la tratament. RA digestive precum greaţa, voma, diareea şi stomatita pot fi limitate prin administrarea concomitentă de acid folic 5 mg, o dată pe săptămână, la 3 zile după administrarea MTX. Dintre RA grave enumerăm: hepatotoxicitatea, pneumonita şi creşterea riscului de infecţii(9).
Cisclosporina şi tacrolimus sunt medicamente care inhibă calcineurina, o enzimă implicată în activarea limfocitelor T, şi care sunt folosite în special pentru prevenirea rejecţiei de transplant.
Sunt utilizate şi în tratamentul formelor acute severe de CU, refractare la alte tratamente, efectul lor instalându-se rapid. Durata tratamentului trebuie limitată la maximum 3-6 luni, din cauza RA severe. Până la 59% dintre pacienţi prezintă: tremor, parestezii, stare generală proastă, cefalee, hepatotoxicitate, hiperplazie gingivală şi hirsutism. Reacţii adverse foarte grave, precum insuficienţă renală şi neurotoxicitate, pot apărea la aproximativ o cincime dintre pacienţi(22).
5. Terapiile biologice
Pentru tratamentul BII se utilizează anticorpi monoclonali, antifactor de necroză tumorală (TNFα). Dintre aceştia, infliximab este un anticorp monoclonal IgG1 chimeric uman-murinic produs în celule hibride murine care se administrează intravenos, iar adalimumab este un anticorp monoclonal uman recombinant produs pe celulele ovariene de hamster chinezesc şi care se administrează subcutanat (tabelul 5)(24,25).

Aceşti anticorpi sunt indicaţi în tratamentul formelor active moderate până la severe de CU sau BC, la pacienţii care nu tolerează sau nu au răspuns la terapia cu CS sau imunosupresoare. Infliximab este autorizat şi pentru tratamentul BC active, fistulizate, la pacienţii care nu au răspuns la tratamentul convenţional (inclusiv antibiotice, drenaj şi terapie imunosupresoare)(9,24,25).
Din cauza numeroaselor reacţii adverse, tratamentul cu aceşti anticorpi trebuie continuat doar dacă se observă un beneficiu clar, confirmat atât de simptomele clinice, cât şi de markerii biochimici şi de investigaţii, precum endoscopia. Dacă boala intră în remisiune, se poate lua în considerare oprirea tratamentului şi reluarea acestuia numai dacă simptomele reapar(9).
Cele mai frecvente reacţii adverse ale terapiilor anti-TNFα sunt:
-
Creşterea riscului de apariţie a infecţiilor oportuniste, precum tuberculoza, hepatita B, pneumonia cu Pseudomonas sau septicemia fungică. Incidenţa acestui tip de infecţii creşte foarte mult când pacienţii sunt sub tratament concomitent cu corticosteroizi sau imunosupresoare. Pacienţii care încep tratamentul cu anticorpi anti-TNFα trebuie testaţi pentru detectarea formelor latente de tuberculoză sau hepatită virală. Pentru screeningul TBC se recomandă efectuarea de radiografii pulmonare, a testului cutanat la tuberculină şi a testului de eliberare a interferonului gama. Cel din urmă prezintă avantajul că rezultatele sale nu sunt influenţate de vaccinarea BCG, aşa cum se întâmplă în cazul IDR-ului la tuberculină. Pentru screeningul hepatitei B se recomandă determinarea: antigenului de suprafaţă al virusului hepatitei B (Ag HBsAg), a anticorpilor împotriva antigenului de suprafaţă al virusului hepatic B (anti-HBs) şi a anticorpilor împotriva antigenului central al virusului hepatic B (anti-HBc)(9,11).
-
Reacţii adverse legate de perfuzare, inclusiv reacţii anafilactice, care pot să apară în timpul sau în decurs de câteva ore după administrarea perfuziei.
-
Formarea de anticorpi anti-infliximab sau anti-adalimumab. Formarea acestora duce la creşterea riscului apariţiei reacţiilor adverse acute legate de perfuzare. De asemenea, s-a observat şi o asociere între apariţia acestor anticorpi şi scăderea duratei răspunsului terapeutic.
-
Efecte cancerigene. S-a observat o creştere a incidenţei afecţiunilor maligne precum limfom, leucemie, melanom, cancer cervical, cancer pulmonar (în special la pacienţii fumători) şi cancer de colon.
-
Demielinizare atât a sistemului nervos central, cu apariţia sclerozei multiple şi nevritei optice, precum şi demielinizare periferică, ducând la apariţia neuropatiior periferice, precum sindromul Guillain-Barré.
-
Insuficienţă cardiacă. Anticorpii anti-TNFα trebuie utilizaţi cu precauţie la pacienţii cu insuficienţă cardiacă uşoară (clasa I/II NYHA) şi sunt contraindicaţi la cei cu insuficienţă cardiacă de clasa III/IV NYHA(9,11,24,25)
În concluzie, BII sunt afecţiuni multifactoriale care sunt răspândite în societatea modernă, fiind o consecinţă a factorilor genetici şi de mediu. Cu toate că au fost înregistrate numeroase progrese în tratamentul acestor boli, cu o îmbunătăţire remarcabilă a calităţii vieţii pacienţilor, nu există în acest moment un tratament curativ. Numeroase studii clinice cu terapii biologice sunt în desfăşurare şi se crede că în următoarele decade vor avea loc schimbări majore în managementul acestor boli.
Abrevieri: 5-ASA - mesalazină; ADA - Adalimumab; AZA - Azatioprină; BC - boală Crohn; BII - boli inflamatorii intestinale; CS - corticosteroizi; CU - colită ulcerativă; IFX - Infliximab; MP 6 - Mercaptopurină; MTX - Metotrexat; RA - reacţii adverse; TNFα - factor de necroză tumorală
Bibliografie
- Bing XIA, Crusius JBA, et al. Inflammatory bowel disease: definition, epidemiology, etiologic aspects, and immunogenetic studies. World J Gastroenterol. 1998, 4(5):446-458.
- Mayo Clinic. Inflammatory bowel disease (IBD). Disponibil on-line la: https://www.mayoclinic.org/diseases-conditions/inflammatory-bowel-disease/symptoms-causes/syc-20353315, accesat februarie 2019.
- Ananthakrishnan AN. Environmental Triggers for Inflammatory Bowel Disease. Curr Gastroenterol Rep. 2013; 15(1): 302.
- Molodecky NA, Kaplan GG. Environmental Risk Factors for Inflammatory Bowel Disease. Gastroenterol Hepatol. 2010, 6(5): 339–346.
- Kaplan GG, Ng SC. Understanding and Preventing the Global Increase of Inflammatory Bowel Disease. Gastroenterology. 2017; 152(2):313-321.
- Ng SC, Shi HY, et al. Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies. Lancet. 2017; 390: 2769–2778.
- Waugh N, Cummins E, et al. Faecal calprotectin testing for differentiating amongst inflammatory and non-inflammatory bowel diseases: systematic review and economic evaluation. Health Technol Assess. 2013; 17(55): 1-211.
- Vavricka SR, Schoepfer A, et al. Extraintestinal Manifestations of Inflammatory Bowel Disease. Inflamm Bowel Dis. 2015; 21(8): 1982–1992.
- Mowat C, Cole A, et al. Guidelines for the management of inflammatory bowel disease in adults. Gut. 2011; 60:571-607.
- Politis DS, Katsanos KH, et al. Pseudopolyps in inflammatory bowel diseases: Have we learned enough? World J Gastroenterol. 2017; 23(9): 1541–1551.
- Matsuoka K, Kobayashi T, et al. Evidence-based clinical practice guidelines for inflammatory bowel disease. J Gastroenterol. 2018; 53(3):305-353.
- Crohn Colitis Foundation. Aminosalicylates. Disponibil on-line la: http://www.crohnscolitisfoundation.org/resources/aminosalicylates.html. Accesat februarie 2019
- Cristea AN (sub red.). Tratat de Farmacologie. Editura Medicală, Bucureşti, 2004.
- ANM/Sulfasalazin-EN/Rezumatul caracteristicilor produsului/Disponibil on-line la www.anm.ro
- ANM/Mesalazina Sofarfarm/Rezumatul caracteristicilor produsului/ Disponibil on-line la www.anm.ro
- ANM/Salofalk/Rezumatul caracteristicilor produsului/ Disponibil on-line la www.anm.ro
- Dobrescu D, Negres S et al. MEMOMED 2019, ediţia a 24-a. Editura Universitară, 2019.
- ANM/Budenofalk/Rezumatul caracteristicilor produsului/ Disponibil on-line la www.anm.ro
- ANM/Cortiment /Rezumatul caracteristicilor produsului/ Disponibil on-line la www.anm.ro
- Mahadevan U. Medical Treatment of Ulcerative Colitis. Clin Colon Rectal Surg. 2004 Feb; 17(1): 7–19.
- Neurath M. Thiopurines in IBD. What Is Their Mechanism of Action? Gastroenterol Hepatol (NY). 2010; 6(7): 435–436.
- Nakase H, Yoshino T, Matsuura M. Role in calcineurin inhibitors for inflammatory bowel disease in the biologics era: when and how to use. Inflamm Bowel Dis. 2014; 20(11):2151-2156.
- ANM/Imuran/Rezumatul caracteristicilor produsului/Disponibil on-line la www.anm.ro
- ANM/Humira/Rezumatul caracteristicilor produsului/Disponibil on-line la www.anm.ro
- ANM/Remicade/Rezumatul caracteristicilor produsului/Disponibil on-line la www.anm.ro