Glaucoma often requires an individualized treatment, combining pharmacotherapy (topical and sometimes systemic), with laser treatment and surgery. Prostaglandin analogues, beta‑blockers and adrenergic agonists are still the gold standard in glaucoma therapy, as single agents or combined. The modern therapy of glaucoma involves combinations of drugs with neuroprotectors of the optic nerve, Rho kinase inhibitors, vasopressin receptors agonists, monoclonal antibodies, agonists of adenosine receptors, and serotoninergic drugs. A modern trend in glaucoma treatment highlights new technologies using stem cells and gene therapy: thus, the administration of genes, gene ablation and stem cell transplant are promising approaches in the management of glaucoma.
Actualităţi în farmacoterapia glaucomului
New insights in the pharmacotherapy of glaucoma
First published: 30 octombrie 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/FARM.190.5.2019.2630
Abstract
Rezumat
Glaucomul necesită un tratament adaptat, combinând farmacoterapia (topică şi, după caz, sistemică) cu tratamentul cu laser şi intervenţii chirurgicale. Medicaţia standard în glaucom o constituie analogii de prostaglandină, beta-blocantele şi agoniştii adrenergici, folosiţi fie ca monoterapie sau în terapie combinată. Tratamentul modern al glaucomului presupune utilizarea asocierii de medicamente clasice într-o formulă cu eficacitate crescută cu factori neuroprotectori ai nervului optic, inhibitori de Rho-kinază, antagonişti ai receptorilor pentru vasopresină, anticorpi monoclonali, agonişti ai receptorilor pentru adenozină şi agenţi serotoninergici. O nouă oportunitate pentru tratamentul glaucomului este aplicarea tehnologiilor legate de utilizarea celulelor stem şi terapia genică. Abordări promiţătoare pentru managementul glaucomului şi al altor afecţiuni neurodegenerative oftalmice le constituie administrarea de gene, ablaţia genelor şi transplantul de celule stem.
Managementul glaucomului se bazează pe terapia medicamentoasă clasică şi modernă, iar în cazul eşecului acestora, pe terapia chirurgicală. Toate medicamentele utilizate în prezent în tratarea glaucomului reuşesc să oprească sau să întârzie agravarea bolii prin reducerea presiunii intraoculare, prevenind astfel lezarea nervului optic. În cazul glaucomului nu este disponibilă o schemă de tratament unanim acceptată, în literatura de specialitate existând controverse privind alegerea strategiei terapeutice potrivite în legătură cu raportul risc/beneficiu/cost al medicaţiei.
Cea mai mare parte a autorilor consideră că tratamentul standard în glaucom este reprezentat de analogii de prostaglandină, beta-blocantele şi agoniştii adrenergici, folosiţi fie ca monoterapie, fie în administrare combinată.
1. Farmacoterapia clasică
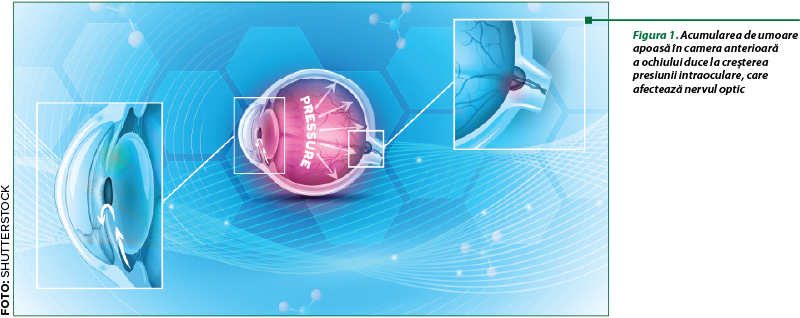
Tratamentul clasic urmăreşte atât prevenirea creşterii presiunii intraoculare prin scăderea producţiei umorii apoase, cât şi ameliorarea simptomatologiei prin acţiune asupra reţelei trabeculare şi favorizarea drenării umorii apoase.
Terapia clasică în glaucom presupune folosirea următoarelor medicamente.
Cu administrare topică
-
agonişti adrenergici: brimonidină, apraclonidină(6)
-
beta-blocante: betaxolol, carteolol, betaxolol, levobunolol, metipranol, timolol(20)
-
inhibitori de anhidrază carbonică: dorzolamidă, brinzolamidă(19)
-
parasimpaticomimetice: pilocarpină, carbacol, demecarium, ecotiofat, isoflurofat
-
analogi de prostaglandine: latanoprost, travoprost, bimatoprost, tafluprost, latanoprosten(19).
Cu administrare sistemică
-
inhibitori de anhidrază carbonică: acetazolamidă, metazolamidă(6).
În prezent sunt disponibile pe piaţă medicamente care conţin asocieri ale acestor substanţe, ca de exemplu timolol şi dorzolamidă, brimonidină şi timolol sau brinzolamidă şi brimonidină, preparate care prezintă avantajul preţului mai redus şi al administrării mai convenabile la pacient(28).
2. Farmacoterapia modernă în glaucom
2.1. Antagoniştii receptorilor de vasopresină (vaptani) produc creşterea diurezei prin acţiune pe subtipul 2 al receptorilor pentru vasopresină din tubul renal colector, ceea ce duce la o excreţie mai intensivă a apei. Ei sunt folosiţi mai frecvent în managementul corecţiei hiponatriemiei din sindromul secreţiei defectuoase de hormon antidiuretic, în insuficienţa cardiacă congestivă, ciroza hepatică, dar ultimele studii indică o eficacitate crescută şi în glaucom, în boala Ménière, în edemul cerebral, sindromul Cushing şi în carcinomul pulmonar cu celule mici. Dintre vaptani, conivaptan se administrează intravenos, în timp ce tolvaptan, lixivaptan şi satavaptan au administrare orală(17,23).
2.2. Anticorpi monoclonali
Noile descoperiri din domeniul angiogenezei şi rolul acesteia în glaucom au dus la extinderea cercetărilor privind opţiunile terapeutice pentru bolile oculare neovasculare. Neovascularizaţia este mediată prin intermediul stimulilor angiogenetici (cum ar fi factorul de creştere endotelială vasculară), care poate fi inhibat direct de bevacizumab sau ranibizumab, medicamente din categoria anticorpilor monoclonali(14). Acestea încetinesc dezvoltarea vaselor noi de sânge prin inhibarea factorului A de creştere endotelială vasculară. Au fost folosite iniţial ca terapie de primă linie în cancerul colorectal metastatic, iar în prezent se utilizează şi în oftalmologie în glaucom, împotriva degenerării maculare legate de vârstă, a retinopatiei diabetice proliferative, a neovascularizaţiei irisului(4).
În glaucom, injecţiile intravitroase de bevacizumab şi-au demonstrat eficacitatea posttrabeculectomie la pacienţii cu edem macular sau neovascularizaţie, prin reducerea vascularizaţiei şi modularea proliferării fibroblastelor în cursul cicatrizării(16).
3. Noi agenţi farmacologic activi în glaucom
În prezent, în glaucom se studiază, atât în studii clinice, cât şi în unele experimentale, o varietate mare de substanţe, cu mecanisme de acţiune diferite(33):
-
inhibitori ai kinazelor (ROCK, JNK, DLK, protein-kinaza C, tirozin-kinaza, miozin-kinaza);
-
latrunculina;
-
agonişti ai receptorilor pentru adenozină;
-
agonişti duali ai receptorilor pentru prostanoizii EP3 şi FP (sepetaprost);
-
agenţi serotoninergici.
3.1. Inhibitorii de Rho-kinază
Familia de Rho-kinaze (A, B şi C) este reprezentată de proteine implicate în reglarea semnalului căii de transducţie şi în funcţiile citoscheletului. Rho-kinazele sunt activate de guanidin trifosfataze, care, ulterior, activează moleculele ROCK1 şi ROCK2, exprimate în reţeaua trabeculară umană, celulele musculare ciliare şi în nervul optic, fiecare cu roluri distincte(5,24).
În timp ce pilocarpina (colinomimetic, cu acţiune la nivelul receptorilor muscarinici M3) diminuează presiunea intraoculară, prin contracţia celulelor musculare ciliare, inhibitorii de Rho-kinază intervin în scăderea acesteia prin relaxarea musculaturii, slăbirea legăturilor intracelulare din matricea extracelulară şi lărgirea reţelei trabeculare(21). Pe lângă scăderea presiunii intraoculare, inhibitorii de ROCK protejează celulele din reţeaua trabeculară, prin reducerea expresiei interleukinelor IL-6 şi IL-8 implicate în stresul oxidativ; îmbunătăţesc vascularizaţia nervului optic, cu rol important în glaucomul cu tensiune normală; facilitează vindecarea endoteliului cornean; protejează celule retiniene ganglionare de neurotoxicitatea glutamatului şi N-metil-D-aspartatului; scad nivelul fibrozei postoperatorii(21).
Descoperirea inhibitorilor de Rho-kinază ca o clasă de medicamente pentru scăderea presiunii intraoculare la pacienţii cu glaucom şi hipertensiune intraoculară reprezintă un triumf în cercetarea translaţională. Inhibitorii de Rho-kinază sunt eficace singuri sau combinaţi cu alte medicamente clasice în tratamentul glaucomului. Acestea oferă, de asemenea, posibilitatea unei activităţi neuroprotectoare, un impact favorabil asupra fluxului sangvin ocular şi chiar un efect antifibrotic, care poate fi util în chirurgia convenţională a glaucomului. Reacţiile adverse locale, inclusiv hiperemia conjunctivală, hemoragiile subconjunctivale şi cornea verticillata sunt frecvente. Dezvoltarea inhibitorilor de Rho-kinază cu acţiune ţintită asupra celulelor de la nivelul căilor de evacuare şi al retinei reprezintă o direcţie cu un mare impact clinic în tratamentul medical şi chirurgical al glaucomului. Doi noi agenţi hipotensivi oculari au fost aprobaţi pentru utilizare clinică: ripasudil în Japonia şi netarsudil în SUA(33).
Din 2018 este disponibil pe piaţă medicamentul netarsudil (cunoscut drept compusul AR-13503), un inhibitor ROCK cu activitate de blocare a transportului noradrenalinei(13,15).
Ripasudil (codificat K-115) este un alt inhibitor de Rho-kinază aflat în studii clinice la pacienţi cu glaucom. În studiile de fază I s-a pus în evidenţă faptul că ripasudil produce scăderea presiunii intraoculare atât în administrare unică, cât şi în utilizare pe termen lung sub formă de instilaţii, în concentraţie de 0,4% sau 0,8%, cu efect maxim la două ore după instilare. Studii de fază II, care au evaluat doza minimă necesară pentru scăderea presiunii intraoculare la pacienţii cu glaucom în unghi deschis, au relevat faptul că 0,4% reprezintă doza optimă pentru controlul presiunii intraoculare în administrare topică, de două ori pe zi(32).
Alţi inhibitori de Rho-kinază (de exemplu: AR-12286, AR-13324, SNJ-1656) se află, de asemenea, în studii clinice controlate la pacienţi cu glaucom(33).
3.2. Latrunculina
Latrunculinele reprezintă o familie de produse naturale şi toxine produse de anumiţi bureţi, din genurile Latrunculia şi Negombata, de unde derivă numele. Se leagă de monomerii de actină în apropierea fantei de legare a nucleotidelor, acţionând asupra reţelei trabeculare prin inhibarea polimerizării actinei şi sechestrarea monomerilor acesteia, ceea ce duce la intensificarea evacuării umorii apoase. În studiile experimentale efectuate pe maimuţe, latrunculina B favorizează eliminarea la nivel trabecular, prin acţiune asupra citoscheletului de actină(26).
Studii clinice de fază I au relevat faptul că administrarea de colir cu latrunculină B în două prize zilnice a scăzut semnificativ presiunea intraoculară, la pacienţi cu hipertensiune oculară sau cu glaucom primar cu unghi deschis în fază precoce(12,26).
3.3. Agoniştii receptorilor adenozinici
Adenozina este un aminoacid care modulează procesele fiziologice şi fiziopatologice prin activarea proteinei G, în urma cuplării cu receptorii de adenozină (A1, A2a, A2b, A3), care sunt exprimaţi în întreg organismul, inclusiv în ochi(18). Au fost obţinuţi agenţi farmacologici activi care mimează acţiunea adenozinei sau agonişti ai receptorilor pentru adenozină pentru a fi utilizaţi în tratamentul glaucomului, datorită activităţii lor la nivelul căii de eliminare a umorii apoase.
Activarea receptorului adenozinic A1 de către agonişti precum N6-ciclohexiladenozina reduce presiunea intraoculară prin facilitarea eliminării umorii apoase, care se asociază cu eliberarea crescută a proteazei specifice pentru metaloproteinaza matriceală 2, care participă la remodelarea reţelei trabeculare prin digerarea proteinelor matricei extracelulare(9). Din păcate, penetrarea scăzută a corneei de către N6-ciclohexiladenozină în preparatele topice limitează mult utilitatea sa clinică(18). Trabodenozonul a fost sintetizat ca un nou agent cu specificitate mare pentru receptorul adenozinic A1, cu o bună capacitate de penetrare a corneei. Acesta scade eficient presiunea intraoculară la mai multe specii de animale, inclusiv la oameni(22,34).
CF101 este în prezent unul dintre puţinele medicamente cu administrare orală folosit în terapia glaucomului, în studii de fază II dovedind eficacitate şi toleranţă, cu un efect antiinflamator la nivelul corneei când este administrat în doză de 1 mg de două ori pe zi(11).
3.4. Steroizii angiostatici
Steroizii angiostatici au fost, de asemenea, testaţi ca posibili agenţi farmacologici care scad presiunea intraoculară în diferite tipuri de glaucom. Unul dintre compuşii studiaţi este anecortave acetat, o moleculă sintetică derivată din cortizol, la care gruparea hidroxil 11-b este înlocuită cu o dublă legătură între atomii de carbon 9 şi 11 şi se adaugă o grupare acetat la carbonul 21. Aceste modificări structurale fac ca acest compus să fie lipsit de acţiuni glucocorticoide şi mineralocorticoide(27).
Anecortave acetat are o activitate antiangiogenică prin inhibarea proteazelor care mediază migrarea celulelor endoteliale vasculare şi a fost evaluat ca terapie potenţială pentru degenerarea maculară neovasculară legată de vârstă. La pacienţii diabetici cu glaucom neovascular, respectiv la pacienţii cu hipertensiune oculară postterapie locală intravitreală cu corticosteroizi, a fost demonstrat faptul că reduce neovascularizaţia din segmentul anterior al ochiului, producând totodată o scădere remarcabilă şi de durată a presiunii intraoculare(25).
3.5. Agonistul dual al receptorilor prostanoizi EP3 şi FP
Sepetaprost (codificat ONO-9054) este un nou agonist dual al receptorilor prostanoizi EP3 şi FP care reduce presiunea intraoculară în principal prin creşterea eliminării umorii apoase, prin acţiune directă la nivelul căii patogenice uveosclerale(31).
În prezent se află în studii clinice la pacienţi cu hipertensiune oculară şi la cei cu glaucom în unghi deschis, pentru evaluarea eficacităţii terapeutice în comparaţie cu medicamentul clasic, latanoprost, un analog de prostaglandină F2a şi agonist selectiv al receptorului prostaglandinei F(10). Investigaţiile au evidenţiat că medicamentele testate prezintă eficacitate similară în ceea ce priveşte scăderea presiunii intraoculare în cursul dimineţii, cu efecte mult mai intense şi mai durabile pe parcursul unei zile observate pentru sepetaprost(1).
3.6. Agenţi serotoninergici
Serotonina (5-hidroxitriptamina; 5HT) este un neurotransmiţător endogen major al sistemului nervos central la mamifere, a cărei prezenţă a fost detectată şi în umoarea apoasă şi corpul ciliar al subiecţilor umani. Mai mult, s-a dovedit că nervii serotoninergici inervează diferite ţesuturi oculare, inclusiv corpul ciliar, ceea ce sugerează faptul că receptorii serotoninergici pot juca un rol important în medierea dinamicii umorii apoase şi deci în modularea presiunii intraoculare(3).
Studii experimentale au relevat faptul că AL-34662, un agonist selectiv al receptorilor serotoninergici 5HT2A, 5HT2B şi 5HT2C, reduce în mod eficient presiunea intraoculară, într-un model experimental de glaucom la maimuţe(29). Pe de altă parte, s-a pus în evidenţă faptul că ketanserina şi sarpogrelatul, antagonişti potenţi ai receptorilor alfa 1 adrenergici şi serotoninergici 5HT2, au demonstrat activitate hipotensivă oculară la pacienţii cu glaucom(34).
4. Terapia genică în glaucom
Majoritatea tipurilor de glaucom sunt induse de o disfuncţie a reţelei trabeculare, ceea ce duce la rezistenţa la scurgere a umorii apoase şi la creşterea presiunii intraoculare, cu deteriorarea celulelor nervoase retiniene. Noile terapii sunt individualizate şi au ca scop împiedicarea degradării celulelor nervoase şi protejarea acestora, precum şi modificarea reţelei trabeculare pentru scăderea presiunii intraoculare(30).
Terapia genică, pe lângă frecvenţa scăzută de administrare şi eficacitatea sporită, are avantajul de a acţiona direct asupra materialului genetic al celulelor din reţeaua trabeculară. Pentru aceasta sunt folosite virusurile, care sunt purtători ai materialului genetic şi au proprietatea de a intra în celulă şi de a o modifica. Cu ajutorul biologiei moleculare şi al tehnicilor de recombinare a ADN-ului, un virus poate fi modificat astfel încât să şteargă orice secvenţă dorită din materialul genetic al celulei şi să o înlocuiască apoi cu o altă secvenţă în celula-ţintă(2).
În glaucom, terapia genică acţionează asupra structurilor cu rol important în această patologie: reţeaua trabeculară, epiteliul ciliar, muşchiul ciliar, celulele retiniene ganglionare şi celulele Müller. Virusurile folosite sunt: adenovirusuri, virusul herpes simplex, lentivirusurile, virusul imunodeficienţei umane(2,8).
5. Terapia cu celule stem
Proprietăţile celulelor stem (capacitatea de reînnoire şi de a se diferenţia pe multiple linii celulare) fac posibilă folosirea lor în tratamentul bolilor degenerative, inclusiv cele oculare, care duc la orbire. Astfel, injecţiile intravitreale de celule stem au un efect neuroprotector prin diferenţiere în celule neuronale, secreţia factorilor neurotrofici şi a citokinelor antiinflamatorii, eficacitatea acestora fiind comparabilă cu cea a terapiei genice(7,35).
Bibliografie
- Berlin MS, Rowe-Rendleman C, Ahmed I et al. EP3/FP dual receptor agonist ONO-9054 administered morning or evening to patients with open-angle glaucoma or ocular hypertension: results of a randomised crossover study.
- Br J Ophthalmol 2016; 100: 843-7.
- Borrás T. The pathway from genes to gene therapy in glaucoma: a review of possibilities for using genes as glaucoma drugs. Asia Pac J Ophthalmol 2017; 6(1): 80-93.
- Carta F, Supuran CT, Scozzafava A: Novel therapies for glaucoma: a patent review 2007-2011. Expert Opin Ther Pat 2012; 22: 79-88.
- Chen G, Li W, Tzekov R et al. Bevacizumab versus ranibizumab for neovascular age-related macular degeneration: a meta-analysis of randomized controlled trials. Retina 2015; 35(2): 187-93.
- Cholkar K, Trinh HM, Pal D et al. Discovery of novel inhibitors for the treatment of glaucoma. Expert Opin Drug Discov 2015; 10(3): 293-313.
- Conlon R, Saheb H, Ahmed II. Glaucoma treatment trends: a review.
- Can J Ophthalmol 2017; 52(1): 114-124.
- Daliri K, Ljubimov AV, Hekmatimoghaddam S. Glaucoma, stem cells, and gene therapy: where are we now? Int J Stem Cells 2017; 10(2): 119-128.
- Demetriades AM. Gene therapy for glaucoma. Curr Opin Ophthalmol 2011; 22(2): 73-7.
- Dismuke WM, Overby DR, Civan MM et al. The value of mouse models for glaucoma drug discovery. J Ocul Pharmacol Ther 2016; 32: 486-487.
- Ellis EM, Berlin MS, Ward CL et al. Ocular hypotensive effect of the novel EP3/FP agonist ONO-9054 versus Xalatan: results of a 28-day, double-masked, randomised study. Br J Ophthalmol 2017; 101: 796-800.
- Fishman P, Cohen S, Bar-Yehuda S. Targeting the A3 adenosine receptor for glaucoma treatment (review). Mol Med Rep 2013; 7(6): 1723-5.
- Harasymowycz P, Birt C, Gooi P et al. Medical management of glaucoma in the 21st century from a Canadian perspective. J Ophthalmol 2016; Article ID 6509809: 1-22.
- Hoy SM. Netarsudil ophthalmic solution 002%: first global approval. Drugs 2018; 78(3): 389-96.
- Katsanos A, Gorgoli K, Mikropoulos DG et al. Assessing the role of ranibizumab in improving the outcome of glaucoma filtering surgery and neovascular glaucoma. Expert Opin Biol Ther 2018; 18(6): 719-724.
- Kazemi A, McLaren JW, Kopczynski CC et al. Effects of netarsudil ophthalmic solution on aqueous humor dynamics in a randomized study in humans. J Ocul Pharmacol Ther 2018; 34(5): 380-6.
- Kodjikian L, Decullier E, Souied EH et al. Bevacizumab and ranibizumab for neovascular age-related macular degeneration: an updated meta-analysis of randomised clinical trials. Graefes Arch Clin Exp Ophthalmol 2015; 252(10): 1529-37.
- Krishnankutty SV, Rajan S. The effect of intravenous conivaptan on intraocular pressure. J Ophthalmic Vis Res 2016; 11(1): 126-7.
- Li G, Torrejon KY, Unser AM et al. Trabodenoson, an adenosine mimetic with A1 receptor selectivity lowers intraocular pressure by increasing conventional outflow facility in mice. Invest Ophthalmol Vis Sci 2018; 59(1): 383-392.
- Lusthaus J, Goldberg I. Current management of glaucoma. Med J Aust 2019; 210(4): 180-187.
- Mantravadi AV, Vadhar N. Glaucoma. Prim Care 2015; 42(3): 437-49.
- Moshirfar M, Parker L, Birdsong OC et al. Use of Rho kinase inhibitors in ophthalmology: a review of the literature. Med Hypothesis Discov Innov Ophthalmol 2018; 7(3): 101-111.
- Myers J, Sall K, DuBiner H et al. A randomized, phase II study of trabodenoson (INO-8875) in adults with ocular hypertension (OHT) or primary open-angle glaucoma (POAG). Ophthalmic Res 2017; 57: 201-207.
- Narayen G, Mandal SN. Vasopressin receptor antagonists and their role in clinical medicine. Indian J Endocrinol Metab 2012; 16(2): 183-91.
- Okumura N, Nakao S, Inoue T et al. Rho kinase in eye disease. J Ophthalmol 2017; 2017: 9281745.
- Prata TS, Tavares IM, Mello PA et al. Hypotensive effect of juxtascleral administration of anecortave acetate in different types of glaucoma.
- J Glaucoma 2010; 19(7): 488-92.
- Rasmussen CA, Kaufman PL, Ritch R et al. Latrunculin B reduces intraocular pressure in human ocular hypertension and primary open-angle glaucoma. Transl Vis Sci Technol 2014; 3(5): 1.
- Robin AL, Suan EP, Sjaarda RN et al. Alcon Anecortave Acetate for IOP Research Team: Reduction of intraocular pressure with anecortave acetate in eyes with ocular steroid injection-related glaucoma. Arch Ophthalmol 2009; 127: 173-178.
- Robina AL, Muir KW. Medication adherence in patients with ocular hypertension or glaucoma. Expert Rev Ophtalmol 2019; 1-12.
- Sharif NA. Serotonin-2 receptor agonists as novel ocular hypotensive agents and their cellular and molecular mechanisms of action. Curr Drug Targets 2010; 11(8): 978-93.
- Solinís MÁ, del Pozo-Rodríguez A, Apaolaza PS et al. Treatment of ocular disorders by gene therapy. Eur J Pharm Biopharm 2015; 95(Pt B): 331-42.
- Suto F, Rowe-Rendleman CL, Ouchi T et al. A novel dual agonist of EP3 and FP receptors for OAG and OHT: safety, pharmacokinetics and pharmacodynamics of ONO-9054 in healthy volunteers. Invest Ophthalmol Vis Sci 2015; 56: 7963-70.
- Tanihara H, Inoue T, Yamamoto T et al. One-year clinical evaluation of 04% ripasudil (K-115) in patients with open-angle glaucoma and ocular hypertension. Acta Ophthalmol 2016; 94(1): e26-34.
- Tanna AP, Johnson M. Rho kinase inhibitors as a novel treatment for glaucoma and ocular hypertension. Ophthalmology 2018; 125(11): 1741-1756.
- Vicente A, Prud’homme S, Ferreira J et al. Open-angle glaucoma: drug development pipeline during the last 20 years (1995-2015). Ophthalmic Res 2017; 57(4): 201-207.
- Zhu W, Gramlich OW, Laboissonniere L et al. Transplantation of iPSC-derived TM cells rescues glaucoma phenotypes in vivo. Proc Natl Acad Sci USA 2016; 113: E3492-E3500.
Articole din ediţiile anterioare
Imunoterapia în bolile neoplazice
Tumorile maligne apar când celulele neoplazice scapă de sub supravegherea sistemului imunitar.
Terapia imunosupresivă după transplantul de organ solid
Transplantul de organe solide este adesea salvator de viaţă. Transplantarea unei grefe diferite genetic de organismul transplantatului determină ră...
Imunoterapeutice
Una dintre ariile terapeutice cu cea mai spectaculoasă dezvoltare în ultimii ani este cea a medicamentelor care îşi exercită efectele terapeutice p...
Glaucomul – tipuri, simptome şi tratament
Glaucomul este considerat, la nivel mondial, cea de-a doua cauză de orbire, după cataractă. Cauza principală este creşterea presiunii intraoculare,...