Increased incidence of diuretic resistance may be caused by: patient noncompliance, incorrect diagnosis, pharmacokinetic and pharmacodynamic properties of the diuretic, renal and extrarenal disease. The mechanisms of diuretic resistance can be determined by changes in pharmacokinetics and pharmacodynamics of the drugs; pathological disorders in cardiovascular, renal, hepatic diseases, by and drug interactions. Diuretic resistance can be overcome by basic measures (reducing sodium intake; suspending the drugs that reduce the efficiency of diuretics; establishing effective dosage; increasing dosage of diuretics; adjusting diuretic administration regimen; substituting or using an alternative loop diuretic; intravenous administration of diuretic; continuous infusion of diuretic; combined therapy with other classes of diuretics) and alternatives (use of hypertonic saline solutions; use of positive inotropic drugs; management of intra-abdominal pressure; albumin infusion; administration of type 2 receptor antagonists of vasopressin, glucocorticoids, calcium sensitizers, vasodilators; use of ultrafiltration).
Mecanismele şi managementul rezistenţei la diuretice
Mechanisms and management of diuretic resistance
First published: 21 noiembrie 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/FARM.191.6.2019.2692
Abstract
Rezumat
Creşterea incidenţei rezistenţei la diuretice poate fi cauzată de: necomplianţa pacientului, diagnosticul incorect, proprietăţile farmacocinetice şi farmacodinamice ale diureticului, patologia renală şi extrarenală. Mecanismele rezistenţei la diuretice pot fi determinate de modificările farmacocineticii şi farmacodinamicii preparatelor, de dereglările patologice în maladiile cardiovasculare, renale sau hepatice şi de interacţiunile medicamentoase. Rezistenţa la diuretice poate fi depăşită prin măsuri de bază (reducerea aportului de sodiu; suspendarea preparatelor care reduc eficacitatea diureticelor; stabilirea dozei eficiente; creşterea dozelor de diuretic; ajustarea regimului de administrare a diureticelor; substituirea sau utilizarea unui diuretic de ansă alternativ; administrarea intravenoasă a diureticului; perfuzia continuă a diureticului; terapia combinată cu alte clase de diuretice) şi alternative (utilizarea soluţiei saline hipertone; folosirea preparatelor inotrop pozitive; managementul presiunii intraabdominale; infuzia de albumină; administrarea antagoniştilor receptorilor de tip 2 ai vasopresinei, glucocorticoizilor, sensitizatorilor calciului, vasodilatatoarelor; efectuarea ultrafiltraţiei).
Rezistenţa la diuretice este în creştere permanentă la pacienţii cu patologie cardiacă, hepatică sau renală. Prin rezistenţă la diuretice (cel mai frecvent se asociază cu rezistenţa la diureticele de ansă) se subînţelege o diminuare şi/sau absenţa efectului la doze adecvate de diuretic. Se mai estimează că prin rezistenţă se consideră eşecul de a reduce volumul de lichid extracelular la doze adecvate de diuretic(5,11,14).
O apreciere mai amplă a rezistenţei la diuretice s-a definit în baza următoarelor criterii: modificarea greutăţii corporale de la 0 la 2,7 kg la 40 mg de furosemid, un volum al urinei sub 1400 ml; excreţie urinară de sodiu sub 0,2% de la nivelul iniţial; o concentraţie urinară de sodiu şi nivel de furosemid sub 2 mmol/mg; niveluri urinare de clor la nivelul de bază (97 până la 103 mEq/l). Aceste criterii, definite pentru furosemid, pot fi valabile şi pentru alte diuretice de ansă la doze echivalente la administrarea intravenoasă, după cum urmează: 40 mg furosemid, 20 mg torasemid şi 1 mg bumetanid. Rezistenţa la diuretice, definită prin aceste criterii, poate fi completată de un şir de parametri în anumite patologii. Astfel, în insuficienţa cardiacă cronică (ICC), rezistenţa poate fi determinată de reducerea tensiunii arteriale (TA) şi a azotului, ureei, insuficienţă cardiacă de origine ischemică, diabet zaharat (DZ) etc.(5)
Rezistenţa la diuretice poate fi determinată de mai mulţi factori:
-
diagnostic incorect – edem venos şi/sau limfatic; suprasolicitarea spaţiului intracelular cu micşorarea celui intravascular;
-
noncomplianţa pacientului – nerespectarea restricţiei la sodiu şi/sau volumul de lichide; încălcarea regimului de administrare a diureticului (evitarea utilizării, reducerea dozelor sau frecvenţei administrării etc.);
-
proprietăţile farmacocinetice – diminuarea absorbţiei (edemul mucoasei intestinale, staza în circuitul mare etc.); reducerea secreţiei tubulare; concurenţa pentru secreţia tubulară cu alte substanţe endo- sau exogene (antiinflamatoare nesteroidiene, probenecid, toxine uremice etc.); modificarea metabolismului etc.;
-
proprietăţile farmacodinamice – reducerea concentraţiei diureticului la locul de acţiune; disconcordanţa dintre durata de acţiune şi regimul de dozare; doze neadecvate la trecerea de la administrarea intravenoasă la cea internă etc.;
-
patologia renală – reducerea fluxului renal şi a filtraţiei glomerulare; micşorarea masei funcţionale a rinichilor; sindrom nefrotic; activarea sistemului renină-angiotensină-aldosteron (SRAA) şi a celui simpatic; remodelarea nefronului (hiperplazia şi hipertrofia celulelor tubilor distali); creşterea aportului şi absorbţiei sodiului în tubii distali;
-
patologiile extrarenale – insuficienţa cardiacă; ciroza hepatică; hipoalbuminemia; hipotensiunea arterială; DZ etc.(5,8,14,16)
Mecanismele rezistenţei la diuretice
Rezistenţa la diuretice poate fi explicată prin mai multe mecanisme care survin în urma: modificărilor farmacocineticii şi farmacodinamicii; dereglărilor patologice în maladiile cardiovasculare, renale, hepatice etc.; interacţiunilor medicamentoase etc.(1,3,4,5,6,14)
Modificările farmacocinetice
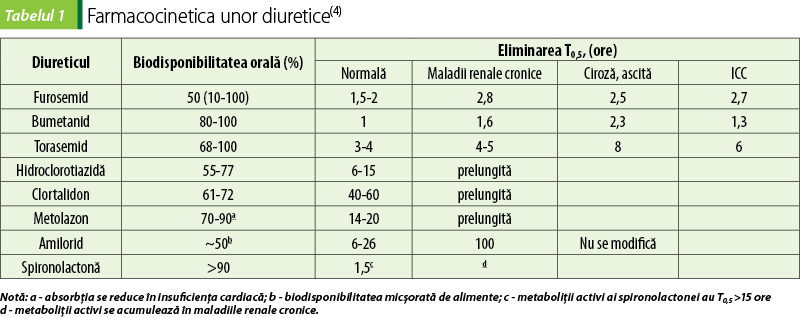
Pentru aprecierea mecanismelor farmacocinetice ale rezistenţei la diuretice este necesară evaluarea parametrilor farmacocinetici: biodisponibilitatea (Bd), a volumul de distribuţie (Vd), timpul de înjumătăţire (T0,5) metabolizarea, inclusiv în stările patologice. Modificările unor parametri farmacocinetici ai diureticelor în maladiile renale, ciroza hepatică şi insuficienţa cardiacă, ilustrate în tabelul 1, vor influenţa absorbţia, distribuţia, metabolismul şi excreţia diureticelor. La administrarea internă, absorbţia diureticelor de ansă constituie pentru furosemid 40-60% (cu variaţii de la 10% la 100%), bumetanid 80-100%, iar torasemid 68-100% (figura 1A, tabelul 1). Biodisponibilitatea acestora poate fi redusă la pacienţii cu ICC, ciroză hepatică şi sindrom nefrotic din cauza diminuării circulaţiei la nivelul intestinului şi a edemului mucoasei. În aceste situaţii, biodisponibilitatea totală poate fi în limitele normale, dar concentraţiile plasmatice pot fi inferioare celor de prag pentru realizarea natriurezei (figura 1B). La pacienţii cu edeme, în comparaţie cu indivizii sănătoşi, sunt necesare concentraţii de prag mai mari pentru dezvoltarea efectului diuretic(4,11).
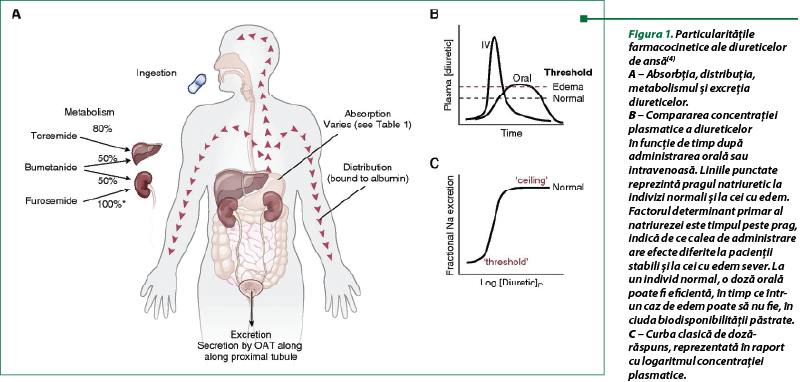
În sânge, diureticele de ansă se cuplează intens cu proteinele plasmatice (95%), iar proteinele pot îndeplini rolul de transportor spre locul de acţiune (rinichi); din aceste considerente, hipoalbuminemia, care deseori poate însoţi afecţiunile cardiovasculare, hepatice şi renale, poate diminua aportul diureticelor de ansă în tubii renali. Pot fi importante procesele de metabolizare şi eliminare a diureticelor de ansă. Astfel, furosemidul se elimină 50% sub formă neschimbată, iar restul, posibil, se supune glucuronizării, preponderent la nivelul rinichilor. Torasemidul se metabolizează predominant la nivelul ficatului, iar bumetanidul, proporţional, se supune metabolizării hepatice şi secreţiei renale (figura 1A). În insuficienţa renală, perioada de înjumătăţire T0,5 a furosemidului este prelungită ca urmare a micşorării secreţiei tubulare şi glucuronizării, în timp ce a torasemidului şi bumetanidului nu este modificată(4).
Diureticele, cu excepţia celor osmotice şi a antagoniştilor concurenţi ai aldosteronului (spironolactona, eplerenona), îşi exercită acţiunile prin legarea cu transportorii membranei apicale luminale. Din aceste considerente, diureticele de ansă, inhibitorii carboanhidrazei, tiazidele şi preparatele înrudite trebuie să fie secretate la nivelul tubilor proximali, preponderent segmentele S2 şi S3, deoarece nu se supun filtrării glomerulare din cauza cuplării intense cu proteinele plasmatice. Secreţia diureticelor din aceste grupe este asigurată de transportorii anionici organici (OAT1, OAT3) pe calea acizilor organici, iar a antagoniştilor neconcurenţi ai aldosteronului (amilorid, triamteren) pe calea bazelor organice. Activitatea transportorilor anionici poate fi inhibată de unele medicamente (antiinflamatoare nesteroidiene, antihipertensive, antibiotice, antivirale), acizi organici şi toxine endogene, care contribuie la dezvoltarea rezistenţei(3,4,11).
În maladiile renale cronice cu insuficienţă renală se poate dezvolta acidoza metabolică cu uremie care dereglează funcţiile tubilor proximali, cu reducerea secreţiei diureticelor şi instalarea rezistenţei. Administrarea în aceste cazuri a bazelor (hidrocarbonatul de sodiu) pentru corecţia acidozei poate ameliora secreţia diureticelor în tubii proximali(4).
Perioada de înjumătăţire determină frecvenţa administrării diureticelor. Astfel, tiazidele şi preparatele înrudite, antagoniştii neconcurenţi ai aldosteronului cu T0,5 mare se indică o dată/zi. Diureticele de ansă cu T0,5 mult mai mic şi o durată scurtă de acţiune a efectelor (bumetanid – 1 şi 2,5-3 ore, furosemid – 1,5-2 şi 3-4 ore, torasemid – 3-4 şi 6-8 ore, respectiv) la administrarea de 1-2 ori/zi pot determina o perioadă semnificativă de absenţă a diureticului la locul de acţiune, cu reabsorbţia sodiului şi dezvoltarea fenomenului de „revenire”(7).
Modificările farmacodinamice
Printre mecanismele farmacodinamice se pot enumera: reducerea disponibilului de diuretic la locul de acţiune; dezvoltarea mecanismelor contrareglatorii şi compensatorii; readaptarea compensatorie tubulară; dezvoltarea hipotensiunii arteriale, hipocloremiei, hiponatriemiei şi hipovolemiei; interacţiunile medicamentoase(1,5,7,8,11,15).
Reducerea disponibilului de diuretic la locul de acţiune (la pacienţii cu insuficienţă cardiacă sau ciroză hepatică) poate fi determinată de vasoconstricţia renală în urma micşorării debitului cardiac sau a vasodilataţiei splancnice(8).
Readaptarea compensatorie tubulară
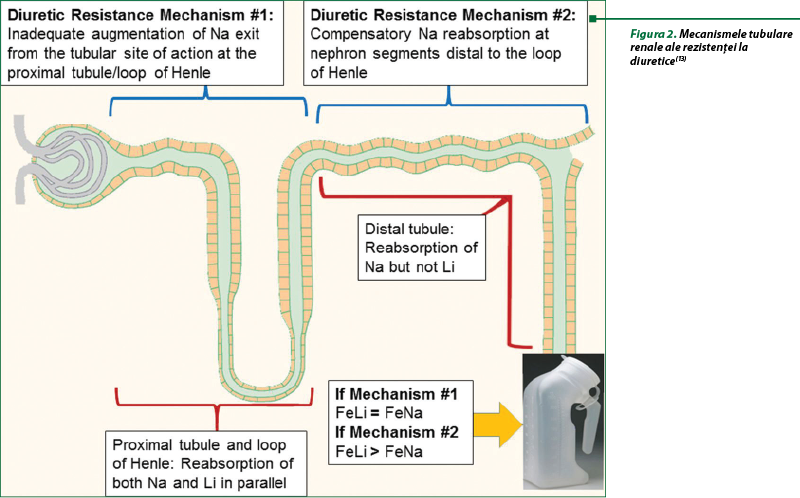
Din cauza activării SRAA, precum şi a fenomenului de frânare, creşte reabsorbţia de sodiu în tubii proximali. Utilizarea de durată a diureticelor de ansă contribuie la creşterea aportului de sodiu în tubii distali, cu hiperplazia şi hipertrofia compensatorie a acestora şi cu reabsorbţia mai accentuată a sodiului (figura 2). Acest mecanism de rezistenţă poate fi depăşit folosind un blocaj secvenţial al nefronilor cu diuretice tiazidice(5,13).
Interacţiunile medicamentoase. Unele medicamente, precum antiinflamatoarele nesteroidiene (AINS), pot reduce efectul diureticelor prin: scăderea sintezei prostaglandinelor (PGI2), cu diminuarea vasodilataţiei renale induse de furosemid; majorarea potenţialului vasoconstrictor al endotelinei; creşterea reabsorbţiei sodiului în alte zone ale nefronului; hipertensiunea arterială. Mai multe studii au demonstrat că acidul acetilsalicilic (nu numai în doze mari, dar şi în doze mici) poate inhiba venodilataţia, iar în urma administrării de furosemid, creşte necesitatea în diuretic. S-a constatat că antiinflamatorul nesteroidian, chiar şi în doze mici, poate neutraliza efectele favorabile ale inhibitorilor enzimei de conversie a angiotensinei, prin blocarea producţiei de prostaglandină şi îmbunătăţirea potenţialului vasoconstrictor al endotelinei(5).
Mecanismul care stă la baza unui răspuns slab la diureticele de ansă poate fi explicat prin modificări la nivelul tubului proximal (mecanismul nr. 1) sau tubului distal (mecanismul nr. 2). Reabsorbţia de litiu are loc în paralel cu sodiul în tubul proximal şi ansa Henle, dar este relativ necompletată cu reabsorbţia de sodiu în tubul distal. Astfel, prin determinarea modificărilor în excreţia de litiu, putem aprecia răspunsul tubului proximal şi al ansei Henle la diureticul de ansă, indiferent dacă sodiul este reabsorbit în tubul distal.
Activarea sistemelor contrareglatoare
Printre mecanismele probabile de rezistenţă la diuretice în maladiile cardiovasculare se menţionează activarea sistemelor de retenţie de sodiu ca răspuns contrareglator şi modificările farmacocineticii diureticelor de ansă. Pierderea de sodiu şi apă din cauza administrării diureticelor declanşează activarea SRAA, care contribuie la o reabsorbţie crescută de sodiu de-a lungul nefronului distal. Deoarece concentraţia plasmatică a medicamentului administrat oral scade în timpul zilei, aceste mecanisme compensatorii determină retenţia postdiuretică de sodiu, care implică toate segmentele tubulare. S-a demonstrat că această retenţie de sodiu este mai intensă când intervalele fără medicamente sunt mai lungi decât patru T0,5 ale diureticelor de ansă. Survin modificări de adaptare funcţională şi structurală la nivelul rinichilor, care constituie aşa-numitul „fenomen de frânare”, constând în reglarea proteinelor implicate în reabsorbţia renală a sodiului. Acesta este efectul adaptării la administrarea prelungită de diuretice de ansă, care implică o povară de sodiu urinară cronică crescută pe segmentele nefronului distal. Rezistenţa acută la utilizarea dozelor iniţiale de diuretice de ansă apare ca răspuns la epuizarea volumului şi este mediată de angiotensina II şi de sistemul nervos simpatic prin expresia şi activitatea crescută a transportatorilor de sodiu, inclusiv responsabil de schimbul de sodiu-hidrogen. La utilizarea de durată a furosemidului, datorită inhibării a Na+-K+-2Cl- la nivelul segmentului ascendent al ansei Henle, în segmentele tubilor distali se stimulează expresia şi activitatea cotransportorilor sensibili la tiazide (cotransportor de clorură de Na). S-au demonstrat o creştere a activităţii Na+K+-ATP-azei pe membrana bazolaterală, regruparea subunităţilor α, β şi γ ale canalului de sodiu epitelial, hipertrofia celulelor epiteliale, lărgirea lumenului tubular şi supraexpresia porinelor canalului de apă în celulele principale ale tubului distal, cu o localizare predominantă pe membrana apicală(1,2,5,6,11,14).
Un mecanism implicat în rezistenţa la diuretice s-ar reduce la reglarea compensatorie a transportorilor de sodiu care nu sunt blocaţi de diuretic. Se presupun mai multe mecanisme sistemice şi locale. Sistemul renină-angiotensină sistemic este activat în insuficienţa cardiacă şi ciroza hepatică şi devine activat şi prin tratament cu diuretice de ansă. La pacienţii cu insuficienţă cardiacă cronică, nivelurile plasmatice de aldosteron pot fi crescute chiar şi în prezenţa activităţii normale a reninei plasmatice şi la concentraţii plasmatice normale de potasiu. Concentraţiile plasmatice majorate ale angiotensinei II şi aldosteronului pot activa transportorii de sodiu în tubii distali. Angiotensina II stimulează reabsorbţia de sodiu în tubii proximali cu reducerea conţinutului de sodiu distal şi va contribui la instalarea rezistenţei. Se estimează că sistemul renină-angiotensină sistemic şi intrarenal poate funcţiona independent. În mai multe stări patologice, sistemul renină-angiotensină intrarenal poate fi activat, ceea ce duce la creşterea producţiei de angiotensină II în rinichi, care activează transportorii de sodiu prin receptorii apicali ai angiotensinei de tip I. S-a relatat că remodelarea nefronului şi semnalizarea paracrină (secreţie de α-cetoglutarat) sunt de asemenea implicate în răspunsul compensator la diuretice(8).
Studii recente au identificat legătura dintre hipocloremie şi rezistenţa la diuretice (figura 3). Detectarea de sodiu/clor este un proces‑cheie fiziologic pentru menţinerea homeostaziei lichidului şi implică atât sistemul nervos central, cât şi rinichii. În rinichi a fost identificată o familie de kinaze sensibile la cloruri, care reprezintă mecanismul molecular al detectării clorului. S-a estimat că hipocloremia este atât cauza, cât şi consecinţa transportului de sare şi apă demodulat de-a lungul tubului renal, ca răspuns la diferitele mecanisme patologice implicate în extinderea volumului şi manipularea tubulară a sării în maladiile cardiovasculare. S-a raportat o prevalenţă a hipocloremiei, care a depăşit-o pe cea a hiponatremiei, în special la pacienţii care necesită doze mai mari de diuretice de ansă. La aceşti pacienţi, excreţia de apă nu a fost modificată, ceea ce sugerează epuizarea, şi nu diluarea, ca principal mecanism de susţinere a diurezei. Administrarea internă a clorurii de lizină a îmbunătăţit răspunsul la diuretice şi a mai mulţi parametri cardio-renali. S-a estimat că hipocloremia este în principal un indicator al intensităţii tratamentului diuretic, precum şi un predictor independent al mortalităţii la pacienţii cu hipertensiune pulmonară. Astfel, o mai bună înţelegere a mecanismelor care stau la baza rezistenţei la diuretice va permite abordarea de noi strategii terapeutice bazate pe corecţia hipocloremiei(11).
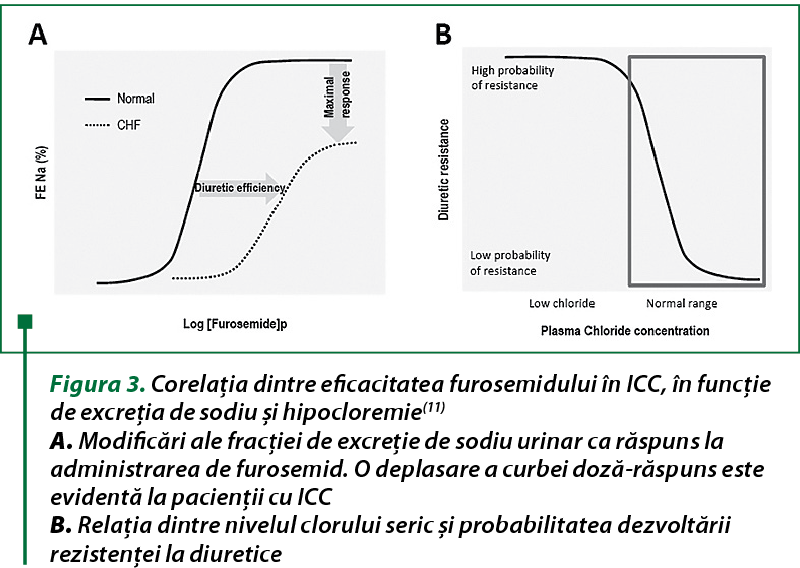
Diureticele de ansă au o curbă de doză-răspuns în formă de sigmoid cu cel mai mare efect de excreţie de sodiu urinar între doza minimă eficientă şi doza de plafon. Determinarea pragului renal şi a dozelor maxime eficiente de diuretice de ansă este o etapă crucială, deoarece orice creştere suplimentară a dozei peste valoarea maximă nu îmbunătăţeşte efectul diuretic. Maladiile cardiovasculare pot afecta farmacocinetica diureticelor de ansă şi au drept consecinţă o deplasare a curbei doză-răspuns în dreapta şi în jos (figura 3A)(11).
Strategii pentru depăşirea rezistenţei la diuretice
Rezistenţa la diuretice poate fi depăşită prin măsuri complexe bazate pe verigile patogenetice responsabile de rezistenţă şi se pot reduce la iniţiale şi alternative. Printre cele iniţiale (de bază) putem menţiona: reducerea aportului de sodiu; suspendarea preparatelor care reduc eficacitatea diureticelor; stabilirea dozei eficiente; creşterea dozelor de diuretic; ajustarea regimului de administrare a diureticelor; substituirea sau utilizarea unui diuretic de ansă alternativ; administrarea intravenoasă a diureticului; perfuzia continuă a diureticului; terapia combinată cu alte clase de diuretice. Măsurile alternative pot fi: utilizarea soluţiei saline hipertone; folosirea preparatelor inotrop pozitive; managementul presiunii intraabdominale; infuzia de albumină; administrarea antagoniştilor receptorilor de tip 2 ai vasopresinei, glucocorticoizilor, sensitizatorilor calciului, vasodilatatoarelor; efectuarea ultrafiltraţiei(1,5,7,8,11,14).
Reducerea aportului de sodiu
Restricţia dietetică de sodiu este un factor determinant al eficacităţii diuretice. Aceasta se bazează în principal pe presupunerea că restricţia dietetică a sării ajută la controlul supraîncărcării de lichide. Astfel, restricţionarea aportului de sodiu la mai puţin de 100 mmol sau mEq/zi ajută la obţinerea unei balanţe negative de sodiu. Restricţionarea de sodiu reduce la minimum retenţia de sodiu postdiuretică, ceea ce duce la un echilibru negativ de lichide şi sodiu. Dacă aportul dietetic de sodiu este ridicat, retenţia de sodiu postdiuretică compensează aproape în totalitate pierderea de sodiu indusă de diureticul de ansă. O excreţie de sodiu urinară în 24 de ore mai mare de 100 mmol sau mEq/zi sau o excreţie fracţională a valorii de sodiu peste 2% indică nerespectarea restricţiei de sodiu şi exclude adevărata rezistenţă la diuretice. Din aceste considerente, primul pas pentru combaterea rezistenţei la diuretice este de a asigura respectarea de către pacient a unei restricţii adecvate de sodiu(5,14).
Recent, această presupunere a fost pusă sub semnul întrebării ca urmare a faptului că o dietă foarte scăzută în sodiu este asociată cu un efect mai slab al tratamentului diuretic şi poate duce la hiponatremie şi hipocloremie, care ar putea fi ele însele responsabile pentru rezistenţa la diuretice. Totodată, o dietă cronică cu restricţie de sodiu poate duce la o infiltrare a cationului în matricea extracelulară şi în oase, cu osteoporoză(11).
Stabilirea dozei unice eficiente
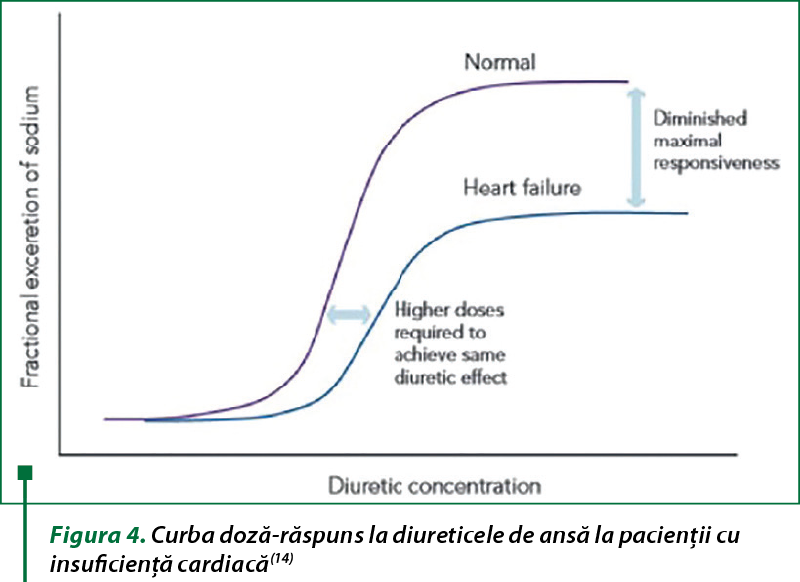
Diureticele de ansă au o curbă doză-răspuns, iar efectul începe numai după ce concentraţia de diuretic atinge un prag terapeutic în lumenul tubilor renali. La pacienţii cu insuficienţă cardiacă şi sindrom cardiorenal, curba doză-răspuns se modifică în jos şi spre dreapta (figura 4). În acest caz, bolnavii au nevoie de doze mai mari de diuretice de ansă pentru a atinge nivelul terapeutic la locul de acţiune. Dozele de diuretice sub pragul menţionat sunt ineficiente, deci este necesară o doză mare, mai eficientă, decât administrarea mai frecventă a unei doze inadecvate(14).
Ajustarea dozelor de diuretice şi a regimului de administrare
Deoarece majoritatea diureticelor de ansă au acţiune de scurtă durată, administrarea mai frecventă a diureticului (de 3 ori pe zi sau mai mult) va contribui la reducerea intervalului fără medicamente şi poate ajuta la depăşirea retenţiei postdiuretice de sodiu şi la restabilirea răspunsului diuretic. În funcţie de patologia cardiacă, hepatică sau renală, e necesar să fie luate în considerare modificările T0,5 ale diureticelor de ansă pentru selectarea adecvată a intervalului între prizele medicamentelor (tabelul 1)(14).
În funcţie de severitatea maladiilor cardiovasculare, hepatice sau renale, e necesar să fie ajustate doza diureticelor (de ansă, tiazidice, antagoniştii aldosteronului) şi frecvenţa de administrare (în funcţie de T0,5), pentru a menţine concentraţia plasmatică a diureticului la starea de echilibru şi pentru a reduce intervalele fără medicamente (esenţială pentru diureticele cu T0,5 scurt). În situaţiile când persistă retenţia excesivă de lichide, în pofida ajustărilor dietetice şi ale medicamentelor, medicul poate avea câteva opţiuni: să treacă de la terapia orală la administrarea intravenoasă a diureticului; să iniţieze terapia diuretică combinată; să asocieze la diureticele de ansă o infuzie cu soluţie salină hipertonă (în cazul hiponatremiei); să folosească antagoniştii vasopresinei (vaptanii) în cazul hiponatremiei de diluţie (retenţie excesivă de apă); să înceapă ultrafiltrarea, dacă terapia medicamentoasă nu reuşeşte să obţină o îmbunătăţire clinică(11).
Substituţia cu diureticul alternativ
Absorbţia gastrointestinală şi biodisponibilitatea diureticelor de ansă pot varia considerabil şi acest lucru ar putea fi un factor al unui răspuns slab (tabelul 1). Uneori, înlocuirea furosemidului cu doze comparabile de bumetanid sau torasemid poate fi suficientă pentru a creşte diureza şi a restabili eficacitatea(3,4,14).

Administrarea intravenoasă. Concentraţia maximă a diureticului şi la locul acţiunii în lumenul tubilor renali poate fi inadecvată, din cauza reducerii absorbţiei şi biodisponibilităţii în prezenţa edemului gastrointestinal, gastroparezei şi a golirii gastrice întârziate, a insuficienţei cardiace decompensate, hipoperfuziei renale sau a secreţiei afectate ca urmare a hipoalbuminemiei sau afecţiunilor renale. Trecerea la administrarea intravenoasă a diureticului poate îmbunătăţi diureza(5,14).
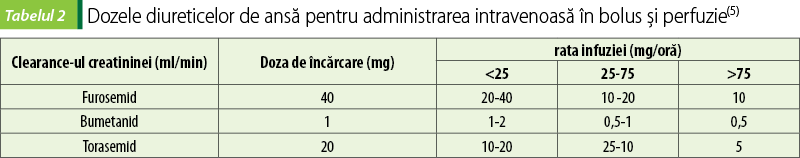
Un mecanism de rezistenţă la diuretice este absorbţia deficitară a diureticelor de ansă, fără o micşorare absolută a biodisponibilităţii care duce la întârzierea şi scăderea concentraţiilor maxime în urină. În această situaţie se poate recomanda creşterea moderată a dozei sau trecerea la administrarea intravenoasă. După câteva minute de la injectarea în bolus a furosemidului la pacienţii cu simptome de congestie de origine cardiovasculară, scade presiunea în artera pulmonară şi creşte capacitatea venoasă datorită efectului vasodilatator al diureticului. Preocuparea pentru injectarea rapidă intravenoasă a unui diuretic de ansă în doze mari este dezvoltarea ototoxicităţii, în special la pacienţii care primesc simultan alte medicamente ototoxice, cum ar fi aminoglicozidele. Pentru a evita această complicaţie, rata maximă recomandată de infuzie de furosemid este de 4 mg/min. Se recomandă să se infuzeze lent furosemidul când dozele sunt mai mari de 80 mg, pentru a se evita creşterea concentraţiei serice maxime. Infuzia continuă intravenoasă a unui diuretic de ansă se poate dovedi eficientă când alte strategii de gestionare a rezistenţei la diuretice au eşuat. S-a constatat că este o terapie sigură şi eficientă la pacienţii cu insuficienţă cardiacă refractari la doze mari, precum şi la terapia diuretică intravenoasă în bolus. În comparaţie cu dozele de bolus, infuzia continuă de diuretic poate fi mai eficientă, prin scădea fluctuaţiilor volumului intravascular, o diureză pe oră mai graduală şi relativ constantă, cu limitarea efectului retenţiei de sodiu postdiuretice. Unele studii au demonstrat că furosemidul, administrat sub formă de perfuzie continuă, a fost mai eficient decât dozele de bolus intermitente cu micşorarea dozelor de diuretic necesare pentru a produce aceeaşi diureză. Concomitent, nu s-au constatat diferenţe semnificative în efectele adverse şi modificarea creatininei. Conceptele farmacodinamice susţin eficacitatea superioară a perfuziei continue a diureticelor de ansă, cu excepţia acidului etacrinic. Se recomandă iniţial administrarea unei doze în bolus a unui diuretic de ansă cu o perfuzie continuă sau când rata de perfuzie este crescută pentru a reduce timpul de început al acţiunii medicamentului. Dozele diureticelor de ansă în bolus şi pentru perfuziile continue sunt redate în tabelul 2(5,11,14).
Terapia diuretică combinată
Terapia diuretică combinată constă dintr-o blocare secvenţială a absorbţiei de sodiu de-a lungul nefronului, pentru a preîntâmpina retenţia de sodiu în tubii renali. În mare parte, asocierea la diureticul de ansă depinde de particularităţile verigilor patogenetice implicate în maladiile cardiovasculare, hepatice, renale etc. În maladiile cardiovasculare cu congestie simptomatică de lichide, combinaţia de tiazide (bendrofluazidă sau metolazon) cu furosemid a arătat o ameliorare clinică mai bună faţă de monoterapie, dar şi faţă de diureticul de ansă. Creşterea activităţii SRAA argumentează asocierea antagoniştilor concurenţi (spironolactona, canrenona) şi neconcurenţi (amilorid) ai aldosteronului cu alte diuretice la pacienţii cu maladii cardiovasculare datorită blocării reabsorbţiei sodiului în tubii distali, diminuării sclerozei miocardului şi fibrozei peretelui arterial, cu reducerea mortalităţii. Concomitent, utilizarea combinaţiilor trebuie monitorizată, din cauza riscului mare de a dezvolta tulburări electrolitice (hiperkaliemie, hiponatriemie, hipocloremie) şi dereglări ale funcţiei renale(11).
Diureticele tiazidice şi înrudite în terapia combinată sunt benefice datorită duratei mai lungi de acţiune, care permite menţinerea diurezei după ce acţiunea diureticelor de ansă cu acţiune mai scurtă s-a terminat. Se consideră că aceste diuretice, în asociere cu diferite diuretice de ansă, manifestă efecte sinergice similare, deşi în unele studii metolazonul se consideră prioritar, posibil datorită inhibării funcţiei tubilor proximali. Metolazonul are absorbţie lentă şi variabilă la pacienţii cu edeme, astfel încât efectul maxim apare numai după câteva ore. Majoritatea studiilor au raportat beneficiile terapiei combinate la administrarea în acelaşi timp a ambelor diuretice. În terapia diuretică combinată, sunt necesar de reţinut următoarele: suplimentarea diureticelor tiazidice sau înrudite poate induce diureză la pacienţii refractari la doze masive de diuretic de ansă; combinarea diureticelor de ansă cu tiazidele poate fi eficientă la pacienţii cu boală renală cronică avansată; efectele sinergice ale diureticelor tiazidice asupra diurezei par a fi un efect de clasă observat la toate medicamentele; se poate dezvolta hipokalemia potenţial periculoasă, care necesită monitorizare riguroasă; se pot observa creşteri reversibile sau reduceri ale creatininei în ser; siguranţa şi efectele asupra morbidităţii şi mortalităţii nu sunt certe(6).
Pentru terapia combinată cu diureticele de ansă se recomandă diureticele tiazidice şi înrudite în doze echivalente şi maxime pe zi, acestea reieşind şi din durata lor de acţiune (tabelul 3).
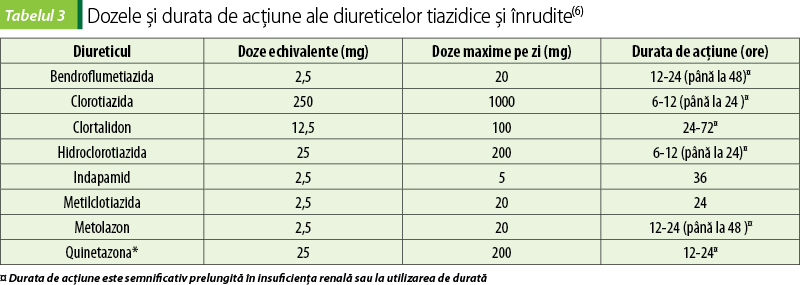
Beneficiile şi riscurile terapiei diuretice combinate sunt prezentate în tabelul 4.
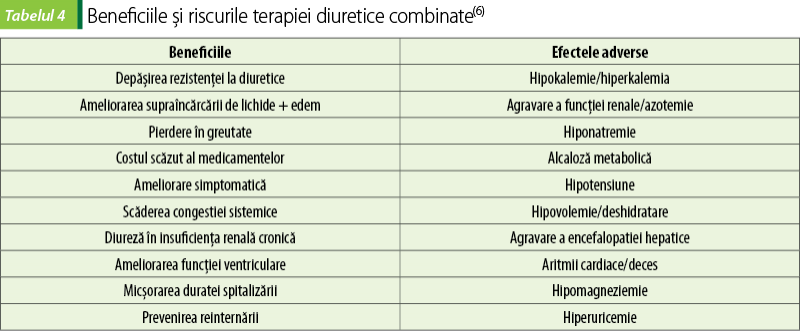
Efectele adverse ale terapiei diuretice combinate
Efectele adverse clinic manifestate ale terapiei diuretice combinate sunt frecvente, necesitând o monitorizare atentă a electroliţilor în ser şi a funcţiei renale. Hipokalemia este deosebit de frecventă, iar pierderile de potasiu din ser (0,4-0,8 mEq/l) sunt semnificative, în pofida suplimentării de potasiu şi/sau a utilizării diureticelor economisitoare de kaliu (spironolactonă etc.), care pot reduce, dar nu împiedică în totalitate pierderile. Pierderea de potasiu în urină şi hipokalemia rezultată tind să se coreleze cu excreţia totală de sodiu în urină şi concentraţia de sodiu în urina finală. Diureticele tiazidice produc o pierdere mai mare de potasiu în urină pe unitatea de excreţie de sodiu în urină decât cele de ansă, iar terapia combinată este în special predispusă la excreţia masivă de potasiu în urină, în special cu doze mai mari de diuretice de ansă. La pacienţii spitalizaţi predispuşi la hipokalemie, poate fi necesară o monitorizare de două ori pe zi a nivelului de potasiu, cu suplimentarea agresivă a deficitelor de potasiu. Hipokalemia este adesea asociată cu alcaloza metabolică hipocloremică datorată pierderilor de clor, care depăşesc de obicei pierderile de sodiu în urină. Hipomagneziemia se poate dezvolta concomitent şi poate agrava hipokalemia. Hipokalemia, cu sau fără hipomagneziemie, poate creşte riscul de aritmii cardiace şi de deces, în special la pacienţii care primesc digoxină sau antiaritmice. Hiponatremia poate surveni deoarece creşterea excreţiei de sodiu în urină este mai mare decât creşterea excreţiei de apă cu o urină hipertonă după terapia diuretică combinată comparativ cu diureticul de ansă singur. Hiponatremia este mai puţin frecventă decât hipokalemia şi a fost rareori simptomatică, dar poate fi un marker al rezultatelor adverse ale insuficienţei cardiace. Se poate constata o deshidratare în caz de volume mari de urină, caz în care va fi necesară suplimentarea de lichide. Se poate dezvolta o hipotensiune cu o reducere medie de 10/8 mm Hg a tensiunii arteriale(6).
Infuzia salină hipertonică la doze mari de diuretice de ansă
Rezistenţa la diuretice este determinată în mare parte de reabsorbţia de sodiu în tubii distali. Clorul pare să joace un rol major în mecanismele care declanşează recuperarea neurohormonală de sodiu. În consecinţă, posibilele consecinţe negative ale restricţiei sării au fost recent revizuite. Concomitent au fost raportate posibile efecte benefice ale administrării intravenoase a soluţiei saline hipertonice (1,4%) în asociere cu diureticele de ansă la pacienţii cu maladii cardiovasculare demonstrate prin creşterea debitului urinar şi a ratei excreţiei de sodiu, cu devierea curbei doză-răspuns la stânga. Prin urmare, eficacitatea suplimentării cu clor sau soluţie salină hipertonică pentru a depăşi rezistenţa la diuretice susţine rolul hipocloremiei/hiponatremiei în dezvoltarea rezistenţei. Mecanismele responsabile de eficacitatea soluţiei hipertone sunt determinate, posibil, de activarea cotransportatorului de sodiu-potasiu-2-clor, cu creşterea excreţiei de sodiu, şi de normalizarea/creşterea clorului extracelular şi intracelular, care ar inhiba canalele epiteliale de Na şi ar restabili excreţia de sodiu(11).
Antagoniştii vasopresinei (vaptanii) în managementul rezistenţei la diuretice
Producţia de vasopresină, influenţată de stimulii osmotici şi nonosmotici, de către celulele neurosecretorii ale hipotalamusului, joacă un rol principal în reglarea renală a apei şi a volumului de sânge. Stimularea nonosmotică de secreţie a vasopresinei în maladiile cardiovasculare duce la retenţia renală de apă, cu două consecinţe principale: creşterea preîncărcării cordului; hipoosmolalitate cu hiponatremie diluantă. Acestea din urmă predispun la aritmii severe şi decompensare acută a inimii. Pentru antagonizarea vasopresinei au fost elaboraţi antagoniştii ei, sub denumirea de vaptani. Tolvaptanul este un antagonist competitiv al receptorului V2 aprobat pentru corecţia hiponatremiei euvolemice şi hipervolemice la pacienţii cu maladii cardiovasculare, ciroză şi sindrom de secreţie inadecvată de hormon antidiuretic. Utilizarea tolvaptanului a fost asociată cu o îmbunătăţire persistentă şi semnificativă a nivelului seric de sodiu(11).
Managementul presiunii intraabdominale
Hipertensiunea intraabdominală este definită ca o presiune de 12 mmHg sau mai mare. Congestia splanhnică şi interstiţială poate provoca o presiune intraabdominală ridicată în absenţa ascitei în maladiile cardiovasculare decompensate. La astfel de pacienţi, o majorare a presiunii intraabdominale creşte presiunea venoasă renală, cu reducerea gradientului de perfuzie transrenală şi perfuzie renală. Presiunea intraabdominală ridicată determină, de asemenea, creşterea presiunii interstiţiale renale, care se opune presiunii nete de filtrare. Ambele contribuie la afectarea renală şi la rezistenţa la diuretice. Când terapia intravenoasă cu diuretice de ansă eşuează, măsurarea presiunii intraabdominale este o procedură ieftină şi minim invazivă, care exclude o cauză de rezistenţă la diuretic. Dacă presiunea intraabdominală este de peste 20 mmHg, se poate obţine o reducere a acesteia prin mobilizarea lichidului din spaţiul al treilea printr‑o combinaţie de diuretice, vasodilatatoare şi/sau inotrope. Scopul terapeutic este realizarea unei presiuni de perfuzie abdominală de peste 60 mmHg (cu o presiune intraabdominală de 5 până la 7 mmHg), ceea ce semnifică un rezultat favorabil (îmbunătăţirea perfuziei renale, a filtrării renale şi diurezei)(5).
Infuzie cu albumină
Infuzia simultană de diuretic şi albumină ar putea îmbunătăţi uşor rezistenţa la diuretice. Analiza studiilor clinice randomizate la adulţi cu hipoalbuminemie a constatat efecte tranzitorii cu o semnificaţie clinică modestă la administrarea concomitentă a diureticelor de ansă şi a albuminei versus diuretice de ansă. Această intervenţie trebuie luată în considerare doar la pacienţii cu hipoalbuminemie severă când abordările terapeutice au eşuat(5).
Dopamina în doză renală
Dozele mici de dopamină (<3 µg/kg/min) stimulează receptorii dopaminergici periferici, cu vasodilataţie renală, coronariană, splanhnică şi cerebrală. Eficacitatea reală a dopaminei se va constata la pacienţii cu maladii cardiovasculare acute şi cu hipotensiune arterială(5).
Alte abordări
Rezistenţa diuretică este foarte frecventă în ICC. Glucocorticoizii au fost folosiţi pentru a gestiona rezistenţa diuretică înainte de apariţia diureticelor de ansă. Mai multe dovezi recente confirmă faptul că glucocorticoizii pot ajuta şi la depăşirea rezistenţei la diureticele de ansă. Suplimentarea prednisonului (1 mg/kg pe zi, doză maximă de 60 mg/zi) la tratamentul standard a dublat volumul zilnic de urină, a ameliorat simptomele ICC şi a redus nivelul creatininei. La nivelul rinichilor, glucocorticoizii cresc sensibilitatea renală la peptida natriuretică atrială prin creşterea densităţii receptorului A din stratul medular al tubului colector renal. Utilizarea pe termen scurt a glucocorticoizilor la terapia convenţională poate potenţa reactivitatea renală la terapia diuretică în cazul pacienţilor cu insuficienţă cardiacă. Administrarea de scurtă durată a glucocorticoizilor cu acţiune mineralocorticoidă minimă la pacienţii cu insuficienţă cardiacă, pentru tratamentul altor afecţiuni comorbide acute (gută acută), este sigură şi poate fi chiar avantajoasă(9,10).
Creşterea necontrolată a utilizării diureticelor de ansă poate afecta funcţia renală din cauza hipotensiunii arteriale şi hipovolemiei, precum şi creşte riscul de complicaţii tromboembolice şi de moarte subită cardiacă. La pacienţii cu insuficienţă cardiacă decompensată, care, alături de edemele periferice, prezintă acumulări de lichide în cavităţile seroase, se poate dezvolta rezistenţa la diuretice. Rezistenţa la diuretice poate fi falsă sau adevărată.
Rezistenţa falsă se poate constata în caz de: administrare a diureticului concomitent cu masa (alimentele reduc absorbţia furosemidului); dereglare a funcţiilor rinichilor cu proteinurie (albuminele cuplează furosemidul în tubii renali proximali şi micşorează disponibilul de preparat liber la nivelul membranei apicale a ansei Henle); tromboze ale venelor renale cu reducerea microcirculaţiei şi a diurezei; administrare de medicamente care pot antagoniza efectele diureticelor (antiinflamatoarele nesteroidiene reduc sinteza prostaglandinelor, necesare pentru acţiunea vasodilatatoare a diureticelor de ansă la nivel renal, cu redistribuirea fluxului sangvin); administrare a preparatelor care concurează cu secreţia în tubii proximali a diureticelor (probenecid etc.); diminuarea funcţiei contractile a miocardului, inclusiv prin medicamente inotrop negative. Rezistenţa în aceste cazuri poate fi depăşită prin: administrarea furosemidului cu cel puţin 40 de minute înainte de micul dejun; utilizarea de torasemid sau bumetanid, care se cuplează slab cu proteinele; evitarea folosirii concomitente a diureticelor de ansă cu antiinflamatoarele nesteroidiene, probenecidul şi preparatele inotrop negative (beta-adrenoblocante, blocantele canalelor de calciu etc.); ameliorarea funcţiei contractile a miocardului prin medicamente inotrop pozitive (dopamină, dobutamină, glicozide cardiace etc.)(15).
Rezistenţa adevărată la diuretice poate fi precoce sau tardivă. Rezistenţa precoce (fenomenul de ricoşet) se dezvoltă în primele ore sau zile după iniţierea terapiei cu diuretice în doze mari cu dezvoltarea rapidă a deshidratării şi hipovolemiei, prin creşterea activităţii neurohormonilor (aldosteronului etc.). În acest caz, are loc o retenţie de sodiu „ricoşet”, care vizează restabilirea homeostazei apoase a organismului. În primul rând, aceasta se referă la furosemid, care are un efect diuretic puternic, dar scurt. În prezenţa furosemidului are loc excreţia pronunţată de sodiu, dar, după ce efectul diuretic încetează, se constată o retenţie excesivă de sodiu postdiuretică, datorită activării sistemului renină-angiotensină-aldosteron (SRAA) ca răspuns la diureza masivă cu hiponatremie. Pentru a reduce fenomenul de ricoşet, diureza trebuie să fie adecvată, dar nu excesivă, cu administrarea simultană obligatorie a inhibitorilor enzimei de conversie a angiotensinei (IECA – enalapril, lisinopril etc.) şi/sau a antagoniştilor concurenţi ai aldosteronului (spironolactonă, eplerenonă). De asemenea, se recomandă administrarea furosemidului nu în bolus, ci prin perfuzie continuă cu o viteză de 5-10 mg/oră sau substituirea acestuia cu un alt diuretic de ansă cu o perioadă de înjumătăţire mai lungă (torasemid retard), care va asigura o excreţie constantă de sodiu în timpul zilei. O alternativă poate fi asocierea terapiei diuretice cu soluţii hipertone (1,4% şi 4,6% soluţie de clorură de sodiu), care va determina un efect diuretic şi natriuretic mai mare(16).
În figura 5 sunt prezentate locurile de acţiune a diureticelor, cauzele posibile ale rezistenţei la diuretice şi principiile de management a acesteia.
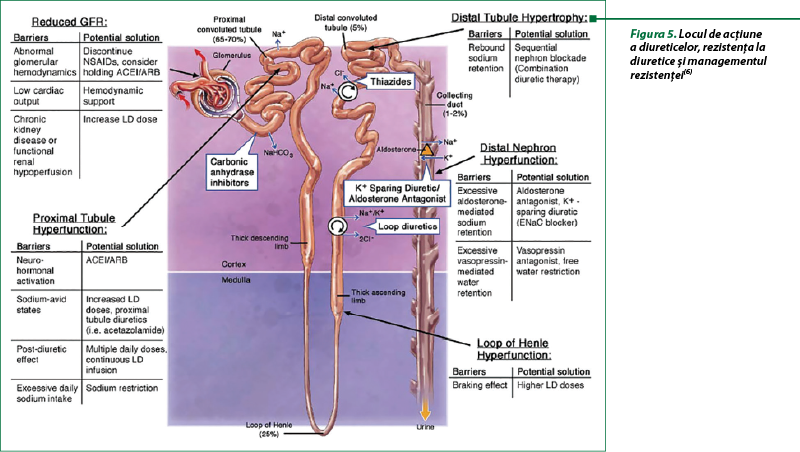
Figura prezintă locurile de acţiune diuretică şi retenţie de sodiu cu strategii sugerate pentru a depăşi rezistenţa diuretică. Livrarea de sodiu în lichidul tubular este determinată de viteza de filtrare glomerulară (GFR). Procentul de sodiu filtrat reabsorbit în fiecare segment de nefron este notat între paranteze. Tubulul contort proximal absoarbe majoritatea reabsorbţiei sodice filtrate şi proximale fiind crescut în stările de reţinere a sodiului sub controlul neurohormonilor (α1‑adrenergic, angiotensina-II), producând efectul postdiuretic. Ansa Henle este locul de acţiune al diureticelor de ansă (LD) şi absoarbe cea mai mare parte a sodiului care scapă de tubul proximal; efectul de frânare pare să se producă aici datorită reglării ridicate a transportorului Na/K/Cl după expunerea la LD. Tubulul convolut distal reabsoarbe o cantitate mai mică de sodiu filtrat prin cotransportorul Na/Cl (inhibat de diureticele de tip tiazidă [TD]), dar dimensiunea şi funcţia pot creşte dramatic după expunerea cronică la LD, reprezentând retenţia de sodiu în revenire. Tubul colector distal este locul reabsorbţiei de sodiu şi apă reglată sub controlul aldosteronului şi vasopresinei prin canale epiteliale de sodiu (ENaC) şi, respectiv, pori pentru apă. La un singur pacient pot apărea mai multe mecanisme de rezistenţă diuretică, necesitând o abordare sistematică a terapiei diuretice.
Concluzii
Managementul rezistenţei la diuretice va fi determinat de analiza minuţioasă a cauzelor şi mecanismelor rezistenţei, de patologia de bază şi cea comorbidă, care vor permite selectarea strategiei optime de soluţionare a rezistenţei. Acestea din urmă se vor referi la măsuri de bază (reducerea aportului de sodiu; suspendarea preparatelor care reduc eficacitatea diureticelor; stabilirea dozei eficiente; creşterea dozelor de diuretic; ajustarea regimului de administrare a diureticelor; substituirea sau utilizarea unui diuretic de ansă alternativ; administrarea intravenoasă a diureticului; perfuzia continuă a diureticului; terapia combinată cu alte clase de diuretice) şi alternative (utilizarea soluţiei saline hipertone; folosirea preparatelor inotrop pozitive; managementul presiunii intraabdominale; infuzia de albumină; administrarea antagoniştilor receptorilor de tip 2 ai vasopresinei, glucocorticoizilor, sensitizatorilor calciului, vasodilatatoarelor; efectuarea ultrafiltraţiei).
Bibliografie
- Aronson D. The complexity of diuretic resistance. European Journal of Heart Failure. 2017; 19,1023–1026.
- Cadnapaphornchai MA et al. The nephrotic syndrome: pathogenesis and treatment of edema formation and secondary complications. Pediatr Nephrol (2014) 29:1159–1167.
- Ellison DH. Clinical Pharmacology in Diuretic Use. CJASN August 2019, 14 1248-1257.
- Ellison DH, Felker GM. Diuretic Treatment in Heart Failure. N Engl J Med 2017; 377: 1964-75.
- Jardim SI. et al. A 2018 overview of diuretic resistance in heart failure. Cardiologia. 2018. 37(11), 935-945.
- Jentzer JC, DeWaldR DTA, Hernandez AF. Combination of Loop Diuretics With Thiazide-Type Diuretics in Heart Failure. Journal of the American College of Cardiology. 2010 November; 55(19,2); 1527-1534.
- Jha VK, Padmaprakash KV, Pandey R. Diuretic strategies in medical disorders. Curr Med Issues 2018;16:60-7.
- Hoorn EJ, Ellison DH. Diuretic Resistance. Am J Kidney Dis. 2017 Jan; 69(1): 136–142.
- Liu C, Liu K. Effects of glucocorticoids in potentiating diuresis in heart failure patients with diuretic resistance. J Card Fail. 2014 Sep;20(9):625-9.
- Lei L, Mao Y. Hormone treatments in congestive heart failure. J Int Med Res. 2018 Jun;46(6):2063-2081.
- Masella C et al. Diuretic Resistance in Cardio-Nephrology: Role of Pharmacokinetics, Hypochloremia, and Kidney Remodeling. Kidney Blood Press Res. 2019;44(5):915-927.
- Qavi AH, Kamal R, Schrier RW. Clinical Use of Diuretics in Heart Failure, Cirrhosis, and Nephrotic Syndrome. Int J Nephrol. 2015;2015:975934.
- Rao VS et al. Compensatory Distal Reabsorption Drives Diuretic Resistance in Human Heart Failure. JASN November 2017, 28(11) 3414-3424.
- Shah N et al. A perspective on diuretic resistance in chronic congestive heart failure. Ther Adv Cardiovasc Dis. 2017 Oct; 11(10): 271–278.
- Gherasimeniuc DS, Pilipciuc DV, Mitcovskaia NP. Patogheneticeschie osnovî terapii paţientov s decompensirovannoi hronicescoi serdecinoi nedostatocinostiu. Neotlojnaia cardiologhia i cardiovasculearnîe rischi. 2019, 3(1), 582-594.
- Fomin VV, Hamhoeva MS. Rezistentnosti c diureticam: pricinî, mehanismî i vozmojnosti preodolenia. Farmateca. 2010, 12, 19-23.
Articole din ediţiile anterioare
Utilizarea terapeutică a diureticelor – o privire de ansamblu
Apa constituie aproximativ 60% din greutatea corpului uman adult şi este responsabilă pentru multe dintre procesele fiziologice. Astfel, homeostazi...