The aortic coarctation (CoA) is the most frequently omitted ductal-dependent cardiac deffect on neonatal screening and also one of the most difficult diagnosis to establish before birth. It is estimated that 60-80% from the newborns with isolated CoA are discharged at home from neonatal departament as healthy babies, later developing hemodynamic complications, that appear suddenly or gradually as a consequence of closing the arterial ductus. So, it is absolutely necessary to make the cardiac screening for every newborn before discharging. It consists of pre- and postductal pulsoximetry and measuring the blood pressure to all four limbs. Also, it is necessary to confirm this diagnosis by the fetal cardiologist in all cases of CoA suspected and the pregnant women to be oriented for delivery in a specialized centre in cardiac intensive neonatal care. At fetal ultrasound, the suspicion of CoA is increased by ventricular and large vessels disproportion signs and in 4-chambers view and/or 3-vessels and trachea especially in the first and second trimesters of pregnancy. However, the prenatal screening registers a high rate of fals-positive and false-negative results. The prenatal diagnosis improves and reduces the morbidity by allowing to plan the delivery in a tertiary center and to establish the treatment with PGE to prevent the constriction of arterial duct. We present the case of a term newborn (38 weeks) born by caesarian section performed in the Obstetrics and Ginecology Clinic of the “Elias” Hospital, antenatal suspicioned with CoA, following two ultrasounds performed at 34 and 35 weeks of gestation.The newborn is treated with PGE medication from the first hour of life. After two days of life, the pediatric cardiologist excluded this diagnosis by echocardiography in “M.S. Curie” Hospital. The treatment with PGE was slowly interrupted and the neonatal evolution was favorable.
Coarctaţia de aortă - dificultăţi de diagnostic fetal. Prezentare de caz şi review al literaturii
Aortic coarctation - difficulties of fetal diagnosis. Case report and literature review
First published: 22 mai 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Gine.16.2.2017.768
Abstract
Rezumat
Coarctaţia de aortă (CoA) este defectul cardiac ductal-dependent cel mai frecvent omis în cadrul screeningului neonatal şi, de asemenea, este unul dintre diagnosticele cel mai dificil de stabilit prenatal. Se estimează că 60-80% dintre nou-născuţii cu CoA izolată sunt externaţi din maternitate ca bebeluşi sănătoşi, ajungând ulterior să dezvolte complicaţii hemodinamice, instalate brusc sau gradual odată cu închiderea canalului arterial (CA). De aceea, este imperios necesară efectuarea screeningului cardiologic al tuturor nou-născuţilor înainte de externare, constând în pulsoximetrie pre- şi postductală şi măsurarea presiunii arteriale (TA) la toate cele patru membre. De asemenea, la toţi nou-născuţii suspicionaţi intrauterin cu acest defect se impune confirmarea diagnosticului de CoA de către specialistul în cardiologie fetală, iar gravida va fi îndrumată să nască într-un centru specializat în îngrijiri neonatale intensive cardiace. La ecografia fetală, suspiciunea de CoA este accentuată de semnul disproporţiei ventriculare şi marilor vase în fereastra 4-camere şi/sau fereastra 3-vase şi trahee, mai ales în trimestrele I şi al II-lea de sarcină. Cu toate acestea, la screeningul prenatal se înregistrează în continuare o rată crescută de rezultate fals-negative şi fals-pozitive. Diagnosticul prenatal îmbunătăţeşte şi reduce morbiditatea prin permiterea planificării într-un centru terţiar şi instituirea tratamentului cu prostaglandină (PGE) pentru a preveni constricţia CA. Prezentăm cazul unui nou-născut la termen (38 de săptămâni), prin operaţie cezariană, efectuată în Clinica de Obstetrică şi Ginecologie a Spitalului Universitar „Elias”, suspicionat intrauterin, în urma a două ecografii efectuate la 34 şi respectiv 35 de săptămâni, cu diagnosticul de CoA, pentru care s-a instituit din primele momente de viaţă infuzie cu PGE . Ulterior, efectuându-se de către cardiologul pediatru, în Spital „M.S. Curie”, la 2 zile de viaţă, o ecocardiografie, acest diagnostic este exclus şi se întrerupe treptat tratamentul cu PGE, evoluţia fiind favorabilă.
Introducere, patologie şi hemodinamică
Coarctaţia de aortă (CoA) se caracterizează prin îngustarea arcului aortic, distal de locul de inserţie a ductului arterial. Severitatea acestui defect merge de la o uşoară îngustare a capătului distal al arcului aortic până la hipoplazia severă a întregului arc aortic. CoA însumează 8% din defectele congenitale cardiace, apărând la 0,2-0,6% dintre nou-născuţi vii (figura 1).
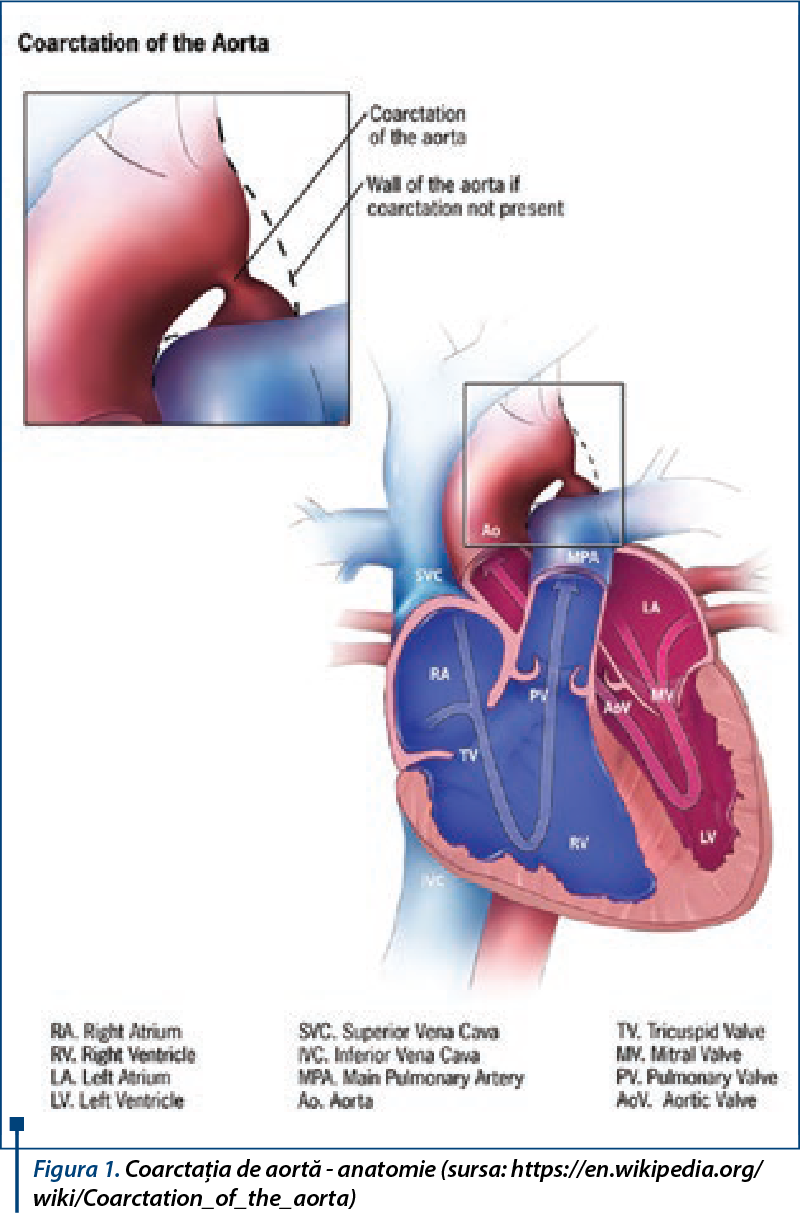
Mecanismul exact al producerii CoA nu este clar înţeles. Cel mai frecvent sunt amintite teoria hemodinamică, care propune drept cauză a CoA reducerea fluxului prin arcul aortic, şi teoria ţesutului ductal ectopic, care sugerează că îngustarea aortică este dată de migrarea ţesutului ductal către aortă. Similar multor forme de boală cardiacă congestivă, etiologia CoA poate fi explicată de ipoteza moştenirii multifactoriale. Prevalenţa CoA în anomalii genetice, precum sindromul Turner (45,X), este de 15-20%.
La făt, consecinţele hemodinamice sunt reduse pentru că istmul primeşte doar 10% din debitul cardiac. După naştere, odată cu închiderea ductului arterial, apar modificări hemodinamice, cu atât mai importante, cu cât îngustarea este mai mare: de la HTA sistemică uşoară la insuficienţă cardiacă congestivă (ICC).
CoA impune o postsarcină crescută asupra VS, ceea ce duce la hipertrofie ventriculară stângă compensatorie. Când postsarcina creşte rapid (obstrucţie aortică bruscă), aşa cum apare după închiderea ductului arterial la nou-născuţii cu CoA, pot să apară rapid ICC şi şoc. Ca urmare a constricţiei ductului arterial, postsarcina VS creşte rapid, cu consecinţa creşterii presiunilor sistolice şi diastolice ale VS. Acestea cauzează creşterea presiunii în atriul stâng, care poate deschide foramen ovale (FO), ducând la şunt stânga-dreapta şi dilataţia AD şi a VD. Dacă FO nu se deschide, presiunile venoase pulmonare cresc şi se dezvoltă dilataţia VD.
Postsarcina VS poate, de asemenea, creşte gradual, permiţând copilului cu CoA mai puţin severă să dezvolte vase arteriale colaterale care parţial by-passează obstrucţia aortică. Aceşti copii pot fi asimptomatici până când HTA este detectată sau apar alte complicaţii. Mecanismul HTA nu este bine cunoscut, totuşi în apariţia ei sunt incriminate obstrucţia mecanică şi mecanismele mediate de renină-angiotensină.
Prognostic
Factorii care afectează prognosticul pe termen lung sunt vârsta la care se practică operaţia, gradul şi durata HTA anterior operaţiei. Mortalitatea în rândul pacienţilor la care CoA nu a fost reparată chirurgical este de 90% la vârsta de 50 de ani, cu o medie de 35 de ani. În ultimii ani, mortalitatea este adesea determinată de vârsta şi greutatea pacientului şi de anomaliile cardiovasculare majore asociate
Tipuri de coarctaţie aortică
Deşi iniţial CoA a fost clasificată în două tipuri - preductală (tipul infantil) şi postductală (tipul adult) -, ulterior explorarea anatomică şi intraoperatorie a arătat că toate CoA sunt juxtaductale, localizate în partea opusă deschiderii ductului arterial în aortă. CoA clasică este situată în aorta toracică, distal de originea arterei subclavii stângi, la nivelul structurii ductale(1).
Dilataţia Ao descendente imediat distal de segmentul îngustat (dilataţie post-stenotică) este de obicei prezentă. O leziune de jet pe peretele Ao distal de locul coarctaţiei poate fi de asemenea prezentă. Gradul de hipoplazie a istmului aortei (porţiunea aortei dintre originea arterei subclavii stângi şi ductul arterial) poate fi semnificativ în CoA simptomatică la nou-născuţi şi sugari, la fel şi arcul aortic transvers (arcul dintre originea arterei inominate drepte şi artera subclavie stângă). La copii şi adulţi, istmul aortic este doar uşor îngustat (figura 2).
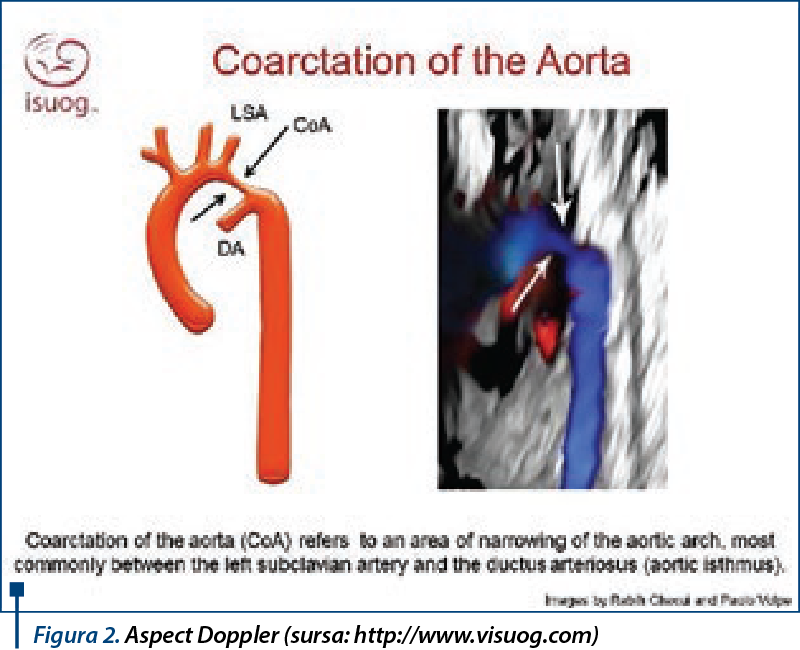
Anomalii cardiace asociate
În 35-45% din cazuri, CoA este un defect cardiac izolat, iar în restul de 55-65% din cazuri sunt asociate alte anomalii cardiace(3): DSV, anomalii valvulare aortice şi mitrale, bicuspidie aortică valvulară, transpoziţie de mari vase, DORV, persistenţa venei cave superioare stângi, sindrom Shone(1,3). Malformaţiile extracardiace apar în 25-35% din cazuri: urinare, gastrointestinale, de SNC şi anomalii faciale(7,9). Există un risc crescut de anomalii cromozomiale, de până la 30%.
Manifestări clinice
Prezenţa defectelor asociate şi a anomaliilor arcului aortic, mărimea ductului arterial, rapiditatea închiderii CAP şi nivelul rezistenţei vasculare pulmonare determină momentul apariţiei manifestărilor clinice şi severitatea lor.
Formele de CoA cu debut clinic precoce. Nou-născuţii şi sugarii pot prezenta dificultăţi de alimentare, tahipnee, letargie şi progresie către ICC şi şoc. Nou-născuţii pot fi externaţi în stare generală bună, iar deteriorarea clinică poate să se producă acasă, odată cu închiderea CA. Apariţia simptomelor poate fi accelerată de prezenţa anomaliilor cardiace asociate, precum DSV. Simptomele pot fi iniţial subtile dacă închiderea CA se produce lent, iar stabilirea diagnosticului poate fi dificilă în acest caz.
Semnele-cheie de diagnostic sunt: discrepanţa TA dintre extremităţile superioare şi inferioare şi scăderea sau absenţa la palpare a pulsului la extremităţi. Când nou-născutul este în şoc, toate pulsurile sunt diminuate.
Cianoza diferenţială (extremităţi superioare rozate cu extremităţi inferioare cianotice) poate fi documentată prin pulsoximetria pre- şi postductală. Totuşi, în prezenţa leziunilor cu şunt larg stânga-dreapta (de exemplu, defect septal ventricular - DSV), saturaţiile AP şi Ao devin aproximativ egale, fără evidenţierea oximetriei diferenţiale.
Suflul sistolic cardiac asociat CoA poate fi nespecific. De obicei, este infraclavicular stâng şi subscapular stâng. Sufluri adiţionale datorate prezenţei altor anomalii asociate, precum DSV sau stenoza valvulară aortică, pot fi de asemenea detectate. Un clic de ejecţie poate semnifica prezenţa bicuspidiei aortice, iar un ritm de galop poate indica disfuncţia ventriculară.
Formele de CoA cu debut întârziat. Pacienţii se prezintă frecvent după perioada neonatală cu HTA şi suflu cardiac. Aceşti pacienţi adesea nu ajung să dezvolte ICC, datorită prezenţei vaselor arteriale colaterale.
Alte simptome prezentate pot fi: cefalee, dureri anginoase, oboseală, rar claudicaţie sau chiar hemoragie intracraniană ameninţătoare de viaţă.
Palparea pulsurilor femurale şi măsurarea TA la toate cele patru membre în timpul examenului clinic de rutină sunt necesare pentru a evita întârzierea diagnosticului. Sugarii mai mari şi copiii se pot prezenta cu HTA şi suflu sistolic. Ocazional, TA la braţul stâng este mai scăzută decât cea de la braţul drept, dacă originea arterei subclavii stângi este din coarctaţie. Similar, anomalii ale originii arterei subclavii stângi (sub nivelul coarctaţiei) pot produce scăderea sau absenţa pulsului brahial drept.
La copiii mai mari şi adulţi, cel mai bun diagnostic al CoA se pune pe baza palpării simultane a pulsurilor femurale şi brahiale. TA în ambele braţe şi unul din membrele inferioare trebuie măsurate. O diferenţă mai mare de 20 mmHg în favoarea braţelor poate fi considerată dovadă de CoA.
Un suflu sistolic sau continuu în aria subclaviculară stângă şi subscapular stâng poate fi prezent. Un clic de ejecţie poate fi auscultat în caz de biscupidie aortică şi un suflu de stenoză aortică sau de insuficienţă aortică este prezent. Similar, un suflu de stenoză mitrală sau de obstrucţie a tractului de ejecţie a VS poate să apară. Un ritm de galop poate apărea în prezenţa unui VS necompliant hipertrofic.
Investigaţii paraclinice
Analize de laborator
La nou-născuţii care prezintă semne de şoc, sunt necesare:
- Hemoculturi, urocultură, cultură LCR pentru a exclude şocul septic.
- Ionogramă, uree, creatinină, glicemie.
- EAB arteriale şi nivelul lactatului seric.
- Analiza urinei, ionogramă, uree, creatinină, glicemie.
Puloximetria pre- şi postductală poate arăta existenţa şuntului dreapta-stânga, în special la nou-născuţi.
Electrocardiograma
ECG-ul la nou-născuţi şi sugari cu debut precoce al CoA poate să arate semne de HVD. La pacienţii cu debut întârziat, ECG-ul poate fi normal sau poate releva HVS şi semne de ischemie de ventricul stâng (figura 3).
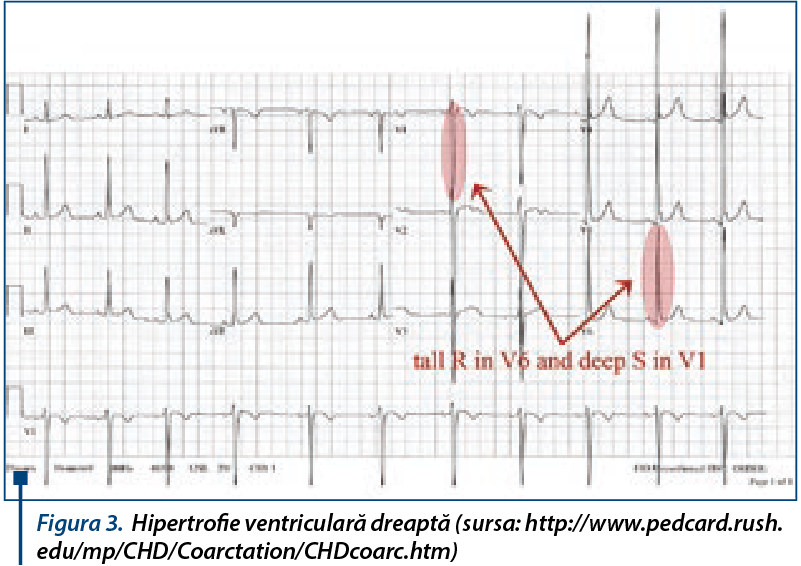
Radiografia toracică
La pacienţii cu debut precoce, radiografia toracică poate arăta cardiomegalie, edem pulmonar şi alte semne de ICC (figura 4).
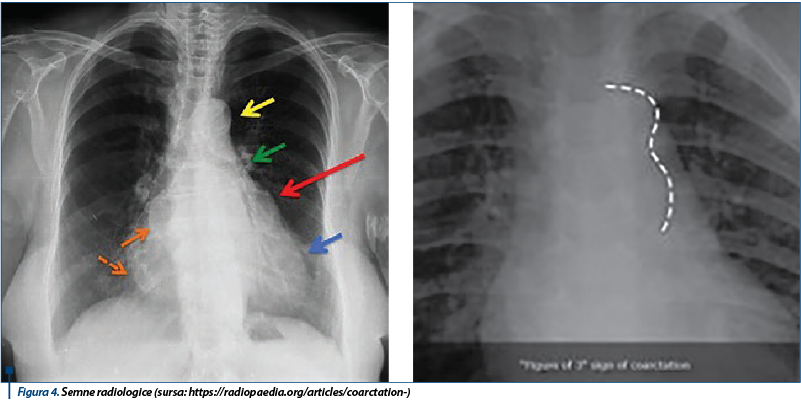
La pacienţii cu debut întârziat, radiografia toracică poate să arate cardiomegalie. Semnul „3” inversat al esofagului plin cu bariu sau un semn „3” în fereastră frontală poate fi observat. Impresiunile costale secundare vaselor colaterale dezvoltate pot fi de asemenea prezente.
Scanarea prin MRI şi CT
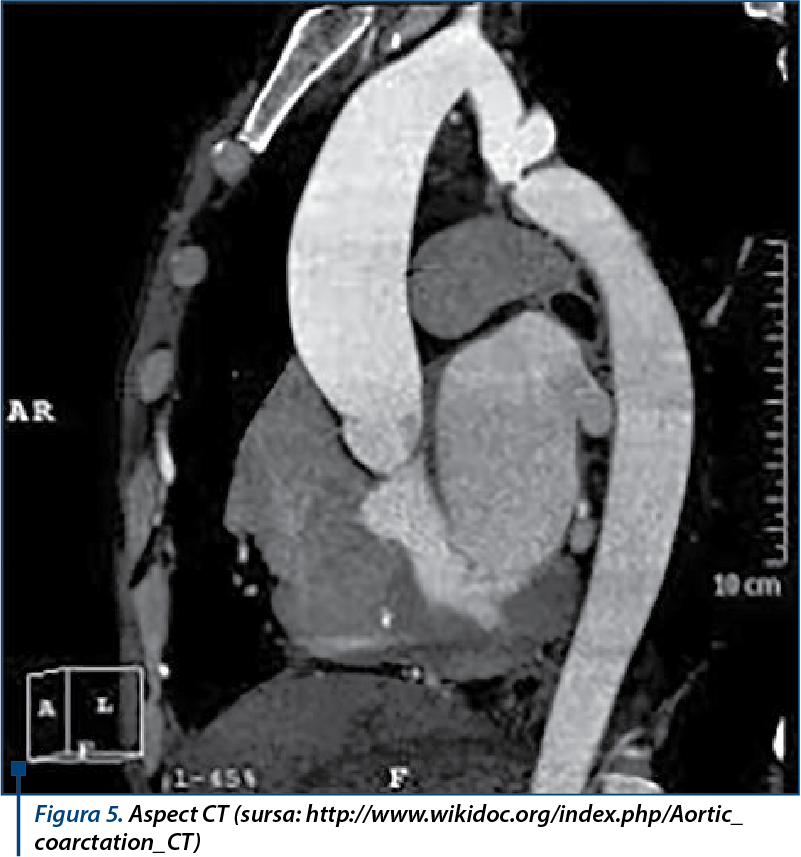
MRI şi CT sunt utile la pacienţii mai în vârstă sau postoperator pentru a evalua obstrucţia reziduală a arcului aortic, hipoplazia arcului sau anevrisme. Peakul sistolic al gradientului de presiune poate fi, de asemenea, calculat utilizând dinamicile fluidelor computerizate bazate pe MRI (figura 5).
Cateterismul cardiac
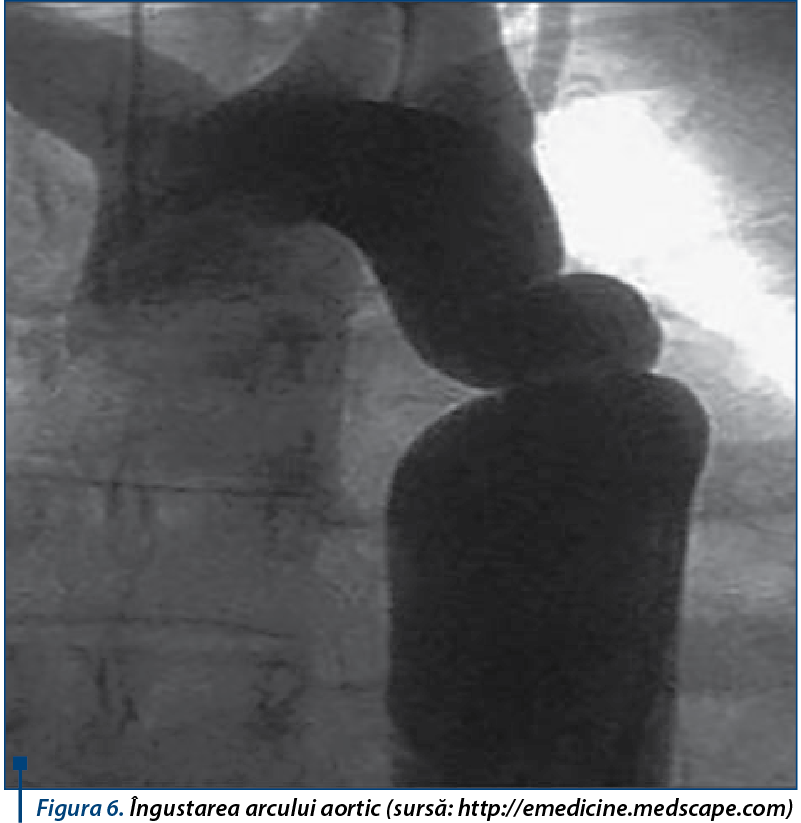
Cateterizarea cardiacă şi cineangiografia selectivă pot să nu fie necesare pentru diagnostic. Totuşi, ele permit evaluarea severităţii CoA, natura anatomică a obstrucţiei aortice (segment scurt sau lung) şi anatomia arcului, incluzând hipoplazia arcului transvers sau istmul (figura 6).
Semne ecografice intrauterine care sugerează diagnosticul de CoA
CoA este una din cel mai dificil de detectat leziuni la screeningul prenatal şi postnatal şi ameninţătoare de viaţă dacă este nediagnosticată. Îmbunătăţirea sensibilităţii diagnosticului de CoA este posibilă prin includerea ferestrelor transverse ale arcului aortic şi arcului ductal cu disproporţie. Scorurile Z istmice şi raportul diametrelor istm/duct separă fetuşii la risc de CoA de fetuşii normali, dar nu pot reduce rata diagnosticelor fals-pozitive.
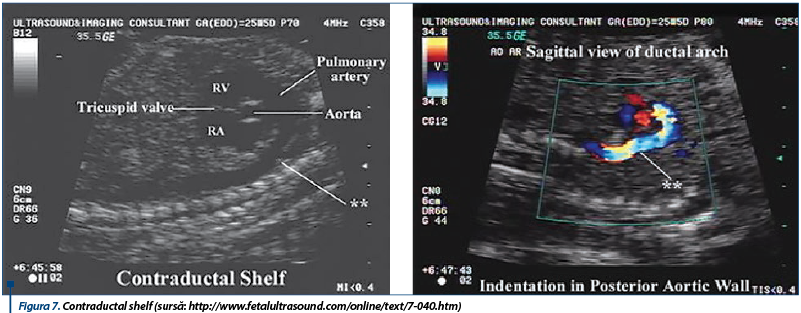
„Contraductal shelf” este dat de ţesutul rezidual fibros derivat din ductul arterial. Prezenţa contraductal shelf este, de asemenea, un indicator excelent pentru CoA(4,11) (figura 7).
CoA este unul dintre defectele cardiace cel mai dificil de depistat înaintea naşterii. Suspiciunea este ridicată de semnul disproporţiei în fereastra 4 şi/sau 3 vase şi trahee (screening de rutină), care poate vizualiza disproporţia de mari vase, acesta fiind un semn anormal în trimestrele I şi al II-lea.
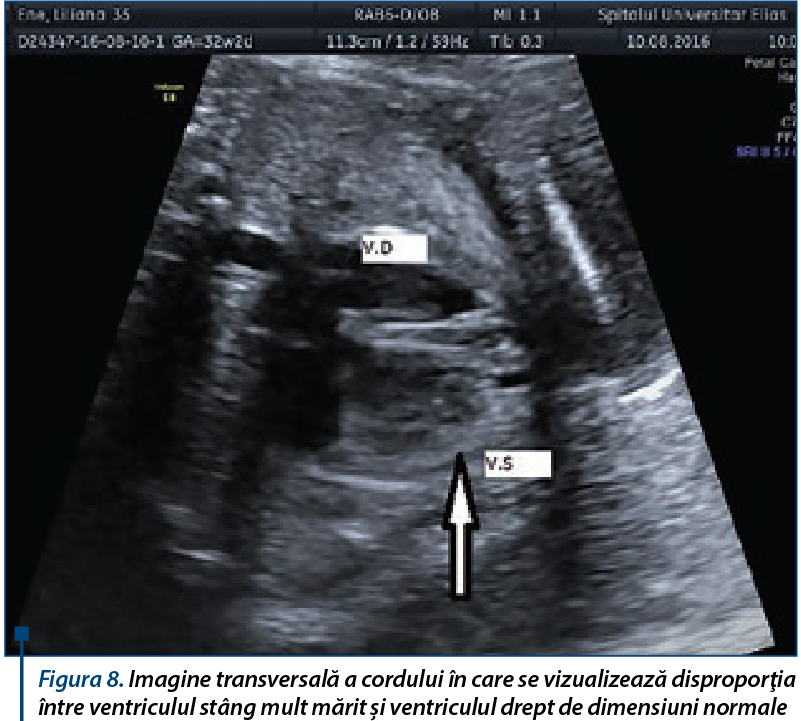
Disproporţia ventriculară ridică suspiciunea unei CoA cu un VS disproporţionat mai mic decât VD. Această disproporţie are o sensibilitate moderată şi o specificitate mică şi o valoare predictivă pozitivă scăzută pentru diagnostic(5,6) (figura 8). Suspiciunea creşte dacă se fac şi alte măsurători: diametrul istmului aortic, raportul istm/duct arterial, scorurile Z derivate din măsurătorile istmului aortic distal şi ductului arterial, prezenţa contraductal shelf şi obstrucţia fluxului la nivelul istmului în fereastra sagitală. Această disproporţie este mai specifică în trimestrul al II-lea şi mai puţin specifică în trimestrul al III-lea(2,12,18). Rezultate fals-pozitive apar după 34 de săptămâni, pentru că în trimestrul al III-lea există un grad de disproporţie fiziologică (normal: VS/VD<1,5). Diagnosticele diferenţiale ale disproporţiei cardiace izolate în fereastra 4 camere includ: anevrism de venă Galen, aneuploidia, anemia şi restricţia de creştere cauzată de insuficienţa placentară. Fereastra 3 vase şi trahee - screening de rutină - poate vizualiza disproporţia de mari vase, care este un semn anormal în trimestrele I şi al II-lea.
Raportul istm/duct şi unghiul istm/duct. Fereastra 3 vase şi trahee permite compararea arcului aortic şi a ductului arterial şi determinarea istmului fetal(16). Raportul normal diametru istm aortic/diametru duct arterial este de 0,74-1,23. Raporturi sub 0,74 ridică suspiciunea de CoA. Unghiul aortic/ductal în fereastra sagitală care include arcurile aortic distal şi ductal şi aorta descendentă proximal utilizează power Doppler 2D. Valori normale = 128,2° - 167°. În CoA = 82,2º - 125º.
Scorurile Z istmice - pentru diametrul istmului aortic măsurat imediat înaintea intrării în aorta descendentă în fereastra 3 vase şi trahee şi raportul duct/istm - sunt indicatori sensibili pentru CoA(16) (figura 9). Ei cuantifică gradul hipoplaziei arcului aortic şi sunt în relaţie cu vârsta gestaţională a femurului(10). Măsurătorile seriate ale acestor scoruri pot face diferenţa între fetuşii care necesită operaţie şi cei care să fie doar ţinuţi sub observaţie.
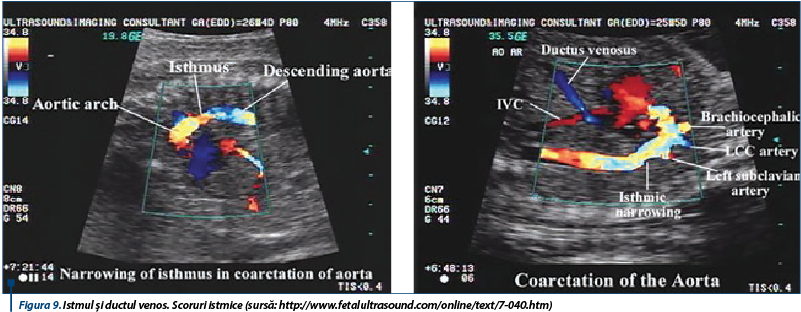
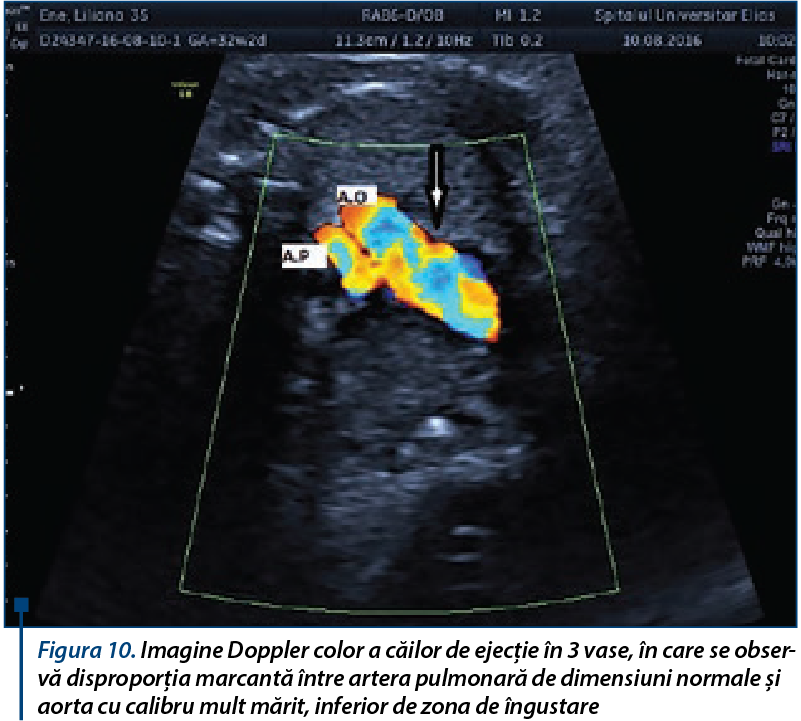
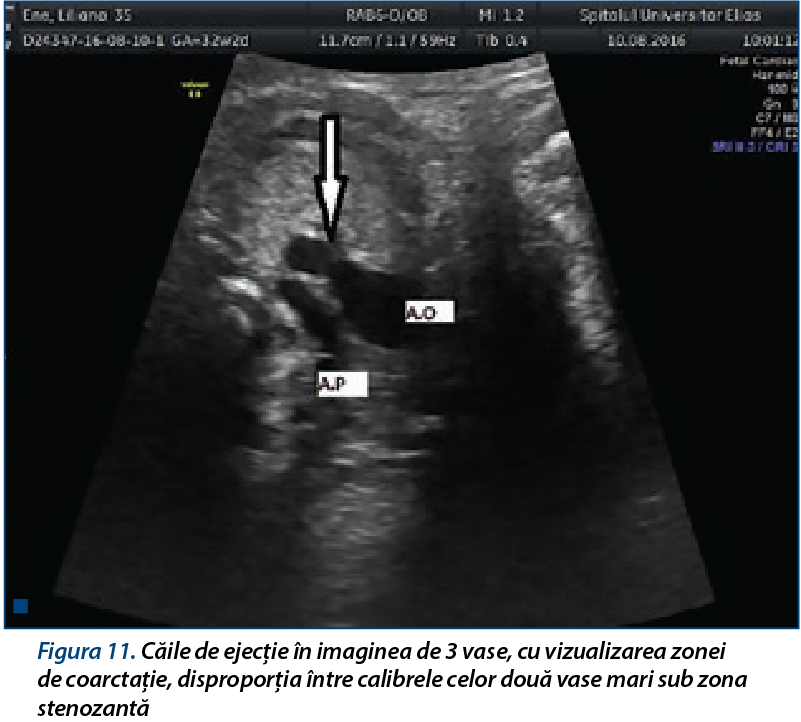
Discrepanţa marilor vase. CoA este aproape întotdeauna asociată cu o discrepanţă a diametrelor marilor vase, unde diametrul AP este mai mare decât diametrul Ao în timpul diastolei(8) (figurile 10 şi 11). Mecanismul este dat de redistribuţia fluxului sangvin datorată rezistenţei crescute a tractului de ejecţie a VS.
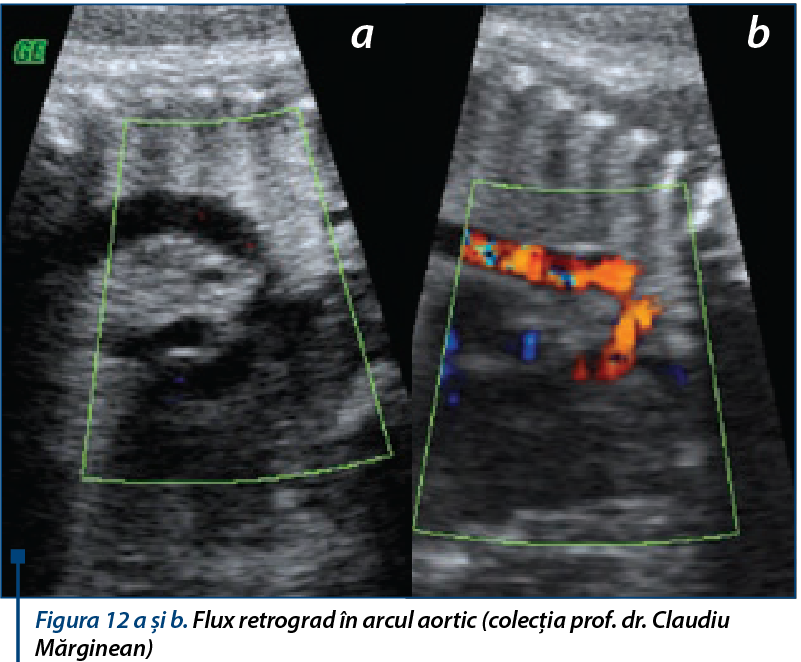
Doppler flow. Fluxul retrograd din arcul aortic fetal coroborat cu un VS mic ridică suspiciunea de CoA(14,17) (figura 12 a şi b).
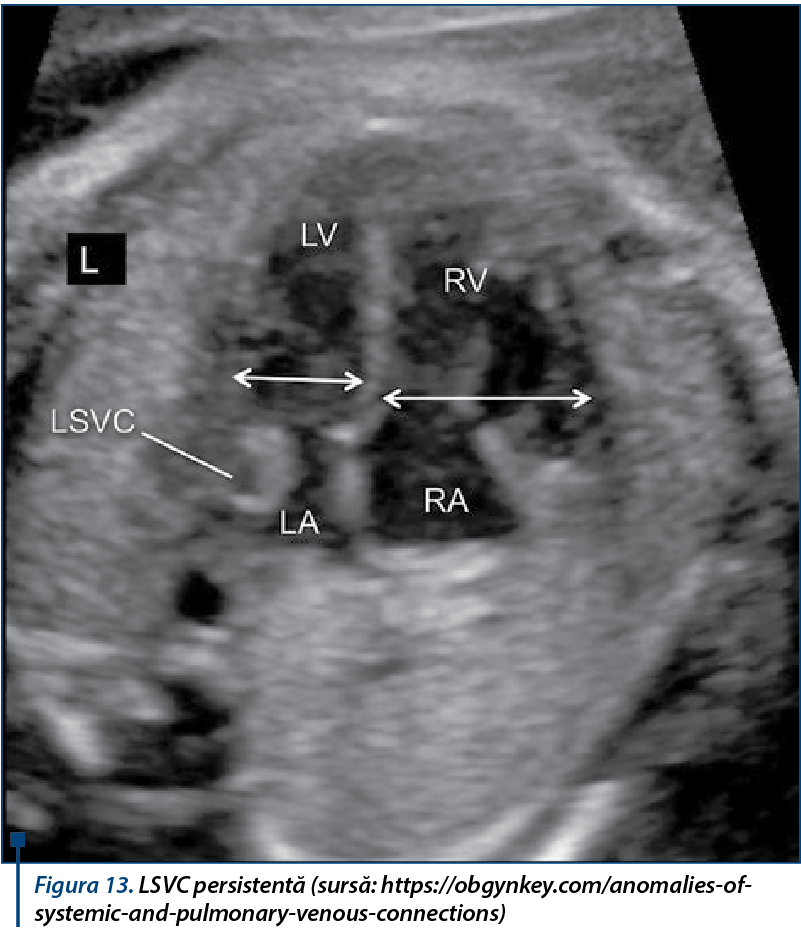
Vena cavă superioară stângă (LSVC) persistentă: când este doar izolată, nu pune probleme, ea este însă frecvent asociată cu CoA(15) (figura 13).
Diagnostic diferenţial
- Stenoza aortică
- Întreruperea arcului aortic
- Obstrucţia tractului de ejecţie a ventriculului stâng
- Hipertensiunea arterial esenţială
- Stenoza de arteră renală
- Feocromocitom.
Tratament medical
CoA cu debut precoce
- Tratamentul IC congestive cu diuretice şi inotropice.
- Prostaglandină E1 (0,05-0,15 mcg/kg/min) infuzată intravenos pentru a menţine deschis ductul arterial.
- Ventilaţie mecanică la cei cu detresă respiratorie.
- Inotropice pozitive infuzate (dopamine, dobutamine, epinephrine), când este prezentă disfuncţia ventriculară, în special cu hipotensiune arterială.
- Un cateter urinar va monitoriza perfuzia renală şi debitul urinar.
- ABG pentru depistarea acidozei.
- Un cateter la NN pentru infuzia de PGE.
- Pacienţii astfel stabilizaţi sunt candidaţi mai buni pentru operaţie sau cateterism intervenţional şi studii angiografice, mai ales în prezenţa defectelor asociate.
CoA cu debut întârziat
Tratamentul HTA
- Hipertensiunea preoperatorie poate fi tratată cu beta-blocanţi, care reduc severitatea hipertensiunii postoperatorii. Ameliorarea promptă a obstrucţiei aortice este de preferat decât să se aştepte tratarea hipertensiunii cu medicamente(1). Hipertensiunea postoperatorie poate fi tratată pentru scurt timp cu vasodilatatoare precum nitroprusiatul sodic şi beta-blocanţi i.v. ca esmoloul, când terapia antihipertensivă pe termen lung este necesară. Beta-blocanţii pot fi continuaţi şi dacă nu există obstrucţie reziduală a arcului aortic, iar ACE inhibitorii sau antagoniştii angiotensinei II, dacă hipertensiunea persistă în ciuda terapiei beta-blocante, pot fi adăugaţi.
Tratamentul chirurgical
Hipertensiunea arterială semnificativă şi ICC sunt indicaţii de operaţie. Ameliorarea obstrucţiei aortice şi tehnicile prin cateterism intervenţional sunt alternative la operaţie. La nou-născuţii şi sugarii simptomatici, intervenţia chirurgicală se face de urgenţă imediat după stabilizare. Pacienţii asimptomatici ar trebui supuşi procedeelor elective, după evaluarea anomaliilor asociate. La aceştia se preferă amânarea intervenţiei până la vârsta de 3-5 ani, pentru a permite aortei să fie mai largă decât jumătate din calibrul anticipat la vârsta adultă.
Corecţia chirurgicală a CoA este tratamentul de elecţie. Au fost dezvoltate tehnici chirurgicale diverse: rezecţie şi anastomoză termino-terminală, aortoplastie cu patch, bypass cu grefă tubulară. Tehnicile chirurgicale obişnuite sunt: rezecţia segmentului coarctat cu anastomoză termino-terminală şi termino-laterală a arterei subclavie, şi aortoplastie lărgită. În prezent se raportează o rată de recoarctare de 20%.
Prognosticul depinde de severitatea leziunii, de prezenţa leziunilor cardiace şi extracardiace asociate care pot influenţa semnificativ mortalitatea operatorie şi durata de viaţă, precum şi de conduita perinatală corectă(13).
Mortalitatea globală este mai mică de 5% pentru CoA izolată şi este o boală cu durată lungă de viaţă. Ameliorarea obstrucţiei, controlul HTA şi urmărirea pe termen lung pentru apariţia obstrucţiilor recurente sunt necesare. Decesul poate apărea secundar recoarctaţiei, anevrismelor la locul coarctaţiei sau la distanţă, ICC, endocarditei bacteriene şi HTA.
Factorii care afectează prognosticul pe termen lung sunt: vârsta la care se practică operaţia şi gradul şi durata HTA anterior operaţiei. Rata mortalităţii în rândul pacienţilor la care CoA nu a fost reparată chirurgical a fost de 90% la vârsta de 50 ani, cu o medie de 35 ani. În ultimii ani, mortalitatea este adesea determinată de vârstă şi de greutatea pacientului, dar şi de anomaliile cardiovasculare majore asociate.
Raportare de caz
Prezentăm cazul unui nou-născut normoponderal, născut în Clinica de Obstetrică-Ginecologie a Spitalului Universitar „Elias”, provenit din sarcină obţinută prin fertilizare in vitro (FIV), urmărită şi investigată corespunzător, cu screening prenatal negativ până la 34 de săptămâni de gestaţie, când la morfologia de trimestru III se ridică suspiciunea de CoA prin evidenţierea disproporţiei ventriculare în favoarea VD, raportul VD/VS fiind de 1,88, iar în privinţa disproporţiei vaselor mari, raportul AP/Ao a fost 1,38. Tot atunci s-a mai observat şi o dilataţie a ductului arterial, interpretată ca posibil anevrism de duct arterial.
La repetarea examenului ecocardiografic, la 35 de săptămâni de sarcină, într-un alt centru de diagnostic, se menţine suspiciunea de CoA, prin hipertrofia VD şi a atriului drept, diametrul AP fiind de 2,3 cm, diametrul Ao fiind de 0,68 cm, neputându-se exclude anevrismul de duct arterial.
Odată cu întărirea suspiciunii de CoA fetală, gravida este îndrumată să nască într-un centru specializat în tratamentul malformaţiilor cardiace şi congenitale, şi anume în Centrul Regional de Terapie Intensivă Neonatală din Târgu-Mureş, pentru a-i oferi nou-născutului posibilitatea tratamentului medical şi chirurgical adecvat.
Travaliul debutează însă mai devreme, la 38 de săptămâni de sarcină, cu RPM şi CUD, iar gravidă naşte în maternitatea noastră, prin operaţie cezariană, prezentaţie craniană, un nou-născut de sex masculin, AGA, cu greutatea de 3100 grame, talia 49 cm, scor Apgar 9, lichid amniotic fără modificări, circulară laxă pericervicală de cordon ombilical.
La naştere, nou-născutul este normal dezvoltat, în afara unui discret sindrom funcţional respirator (SFR), nu prezintă semne clinice evidente de afectare cardiacă (tegumente şi mucoase rozate, acrocianoză, SpO2>95% în aer atmosferic, TA normale la toate cele patru membre, fără diferenţe notabile pre- şi postductale, pulsuri prezente la arterele femurale, timp de recolorare capilară de 3 secunde).
Nici paraclinic nu s-au evidenţiat modificări care să susţină diagnosticul suspicionat antenatal: EAB arterial - oxigenare şi ventilaţie adecvate (pO2: 87 mmHg, pCO2: 38 mmHg) şi lipsa acidozei (pH: 7,41), iar radiografia cardiopulmonară relevă: siluetă cardiacă fără particularităţi, plămâni normal vascularizaţi şi normal expansionaţi la perete, fără condensări.
Având în vedere diagnosticul de CoA suspicionat intrauterin şi neavând imediat după naştere posibilitatea examinării ecocardiografice competente, se decide administrarea de PGE la o rată de infuzie i.v. de 0,05 ug/kg/min pentru a menţine ductul arterial permeabil, precum şi medicaţie inotrop pozitivă: dopamină 5 ug/kg/min, cu dobutamină 5 ug/kg/min, medicaţie administrată pe cateter venos cental percutanat. Profilactic, primeşte antibioterapie cu ampicilină şi gentamicină i.v., iar până la stabilirea unui aport oral adecvat primeşte suplimentar alimentaţie parenterală.
Evoluţia clinică a nou-născutului se menţine satisfăcătoare, cu tegumente rozate, timp de recolorare capilară de 3 secunde, SpO2>94% în aer atmosferic, TAM> 40 mmHg pre- şi postductală, AV 140-160 bpm în repaus, care urcă la 180 bpm în timpul efortului de supt şi de plâns, SFR se menţine uşor/moderat, şoc apexian puternic şi apare suflu sistolic parasternal stâng grad II/6 caracteristic persistenţei de canal areterial (CAP) (cu maximul de intensitate subclavicular stâng şi cu iradiere interscapulovertebrală), abdomen hipoton şi destins de volum, suplu la palpare, nu oboseşte în timpul suptului, toleranţă digestivă bună, reactivitate bună, uşor hipoton. EAB arterial se menţine normal. Hemogramă şi CRP normale.
La două zile de viaţă, nou-născutul este examinat cardioecografic, la Spitalul „M.S. Curie”, de către specialistul cardiolog. În urma acestui prim examen se obiectivează HVD moderat/severă, regurgitare tricuspidiană de grad II, gradient maxim VD-AD=60 mmHg, arc aortic normal conformat, CAP cu calibru larg, HTP moderată, şi se concluzionează: DSA tip OS mic, HVD moderat/severă, fără criterii de coarctaţie de aortă. Ca recomandări de tratament se indică întreruperea treptată a administrării de PGE şi scăderea progresivă a dozelor de inotropice până la întreruperea lor, nou-născutul urmând să fie reevaluat ecografic la externarea din maternitate.
Cu aceste recomandări, evoluţia clinică a nou-născutului în maternitate a fost favorabilă, putând fi externat la 6 zile de viaţă, cu stare generală bună, icter fiziologic, echilibrat cardiorespirator, fără SFR, suflul sistolic (după o perioadă iniţială de accentuare la gradul III-IV/6) s-a remis complet până în ziua externării, fără dificultăţi la supt, cu toleranţă digestivă bună şi tonus îmbunătăţit.
Reevaluarea cardioecografică la externare a evidenţiat: arc aortic normal conformat, minimă pensare Ao istmică, cu flux laminar şi viteză sistolică ~ 1,6 m/secunde; distal de Ao istmică, Ao toracică este uşor dilatată, calibru ~ 7,8 mm, viteza Ao abdominală este 1,1 m/s; se menţine HVD; perete liber VD 5 mm, fără HTP, concluzionând: persistenţa FO, HVD moderată, uşoară pensare Ao istmică, fără criterii de CoA. Recomandările făcute au fost: fără restricţii din punct de vedere cardiologic şi reevaluare peste o lună.
Discuţii
Cazul prezentat aduce în discuţie dificultăţile de diagnosticare antenatală, cu acurateţe, a anumitor malformaţii cardiace şi în special a CoA izolatate. În acest caz este vorba despre rezultate fals-pozitive, care pot apărea mai frecvent în trimestrul al III-lea de sarcină, când semnele ecografice sugestive de CoA se pot confunda cu cele fiziologice, şi ne referim mai ales la criteriul disproporţiei ventriculare. Celălalt criteriu ecografic fals-pozitiv - şi anume al disproporţiei marilor vase - este, de fapt, datorat unui posibil anevrism de duct arterial.
Pentru un managementul obstetrical corect ar fi utilă o scanare anatomică detaliată, pentru a exclude prezenţa anomaliilor extracardiace posibil asociate. Cariotipul este indicat deoarece există un risc mare de anomalii cromozomiale. Dacă există o suspiciune a unei anomalii de arc aortic, naşterea ar trebui planificată într-un centru de referinţă terţiar, cu scopul de a permite transferul precoce al nou-născutului într-o unitate de cardiologie pediatrică, pentru diagnosticul final şi managementul corect. În fapt, CoA critică este un defect duct-dependent, iar menţinerea permeabilă a canalului arterial este necesară.
Concluzii
CoA rămâne una din malformaţiile cardiace cel mai dificil de diagnosticat la screeningul prenatal şi postnatal şi ameninţătoare de viaţă dacă este nediagnosticată la timp. Stabilirea diagnosticului antenatal este foarte importantă pentru aplicarea precoce a conduitei terapeutice specializate. Când se suspicionează diagnosticul de CoA, gravida trebuie urmărită îndeaproape în ultima parte a sarcinii, iar naşterea trebuie să aibă loc într-un centru specializat în îngrijiri de terapie intensivă cardiacă. Tratamentul chirurgical, aplicat după stabilizarea clinică a nou-născutului cu semne precoce de CoA, are rezultate bune. Totuşi, morbiditatea şi mortalitatea rămân crescute. Managementul instituit prompt, printr-un diagnostic intrauterin precoce, poate reduce mortalitatea perinatală şi complicaţiile pe termen lung.
Bibliografie
2. Allan LD, Crawford DC, Tynan M. Evolution of coarctation of the aorta in intrauterine life. Br Heart J 1984; 52:471-3.
3. Brierley J, Redington AN. “Aortic coarctation and interrupted aortic arch.” In: Anderson RH, Macartney FJ, Shinebourne EA, et al. eds. Paediatric Cardiology. Edinburgh: Churchill Livingstone, 2001: 1523–58.
4. Benacerraf BR, Saltzman DH, Sanders SP. Sonographic sign suggesting the prenatal diagnosis of coarctation of the aorta. J Ultrasound Med, 1989; 8:65-9.
5. Brown DL. Sonographic assessment of fetal arrhythmias. AJR 1997; 169:1029-1033.
6. Brown DL, Durfee SM, Hornberger LK. Ventricular discrepancy as a sonographic sign of coarctation of the fetal aorta: How reliable is it? J Ultrasound Med, 1997; 16:95-9.
7. Doyle NM, Mastrobattista JM, Thapar MK, et al. Perinatal pseudocoarctation: echocardiographic findings in vein of Galen malformation. J Ultrasound Med. 2005; 24:93–8.
8. Espinoza J, Romero R, Kusanovic JP, et al. Prenatal diagnosis of coarctation of the aorta with the multiplanar display and B-flow imaging using 4-dimensional sonography. J Ultrasound Med. 2009; 28:1375–8.
9. Ferencz C, Rubin JD, McCarter RJ et al. Cardiac and non-cardiac malformations: Observations in a population based study. Tetralogy, 1987; 35:367-78.
10. Hornberger LK, Sahn DJ, Kleinman CS et al. Antenatal diagnosis of coarctation of the aorta: A multicenter experience. J Am Coll Cardiol, 1994; 23(2):417-23.
11. Hutchins GM. Coarctation of the aorta explained as a branch pint of the ductus arteriosus. Am J Pathol, 1971; 63:203-9.
12. Head CEG, Jowett VC, Sharland GK, Simpson JM. Timing of presentation and postnatal outcome of infants suspected of having coarctation of the aorta during fetal life. Heart, 2005; 91:1070–4.
13. Paladini D, Volpe P, Russo MG, et al. Aortic coarctation: prognostic indicators of survival in the fetus. Heart, 2004; 90:1348–9.
14. Paladini D, Sorrentino M, Pastore G, et al. OC08.01: B-flow derived M-mode is a reliable tool to detect diastolic run-off in fetal aortic coarctation. Ultrasound Obstet Gynecol, 2012; 40:15.
15. Pasquini L, Fichera A, Tan T, et al. Left superior caval vein: a powerful indicator of fetal coarctation. Heart, 2005; 91:539–40.
16. Pasquini L, Mellander M, Seale A, et al. Z-scores of the fetal aortic isthmus and duct: an aid to assessing arch hypoplasia. Ultrasound Obstet Gynecol. 2007; 29:628–33.
17. Pooh RK. New application of B-flow sono-angiography in perinatology. Ultrasound Obstet Gynecol. 2000; 15:163.
18. Mihăilescu IC, Mitran M, Marinescu B. Indexul miocardic (Tei index) în cadrul evaluării Doppler a funcţiei cardiace fetale. Ginecologia.ro, 2013; 1(2):14-7.
Articole din ediţiile anterioare
Sindrom Cornelia de Lange asociat cu anomalie congenitală de cord. Prezentare de caz
Sindromul Cornelia de Lange este un sindrom plurimalformativ, caracterizat prin aspect tipic al feţei, retard de creştere intrauterină, dar şi post...
Caracteristicile neonatale în malformaţiile cardiace congenitale – experienţa noastră
Introducere. Malformaţiile cardiace congenitale (MCC) reprezintă cel mai frecvent defect congenital, apărând la 1% până la 5% din nou-născuţii ...
Hipernatremia la nou-născuţii alăptaţi - o posibilă cauză de afectare cerebrală
Deshidratarea Hipernatremică Neonatală a nou-născuţilor alimentaţi la sân (Neonatal Hypernatremia Deshydration of Breastfed infants - BNHD) este o ...
Clamparea întârziată la nou-născuţii din sarcină gemelară
Sarcinile multiple sunt situaţii unice în care medicii obstetricieni şi neonatologi pot avea o atitudine ezitantă privind efectuarea clampării înt...