Encapsulated peritoneal sclerosis or sclerosing peritonitis is a clinical-morphological entity that raises real challenges for the diagnosis and the treatment. Although it occurs in many other conditions, it represents a complication of peritoneal dialysis closely related to its long-period use. The purpose of this article is to present the case of a 26-year-old patient with lupus erythematosus systemic and chronical renal failure who has been in the peritoneal dialysis program for 11 years, in whom surgery was performed for haemoperitoneum caused by a ruptured ovarian cyst and intraoperatively was found encapsulated peritoneal sclerosis, and discuss the risk factors, diagnosis difficulties and surgical challenges of the disease. The diagnosis is based on symptoms, imagistics and histopathology, but often constitutes an incidental finding during other interventions. The treatment for sclerosing peritonitis is medical and surgical. Medical treatment with corticosteroids, immunosuppressive and antifibrotic agents has questionable results. Surgical treatment is based primarily on peritoneal dialysis catheter removal and switching patients on hemodialysis. Fibrotic membrane removal is attempted in the gut or, if not possible, multiple relaxation incisions are made in this membrane. In the presence of complications we can practice multiple segmentary bowel resections with anastomosis or enterrorraphy, usually followed by other complications. The prognosis of these patients is not good, death occurring in less than two years after the diagnosis.
Peritonita sclerozantă - probleme de tactică operatorie la o pacientă cu chist ovarian eclatat
Sclerosing peritonitis - operative tactic issues in a patient with ruptured ovarian cyst
First published: 15 martie 2016
Editorial Group: MEDICHUB MEDIA
Abstract
Rezumat
Peritonita sclerozantă sau scleroza peritoneală incapsulantă (SPI) reprezintă o entitate clinico-morfologică ce pune reale probleme de diagnostic şi tratament. Deşi apare în numeroase alte condiţii, reprezintă o complicaţie a dializei peritoneale, în strânsă legătură cu durata lungă de efectuare a acesteia. Scopul acestui articol este de a prezenta cazul unei paciente de 26 de ani, cu lupus eritematos sistemic şi insuficienţă renală cronică, în program de dializă peritoneală de 11 ani, la care se intervine chirurgical pentru hemoperitoneu pentru chist ovarian eclatat, la care intraoperator se constată scleroză peritoneală incapsulantă, şi de a discuta factorii de risc, dificultăţile de diagnostic şi provocările chirurgicale ale acestei afecţiuni. Diagnosticul se bazează pe simptomatologie, imagistică şi examen histopatologic, dar de multe ori constituie o descoperire întâmplătoare cu ocazia altor intervenţii. Tratamentul peritonitei sclerozante este medical şi chirurgical. Tratamentul medical, incluzând corticoterapie, imunosupresoare şi agenţi antifibrotici, are rezultate discutabile. Tratamentul chirurgical se bazează în primul rând pe extragerea cateterului de dializă peritoneală şi trecerea pacientei pe hemodializă. Se încearcă îndepărtarea membranei fibrotice de la nivelul intestinului sau, dacă nu este posibil, multiple incizii de relaxare în această membrană. În prezenţa complicaţiilor, se practică enterectomii segmentare cu anastomoze sau enterorafii, frecvent urmate de complicaţii. Prognosticul acestor pacienţi este rezervat, decesul apărând la mai puţin de doi ani de la diagnostic.
Introducere
Scleroza peritoneală incapsulantă (SPI) sau peritonita sclerozantă reprezintă o entitate clinico-morfologică ce pune reale probleme de diagnostic şi tratament. Ea reprezintă una dintre cele mai periculoase complicaţii ale dializatului peritoneal(1). Este o complicaţie rară, dar în strânsă legătură cu durata îndelungată de efectuare a dializei peritoneale. Se caracterizează prin fenomene ocluzive cronice intestinale, persistente, intermitente sau recurente(7), ca rezultat al aderenţelor ce formează o membrană ce încapsulează ansele intestinale, la care se adăugă inflamaţia locală şi sistemică.
Cei trei piloni de diagnostic sunt reprezentaţi de manifestările clinice, semnele radiologice şi examenul histopatologic. Manifestările clinice sunt simptome gastrointestinale nespecifice, de multe ori interpretate în contextul eşecului dializei peritoneale. Semnele radiologice specifice ocluziilor intestinale apar doar în fazele târzii ale afecţiunii. Examenul histopatologic este singurul care pune diagnosticul definitiv. Astfel, putem afirma că diagnosticul de SPI este de cele mai multe ori întârziat sau că SPI poate reprezenta chiar o descoperire întâmplătoare cu ocazia altor intervenţii.
Odată diagnosticată, afecţiunea pune reale probleme de tratament. Deşi s-au încercat diverse tratamente medicale, au rezultate îndoielnice. Tratamentul chirurgical se adresează în primul rând complicaţiilor, dar este la rândul lui urmat de numeroase complicaţii. Principalul pas al tratamentului este reprezentat de extragerea cateterului de dializă peritoneală şi de trecerea pacientului pe hemodializă, dar degradarea morfologică poate continua chiar şi în absenţa continuării dializei peritoneale.
Prognosticul acestor pacienţi este rezervat, decesul survenind de cele mai multe ori la mai puţin de 2 ani de la diagnostic, în special prin complicaţii ale afecţiunii, între 25% şi 55% chiar în primul an(3).
Scopul acestei lucrări este de a prezenta cazul unei paciente cu IRC în stadiu final, în program de dializă peritoneală de 11 ani, cu chist ovarian eclatat, la care intraoperator se diagnostichează scleroză peritoneală incapsulantă. Lucrarea aduce în discuţie factorii de risc, dificultatea unui diagnostic precoce şi opţiunile terapeutice .
Prezentare de caz
Prezentăm cazul unei paciente în vârstă de 26 de ani, din mediul rural, internată în secţia de chirurgie a Spitalului Clinic de Nefrologie „Dr. Carol Davila” Bucureşti prin transfer de pe secţia nefrologie, cu indicaţia de extragere a cateterului peritoneal.
Pacienta a fost internată pe secţia de nefrologie pentru edeme generalizate şi deficit de ultrafiltrare. Pacienta era cunoscută cu lupus eritematos sistemic în evoluţie de 12 ani, pentru care a urmat corticoterapie conform protocoalelor terapeutice în vigoare. În evoluţie, pacienta a dezvoltat numeroase complicaţii: hipertensiune arterială, cataractă subcapsulară, meno-metroragii urmate de amenoree, inclusiv glomerulonefrită proliferativă endocapilară difuză cu boală renală în stadiul V. Dată fiind vârsta tânără a pacientei, s-a optat pentru dializa peritoneală pe care o efectua de circa 11 ani, în sistem CAPD (Dializă Peritoneală Continuă Ambulatorie). Pentru nefropatia lupică, pacienta a urmat terapie imunosupresoare (9 pulsuri de ciclosporină şi ciclofosfamidă), terapie anticoagulantă, plasmafereză, tratament antihipertensiv şi eritropoietină. În timpul tratamentului de dializă peritoneală, evoluţia a fost dominată de trei episoade de peritonită de etiologie variată: tuberculoasă, enterococ, respectiv stafilococ auriu. Cu doi ani înainte de actuala internare, pacienta a început să dezvolte deficit de ultrafiltrare. Biologic, pacienta a prezentat anemie moderată, trombopenie şi hiperhidratare, astfel încât s-a indicat iniţierea tratamentului de hemodializă şi suprimarea dializei peritoneale.
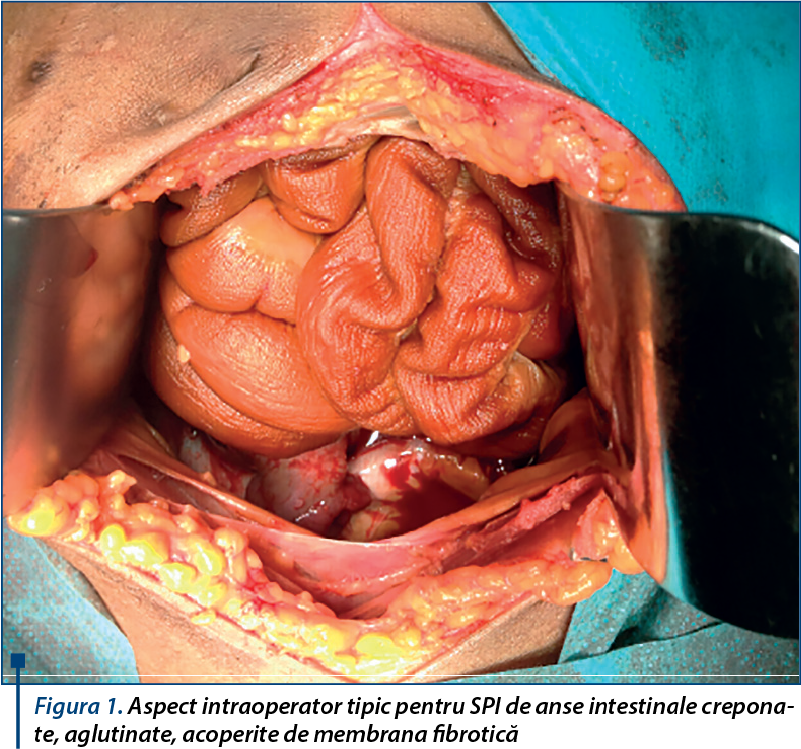
La internare pe secţia chirurgie se constată pacientă anorexică, cu tegumente şi mucoase palide, echilibrată hemodinamic şi respirator, cu abdomen suplu, mobil cu mişcările respiratorii, dureros spontan şi la palpare difuz, fără semne de iritaţie peritoneală, pe cateterul de dializă peritoneală intermitent înregistrându-se efluent uşor sangvinolent.
Se decide intervenţia chirurgicală şi se practică montare de cateter venos central jugular drept în vederea hemodializei şi, ulterior, extragerea cateterului de dializă peritoneală. În momentul extragerii cateterului, se observă la nivelul capătului terminal prezenţa de sânge lacăt. Se decide conversia. Se pătrunde în cavitatea peritoneală şi se constată sânge lacăt în cantitate de circa 600 ml, peritoneu parietal mult îngroşat, intestine acoperite de o seroasă îngroşată, cartonată, intens aderente între ele sub forma unei capsule creponate, trompa dreaptă mult mărită de volum şi deformată, chist ovarian hematic eclatat, cu hematom local ce împinge uterul spre posterior şi îl deviază spre stânga. Se practică adezioliza, anexectomie dreaptă, lavaj şi drenaj al cavităţii peritoneale.
Evoluţia pacientei a fost stabilă timp de circa 12 ore postoperator, când starea generală se agravează brusc, devine instabilă hemodinamic şi se înregistrează evacuare de sânge atât la nivelul tubului de dren, cât şi din tunelul parietal al fostului cateter de dializă peritoneală. Se reintervine chirurgical şi se constată sângerare difuză peritoneală şi sângerare la nivelul tunelului fostului cateter de dializă peritoneală. Se practică hemostaza chirurgicală cu fire transfixiante, aplicare de bureţei hemostatici, sutură dreaptă abdominală şi repoziţionare drenaj pelvian. Evoluţia postoperatorie este favorabilă, pacienta transferându-se către secţia de nefrologie a 5-a zi postoperator.
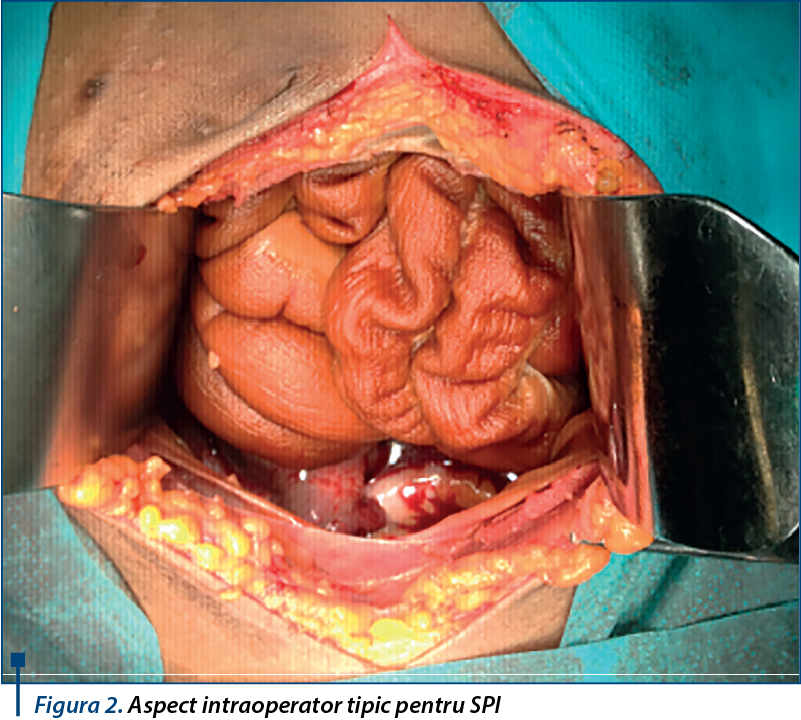
Examenul histopatologic al specimenului peritoneal relevă procese de fibroză difuză şi microtromboze în sectorul arteriovenular (aspect de peritonită sclerozantă), iar la nivelul ovarului se evidenţiază corp galben transformat chistic, hemoragic, efractat, cu reacţie inflamatorie xanto-granulomatoasă, cu marcate depozite de hemosiderină şi asociat chist epidermoid tapetat în interior de un epiteliu scuamos nekeratinizant, focal cu acantoză şi parakeratoză. În ţesuturile perianexiale s-au găsit întinse sufuziuni hemoragice.
În următoarea perioadă, pacienta dezvoltă un nou episod de peritonită (stafilococ coagulazo-negativ şi enterococ), numeroase episoade subocluzive, EPA, convulsii tonico-clonice, urmate de un episod de stop cardiorespirator resuscitat (AVC prin tulburări de flux venos la nivel cortical bilateral, centropontin).
Pacienta a decedat la un an de la diagnostic prin accident vascular cerebral, fără a se înregistra fenomene franc ocluzive intestinale în această perioadă.
Discuţii
Substituţia funcţiei renale prin dializa peritoneală a fost introdusă în 1978 în America de Nord(10), iar în ţara noastră, la Bucureşti, la Spitalul Cantacuzino, în anul 1995. La sfârşitul anului 2015 se înregistrau în ţara noastră, conform Registrului Renal Român, 11.765 de pacienţi cu IRC, din care 623 erau trataţi prin dializă peritoneală (5,29%), cu o incidenţă a dializaţilor peritoneal de 65 de cazuri, în continuă scădere în ultimii ani.
Utilizarea membranei peritoneale pentru ultrafiltrare a creat însă oportunitatea apariţiei modificărilor morfologice în structura acesteia(8). Una dintre afecţiunile determinate de aceste modificări, ce pune reale probleme de diagnostic şi conduită terapeutică, este scleroza peritoneală incapsulantă. Este cunoscută sub diferite denumiri, printre care şi peritonită sclerozantă. Primii pacienţi dializaţi peritoneal cu această afecţiune au fost raportaţi în 1980 de Ghandhi et al. şi Denis et al.(9), fiind considerată pe atunci o complicaţie fatală a dializei peritoneale(9).
Deşi apare în strânsă legătură cu dializa peritoneală, există numeroşi factori favorizanţi pentru dezvoltarea afecţiunii: peritonite repetate, tumori maligne peritoneale sau abdominale, tuberculoză abdominală, după transplant de ficat, în anumite boli autoimune, utilizare de dezinfectanţi intraperitoneali pe bază de talc, utilizarea agenţilor alcalinizanţi (acetat, lactat), administrare intraperitoneală de medicamente, utilizarea de beta-blocante, de icodextrină, în utilizarea de clorhexidină în dezinfectarea tubulaturii pentru dializă, de povidone-iodină în dezinfecţie(4,7,8,9). Totuşi, au fost descrise şi cazuri idiopatice(3).
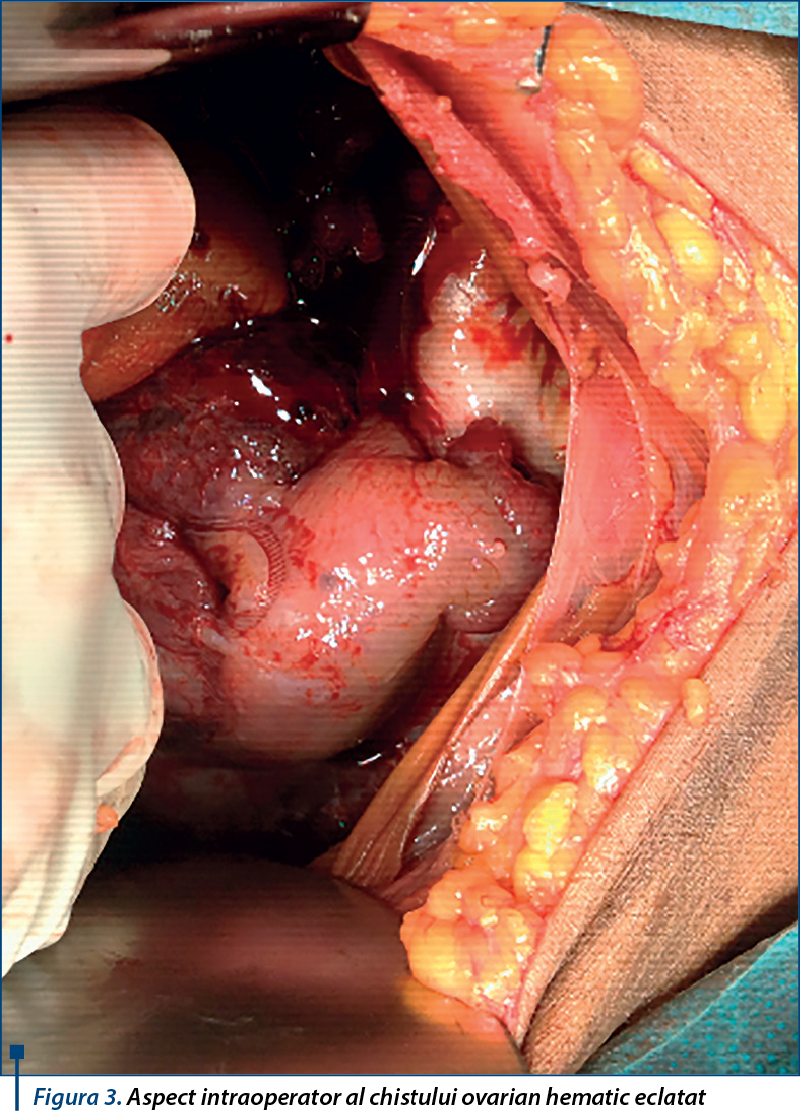
O menţiune specială trebuie făcută asupra peritonitelor severe ce apar în timpul tratamentului de dializă peritoneală(8,11). Etiologia acestora poate fi bacteriană (stafilococ auriu în special), fungică sau determinată de Pseudomonas sp, dar un rol important este deţinut de peritonita tuberculoasă(8,9). În cazul prezentat anterior, pacienta a prezentat în antecedente trei episoade de peritonită, dintre care două se încadrează ca factori de risc major, una determinată de stafilococ auriu şi una tuberculoasă.
Este o afecţiune rară, incidenţa ei variind foarte mult, între 0,7% şi 7,3%(9), fiind însă în strânsă legătură cu durata îndelungată de efectuare a dializei peritoneale, şi nu cu tipul de dializă peritoneală. Conform unui studiu prospectiv efectuat de Kawanishi et al., începând cu 1999, pe 1.958 de pacienţi trataţi prin dializă peritoneală, între care se raportează 48 de pacienţi cu SPI, există rate sensibil egale de dezvoltare a SPI atât pentru DPA (dializa peritoneală automată), cât şi pentru DPCA, însă riscul de dezvoltare a SPI creşte în funcţie de durată de efectuare a dializei peritoneale, fiind maxim după 8 ani(3,9) şi apărând extrem de rar sub 2 ani de tratament(7).
Pacienta prezentată era în program de dializă peritoneală de 10 ani la momentul internării, efectuată în sistem DPCA.
Mecanismul de producere nu este foarte clar înţeles, dar sunt luaţi în considerare doi factori: pe de o parte, deteriorarea peritoneului, ca urmare a contactului timp îndelungat cu dializatul peritoneal şi, pe de altă parte, asocierea cu un factor supraadăugat de tipul inflamaţiei(6,9).
Diagnosticul este foarte dificil, de multe ori reprezentând o descoperire accidentală cu ocazia altor intervenţii sau chiar fiind stabilit la mult timp după încetarea dializei peritoneale(3). Cei trei piloni de diagnostic sunt reprezentaţi de: clinică, radiologie şi confirmarea histopatologică(1,2). Clinica este nespecifică, cu simptome sugerând obstrucţia intestinală (greaţă, vărsături, tulburări de tranzit intestinal, durere abdominală(2)), la care se adaugă anorexie, scădere marcată în greutate şi depleţie nutriţională(4).
Depleţia nutriţională se datorează ileusului cronic, pe de o parte, inflamaţiei, pe de altă parte, dar este şi rezultatul endotoxemiei şi infecţiilor(10). Astfel, ori de câte ori înregistrăm simptomatologie gastrointestinală nespecifică la un pacient dializat peritoneal, trebuie să ne gândim la posibilitatea SPI. Alte simptome înregistrate sunt: prezenţa ascitei, a febrei joase (consecinţa inflamaţiei), a unui dializat peritoneal sangvinolent şi, într-o fază avansată, palparea unei formaţiuni tumorale abdominale reprezentată de masa anselor intestinale încapsulate (denumite cocon)(4). Pacienţii pot prezenta creşterea markerilor inflamatori(3), în special a proteinei C reactive(6,9). Toate aceste simptome apar însă în fazele avansate. În fazele precoce ale afecţiunii se înregistrează deficit de ultrafiltrare şi modificări ale statusului funcţional(2,11).
La internare, pacienta era anorexică, cu scădere marcată ponderală, fapt ce a fost atribuit bolii de bază. Deşi nu prezentase simptomatologie ocluzivă, deficitul de ultrafiltrare apăruse cu doi ani anterior internării, iar prezenţa efluxatului hemoragic a fost interpretată în context de peritonită. Astfel, diagnosticul a fost mult întârziat şi a reprezentat o descoperire întâmplătoare în contextul chistului ovarian eclatat.
Fenomenele ocluzive sau subocluzive se datorează capsulei fibroase ce înconjoară ansele intestinale şi care se extinde şi la nivelul peritoneului parietal. Din acest motiv, simptomatologia apare doar în fazele avansate ale afecţiunii; în fazele precoce, membrana fiind foarte subţire, nu determină fenomene ocluzive(9). Examenele radiologice, de asemenea nespecifice, pot sugera semnele obstrucţiei intestinale. Computer-tomografia abdominală poate arăta prezenţa calcificărilor la nivelul peritoneului, a îngroşării seroasei peritoneale a intestinului subţire, dar şi a intestinului gros, prezenţa aderenţelor între ansele intestinale, prezenţa lichidului peritoneal, a unor septuri intraperitoneale sau chiar niveluri hidroaerice(2,8). PET-scan poate avea un rol în special în fazele timpurii ale inflamaţiei(3). Alte investigaţii, de tipul ecografiei, radiografiei abdominale sau chiar IRM-ul nu sunt suficient de sensibile(1). Ultrasonografia poate furniza un semn caracteristic: o imagine trilaminară, dar necesită prezenţa ascitei(8). În cazul prezentat, pacienta efectuase numeroase ultrasonografii şi radiografii abdominale, fără semne evidente de boală. CT sau IRM nu au fost efectuate în timpul evoluţiei afecţiunii.
Examenele histopatologice relevă prezenţa modificărilor peritoneului atât macroscopic, cât şi microscopic. Macroscopic, peritoneul apare profund alterat: ansele intestinale sunt unite, aderente, prin prezenţa unei membrane fibroase groase, fapt ce duce la rigiditatea lor şi la scăderea motilităţii(5). Pot fi afectate toate organele acoperite de peritoneu, dar şi peritoneul parietal. Această membrană va înveli organele intraperitoneale, în special masa anselor intestinale, formând coconul abdominal(5,6). Aceasta este etapa când formaţiunea devine palpabilă, asemănătoare unei tumori. Aspectul macroscopic este singurul caracteristic afecţiunii şi este obţinut prin laparoscopie sau celiotomie(1,6).
Microscopic se notează apariţia ţesutului de legătură fibros hialinizant, a denudării mezoteliale, a celulelor specifice inflamaţiei cronice (leucocite, eritrocite, macrofage şi celule gigante(5)), umflarea fibroblastelor peritoneale, depozite de calciu(1,3). În unele cazuri poate apărea chiar osificarea peritoneului(5). Se înregistrează vasculopatii ale venulelor postcapilare caracterizate prin îngustare luminală până la obstrucţie, neovascularizaţie progresivă şi limfangiogeneză(10), dar şi scleroza degenerativă a vaselor capilare(9). Capsula are drept element dominant depozitele de fibrină(1,9). Modificările vasculare pot avea drept rezultat sângerarea perivasculară(1), ducând la sângerare focală a peritoneului şi la cantităţi variabile de ascită hemoragică(6).
Examenele histopatologice ale specimenului de biopsie peritoneală şi al piesei (ovar) pun în evidenţă prezenţa fibrozei peritoneale şi a modificărilor vasculare de la nivelul peritoneului, confirmând suspiciunea de peritonită sclerozantă ridicată intraoperator pe baza aspectului macroscopic.
Tratamentul medical, cu rezultate discutabile, se bazează pe utilizarea corticosteroizilor şi a imunosupresoarelor (ciclosporina, micophenolate şi azatioprina)(3,8). Corticosteroizii, datorită efectului antiinflamator, înregistrează o oarecare ameliorare în statusul pacienţilor(3). Pot fi folosiţi ca monoterapie sau pot fi utilizaţi alături de imunosupresoare.
Tamoxifenul poate fi utilizat datorită proprietăţilor antifibrozante, efectul lui fiind maxim în special în fazele incipiente ale afecţiunii şi asociat cu nutriţie parenterală totală(10). În caz de malnutriţie severă, există autori care recomandă utilizarea nutriţiei parenterale totale(5,11). În cazul pacientei noastre, ea a dezvoltat SPI, în ciuda corticoterapiei pe care a urmat-o timp îndelungat pentru LES, dar şi a tratamentului imunosupresor pe care l-a urmat în evoluţia bolii, demonstrând limitele tratamentului medical.
Tratamentul chirurgical are drept prim pas extragerea cateterului de dializă peritoneală şi trecerea pacientei pe hemodializă(8). Totuşi, alterarea peritoneală şi procesul de fibrozare pot continua. De aceea, în multe cazuri, diagnosticul se stabileşte la mult timp după încetarea dializei peritoneale. Abordarea chirurgicală a afecţiunii este dictată de cele mai multe ori de situaţia intraoperatorie. În absenţa complicaţiilor, se practică enteroliza, cu excizia peritoneului afectat şi a membranei fibroase, ce acoperă intestinele. Indicaţiile operatorii sunt obstrucţia intestinală, deteriorarea statusului nutriţional, hemoragia intraperitoneală, peritonitele secundare ori apariţia zonelor de infarctizare(4).
S-a observat o îmbunătăţire a simptomelor ocluzive după tratamentul chirurgical. Totuşi, chirurgia nu are nici un efect asupra deteriorării peritoneale, existând cazuri de progresie a acesteia şi de reformare a capsulei şi recurenţă a SPI într-un interval mai mic de un an la unii pacienţi(9). Tratamentul chirurgical este marcat de numeroase complicaţii, existând un mare risc de hemoragie şi perforaţie intestinală în timpul exciziei membranei fibrotice de la nivelul intestinului sau al peritoneului parietal sclerotic. Astfel, în prezenţa acestor complicaţii, se recomandă enterectomie cu entero-entero-anastomoză, urmată la rândul ei de numeroase fistule intestinale, fapt ce agravează şi mai mult prognosticul acestor pacienţi. În cazul în care excizia membranei fibroase nu este posibilă din cauza complicaţiilor, se poate încerca efectuarea a numeroase incizii de relaxare în membrana fibrotică. Trebuie menţionat că rezultatul tratamentului chirurgical este mult mai bun în absenţa enterectomiilor(3,11).
Pacientei noastre i s-au prelevat specimene de biopsie peritoneală, s-a practicat anexectomie dreaptă pentru chistul hemoragic ovarian drept eclatat, s-au practicat lavaj şi drenaj peritoneal. Din cauza riscurilor crescute de sângerare şi perforaţie, s-a practicat o intervenţie conservatoare, fără enteroliză. Chiar şi în aceste condiţii, postoperator a prezentat o complicaţie hemoragică ce a determinat reintervenţia pentru hemostaza secundară.
În acest caz, pacienta a prezentat mai mulţi factori de risc pentru SPI. Ea a fost expusă fluidului de dializă peritoneală pentru o perioadă foarte lungă de timp, de circa 10 ani. În timpul acestei perioade, ea a prezentat trei episoade de peritonită, de etiologie variată, inclusiv tuberculoasă. Deşi a urmat tratament cu corticosteroizi şi imunosupresoare, evoluţia ei a fost spre dezvoltare de SPI. Diagnosticul a fost tardiv, intraoperator cu ocazia altei afecţiuni, iar evoluţia postoperatorie a fost grevată de numeroase complicaţii imediate şi la distanţă.
Concluzii
SPI este o afecţiune rară, dar deosebit de gravă prin evoluţia ei. Prezintă numeroşi factori de risc, dintre care cel mai important este durata lungă de efectuare a dializei peritoneale. Opţiunile terapeutice sunt limitate, mortalitatea fiind foarte ridicată, în special în primul an de la diagnostic.
Tratamentul acestor pacienţi trebuie făcut în centre specializate, de echipe multidisciplinare din care să facă parte nefrologul şi chirurgul familiarizat cu tehnicile chirurgicale necesare acestor pacienţi. Deosebit de importante în managementul acestor pacienţi sunt extragerea cateterului de dializă peritoneală şi trecerea pe hemodializă. Tratamentul chirurgical, deşi esenţial, este urmat de un mare număr de complicaţii.
Bibliografie
2. Braun N, Fritz P, Ulmer C, Latus J, Kimmel M, Biegger D, Ott G, Reimold F, Thon KP, Dippon J, Segerer S, Alscher MD - Histological Criteria for Encapsulating Peritoneal Sclerosis – A Standardized Approach, PLOS One, 2012, Vol 7, Issue 11, e 48647, 1-8.
3. Chembo CL, Macdonald A, Hay N, Matheson P, Pidgeon G, Leikis M – Encapsulating peritoneal sclerosis - a complication of peritoneal dialysis, NZMJ 2011, vol 124, no 1342, 89-93.
4. Dellen D, Augustine T – Encapsulating peritoneal sclerosis, British Journal of Surgery 2012, 99, 601-602.
5. Garosi G, Di Paolo N - Peritoneal Sclerosis: One or Two Nosological Entities, Seminars în Dialysis- Vol 13, No 5, 2000, 297-308.
6. Honda K, Oda H - Pathology of encapsulating peritoneal sclerosis, Peritoneal Dialysis International, Vol. 25 (2005), Suppl. 4, S19-S29.
7. Johnson DW, Cho Y, Livingston BER, Hawley CM, McDonald SP, Brown FG, Rosman JB, Bannister KM, Wiggins KJ - Encapsulating peritoneal sclerosis: incidence, predictors, and outcomes, Kidney International (2010) 77, 904-912.
8. Kawaguchi Y, Kawanishi H, Mujais S, Topley N, Oreopoulos DG - Encapsulating peritoneal sclerosis: definition, etiology, diagnosis, and treatment, Peritoneal Dialysis International, Vol. 20, Suppl. 4, S43-S55.
9. Kawanishi H - Encapsulating peritoneal sclerosis - review article, Nephrology 2005, 10, 249-255.
10. Nakayama M, Terawaki H - Multidisciplinary clinical strategies for encapsulating peritoneal sclerosis în peritoneal dialysis: Update from Japan, Internaţional Journal of Urology (2014) 21, 755-761.
11. Negoi D, Khanna R - Ultrafiltration Failure and Encapsulating Peritoneal Sclerosis, Handbook of Dialysis Therapy (4th edition), Elsevier 2008, 628-639.
Articole din ediţiile anterioare
Depresia perinatală
Depresia postpartum reprezintă un subiect important în obstetrică, afectând 13% dintre femei în timpul sarcinii sau în primul an post-partum, du...
Complicaţiile hipertensiunii arteriale induse de sarcină – management terapeutic şi prognostic
Managementul sarcinii asociate cu hipertensiune gestaţională se realizează în funcţie de severitatea hipertensiunii arteriale, de vârsta ges...
Diabetul gestaţional
Diabetul gestaţional afectează 3-9% din sarcini, implicaţiile acestuia asupra mamei şi copilului fiind uriaşe, întrucât creşte riscul complicaţiilo...
Complicaţiile perinatale şi neonatale la pacientele cu răspuns ovarian scăzut în sarcinile obţinute prin proceduri de reproducere umană asistată
In vitro fertilization (IVF) technologies with a controlled ovarian hyperstimulation approach have classified patients into three different groups ...