Hypersensitivity pneumonitis (HP), previously called extrinsic allergic alveolitis, is a form of diffuse interstitial lung disease resulting from sensitization to an inhaled antigen, involving complex hypersensitivity reactions types III and IV. The disease can be caused by multiple agents that are present at work places and at home, such as microbes, animal and plant proteins, organic and inorganic chemicals. HP is classified as acute/subacute or chronic, depending on the intensity and frequency of exposure to causative antigens. Diagnostic criteria have been proposed, based on exposure, clinical presentation, lung function tests, imaging findings, bronchoalveolar lavage, and biopsies. Being an immune reaction in the lung, the most obvious treatment of HP is avoidance of the contact with the offending antigen, although the complete removal is not always possible. Systemic corticosteroids represent the only reliable pharmacologic treatment of the disease, but they do not alter the long-term outcome, and prognosis is poor, leading to irreversible lung damage in the form of fibrosis or emphysema, respiratory insufficiency and even death.
Pneumonita de hipersensibilitate
Hypersensitivity pneumonitis
First published: 19 mai 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/MED.117.3.2017.743
Abstract
Rezumat
Pneumonita de hipersensibilitate (PH), numită anterior şi alveolita alergică extrinsecă, este o formă de boală pulmonară interstițială difuză, rezultată din sensibilizarea la un antigen inhalant, care implică reacții complexe de hipersensibilitate de tipurile III și IV. PH poate fi cauzată de mai mulți agenți, prezenţi în mediul profesional sau acasă, cum ar fi agenţi infecţioşi, proteine de origine animală și vegetală, produse chimice organice și anorganice. Boala este clasificată ca acută/subacută sau cronică, în funcție de intensitatea și frecvența expunerii la antigenele cauzale. Au fost propuse criterii de diagnostic bazate pe istoricul de expunere la posibilii agenţi cauzali, prezentarea clinică, probe funcţionale ventilatorii, investigaţiile imagistice, rezultatele lavajului bronhoalveolar şi ale biopsiilor. Fiind o reacție imunologică pulmonară, tratamentul cel mai evident al pneumonitei de hipersensibilitate este evitarea contactului cu antigenul cauzal, cu toate că îndepărtarea completă nu este întotdeauna posibilă. Corticosteroizii sistemici reprezintă singurul tratament farmacologic al bolii, dar nu modifică prognosticul pe termen lung, care este nefavorabil, putând duce la leziuni ireversibile pulmonare sub formă de fibroză sau emfizem, insuficiență respiratorie şi chiar deces.
Introducere
Pneumonita de hipersensibilitate (PH) este termenul preferat în prezent pentru a desemna boala anterior cunoscută ca alveolită alergică extrinsecă. PH este un sindrom care implică parenchimul pulmonar și în mod specific alveolele, bronhiolele terminale și interstiţiul alveolar, fiind cauzat de o reacție de hipersensibilitate de tip întârziat. O astfel de reacție este determinată de inhalarea repetată și prelungită a diferite tipuri de pulberi organice sau alte substanțe la care pacientul este sensibilizat, în principal din substanţe organice de origine animală sau vegetală, mai rar produse chimice anorganice. Adesea, această afecţiune apare ca urmare a expunerii profesionale, categoriile profesionale la risc fiind lucrători în medii contaminate cu praf organic de diferite origini, în special fermieri sau crescători de animale. O multitudine de substanțe pot determina sensibilizare şi pot conduce la PH, cum ar fi praful aviar, praful de fân, mucegaiurile, ciupercile, urina de șobolan sau alte rozătoare, tutunul, rumeguşul, praful de plută, reziduuri din plastic, rășini epoxidice, detergenți enzimatici. Sindromul este foarte variabil în ceea ce priveşte severitatea simptomelor, prezentarea clinică și prognosticul, în funcție de natura agentului cauzal, durata expunerii, factorii ce ţin gazdă și de caracteristicile antigenului.Epidemiologie
Pneumonita de hipersensibilitate este o boală rară. Un studiu epidemiologic american care a estimat incidența anuală a bolilor pulmonare interstiţiale la 30/100000 a găsit că PH reprezintă 2% din aceste cazuri. Studii din ţări europene au relevat însă o proporţie mai mare a PH în cadrul bolilor interstiţiale pulmonare, respectiv între 4% şi 15%. Studiile epidemiologice care să aprecieze corect prevalența PH în Europa sunt însă dificil de realizat, deoarece criteriile de diagnostic nu sunt universal acceptate şi urmate, precum şi din cauza diferenţelor geografice, incluzând clima şi practicile agricole, care pot diferi mult de la o ţară la alta. În România, nu avem disponibile date epidemiologice pentru PH.
Mecanism fiziopatologic
Pneumonita de hipersensibilitate este o afecţiune imunopatologică la indivizi susceptibili, în care leziunile de la nivel pulmonar apar ca rezultat al unor reacţii imunologice complexe atât de tip celular, cât şi umoral. Baza genetică a PH este incomplet înţeleasă în prezent şi, deşi unele studii sugerează că polimorfisme genetice din cadrul antigenului leucocitar uman (HLA) de clasa a II-a cresc riscul pentru PH în anumite populații (de exemplu, în Japonia), nu au fost identificaţi factori genetici asociaţi în mod constant cu boala.
Antigene inhalate cu diametrul mai mic de 5 µm pot ajunge la parenchimul pulmonar, trecând de vasele limfatice, și se pot depune la nivelul bronhiolelor respiratorii. În cazul în care sunt expuși la agenți capabili de a induce PH, cei mai mulţi indivizi dezvoltă toleranță imunologică, iar inhalarea antigenului poate duce la o creștere ușoară a limfocitelor locale, fără semnificație clinică. La indivizii susceptibili însă, inhalarea antigenului nu este urmată de inducerea toleranței, ci de declanşarea unor reacţii imunologice.
Agenţii patogeni implicaţi în PH, deşi extrem de diverşi ca structură biologică şi chimică, determină caracteristici clinice similare, cu o implicare aproape exclusivă a căilor respiratorii distale, cu infiltrare interstițială şi alveolară, cu celule inflamatorii și titruri mari de anticorpi serici precipitanţi (precipitine) împotriva antigenelor responsabile de inflamaţia alveolară, cu niveluri normale de IgE serice și eozinofile. Patogeneza PH este destul de uniformă, indiferent de agentul cauzal: răspunsul inflamator al mucoasei alveolare este o reacție de hipersensibilitate de tip III (mediată prin complexe imune) şi/sau de tip IV (mediată de limfocite T).
În PH acută, inflamația parenchimului pulmonar pare a fi mediată în principal printr-o reacţie de hipersensibilitate de tip III, așa cum este sugerat de prezența unor titruri mari de anticorpi precipitanţi de tip IgG antigen-specifici și de o creștere a neutrofilelor pulmonare. Formele subacută și cronică de PH sunt caracterizate printr-un răspuns imun mediat de celulele T, cu creșterea migrației limfocitelor T și dezvoltarea unei alveolite limfocitare T caracteristice. Reacţia de hipersensibilitate întârziată (de tip IV), mediată de limfocitele T, este un alt important mecanism imunologic din patogeneza PH. Rețeaua de citokine secretate de celulele T helper 1 joacă un rol-cheie în dezvoltarea PH de tip acut, iar mai târziu, în forma cronică, se dezvoltă un răspuns imun de tip T helper 2. De fapt, caracteristicile asociate cu PH cronică includ o creștere treptată a celulelor T CD4+ și a raportului CD4+/CD8+, cu o modificare spre diferenţierea celulelor T helper 2 și a profilului lor de citokine, precum și o scădere a celulelor T CD8+, ceea ce conduce la fibroză pulmonară. Inhalarea cronică a antigenelor aerosolizate determină şi acumulare de celule T helper 17, care pot contribui la dezvoltarea fibrozei pulmonare (prin promovarea depunerilor de colagen), așa cum s-a arătat prin efectul protector al depleției de IL-17.
Aspectul histopatologic este caracterizat printr-o infiltrare bronhiolocentrică cu celule mononucleare interstițiale, mici granuloame non-necrotizante formate din celule epitelioide, pneumonită celulară difuză şi grade variabile de fibroză pulmonară. Granuloamele au fost observate în mod obișnuit în peretele bronhiilor și în alveole în pneumonita de hipersensibilitate subacută; acestea sunt mai mici de 150 µm în diametru, mai mici decât cele observate în sarcoidoză. Precipitinele împotriva antigenului cauzal și depozite de imunoglobuline și complement au fost identificate în pereții vaselor.
Agenţi cauzali
Mai mult de 200 de antigene au fost identificate ca agenți cauzali pentru PH. Majoritatea antigenelor cauzale ale PH sunt derivate din fungi, bacterii, protozoare și proteine animale, ori sunt compuși chimici cu greutate moleculară mică. PH a fost clasificată în trecut ca o boală profesională, deoarece cele mai multe cazuri au fost înregistrate la expunerea la locul de muncă la antigeni specifici pentru acel mediu (plămânul fermierului, suberoza, plămânul crescătorului de păsări etc.). În timp însă s-a observat că şi expunerea la antigene obişnuite în mediul de la domiciliu poate duce la apariţia PH, în condiții de viață comune, în cazuri individuale. Noi surse de particule organice din aer sunt recunoscute în fiecare an drept agent cauzal pentru PH.În tabelul 1 se regăsesc o parte din antigenele cauzale ale PH, sursa lor şi boala determinată.
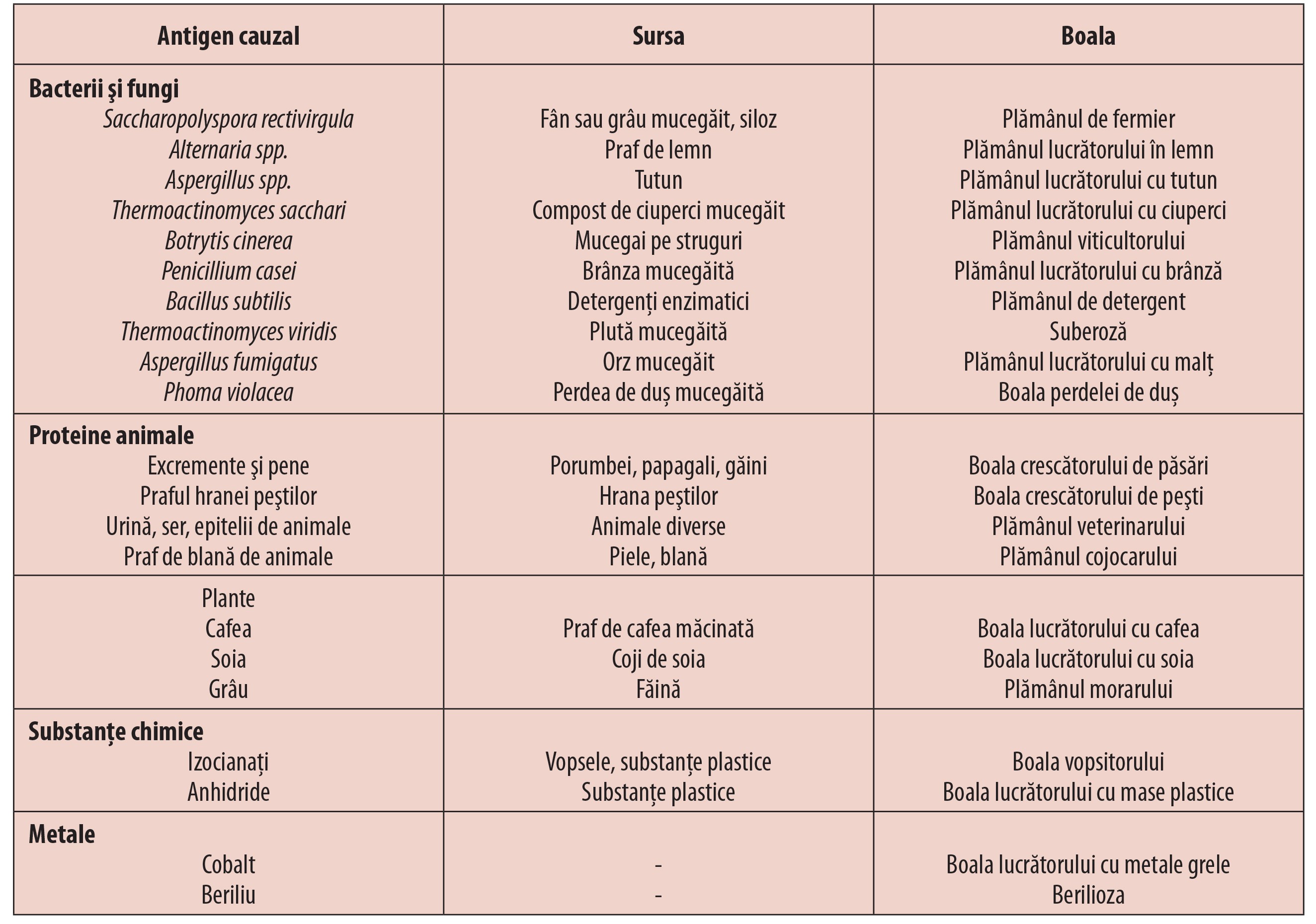
Tablou clinic
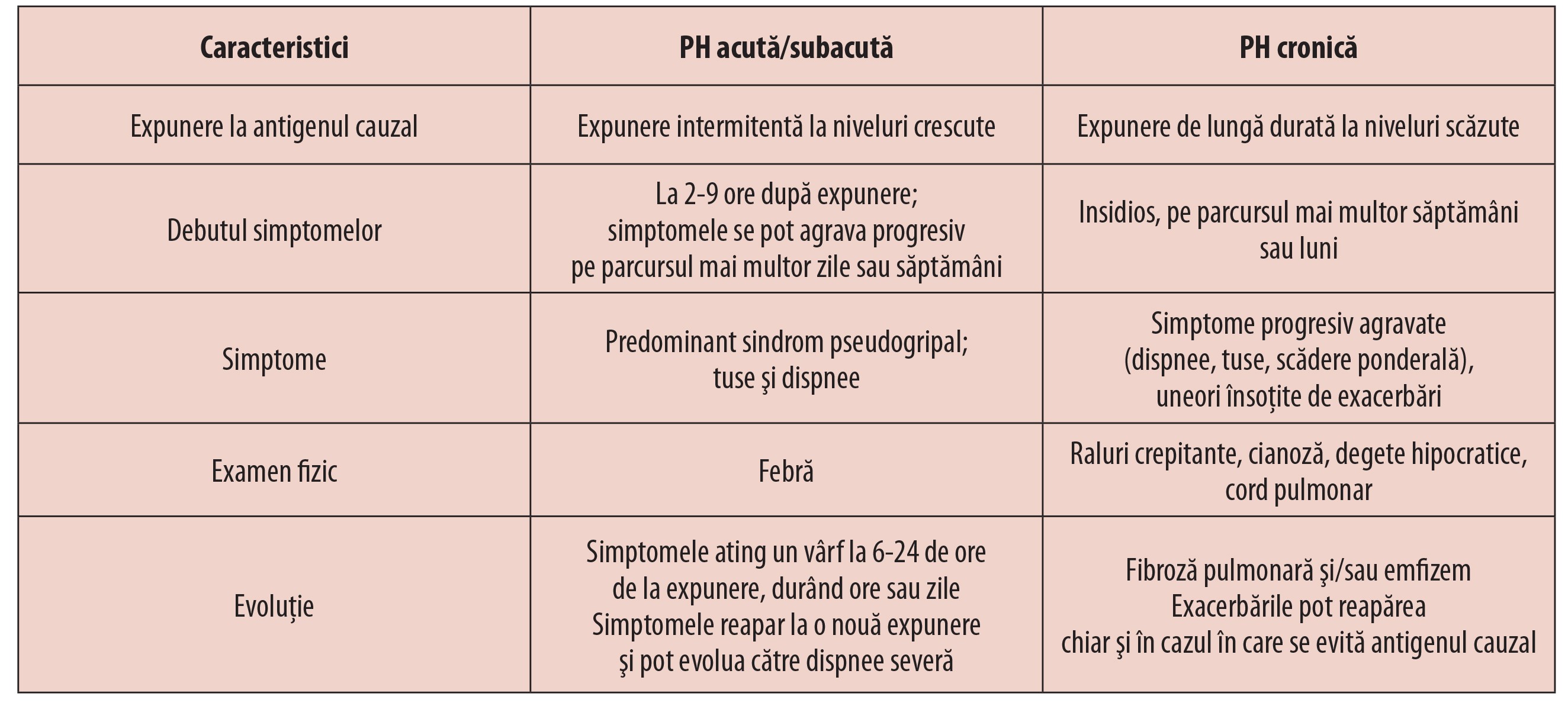
Din punct de vedere clinic, PH poate fi clasificată în acută/subacută sau cronică, în funcție de intensitatea și frecvența expunerii la antigenele cauzale. În tabelul 2 sunt rezumate principalele caracteristici ale formelor clinice de PH.
- PH acută apare după câteva ore sau zile de expunere la antigen, la expunerea intermitentă şi pe termen scurt. Simptomele pacientului încep cu febră, tuse, dispnee, astenie și stare generală alterată, care pot persista timp de aproximativ o săptămână după ce se termină expunerea la agentul cauzal. Exacerbările ar putea coincide cu revenirea la locul de muncă și dispar atunci când pacientul este departe de mediul profesional sau de locul unde a fost expus la alergen pentru o perioadă suficientă. La auscultaţia pulmonară pot fi remarcate raluri crepitante în ambele câmpuri pulmonare, dar uneori examenul clinic pulmonar poate fi normal. Manifestările radiologice ale PH acute sunt cele de edem pulmonar acut şi se indică efectuarea tomografiei computerizate (CT) pentru a evalua mai bine acești pacienți. Examenul CT de înaltă rezoluţie ar putea arăta opacități difuze bilaterale în geam mat și, în special în formele subacute, noduli centrolobulari prost delimitaţi și zone lobulare de opacitate. Opacităţile în geam mat reflectă în primul rând o pneumopatie interstițială limfocitară difuză, în timp ce nodulii centrolobulari slab delimitaţi pot fi cauzaţi de bronşiolita celulară sau de zone focale de organizare pneumonică. În timpul episodului acut, funcția respiratorie este redusă, cu alterarea capacităţii de difuziune a monoxidului de carbon (DLCO). Analizele de laborator pot prezenta o ușoară eozinofilie, cu niveluri normale de IgE.
- PH subacută este un fenotip deosebit de dificil de identificat, cauzat de o expunere mai îndelungată la agentul cauzal comparativ cu forma acută. Debutul este insidios din punct de vedere clinic, cu tuse productivă, dispnee şi astenie. În rest, forma subacută nu este foarte diferită de forma acută.
- PH cronică apare ca urmare a unei expuneri continue la agentul patogen, provocând o inflamaţie constantă ce determină în timp fibroză pulmonară ireversibilă. Forma cronică are un debut mai insidios decât cea subacută, evoluând pe o perioadă de luni sau ani, cu dispnee progresivă şi episoade recurente de wheezing şi febră. Simptomele, urmate în timp de o insuficiență respiratorie, conduc de cele mai multe ori la fibroză pulmonară. Radiografia pulmonară arată o fibroză interstițială difuză; spirometria demonstrează un sindrom restrictiv, uneori asociat cu obstrucţie. DLCO este foarte scăzută. În forma cronică, mai multe luni de expunere la un nivel scăzut la alergen pot conduce la simptome respiratorii foarte insidioase, cu dispnee, tuse productivă cu spută (uneori mucopurulentă), anorexie şi pierdere în greutate. Modelul formei cronice poate fi similar cu alte forme de boli pulmonare fibrotice, evoluând în cele mai multe cazuri spre o boală progresivă și ireversibilă, în pofida evitării expunerii la agentul cauzal şi a tratamentului cu corticosteroizi sistemici.
Diagnostic
Pneumonita de hipersensibilitate este de multe ori nerecunoscută şi în mod frecvent diagnosticată greşit ca infecție respiratorie sau boală pulmonară interstițială idiopatică, din cauza incidenței sale relativ scăzute în populația generală. Mai mult decât atât, variabilitatea largă în prezentarea clinică a bolii duce de multe ori la subdiagnosticare, cu excepția cazului în care medicul o ia în considerare în mod specific ca pe o posibilitate de diagnostic. La unii pacienți, simptomele respiratorii sunt principala caracteristică a prezentării clinice, în timp ce, la alte persoane, manifestările sistemice, cum ar fi anorexia şi pierderea în greutate, sunt în primul plan şi umbresc simptomele respiratorii, care sunt intermitente, corespunzând expunerilor episodice la agentul cauzal sau chiar lipsesc în forma cronică a bolii.Diferite criterii de diagnostic au fost propuse pentru PH, dar niciunul dintre acestea nu a fost validat. Ca atare, diagnosticul se bazează pe integrarea unei varietăți de factori, inclusiv antecedente de expunere la antigen, anticorpi precipitanţi la antigenul incriminat, caracteristici clinice, proba de provocare inhalatorie, lavaj bronhoalveolar și modificări radiologice şi morfopatologice.
Un indice ridicat de suspiciune și o anamneză atentă, realizată într-un mod sistematic pentru a se asigura că sunt obținute toate informațiile relevante privind mediul și locul de muncă, sunt cheile principale pentru a face un diagnostic corect al PH. Odată ce suspiciunea de PH apare pe baza istoricului, investigaţiile ulterioare trebuie să vizeze nu numai identificarea agentului cauzal, dar şi stabilirea unei relații temporale între expunerile de mediu și debutul inițial al simptomelor. Diagnosticul este suspectat de multe ori atunci când există dovezi ale unei boli respiratorii, cu un istoric relevant de expunere la locul de muncă sau în alt mediu și o relație temporală clară între simptome și expunere.
Examenul fizic şi testele de laborator de rutină nu sunt, în general, de ajutor; ele pot evidenţia IgG crescute, factor reumatoid pozitiv, cu eozinofile periferice şi niveluri serice ale IgE în general normale. Agentul cauzal suspectat poate fi identificat cu dozarea anticorpilor precipitanți specifici în serul pacientului, însă precipitinele specifice pot să fie absente la unii pacienţi cu PH, din cauza sensibilității scăzute a acestui test. Sensibilitatea scăzută a determinărilor serice ale precipitinelor antigen-specifice poate fi determinată de mai mulţi factori: antigene slab purificate, concentrarea inadecvată a serului pacientului înainte de testare sau lipsa agentului cauzal în panelul de testare. Mai mult decât atât, trebuie subliniat faptul că până la 40-50% dintre persoanele asimptomatice expuse la același antigen pot avea anticorpi serici IgG specifici, însă aceştia nu au neapărat semnificaţia bolii.
La pacienții cu suspiciune de PH, o anamneză atentă, referitoare la expunerea în mediu și la locul de muncă, ar trebui să ghideze utilizarea panelurilor de anticorpi precipitanți specifici, dar lipsa de consens cu privire la definirea bolii limitează posibilitatea de a ajunge la un anumit diagnostic. Cu toate acestea, au fost propuse mai multe criterii de diagnostic pentru PH. În scopul de a valida criteriile clinice de diagnostic pentru PH, în 2003, grupul de studiu al PH a identificat șase factori predictivi semnificativi:
- expunerea la un antigen cauzal cunoscut;
- prezența precipitinelor serice la antigenul cauzal suspectat;
- simptome respiratorii şi sistemice recurente;
- prezența ralurilor crepitante la auscultaţia pulmonară;
- simptome care apar la 4-8 ore după expunere;
- scădere ponderală.
În PH subacută se descriu micronoduli difuzi, zone de „geam mat“, zone de air-trapping şi modificări discrete de fibroză. În forma cronică de PH se pot observa modificări diverse: noduli centrolobulari, opacităţi difuze în „geam mat”, zone hipertransparente şi modificări importante de fibroză, incluzând bronșiectazii de tracţiune şi aspect de fagure de miere.
Alte investigaţii şi proceduri pot fi utile în diagnosticul PH, cum ar fi lavajul bronhoalveolar (LBA) şi biopsia pulmonară. Prezența unei proporţii de limfocite mai mare sau egală cu 25% în LBA sugerează o boală granulomatoasă, cum ar fi sarcoidoza sau PH, în timp ce un procent de limfocite mai mare de 50% este mai sugestiv pentru PH, mai ales atunci când este asociat cu un procent de neutrofile mai mare de 3% și cu un procent de mastocite mai mare de 1%. O predominanță a limfocitelor T CD8+ în LBA și un raport CD4+/CD8+ subunitar sunt adesea observate în PH, în timp ce un raport supraunitar este asociat cu sarcoidoza, ceea ce sugerează că acest raport ar putea fi utilizat pentru a diferenția PH de sarcoidoză. Studii recente sugerează că un raport CD4+/CD8+ subunitar este asociat cu forma cronică a PH, în timp ce o predominanţă a celulelor T CD4+ este mai frecvent întâlnită în faza acută a bolii.
Utilitatea biopsiilor transbronșice este limitată de obținerea unor rezultate nespecifice la până la 48% din probe; cu toate acestea, prezența unor anumite modificări, cum ar fi infiltratele limfocitare difuze, poate fi înalt sugestivă pentru PH. Biopsiile pulmonare chirurgicale sunt mai sensibile decât biopsiile transbronșice; în stadiul subacut al bolii, modificările histopatologice includ pneumonită interstițială limfoplasmocitară, celule gigante sau granuloame non-necrozante și bronșiolită celulară. În formele cronice ale PH apare un model predominant fibrotic similar unor alte tipuri de boli pulmonare interstițiale.
În concluzie, până în prezent nu avem disponibil niciun standard de aur pentru diagnosticarea pneumonitei de hipersensibilitate. Expunerea profesională sau de mediu la un agent cauzal cunoscut, simptomele recurente după expunere, ralurile crepitante, identificarea precipitinelor serice și, în cele din urmă, scăderea ponderală sunt constatări clinice orientative pentru PH, împreună cu LBA, HRCT și, dacă este necesar, alte proceduri de diagnosticare, cum ar fi biopsia pulmonară.
Tratament
Identificarea expunerii relevante și eliminarea antigenului cauzal au implicaţii prognostice şi terapeutice extrem de importante.Cea mai importantă intervenție în gestionarea PH este evitarea antigenului cauzal, dar eliminarea acestuia din mediu nu este întotdeauna posibilă, deoarece, în mod frecvent, el nu poate fi identificat sau evitarea completă poate însemna schimbări majore în ocupație, hobby-uri sau chiar în mediul casnic. Expunerea continuă conduce la riscul unei afectări pulmonare progresive.
În prezent, curele de corticosteroizi sistemici reprezintă intervenţia farmacologică de primă intenţie în PH atunci când există simptome și anomalii fiziologice, dar nu avem disponibile studii clinice randomizate controlate pentru prednison şi imunosupresoare la pacienţii cu PH fibrotică.
Cele mai bune dovezi disponibile vin dintr-un studiu randomizat, placebo-controlat, la pacienţi cu plămânul fermierului, care a demonstrat o ameliorare mai rapidă a funcţiei pulmonare cu corticosteroizi, în comparaţie cu măsurile de evitare a antigenului, dar nu au existat diferenţe în rezultatele pe termen lung între cele două grupuri. Un subgrup de pacienţi a dezvoltat fibroză progresivă chiar și după îndepărtarea antigenului cauzal. În aceste cazuri, cure prelungite de corticosteroizi sistemici (p.o.) sunt adesea necesare. De aceea, tratamentul fiecărui pacient trebuie să fie individualizat. Doza convențională pentru corticosteroizi pe cale orală este de 0,5-1 mg/kg/zi de prednison, timp de o lună, urmată de o reducere treptată până la o doză de întreținere de 10-15 mg/zi. La pacienții cu tuse, wheezing sau disfuncţie ventilatorie obstructivă, utilizarea de bronhodilatatoare și corticosteroizi inhalatori este eficientă. În funcție de caracteristicile clinice ale pacientului, pot fi prescrise şi terapii de susţinere, cum ar fi terapia cu oxigen, dacă saturația de oxigen din sânge este permanent sub 90%, sau opioide pentru a controla dispneea sau tusea cronică refractară la alte tratamente.
În PH cronică progresivă pot fi adăugate la corticosteroizi medicamente imunosupresoare, dar, din nou, nu există studii clinice controlate disponibile pentru a sprijini această strategie. Recent, rituximabul (anticorp monoclonal anti-CD20) a fost utilizat ca tratament alternativ într-un caz de PH cronică progresivă, refractară la tratamentul convenţional.
Nu există deocamdată dovezi care să susțină prescrierea agenților antifibrotici (nintedanib și prifenidonă) în tratamentul PH cronice.
În cazurile de PH cronică progresivă, care nu răspund la corticosteroizi şi/sau terapie imunosupresoare, trebuie luat în considerare transplantul pulmonar, dar este important să menţionăm că procedura nu este curativă: dacă după transplant pacientul va fi expus din nou la antigenul cauzal, o nouă inflamaţie alergică poate afecta grav organul transplantat. Tratamentul are mai mult succes atunci când PH este diagnosticată în stadiile incipiente, înainte de a se produce leziuni pulmonare permanente și ireversibile.
Concluzii
Pneumonita de hipersensibilitate este un sindrom pulmonar complex, caracterizat prin inflamație difuză a parenchimului pulmonar și a căilor respiratorii, ca răspuns la inhalarea de antigeni la care individul a fost sensibilizat în prealabil. Boala are manifestări clinice caracteristice, dar şi suprapunere substanțială cu alte pneumopatii interstiţiale. Patogeneza bolii nu este încă pe deplin înțeleasă, iar identificarea și eliminarea agenților cauzali rămân piatra de temelie a tratamentului și un determinant major al prognosticului. În cele din urmă, și probabil cel mai important, PH cronică ar trebui să fie întotdeauna luată în considerare și exclusă înainte de a se pune un diagnostic de fibroză pulmonară idiopatică.Bibliografie
2. Pereira C.A., Gimenez A., Kuranishi L., Storrer K. Chronic hypersensitivity pneumonitis. Journal of Asthma and Allergy. 2016; 9:171-181.
3. Lacasse Y., Cormier Y. Hypersensitivity pneumonitis. Orphanet Journal of Rare Diseases. 2006; 1:25.
4. Lacasse Y., Selman M., Costabel U., Dalphin J.C., Ando M., Morell F., Erkinjuntti-Pekkanen R., Muller N., Colby T.V., Schuyler M., Cormier Y., H.P. Study Group Clinical diagnosis of hypersensitivity pneumonitis. Am J Respir Crit Care Med. 2003; 168:952-958.
5. Fink J.N., Ortega H.G., Reynolds H.Y., Cormier Y.F., Fan L.L., Franks T.J., et al. Needs and opportunities for research in hypersensitivity pneumonitis. Am J Respir Crit Care Med. 2005; 171:792-798.
6. Spagnolo P., Rossi G., Cavazza A., et al. Hypersensitivity pneumonitis: a comprehensive review. J. Investig Allergol Clin Immunol. 2015; 25(4):237-250.
7. Selman M., Pardo A., King T.E., Jr. Hypersensitivity pneumonitis: insights in diagnosis and pathobiology. Am J Respir Crit Care Med. 2012; 186(4):314-324.
8. Grunes D., Beasley M.B. Hypersensitivity pneumonitis: a review and update of histologic findings. J. Clin Pathol. 2013; 66(10):888-895.
9. Churg A., Sin D.D., Everett D., Brown K., Cool C. Pathologic patterns and survival in chronic hypersensitivity pneumonitis. Am J Surg Pathol. 2009; 33(12):1765-1770.
10. Costabel U., Bonella F., Guzman J. Chronic hypersensitivity pneumonitis. Clin Chest Med. 2012; 33(1):151-163.
11. Mohr L.C. Hypersensitivity pneumonitis. Curr Opin Pulm Med. 2004; 10:401-411.
12. Jacobs R.L., Andrews C.P., Coalson J.J. Hypersensitivity pneumonitis: beyond class occupational disease-changing concepts of diagnosis and management. Ann Allergy Asthma Immunol. 2005; 95(2):114-127.
13. Millerick-May M.L., Mulks M.H., Gerlach K.R., et al. Hypersensitivity pneumonitis and antigen identification - an alternate approach. Respir Med. 2016; 112:97-105.
14. Lima M.S., Coletta E.N., Ferreira R.G., et al. Subacute and chronic hypersensitivity pneumonitis: histopathological patterns and survival. Respir Med. 2009; 103(4):508-515.
15. Hanak V., Golbin J.M., Ryu J.H. Causes and presenting features in 85 consecutive patients with hypersensitivity pneumonitis. Mayo Clin Proc. 2007; 82(7):812-816.
16. Glazer C.S., Rose C.S., Lynch D.A. Clinical and radiologic manifestations of hypersensitivity pneumonitis. J. Thorac Imaging. 2002; 17(4):261-272.
17. Navarro C., Mejia M., Gaxiola M., et al. Hypersensitivity pneumonitis. Treat Respir Med. 2006; 5(3):167-179.
18. Oshimo S., Bonella F., Guzman J., Costabel U. Hypersensitivity pneumonitis. Immunol Allergy Clin North Am. 2012; 32(4):537-556.
19. Keir G.J., Maher T.M., Ming D., et al. Rituximab in severe, treatment-refractory interstitial lung disease. Respirology. 2013; 19(3):353-359.
20. Kern R.M., Singer J.P., Koth L., et al. Lung transplantation for hypersensitivity pneumonitis. Chest. 2015; 147(6):1558-1565.
Articole din ediţiile anterioare
Rolul şi importanţa medicului de familie în diagnosticul fibrozei pulmonare idiopatice
Fibroza pulmonară idiopatică reprezintă una dintre cele mai provocatoare boli pentru clinician. Este o formă specifică de pneumopatie interstiţială...
Tratamentul afectării pulmonare în sclerodermia sistemică
Sclerodermia este o boală a ţesutului conjunctiv cu etiologie şi patogenie complexe, incomplet cunoscută. Cea mai frecventă cauză de deces la pacie...