Haemolytic uremic syndrome (HUS) is a disease of the whole body, with damage in small blood vessels due to toxins (typical HUS). We design to introduce in discussion essential elements linked to this pathology for family practitioners. The types of HUS were reviewed by expert panels and a consensus in 2015 was presented the modern way of those modifications. Cases who present with diarrhea (epidemic) are called classic D + HUS. The etiology is bacterial (commonly E. coli secreting Shigatoxin) and other bacterial or viral infections, too. Pathological we have a blocking blood flow in the kidneys, clinical the most obvious and translated para-clinically by levels that shows acute renal failure, but besides kidney and intestines, any other organ may be affected by intravascular thrombosis leading to organ damage, which influences the mortality. Anemia is another important feature, with RBC modified by destruction. Therapy is closely linked to the need for dialysis, but there are cases that do well without an organ failure and a need for more complex therapies. Basic hygiene - washing vegetables, fruits and hands are the main methods to prevent this illness.
Sindromul hemolitic-uremic, date necesare practicianului
Haemolytic uraemic syndrome - data necessary to the practitioner
First published: 03 ianuarie 2016
Editorial Group: MEDICHUB MEDIA
Abstract
Rezumat
Sindromul hemolitic-uremic (SHU) este o afecțiune complexă a întregului organism, cu afectarea vaselor mici de sânge din cauza unei toxine (în cazul formei numite tipice). Etiologia este dată de germeni bacterieni (cel mai frecvent E. coli secretor de Shigatoxină), dar și de alte infecții bacteriene sau virale. În cazurile de epidemie, subtipurile de E. coli enteropatogene sunt cel mai des incriminate, afecțiunea fiind cu diaree, de unde și denumirea clasică D+ SHU . Ne propunem să prezentăm elementele esențiale pentru practician legate de această patologie. Tipurile și cauzele de SHU au fost revizuite de comisii de experți internaționali, iar în consensul din 2015 au fost prezentate variantele incriminate la ora actuală. Morfopatologic, avem o blocare a circulației sangvine la nivelul rinichilor, fiind cea mai evidentă clinic și tradusă paraclinic, prin valori ce dovedesc insuficiența renală acută, dar pe lângă rinichi, orice organ poate fi atins de trombozele intravasculare ducând la afectarea multiplă, ce influențează negativ mortalitatea. Anemia cu eritrocite rupte este o caracteristică de bază a diagnosticului pentru această microangiopatie. Terapia este în principal suportivă, dar strâns legată cu necesitatea dializei, unele cazuri evoluând bine, fără a necesita terapii complexe. Regulile de igienă de bază - spălatul legumelor, fructelor consumate și a mâinilor ar fi principalele metode de prevenire a îmbolnăvirii.
Introducere
Sindromul hemolitic-uremic este o boală ce atinge întregul organism, produsă prin afectarea vaselor mici de sânge, din cauza efectului unei toxine. Primul caz a fost descris de Gasser în 1955. În literatură, acronimele SHU (sindrom hemolitic-uremic) și PTT (purpura trombocitopenică trombotică/idiopatică) au fost frecvent folosite alternativ pentru boli cu caractere similare. Acest lucru a provocat confuzie deseori în trecut, ducând la multe discuții în lumea medicală. Din punct de vedere istoric, definirile sindromului hemolitic-uremic și ale PTT s-au bazat pe criteriile clinice ale HUS, clasică fiind triada clinică ce cuprinde insuficiența renală acută, anemia hemolitică microangiopatică și trombocitopenia; iar PTT are caracteristici suplimentare, care sunt febra și semnele neurologice(1,2). Cu toate acestea, la mulți pacienți cu febră, cu diagnosticul de SHU, există semne neurologice care sunt evidente. Modificarea patologică - microangiopatie trombotică, leziune ocluzivă arteriolo-capilară prin formare de trombi din plachete ori fibrină și/sau modificări ale intimei vasului. Totuși, recunoaștem că există o mare suprapunere a celor două definiții. O diferență majoră este cea legată de vârstă. În general, pacienții cu caracteristici clinice ale SHU sunt mai tineri (de la 1 la 5 ani), în timp ce pacienții cu PTT tind să fie majoritar de vârstă adultă (20-40 de ani). Este extrem de important ca diagnosticul diferențial dintre cele două etiologii să fie făcut cât mai rapid, metodele terapeutice cu care se poate interveni fiind diferite.
Concepte de etiologie și patogeneză
Cu toate că este de la sine înțeles că, în fiecare caz de SHU sau PTT, etiologia și patogeneza sunt individualizate, într-o mare măsură, ele determină evoluția clinică, existând o stufoasă literatură medicală care confirmă acest lucru. De exemplu, forma frecventă în copilărie - cea de SHU, precedată de diaree (așa-numita SHU diaree-pozitivă, adică D+SHU) - este strâns legată de verocitotoxină (sinonime sunt toxina Shiga sau toxina Shiga-like), care este produsă de o infecție cu anumite tipuri de Escherichia coli (E. coli). Aceasta este de obicei o afectare de scurtă durată, care are o evoluție relativ benignă și nu există nici o recidivă sau sechelaritate marcantă. Prin contrast, SHU cu componenta genetică, care asociază mutații în cascada complementului, are un prognostic modest și un risc destul de frecvent de recidivă și de pierdere (prin rejet) a grefei după transplant(1-6).
În practica clinică, adesea, în afară de câteva subgrupuri bine definite, etiologia și patogeneza afecțiunii rămân neexplicate. Aceasta se datorează parțial etiologiei ce nu a fost investigată pe deplin sau pentru că investigațiile necesare s-au dovedit indisponibile în afara unui cadru oferit doar în centrele de cercetare (mai ales pentru cele D-). În acest moment, la nivel european, precum și internațional, există grupuri de lucru care au înființat registre de boli pentru cazurile din copilărie cu SHU și încurajează gruparea a cât mai multor centre ce raportează aceste cazuri.
SHU produsă de agenți infecțioși este o cauză relativ comună de insuficiență renală acută la copii și duce la o morbiditate și o mortalitate semnificativă, chiar în timpul fazei acute a bolii. În plus față de morbiditatea și mortalitatea care nu sunt de neglijat, complicațiile renale și extrarenale pe termen lung pot apărea la un număr important de copii, imediat după episodul acut de SHU. Agentul infecțios cel mai comun care cauzează SHU este E. coli enterohemorhagic, care produce toxina Shiga (EHEC ).
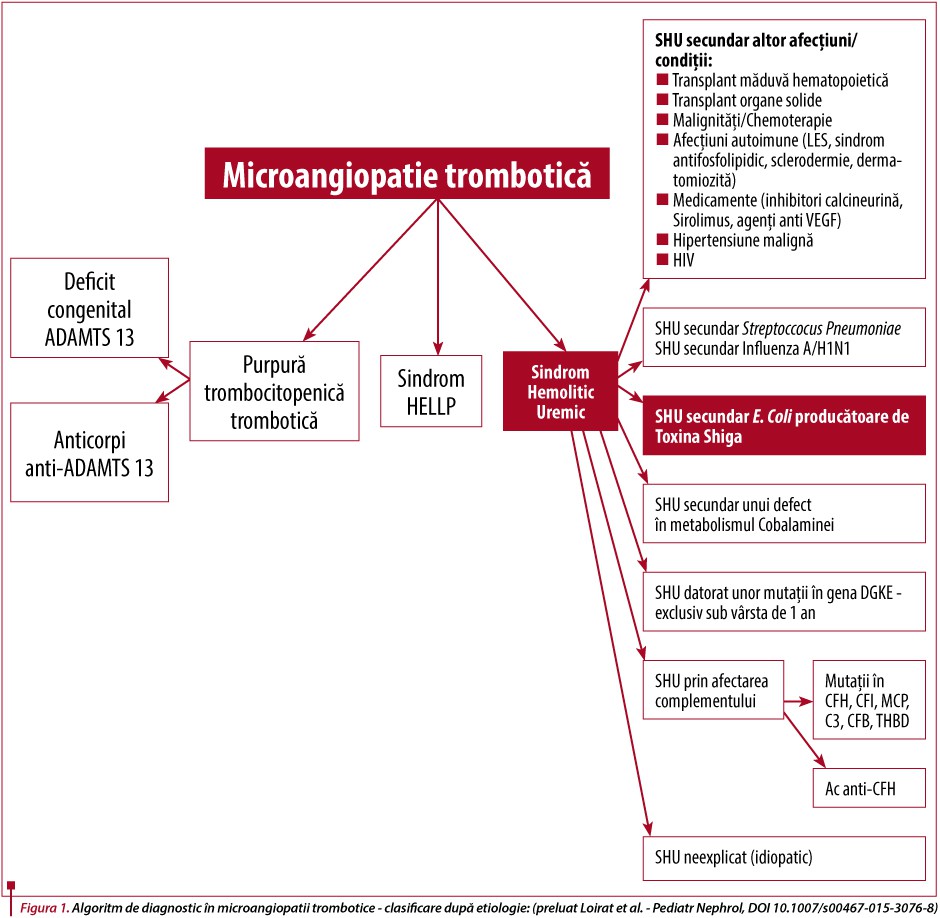
Așa cum este descris mai jos, SHU poate apărea și după infecții cu Streptococcus pneumoniae (în situațiile de septicemie cu pneumococ); chiar poate fi în mod particular sever și are o mai mare mortalitate și morbiditate, dar poate fi secundar și altor infecții bacteriene sau virale. D+SHU sau SHU tipic a fost legat de infecția cu E. coli producătoare de toxină Shiga, fapt dovedit la începutul anilor ’80 de Karmali. Această clasificare pe care o folosim și noi, fiind clasică, ce leagă D+ sau D- de SHU și are legătură cu prezența sau absența diareei, nu se mai recomandă a fi folosită, acest simptom nefiind definitoriu pentru tipul de sindrom hemolitic-uremic, după consensul din 2014 (figura 1).
Epidemiologie
Manifestările clinice clasice ale SHU includ triada anemie hemolitică microangiopatică, trombocitopenie și insuficiență renală acută. Cu toate acestea, studiile epidemiologice efectuate în focarele de enterocolită hemoragică și D+SHU au arătat în mod clar că unii pacienți dezvoltă anemie hemolitică și/sau trombocitopenie cu puține elemente de afectare renală, în timp ce alți copii dezvoltă afectare renală substanțială, dar cu număr de trombocite nemodificat.
În 1993, un focar în vestul Statelor Unite ale Americii a dus la mai multe cazuri de SHU severă cu complicații, apoi alte 11 cu complicații extrarenale în 1996. Peste 5.000 de elevi japonezi au fost infectați cu E. coli producătoare de verocitotoxină, un focar în Scoția a determinat 20 de decese și un alt focar în SUA a fost cauzat de un suc de mere contaminat, iar în studiile de caz controlate, consumul de hamburger și/sau consumul de carne nepreparată corespunzător sau semipreparată a fost asociat cu toxina Shiga produsă de infecția cu E. coli enterohemoragic (EHEC). Cu toate că în SUA hamburgerul de vită preparat insuficient a fost cel mai comun vector de transmitere a infecției EHEC în trecut, sucul de mere, varza, părți de ridiche (dar și alte legume - vezi cazurile din Germania ultimilor ani) și cârnații, precum și alte surse de proveniență alimentară au fost, de asemenea, implicate în răspândirea toxinei produse de E coli. În timp ce epidemiile sunt notabile, majoritatea cazurilor de SHU datorate E. coli sunt sporadice, fără identificarea unei surse specifice pentru toxina Shiga.
Într-o studiu canadian prospectiv efectuat la copii, dintr-un număr total de 136 de cazuri, toate cuprinzând copii cu vârsta de peste 2 ani, 121 au fost endemice, în timp ce doar 15 au fost epidemice. Incidența anuală în acest studiu a fost de 1,11 cazuri la 100.000 de copii sub vârsta de 16 ani, fiind bine documentate prospectiv, multicentric. Un alt studiu prospectiv efectuat în Germania și Austria a implicat 394 de copii, incidența SHU fiind de 0,7 la 100.000 și de 0,4 la 100.000 de copii sub 15 de ani(7,8).
Motivul incidenței variabile în diferite regiuni este neclar, dar poate fi legat de expunerea la EHEC și potențiale susceptibilități genetice ale populației(9).
În timp ce consumul de produse alimentare contaminate este cel mai frecvent mecanism de expunere la toxina Shiga din E. coli, există o posibilitate redusă ca transmiterea să se facă de la persoane infectate, debutul simptomelor concomitent sugerând o expunere comună, în timp ce debutul simptomelor în timp de mai multe zile sugerând infectare unul după altul, mai târziu sau mai repede. Deși transmiterea a fost citată și de la mame la copil!
Rezervorul de E. coli secretor de toxină sunt animalele domestice (copitate), dar și unele animale sălbatice - sursa principală sunt legumele contaminate, fructele, carnea și apa contaminată; foarte rar se transmite de la om la om, dar nu este exclus. O157:H7 este serotipul cel mai frecvent implicat în infecție producătoare de toxină Shiga din Statele Unite și Europa. Tulpini care nu sunt H7 sunt în curs de descoperire. La cei din studiul european prospectiv de 394 de copii descris mai sus, serotipurile diferite de O157:H7 au fost detectate la 43% din probele din scaun de la pacienții cu HUS; O26 a fost detectat la 15%, O157-legat de sorbitol a fost detectat la 10%, O145 la 9%, O103 în 3%, iar O111 și O104 au fost și ele prezente.
Odată ce o persoană este infectată cu E. coli de aceste tipuri, ea va produce toxina Shiga, dar procentul de pacienți care trec la SHU manifest variază de la aproximativ 5% până la 15%. La copiii sub 5 ani, procentul celor care dezvoltă anemie hemolitică sau SHU a fost de 12,9%, comparativ cu 6,8% și 8% pentru copiii cu vârsta cuprinsă între 5 până la 9,9 ani și peste 10 de ani. S-a încercat găsirea unei corelații între numărul de leucocite și riscul de a dezvolta SHU în cazul unei diarei: copiii cu leucocitele peste 13.000/mm3 în primele 3 zile de boală cu E. coli producătoare de toxină Shiga au avut o creștere de șapte ori a riscului de a dezvolta SHU, comparativ cu restul. Utilizarea agenților antimotilitate intestinală a fost, de asemenea, asociată cu un risc mai mare de dezvoltare a SHU. Sunt multipli alți factori discutați în literatură care pot avea influență asupra evoluției SHU (antibioticele administrate rapid - se pare că anumite antibiotice, și aici ciprofloxacina este principalul antibiotic incriminat, cresc transcripția de toxină, fluidele IV în cantitate mare etc.), dar care nu au convins comitetele ce studiază afecțiunea să fie introduse ca unele criterii valide în recomandări.
Din experiența noastră publicată sau comunicată în diferite ocazii, 49 de cazuri (43 la București și 6 la Timișoara) au fost depistate cu acest diagnostic în ultimii 15 ani, vârstele fiind de la 1 la 17 ani. Majoritatea celor din Capitală sunt din categoria cazurilor cu diaree, iar la cele din vestul țării formele denumite atipice au dominat.
Manifestările clinice
Odată ce o persoană este expusă la E. coli producătoare de toxina Shiga, simptomele diareei apar de obicei la 3 până la 7 zile după contactul infectant, iar diareea devine sângerândă la cea mai mare parte a copiilor. Alte simptome întâlnite sunt durerile colicative (crampe) abdominale, care pot fi destul de severe. La copiii care dezvoltă SHU, diareea începe să dispară în momentul în care aceștia încep să devină anemici (palizi) și scăderea cantității de urină (oliguria) poate fi notată. Manifestările majore ale SHU includ triada trombocitopenie, anemie hemolitică microangiopatică și insuficiență renală acută. Anemia hemolitică este Coombs negativă și schizocitele sunt prezente pe frotiul periferic din sânge. De asemenea, scăderea haptoglobinei este notabilă, dar nespecifică, rinichii și tractul gastrointestinal sunt organele cel mai frecvent afectate în SHU, dar și atingerea sistemului nervos central (SNC) poate fi întâlnită. Colita severă poate duce la necroză transmurală, cu perforație și/sau dezvoltarea ulterioară a stricturilor. Creșterea enzimelor pancreatice poate fi întâlnită, în special ca reacție pancreatică, iar semne de pancreatită severă pot fi detectate prin ecografie sau CT. Manifestarea extrarenală principală este prezența de microtromboze în diverse organe, care poate duce la leziuni ischemice grave. Implicarea sistemului nervos central în SHU tipic este mai rară, dar atunci când apare, se prezintă cu letargie, iritabilitate, convulsii. În cazurile mai severe, afectarea SNC duce la pareză, edem cerebral sau chiar stare de comă. Implicarea miocardului e posibilă. Având în vedere faptul că microangiopatia poate apărea în orice organ, literatura a mai descris afectări pulmonare, oculare, musculare și cutanate.
Mortalitatea SHU este raportată a fi între 3% și 5%, iar decesul din cauza SHU este aproape întotdeauna asociat cu boli extrarenale severe, inclusiv cea a SNC.
În timpul fazei acute a SHU, secțiuni ale rinichiului examinate morfopatologic arată o afectare microvasculară caracterizată prin depunerea unor microtrombi și, asociat, modificări ale celulelor endoteliale glomerulare, distruse și infiltrate. Modificări patologice similare au fost descrise în alte organe, inclusiv colon, pancreas, mușchiul scheletic și miocardic, dar și SNC. Aceste cercetări demonstrează că SHU este o boală sistemică fiind caracterizată prin lezarea celulelor endoteliale, rolul toxinei Shiga în medierea procesului fiind cert.
Complicațiile pe termen lung - sechelaritate
Progrese tehnice în terapia prin dializă și a îngrijirii mai bune în sectorul de terapie intensivă a copilului în stare critică au dus la o reducere semnificativă a mortalității acute prin SHU, astfel încât complicațiile cronice la supraviețuitorii pe termen lung sunt din ce în ce mai întâlnite.
Biopsiile renale efectuate la copii cu antecedente de SHU și proteinurie reziduală au demonstrat că majoritatea acestora au scleroză globală și segmentară cu fibroză interstițială, sugerând că acești copii sunt la risc pentru dezvoltarea ulterioară a insuficienței cronice. În plus, determinarea ambulatorie a tensiunii arteriale în scopul monitorizării a atestat anormalități la copii cu istoric de SHU.
O metaanaliză a demonstrat că decesul sau progresia spre stadiul final de boală renală este prezent la 12% dintre copiii cu diaree asociată SHU, iar 25% dintre supraviețuitori prezintă sechelaritate pe termen lung. Tratamentul modern cu IECA a sechelelor după SHU poate ajuta la conservarea funcției renale.
Managementul și intervenția în D+HUS
În cazul în care un pacient se prezintă cu anemie, trombocitopenie și afectare renală, diagnosticul de microangiopatie trombotică trebuie suspectat, iar tratamentul, orientat spre acest diagnostic. Trebuie efectuate testele necesare pentru confirmarea anemiei hemolitice cu test Coombs negativ, haptoglobină mult scăzută, lactico-dehidrogenază crescută semnificativ și prezența eritrocitelor rupte (numite divers - în cască, fragmente, schizocite), trebuie confirmat numărul scăzut de trombocite și măsurată atent funcția renală prin diureză orară, dar și biomarkeri sangvini (uree, creatinină, acid uric). De reținut că triada de evenimente poate apărea în decurs de câteva zile și că, la început, pot să nu fie toate prezente deodată. După confirmarea SHU, în toate cazurile, trebuie determinată etiologia și efectuat diagnosticul diferențial.
Terapii:
Majoritatea copiilor cu SHU dezvoltă un anumit grad de insuficiență renală și aproximativ două treimi dintre copiii cu SHU vor necesita terapie prin dializă, în timp ce aproximativ o treime va avea afectare renală mai ușoară, fără a fi nevoie de terapie de epurare.
Problemele specifice de gestionare a SHU includ managementul complicațiilor hematologice ale SHU, monitorizarea pentru atingerile extrarenale din SHU, evitând medicamente antidiareice, antimotilitate, dar și evitând, eventual, și terapia cu antibiotice (controversată). Managementul complicațiilor hematologice ale SHU, inclusiv anemia hemolitică și trombocitopenia, ar trebui să mai presupună analize amănunțite de laborator, pentru că unii copii prezintă anemie strict din cauza hemolizei rapide. Se poate dezvolta icter în urma procesului hemolitic, caracterizat printr-o creștere a bilirubinei indirecte. Este necesară transfuzia de masă eritrocitară când hemoglobina scade rapid și/sau în cazul în care hemoglobina a atins nivelul de 6-7 g/dl. Pot fi utilizate tratamente cu diuretice în caz de suprasarcină de volum, cu monitorizarea atentă a tensiunii arteriale și respiratorii, precum și a cantității de urină.
Trombocitopenia poate fi severă, dar administrarea de masă trombocitară este de obicei limitată la copilul care are nevoie de o procedură chirurgicală sau la copilul cu hemoragie masivă. Riscul de tromboză este temerea.
Rinichiul și tractul gastrointestinal sunt organele cel mai frecvent afectate în SHU, dar și alte organe sunt atinse într-un număr considerabil de cazuri. Este foarte important să se evalueze prezența și gradul de atingere extrarenală, pentru a trata corespunzător, deoarece aceste complicații extrarenale contribuie la creșterea mortalității prin SHU.
Tratamentul antibiotic și forme mai rare
Unele studii au demonstrat efectele nocive ale terapiei cu antibiotice în colita hemoragică. Copiii cu infecție producătoare de toxină Shiga (E. coli) care au primit tratament cu antibiotice au fost mai susceptibili de a dezvolta SHU grav, comparativ cu copiii care nu au primit antibiotice(10). Alte studii nu au demonstrat o astfel de asociere, iar recent o metaanaliză a concluzionat că administrarea antibioticelor la persoanele infectate cu toxina Shiga nu a fost asociată cu dezvoltarea de HUS(11,18). Studiile in vitro au arătat însă faptul că unele antibiotice promovează producția și eliberarea de toxină Shiga. În prezent, nu există un consens cu privire la utilizarea terapiei cu antibiotice la copiii cu colită hemoragică sau SHU(12-18).
O formă rară de SHU poate să apară ca urmare a unei infecții invazive cu S. pneumoniae. Infecția precedentă este de obicei severă, iar copiii se pot prezenta cu septicemie, meningită și/sau pneumonie cu empiem(19-23).
SHU asociat cu Shigella dysenteriae a apărut în India și în Africa. Acesta este, de obicei, complicat de dizenterie severă și colaps cardiovascular și are o rată de morbiditate și mortalitate mai mare decât SHU asociat cu E. coli(25,26,27).
SHU a fost, de asemenea, raportat după Entamoeba histolytica intestinală și, de asemenea, în asociere cu infecția cu HIV și HTLV-1(28-29).
Câteva concluzii
Aceste date pot fi utile înțelegerii SHU tipic, dar formele actualmente discutate des ca terapie după consensul de anul trecut (Loirat et al. în Pediatr. Nephrol, vezi clasificarea din figura 1) și alăturate încercărilor noastre de diagnostic și tratament(30) sunt cele legate de formele atipice (secundare sau asociate). Foarte importantă, chiar esențială la noi, este elaborarea de strategii pentru prevenirea infecției cu E coli și producerea de SHU, prin începerea unei campanii de educare a populației în privința igienei mâinilor. Inclusiv unele programe ale Ministerului ar trebui să încurajeze spălatul mâinilor mai des, dar și cel al alimentelor, mai ales vegetale ce au frunze ori cele ce vin în contact cu solul și dejecțiile unor animale. Din punct de vedere medical, informarea corectă și educația rețelei primare sunt cruciale pentru trimiterea pacienților în timp optim și tratarea corespunzătoare în centre ce pot asigura asistența potrivită cazurilor.
Bibliografie
2. Su C, Brandt LJ: Escherichia coli 0157 : H7 infection in humans, Ann Intern Med 123:698-714, 1995.
3. Besbas N, Karpman D, Landau D, Loirat C, Proesmans C, et al; European Paediatric Working Group for HUS: A classification of hemolytic uremic syndrome and thrombotic thrombocytopenic purpura and related disorders, Kidney Int 70:423-31, 2006.
4. Rowe PC, Orrbine E, Wells GA, Yetisir E, et al: Risk of hemolytic uremic syndrome after sporadic Escherichia coli O157: H7 infection: results of a Canadian collaborative study, J Pediatr 132:777- 82, 1998.
5. BS, Meyers KE, Schulman SL: The pathogenesis and treatment of the hemolytic uremic syndrome, J Am Soc Nephrol 9:1126-33, 1998.
6. Gianvita A, Tozzi AE, De Petris, et al: Risk factors for poor prognosis in children with hemolytic uremic syndrome, Pediatr Nephrol 18:1229-35, 2003.
7. Gerber A, Karch H, Allerberger F, et al: Clinical course and the role of Shiga toxin producing Escherichia coli infection in the hemolytic uremic syndrome in pediatric patients, 1997-2000 in Germany and Austria: a prospective study, J Infect Dis 186:493-500, 2002.
8. Verweyen HM, Karch H, Allerberger F, Zimmerhackl LB: Entero-hemorrhagic Escherichia coli (EHEC) in pediatric hemolytic uremic syndrome: a prospective study in Germany and Austria, Infection 27:341-47, 1999. 19.
9. Warwicker P, Goodship TJH, Donne RL, Pirson Y, et al: Genetic studies into inherited and sporadic hemolytic syndrome, Kidney Int 53:836-44, 1998. 20.
10. Wong CS, Jelacic S, Habeeb RL, Watkins SL, Tarr PI: The risk of hemolytic uremic syndrome after antibiotic treatment of Escherichia coli O157:H7 infections, N Engl J Med 342:1930-36, 2000.
11. Safdar N, Said A, Gangnon RE, Maki GD: Risk of hemolytic uremic syndrome after antibiotic treatment of Escherichia coli O157:H7 enteritis: a meta-analysis, JAMA 288:996-1001, 2002.
12. Trachtman H, Christen E, Cnaan A, et al: Urinary neutrophil gelatinase-associated lipocalcin in D+HUS: a novel marker of renal injury, Pediatr Nephrol 21:989-94, 2006.
13. Maroeska D, te Loo WM, Monnens LAH, et al: Binding and transfer of veroytotoxin by polymorphonuclear leukocytes in hemolytic uremic syndrome, Blood 95:3396-402, 2000.
14. Exeni RA, Fernandes GC, Palermo MS: Role of polymorphonuclear leukocytes in the pathophysiology of typical hemolytic uremic syndrome, Scientific World J 7:1155-64, 2007.
15. Kamitsuji H, Nonaami K, Ishikawa N, et al: Elevated tissue factor circulating levels in children with hemolytic uremic syndrome caused by verotoxin producing E. coli, Clin Nephrol 53:319-24, 2000.
16. Fernandez GC, Te Loo MW, van der Velden TJA, et al: Decrease of thrombomodulin contributes to the procoagulant state of the endothelium in hemolytic uremic syndrome, Pediatr Nephrol 18:1066-68, 2003.
17. Siegler R, Oakes R: Hemolytic uremic syndromepathogenesis, treatment, and outcome, Curr Opin Pediatr 17:200-04, 2005.
18. Molbak K, Mead PS, Griffin PM: Antimicrobial therapy in patients with Escherichia coli O157 : H7 infection, JAMA 288:1014-16, 2002.
19. Cabreba GR, Fortenberry JD, Warshaw BL, et al: Hemolytic-uremic syndrome associated with invasive Streptococcus pneumoniae infection, Pediatrics 101:699-703, 1998.
20. Nathanson S, Deschenes G: Prognosis of Streptococcus pneumoniae induced hemolytic uremic syndrome, Pediatr Nephrol 16:362-65, 2001.
21. Proulz F, Liet JM, Michele D, et al: Hemolytic uremic syndrome associated with invasive Streptococcus infection, Pediatrics 105:462- 63, 2000.
22. Brandt J, Wong C, Mihm S, et al: Invasive pneumococcal disease and hemolytic uremic syndrome, Pediatrics 110:371-75, 2002.
23. Cochran JB, Panzarino VM, Maes LY, Tecklenburg FW: Pneumococcus-induced T-antigen activation in hemolytic uremic syndrome, Pediatr Nephrol 19:317-21, 2004.
24. Gafencu M, Doros G, Limoncu O, Oprescu I, Botiz A, Complication of Hus in Children, BANTAO Congress, October 13-15, 2011, Halkidichi, Greece
25. Butler T, Islam MR, Azad MAK, Jones PK: Risk factors for development of hemolytic uremic syndrome during shigellosis, J Pediatr 110:894-97, 1987.
26. Bhimma R, Rollins NC, Coovadia HM, Adhikari M: Postdysenteric hemolytic uremic syndrome in children during an epidemic of Shigella dysentery in Kwazulu/Natal, Pediatr Nephrol 11:560-64, 1997.
27. Houdouin V, Doit C, Mariana P, et al: A pediatric cluster of Shigella dysenteriae serotype 1 diarrhea with hemolytic uremic syndrome in 2 families from France, Clin Infect Dis 38:96-99, 2004.
28. Cabagnaro F, Guzman C, Harris P: Hemolytic uremic syndrome associated with Entamoeba histolytica intestinal infection, Pediatr Nephrol 21:126-28, 2006.
29. Turner ME, Kher K, Rakusan T, et al: Atypical HUS in human immunodeficiency virus 1 infected children. Pediatr Nephrol 11:161-63, 1997.
30. Lungu AC, Limoncu O, Teleanu R, Stoica C, Gafencu M, Anti-factor H autoantibody–associated hemolytic uremic syndrome - first case in Romania treated with eculizumab, poster at 5th International Conference "HUS & related disorders". Innsbruck 2015.
Articole din ediţiile anterioare
Vaccinul - vinovatul de serviciu?
Este imposibil să-ți imaginezi, de pe băncile Facultății de Medicină, dar chiar și ca medic rezident în Medicina de familie, ce provocare reprezint...
Profilaxia şi managementul ulcerului diabetic
Diabetul zaharat, patologie cronică ce este caracterizată prin valori crescute ale concentraţiei de glucoză în sânge, are o prevalenţă în Român...
Complianţa la normele de igienă privind utilizarea lentilelor de contact şi riscul infecţiilor corneene
Lentilele de contact sunt dispozitive medicale utilizate de aproximativ 300 de milioane de oameni din întreaga lume, în principal pentru c...