Pulmonary tuberculosis is still a challenge for the practitioner, considering the differential diagnosis of any pulmonary opacity. Although vaccination is performed correctly in Romania, there is still a relatively constant number of cases diagnosed in recent years in children. Proper treatment leads to complete healing, but early diagnosis is essential and important, especially from the epidemiological point of view. The authors present the case of a teenager admitted for persistent pneumopathy, to which the bacteriological confirmation established the diagnosis.
Tuberculoza pulmonară − o provocare la vârsta pediatrică
Pulmonary tuberculosis − a challenge at pediatric age
First published: 29 mai 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Pedi.50.2.2018.1777
Abstract
Rezumat
Tuberculoza pulmonară încă reprezintă o provocare pentru medicul practician, intrând în diagnosticul diferenţial al oricărei opacităţi pulmonare. Deşi vaccinarea este realizată corect în România, totuşi există un număr relativ constant de cazuri diagnosticate în ultimii ani la copii. Tratamentul corect duce la vindecare completă, dar diagnosticul precoce este esenţial şi important din punct de vedere epidemiologic. Autorii prezintă cazul unei adolescente internate pentru o pneumopatie trenantă, la care confirmarea bacteriologică a tranşat diagnosticul.
Introducere
Tuberculoza (TB) la copii reprezintă o problemă majoră pentru sănătatea publică la nivel mondial. Organizaţia Mondială a Sănătăţii (OMS) a raportat că aproximativ 9 milioane de persoane dezvoltă tuberculoză în fiecare an, dintre care aproximativ 1 milion (11%) apar la copiii cu vârste mai mici de 15 ani. Copiii reprezintă 3-6% din numărul total de cazuri de TB în ţările dezvoltate şi peste 25% din numărul de cazuri din ţările în curs de dezvoltare(1). Cu toate acestea, tuberculoza la vârsta pediatrică a fost relativ neglijată de mai mulţi ani, în principal din cauza dificultăţilor în izolarea micobacteriilor la copii. S-au înregistrat progrese în diagnosticarea şi tratamentul TB la vârsta pediatrică şi, mai recent, definirea unui management adecvat al TB la copil a devenit unul dintre principalele aspecte ale eforturilor globale de control al tuberculozei.
Prezentarea cazului
G.R.E., de sex feminin, în vârstă de 17 ani şi 8 luni, din mediul rural, aflată la prima spitalizare în clinică, a fost internată prin transfer de la Spitalul Orăşenesc Hârlău după o spitalizare de aproximativ 7 zile pentru astenie şi tuse productivă persistentă.
Antecedente heredo-familiale: mama (43 de ani) cunoscută cu tiroidită autoimună, cu hipotiroidie în tratament, tatăl (48 de ani) aparent sănătos, un frate de 23 de ani aparent sănătos şi un frate de 7 ani cu sindrom Down.
Antecedente personale fiziologice. Este al doilea copil al cuplului, fără elemente de interes clinic în mica copilărie. Menarhă instalată la vârsta de 14 ani, ultima menstruaţie în luna anterioară internării. Antecedentele personale patologice au fost nesemnificative, până la momentul internării actuale, pacienta nemaifiind spitalizată.
Condiţii de viaţă şi mediu. Locuieşte la casă, în mediul rural, are contact cu animale de casă, neagă contactul cu persoanele bolnave; de asemenea, neagă consumul de etanol sau tutun.
Medicaţia de fond administrată anterior internării: amoxicilină-clavulanat 1 g per os, 1 comprimat la 12 ore, timp de 10 zile anterior internării la spitalul din Hârlău, apoi cefotaxim şi gentamicină timp de 7 zile, injectabil.
Istoricul bolii. Debutul afecţiunii a fost insidios, cu două săptămâni anterior internării la Spitalul Orăşenesc Hârlău, iar după o saptămână de tratament antibiotic injectabil cu cefotaxim şi gentamicină, simptomatologia nu a prezentat ameliorare, persistând tusea productivă, în chinte, cu junghi toracic stâng, iar clinic asocia raluri subcrepitante şi de transmisie, bilateral. În această perioadă, pacienta nu a prezentat febră, dar starea generală era influenţată şi prezenta astenie marcată.
Examenul clinic la internare a evidenţiat următoarele modificări patologice: stare generală uşor influenţată, afebrilă la examinare, facies încercănat, tegumente palide, limba saburală, raluri de transmisie diseminate pe ambele arii toracice şi raluri subcrepitante mai importante pe partea stângă, la nivel bazal; iniţial, tusea a fost semiproductivă, iar apoi a apărut expectoraţia mucopurulentă.
Diagnosticul de etapă este încă neconcludent, oscilând între o pneumonie de etiologie bacteriană (stafilococică) şi tuberculoză pulmonară.
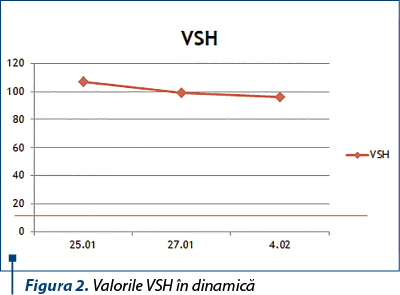
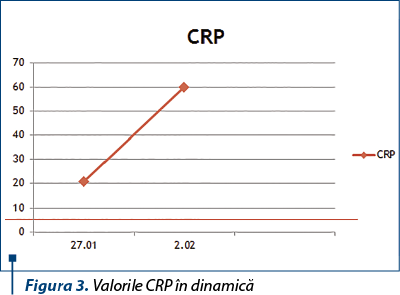
Investigaţiile biologice au relevat: neutrofilie (76%), limfopenie (12,3%), anemie hipocromă microcitară cu hemoglobina=9,9 g/dL, hematocrit=31%, indicii eritrocitari scăzuţi, respectiv VEM=71,2 fL, HEM=22,7 pg, CHEM=31,8 g/dL; trombocitoză reactivă (486 plachete/mmc), hiposideremie (22 mg/dL), hipocalcemie (3,6 mg/dL), imunogramă cu hiper-IgG (1877 mg/dL), hiperstimulare ce apare mai frecvent în infecţiile de lungă durată, funcţia hepatică şi renală normală. De asemenea, prezenţa sindromului inflamator, care se menţine crescut pe parcursul internării (în dinamică, observăm creşterea CRP-ului, în figura 3).
Având în vedere antecedentele heredo-familiale, s-au efectuat hormonii tiroidieni (TSH şi fT4), care au confirmat hipotiroidia, iar mai departe se recomandă consult endocrinologic pentru investigaţii suplimentare şi stabilirea schemei de tratament. S-a recoltat spută pentru BK, iar examenul direct pe lamă a obiectivat prezenţa de micobacterii cu +++. De asemenea, s-a efectuat IDR cu 5 uPPD (purified protein derivative), iar la 72 de ore s-a observat un diametru al induraţiei de 14 mm (testul este pozitiv la un diametru de peste 10 mm, încadrându-se astfel în tipul Palmer III).
Radiografia toracică efectuată la Hârlău a evidenţiat prezenţa unei opacităţi de intensitate medie-mare, neomogenă, cu schiţă de bronhogramă aerică şi două radiotransparenţe, centrale, cu perete gros, localizate bazal stâng, şi lichid pleural stâng. Cord, mediastin: normale radiologic. Se recomandă CT toracic nativ şi cu substanţă de contrast.
CT-ul nativ şi cu substanţă de contrast obiectivează un focar de condensare la nivelul segmentului lateral LIS, multiple zone aerice cu dimensiuni variabile şi leziuni micronodulare cu aspect de diseminare bronhogenică la nivelul segmentului bazal posterior al LIS. Adenopatii bronhopulmonare neconfluente. Absenţa revărsatului pleuro-pericardic decelabil radiologic.
A doua radiografie toracică relevă prezenţa unei opacităţi de intensitate medie, neretractilă, bazală stângă, neomogenă, prin prezenţa de zone aerice la interior, cu dimensiuni variabile, cea mai mare de 2,6/3,3 cm. Pe incidenţa de profil, opacitatea se proiecteaza posterior. Cord etalat pe diafragm. Mediastin fără modificări.
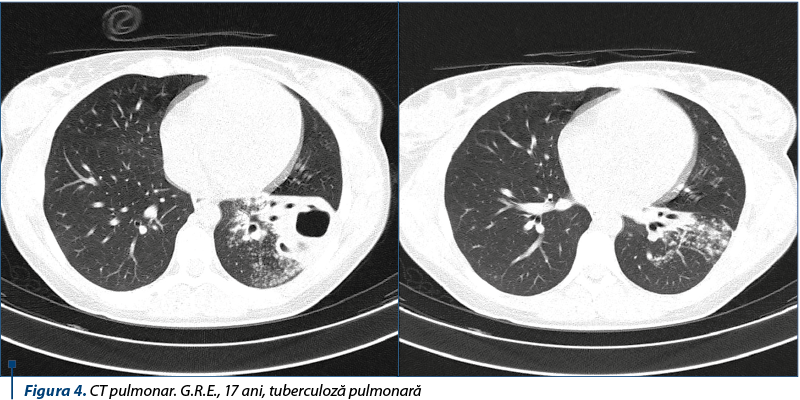
În urma coroborării datelor anamnestice, clinice şi paraclinice, diagnosticul pozitiv este de tuberculoză pulmonară lob inferior stâng (suprainfectată?), spasmofilie hipocalcemică şi anemie feriprivă.
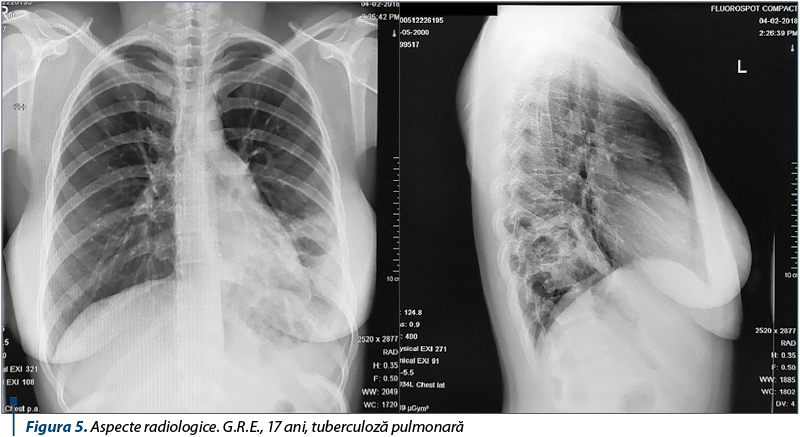
De asemenea, am exclus, în prezenţa tabloului complet al bolii, alte opacităţi (atelectazii, sechestraţie pulmonară, chist suprainfectat, infarct pulmonar) sau pneumonia interstiţială (starea generală, examenul fizic şi cel radiologic sunt diferite).
-
Pneumonii: pneumonia pneumococică, pneumonia stafilococică, pneumonia cu germeni atipici, pneumonia cu H. influenzae, pneumoniile cu germeni Gram-negativi, anaerobi, pneumonia micotică (evoluţie staţionară – biologic şi radiologic, sub antibioterapie prelungită).
-
Abcesul pulmonar (eventual secundar aspiraţiei unui corp străin radiotransparent – nu are aspect radiologic caracteristic).
-
Malformaţii chistice pulmonare – chist solitar (CT-ul exclude), plămân polichistic – formă infectată (lipseşte dinamica radiologică).
-
Chist hidatic evacuat şi suprainfectat (absenţa eozinofiliei, radiologic infirmat).
-
Deficit imun umoral (electroforeza proteinelor şi imunograma normală).
În timpul spitalizării, pacienta a primit tratament antibiotic cu teicoplanină (600 mg pe zi, intravenos, apoi 400 mg/zi), bronhodilatator cu durată scurtă de acţiune (salbutamol 8 mg/zi, în 4 prize), fluidifiant (acetilcisteină 600 mg/zi în trei prize, oral), antimicotic (diflucan 400 mg – 200 mg – 100 mg, p.o.) antiinflamator nesteroidian (ibuprofen 600 mg/3/zi, p.o.) şi inhibitor de pompă de protoni (esomeprazol 40 mg, oral) cu evoluţie staţionară după 10 zile de terapie. Anterior internării în Clinica II Pediatrie Iaşi, aceasta a primit tratament cu amoxicilină-clavulanat 1 g, un comprimat la 12 ore, oral, timp de 10 zile, la recomandarea medicului de familie, după care a continuat cu cefotaxim şi gentamicină intravenos, fenspirid oral, calciterapie şi probiotice pe o perioadă de 7 zile, fără nicio ameliorare clinică sau paraclinică. După ce am primit toate rezultatele şi s-a confirmat etiologia, pacienta a fost transferată într-un centru specializat, unde a început tratamentul cu antituberculoase.
Prognosticul pe termen lung este unul favorabil dacă pacienta este compliantă şi respectă conduita terapeutică. Se impune monitorizarea lunară a funcţiei hepatice, pentru a evita eventualele complicaţii (suprainfecţie, abcedare, emfizem, pneumotorax, tulburări de mecanică ventilatorie, diseminarea infecţiei la distanţă).
Particularitatea cazului este reprezentată de evoluţia trenantă a unei tuberculoze pulmonare, cu localizare inferioară, la o adolescentă normal dezvoltată staturo-ponderal, fără antecedente personale patologice semnificative şi fără deficit imun umoral.
Discuţii
Tuberculoza pulmonară este o boală infecto-contagioasă, al cărei agent etiologic este bacilul Koch. Tuberculoza reprezintă un ansamblu de simptome nespecifice şi polimorfe, încât nu putem concretiza manifestări tipice de boală, doar cele generale mai frecvente, respectiv în funcţie de forma de boală (fatigabilitate, astenie, transpiraţii nocturne, scădere ponderală, tuse seacă, subfrebrilitate). De aceea, trebuie suspicionat în context epidemiologic, alături de examenele paraclinice pentru confirmare.
Din punctul de vedere al debutului, tuberculoza se clasifică în forma primară, secundară şi cea latentă. Forma primară apare atât la copil, cât şi la adult. În 90% din cazuri, este o boală asimptomatică, subclinică, iar cea mai frecventă localizare este la nivel pulmonar.
Factorii de risc pot fi extrinseci şi intrinseci. Cel mai important factor de risc este infecţiozitatea cazului de tuberculoză cu care un organism inocent intră în contact. Astfel, persoanele care intră în contact cu bolnavi cu potenţial mare de diseminare sunt mai susceptibili la infecţie şi mai predispuşi la instalarea bolii. Alţi factori de risc sunt reprezentaţi de condiţiile de igienă, stilul de viaţă şi alimentaţia. Dintre factorii intrinseci, de subliniat imunocompetenţa persoanei expuse, bolile asociate (o condiţie importantă fiind infecţia cu HIV sau deficite imune umorale)(2).
Există mai multe discrepanţe în confirmarea diagnosticului de TBC. Diferenţele majore privesc interpretarea IDR-ului. Majoritatea ghidurilor stabilesc un diametru relevant pentru diagnostic de 10 mm pentru orice copil şi de 5 mm pentru copiii cu risc sporit, deşi ghidurile americane(3,4) admit până la 15 mm pentru copiii fără factori de risc şi până la 10 mm pentru copiii cu factori de risc minori, menţinând diametrul de 5 mm numai pentru populaţia cu risc crescut. Considerând că sensibilitatea şi specificitatea IDR-ului sunt influenţate de cutofful folosit, diferenţele dintre ghiduri nu sunt doar academice, ci au şi consecinţe importante pentru practica clinică. Recomandările diferă substanţial şi în ceea ce priveşte utilizarea quantiferonului pentru diagnosticarea infecţiei cu TBC. Ghidurile din ţările cu venituri ridicate promovează pe larg utilizarea quantiferonului, în timp ce OMS(5) recomandă cu insistenţă ca acesta să nu înlocuiască IDR-ul pentru detectarea infecţiei TBC la copiii din ţări cu venituri mici sau medii(6).
Deşi toate ghidurilor subliniază importanţa testelor şi a genotipului de susceptibilitate la medicamente, orientările din ţările cu venituri reduse nu recomandă aceste teste în mod obişnuit tuturor pacienţilor, probabil din cauza costurilor şi a lipsei de facilităţi.
În ciuda progreselor înregistrate în instrumentul de diagnosticare a TBC în ultimul deceniu, se descrie o lipsă de uniformitate a disponibilităţii, indicaţiei şi interpretării lor, având consecinţe importante pentru practica clinică. Cercetări suplimentare sunt necesare pentru un diagnostic cât mai precis, şi nu numai pentru a îmbunătăţi gestionarea cazurilor individuale, ci şi pentru a oferi o bază validă pentru analiza datelor epidemiologice, evaluarea eficacităţii medicamentelor şi îmbunătăţirea studiilor clinice.
Obiectivele tratamentului cu tuberculostatice sunt reprezentate de ameliorarea simptomatologiei, resorbţia lichidului (dacă este asociată şi pleurezia), prevenirea sechelelor fibroase şi a diseminărilor, asigurarea unei funcţii pulmonare normale şi, bineînţeles, identificarea contacţilor.
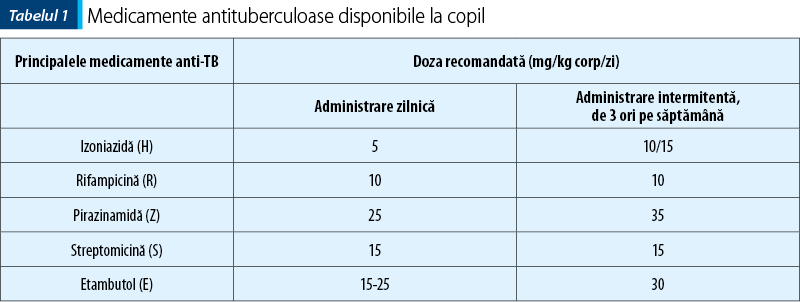
Medicamentele antituberculoase se împart în:
-
de primă linie, care sunt mai eficiente şi mai puţin toxice: izoniazida, rifampicina, pirazinamida, streptomicina şi etambutolul;
-
de rezervă, care sunt mai puţin eficiente, mai toxice şi se folosesc doar în tratamentul individualizat al tuberculozei multichimiorezistente(2).
Principii care se impun pentru creşterea eficienţei terapiei şi prevenirea instalării chimiorezistenţei: terapie standardizată, etapizată, regularitatea şi continuitatea administrării pe întreaga durată a tratamentului, gratuitatea şi accesibilitatea mijloacelor terapeutice, doză adecvată şi administrarea direct observată(2).
Principalul punct de dezacord este reprezentat de regimurile zilnice şi intermitente (de două ori sau de trei ori pe săptămână) recomandate. Lipsa dovezilor între metabolismul medicamentelor şi eficacitatea regimurilor intermitente de tratament în copilărie este, probabil, principalul motiv al acestei descoperiri. Sunt necesare studii suplimentare pentru a clarifica această problemă. Aderenţa slabă la terapie reprezintă o problemă preocupantă, mai ales la vârsta adolescenţei. Datele privind eficacitatea şi siguranţa combinaţiilor de tuberculostatice clasice sau de rezervă sunt necesare înainte de a se adresa recomandări noi. Mai mult, noile scheme de tratament, indicate şi pentru TB activă, ar trebui analizate în studiile viitoare, pentru a îmbunătăţi respectarea tratamentului.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Stop TB Partnership Childhood TB Subgroup; World Health Organization. Guidance for National Tuberculosis Programmes on the management of tuberculosis in children. World Health Organization. 2006; Geneva.
- Crişan-Dabija R, Mihăescu T, Lovin S. Pneumologie clinică. Ed. Tehnopress. 2016; Iaşi, pp. 96-97, 103, 115-116.
- American Academy of Pediatrics. Tuberculosis. In: Pickering LK, editor. Red book: 2012 Report of the Committee on Infectious Diseases. 29th ed. Elk Grove Village, Illinois, USA: American Academy of Pediatrics. 2012; pp. 736–759.
- Centers for Disease Control and Prevention. American Thoracic Society and Infectious Diseases Society of America. Diagnostic Standards and Classification of Tuberculosis in Adults and Children. Am J Respir Crit Care Med. 2000; 14:1376-1395.
- World Health Organization. Rapid advice. Treatment of tuberculosis in children. World Health Organization. 2010; Geneva.
- World Health Organization. Use of tuberculosis interferon-gamma release assays (IGRAs) in low- and middle-income countries: policy statement. World Health Organization. 2011; Geneva.
Articole din ediţiile anterioare
Abdomenul acut chirurgical - capcane de diagnostic
În literatura de specialitate, aproximativ 40% dintre cazurile de abdomen acut chirurgical sunt reprezentate de apendicită acută. Plecând de la ace...
Secvenţa ABC sau secvenţa CAB în resuscitarea cardiopulmonară pediatrică?
O resuscitare cardiopulmonară de calitate este esenţială în cazul unui pacient aflat în stop cardiac. Şansele de supravieţuire şi calitatea ulteri...
Aspecte biochimice şi imunobiologice în malnutriţia protein-calorică la copil
Malnutriţia protein-calorică se caracterizează prin greutatea mică a copilului faţă de greutatea pe care ar trebui să o aibă la vârsta respectivă ş...
Hipertensiunea arterială la copilul de azi – începutul unei boli cronice la adultul de mâine
Hipertensiunea arterială la copil reprezintă un sindrom clinic care apare atunci când valoarea tensiunii arteriale depăşeşte percentila 95 pent...