The use and abuse of psychoactive substances and the complications that derive from them represent a major public health problem. An increasing numbers of new psychoactive substances (NPS) are available on the market as previous substances disappear, generating a constant flow of drugs and constant variations in psychopharmacological properties. This dynamic comes with important difficulties in identifying the substances and their psychopharmacological mechanisms and in the substance-specific treatment. The International Classification of Diseases, the 11th revision (ICD-11), reclassifies the substances and pathologies to enable a better management of the disorders. Psychiatry occupies an important role in the management of substance use disorders along with several medical specialties, psychology, psychotherapy and other fields. The pharmacological treatment of these disorders can be applied in acute states such as acute intoxication and overdose, withdrawal states, substance-induced psychosis, delirium and also in the long-term management of withdrawal. Severe cases of agitation and aggressiveness were observed in patients using especially NPS and not rarely with legal implications. One particular situation that began to emerge on a worldwide scale is the multiple-drug use where the psychoactive substances can create unpredictable and life-threatening situations. In these cases, the treatment implies advanced knowledge of pharmacology and the long-term management has poor outcomes.
Managementul tratamentului tulburărilor cauzate de consumul de substanţe psihoactive
Treatment management of psychoactive substance use disorders
First published: 15 noiembrie 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Psih.59.4.2019.2604
Abstract
Rezumat
Consumul şi abuzul de substanţe psihoactive şi complicaţiile care decurg din acestea reprezintă o problemă majoră de sănătate publică. Creşterea numărului de noi substanţe psihoactive (NPS) disponibile pe piaţă împreună cu dispariţia celor anterioare generează un flux constant de substanţe şi variaţii constante în proprietăţile lor psihofarmacologice. Această dinamică vine cu importante dificultăţi în identificarea substanţelor şi a mecanismelor lor psihofarmacologice şi în tratamentul specific substanţei. Clasificarea Internaţională a Bolilor, a 11-a ediţie (ICD-11), reclasifică substanţele şi patologiile, pentru a permite o mai bună gestionare a tulburărilor. Psihiatria ocupă un rol important în managementul tulburărilor consumului de substanţe, împreună cu mai multe specialităţi medicale, psihologia, psihoterapia şi alte domenii. Tratamentul farmacologic al acestor afecţiuni poate fi abordat în stări acute ca intoxicaţia acută şi supradozajul, stările de sevraj, psihoza indusă de substanţe, delirium şi, pe termen lung, în managementul sevrajului. Au fost observate cazuri severe de agitaţie şi agresivitate la pacienţii care utilizează în special noile substanţe – şi, nu rar, cu implicaţii legale. O situaţie particulară care a început să se dezvolte la scară mondială este consumul de droguri multiple, în care substanţele psihoactive pot crea situaţii imprevizibile şi care pot pune viaţa în pericol. În aceste cazuri, tratamentul implică cunoştinţe avansate de farmacologie, iar managementul pe termen lung are rezultate modeste.
Introducere
Problematica toxicomaniilor, deşi nu este nouă, a luat amploare în ultimii ani, prin creşterea marcantă atât a numărului de substanţe psihoactive şi a mecanismelor psihofarmacologice diferite, cât şi a numărului de utilizatori, cu diversificarea vârstelor, ajungând a fi inclusiv o problemă în sfera patologiei psihiatriei pediatrice. Spectrul extins al substanţelor şi implicaţiile tot mai profunde asupra psihopatologiei au dus la nevoia de concretizare şi dezvoltare a abordării terapeutice, atât din punctul de vedere al intervenţiilor psihosociale, cât şi din punct de vedere farmacologic(1).
Ultimele date disponibile la nivel global, colectate şi puse la dispoziţie de UNDOC (United Nations Office on Drugs and Crimes) prin publicaţia World Drug Report 2019, indică faptul că, în cursul anului 2017, 5,7% din populaţia globului a folosit cel puţin un drog (271 de milioane de oameni), în 2017 fiind înregistrate aproximativ 585 000 de decese datorate direct sau indirect abuzului de substanţe, dintre care 76% datorate abuzului de opioide(2).
O altă problemă majoră este reprezentată de uzul şi abuzul nonmedical de produse farmaceutice, de la benzodiazepine la fentanyl, cu predominanţa opioidelor în Europa şi a benzodiazepinelor în peste 60 de ţări(3,4).
Din cauza fluidităţii pieţei de substanţe ilicite, managementul terapeutic este dificil şi, în cele mai multe cazuri, simptomatic. Ritmul accelerat al sintezei de noi substanţe (aproximativ 500/an în perioada 2015-2017) şi dispariţia altor substanţe fac ca monitorizarea şi identificarea, dar şi adaptarea mijloacelor de abordare farmacologică să fie ţinte greu de atins, dacă nu chiar imposibile(5).
Clasificări diagnostice
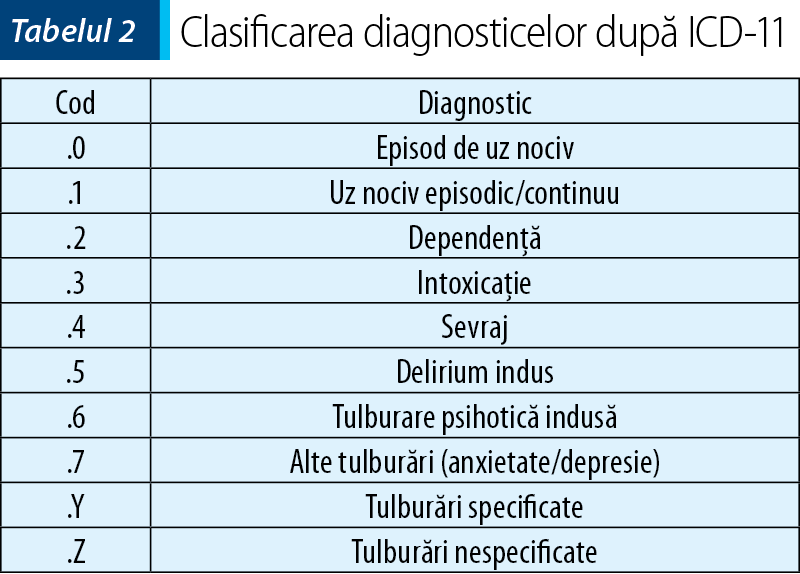
În întâmpinarea acestei problematici, Organizaţia Mondială a Sănătăţii (OMS), prin modificările aduse în ICD-11, încearcă o grupare cu o exactitate mai ridicată faţă de ICD-10 a acestor substanţe, în funcţie de structura chimică, de farmacologia substanţei, dar şi în funcţie de efectele asupra SNC (sistemul nervos central) (tabelul 1) şi totodată o clasificare a nosologiei care să permită practicianului o precizie crescută a diagnosticului, dar şi personalizarea acestuia (tabelul 2). De menţionat este faptul că ICD-11 include trei categorii dedicate substanţelor necunoscute, ca răspuns la probabilitatea crescută de a le întâlni în practică.

OMS împreună cu UNDOC au elaborat în 2016 un document intitulat International standards in the treatment of drug use disorders, care stabileşte principalele principii de tratament al tulburărilor consumului de substanţe, subliniind importanţa accesibilităţii şi promovării tratamentului, personalizarea acestuia ţinând cont şi de subgrupuri populaţionale şi de condiţii de viaţă, dar şi asigurarea standardelor etice, cu respectarea drepturilor omului şi a demnităţii pacienţilor(6).
Managementul terapeutic
Managementul abuzului de substanţe şi a consecinţelor sale este complex şi implică un efort comun, interdisciplinar, al mai multor specialităţi medicale (psihiatrie, medicină de urgenţă, terapie intensivă, nefrologie etc.), al multor profesiuni nonmedicale (psihologi, asistenţi sociali etc.), dar şi suport din partea autorităţilor publice. Astfel tratamentul tulburărilor de consum nu se rezumă la prescrierea de medicamente, ci şi la intervenţii de suport şi psihosociale. Cu toate acestea, din cauza severităţii efectelor substanţelor psihoactive, a complicaţiilor şi posibilelor comorbidităţi, mulţi consumatori ajung în servicii de urgenţă, unde intervenţiile sunt cu precădere farmacologice.
Un prim pas, foarte important, în managementul terapeutic este identificarea substanţei de abuz, evaluarea statusului somatic şi psihic, dar şi a contextului social şi familial, urmate de stabilirea ţintelor terapeutice. Stările de intoxicaţie acută, supradoză şi de sevraj au potenţialul de a pune în pericol viaţa pacientului şi au nevoie de tratament prompt şi bine direcţionat, uneori fiind necesară chiar şi începerea manevrelor de resuscitare(7).
În această etapă se decide asupra mediului în care se va realiza tratamentul. Factorii care se iau în considerare sunt posibilităţile de acces la tratamente specifice, gradul de restricţie la posibile substanţe de abuz, accesul la servicii medicale şi psihiatrice şi, nu în ultimul rând, statusul psihic şi somatic al consumatorului . Astfel, spitalizarea este recomandată în caz de supradoză cu risc vital, cu grad de risc ridicat pentru complicaţii, comorbidităţi importante şi comportamente cu risc pentru sine sau cei din jur(8).
Intoxicaţia acută şi supradoza
În cadrul intoxicaţiei acute şi al supradozei, examinarea somatică trebuie realizată rapid şi eficient, în vederea echilibrării pacientului. Astfel, se urmăresc: starea de nutriţie, temperatura corporală (deseori pacienţii pot fi hipotermici în cazul drogurilor cu efect deprimant al SNC şi hipertermici în cazul stimulentelor), tensiunea, pulsul, identificarea potenţialelor aritmii, frecvenţa respiratorie, nivelul conştienţei şi evaluarea potenţialelor traumatisme cranio-cerebrale(9). De asemenea, recoltarea probelor biologice este esenţială, deoarece acestea pot releva afectări organice (hepatite B sau C, insuficienţă hepatică, insuficienţă renală, diselectrolitemii severe etc.), iar deseori pot pune în evidenţă un sindrom de rabdomioliză, care poate duce la insuficienţă renală, cu necesitatea dializei(10).
Tulburările de conştienţă beneficiază de aportul tiaminei (vitamina B1), administrată în doze de 200-500 mg de 3 ori pe zi, înaintea administrării glucozei şi, în cazul hipoglicemiei, administrarea de dextroză intravenos.
Managementul în această etapă se rezumă de cele mai multe ori la monitorizare şi suport vital, deoarece majoritatea substanţelor nu au antidot specific. Excepţiile notabile sunt constituite de opioide şi benzodiazepine. Astfel, în cazul opioidelor, tratamentul este constituit din Naloxonă în doze de 0,4 mg cu repetarea la 30-60 de minute, până la stabilizarea pacientului(11), iar în cazul benzodiazepinelor, Flumazenil, acesta nefiind indicat în faza acută din cauza riscului ridicat de crize convulsive(12). Fenomenele psihotice şi agitaţia se pot aborda utilizând sedative de tip benzodiazepinic sau antipsihotice (Haloperidol, Quetiapină, Ziprasidonă)(13).
Sindromul de sevraj
Sindromul de sevraj poate fi abordat terapeutic şi în regim ambulatoriu. Spitalizarea se recomandă în special în cazul pacienţilor cu confuzie sau delirium, complicaţii severe, comorbidităţi în sfera respiratorie, circulatorie sau hepatică, situaţii care necesită o atenţie sporită(14).
Managementul acestuia implică sedarea pacienţilor, suport şi monitorizare într-un mediu liniştit şi securizat, reechilibrarea hidrică şi electrolitică şi evaluarea medicaţiei cronice a pacientului, cu sistarea medicamentelor contraindicate în sevraj(15).
Un risc major, care nu implică patologii somatice, este reprezentat de sevrajul la psihostimulente, deoarece în fază acută se poate prezenta sub formă de tulburare psihotică cu un grad ridicat de agitaţie psihomotorie şi agresivitate sau sub formă de episod depresiv cu un risc crescut de suicid(16-18).
Deseori, în cadrul sevrajului, în special la alcool şi benzodiazepine, pacientul dezvoltă stări de confuzie si delirium, cu mortalitate de până la 40% fără tratament. Asigurarea unui mediu minim stimulant, reasigurarea şi reorientarea pacienţilor şi excluderea altor cauze, psihice sau organice, constituie primele etape în management. Sedarea pacienţilor se poate realiza atât cu benzodiazepine (Diazepam, Lorazepam), cât şi cu antipsihotice (Olanzapină 2,5-5 mg/6-8 ore sau Haloperidol 2,5-5 mg/4-6 ore)(19,20).
Tulburarea psihotică indusă
Majoritatea substanţelor – cele mai multe în intoxicaţie acută (amfetamine, cocaină, MDMA, cannabis, halucinogene, PCP, ketamină), dar şi în sevraj (alcool, benzodiazepine, barbiturice) – pot declanşa o tulburare psihotică indusă, fără a fi necesară existenţa unei comorbidităţi din spectrul psihozelor, dar pot constitui un diagnostic diferenţial dificil cu acestea(21,22).
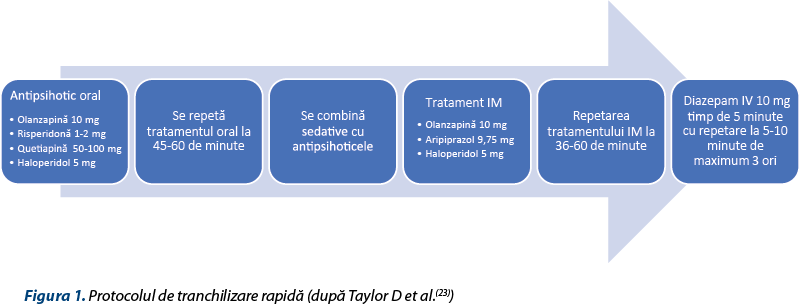
Deoarece mulţi pacienţi pot prezenta agitaţie psihomotorie marcantă, ostilitate, iritabilitate, comportament dezorganizat, aceştia pot reprezenta un real pericol pentru sine, dar şi pentru personalul medical, motiv pentru care, înainte de orice gest terapeutic, se va asigura siguranţa pacientului, a personalului şi a celorlalţi pacienţi, uneori fiind necesară imobilizarea. O etapă esenţială este reprezentată de „de-escalare” în care se încearcă liniştirea pacientului prin plasarea sa într-un mediu puţin stimulant, izolat şi prin tehnici verbale de calmare. În cazul eşecului se poate recurge la protocolul de tranchilizare rapidă (figura 1)(23).
Problematica majoră a tulburării psihotice induse de substanţe psihoactive este reprezentată de rata de conversie în schizofrenie sau în tulburare afectivă bipolară. Cea mai înaltă rată de conversie a fost observată în cadrul psihozei induse de canabis – 47%, urmată de amfetamine, cu 32,3%, cu o medie generală de 32%. Durata medie dintre primul diagnostic şi cel de schizofrenie a fost de 3 ani pentru schizofrenie şi de 4,5 ani pentru tulburările afective bipolare(24-26).
Tulburarea consumului de substanţe psihoactive multiple
Policonsumul reprezintă o provocare atât diagnostică, dar şi de management, deoarece sumarea efectelor substanţelor psihoactive, deseori necunoscute, poate deveni imprevizibilă. Una dintre cele mai întâlnite substanţe care este utilizată în asociere este alcoolul, având efect deprimant al SNC, efect potenţat de cele mai multe ori cu asocierea sa cu opioidele, astfel generând un pericol vital(27).
Stabilizarea pacientului, identificarea substanţei care prezintă cel mai mare risc pentru sănătate, urmate de tratamentul specific acestei substanţe sunt etapele primordiale în managementul terapeutic în fază acută(28,29). Pe termen lung, cele mai indicate intervenţii terapeutice sunt cele psihosociale, dar în cadrul policonsumului au rezultate modeste(30,31).
Concluzie
Managementul toxicomaniilor este un proces amplu şi complex care implică cunoştinţe avansate de farmacologie şi o atenţie sporită asupra planului somatic, din cauza multiplelor substanţe psihoactive nou apărute, cu efecte necunoscute. Fluxul constant de substanţe nu ne permite identificarea lor şi descoperirea unui tratament specific, fiind nevoiţi de cele mai multe ori să ne rezumăm la un tratament suportiv. Un vid de cunoştinţe se regăseşte în zona policonsumului, alimentat de asemenea de schimbările rapide de molecule, o zonă cu un risc vital ridicat şi cu o pondere crescândă în rândul consumatorilor.
Bibliografie
- Schifano F, Napoletano F, Chiappini S, Guirguis A, Corkery JM, Bonaccorso S, et al. New/emerging psychoactive substances and associated psychopathological consequences – Corrigendum. Psychol Med. 2019 Sep 12;1.
- World Drug Report 2019. UN; 2019. (World Drug Report).
- Novak SP, Håkansson A, Martinez-Raga J, Reimer J, Krotki K, Varughese S. Nonmedical use of prescription drugs in the European Union. BMC Psychiatry. 2016 Dec 4;16(1):274.
- Schifano F, Chiappini S, Corkery J, Guirguis A. Abuse of Prescription Drugs in the Context of Novel Psychoactive Substances (NPS): A Systematic Review. Brain Sci. 2018 Apr 22;8(4):73.
- Wadsworth E, Drummond C, Deluca P. The Dynamic Environment of Crypto Markets: The Lifespan of New Psychoactive Substances (NPS) and Vendors Selling NPS. Brain Sci. 2018 Mar 16;8(3).
- Busse A, Gerra G, Koutsenok I, Saenz E. International standards on the treatment of drug use disorders. Drug Alcohol Depend. 2015 Nov;156:e32.
- Strang J, Independent Expert Working Group. Drug misuse and dependence: UK guidelines on clinical management. 2017.
- Reus VI, Fochtmann LJ, Bukstein O, Eyler AE, Hilty DM, Horvitz-Lennon M, et al. The American Psychiatric Association Practice Guideline for the Pharmacological Treatment of Patients With Alcohol Use Disorder. Am J Psychiatry. 2018 Jan;175(1):86–90.
- Erickson TB, Thompson TM, Lu JJ. The approach to the patient with an unknown overdose. Emerg Med Clin North Am. 2007 May;25(2):249–81; abstract vii.
- Jayakrishnan B, Al Asmi A, Al Qassabi A, Nandhagopal R, Mohammed I. Acute drug overdose: clinical profile, etiologic spectrum and determinants of duration of intensive medical treatment. Oman Med J. 2012 Nov;27(6):501–4.
- Boyer EW. Management of Opioid Analgesic Overdose. N Engl J Med. 2012 Jul 12;367(2):146–55.
- Veiraiah A, Dyas J, Cooper G, Routledge PA, Thompson JP. Flumazenil use in benzodiazepine overdose in the UK: a retrospective survey of NPIS data. Emerg Med J. 2012 Jul;29(7):565–9.
- Rech MA, Donahey E, Cappiello Dziedzic JM, Oh L, Greenhalgh E. New Drugs of Abuse. Pharmacother J Hum Pharmacol Drug Ther. 2015 Feb;35(2):189–97.
- Alan D, Kaye N, Vadivelu R, D U. Substance Abuse. Kaye AD, Vadivelu N, Urman RD, editors. New York, NY: Springer New York; 2015.
- Lingford-Hughes A, Welch S, Peters L, Nutt D, British Association for Psychopharmacology, Expert Reviewers Group. BAP updated guidelines: evidence-based guidelines for the pharmacological management of substance abuse, harmful use, addiction and comorbidity: recommendations from BAP. J Psychopharmacol. 2012 Jul 23;26(7):899–952.
- Darke S, Torok M, Kaye S, Ross J. Attempted Suicide, Self-Harm, and Violent Victimization among Regular Illicit Drug Users. Suicide Life-Threatening Behav. 2010 Dec;40(6):587–96.
- Phillips KA, Epstein DH, Preston KL. Psychostimulant addiction treatment. Neuropharmacology. 2014 Dec;87:150–60.
- D’Souza MS, Markou A. Neural substrates of psychostimulant withdrawal-induced anhedonia. In: Behavioral neuroscience of drug addiction. 2010 (pp. 119-178). Springer, Berlin, Heidelberg.
- Schuckit MA. Recognition and Management of Withdrawal Delirium (Delirium Tremens). Longo DL, editor. N Engl J Med. 2014 Nov 27;371(22):2109–13.
- Morandi A, Davis D, Taylor JK, Bellelli G, Olofsson B, Kreisel S, et al. Consensus and variations in opinions on delirium care: a survey of European delirium specialists. Int Psychogeriatrics. 2013 Dec 20;25(12):2067–75.
- Wilson L, Szigeti A, Kearney A, Clarke M. Clinical characteristics of primary psychotic disorders with concurrent substance abuse and substance-induced psychotic disorders: A systematic review. Schizophr Res. 2018 Jul;197:78–86.
- Tandon R, Shariff SM. Substance-Induced Psychotic Disorders and Schizophrenia: Pathophysiological Insights and Clinical Implications. Am J Psychiatry. 2019 Sep 1;176(9):683–4.
- Taylor DM, Barnes TR, Young AH. Taylor D, Young A, Barnes T. The Maudsley Prescribing Guidelines in Psychiatry. 13th ed. Wiley-Blackwell; 2018 May 14.
- Ghose S. Substance-Induced Psychosis: An Indicator of Development of Primary Psychosis? Am J Psychiatry. 2018 Apr 1;175(4):303–4.
- Niemi-Pynttäri JA, Sund R, Putkonen H, Vorma H, Wahlbeck K, Pirkola SP. Substance-Induced Psychoses Converting Into Schizophrenia. J Clin Psychiatry. 2013 Jan 15;74(01):e94–9.
- Marconi A, Di Forti M, Lewis CM, Murray RM, Vassos E. Meta-analysis of the Association Between the Level of Cannabis Use and Risk of Psychosis. Schizophr Bull. 2016 Sep;42(5):1262–9.
- Edwards KA, Vowles KE, Witkiewitz K. Co-use of Alcohol and Opioids. Curr Addict Reports. 2017 Jun 26;4(2):194–9.
- Saunders JB, Conigrave KM, Latt NC, Nutt DJ, Marshall EJ, Ling W, et al., editors. Addiction medicine. 2nd ed. Oxford: Oxford University Press; 2016.
- Mack AH, Brady KT, Frances RJ, Miller SI, editors. Clinical textbook of addictive disorders. 4th ed. New York: The Guilford Press; 2016 May 13.
- Dutra L, Stathopoulou G, Basden SL, Leyro TM, Powers MB, Otto MW. A Meta-Analytic Review of Psychosocial Interventions for Substance Use Disorders. Am J Psychiatry. 2008 Feb;165(2):179–87.
- Connor JP, Gullo MJ, White A, Kelly AB. Polysubstance use. Curr Opin Psychiatry. 2014 Jul;27(4):269–75.