Toxoplasmosis is a parasitic infection caused by Toxoplasma gondii. When primary acute infection is acquired during pregnancy, the mother can be asymptomatic but the fetus may be congenitally infected, the results being severe neurological and ocular sequelae. The prevalence of congenital toxoplasmosis is 1-2 cases in 10.000 newborns. The present paper aims at presenting a complete diagnosis and treatment protocol of acute toxoplasmosis infection during pregnancy. International scientific papers and protocols of recent date have been reviewed. The main conclusion is that screening should be offered in every pregnancy, and primary diagnosis should comprise a serologic profile (IgG, IgM, IgA, IgE). In case of a positive serological screening, the testing must be repeated, and treatment (spiramycin) is begun until the second results. In pregnancies over 18 weeks an amniocentesis is indicated to confirm fetal congenital infection. The treatment for acute fetal infection is a combination of pyrimethamine, sulfadiazine, and folinic acid. Studies conducted on fetal sequelae in case of acute toxoplasmosis infection in first trimester pregnancies concluded that therapeutic abortion is not indicated.
Managementul infecţiei acute cu Toxoplasma gondii în sarcină – review de literatură
The management of acute Toxoplasma gondii infection during pregnancy – literature review
First published: 22 martie 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Gine.19.1.2018.1511
Abstract
Rezumat
Toxoplasmoza este o infecţie parazitară cauzată de Toxoplasma gondii. Atunci când infecţia primară acută are loc în timpul sarcinii, aceasta poate să fie asimptomatică pentru mamă, dar poate să producă o infecţie congenitală severă, cu sechele neurologice şi oculare fetale. Prevalenţa infecţiei toxoplasmice congenitale este de 1-2 cazuri la 10.000 de nou-născuţi. Lucrarea de faţă are ca scop să prezinte un protocol complet de diagnostic şi tratament al infecţiei acute cu Toxoplasma gondii în sarcină. Pentru atingerea scopului s-au revizuit articole şi ghiduri din literatura internaţională de specialitate de dată recentă. Principalele concluzii atestă ca prim pas în diagnosticarea infecţiei realizarea unui profil serologic cuprinzând IgG, IgM, IgA şi IgE. În cazul suspectării unei infecţii acute, testarea trebuie repetată, până la sosirea rezultatelor instituindu-se un tratament medicamentos cu spiramicină. La sarcinile de peste 18 săptămâni se va indica efectuarea unei amniocenteze pentru confirmarea transmiterii fetale. Tratamentul infecţiei fetale constă în administrarea unei combinaţii de pirimetamină, sulfadiazină şi acid folinic. Principalele studii despre afectarea fetală în cazul infecţiei acute în primul trimestru de sarcină au concluzionat că avortul terapeutic nu este indicat.
Introducere
Toxoplasmoza este o infecţie parazitară cauzată de Toxoplasma gondii. Când infecţia are loc în timpul sarcinii, deşi asimptomatică pentru mamă, aceasta poate genera o infecţie congenitală severă, cu afectarea neurologică şi oculară a fătului. Doar 38% din femeile din SUA prezintă anticorpi împotriva toxoplasmei de la o infecţie anterioară, 62% aflându-se la risc de a contracta infecţia în timpul sarcinii(1). Odată cu introducerea metodelor de prevenţie a toxoplasmozei, rata infecţiei primare a scăzut considerabil. În prezent, rata infecţiei neonatale este de 1-2 cazuri la 10.000 de nou-născuţi(2).
Infecţia cu Toxoplasma gondii în timpul sarcinii, precum şi transmiterea acesteia la nou-născut continuă să fie cauza unei afecţiuni grave, dar care poate fi prevenită. S-a estimat că între 500 şi 5.000 de copii se nasc anual infectaţi în SUA. Deşi aparent sănătoşi la naştere, sechelele semnificative pe termen lung devin evidente abia la luni sau ani distanţă.
Transmitere
Mai multe studii au dezvăluit principalele căi de transmitere a infecţiei cu Toxoplasma gondii, acestea fiind ingestia de chisturi tisulare din carne incomplet preparată sau din oochisturi din sol, alimente ori apă contaminate cu fecale de pisică(3,4). Studiile recente au demonstrat că, totuşi, contactul direct cu pisicile nu reprezintă un factor de risc semnificativ pentru contractarea infecţiei în timpul sarcinii(5).
Infecţia congenitală fetală poate avea loc numai în timpul fazei acute a infecţiei, când toxoplasma aflată în sângele matern este transportată către placentă şi făt. Formarea de anticorpi ca răspuns la prezenţa infecţiei transformă parazitul din stadiul de trofozoid la forma de chist tisular şi astfel acesta nu mai poate circula prin sângele matern şi nici nu mai poate provoca infecţia congenitală. De aceea, infecţia fătului cu toxoplasma nu a fost raportată la femeile cu toxoplasmoză cronică, dobândită anterior sarcinii. Forma chistică persistă în ţesuturile gazdei (creier, muşchi), generând o infecţie cronică(6,7).
Screening
Nu există un consens internaţional referitor la metoda de screening împotriva toxoplasmozei. Astfel, protocoalele societăţilor de specialitate din SUA, Canada şi Anglia nu recomandă screeningul universal de rutină, pe când anumite societăţi din Europa susţin testarea universală (lunară/bilunară/trimestrială)(8,9,10,11,22).
Recomandarea împotriva screeningului universal în America de Nord şi Anglia se bazează pe prevalenţa scăzută a bolii, existenţa a foarte puţine laboratoare capabile de a efectua testări serologice standardizate, lipsa unui tratament înalt eficient şi costurile crescute ale screeningului. Pentru ca screeningul să fie eficient, acesta trebuie repetat la maximum o lună, oferind astfel posibilitatea iniţierii tratamentului precoce. Totuşi, testările repetate duc la o creştere a costurilor şi tratamentelor nenecesare la paciente cu rezultate fals pozitive. Aceste limitări trebuie puse în balanţă cu eficienţa aparentă a tratamentului infecţiei acute cu privire la reducerea deceselor şi a sechelelor grave(12).
Conform protocoalelor internaţionale, screeningul de rutină este recomandat pacientelor cu risc înalt (imunodeprimate, HIV-pozitive) sau la cele la care există suspiciunea de infecţie în urma unor descoperiri ecografice (hidrocefalie, calcificări intracraniene, microcefalie, RCIU, ascită sau hepatoslenomegalie)(13). O posibilitate de screening, adoptată actualmente în Danemarca şi unele state americane, este aceea de testare neonatală, metodă ce permite diagnosticul inclusiv al cazurilor subclinice (nu există însă certitudinea reducerii gravităţii sechelelor pe termen lung).
Interpretarea rezultatelor screeningului
Screeningul pentru detectarea anticorpilor specifici IgG sau IgM este esenţial în diagnosticarea infecţiei acute cu Toxoplasma gondii în sarcină.
Testul Sabin-Feldman, ce măsoară titrul anticorpilor IgG, este standardul de aur. Titrurile de anticorpi sunt adesea nedetectabile până la 1-2 săptămâni după infectarea parazitară şi pot persista la valori scăzute toată viaţa. Titruri crescute ale anticorpilor specifici trebuie să fie documentate în vederea diagnosticării corecte a infecţiei cu Toxoplasma gondii în sarcină.
O valoare stabilă a titrului de anticorpi IgG indică o infecţie cronică ce nu pune în pericol fătul. Pentru observarea stabilităţii, repetarea dozării anticorpilor trebuie realizată la o distanţă de minimum trei săptămâni, la acelaşi laborator. O creştere de 4 ori sau mai mult a valorii poate să indice o infecţie acută. Valori fals pozitive sunt frecvent înregistrate când testele se realizează la laboratoare diferite sau în momente diferite ale zilei.
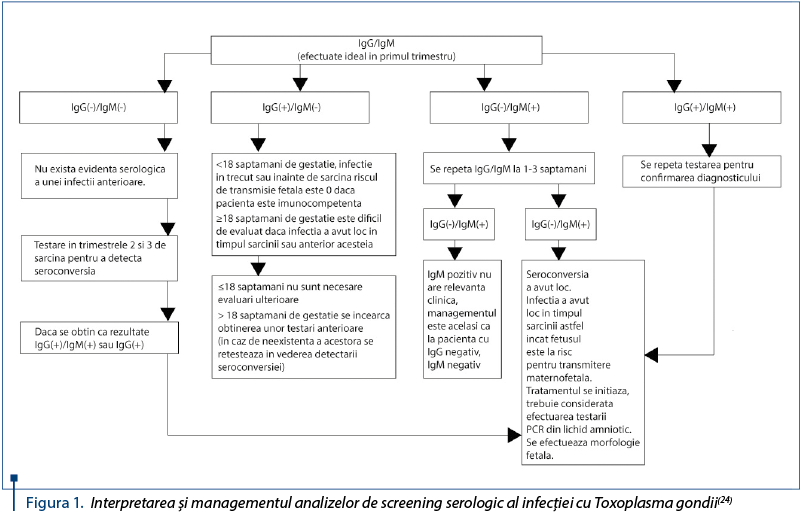
Prezenţa anticorpilor IgM poate fi determinată prin metoda ELISA după 1-2 săptămâni de la momentul infectării. Trebuie reţinut faptul că titrul anticorpilor IgM poate rămâne ridicat timp de un an post-expunere, de aceea nu este sugestiv în diagnosticul infecţiei acute, în special la momentul la care nu este însoţit de un titru IgG modificat. Dozarea anticorpilor IgM se repetă, de asemenea, la interval de trei săptămâni, de preferat la acelaşi laborator. Un titru al anticorpilor IgM aflat în creştere este diagnostic pentru infecţia acută.
Dacă infecţia este dobândită anterior concepţiei, este puţin probabil ca fătul să fie afectat. Un titru absent al anticorpilor IgM exclude o infecţie recentă, cu excepţia situaţiei în care testele sunt efectuate prea devreme post-expunere. Femeile la care anticorpii IgG sunt pozitivi şi anticorpii IgM sunt negativi sunt considerate imunizate, iar feţii nu prezintă risc de a dezvolta toxoplasmoză congenitală(2).
Diagnostic
Confirmarea infecţiei primare acute este de o importanţă majoră în vederea evaluării riscului de transmitere materno-fetală, iniţierii tratamentului medicamentos şi oferirii consilierii adecvate. Pentru a determina cu o acurateţe ridicată probabilitatea unei infectări recente, există teste specifice, ca de exemplu testarea avidităţii anticorpilor IgG(14). Testarea avidităţii IgG măsoară puterea legăturilor acestora cu Toxoplasma gondii(15). În cele mai multe cazuri, aviditatea IgG creşte pe parcursul a 5 luni după momentul infectării. Astfel, pacienta cu o infecţie acută (sub 5 luni) o să prezinte un index scăzut de aviditate, pe când pacientele cu o infecţie anterioară sarcinii vor prezenta un index de aviditate mare(16).
Aşa cum a fost menţionat anterior, diagnosticul poate să fie ghidat şi de descoperiri ecografice. Nespecificitatea markerilor ecografici îi plasează mai mult în sfera ajutorului oferit pentru monitorizarea gravităţii efectelor infecţiei asupra fătului, decât în calitatea de instrument de diagnostic.
Amniocenteza reprezintă singura metodă de diagnostic de certitudine a transmiterii materno-fetale (sensibilitate de 81-90%, specificitate de 96-100%). Din cauza riscurilor asociate metodei invazive de testare, primul pas este reprezentat de consilierea adecvată a pacientelor. Necesitatea amniocentezei trebuie să fie ghidată de vârsta gestaţională la momentul diagnosticului, de imposibilitatea unui diagnostic precis prin metode serologice şi de existenţa de markeri ecografici sugestivi pentru infecţie toxoplasmică. Amniocenteza nu poate fi efectuată anterior împlinirii vârstei gestaţionale de 18 săptămâni din cauza ratelor mari de rezultate fals pozitive; de asemenea, procedura nu trebuie efectuată la mai puţin de 4 săptămâni de la momentul suspicionat de infectare, din cauza ratelor mari de rezultate fals negative(15).
Analiza fetală sangvină (cordonocenteza), considerată anterior ca fiind gold standard în diagnosticul infecţiei fetale, nu mai este actualmente indicată ca test diagnostic din cauza ratelor ridicate de sensibilitate şi specificitate a PCR-ului din lichidul amniotic şi, totodată, a asocierii unor riscuri suplimentare fetale ale procedurii(14,15,16).
Tratament
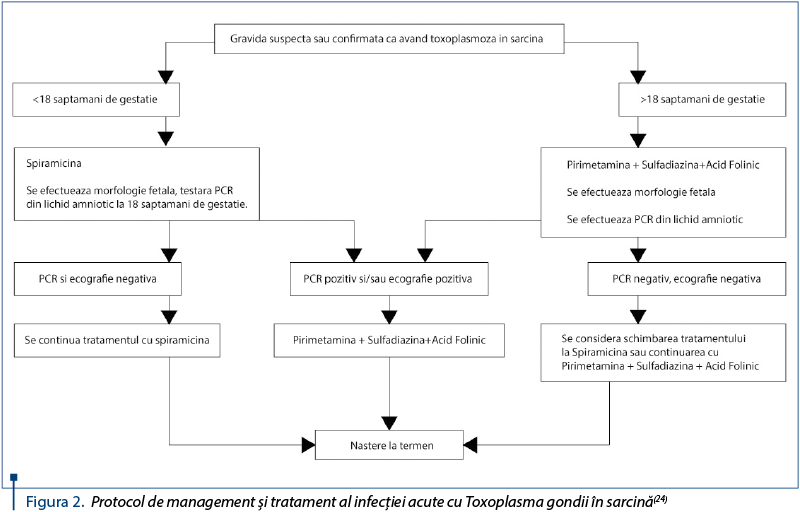
Odată ce testele serologice relevă o infectare recentă (în primele 18 săptămâni de gestaţie sau la scurt timp înaintea concepţiei), se recomandă prevenirea transmiterii verticale a parazitului prin tratament medicamentos cu spiramicină. Dacă infecţia fetală este confirmată printr-un rezultat pozitiv din lichidul amniotic, la 18 săptămâni de gestaţie sau după, se recomandă tratament medicamentos cu pirimetamină, sulfadiazină şi acid folinic (în cazul în care pacienta se află deja în tratament cu spiramicină, se indică modificarea tratamentului cu asocierea celorlalte trei). În unele centre din Europa, modificarea tratamentului are loc între săptămânile 14 şi 16(11).
Din cauza ratelor mari de transmitere observate după 18 săptămâni de gestaţie, tratamentul cu spiramicină, pirimetamină şi acid folinic este utilizat şi la pacientele care au fost infectate după 18 săptămâni, în încercarea de a preveni transmiterea verticală, iar în cazul în care aceasta a avut loc, pentru a oferi tratament fătului, reducând riscul apariţiei sechelelor neurologice grave. Pirimetamina nu este utilizată înainte de 18 săptămâni, deoarece are un efect potenţial teratogen.
Utilizarea spiramicinei, antibiotic din clasa macrolidelor, a determinat scăderea ratei transmiterii verticale cu aproximativ 60%. Efectul protector este mai pronunţat la femeile infectate în primul trimestru de sarcină. Spiramicina nu traversează însă bariera fetoplacentară, de aceea nu este utilizată de primă intenţie în tratamentul fătului. Nu există date care să demonstreze efectul teratogen al spiramicinei. Se administrează până la momentul naşterii chiar şi la pacientele cu rezultat negativ din lichidul amniotic, luând în considerare posibilitatea unei infecţii tardive de la o placentă infectată precoce. Spiramicina se administrează oral, în doză de 1 g (3 milioane UI) la 8 ore (cu un maxim de 3 g/9 milioane UI pe zi)(17).
Asocierea de pirimetamină, sulfadiazină şi acid folinic este recomandată tuturor gravidelor cu infecţie cu Toxoplasma gondii după 18 săptămâni de gestaţie, precum şi celor la care infecţia fetală a fost confirmată prin test PCR pozitiv din lichidul amniotic sau este suspectată prin malformaţii fetale congenitale detectate prin screening ecografic(18). Acest regim terapeutic este utilizat în încercarea unui tratament eficient al infecţiei fetale, în special la gravidele la care nu se poate realiza amniocenteza în vederea prelevării de lichid amniotic pentru efectuarea PCR sau la cele la care infecţia maternă are loc după 18 săptămâni de gestaţie(19).
În Franţa, regimul de administrare a tratamentului medicamentos este următorul:
- Pirimetamină – 25 mg p.o. o dată pe zi
- Sulfadiazină – 4 g/zi p.o. divizată în 2/4 prize
- Acid folinic – 10 până la 25 mg/zi p.o. o dată pe zi (acidul folic nu este un substitut adecvat)(20,21).
Managementul sarcinii
O lungă perioadă de timp s-a considerat necesar avortul în cazul diagnosticării infecţiei acute cu Toxoplasma gondii în primul trimestru de sarcină. Începând cu 1994, odată cu primele studii realizate asupra efectelor pe termen lung ale infecţiei congenitale, avortul nu a mai fost recomandat.
În Franţa, ţară în care există un protocol de screening prenatal TORCH, avortul este descurajat, terminarea sarcinii fiind rezervată cazurilor cu markeri ecografici de anomalii intracraniene fetale şi doar după confirmarea diagnosticului prin PCR din lichidul amniotic. Raţionamentul are la bază rezultatele studiilor ce au demonstrat rata relativ mică de infecţie congenitală şi prognosticul bun al nou-născuţilor, cu diferenţe minime de dezvoltare la 3-4 ani faţă de copiii neinfectaţi(21,23,25).
Concluzii şi recomandări
- Prevenţia infecţiei acute cu Toxoplasma gondii în sarcină se realizează primar prin informarea gravidelor privind sursele de infecţie şi metodele de evitare a acestora.
- Screeningul serologic universal este o metodă bună de depistare a infecţiei primare sau a seroconversiei, însă doar atunci când este efectuat corect (retestare lunară, la acelaşi cabinet), rezultând costuri majore.
- O categorie de paciente la care screeningul toxoplasmei este obligatoriu sunt pacientele imunodeprimate (ex.: HIV-pozitive), la care se poate produce seroconversia spontană.
- Este necesară testarea infecţiei toxoplasmice la momentul în care ecografia fetală decelează anomalii, incluzând (fără a se limita doar la) calcificări intracraniene, microcefalie, hidrocefalie, ascită, hepatosplenomegalie, restricţie de creştere intrauterină severă.
- Dacă testul de screening ridică suspiciunea unei infecţii recente la o pacientă gravidă, primul pas este retestarea la 1-3 săptămâni. Dacă rezultatul se menţine pozitiv, testul de aviditate al IgG este următorul pas. Confirmarea diagnosticului se face prin efectuarea PCR din lichidul amniotic.
- Dacă infecţia maternă este confirmată şi vârsta gestaţională este mai mică de 18 săptămâni, se recomandă instituirea unui tratament medicamentos bazat pe spiramicină.
- Dacă infecţia maternă este confirmată şi vârsta gestaţională depăşeşte 18 săptămâni, protocolul de tratament medicamentos cuprinde asocierea pirimetamină + sulfadiazină + acid folinic.
- Actualmente, nici un protocol internaţional nu menţionează ca fiind necesară oprirea cursului sarcinii.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Sever JL, Ellenberg JH, Ley AC et al. Toxoplasmosis: Maternal and pediatric findings in 23,000 pregnancies. Pediatrics. 1988;82:181-92.
- Foulon W, Naessens A, Ho-Yen D. Prevention of congenital toxoplasmosis. J Perinat Med. 2000;28:337-45.
- Dubey JP, Beattie CP. Toxoplasmosis of Animals and Man. CRC Press. 1988 Boca Raton, Florida.
- Kapperud G, Jenum PA, Stray-Pedersen B et al. Risk factors for Toxoplasma gondii infection in pregnancy: Results of a prospective case-control study in Norway. Am J Epidemiol. 1996;144:405.
- Cook AJC, Gilbert RE, Buffolano W et al. Sources of toxoplasma infection in pregnant women: European multicentre case-control study. Br Med J. 2000;321:142-7.
- Remington JS, Cavanaugh EN. Isolation of the encysted form of Toxoplasma gondii from human skeletal muscle and brain. N Engl J Med. 1965;273:1308-10.
- Wong SY, Remington JS. Toxoplasmosis in pregnancy. Clin Infect Dis. 1994;18:853-62.
- Gilbert RE, Peckham CS. Congenital toxoplasmosis in the United Kingdom: to screen or not to screen? J Med Screen. 2002;9:135.
- Paquet C, Yudin MH. Society of Obstetricians and Gynaecologists of Canada. Toxoplasmosis in pregnancy: prevention, screening, and treatment. J Obstet Gynaecol Can. 2013;35:78.
- ACOG. Practice bulletin no. 151: Cytomegalovirus, parvovirus B19, varicella zoster, and toxoplasmosis in pregnancy. Obstet Gynecol. 2015;125:1510. Reaffirmed 2017.
- Gilbert R, Gras L. European Multicentre Study on Congenital Toxoplasmosis. Effect of timing and type of treatment on the risk of mother to child transmission of Toxoplasma gondii. BJOG. 2003;110:112.
- Cortina-Borja M, Tan HK, Wallon M, et al. Prenatal treatment for serious neurological sequelae of congenital toxoplasmosis: an observational prospective cohort study. PLoS Med. 2010;7.
- Montoya JG, Remington JS. Management of Toxoplasma gondii infection during pregnancy. Clin Infect Dis. 2008;47(4):554-66.
- Petersen E, Borobio MV, Guy E, Liesenfeld O, Meroni V, Naessens A, et al. European multicenter study of the LIAISON automated diagnostic system for determination of Toxoplasma gondii - specific immunoglobulin G (IgG) and IgM and the IgG avidity index. J Clin Microbiol. 2005;43(4):1570-4.
- Montoya JG. Laboratory diagnosis of Toxoplasma gondii infection and toxoplasmosis. J Infect Dis. 2002;185(Suppl 1):S73-82.
- Pour Abolghasem S, Bonyadi MR, Babaloo Z, Porhasan A, Nagili B, Gardashkhani OA, et al. IgG avidity test for the diagnosis of acute Toxoplasma gondii infection in early pregnancy. Iran J Immunol. 2011;8(4):251-5.
- Thiebaut R, Leproust S, Chene G, Gilbert R. Effectiveness of prenatal treatment for congenital toxoplasmosis: a meta-analysis of individual patients’ data. Lancet. 2007;369:115-22.
- Kieffer F, Wallon M, Garcia P, Thulliez P, Peyron F, Franck J. Risk factors for retinochoroiditis during the first 2 years of life in infants with treated congenital toxoplasmosis. Pediatr Infect Dis J. 2008;27:27-32.
- Foulon W, Villena I, Stray-Pedersen B, et al. Treatment of toxoplasmosis during pregnancy: a multicenter study of impact on fetal transmission and children’s sequelae at age 1 year. Am J Obstet Gynecol. 1999;180:410-5.
- Remington JS, McLeod R, Thulliez P, Desmonts G. Toxoplasmosis. In: Infectious Disease of the Fetus adn Newborn Infant, 6th ed, Remington JS, Klein J, Wilson CB, Baker CJ (Eds), Elsevier Saunders, Philadelphia. 2006;947.
- Binquet C, Wallon M, Metral P, et al. Toxoplasmosis seroconversion in pregnant women. The differing attitudes in France. Presse Med. 2004;33:775.
- Stan D, Mitran M. The congenital toxoplasmosis. Ginecologia.ro. 2014;3(5):42-3.
- Roşca I, Rusu R, Prisăcariu L, Şărban AM, Mitran M, Oriţă V. Infecţia congenitală cu citomegalovirus, prezentare de caz. Ginecologia.ro. 2013;1(1):22-5.
- Goldstein EJC, Montoya JG, Remington JS. Management of Toxoplasma gondii infection during pregnancy. Clin Inf Dis. 2008;47(4):554-66.
- Berrebi A, Kobuch WE, Bessieres MH, et al. Termination of pregnancy for maternal toxoplasmosis. Lancet. 1994;344:36.
Articole din ediţiile anterioare
Copiii şi societatea modernă
În procesul devenirii şi desăvârşirii de sine, cuplul şi familia sunt calea, mijlocul şi şansa ca matrice fundamentală a vieţii. În şi prin familie...
Rolul infecţiilor orale în naşterea prematură
Prematuritatea şi greutatea scăzută la naştere sunt unele din complicaţiile frecvente ale sarcinilor. Infecţiile orale, în special bolile parodonta...
Tratamentul medical al endometriozei: este opţiunea medicului?
Introducere. Endometrioza este o patologie cronică benignă, iar managementul ei implică adoptarea unei strategii pe termen lung care include tr...
Delivrenţa
Imediat după naşterea fătului, începe periodul III al naşterii, în care placenta este eliminată. Delivrenţa sau expulzia placentei, constă în succe...