Most patients with chronic kidney disease (CKD) have hypertension, and CKD is characterized by high and very high cardiovascular disease rates. Hypertension is an important cardiovascular risk factor, and its treatment prevents major cardiovascular events and lowers mortality of all causes and especially cardiovascular mortality. Therefore antihypertensive therapy is part of the management of chronic kidney disease. Effective blood pressure control decreases not only the risk of fatal and non-fatal cardiovascular events, but also reduces the rate of progression of renal impairment. Target bloodline values are not definitively established, but most guidelines recommend lowering systolic blood pressure to values below 140-130 mmHg, depending on the presence of proteinuria. Additional studies are needed to establish the blood pressure (BP) target, especially for patients with GFR below 45 ml/min./1.73 m2, where the benefits of too aggressive BP may be outweighed by the risk of progression to renal insufficiency. Most patients with chronic kidney disease require therapy with two or three therapeutic agents, the most commonly used drugs being ACE inhibitors/ARB (if there is intolerance to ACE inhibitors), calcium channel blockers and diuretics.
Abordarea hipertensiunii arteriale la pacienţii cu boală cronică de rinichi
Hypertension approach in patients with chronic kidney disease
First published: 20 octombrie 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/MED.125.5.2018.2004
Abstract
Rezumat
Majoritatea pacienţilor cu boală cronică de rinichi (BCR) au hipertensiune arterială şi prezintă risc înalt şi foarte înalt de evenimente cardiovasculare. Hipertensiunea arterială reprezintă, la rândul ei, un factor de risc cardiovascular extrem de important, iar tratarea ei scade rata evenimentelor majore cardiovasculare şi reduce mortalitatea de toate cauzele, în special mortalitatea de cauză cardiovasculară. De aceea, tratarea hipertensiunii arteriale face parte din managementul bolii cronice de rinichi. Controlul eficient al tensiunii arteriale scade nu doar riscul de evenimente cardiovasculare fatale şi nonfatale, dar reduce şi rata de progresie a deteriorării funcţiei renale. Valorile-ţintă ale tensiunii arteriale (TA) nu sunt definitiv stabilite, dar majoritatea ghidurilor recomandă scăderea TA sistolice la valori sub 140-130 mmHg, în funcţie de prezenţa proteinuriei. Sunt necesare studii suplimentare pentru a stabili pragul-ţintă al tensiunii arteriale mai ales la pacienţii cu rata de filtrare glomerulară (RFG) sub 45 ml/min./1,73m2, la care beneficiile scăderii TA prea agresiv ar putea fi depăşite de riscul progresiei spre insuficienţă renală. Majoritatea pacienţilor cu boală renală cronică necesită terapie cu doi sau trei agenţi terapeutici, cele mai folosite medicamente fiind inhibitorii enzimei de conversie (IECA)/ blocanţii receptorilor angiotensinei (BRA) în cazul intoleranţei la IECA, blocanţii canalelor de calciu şi diureticele.
Rinichii joacă un rol esenţial atât în producerea, cât şi în progresia hipertensiunii arteriale (HTA); în acelaşi timp, afectarea renală cronică determină un profil aparte al pacientului hipertensiv, necesită terapie specifică şi adesea monitorizare pluridisciplinară. În unele situaţii poate deveni dificil de precizat relaţia cauză-efect, respectiv dacă ne aflăm în faţa unei HTA secundare de cauză renală sau dacă boala renală este consecinţa afectării de organ în evoluţia hipertensiunii. Oricare ar fi situaţia, este demonstrat faptul că pacienţii care prezintă concomitent HTA şi afectare a funcţiei renale au evoluţie şi prognostic nefavorabile, în special în absenţa unui tratament adecvat. Ischemia renală şi hipoxia, mecanism frecvent întâlnit în special la vârstnici, determină stimularea sistemului renină-angiotensină-aldosteron (SRAA) şi a sistemului nervos simpatic. Consecinţa este vasoconstricţia renală, scăderea fluxului sanguin renal şi a ratei de filtrare glomerulară (RFG), creşterea secreţiei de angiotensină şi aldosteron, cu creşterea consecutivă a retenţiei de sare şi apă(1). Pe de altă parte, hipertensiunea arterială netratată sau incorect tratată are drept consecinţe dezvoltarea nefropatiei hipertensive şi progresia afectării renale, scăderea RFG şi apariţia proteinuriei. HTA, alături de diabetul zaharat de tip 2 şi sindromul metabolic sunt considerate în prezent principalele cauze ale bolii cronice de rinichi în ţările occidentale.
Boala cronică se defineşte ca prezenţa afectării funcţiei renale sau a structurii renale pe o perioadă de cel puţin trei luni, fiind necesară evidenţierea scăderii eRFG<60 ml/min./1,73 m2 cel puţin la două determinări efectuate la distanţă de 90 de zile (cu sau fără prezenţa markerilor de afectare renală: albuminurie, hematurie de origine renală, tulburări electrolitice, modificări histologice sau structurale renale identificate imagistic, istoric de transplant renal). Boala cronică de rinichi reprezintă un factor de risc cardiovascular, iar hipertensiunea arterială, la rândul ei, netratată corect, agravează evoluţia bolii renale, grăbind evoluţia spre insuficienţă renală.
Pacienţii cu boală cronică de rinichi prezintă, pe lângă factorii de risc tradiţionali, şi factori de risc netradiţionali (tabelul 1), care contribuie, pe de o parte, la creşterea riscului de evenimente cardiovasculare majore letale sau neletale, dar şi la progresia afectării funcţiei renale.
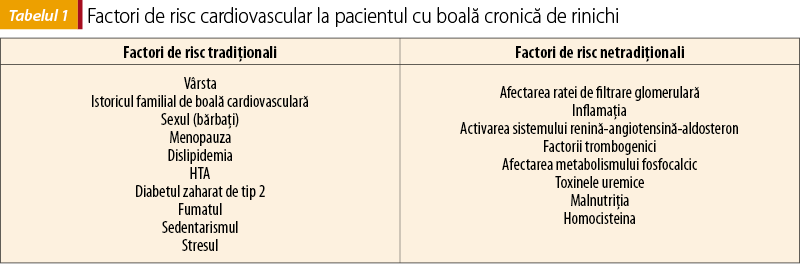
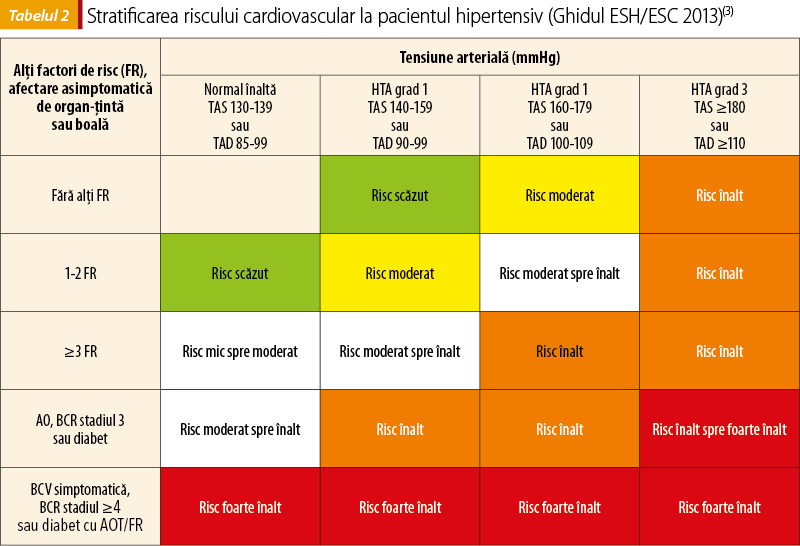
Estimarea riscului cardiovascular la pacienţii cu BCR este subestimată de scorurile pe care le utilizăm la ceilalţi pacienţi; de aceea, toate ghidurile consideră că pacienţii cu BCR în stadiul 3-5 (RFG<60 ml/min./1,73 m2) se află la risc înalt şi foarte înalt (IA)(2). HTA, la rândul ei, constituie factor de progresie a bolii renale, iar decelarea determinărilor subclinice sau clinice de organ poziţionează pacientul la risc înalt sau foarte înalt (tabelul 2)
Caracteristic pacienţilor cu afectare cronică de rinichi este profilul special al hipertensiunii (tabelul 3), frecvent constatându-se creşteri nocturne sau puseuri matinale, HTA mascată, HTA rezistentă, ce răspunde greu la tratament, sau hipotensiune posturală(4), ce afectează calitatea vieţii, fiind vorba cel mai adesea de pacienţi vârstnici. Acest profil al tensiunii arteriale (TA) reprezintă el însuşi un factor de risc pentru evenimente majore, de aceea este important să monitorizăm TA pe 24 de ore şi apoi terapia medicamentoasă să fie indicată în funcţie de profilul obţinut. Pacienţii hipertensivi cu boală cronică de rinichi se află, prin urmare, la risc crescut de a dezvolta complicaţii şi evenimente cardiovasculare, de aceea monitorizarea lor implică, pe lângă examenul clinic periodic, determinarea creatininei şi calcularea ratei de filtrare glomerulară (utilizând formule de calcul MDRD, CKD-EPI, CKD-EPI Cystatin C Equation, CKD-EPI Creatinine-Cystatin C Equation), identificarea albuminuriei şi a altor markeri de afectare renală (hematurie, anormalităţi ale electroliţilor, anomalii structurale renale identificate prin metode imagistice, modificări histologice de origine renală, istoric de transplant renal). Funcţia renală trebuie evaluată periodic la toţi pacienţii (cel puţin anual) şi de câte ori apare o modificare în parametrii clinici şi paraclinici, în cazul pacienţilor hipertensivi sau diabetici. Pe lângă măsurarea creatininei serice şi calcularea ratei de filtrare glomerulară, examenul sumar de urină cu bandeletă reactivă ar trebui efectuat de rutină tuturor pacienţilor(3); când rezultatele evidenţiază modificări anormale, sunt necesare explorări suplimentare: determinarea cantitativă a proteinuriei, determinarea raportului albuminurie/creatinurie în urina de dimineaţă, examenul sedimentului urinar, ionograma serică (monitorizarea potasemiei în mod special, existând risc de hiperpotasemie), examinări imagistice (ecografie, tomografie, scintigrafie, ecografie Doppler de artere renale, angio-RMN).

Îngrijirea pacienţilor hipertensivi cu boală cronică de rinichi presupune muncă în echipă, medici de familie, cardiologi, nefrologi, urologi, diabetologi colaborând în cadrul unor protocoale terapeutice şi de monitorizare. Planul de management cuprinde stabilirea stadiului bolii renale, clasificarea nivelului de hipertensiune şi a tipului de hipertensiune, stabilirea riscului cardiovascular, dar şi a riscului de progresie a bolii renale. Tratamentul se adresează atât hipertensiunii, cât şi bolii renale, încetinirea progresiei alterării funcţiei renale fiind realizată şi prin controlul adecvat al tensiunii arteriale şi al celorlalţi factori de risc.
Obiectivele tratamentului la pacienţii hipertensivi cu boală cronică de rinichi sunt: atingerea valorilor-ţintă pentru TA, reducerea albuminuriei, scăderea riscului cardiovascular prin tratarea tuturor factorilor de risc. Ţintele tensiunii au fost considerate în diferite ghiduri (ESC/ESH 2013, KIDGO 2012), în funcţie de nivelul proteinuriei: 140/90 mmHg dacă proteinuria este nesemnificativă, respectiv 130/80 mmHg dacă albuminuria≥300 mg/24 de ore(3,2). Ghidul american (AAC 2017) consideră ca ţintă de atins 130/80 mmHg pentru toţi pacienţii cu boală cronică de rinichi, iar prezenţa albuminuriei peste 300 mg/zi reprezintă indicaţie pentru utilizarea inhibitorilor enzimei de conversie(6). Ghidul ESC/EHA 2018 stabileşte ca valori-ţintă recomandate pentru pacienţii cu boală cronică de rinichi între 130 şi 140 mmHg (IA). Valorile optime considerate ca ţintă pentru pacienţii cu boală renală constituie încă o problemă care nu şi-a găsit pe deplin răspunsul. Analizele post hoc ale studiului SPRINT (în care valorile-ţintă ale tensiunii arteriale au fost 140 mmHg şi, respectiv, 120 mmHg) au arătat că un control intensiv al TA la pacienţii nediabetici cu afectare moderată sau avansată a funcţiei renale nu pare să scadă riscul cardiovascular al acestora, dar ar putea să crească riscul injuriei acute a rinichiului, probabil consecinţă a hipoperfuziei renale, cunoscându-se faptul că scăderea TA sub 120 mmHg poate avea consecinţe negative de creştere a mortalităţii, conform curbei J a hipertensiunii. Au existat şi alte studii care au confirmat existenţa riscului de insuficienţă renală acută la pacienţii cu afectare renală trataţi agresiv, astfel încât se pune problema evaluării risc-beneficiu în cazul tratării hipertensiunii la pacienţii cu RFG<45 ml/min./1,73 m2(7). Pe de altă parte, sunt studii care arată că scăderea intensivă a TA sistolice (dar nu sub 120 mmHg) la pacienţii cu afectare renală, nedializaţi, a determinat scăderea mortalităţii de orice cauză(8). Valorile-ţintă optime pentru pacienţii cu boală cronică de rinichi rămân încă o problemă de studiat, deocamdată majoritatea ghidurilor indicând beneficii ale reducerii TA între 130 mmHg şi 140 mmHg(9).
Atingerea obiectivelor presupune tratament igienodietetic şi medicamentos.
a) Tratament nemedicamentos
Scăderea în greutate şi dieta hipocalorică se recomandă persoanelor obeze sau supraponderale, cu reducerea şi menţinerea IMC între 18,5 şi 24,9 kg/m2 şi a circumferinţei abdominale ≤102 cm la bărbaţi şi ≤88 cm la femei. Scăderea în greutate, pe de o parte, reduce TA, dar în acelaşi timp există studii observaţionale care au arătat că menţinerea unui IMC în limite, mai ales în stadiile G1-G2, are un efect benefic şi asupra proteinuriei şi determină un prognostic pe termen lung mai bun al bolii renale(5). Dieta recomandată pentru reducerea ponderală nu este întotdeauna foarte uşor de realizat, întrucât aportul proteic nu trebuie să depăşească 1,3 g/kg/zi; de asemenea, dacă pacientul are diabet zaharat, dieta trebuie să fie şi hipoglucidică, iar lipidele nu pot fi administrate în exces deoarece ar determina modificări dislipidemice, crescând riscul cardiovascular. Pe de altă parte, în stadiile avansate (G5 şi dializă) nu se recomandă reducerea excesivă a greutăţii, întrucât, în aceste stadii, conform ,,paradoxului greutăţii”, o greutate mai mare poate avea efect protector.
Ghidurile recomandă restricţie moderată a consumului de proteine (0,8 g/kg/zi) pentru adulţii cu sau fără diabet zaharat şi RFG<30 mg/kg/1,73 m2. În stadiile G1, G2 şi G3 este permis un consum de proteine individualizat, care însă să nu depăşească 1,3 g/kg/zi. În prezent nu se mai recomandă restricţii severe de proteine (<0,6 g/kg/zi) din cauza riscului de malnutriţie.
Există studii observaţionale care au arătat că dieta de tip vegetarian ar avea efect protector asupra funcţiei renale atât în prevenţia primară, cât şi în prevenţia secundară şi că ar fi asociată cu un risc mai scăzut de mortalitate de toate cauzele la pacienţii cu BCR(10). Beneficiile dietei vegetariene în boala renală apar şi datorită faptului că biodisponibilitatea fosfatului din proteinele vegetale este redusă. De asemenea, vegetarienii se pare că au sensibilitatea periferică la insulină crescută şi niveluri scăzute ale glicemiei şi ale producţiei de glucoză endogenă(11).Totuşi, atunci când dieta vegetariană este asociată cu aport de proteine şi aport energetic redus, pot apărea efecte nefavorabile. În cazul pacienţilor cu BCR este necesar un aport proteic şi energetic suficient, pentru a evita malnutriţia protein-calorică, în special în fazele avansate. De aceea, este necesar ca pacienţii cu BCR să beneficieze de monitorizare nutriţională regulată de specialitate şi de indicaţii clare în ceea ce priveşte dieta(12).
Scăderea consumului de sare este indicată tuturor pacienţilor hipertensivi, dar la bolnavul cu afectare renală se indică reducerea aportului de sare sub 2 g Na+/zi (5 g NaCl/zi), întrucât aportul de sare, pe lângă creşterea TA, poate determina şi afectarea funcţiei renale. Consumul de alcool este recomandat să fie redus sub 14 unităţi pe săptămână pentru bărbaţi şi sub 8 unităţi pe săptămână pentru femei (pentru simplificare, unitatea de alcool este definită ca echivalent a 125 ml vin sau 250 ml bere).
Oprirea fumatului este indicată în toate cazurile, scăzând riscul cardiovascular şi încetinind totodată şi progresia afectării funcţiei renale; sunt necesare susţinerea şi consilierea pacienţilor, încurajarea lor, oferirea suportului motivaţional, uneori se recurge la medicaţie (substituenţi nicotinici, bupropion, vareniclină utilizată în doze reduse în cazul insuficienţei renale).
Încurajarea practicării exerciţiului fizic aerobic, 30-60 minute/zi minimum 3-5 zile pe săptămână, este benefică atât pentru scăderea riscului cardiovascular şi reducerea TA, cât şi pentru evoluţia afectării renale, existând unele studii observaţionale care au arătat că persoanele sedentare cu boală cronică de rinichi în stadiul 5 au risc mai mare de deces decât persoanele active(13).
b) Terapia medicamentoasă
Alegerea terapiei medicamentoase se face ţinând cont de vârstă, comorbidităţi, valorile TA, de gradul afectării renale, riscul de progresie a deteriorării funcţiei renale şi de toleranţa tratamentului. Scăderea valorilor TA este adesea dificilă la pacienţii cu afectare renală şi în special la cei vârstnici sau la cei cu diabet zaharat, care asociază frecvent TA diastolică redusă, presiunea pulsului ridicată şi rigiditate vasculară crescută(5). În cazul pacienţilor vârstnici se indică escaladarea graduală a terapiei cu adaptarea dozelor în funcţie de toleranţă, întrucât riscul tulburărilor electrolitice, al deteriorării acute a funcţiei renale, al hipotensiunii ortostatice şi al reacţiilor adverse medicamentoase este mai mare. Tratamentul trebuie, prin urmare, individualizat şi, de cele mai multe ori, sunt necesari doi sau trei agenţi terapeutici. Este unanim recunoscut că utilizarea blocanţilor SRAA (IECA/BRA) reprezintă prima linie de tratament (exceptând cazurile în care aceştia sunt contraindicaţi), având efecte benefice protectoare asupra funcţiei renale şi fiind mai eficienţi decât alte antihipertensive în reducerea albuminuriei. De obicei este necesară terapia combinată şi se recomandă asocierea unui inhibitor al SRAA cu un alt antihipertensiv(3). Nu există studii clare asupra agenţilor terapeutici preferaţi pentru liniile a doua şi a treia, importantă fiind scăderea tensiunii arteriale, iar pentru creşterea complianţei este benefică utilizarea pilulei combinate (cu doi-trei agenţi terapeutici), cu administrare unică pe parcursul zilei. Combinaţia a doi inhibitori ai SRAA nu este recomandată, deşi ar putea avea efecte benefice în reducerea proteinuriei(3).
Inhibitorii enzimei de conversie a angiotensinei (IECA) sunt medicamente de primă intenţie la adulţii cu HTA şi BCR stadiu ≥3 sau BCR stadiul 1-2 şi albuminurie ≥300 mg/zi, întrucât încetinesc şi progresia bolii renale. În cazul unui filtrat glomerular scăzut pot fi administraţi IECA cu eliminare hepatică crescută (50%), cum ar fi trandolapril sau fosinopril. Blocanţii receptorilor de angiotensină (BRA) sunt indicaţi când IECA nu sunt toleraţi sau nu reuşesc să controleze valorile tensionale. Se preferă BRA cu eliminare hepatică de peste 95% (irbesartan, telmisartan) faţă de cei cu eliminare hepatică mai redusă ‒ 40% (candesartan). Toate ghidurile contraindică asocierea IECA cu BRA, întrucât riscul de deteriorare acută a rinichiului, de hipotensiune şi de hiperpotasemie este foarte mare. Combinaţia candesartan sau valsartan şi un IECA poate fi utilizată la bolnavii simptomatici cu insuficienţă cardiacă refractară, doar în spital, de către medicii specialişti, pentru perioade foarte scurte şi sub supraveghere atentă a funcţiei renale şi a electroliţilor (în special potasiu)(2). De asemenea, stenoza bilaterală de artere renale necesită monitorizare atentă a electroliţilor şi a funcţiei renale (boala renovasculară nu reprezintă o contraindicaţie absolută, dar necesită precauţie), ca şi depleţia de fluide. Uneori este necesară scăderea temporară a dozelor de IECA, în cazul pacienţilor cu deshidratare (diaree, vărsături, febră). O mare problemă o reprezintă infecţiile intercurente, stările febrile şi utilizarea antiinflamatoarelor nesteroidiene la pacienţii renali hipertensivi care au în schema terapeutică IECA/BRA, deoarece se poate produce injurie acută a rinichilor, cu prăbuşirea bruscă a ratei de filtrare glomerulară. De aceea, mai ales la vârstnici, se vor supraveghea atent stările infecţioase şi febrile şi se evită antiinflamatoarele de uz sistemic, preferându-le pe cele topice. O creştere a creatininei cu peste 30%, respectiv o scădere a RFG cu mai mult de 25% impun oprirea temporară a IECA/BRA, repetarea testelor, căutarea altor cauze de progresie renală (depleţie volumică, stări infecţioase, utilizarea de antiinflamatoare), investigarea unei posibile stenoze de artere renale. În cazul în care RFG scade cu mai puţin de 25% sau creatinina creşte cu mai puţin de 30%, se repetă testarea peste una-două săptămâni, fără a se opri medicaţia hipotensoare, dar cu urmărirea atentă a electroliţilor(4). IECA şi BRA au efecte benefice vasoprotectoare şi de scădere a riscului cardiovascular, fiind utili şi pentru alte comorbidităţi vasculare pe care pacienţii le-ar putea prezenta (insuficienţă cardiacă, infarct miocardic, accident vascular cerebral) şi rămân în continuare cei mai indicaţi agenţi terapeutici la bolnavul hipertensiv cu afectare renală.
Antagoniştii aldosteronici (spironolactona, eplerenona) au indicaţii limitate la pacienţii cu afectare a funcţiei renale, din cauza riscului mare de hiperkaliemie; studiile au arătat însă că adăugarea antialdosteronicelor la terapie ar fi benefică pentru reducerea albuminuriei(9). Cu toate acestea, când RFG scade sub 30 ml/min./1,73 m2, este recomandat în ghiduri să se evite antialdosteronicele, ca şi diureticele tiazidice (hidroclorotiazida, indapamid), fiind indicate diureticele de ansă (furosemid). Se evită asocierea unui antagonist de aldosteron cu un inhibitor al SRAA, din cauza riscului de reducere excesivă a funcţiei renale şi de hiperpotasemie(3).
Diureticele tiazidice şi tiazid-like (preferate de ghidul NICE) sunt utilizate ca medicaţie adiţională la pacienţii hipertensivi cu RFG >30 ml/min./1,73 m2; ele scad retenţia de apă şi sare, dar exercită şi un efect vasodilatator direct şi indirect(5). Când RFG scade sub 30 ml/min./1,73 m2, este indicată utilizarea diureticelor de ansă (furosemid), cu menţiunea că ele sunt mai eficiente îndeosebi pe termen scurt şi că uneori sunt necesare doze crescute de diuretic pentru a obţine efectele dorite (de exemplu, într-o insuficienţă cardiacă congestivă pot fi necesare doze mari de diuretic pentru a scădea congestia periferică sau pulmonară). Combinaţia diureticelor de ansă şi a celor tiazidice este recomandată atunci când volumul extracelular este mare, când există congestie periferică (cum ar fi cazul insuficienţei cardiace). Se recomandă utilizarea diureticelor sub monitorizarea tensiunii arteriale, a greutăţii, a ionogramei (potasiu seric) şi a funcţiei renale (creatinină, RFG). Combinaţia diureticelor tiazidice cu antialdosteronice este indicată în caz de hipopotasemie, sub supravegherea ionogramei serice.
Blocantele canalelor de calciu (BCC) au rol benefic asupra scăderii tensiunii arteriale. Asocierea BCC cu IECA/BRA are ca efect diminuarea reacţiilor adverse ale blocantelor de calciu (edeme maleolare) datorate dilatării arteriolelor precapilare, fiind astfel mai bine tolerate. BCC dihidropiridinice blochează predominant arteriolele aferente şi cresc presiunea intraglomerulară şi excreţia de albumină; de aceea, nu sunt indicate la bolnavii cu albuminurie fără să fie asociate cu IECA/BRA, care au efect vasodilatator predominant pe arteriolele eferente(5). Blocanţii canalelor de calciu nu se acumulează la pacienţii cu boală renală cronică, cu excepţia nicardipinei şi nimodipinei, care din acest motiv ar trebui evitate. Blocanţii canalelor de calciu non-dihidropiridinici, utilizaţi când există tahiaritmii supraventriculare, se recomandă să nu se asocieze cu betablocante, din cauza efectului inotrop negativ care se cumulează.
Betablocantele (BB) nu sunt considerate agenţi hipotensori de primă linie la pacientul hipertensiv cu boală renală cronică, dar ele vor fi indicate ferm atunci când patologia asociată necesită betablocante (insuficienţă cardiacă, sindroame coronariene). Se pot utiliza carvedilol, nebivolol, metoprolol succinat în doze neajustate; când RFG scade sub 30 ml/min./1,73 m2, poate fi necesară scăderea dozelor. Bisoprolul şi atenololul (hidrofile) se pot acumula sub formă de metaboliţi activi la pacientul renal şi pot determina bradiaritmii, de aceea se recomandă evitarea lor când filtratul glomerular este redus.
Alfa-1 blocantele (prazosin, doxazosin, terazosin) nu sunt utilizate de rutină ca antihipertensive din cauza faptului că sunt frecvent asociate cu hipotensiune ortostatică, dar ele pot fi luate în consideraţie la bărbaţii cu hipertrofie benignă de prostată simptomatică, pentru efectul benefic asupra simptomelor celei din urmă; de menţionat că dozele nu necesită ajustare cu gradul de afectare a funcţiei renale.
Agoniştii centrali alfa-adrenergici sunt consideraţi ca adjuvanţi în special în cazul HTA rezistente, efectul lor fiind de vasodilataţie periferică. Metildopa şi clonidina nu necesită în general reducerea dozelor la pacienţii cu afectare moderată a funcţiei renale; în cazul în care RGF<50 ml/min./1,73 m2, se măreşte intervalul dintre administrări la 8-12 ore, în funcţie de valoarea RFG. Moxonidina este excretată în mare parte renal şi necesită reducerea dozelor la jumătate. Rilmenidina se poate administra până la RFG 15 ml/min./1,73 m2, după care este contraindicată(2).
Strategia de tratament în HTA din boala cronică de rinichi (definită ca RFG<60 ml/min./1,73 m2 cu sau fără proteinurie), recomandată de ghidurile în vigoare, este prezentată în tabelul 4.
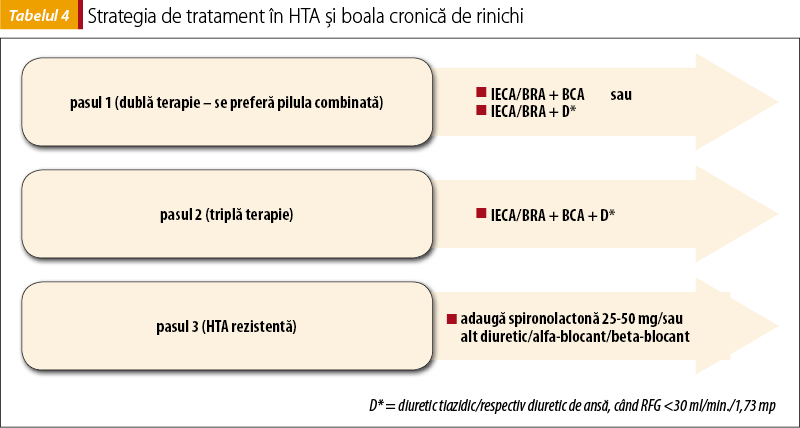
Pe lângă reducerea TA, atingerea ţintelor dorite şi reducerea albuminuriei, la pacientul hipertensiv cu boală cronică de rinichi se recomandă tratarea tuturor factorilor de risc asociaţi: dislipidemie, diabet zaharat, hiperuricemie. Întrucât pacientul cu boală renală se caracterizează printr-un profil lipidic intens aterogen şi risc cardiovascular foarte înalt, ţintele de LDL colesterol sunt sub 70 mg/dl sau scăderea LDL colesterolului cu peste 50% din valoarea iniţială, obiective care pot fi atinse cu ajutorul statinelor (de preferat statine cu eliminare renală minimă: atorvastatina, fluvastatina, pitavastatina), asociate sau nu cu ezetimib 10 mg/zi. Fenofibratul se va evita la pacienţii cu RFG redusă. Antiplachetarele (aspirina) se vor folosi la pacienţii cu boală renală cronică ca prevenţie secundară, nedovedindu-şi efectele benefice în prevenţia primară (riscul de hemoragii depăşind efectele benefice). La pacienţii cu diabet zaharat se indică obţinerea unui control bun al glicemiei şi menţinerea HbA1c<7,5%, evitând tratarea agresivă a diabetului, întrucât riscul de hipoglicemie la pacienţii cu BCR este mai mare decât la cei fără afectare renală. Utilizarea metforminului este sigură dacă RFG este peste 45 ml/min./1,73 m2, după care dozele trebuie ajustate şi revizuită întreaga terapie antidiabetică.
În concluzie, pacientul hipertensiv cu boală cronică de rinichi este un pacient aflat la risc cardiovascular înalt şi foarte înalt, cu creşterea ratei evenimentelor cardiovasculare majore, dar şi cu creşterea riscului de progresie a deteriorării funcţiei renale. HTA este una dintre principalele cauze ale bolii cronice de rinichi sau poate fi ea însăşi secundară afectării renoparenchimatoase sau renovasculare. De aceea, sunt necesare monitorizarea parametrilor clinici şi paraclinici şi tratarea hipertensiunii, cu atingerea ţintelor propuse de ghiduri, utilizând combinaţii de doi-trei agenţi hipotensori, alături de măsurile nefarmacologice, adesea fiind nevoie de lucrul în echipă. Abordarea pacienţilor va ţine seama de vârstă, comorbidităţi, stadiile hipertensiunii şi ale bolii renale, precum şi de prezenţa proteinuriei. Terapia corectă a hipertensiunii scade atât riscul de evenimente cardiovasculare, riscul de mortalitate de orice cauză, cât şi întârzie progresia afectării funcţiei renale spre stadiile finale şi dializă.
Conflict of interests: The author declares no conflict of interests.
Bibliografie
- Guyton&Hall. Tratat de fiziologie a omului. 11th ed. Cuculici GP, Gheorghiu AW, editors. Bucureşti: Editura Medicală Callisto; 2007.
- KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney International supplements. 2013 January;3(1).
- Fagard R, Mancia G. Ghidul ESH/ESC pentru managementul hipertensiunii arteriale 2013. Eur Heart J;34.
- Judd E, Calhoun DA. Management of Hypertension in CKD: Beyond the Guidelines. Adv Chronic Kidney Dis. 2015 Mar; 22(2):116-122.
- Cătălina AG, Delia Ş. Hipertensiunea arterală şi boala cronică de rinichi. In Aursulesei V, Bădilă E, Bartoş D, editors. Hipertensiunea arterială. Bucureşti: Niculescu; 2017. 382-396.
- Whelton PK et al. 2017 Guideline for the Prevention, Detection, Evaluation, and Management of High Blood Pressure in Adults. J Am Coll Cardiol. 2017 Sep.
- Obi Y, Kalantar-Zadeh K, Shintani, et al. Estimated glomerular filtration rate and the risk-benefit profile of intensive blood pressure control amongst nondiabetic patients: a post hoc analysis of a randomized clinical trial. J Intern Med. 2017.
- Malhotra R, Ahn NH, Benavente O, et al. Association between more intensive vs. less intensive blood pressure lowering and risk of mortality in chronic kidney disease stages 3 to 5: A systematic review and meta-analysis. Jama Intern Med. 2017.
- Csaba PK. The Ideal Blood Pressure Target for Patients with Chronic Kidney Disease - Searching for the Sweet Spot. Jama Intern Med. 2017 October;177(10).
- Chauveau P, Koppe L, Combe C, et al. Vegetarian diets and chronic kidney disease. Nephrol Dial Transplant. 2018 Jul;5.
- Anna GB, Beata F, Jacek R. Vegetarian Diet in Chronic Kidney Disease - A Friend or Foe. Nutrients. 2017 Apr;9(4):374.
- Chauveau P, Combe C, Fouque D, Aparicio M. Vegetarianism: advantages and drawbacks in patients with chronic kidney diseases. J Ren Nutr. 2013 Nov;23(6):399-405.
- Stack AG, Molony DA, Rves T. Association of physical activity with mortality in the US dialysis population. Am J Kidney Dis. 2005; 45;690-701.
- KDIGO 2017 Clinical practice guideline for the diagnosis, evaluation, prevention and treatment of chronickidney disease-mineral and bone disorder (CKD-MBD). kIsupplements. 2017 July;7(1).
Articole din ediţiile anterioare
Hipertensiunea arterială în sarcină
Hipertensiunea arterială în sarcină este o patologie cu incidenţă în creştere. Prin complexitatea manifestărilor şi severitatea complicaţiilor ma...
Sindromul de apnee în somn - cauză a hipertensiunii arteriale secundare
Afecțiunea, denumită sindrom de apnee în somn (SAS), reprezintă o tulburare de respirație asociată somnului, caracterizată prin episoade repetitive...
Managementul hipertensiunii arteriale la pacientul cu risc cardiovascular înalt
Hipertensiunea arterială este o patologie foarte frecventă, care afectează majoritatea populaţiei, şi în asociere cu diabetul zaharat de tip 2 c...
Relaţia dintre vitamina D şi riscul cardiovascular
În ultimii ani, au existat tot mai multe cercetări ce au încercat să demonstreze rolul pe care vitamina D, şi anume 25 (OH) vitamina D, îl are în o...