Systemic lupus erythematosus is a chronic and multisystemic autoimmune disease that can occur in members of the same family. Genetic factors are still unidentified and not all relatives with these risk factors are predestined to develop the disease, but are more likely(1). Relatives of systemic lupus erythematosus (SLE) patients appear to be at higher risk of SLE and other autoimmune diseases, but individual family risk estimates are largely unavailable or unsafe. Moreover, the relative contribution of genetic factors, shared and divided into the susceptibility of SLE, remains unclear(2,3). The presence of antinuclear antibodies (ANA) is mainly associated with connective tissue diseases. In addition, their presence can also be found in healthy people. These antibodies are more common in women and in elderly people(4,5). It is known that subjects who are in the preclinical stages of SLE are represented in the healthy population with positive ANA autoimmunity, and the early detection of these antibodies often allows a rapid diagnosis of this disease(3).
Testarea anticorpilor ANA la rudele de gradul întâi ale pacienţilor cu lupus eritematos sistemic (LES)
ANA antibodies testing in first-degree relatives of patients with systemic lupus erythematosus
First published: 24 septembrie 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/MED.130.4.2019.2509
Abstract
Rezumat
Lupusul eritematos sistemic este o boală autoimună cronică, multisistemică, ce poate apărea la membrii aceleiaşi familii. Factorii genetici sunt încă neidentificaţi, însă nu toate rudele cu aceşti factori de risc sunt predestinaţi la a dezvolta boala, dar au o probabilitate mai mare(1). Rudele pacienţilor cu lupus eritematos sistemic (LES) par să prezinte un risc mai mare de LES şi alte boli autoimune, însă estimările riscurilor familiale individuale sunt în mare parte indisponibile sau nesigure. Mai mult, contribuţia relativă a factorilor de mediu şi genetici, partajaţi şi împărţiţi la susceptibilitatea SLE, rămâne neclară(2,3). Prezenţa anticorpilor antinucleari (ANA) este în principal asociată cu bolile ţesutului conjunctiv. În plus, prezenţa lor se poate întâlni şi la oameni sănătoşi. Aceşti anticorpi sunt mai frecvenţi la femei şi la vârstnici(4,5). Este cunoscut faptul că persoanele care se află în stadiile preclinice de LES sunt reprezentate în populaţia sănătoasă de autoimunitate ANA pozitivă, iar detectarea acestor anticorpi permite adesea o diagnosticare rapidă a acestei patologii(3).
Introducere
Lupusul eritematos sistemic (LES) se caracterizează prin autoimunitate pozitivă de tip lupic, reprezentată de prezenţa anticorpilor ANA.
Incidenţa unui nivel semnificativ crescut al anticorpilor ANA în populaţia generală este de 2,5%(2). Majoritatea persoanelor cu anticorpi ANA pozitivi nu sunt diagnosticate cu o boală autoimună reumatică, iar probabilitatea de a dezvolta în viitor o astfel de boală este scăzută. Acest lucru este susţinut de faptul că bolile autoimune apar în populaţia generală cu o frecvenţă de 5% până la 7%(5,6), iar apariţia LES în populaţia generală nu depăşeşte 0,1%.
Astfel, prezenţa anticorpilor ANA pozitivi nu ar trebui să încurajeze diagnosticul extins de boli de ţesut conjunctiv la persoanele sănătoase fără semne clinice. Mai mult, prezenţa anticorpilor ANA în populaţia umană sugerează că anticorpii antinucleari pot fi o componentă importantă a răspunsului imun normal. Pe de altă parte, nu trebuie să uităm că prezenţa anticorpilor poate fi observată în ser cu mulţi ani înainte de diagnosticul bolii autoimune. Acesta este cazul lupusului eritematos sistemic şi al sindromului Sjögren, în care anticorpii ANA sunt prezenţi chiar şi cu mulţi ani înainte de apariţia primelor simptome ale bolii(7). Astfel, este cunoscut faptul că persoanele care se află în stadiile preclinice de LES sunt reprezentate în populaţia sănătoasă de autoimunitate ANA pozitivă, iar detectarea acestor anticorpi permite adesea o diagnosticare rapidă a acestei patologii(8).
Având în vedere că anticorpii antinucleari pot fi prezenţi atât la indivizii sănătoşi, cât şi la cei cu afecţiuni non-reumatice, monitorizarea cantităţii suplimentare trebuie efectuată doar în cazul prezenţei simptomelor clinice. Prezenţa anticorpilor ANA fără semne clinice de boală autoimună nu necesită verificări periodice reumatice(9).
Obiective
Luând în considerare datele puţine şi controversate în ceea ce priveşte determinismul genetic al pacienţilor cu LES în rândul rudelor, obiectivul acestui studiu a fost acela de a investiga frecvenţa anticorpilor ANA la rudele de gradul I ale pacienţilor cu LES şi corelarea acestor rezultate cu anumite manifestări clinice sau de organ, precum şi cu activitatea bolii pacienţilor cu LES.
Materiale şi metodă
În perioada ianuarie 2018 – februarie 2019, am înrolat 112 pacienţi cu diagnostic cert de LES respectând criteriile de clasificare SLICC din 2012. Criteriile de excludere a pacienţilor au fost diagnosticul incert/incomplet de LES sau pierderea din evidenţa spitalului a acestor pacienţi.
Datele demografice (vârsta, sexul, rasa) şi clinice (antecedente heredo-colaterale, fumatul) au fost colectate pentru fiecare pacient.
Rezultate
Studiul a inclus 112 pacienţi cu LES, cu o durată a bolii în medie de 11 ani. Toţi pacienţii incluşi în studiu erau de rasă albă, caucaziană.
Distribuţia pe sexe este reprezentată de femei în 77% din cazuri şi de bărbaţi în 23% din cazuri (figura 1).
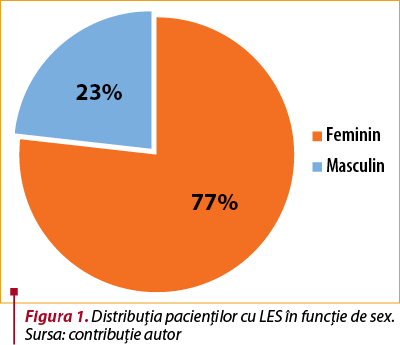
Distribuţia pacienţilor pe grupe de vârstă a arătat că 8 pacienţi erau sub 30 de ani, 64 de pacienţi între 30 şi 50 de ani, iar 40 de pacienţi aveau peste 50 de ani. Vârsta medie este de 47,3±11,9 ani. Distribuţia pe vârste este reprezentată în figura 2.
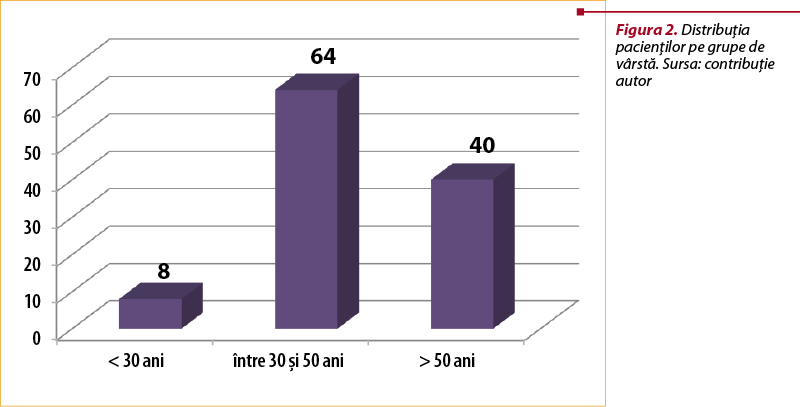
Distribuţia în funcţie de mediul de rezidenţă este reprezentată în figura 3. 53% din pacienţi proveneau din mediul urban şi 47% din mediul rural.
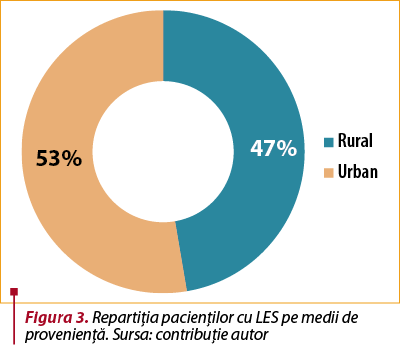
Dintre cei 112 pacienţi cu LES, 6 (5,3%) erau fără studii, 15 (13,3%) au absolvit şcoala primară, 64 (57,1%) au avut grad mediu de educaţie şi 27 (24,1%) aveau grad înalt de educaţie (figura 4). Astfel, putem afirma că profilul socioprofesional al acestor pacienţi este dominat de cei cu grad mediu de educaţie, fapt ce ar putea avea un impact semnificativ asupra recunoaşterii şi înţelegerii gravităţii bolii.
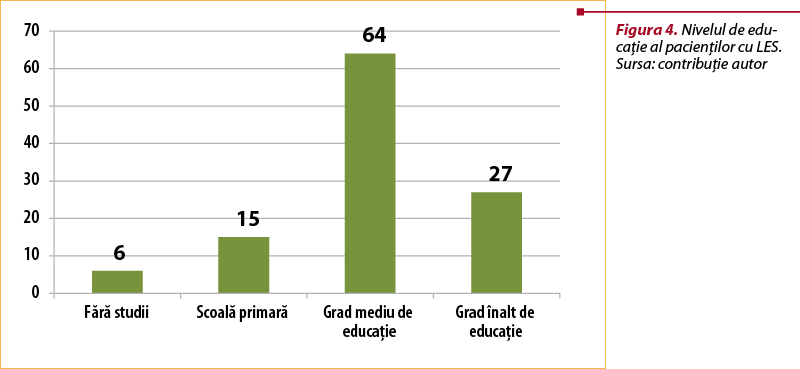
Din punctul de vedere al statusului civil, 61,2% locuiau cu un/o partener/ă şi 38,8% locuiau cu familia sau cu copiii.
Caracteristicile pacienţilor cu LES
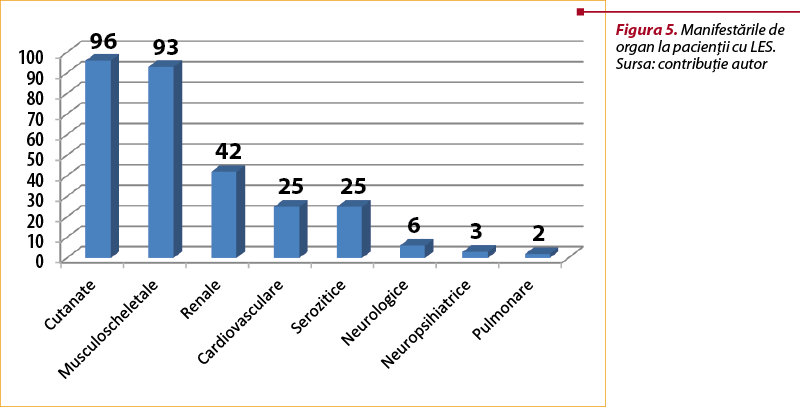
Studiul de faţă a cuprins şi analiza afectărilor de organ la pacienţii cu LES. Manifestările cutante au fost prezente la 96 dintre pacienţi, iar manifestările musculoscheletale la 93 dintre pacienţi. Dintre afectările severe de organ, afectarea renală a fost cea mai frecventă, întâlnită la 42 (37,5%) dintre pacienţi. Manifestările cardiace s-au întâlnit la fel de des precum manifestările serozitice, la 25 dintre pacienţi. În număr mai mic, pacienţii au suferit pe parcursul bolii de manifestări neurologice, neuropsihiatrice şi pulmonare (figura 5).
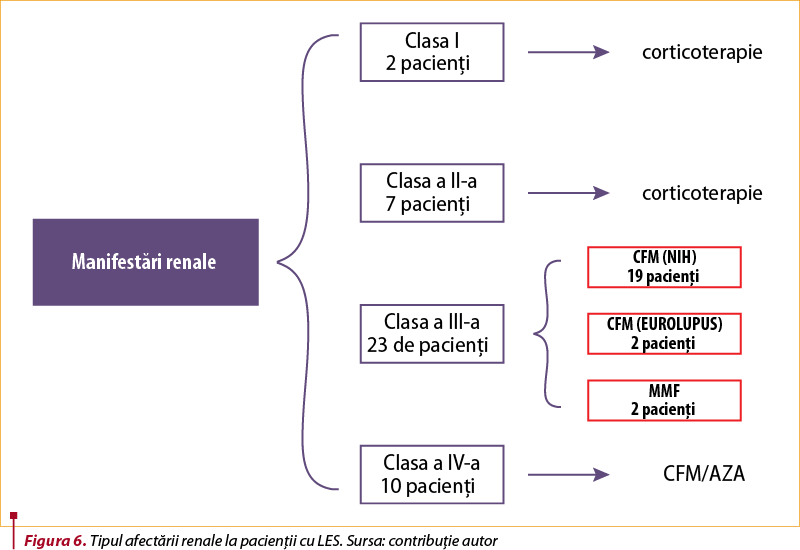
În ceea ce priveşte afectarea renală, dintre cei 42 de pacienţi, tipul predominant a fost glomerulonefrita de clasă III, întâlnită la 23 dintre pacienţi. Mai mult decât atât, afectarea renală a fost observată în special la pacienţii care aveau concomitent şi afectare cardiacă şi prezentau autoimunitate pozitivă cu anticorpi anti-ADN dublucatenari, precum şi hipocomplementemie.
Dintre pacienţii cu nefrită proliferativă focală (clasa III), conform clasificării Societăţii Internaţionale de Nefrologie şi a Societăţii de Patologie Renală (ISN/RPS), 2004, 19 au primit tratament conform regimului terapeutic standard – protocolul NIH (National Institute of Health) şi doar doi au fost trataţi cu ciclofosfamidă, conform protocolului EUROLUPUS. Două paciente au primit tratament cu micofenolat mofetil, în defavoarea ciclofosfamidei, pentru a reduce riscul de infertilitate, acestea având vârsta sub 25 de ani. Tipul afectării renale la pacienţii cu LES este ilustrat în figura 6.
Sindromul antifosfolipidic secundar LES apare mai pregnant la sexul feminin, iar patogeneza acestuia şi patogeneza LES par să fie foarte intricate. În acest studiu, pacienţii au fost diagnosticaţi conform criteriilor de clasificare Sydney din 2006, secundar bolii lupice. Au fost observaţi 31 de pacienţi cu sindrom antifosfolipidic, majoritatea cu anticorpi anti-cardiolipină din clasa IgM şi IgG. Dintre aceştia, 26 de pacienţi urmau tratament cu anticoagulant oral.
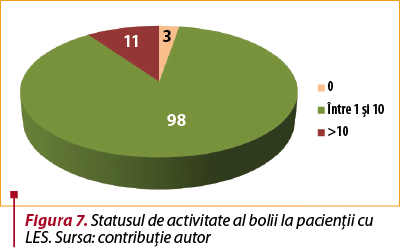
O provocare particulară la pacienţii cu LES a constituit-o mult timp distingerea statusului de boală. Un indice menit să stabilească gravitatea în LES îl constituie scorul SELENA-SLEDAI. Astfel, în prezentul studiu, un scor SELENA-SLEDAI >11, însemnând activitate intensă de boală, a fost întâlnit la 10 pacienţi, un scor SELENA-SLEDAI între 1 şi 10, însemnând activitate moderată de boală, a fost întâlnit la 98 de pacienţi şi doar trei pacienţi atingeau un status inactiv de boală, cu un scor SELENA-SLEDAI=0 (figura 7). 11 pacienţi erau consideraţi cu activitate intensă de boală, fapt ce subliniază încă o dată dificultatea atingerii unei remisiuni.
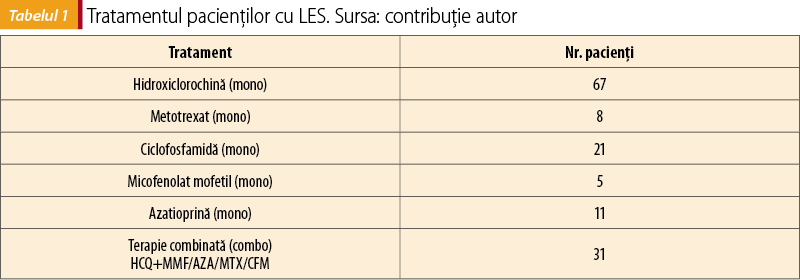
În ceea ce priveşte tratamentul acestor pacienţi cu LES, 67 dintre aceştia urmau monoterapie cu hidroxiclorochină, 21 dintre ei erau în tratament cu ciclofosfamidă, 11 cu azatioprină, 8 cu metotrexat, în special pentru afectarea cutanată sau pentru formele de LES neameninţătoare de viaţă, sau atunci când celelalte medicamente nu au avut beneficii, şi 5 pacienţi urmau tratament cu micofenolat mofetil pentru manifestările severe de organ. 31 dintre aceştia luau tratament combinat hidroxiclorochină şi cu alt imunosupresor, precum azatioprină, micofenolat mofetil, metotrexat sau ciclofosfamidă (tabelul 1).
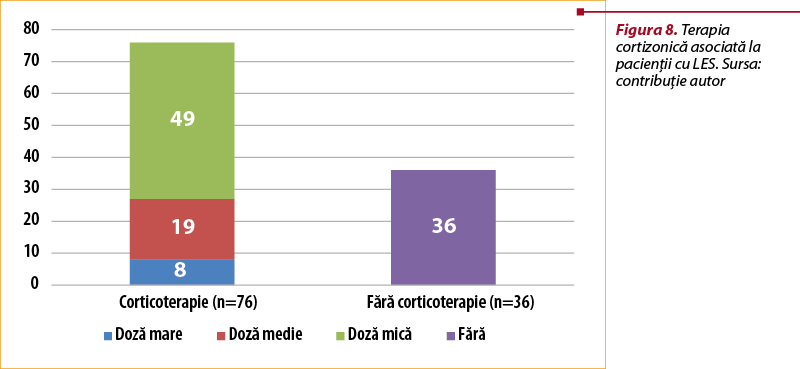
A fost, de asemenea, evaluată şi asocierea corticoterapiei la tratamentul imunosupresor. Astfel, 76 (67,8%) de pacienţi urmau corticoterapie, în timp ce 36 (32,1%) erau fără corticoterapie, lucru ce demonstrează faptul că boala lupică este într-un mare procent total necontrolată. Dintre pacienţii care urmează corticoterapie, 49 sunt cu doză mică, 19 sunt cu doză medie şi 8 pacienţi au doză mare de cortizon (peste 30 mg/zi echivalent prednison) pentru obţinerea controlului asupra manifestărilor bolii (figura 8).
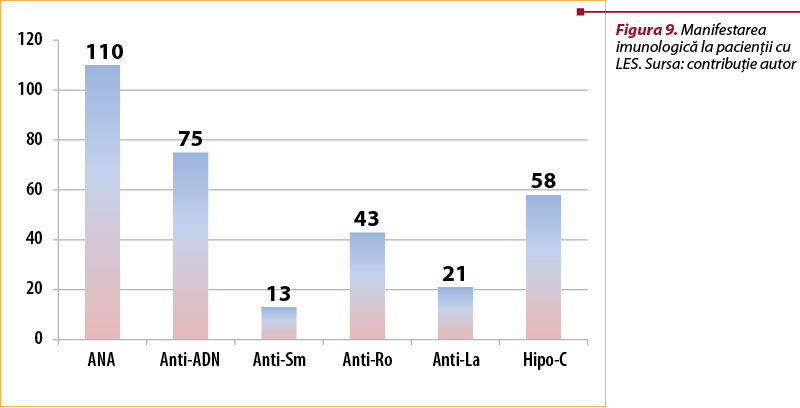
Anomalia imună caracteristică LES este reprezentată de apariţia autoanticorpilor. Astfel, anticorpii ANA au fost prezenţi la 110 pacienţi, anticorpii anti-ADN dublu catenar (ADNdc), care reprezintă un marker de înaltă specificitate în LES, au fost observaţi la 75 de pacienţi, anticorpii anti-Smith (anti-Sm) la 13 pacienţi, anticorpii anti-Ro la 43 de pacienţi şi anticorpii anti-La, la 21 de pacienţi. De asemenea, în momentul studiului, 51,7% dintre pacienţi prezentau hipocomplementemie (figura 9).
Testarea anticorpilor ANA la rudele pacienţilor cu LES
Scopul principal al acestui studiu a fost determinarea numărului de rude de gradul I pe linie dreaptă ascendentă şi descendentă (părinţi, copii) ce prezintă anticorpi ANA pozitivi.
Astfel, rudele de gradul I au fost testate cu ajutorul unei probe sangvine unice, folosind un test de imunofluorescenţă indirectă (IIF) pentru anticorpii ANA. Substratul utilizat de acest test este o linie celulară epitelială umană, fixată (HEp-2). Prin această metodă se pot distinge mai multe aspecte (omogen, pătat, nucleolar, centromer, mitocondrial), care se corelează cu o anumită specificitate a anticorpilor şi, ca urmare, permit asocierea cu o anumită boală şi alegerea ţintită a testelor ulterioare. În cazul probelor pozitive, se realizează diluţii seriale, rezultatul fiind exprimat semicantitativ, sub formă de titru (ultimul titru la care reacţia a fost pozitivă).
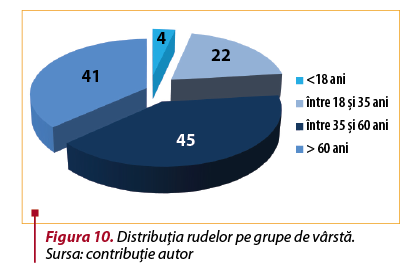
112 rude au fost testate pentru screeningul ANA, dintre care 66 au fost mostre de la mame, 39 de la fiice şi 7 de la fii. 45 (40,1%) aveau vârsta cuprinsă între 35 şi 60 de ani, urmaţi îndeaproape de rudele cu vârsta de peste 60 de ani (36,6%) (figura 10). Pentru prelevarea probelor sangvine ale rudelor <18 ani (4 minori), părinţii şi-au dat acordul prin semnarea unui consimţământ informat.
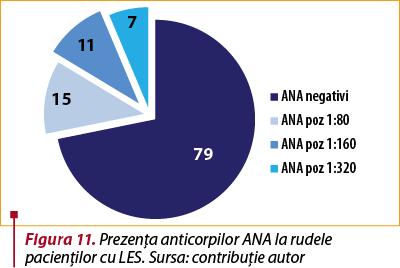
Valoarea rezultatelor s-a considerat pozitivă la o diluţie >1:80. Astfel, din totalul de 112 rude am identificat 33 de rude cu anticorpi ANA pozitivi, dintre care 15 rude cu anticorpi ANA cu titru 1:80, 11 rude cu titru 1:160 şi 7 rude cu titru 1:320 (figura 11). Nicio rudă nu prezenta vreun semn clinic de lupus eritematos sistemic sau vreo altă boală autoimună reumatică.
Discuţie
Un grup care a cuprins 112 pacienţi cu LES a fost studiat, dintre care 86 de femei şi 26 de bărbaţi, cu vârsta medie de 47,3 ani. 53% din pacienţi proveneau din mediul urban şi 47% din mediul rural.
Rezultatele cu privire la caracteristicile clinice şi imunologice ale pacienţilor cu LES au fost superpozabile cu datele din majoritatea studiilor.
Majoritatea pacienţilor (98 de pacienţi) au avut activitate medie de boală, cu scor SELENA-SLEDAI între 1 şi 10.
Cei mai mulţi dintre pacienţi, 67 dintre aceştia, urmau tratament monoterapic cu hidroxiclorochină şi doar 21 de pacienţi utilizau ciclofosfamidă. De asemenea, 31 de pacienţi urmau terapie combinată, respectiv hidroxiclorochină, asociată cu un alt imunosupresor.
A fost, de asemenea, evaluată şi asocierea corticoterapiei la tratamentul imunosupresor. Astfel, 76 (67,8%) de pacienţi urmează corticoterapie, în timp ce 36 (32,1%) de pacienţi sunt fără corticoterapie, lucru ce demonstrează faptul că boala lupică este într-un mare procent total necontrolată.
Dintre pacienţii care urmează corticoterapie, 49 au doză mică, 19 sunt cu doză medie şi 8 pacienţi au doză mare de cortizon.
Importanţa agregării familiale a fost stabilită în acest studiu. Rudele de gradul I ale pacienţilor cu LES au fost testate cu ajutorul unei probe sangvine unice, folosind un test de imunofluorescenţă indirectă (IIF) pentru anticorpii ANA. 112 rude au fost testate pentru screeningul ANA. Astfel, din totalul de 112 rude am identificat 33 de rude cu anticorpi ANA pozitivi, dintre care 13 rude cu anticorpi ANA cu titru 1:80, 11 rude cu titru 1:160 şi 7 rude cu titru 1:320. Patternul de fluorescenţă citoplasmatică a fost de tip omogen în 18 cazuri, pătat în 9 cazuri şi inelar în 6 cazuri.
Dintre rudele pacienţilor cu anticorpi ANA în titru de 1:160, şase aveau în familie rude cu LES cu manifestări cardiace şi neurologice, iar unul avea mama cu afectare neuropsihiatrică. Cinci rude cu anticorpi ANA în titru de 1:160 aveau în familie pacienţi cu LES cu afectare renală. O valoare semnificativă statistic o reprezintă faptul că pacienţii cu anticorpi anti-ADNdc pozitivi se corelează cu anticorpii ANA negativi la rudele de gradul întâi (rS=-0,254, p=0,007).
Una din limitele studiului a constat în faptul că lotul de pacienţi a fost din România. Este recomandat ca screeningul să fie făcut şi în altă ţară, pentru a observa veridicitatea rezultatelor. Un alt punct slab a fost acela că nu s-au cunoscut date paraclinice şi de laborator ale rudelor pacienţilor cu LES, cu excepţia rezultatelor anticorpilor ANA. Corelaţii între nivelul anticorpilor ANA şi anumite anomalii hematologice (leucopenie, trombocitopenie) ar fi fost de mare importanţă pentru a avea mai multe criterii paraclinice cu o probabilitate mai mare de a dezvolta LES în rândul rudelor.
Concluzii
Patogeneza LES este multifactorială, incluzând factori de mediu şi factori genetici. Aceştia din urmă joacă un rol crucial în susceptibilitatea bolii.
Agregarea familială a fost raportată în diverse rânduri în studii observaţionale, dar acesta este primul studiu transversal care a investigat agregarea familială într-un lot de pacienţi cu LES din România. Aceste rezultate pot fi luate în considerare atunci când consiliem familiile acestor pacienţi.
Rudele pacienţilor cu LES au un risc mai mare de a dezvolta LES.
Având în vedere că anticorpii antinucleari pot fi prezenţi atât la indivizii sănătoşi, cât şi la cei cu afecţiuni non-reumatice, monitorizarea cantităţii suplimentare trebuie efectuată doar în cazul prezenţei simptomelor clinice. Prezenţa anticorpilor ANA fără semne clinice de boală autoimună nu necesită verificări periodice reumatice.
Detectarea acestor anticorpi permite adesea o diagnosticare rapidă a acestei patologii. Nu trebuie neglijat faptul că ei pot fi prezenţi la vârste înaintate, fără ca persoana să sufere de vreo boală autoimună.
De asemenea, merită să ţinem seama de faptul că sarcina poate induce apariţia anticorpilor ANA la femeile sănătoase(9). În timpul sarcinii, poate apărea o expunere extinsă la antigenii nucleari. În plus, există o creştere a activităţii inflamatorii, care poate afecta, de asemenea, răspunsul imun(10).
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Rai E, Wakeland EK, Genetic predisposition to autoimmunity - what have we learned? Semin Immunol. 2011 Apr; 23(2):67-83.
- Wandstrat AE, Carr-Johnson F, Branch V, Gray H, Fairhurst AM, Reimold A, Karp D, Wakeland EK, Olsen NJ. Autoantibody profiling to identify individuals at risk for systemic lupus erythematosus. J Autoimmun. 2006 Nov; 27(3):153-60.
- O’Sullivan M, McLean-Tooke A, Loh RK. Antinuclear antibody test. Aust Fam Physician. 2013 Oct; 42(10):718-21.
- Karamehic J, Subasic D, Gavrankapetanovic F, Zecevic L, Eminovic I, Memic S, Seric N, Drace Z. The incidence of antinuclear antibodies (ANA) detected by indirect immunofluorescence assay (IFA) method.Med Arh. 2007; 61(1):16-9.
- Davidson A, Diamond B. Autoimmune diseases. N Engl J Med. 2001 Aug 2; 345(5):340-50.
- Heinlen LD, McClain MT, Merrill J, Akbarali YW, Edgerton CC, Harley JB, James JA. Clinical criteria for systemic lupus erythematosus precede diagnosis, and associated autoantibodies are present before clinical symptoms.Arthritis Rheum. 2007 Jul; 56(7):2344-51.
- Arbuckle MR, McClain MT, Rubertone MV, Scofield RH, Dennis GJ, James JA, Harley JB. Development of autoantibodies before the clinical onset of systemic lupus erythematosus. N Engl J Med. 2003 Oct 16; 349(16):1526-33.
- Li QZ, Karp DR, Quan J, Branch VK, Zhou J, Lian Y, Chong BF, Wakeland EK, Olsen NJ. Risk factors for ANA positivity in healthy persons. Arthritis Res Ther. 2011 Mar 2; 13(2):R38.
- Puszczewicz M, Białkowska-Puszczewicz G, Majewski D. Znaczenie autoprzeciwciał w rozpoznaniu chorób reumatycznych. Post Nauk Med. 2012;2:156–163.
- Bianchi DW, Wataganara T, Lapaire O, Tjoa ML, Maron JL, Larrabee PB, Johnson KL. Fetal nucleic acids in maternal body fluids: an update. Ann N Y Acad Sci. 2006 Sep; 1075():63-73.
Articole din ediţiile anterioare
Agregarea familială la pacienţii cu boli autoimune reumatice
Afecţiunile autoimune reumatice au un determinism multifactorial, fiind cauzate de diverşi factori ambientali ce acţionează pe susceptibilitatea ge...
Displazia cleidocraniană – consideraţii clinice şi de diagnostic la doi fraţi
Displazia cleidocraniană este o boală genetică ce afectează ambele sexe, cu transmitere autozomal dominantă. Anomaliile osoase, asociate cu anoma...