Recurrent aphthous stomatitis is the most common chronic disease of the oral cavity. The basic etiology remains uncertain and no curative treatment is available. From the perspective of the clinical presentation, the recurrent aphthous stomatitis has three characteristic types, namely the minor type, the major type and the herpetiform type. Although the exact etiology is still unknown, potential triggers include: genetic predisposition, viral and bacterial infections, food allergies, vitamin and microelement deficiencies, systemic diseases, increased oxidative stress, hormonal defects, mechanical injury and anxiety.
Abordarea factorilor predispozanţi şi a tipurilor de stomatită aftoasă recurentă
Addressing predisposing factors and types of recurrent aphthous stomatitis
First published: 13 decembrie 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Orl.45.4.2019.2725
Abstract
Rezumat
Stomatita aftoasă recurentă este cea mai frecventă boală cronică a cavităţii bucale. Etiologia de bază rămâne incertă şi nu este disponibil un tratament curativ. Din perspectiva prezentării clinice, stomatita aftoasă recurentă are trei tipuri caracteristice, şi anume: tipul minor, tipul major şi tipul herpetiform. Deşi etiologia exactă este încă necunoscută, printre factorii potenţiali declanşatori se numără: predispoziţia genetică, infecţii virale şi bacteriene, alergii alimentare, deficienţe de vitamine şi microelemente, boli sistemice, stres oxidativ crescut, defecte hormonale, leziuni mecanice şi anxietate.
Introducere
Stomatita aftoasă recurentă este cea mai frecventă leziune recurentă a mucoasei orale, cu o prevalenţă în populaţia generală cuprinsă între 2% şi 50%(1). Poate să apară la copii şi adolescenţi, perturbând calitatea vieţii din cauza dificultăţilor care survin în activităţile zilnice, precum ingestia de lichide şi alimente solide sau vorbirea(1).
Stomatita aftoasă recurentă se caracterizează clinic prin ulceraţii mici, rotunde sau ovoidale, dureroase, care se pot vindeca spontan şi pot fi recurente, cu margini circumscrise, halou eritematos, cu centru pseudomembranos gri-gălbui. Cu 2-24 de ore înainte de debutul ulceraţiei poate să apară o senzaţie de arsură(2). Localizarea specifică este de obicei la nivelul mucoasei bucale şi labiale şi la nivelul limbii.
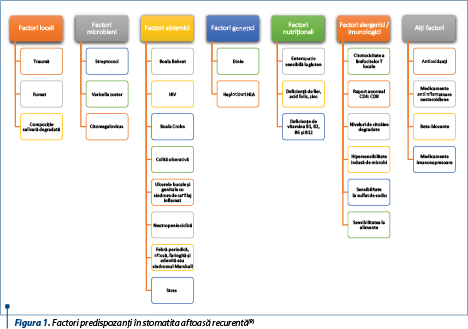
Alte afecţiuni sistemice care provoacă ulceraţii bucale asemănătoare cu stomatita aftoasă recurentă includ: boala Behcet, infecţii recurente cu virus herpetic, neutropenie ciclică, ulceraţii orale în cadrul infecţiei cu HIV sau boli gastrointestinale (boala Crohn şi colita ulceroasă)(3-5). Din perspectiva agenţilor cauzali, mai mulţi factori au fost propuşi ca determinanţi ai stomatitei aftoase recurente. Între aceştia se regăsesc: trauma, factori microbieni, factori nutriţionali (de exemplu, deficienţa de vitamine, de acid folic), factori imunologici, stres psihosocial şi alergii alimentare(2).
Stomatita aftoasă recurentă – clasificare
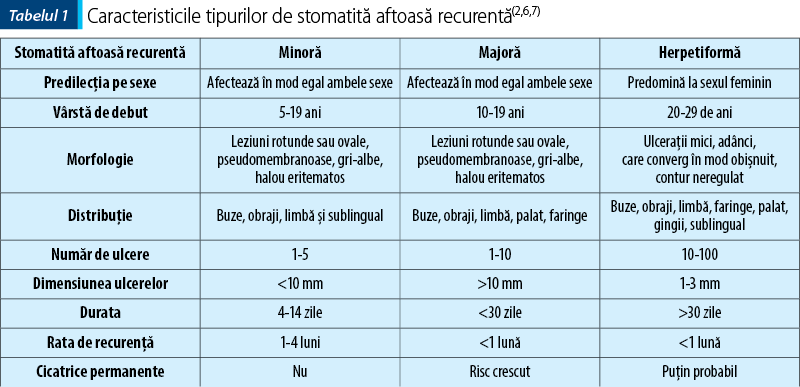
Din perspectiva prezentării clinice, stomatita aftoasă recurentă are trei tipuri caracteristice, şi anume: tipul minor, tipul major şi tipul herpetiform.
Stomatita aftoasă recurentă minoră este prezentă la aproximativ 85% din cazuri. Se caracterizează prin ulcere superficiale cu diametrul mai mic de 1 cm (în general, diametrul lezional este de 4-5 mm), aceste ulcere fiind prezente în număr de 1 până la 5 şi se vindecă fără cicatrice(6).
Stomatita aftoasă recurentă majoră (boala Sutton sau recidivele necrotice ale mucoasei) este prezentă la aproximativ 10-15% din cazuri. Leziunile caracteristice sunt asemănătoare cu cele din stomatita aftoasă recurentă minoră, ulcerele au dimensiuni de peste 1 cm (în general, diametrul lezional este de peste 10 mm), sunt mai adânci, se vindecă cu cicatrice şi se pot vindeca în săptămâni sau luni(6).
Ulceraţiile herpetiforme apar în 5-10% din cazurile de stomatită aftoasă recurentă. Ulcerele herpetiforme sunt mici, de 1-2 mm, cu ulceraţii multiple, în număr de 5-100, împrăştiate pe toată mucoasa bucală. Aceste leziuni nu au nicio legătură cu virusul herpes simplex(7). Toate cele trei tipuri sunt descrise în tabelul 1.
Stomatita aftoasă recurentă – factori predispozanţi
Deşi etiologia exactă este încă necunoscută, printre factorii potenţiali declanşatori se numără: predispoziţia genetică, infecţii virale şi bacteriene, alergii alimentare, deficienţe de vitamine şi microelemente, boli sistemice, stres oxidativ crescut, defecte hormonale, leziuni mecanice şi anxietate(8).
Trauma predispune la stomatită aftoasă recurentă prin inducerea edemelor şi a inflamaţiei celulare timpurii, asociate cu o vâscozitate crescută a matricei extracelulare submucoase orale(10). Aparent, trauma locală este element predispozant doar la acei indivizi care au o predilecţie ereditară pentru boală.
S-a demonstrat o asociere negativă între fumat şi stomatita aftoasă recurentă, în urma expunerii constante a mucoasei orale la nicotină(11). Unele modificări ale compoziţiei salivare, cum ar fi pH-ul, care afectează proprietăţile locale ale salivei, şi o creştere indusă de stres a cortizolului salivar au fost corelate cu stomatita aftoasă recurentă(12).
Deşi s-a sugerat că reactivarea virusului varicelo-zosterian sau a citomegalovirusului uman este asociată cu repetarea frecventă a ulcerelor aftoase, evaluarea ţesutului biopsic din stomatita aftoasă recurentă folosind reacţia în lanţ a polimerazei pentru posibila implicare a herpes virusului 6, citomegalovirusului, virusului varicelo-zosterian sau virusului Epstein-Barr (EBV) nu a găsit dovezi care să susţină rolul acestor virusuri în patogeneza stomatitei aftoase recurente(13).
S-a presupus că Helicobacter pylori, un factor de risc comun pentru ulceraţiile gastrice şi duodenale, are un rol cauzal în stomatita aftoasă recurentă(14). Au existat speculaţii cu privire la posibila implicare a speciilor de streptococi în etiologia stomatitei aftoase recurente, în special S. sanguis 2A, explicaţia fiind că streptococii orali acţionează ca stimulenţi antigenici care reacţionează încrucişat cu proteinele de şoc termic mitocondriale ale keratinocitelor orale, această reacţie inducând intenţionat un răspuns imun mediat de celulele T, care provoacă leziuni ale mucoasei bucale(15).
Sindromul Behcet, caracterizat prin ulceraţii orale şi genitale recurente, a fost asociat cu stomatita aftoasă recurentă. Răspunsul inflamator anormal în sindromul Behcet este cauzat de complexele imune induse de limfocitele T şi de celulele plasmatice. Un titru ridicat de anticorpi anti-Saccharomyces cerevisiae a fost detectat la pacienţii cu sindrom Behcet, în comparaţie cu pacienţii cu stomatită aftoasă recurentă şi cu persoanele aparent sănătoase(16). O altă variantă a sindromului Behcet, care include policondrita recidivantă, o tulburare caracterizată de ulcerele bucale şi genitale, a fost etichetată ca sindrom MAGIC(17).
Bolile inflamatorii intestinale, cum ar fi boala Crohn şi colita ulcerativă, au fost asociate cu ulceraţii orale care se pot asemăna cu stomatita aftoasă recurentă, dar leziunile Crohn au adesea graniţe indurate şi sunt diferite din punct de vedere histologic din cauza naturii granulomatoase a leziunii(18,19).
Boala celiacă este o altă tulburare medicală asociată adesea cu stomatita aftoasă recurentă, dar relaţia de cauzalitate dintre aceste două tulburări nu este complet elucidată. S-a raportat că prevalenţa stomatitei aftoase recurente la pacienţii cu boală celiacă variază de la 4% la 40%(20). În plus, ulceraţiile orale în boala celiacă nu au trăsăturile distinctive ale stomatitei aftoase recurente şi se rezolvă adesea când pacienţii cu boală celiacă încep dieta fără gluten(20). La persoanele HIV-pozitive, stomatita aftoasă recurentă apare mai frecvent, durează mai mult şi provoacă simptome mai dureroase decât la persoanele sănătoase(21). Neutropenia ciclică este asociată şi cu ulceraţii orale recurente în perioadele în care numărul neutrofilelor este sever scăzut(22).
Susceptibilitatea la stomatita aftoasă recurentă este semnificativ crescută prin prezenţa sa la unul sau la ambii părinţi. Persoanele cu antecedente familiale pozitive de stomatită aftoasă recurentă tind să dezvolte stomatită aftoasă recurentă la o vârstă fragedă. Anumite HLA-uri specifice genetic au fost identificate la pacienţii cu stomatită aftoasă recurentă: HLA-A2, HLA-B5, HLA-B12, HLA-B44, HLA-B51, HLA-B52, HLA-DR2, HLA-DR7 şi seria HLA-DQ47(23).
Hipersensibilitatea la anumite substanţe alimentare, germeni orali cum ar fi Streptococcus sanguis şi proteine de şoc termic microbiene au fost sugerate ca factori cauzali posibili, dar încă nu există dovezi concludente care să susţină alergia drept cauză majoră a stomatitei aftoase recurente(24).
Relaţia dintre mai multe reacţii mediate imunologic şi dezvoltarea stomatitei aftoase recurente poate fi explicată prin citotoxicitatea limfocitelor T la nivelul epiteliului oral, prin citotoxicitatea mediată celular dependentă de anticorpi şi prin defectele subpopulaţiilor limfocitelor(25).
Deficienţa nutriţională este aparent un factor etiologic pentru stomatita aftoasă recurentă, aceasta fiind asociată în 5-10% din cazuri cu deficienţa de fier, folat, zinc sau de vitamine B1, B2, B6 şi B12(26).
Evenimentele de viaţă stresante pot creşte şansele ca un pacient sensibil la stomatită aftoasă recurentă să dezvolte o nouă leziune(27-29). Rolul antioxidanţilor în stomatita aftoasă recurentă atrage în continuare atenţia, deoarece nivelurile sanguine şi salivare de antioxidanţi, cum ar fi enzimele eritrocitare superoxid dismutază şi catalază, par a fi mai mari la pacienţii cu stomatită aftoasă recurentă şi cu sindrom Behcet decât la persoanele sănătoase(30,31).
Concluzii
Stomatita aftoasă recurentă este cea mai frecventă boală ulcerativă care afectează mucoasa bucală, cu o etiologie incomplet elucidată. Poate să apară la persoanele sănătoase şi are o prezentare clinică mai severă la pacienţii imunocompromişi. Câţiva factori locali, sistemici, imunologici, genetici, alergici, nutriţionali şi microbieni, precum şi medicamentele imunosupresoare au fost propuse ca agenţi cauzali.
Acknowledgement: All authors contributed equally to the study.
Conflict of interests: The authors declare no conflict of intersts.
Compliance with ethics requirements
The authors declare that all the procedures and experiments of this study respect the ethical standards of the Helsinki Declaration from 1975, as revised in 2008, as well as the national law. The informed consent was obtained from the patient included in the study.
No funding for this study.
Bibliografie
- Han M, Fang H, Li Q, et al. Effectiveness of laser therapy in the management of recurrent aphthous stomatitis: a systematic review. Scientifica. 2016;2016:12.
- Porter SR, Scully C, Pedersen A. Recurrent aphthous stomatitis. Crit Rev Oral Biol Med. 1998;9(3):306–321.
- Olariu C, Nurciu A, Vasilescu I, et al. Afectarea măduvei hematogene la pacienţii cu infecţie HIV. Practica Medicală. 2018;13,2(57):156-161.
- Stănescu AMA, Grăjdeanu IV, Bejan GC, et al. Predicţia prevalenţei HIV până în anul 2022 în România şi Uniunea Europeană. Revista Medicală Română. 2018;LXV(4):261-265.
- Miricescu D, Totan A, Stănescu II, et al. Periodontal disease and systemic health. Revista Medicală Română. 2019;LXVI(3):195-199.
- Wallace A, Rogers HJ, Hughes SC, et al. Management of recurrent aphthous stomatitis in children. Oral Medicine. 2015;42(6):564–572.
- Tarakji B, Gazal G, Al-Maweri SA, et al. Guideline for the diagnosis and treatment of recurrent aphthous stomatitis for dental practitioners. Journal of International Oral Health. 2015;7(5):74–80.
- Najeeb S, Khurshid Z, Zohaib S, et al. Management of recurrent aphthous ulcers using low-level lasers: a systematic review. Medicina. 2016;52(5):263–268.
- Ship II. Socioeconomic status and recurrent aphthous ulcers. J Am Dent Assoc. Jul 1966;73(1):120–123.
- Stone OJ. Aphthous stomatitis (canker sores): a consequence of high oral submucosal viscosity (the role of extracellular matrix and the possible role of lectins). Med Hypotheses. 1991;36(4):341–344.
- Sawair FA. Does smoking really protect from recurrent aphthous stomatitis? Therapeutics and clinical risk management. 2010;6:573–577.
- Albanidou-Farmaki E, Poulopoulos AK, Epivatianos A, et al. Increased anxiety level and high salivary and serum cortisol concentrations in patients with recurrent aphthous stomatitis. Tohoku J Exp Med. 2008;214(4):291–296.
- Lin SS, Chou MY, Ho CC, et al. Study of the viral infections and cytokines associated with recurrent aphthous ulceration. Microbes and infection/Institut Pasteur. 2005;7(4):635–644.
- Victoria JM, Kalapothakis E, de Silva JF, Gomez RS. Helicobacter pylori DNA in recurrent aphthous stomatitis. J Oral Pathol Med. 2003;32(4):219–223.
- Scully C, Gorsky M, Lozada-Nur F. The diagnosis and management of recurrent aphthous stomatitis: a consensus approach. J Am Dent Assoc. 2003;134(2):200–207.
- Krause I, Monselise Y, Milo G, Weinberger A. Anti-Saccharomyces cerevisiae antibodies - a novel serologic marker for Behcet’s disease. Clin Exp Rheumatol. 2002;20(4 Suppl 26):S21–24.
- Imai H, Motegi M, Mizuki N, et al. Mouth and genital ulcers with inflamed cartilage (MAGIC syndrome): a case report and literature review. Am J Med Sci. 1997;314(5):330–332.
- Greenberg MS, Pinto A. Etiology and management of recurrent aphthous stomatitis. Curr Infect Dis Rep. 2003;5(3):194–198.
- Gheorghe G, Ceobanu G, Ilie M, et al. Gastrointestinal and neurological manifestations in systemic lupus erythematosus. Arch Balk Med Union. 2019;54(3):555-560.
- Cheng J, Malahias T, Brar P, et al. The association between celiac disease, dental enamel defects, and aphthous ulcers in a United States cohort. J Clin Gastroenterol. 2010;44(3):191–194.
- Kerr AR, Ship JA. Management strategies for HIV-associated aphthous stomatitis. Am J Clin Dermatol. 2003;4(10):669–680.
- Rodenas JM, Ortego N, Herranz MT, et al. Cyclic neutropenia: a cause of recurrent aphthous stomatitis not to be missed. Dermatology. 1992;184(3):205–207.
- Albanidou-Farmaki E, Deligiannidis A, Markopoulos AK, et al. HLA haplotypes in recurrent aphthous stomatitis: a mode of inheritance? International Journal of Immunogenetics. 2008;35(6):427–432.
- Hasan A, Shinnick T, Mizushima Y, et al. Defining a T-cell epitope within HSP 65 in recurrent aphthous stomatitis. Clin Exp Immunol. 2002;128(2):318–325.
- Lewkowicz N, Lewkowicz P, Dzitko K, et al. Dysfunction of CD4+CD25high T regulatory cells in patients with recurrent aphthous stomatitis. J Oral Pathol Med. 2008;37(8):454–461.
- Dar-Odeh NS, Alsmadi OM, Bakri F, et al. Predicting recurrent aphthous ulceration using genetic algorithms-optimized neural networks. Advances and applications in bioinformatics and chemistry: AABC. 2010;3:7–13.
- Bolocan A, Păduraru DN, Niţipir C, Hainăroşie R, Piţuru SM, Diaconu C, Suceveanu A, Pantea Stoian A. Mixed adenoneuroendocrine carcinoma of the gastrointestinal tract – features, diagnosis, management and prognostics. Romanian Biotechnological Letters, 2018; htpps://doi.org/10.26327/RBL2018.175.
- Ţigliş M, Neagu TP, Elfara M, Diaconu CC, Bratu OG, Văcăroiu IA, Grinţescu IM. Nefopam and its role in modulating acute and chronic pain. Rev Chim (Bucharest). 2018;69(10):2877-2880.
- Gheorghe G, Ceobanu G, Ilie M, Stănescu AMA, Bratu OG, Diaconu CC. Gastrointestinal and neurological manifestations in systemic lupus erythematosus. Arch Balk Med Union. 2019;54(3):555-560.
- Arikan S, Durusoy C, Akalin N, et al. Oxidant/antioxidant status in recurrent aphthous stomatitis. Oral Dis. 2009;15(7):512–515.
- Diaconu CC. Sindromul metabolic. Editura Medicală, Bucureşti, 2011.
Articole din ediţiile anterioare
Oral cavity and laryngeal cancer in patients with metabolic syndrome or type 2 diabetes
Cancerul de laringe este cea mai frecventă formă de cancer în zona capului şi gâtului. Pacienţii diabetici prezintă un risc crescut de a dezvolta c...