Ghidul EAACI/GA²LEN/EDF/WAO pentru definirea, clasificarea, diagnosticul şi managementul urticariei
The EAACI/GA²LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria
Abstract
This evidence- and consensus-based guideline was developed following the methods recommended by Cochrane and the Grading of Recommendations Assessment, Development and Evaluation (GRADE) working group. The conference was held on 1 December 2016. It is a joint initiative of the Dermatology Section of the European Academy of Allergology and Clinical Immunology (EAACI), the EU-founded network of excellence, the Global Allergy and Asthma European Network (GA²LEN), the European Dermatology Forum (EDF) and the World Allergy Organization (WAO) with the participation of 48 delegates of 42 national and international societies. This guideline was acknowledged and accepted by the European Union of Medical Specialists (UEMS). Urticaria is a frequent, mast cell-driven disease, presenting with wheals, angioedema, or both. The lifetime prevalence for acute urticaria is approximately 20%. Chronic spontaneous urticaria and other chronic forms of urticaria are disabling, impair quality of life and affect performance at work and school. This guideline covers the definition and classification of urticaria, taking into account the recent progress in identifying its causes, eliciting factors and pathomechanisms. In addition, it outlines evidence-based diagnostic and therapeutic approaches for the different subtypes of urticaria.Keywords
angioedemaconsensusevidence-basedhiveswhealRezumat
Acest ghid bazat pe dovezi şi acord unanim a fost dezvoltat urmând metodele recomandate de Cochrane şi de Grupul de Lucru privind Aprecierea, Dezvoltarea şi Evaluarea Gradelor de Recomandare (GRADE). Conferinţa a avut loc la 1 decembrie 2016. Ghidul reprezintă o iniţiativă comună a Secţiunii de dermatologie a Societăţii Europene de Alergologie şi Imunologie Clinică (EAACI), reţelei de excelenţă fondate de UE, Reţeaua Europeană de Alergie şi Astm Global (GA²LEN), Forumul European de Dermatologie (EDF) şi Organizaţia Mondială de Alergologie, cu participarea a 48 delegaţi din 42 de societăţi naţionale şi internaţionale. Acest ghid a fost recunoscut şi acceptat de către Uniunea Europeană a Medicilor Specialişti (UEMS). Urticaria este o afecţiune frecventă, ce implică mastocitele, caracterizată de prezenţa papulelor, a angioedemului, sau a ambelor. Prevalenţa de-a lungul vieţii pentru urticaria acută este de aproximativ 20%. Urticaria cronică spontană şi alte forme cronice de urticarie sunt invalidante, interferează cu calitatea vieţii şi afectează performanţa la locul de muncă şi la şcoală. Acest ghid oferă definiţia şi clasificarea urticariei, luând în considerare progresele recente în identificarea cauzelor, a factorilor determinanţi şi privind mecanismele patogenice. În plus, ghidul subliniază importanţa diagnosticului bazat pe dovezi şi abordarea terapeutică pentru diferitele tipuri de urticarie.Cuvinte Cheie
angioedemconsensbazat pe doveziurticariepapule1. Introducere
Acest ghid bazat pe dovezi şi acord unanim a fost dezvoltat urmând metodele recomandate de Cochrane şi de Grupul de Lucru pentru Aprecierea, Dezvoltarea şi Evaluarea Gradelor de Recomandare (GRADE – Grading of Recommendations Assessment, Development and Evaluation). O metodă bazată pe consens a fost utilizată pentru a discuta şi a ajunge la un acord asupra recomandărilor. Conferinţa a avut loc la 1 decembrie 2016 în Berlin, Germania.
Este o iniţiativă comună a Secţiunii de Dermatologie a Academiei Europene de Alergologie şi Imunologie Clinică (EAACI), a Reţelei de Excelenţă fondată în cadrul UE, a Reţelei Europene de Astm şi Alergie Globală (GA²LEN), a Forumului European de Dermatologie (EDF) şi a Organizaţiei Mondiale de Alergologie (WAO), toate acestea oferind finanţare pentru dezvoltarea acestei versiuni actualizate şi revizuite a Ghidului de urticarie EAACI/GA²LEN/EDF/WAO1–4. Aceasta nu a fost finanţată din alte surse.
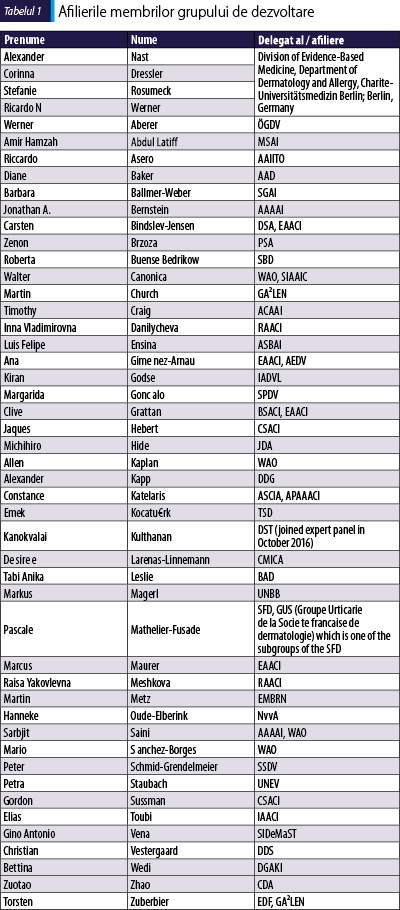
Această revizuire şi actualizare a ghidurilor a fost dezvoltată de 44 de experţi în urticarie din 25 de ţări, dintre care toţi sunt delegaţi ai societăţilor medicale naţionale şi/sau internaţionale (Tabelul 1). Toate societăţile implicate susţin acest ghid şi au susţinut dezvoltarea acestuia prin acoperirea cheltuielilor de călătorie pentru participarea delegaţilor lor la această conferinţa. Dezvoltarea revizuirii şi actualizării acestui ghid a fost susţinută de o echipă de metodişti condusă de Alexander Nast şi a inclus contribuţiile participanţilor la conferinţa tip consens (Tabelul 1).
Diversitatea largă şi numărul mare de subtipuri diferite de urticarie identificate reflectă, cel puţin parţial, faptul că avem o înţelegere din ce în ce mai bună a cauzelor şi a factorilor determinanţi ai urticariei, precum şi a mecanismelor celulare şi moleculare implicate în patogenia ei. Obiectivul acestor ghiduri este de a furniza o definiţie şi o clasificare a urticariei, prin intermediul acestora facilitându-se interpretarea datelor divergente din diferite centre şi zone ale lumii referitoare la cauzele subiacente, factorii determinanţi, povara asupra pacienţilor şi societăţii şi răspunsul terapeutic al diferitelor subtipuri de urticarie. În plus, acest ghid furnizează recomandări pentru diagnosticul şi abordările terapeutice în subtipurile comune de urticarie. Acest ghid este unul global şi ia în considerare faptul că factorii declanşatori ai urticariei la pacienţi, sistemele medicale şi accesul la diagnostic şi tratament variază în diferite ţări.
2. Metode
Metodele detaliate folosite pentru crearea acestei revizuiri şi actualizarea ghidului de urticarie EAACI/GA²LEN/EDF/WAO sunt publicate într-un raport separat de metode, care include toate tabelele GRADE5.
În concluzie, această revizuire şi actualizare a ghidului ia în considerare Instrumentul de Analiză a Ghidurilor de Cercetare şi Evaluare (AGREE II)6 şi metodele sugerate de grupul de lucru GRADE. Revizuirea literaturii a fost realizată prin folosirea metodelor recomandate în Manualul Cochrane pentru Recenzii Sistematice ale Intervenţiilor7.
Experţi din 42 de societăţi au fost nominalizaţi pentru a fi implicaţi în elaborarea ghidului. În primul rând, au fost selectate şi evaluate întrebări‑cheie şi concluzii relevante de către experţi prin folosirea unor instrumente de sondaj online8. Douăzeci şi trei de întrebări‑cheie au fost alese de către 30 de membri ai comitetului de experţi.
Ulterior, am dezvoltat un protocol de revizuire a literaturii, care specifică strategia noastră de căutare în literatură, întrebările care vor fi cercetate (PICO), criteriile de eligibilitate, rezultatele alese de experţi, evaluarea riscului de părtinire şi strategiile pentru transformarea, sinteza şi evaluarea datelor.
Căutarea sistematică în literatură a fost efectuată la 1 iunie 2016 şi au fost obţinute 8 090 de rezultate. Doi evaluatori independenţi au analizat literatura şi au extras date eligibile. După două faze de screening, s-au identificat 65 de studii care îndeplinesc criteriile de includere. Oriunde a fost posibil, am calculat efectul măsurilor prin intervale de încredere şi am realizat metaanalize folosind Review Manager9. Am analizat calitatea dovezilor urmărind GRADE prin utilizarea Instrumentului de Dezvoltare a Ghidului GRADEpro (GDT)10,11. Cinci criterii (şi anume, riscul de părtinire, inconsecvenţa, incorectitudinea, imprecizia şi publicaţiile părtinitoare) au fost evaluate pentru fiecare concluzie, rezultând o evaluare globală a calităţii probelor (Tabelul 2). Măsurarea efectelor, cum ar fi raporturile de risc, exprimă dimensiunile unui rezultat, iar evaluarea calităţii exprimă cât de multă încredere putem avea într‑un rezultat.

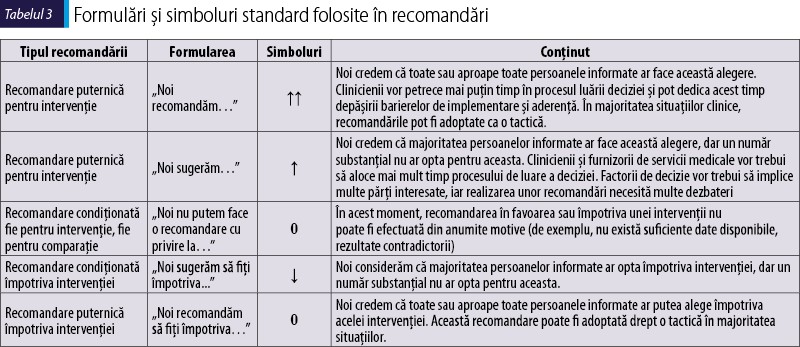
Ulterior au fost create cadre modificate de tip dovadă-decizie (EtD) pentru a ajuta experţii să ia o hotărâre asupra magnitudinii efectului dorit şi nedorit, balanţa dintre cele două, şi să furnizeze o prezentare generală a calităţii. Evaluarea probelor a generat 31 de profiluri bazate pe dovezi de tip GRADE/cadre de tip dovadă-decizie. O recomandare pentru fiecare întrebare‑cheie bazată pe dovezi a fost redactată folosind o formulare standardizată (Tabelul 3).
Într-o rundă de vot online preconferinţă, toate cadrele de tip GRADE dovadă-decizie şi recomandările redactate au fost prezentate şi votate. Dintre cei 41 de participanţi invitaţi (comitetul de experţi), 30 au completat studiul (rată de răspuns de 73%). Rezultatele au fost fie transmise comitetului de experţi, fie integrate în cadrele de tip dovadă-decizie. Toate cadrele de tip dovadă-decizie şi recomandările redactate au fost puse la dispoziţia participanţilor înainte de conferinţa de tip consens.
Pe parcursul conferinţei, toate recomandările au fost votate de peste 250 de participanţi, iar fiecare dintre aceştia a trebuit să prezinte o declaraţie că (i) sunt specialişti care au consultat pacienţi cu urticarie şi (ii) altă declaraţie referitoare la conflictele de interese. O tehnică de grup nominală a fost utilizată pentru a ajunge la un acord cu privire la diferite recomandări12. Conferinţa de consens a urmărit o abordare structurată: prezentarea datelor şi a proiectului de recomandare, discuţie liberă, vot iniţial sau colectare de formulări alternative şi vot final, dacă este necesar. Participanţii eligibili pentru votare au primit câte un card verde şi unul roşu, fiecare dintre acestea fiind ridicat pentru a vota pro sau împotriva unei recomandări propuse. Rezultatele votării au fost înregistrate. Un consens puternic a fost definit printr-un acord >90% şi la 70-89% a fost înregistrat drept consens. Toate recomandările au avut un acord de peste 75%. O revizuire internă şi externă a avut loc.
Toate recomandările consensuale sunt evidenţiate cu albastru, şi acestea sunt indicate fie atunci când sunt bazate pe opinia unui expert (bazate pe consens), fie atunci când sunt bazate pe dovezi şi pe opinia unui expert (bazate pe dovezi şi consens).
3. Definiţie
3.1. Definiţie
Urticaria este o afecţiune caracterizată prin apariţia de papule (leziuni urticariene), angioedem sau ambele. Urticaria trebuie diferenţiată de alte boli în care pot să apară papule şi angioedem sau ambele, de exemplu anafilaxia, sindroame autoinflamatorii, vasculită urticariană sau angioedemul mediat de bradikinină, inclusiv angioedemul ereditar (AEE).
(A). Papulele pacienţilor cu urticarie au 3 trăsături tipice:
un edem central de mărime variabilă, aproape invariabil înconjurat de eritem reflex;
prurit sau uneori senzaţie de arsură;
de natură tranzitorie, pielea revenind la aspectul ei normal de obicei între 30 minute şi 24 ore.
(B). Angioedemul pacienţilor cu urticarie este caracterizat de:
umflătură cu debut brusc de culoare intens eritematoasă sau de culoarea tegumentului, ce afectează dermul inferior şi ţesutul celular subcutanat sau membranele mucoase;
uneori durere mai degrabă decât prurit;
o remisiune mai lentă decât cea a papulelor (uneori poate necesita până la 72 ore).
3.2. Clasificarea urticariei în funcţie de durată şi relevanţa factorilor declanşatori
Spectrul manifestărilor clinice ale diferitelor subtipuri de urticarie este foarte variat. În plus, două sau mai multe subtipuri diferite de urticarie pot coexista la oricare pacient.
Urticaria acută spontană este definită prin apariţia spontană de papule, angioedem sau ambele cu durata sub 6 săptămâni.
|
Cum ar trebui clasificată urticaria? |
||
|
Noi recomandăm ca urticaria să fie clasificată în funţie de durată ca: acută (≤6 săptămâni) sau cronică (>6 săptămâni) Noi recomandăm ca urticaria să fie clasificată ca spontană (fără factori inductori specifici implicaţi) sau inductibilă (cu factori stimulatori implicaţi). |
↑↑ |
>90% |
|
Subtipuri de urticarie cronică |
|
|
Urticarie Cronică Spontană (UCS) |
Urticarie inductibilă |
|
Apariţia spontană de papule, angioedem sau ambele pentru mai mult de 6 săptămâni, de cauză cunoscutăa sau necunoscută |
Dermografism simptomaticb Urticaria la frigc Urticaria presională tardivăd Urticaria solară Urticaria la căldurăe Angioedemul indus de vibraţii Urticaria colinergică Urticaria de contact Urticaria aquagenică |
a De exemplu, autoreactivitatea, adică prezenţa mastocitelor activatoare de auto-anticorpi.
b Denumită şi urticaria factitia sau urticarie dermografică.
c Denumită şi urticarie de contact la frig
d Denumită şi urticaria de presiune
e Denumită şi urticaria de contact la căldură
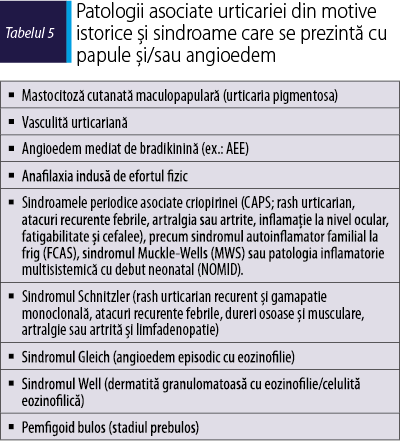
Tabelul 4 prezintă o clasificare a subtipurilor de urticarie cronică (UC) pentru uz clinic. Această clasificare a fost menţinută din ghidul precedent prin consens (>90%) drept urticarie vasculitică, mastocitoză cutanată maculopapulară (denumită anterior urticaria pigmentosa), sindroame autoinflamatorii (ex.: sindroame periodice asociate criopirinei sau sindromul Schnitzler), angioedemul mediat de mediatori non-mastocitari (ex.: angioedemul mediat de bradikinină) şi alte afecţiuni precum sindroamele care se pot manifesta cu papule şi/sau angioedem nu sunt considerate subtipuri de urticarie, din cauza mecanismului fiziopatologic distinct. (Tabelul 5).

|
Mastocitoză cutanată maculopapulară (urticaria pigmentosa) |
|
Vasculită urticariană |
|
Angioedem mediat de bradikinină (ex.: AEE) |
|
Anafilaxia indusă de efortul fizic |
|
Sindroamele periodice asociate criopirinei (CAPS; rash urticarian, atacuri recurente febrile, artralgia sau artrite, inflamaţie la nivel ocular, fatigabilitate şi cefalee), precum sindromul autoinflamator familial la frig (FCAS), sindromul Muckle-Wells (MWS) sau patologia inflamatorie multisistemică cu debut neonatal (NOMID). |
|
Sindromul Schnitzler (rash urticarian recurent şi gamapatie monoclonală, atacuri recurente febrile, dureri osoase şi musculare, artralgie sau artrită şi limfadenopatie) |
|
Sindromul Gleich (angioedem episodic cu eozinofilie) |
|
Sindromul Well (dermatită granulomatoasă cu eozinofilie/celulită eozinofilică) |
|
Pemfigoid bulos (stadiul prebulos) |
Aceste patologii şi sindroame sunt înrudite cu urticaria (1), deoarece se pot prezenta cu papule, angioedem sau ambele şi/sau (2) datorită unor motive istorice.
|
Ar trebui să menţinem clasificarea curentă din ghid a urticariei? |
||
|
Noi recomandăm ca această clasificare din ghid a urticariei cronice să fie menţinută |
↑↑ |
>90% |
3.3. Aspecte fiziopatologice
Urticaria este o patologie mediată de mastocite. Histamina şi alţi mediatori, precum factorul activator plachetar (PAF) şi citokinele eliberate din mastocitele tegumentare activate, duc la activarea terminaţiilor nervoase senzitive, vasodilataţie şi extravazare de plasmă, precum şi la recrutarea celulelor la locul leziunilor urticariene. Semnalele activatoare ale mastocitelor în urticarie sunt slab definite şi par a fi heterogene şi diverse. Din punct de vedere anatomopatologic, papulele sunt caracterizate prin edem al stratului superior şi mediu al dermului, cu dilatare şi creşterea permeabilităţii venulelor postcapilare, precum şi a vaselor limfatice din dermul superior, ducând la transvazarea serului în ţesut.
În angioedem, modificări similare apar în dermul profund şi ţesutul celular subcutanat. Pielea afectată de leziuni urticariene este practic mereu expusă suprareglării moleculelor de adeziune ale celulelor endoteliale, neuropeptidelor şi factorilor de creştere şi unui infiltrat inflamator perivascular mixt de intensitate variabilă, constând în neutrofile cu sau fără eozinofile, bazofile, macrofage şi celule T, dar fără necroza pereţilor vasculari, ceea ce este patognomonic pentru vasculita urticariană13-17. Tegumentul neafectat al pacienţilor cu urticarie cronică spontană (UCS) arată o suprareglare a moleculelor de adeziune18, a eozinofilelor infiltrate şi o expresie citokinică alterată19. O creştere uşoară până la moderată a numărului de mastocite a fost de asemenea raportată de unii autori. Aceste constatări subliniază natura complexă a patogenezei urticariei, care are multe caracteristici, pe lângă eliberarea histaminei din mastocitele dermice20-22. Unele dintre aceste caracteristici ale urticariei sunt de asemenea observate într-o mare varietate de afecţiuni inflamatorii şi, prin urmare, nu sunt specifice sau cu valoare diagnostică. Se doreşte o căutare a biomarkerilor histologici mai specifici pentru diferitele subtipuri de urticarie şi pentru a distinge urticaria de alte afecţiuni23.
3.4. Povara acestei afecţiuni
Povara UC asupra pacienţilor, a familiei şi prietenilor lor, a sistemului de sănătate şi asupra societăţii este substanţială. Utilizarea autoevaluărilor, de către pacient, cum sunt scorul de activitate al urticariei (UAS), scorul de activitate al angioedemului (AAS), chestionarul privind calitatea vieţii în urticaria cronică (CU-Q2oL), chestionarul privind calitatea vieţii în angioedem (AE-QoL) şi testul de control al urticariei (UCT) în studii şi practici clinice, a ajutat la definirea mai bună a efectelor şi impactului UC asupra pacienţilor24. Datele disponibile indică faptul că urticaria afectează semnificativ atât funcţionalitatea obiectivă, cât şi bunăstarea subiectivă25-27. O’Donnell şi colaboratorii au arătat că scorurile stării de sănătate la pacienţii cu UCS sunt comparabile cu cele raportate de pacienţii cu o afecţiune coronariană28. Mai mult decât atât, starea de sănătate, cât şi satisfacţia subiectivă la pacienţii cu UCS sunt mai mici decât la subiecţii sănătoşi şi la pacienţii cu alergie respiratorie29. UC implică, de asemenea, costuri considerabile pentru pacienţi şi pentru societate30–32.
4. Diagnosticul urticariei
4.1. Evaluarea diagnostică în urticaria acută
Urticaria acută, de regulă, nu necesită o evaluare diagnostică, deoarece este de obicei autolimitantă. Singura excepţie este suspiciunea de urticarie acută în urma unei alergii alimentare de tip I la pacienţii sensibilizaţi sau urticaria datorată existenţei altor factori determinanţi, cum ar fi medicamentele antiinflamatoare nesteroidiene (AINS). În acest caz, testele alergologice, precum şi educarea pacienţilor pot fi utile pentru a le permite pacienţilor să evite reexpunerea la factorii cauzali relevanţi.
|
Ar trebui efectuate investigaţii paraclinice de rutină în urticaria acută? |
||
|
Recomandările noastre sunt împotriva oricărei investigaţii paraclinice de rutină diagnostice în urticaria spontană acută (bazat pe consens) |
↓↓ |
>90% |
4.2. Evaluarea diagnostică în UC
Evaluarea diagnosticului de UCS are 3 obiective majore: (i) să excludă diagnosticele diferenţiale, (ii) să evalueze activitatea, impactul şi controlul bolii şi (iii) să identifice factorii declanşatori ai exacerbărilor sau, acolo unde este indicat, orice cauze subiacente. Papulele sau angioedemul pot fi prezente şi în alte afecţiuni. La pacienţii care prezintă numai leziuni urticariene (dar fără angioedem), trebuie exclusă urticaria vasculitică şi bolile autoinflamatorii, cum ar fi sindromul Schnitzler sau sindroamele periodice asociate cu criopirina (CAPS).
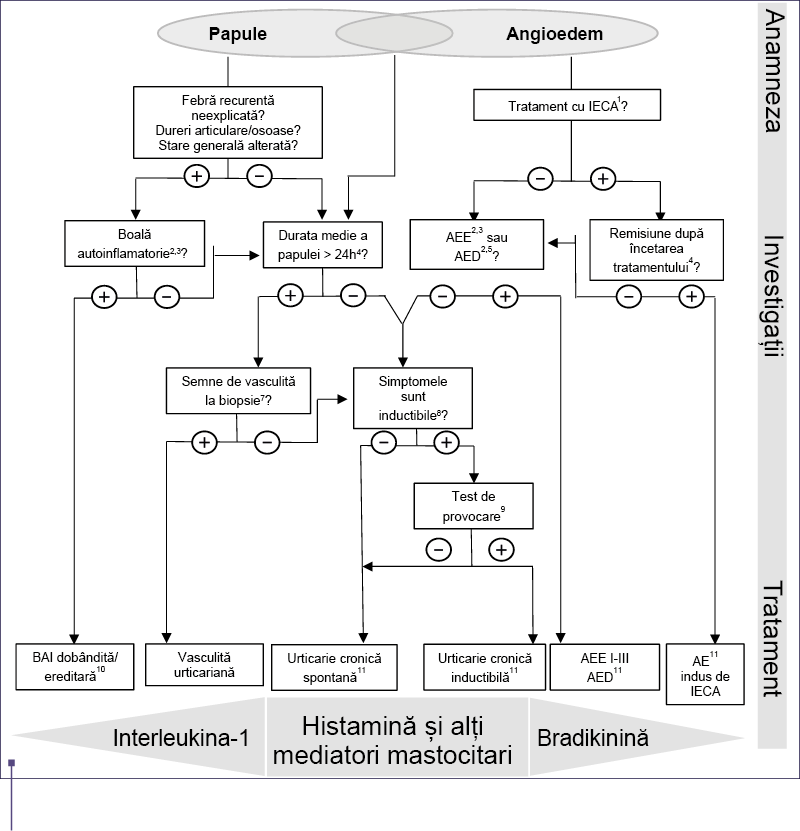
Pe de altă parte, la pacienţii care suferă doar de angioedem recurent (dar fără urticarie), trebuie luate în considerare diagnostice diferenţiale precum alte angioedeme mediate de bradikinină, cum este angioedemul indus de inhibitorii enzimei de conversie a angiotensinei (IECA) sau alt angioedem care nu este mediat de mastocite, adică angioedemul ereditar (AEE) de tip 1-3 (Figura 1). Evaluarea de bază a activităţii bolii (UAS, AAS), a calităţii vieţii (CU-Q2oL, AE-QoL) şi a controlului bolii (UCT) sunt indispensabile pentru a ghida deciziile de tratament, oferind perspective mai bune asupra poverii acestei afecţiuni, precum şi facilitarea, îmbunătăţirea şi standardizarea muncii de documentare, din ce în ce mai importante (a se vedea, de asemenea, secţiunea despre Evaluarea activităţii, impactului şi controlului bolii). Anamneza este esenţială la pacienţii cu urticarie, deoarece factorii declanşatori ai exacerbărilor sunt variabili. La pacienţii cu boală necontrolată şi de lungă durată trebuie efectuate investigaţii mai aprofundate pentru a decela cauzele subiacente.
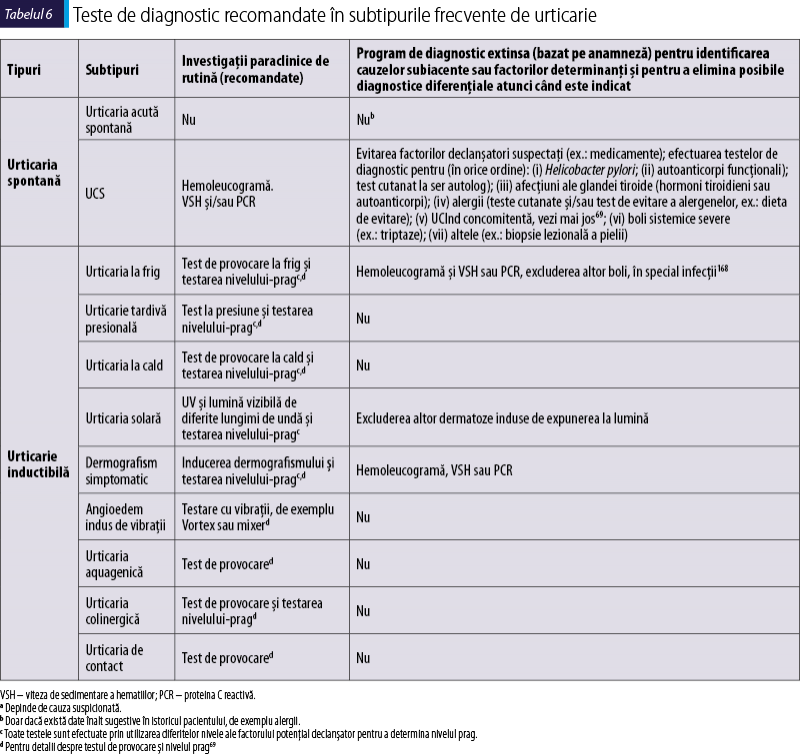
În ultimele decenii s-au înregistrat multe progrese în identificarea cauzelor diferitelor tipuri şi subtipuri de urticarie, de exemplu în UCS33-35. Printre altele, s-au descris autoimunitatea mediată de autoanticorpi funcţionali îndreptaţi împotriva receptorului IgE cu afinitate înaltă sau autoanticorpi IgE faţă de autoantigene, pseudoalergii (reacţii de hipersensibilitate nonalergice) la alimente sau medicamente, şi infecţii acute sau cronice (de exemplu, Helicobacter pylori sau Anisakis simplex) drept cauzatoare de UC (Tabelul 6). Cu toate acestea, există variaţii considerabile ale frecvenţei cauzelor subiacente în diferitele studii. Acest lucru reflectă de asemenea diferenţele regionale din lume; de exemplu, diferenţele în dietă şi în prevalenţa infecţiilor. Astfel, este important să ne amintim că nu toţi factorii posibili cauzali trebuie investigaţi la toţi pacienţii, iar primul pas în diagnostic este o anamneză detaliată, luând în considerare următoarele elemente:
Momentul de debut al bolii
Forma, dimensiunea, frecvenţa/durata şi distribuţia leziunilor urticariene
Angioedemul asociat
Simptomele asociate, de exemplu dureri osoase/articulare, febră, crampe abdominale
Istoricul familial şi personal de urticarie şi angioedem
Declanşarea de către agenţi fizici sau exerciţii fizice
Apariţia în raport cu momentul zilei, weekend-urile, ciclul menstrual, vacanţele şi călătoriile în străinătate
Apariţia în raport cu alimentele sau medicamentele (ex.: AINS, IECA)
Apariţia în raport cu infecţiile, stresul
Alergii, infecţii, boli interne/autoimune, afecţiuni gastrice/intestinale ori alte boli anterioare sau curente
Istoric social şi ocupaţional, activităţi recreaţionale
Terapia anterioară şi răspunsul la terapie, inclusiv doza şi durata
Proceduri diagnostice/rezultate anterioare.
Al doilea pas în stabilirea diagnosticului este examenul fizic al pacientului. Alte investigaţii specifice ar trebui efectuate în cazul în care acestea sunt indicate de istoric şi/sau examenul fizic. Selectarea acestor investigaţii paraclinice depinde, în mare parte, de subtipul urticariei, aşa cum sunt ele sumarizate în Figura 1 şi Tabelul 6.
|
Ar trebui diagnosticul diferenţial luat în considerare la pacienţii cu urticarie cronică spontană? |
||
|
Recomandăm ca diagnosticele diferenţiale să fie luate în considerare la toţi pacienţii cu semne şi simptome sugestive de urticarie cronică pe baza algoritmului de diagnostic (bazat pe consens) |
↑↑ |
>90% |
|
Ce investigaţii de rutină ar trebui efectuate în urticaria cronică spontană? |
||
|
Noi recomandăm investigaţii limitate. Analizele de bază includ hemoleucograma şi PCR şi/sau VSH (bazat pe consens) În UCS recomandăm efectuarea investigaţiilor adiţionale în concordanţă cu istoricul pacientului şi examenul clinic, în special la pacienţii cu durată lungă a bolii şi/sau boală necontrolată (recomandare bazată pe consens) |
↑↑ |
>90% |
|
Ar trebui efectuate investigaţii de rutină în urticaria cronică inductibilă? |
||
|
Recomandăm utilizarea testelor de provocare pentru diagnosticul urticariei cronice inductibile. Recomandăm măsurarea nivelului‑prag prin teste de provocare şi UCT pentru a măsura activitatea şi controlul bolii la pacienţii cu urticarie cronică inductibilă (recomandare bazată pe consens) |
↑↑ |
>90% |
Nu sunt recomandate programele de screening intensive şi costisitoare pentru identificarea cauzelor urticariei. Factorii precizaţi în Tabelul 6 în programul extins ar trebui investigaţi doar în funcţie de istoricul pacientului. Hipersensibilitatea de tip I este o cauză extrem de rară de UCS. Pe de altă parte, reacţiile pseudo-alergice (reacţiile de hipersensibilitate non-alergice) la AINS sau alimentare pot fi mai relevante pentru UCS. Diagnosticul ar trebui să se bazeze pe istoricul pacientului de administrare a AINS sau pe un regim dietetic de eliminare a alimentelor pseudo-alergizante. Alte cauze subiacente de urticarie sunt infecţiile bacteriene, virale, parazitare sau fungice, de exemplu cu H. pylori, streptococi, stafilococi, Yersinia, Giardia lamblia, Mycoplasma pneumoniae, virusurile hepatitice, norovirus, parvovirus B19, Anisakis simplex, Entamoeba spp, Blastocystis spp36–38. Frecvenţa şi relevanţa bolilor infecţioase variază considerabil în funcţie de grupul de pacienţi şi de regiunea geografică din care provine. Anisakis simplex, de exemplu, un peşte nematod marin, este luat în discuţie ca posibilă cauză de urticarie acută spontană recurentă doar în acele regiuni în care peştele crud este consumat in mod frecvent39,40. De asemenea, relevanţa infecţiei cu H. Pylori, a unei infecţii dentare sau auriculare, nazale sau faringiene pare că variază în cadrul diferitelor grupe de pacienţi38,41–44. Este nevoie de mai multe studii pentru a putea face recomandări definitive privind rolul infecţiei în urticarie.
Screeningul afecţiunilor maligne de rutină ca posibile cauze ale urticariei nu este recomandat. Deşi în Taiwan a fost raportată o incidenţă uşor crescută a acestor cazuri45, totuşi nu există o legatură evidentă de cauzalitate între urticarie şi bolile neoplazice. Este necesar să investigăm acest tip de patologie dacă istoricul pacientului este sugestiv în acest sens (ex.: scădere bruscă în greutate).
Testul cutanat la ser autolog (ASST, autologous serum skin test) şi testul de activare al bazofilelor (BAT, basophil activation test) sunt singurele teste de screening disponibile la momentul actual pentru detectarea autoanticorpilor îndreptaţi împotriva IgE sau FcεR1 (receptorul de înaltă afinitate pentru IgE). ASST este un test de screening nespecific ce evaluează prezenţa factorilor care determină eliberarea histaminei în ser, indiferent de tipul acestuia, nu doar autoanticorpii ce produc eliberarea de histamină. ASST ar trebui efectuat cu mare atenţie, existând riscul de transmitere a unor infecţii, dacă, din greşeală, se injectează serul altui pacient. Acest subiect este detaliat separat într-un document de poziţie EAACI/GA2LEN46,47.
BAT evaluează eliberarea de histamină sau exprimarea markerilor de activare de la nivelul bazofilelor din serul donatorilor ca răspuns la stimularea cu serul pacienţilor cu UCS. BAT poate oferi informaţii suplimentare în ceea ce priveşte activitatea bolii la pacienţii cu urticarie48,49, cât şi în ceea ce priveşte stabilirea diagnosticului de urticarie autoimună50. În plus, BAT poate fi utilizat şi ca marker de responsivitate la tratamentul cu ciclosporină A sau omalizumab51,52.
La unii pacienţi cu UCS activă, mai multe grupuri de studiu au remarcat bazopenie serică şi, de asemenea, că bazofilele sanguine prezintă o eliberare scăzută de histamină mediată prin receptorii IgE ca răspuns la anti-IgE. Bazofilele sanguine sunt detectate în leziunile cutanate ale pacienţilor cu UCS19. Remisiunea UCS este asociată cu o creştere a numărului de bazofile sanguine şi a răspunsului histaminei indus de receptorul pentru IgE53,54. O creştere a numărului de bazofile este de asemenea observată în timpul tratamentului anti-IgE55. Această observaţie, însă, trebuie cercetată în viitor, astfel că momentan nu conduce la recomandări diagnostice.
Totuşi, ar trebui să se ia în considerare faptul că un număr scăzut de bazofile sanguine nu ar trebui să ducă la proceduri diagnostice ulterioare. Este cunoscut şi faptul că nivelul D-dimerilor este semnificativ mai crescut la pacienţii cu UCS activă şi el scade în funcţie de răspunsul clinic la omalizumab. Relevanţa acestui fapt nu este clară încă şi la momentul actual nu se recomandă măsurarea nivelului D-dimerilor56,57.
4.2.1. Evaluarea impactului şi controlului asupra activităţii bolii
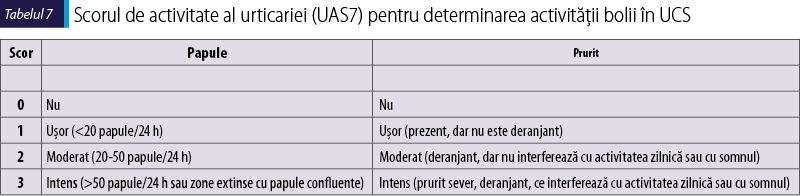
Activitatea bolii în urticaria spontană ar trebui evaluată atât în practica clinică, cât şi în studiile clinice folosind UAS7 (Tabelul 7), un sistem simplu şi uniform de cuantificare, care a fost propus şi validat în ultima versiune a ghidului58,59. UAS7 se bazează pe evaluarea semnelor şi simptomelor‑cheie în urticarie (papule şi prurit), care sunt raportate de pacient, făcând acest scor deosebit de valoros. Utilizarea UAS7 facilitează compararea rezultatelor diverselor studii din centre diferite. Deoarece activitatea urticariei se modifică frecvent, activitatea generală a bolii este cel mai eficient măsurată sfătuind pacientul să îşi noteze o dată pe zi, timp de câteva zile consecutiv, evoluţia bolii pe parcursul a 24 de ore. UAS7 este suma obţinută din punctajul a 7 zile consecutive şi ar trebui utilizat de rutină în practică pentru a determina activitatea bolii şi răspunsul la tratament al pacienţilor cu UCS. Pentru pacienţii cu angioedem s-a dezvoltat şi validat un scor nou, şi anume scorul de activitate a angioedemului (AAS)60. În plus faţă de activitatea bolii, este important de evaluat impactul bolii asupra calităţii vieţii, atât în practica curentă, cât şi în studiile clinice. Recent, testul de control al urticariei (UCT; urticaria control test) a devenit util în evaluarea statusului bolii61,62. UCT a fost dezvoltat şi validat pentru a determina nivelul de control al bolii în toate formele de UC (UCS şi UCInd). UCT conţine doar patru indicatori care diferenţiază în mod clar pacienţii cu boală „bine controlată” de cei cu boală „slab controlată” şi este astfel util în managementul pacienţilor din practica clinică de rutină. Valoarea care diferenţiază un pacient cu o boală bine controlată este 12 din 16 puncte posibile. Acest lucru este util în ajustarea schemei de tratament.
Pacienţilor ar trebui să le fie evaluată activitatea, impactul şi controlul bolii încă de la prima vizită la cabinet şi la toate celelalte controale, cunoscând faptul că anumite teste precum UAS pot fi folosite doar prospectiv, iar altele precum UCT permit o evaluare retrospectivă. În acest scop, la pacienţii cu UC ar trebui utilizate instrumente validate precum UAS7, AAS, CU-Q2oL, AE-QoL şi UCT.
|
Ar trebui pacienţilor cu urticarie cronică să le fie evaluată activitatea, impactul şi controlul bolii? |
||
|
Recomandăm ca pacienţilor cu UC să le fie evaluată activitatea, controlul şi impactul bolii la fiecare vizită medicală (bazat pe consens) |
↑↑ |
>90% |
|
Ce metode ar trebui folosite pentru a evalua şi monitoriza activitatea bolii la pacienţii cu urticarie cronică spontană? |
||
|
Sugerăm utilizarea scorului de activitate a urticariei (UAS7) şi scorul de activitate al angioedemului (AAS) pentru monitorizarea calităţii vieţii la pacienţii cu urticarie cronică spontană (bazat pe consens) |
↑ |
>90% |
|
Ce metode ar trebui folosite pentru a evalua şi monitoriza impactul asupra calităţii vieţii la pacienţii cu urticarie cronică spontană? |
||
|
Sugerăm folosirea chestionarului pentru evaluarea calităţii vieţii la pacienţii cu urticarie (CU-Q2oL) şi chestionarul privind calitatea vieţii la pacienţii cu angioedem (AE-QoL) pentru a evalua impactul bolii asupra calităţii vieţii la pacienţii cu urticarie cronică spontană (bazat pe consens) |
↑ |
>90% |
|
Ce metode ar trebui folosite pentru a evalua şi monitoriza controlul bolii la pacienţii cu urticarie cronică spontană? |
||
|
Sugerăm utilizarea testului de control în urticarie (UCT) pentru evaluarea controlului bolii la pacienţii cu urticare cronică spontană. (bazat pe consens) |
↑ |
>90% |
În UCInd, nivelul‑prag al factorului care determină apariţia simptomelor trebuie identificat pentru a evalua activitatea bolii.
Un exemplu ar putea fi determinarea temperaturii‑prag şi a timpului de expunere pentru testul de provocare la rece în cazul urticariei la frig. Identificarea acestei valori‑prag ajută atât pacientul, cât şi medicul să evalueze mai bine activitatea bolii şi răspunsul la tratament63–68. Scorul cuprins între 0 şi 6 pentru fiecare zi este sumarizat pentru întreaga săptămână (maximum 42).
4.3. Evaluarea diagnostică în UCInd
În UCInd, investigaţiile de rutină pentru stabilirea diagnosticului ar trebui să respecte recomandările stabilite privind definiţia, testele utile pentru diagnostic şi managementul UCInd69. Diverse tipuri de investigaţii sunt utilizate pentru a identifica subtipurile de UCInd şi pentru a determina nivelul‑prag al factorilor declanşatori69. Nivelul‑prag este important deoarece permite evaluarea activităţii bolii şi a răspunsului la tratament. Pentru cele mai multe tipuri de UCInd, sunt disponibile diverse tipuri de teste de provocare standardizate69. Exemplele includ urticaria la frig şi la căldură, pentru care este disponibil un dispozitiv ce foloseşte un element Peltier (TempTest®)70, iar pentru dermografismul simptomatic sau urticaria presională a fost dezvoltat un dermografometru (FricTest®)71,72. În urticaria colinergică este disponibil un test de provocare graduală cu metode de cabinet, de exemplu, ergometria cu monitorizarea pulsului66,73. Pacienţii cu urticarie de contact sau aquagenică ar trebui evaluaţi prin teste de provocare cutanate adecvate69.
4.4. Diagnosticul la copii
Urticaria poate să apară la toate gupele de vârstă, inclusiv la sugari şi copiii mici. Deşi momentan există puţine date despre UCS la copii, studiile recente indică faptul că prevalenţa UCInd şi a UCS, precum şi diversele etiologii subiacente ale UCS sunt foarte asemănătoare cu prevalenţa şi cauzele de la adult, cu mici diferenţe74–77.
Aşadar, metodele de diagnostic la copii ar trebui să fie asemănătoare cu cele folosite în cazul adulţilor.
Evaluarea diagnostică la copiii cu UCS are aceleaşi obiective ca la adult: (i) diagnosticele diferenţiale ar trebui excluse, concentrându-ne în special pe sindromul periodic asociat criopirinei (CAPS). CAPS este o boală rară cu un rash asemănător cu leziunile din urticarie şi care se manifestă în copilărie78. (ii) Dacă este posibil, adică în funcţie de vârsta copilului, ar trebui să se stabilească activitatea, impactul şi controlul bolii, evaluate utilizând scoruri similare cu cele folosite la adulţi, deşi este necesar să subliniem faptul că în prezent nu există instrumente validate pentru copii. (iii) Factorii agravanţi ar trebui identificaţi, iar atunci când este indicat, cauzele subiacente, care sunt asemănătoare cu cele ale adultului, ar trebui investigate. La copiii cu UCInd, ar trebui efectuate teste similare de provocare şi de identificare a nivelului‑prag al factorilor agravanţi.
5. Managementul urticariei
5.1. Consideraţii de bază
Scopul terapiei este să trateze afecţiunea până când aceasta dispare.
Abordarea terapeutică pentru UC poate implica:
identificarea şi înlăturarea cauzelor subiacente,
evitarea factorilor declanşatori
inducerea toleranţei şi/sau
utilizarea de tratament farmacologic pentru a preveni eliberarea mediatorilor mastocitari şi/sau efectele mediatorilor descărcaţi din mastocite
Tratamentul ar trebui să urmeze principiile de bază de a trata cât este nevoie şi cât mai puţin posibil. Acest lucru poate presupune creşterea sau scăderea treptei de tratament în funcţie de evoluţia afecţiunii.
|
Ar trebui ca tratamentul să aibă ca scop controlul complet al simptomelor în urticarie? |
||
|
Recomandăm urmărirea controlului complet al simptomatologiei în urticarie, luând în considerare pe cât posibil siguranţa şi calitatea vieţii ale fiecărui pacient (bazat pe consens) |
↑↑ |
>90% |
5.2. Identificarea şi eliminarea cauzelor subiacente şi evitarea factorilor declanşatori
Pentru a înlătura o cauză subiacentă, este necesar un diagnostic precis. Identificarea unei cauze în UC poate fi totuşi, dificilă în majoritatea cazurilor, de exemplu infecţiile pot reprezenta o cauză, un factor agravant sau pot să nu aibă legătură cu evoluţia bolii. Singura dovadă clară de relaţie cauză-efect a unui agent suspicionat sau declanşator este remisiunea simptomelor după eliminarea lui şi reapariţia lor după reintroducerea printr-un test de provocare dublu‑orb. Remisiunea spontană a erupţiei urticariene poate avea loc oricând, iar eliminarea unui factor suspicionat sau declanşator poate să fie doar o coincidenţă.
5.2.1. Medicamentele
Atunci când aceşti agenţi sunt suspectaţi ca potenţiali declanşatori ai bolii, aceştia ar trebui evitaţi în totalitate, iar în cazul în care sunt indispensabili, ei trebuie înlocuiţi cu altă clasă terapeutică. Medicamentele care pot determina reacţii de hipersensibilitate nonalergice (prototipul fiind AINS) nu doar că pot declanşa boala, dar pot agrava o UCS preexistentă79, motiv pentru care eliminarea lor poate duce la ameliorarea simptomelor la unii pacienţi din grupul din urmă.
|
Ar trebui ca pacienţii cu urticarie cronică spontană să fie sfătuiţi să întrerupă medicaţia suspectată ca posibil factor agravant al bolii? |
||
|
Recomandăm sfătuirea pacienţilor cu urticarie cronică spontană să întrerupă medicaţia suspectată ca posibil factor agravant al bolii, de exemplu AINS (bazat pe consens) |
↑↑ |
>90% |
5.2.2. Stimulii fizici
Evitarea stimulilor fizici, ca parte a tratamentului UCInd, este de dorit, dar în general foarte dificil de realizat. Informaţiile detaliate despre proprietăţile fizice ale respectivului stimul ar trebui să ajute pacientul să recunoască şi să controleze expunerea în viaţa de zi cu zi. De aceea, de exemplu, în urticaria presională tardivă şi în dermografismul simptomatic, este important să subliniem că presiunea este definită ca raportul forţă pe suprafaţă şi că, măsuri simple, cum ar fi creşterea în lăţime a mânerelor genţilor grele pentru urticaria presională sau reducerea fricţiunii în dermografismul simptomatic, pot fi utile în prevenirea apariţiei simptomelor. Aspecte similare trebuie avute în vedere pentru urticaria la rece, unde trebuie să amintim impactul factorului suplimentar de răcire al curenţilor de aer reci. În urticaria solară este importantă determinarea exactă a lungimilor de undă ce o declanşează, pentru a stabili tipul filtrului de protecţie solară necesar sau folosirea de becuri cu filtru UV-A. Totuşi, pentru mulţi pacienţi nivelul‑prag al factorului fizic relevant este mic, iar prevenţia totală a simptomelor este practic imposibilă. De exemplu, dermografismul simptomatic sever se poate confunda uneori cu UCS deoarece pot apărea, aparent spontan, leziuni urticariene chiar şi acolo unde hainele largi realizează un contact minim cu pielea, sau scărpinatul involuntar al pacientului produce leziuni urticariene în acea zonă.
5.2.3. Eradicarea agenţilor infecţioşi şi tratamentul proceselor inflamatorii
În contrast cu UCInd, UCS se asociază frecvent cu o varietate de boli inflamatorii sau infecţioase. Această asociere este considerată importantă în anumite circumstanţe, dar există şi studii cu rezultate contradictorii şi cu imperfecţiuni în metodologia de studiu. Aceste infecţii, care ar trebui tratate corespunzător, precum cele de tract gastrointestinal cu agenţi patogeni ca infecţia cu H. pylori sau infecţii bacteriene ale nazofaringelui80, (chiar dacă la nivel de pacient individual, asocierea cu urticaria nu este clară, iar o metaanaliză a evidenţiat o corelaţie slabă cu tratamentul de eradicare80, H.pylori trebuie eradicat, deoarece a fost sugerată asocierea acestuia cu neoplasmul gastric81). Paraziţii intestinali, o cauză rară posibilă a UCS în ţările industrializate dezvoltate, ar trebui eliminaţi, dacă este cazul80,82. În trecut, candidoza intestinală era considerată o cauză importantă a UCS80, dar cercetările recente nu au reuşit să susţină rolul etiologic semnificativ al acesteia83. Pe lângă bolile infecţioase, procesele cronice inflamatorii determinate de alte afecţiuni au fost identificate ca potenţiali factori declanşatori ai UCS. Această asociere a fost demonstrată în mod special pentru gastrită, reflux gastroesofagian sau procese inflamatorii ale vezicii biliare ori ale ductelor biliare84,85.
Totuşi, similar infecţiilor, este greu de determinat dacă acestea sunt cauze relevante ale UCS, dar ele trebuie tratate deoarece multe dintre acestea sunt asociate cu apariţia malignităţilor.
5.2.4. Reducerea stresului fizic şi emoţional
Deşi mecanismele exacerbărilor induse de stres nu sunt bine investigate, anumite dovezi corelează activitatea şi severitatea bolii cu nivelul stresului86. Aceste afirmaţii sunt valabile atât pentru stresul emoţional, cât şi pentru stresul fizic, care poate fi relevant în dezvoltarea anumitor simptome, aşa cum se întâmplă în urticaria colinergică87.
5.2.5. Reducerea auto-anticorpilor funcţionali
A fost demonstrat că reducerea directă a autoanticorpilor prin plasmafereză la anumiţi pacienţi cu boală severă aduce un beneficiu temporar88. Din cauza experienţei reduse şi a costului ridicat al acestei terapii, ea este sugerată la pacienţii cu UCS cu autoanticorpi pozitivi, care nu răspund la nicio altă formă de tratament.
5.2.6. Managementul dietei
Alergia alimentară IgE-mediată este extrem de rar cauza subiacentă a UCS84,89. Dacă sunt identificate, alergenele alimentare specifice trebuie excluse în măsura în care acest lucru este posibil, ceea ce va conduce la o remisiune a simptomelor în mai puţin de 24 de ore. La unii pacienţi cu UCS au fost observate reacţii pseudoalergice (reacţii de hipersensibilitate non-IgE- mediate) la anumite ingrediente naturale şi în anumite cazuri la aditivii alimentari84,89-93. O dietă fără psudoalergene, ce conţine niveluri scăzute de pseudoalergene alimentare naturale, cât şi artificiale, a fost testată în ţări diferite94; de asemenea o dietă săracă în histamină poate ameliora simptomatologia la aceşti pacienţi95. Aceste diete sunt controversate, eficienţa lor nefiind încă demonstrată prin studii calitative dublu-orb placebo‑controlate. Totuşi, atunci când sunt recomandate, ele trebuie menţinute pentru o perioadă de cel puţin 2-3 săptămâni pentru ca efectele benefice să poată fi observate. Trebuie subliniat că acest tip de tratament necesită pacienţi complianţi, iar rata de success poate varia considerabil în funcţie de diferenţele regionale alimentare şi de obiceiurile dietetice. Sunt necesare mai multe studii despre efectul ingredientelor naturale şi artificiale din alimente în ceea ce priveşte inducerea urticariei.
5.3. Inducerea toleranţei
Inducerea toleranţei poate fi utilă în anumite subtipuri de urticarie. Exemplele includ urticaria la rece, urticaria colinergică şi urticaria solară, unde chiar şi curele scurte de expunere la UV-A pot avea efecte pozitive în decurs de trei zile96. Totuşi, inducerea toleranţei durează doar câteva zile, aşadar este necesară expunerea zilnică la stimul prin respectarea unui nivel‑prag. Inducerea toleranţei şi menţinerea ei deseori nu sunt acceptate de către pacient, de exemplu în cazul urticariei la frig, când sunt necesare băi/duşuri reci zilnice pentru inducerea toleranţei.
5.4. Tratament farmacologic simptomatic
Un principiu de bază al tratamentului farmacologic este de a ţinti remiterea totală a simptomatologiei. Un alt principiu general al farmacoterapiei este acela de a folosi cât de mult este necesar şi cât mai puţin posibil. De aceea, cantitatea şi selectarea medicaţiei pot varia pe parcursul bolii.
Principala opţiune a terapiilor ce vizează reducerea simptomatologiei este aceea de a reduce efectul mediatorilor mastocitari precum histamina, PAF şi ai altora asupra organelor‑ţintă. Multe dintre simptomele urticariei sunt mediate în principal de acţiunea histaminei la nivelul receptorilor H1 localizaţi la nivelul celulelor endoteliale (papula) şi nervilor senzitivi (senzaţie de arsură şi prurit). Astfel, tratamentul continuu cu antihistaminice H1 are o importanţă deosebită în tratamentul urticariei (datele de siguranţă sunt disponibile pentru utilizarea continuă cu o durată de mai mulţi ani). Administrarea continuă a antihistaminicelor H1 în UC este susţinută nu doar de studiile clinice97,98, dar şi de mecanismul de acţiune al acestor medicamente, şi anume că acestea sunt agonişti inverşi cu activitate preferenţială pentru starea inactivă a receptorilor H1 histaminici, pe care îi stabilizează în această conformaţie, schimbând echilibrul către starea inactivă.
Totodată, şi alţi mediatori specifici mastocitelor (PAF, leucotriene, citokine) pot fi implicaţi, putând fi observat un infiltrat celular pronunţat ce conţine bazofile, limfocite şi eozinofile99. Acestea pot răspunde rapid la o cură scurtă de corticosteroizi, dar pot să fie refractare la antihistaminice.
Aceste principii generale de farmacoterapie se aplică tuturor formelor de urticarie acută sau cronică. Diferenţa dintre urticaria spontană şi UCInd constă în faptul că în unele forme de urticarie la agenţi fizici, cum este cea indusă de frig, tratamentul la nevoie poate fi mai util decât un tratament continuu. De exemplu, când un pacient ştie că urmează să se expună la frig sau că merge să înoate vara, administrarea de antihistaminice cu două ore înainte de activitatea planificată se poate dovedi suficientă.
Antihistaminicele sunt disponibile pentru tratamentul urticariei din 1950. Prima generaţie de antihistaminice au o acţiune pronunţată anticolinergică şi o acţiune sedativă asupra sistemului nervos central (SNC), fiind descrise multe interacţiuni cu alcoolul şi cu medicamente ce pot afecta SNC, cum sunt analgezicele, hipnoticele, sedativele şi timostabilizatoarele. Pot interfera cu perioada somnului cu mişcări oculare rapide (REM; rapid eye movement) şi au impact asupra procesului de învăţare şi a performanţei. Afectarea este în special evidentă în timpul executării mai multor sarcini simultan sau în timpul executării unor sarcini complexe senzoriale şi motorii cum este, de exemplu, şofatul. Într-un document de poziţie GA2LEN100, este recomandat cu fermitate ca tratamentul cu antihistaminice de generaţia întâi să nu mai fie folosit la adulţi şi mai ales la copii în afecţiunile alergice. Această perspectivă este împărtăşită şi de ghidul OMS ARIA101. Având în vedere dovezile puternice ale efectelor adverse, potenţial severe, ale antihistaminicelor vechi sedative (au fost raportate supradoze letale), recomandăm evitarea folosirii lor ca tratament de rutină de primă linie pentru UC, cu excepţia puţinelor locuri din lume, unde antihistaminicele moderne de generaţia a 2-a nu sunt disponibile. Efectele adverse ale primei generaţii de antihistaminice H1 sunt cel mai pronunţate la prometazină, difenhidramină, ketotifen şi clorfeniramină, fiind bine înţelese. Ele penetrează bariera hemato-encefalică, legându-se de receptorii H1 de la nivelul SNC şi interferează cu efectele de neurotransmiţător ale histaminei. Studiile ce au utilizat tomografia cu emisie de pozitroni (PET-CT) evidenţiază penetrarea lor la nivelul creierului uman şi oferă un nou etalon, conform căruia ocuparea receptorilor H1 de la nivelul SNC poate fi direct corelată cu efectele directe asupra funcţiei SNC102.
Dezvoltarea antihistaminicelor de generaţia a 2-a a condus la apariţia de medicamente cu efect sedativ minim sau nesedative şi fără efecte anticolinergice. Totuşi, două dintre primele antihistaminice H1 de generaţia a 2-a, astemizol şi terfenadina, care în principiu erau promedicamente ce necesitau metabolizare hepatică pentru activare completă, aveau efecte cardiotoxice dacă metabolizarea hepatică era blocată de administrarea concomitentă de inhibitori ai izoenzimei 3A4 a citocromului P450 (CYP), cum ar fi ketoconazolul sau eritromicina. Aceste două medicamente nu mai sunt disponibile în majoritatea ţărilor şi nu recomandăm folosirea lor.
Progresul cercetărilor privind profilul de siguranţă al medicamentelor a fost obţinut în ultimele decade prin apariţia unui număr considerabil de antihistaminice noi de generaţia a 2-a102. Nu toate antihistaminicele au fost testate specific pentru urticarie, dar sunt disponibile multe studii pentru antihistaminicele nesedative, de exemplu cetirizină, desloratadină, fexofenadină, levocetirizină, loratadină, ebastină, rupatadină şi bilastină. Antihistaminicele moderne de generaţia a 2-a trebuie considerate prima linie de tratament simptomatic în urticarie, datorită profilului lor de siguranţă bun. Totuşi, studii clinice de actualitate, bine structurate, care să compare eficacitatea şi siguranţa antihistaminicelor H1 de generaţia a 2-a în urticarie lipsesc.
|
Sunt de preferat antihistaminicele H1 de generaţia a doua în detrimentul celor de generaţia întâi pentru tratamentul urticariei cronice? |
||
|
Sugerăm utilizarea antihistaminicelor H1 de generaţia a 2-a în detrimentul celor de generaţia întâi pentru tratamentul pacienţilor cu urticarie cronică (bazat pe dovezi şi consens) |
↑ |
>90% |
|
Ar trebui folosite ca primă linie de tratament antihistaminicele H1 de generaţie a 2-a în tratamentul urticariei? |
||
|
Recomandăm folosirea antihistaminicelor de generaţie a 2-a ca primă linie de tratament în urticaria cronică (bazat pe dovezi şi consens) |
↑↑ |
>90% |
|
Ar trebui antihistaminicele H1 de generaţia a 2-a moderne administrate la nevoie sau regulat în tratamentul urticariei? |
||
|
Sugerăm administrarea regulată a antihistaminicelor de generaţia a 2-a la pacienţii cu urticarie cronică (bazat pe dovezi şi consens) |
↑ |
>90% |
|
Ar trebui folosite simultan antihistaminice H1 de generaţia a 2-a diferite? |
||
|
Recomandarea este împotriva folosirii simultane a antihistaminicelor diferite (bazat pe consens) |
↓↓ |
>90% |
Există studii care demonstrează beneficiul unor doze crescute de antihistaminice H1 de generaţia a 2-a la anumiţi pacienţi103-105, confirmate de studiile anterioare cu aceleaşi rezultate legate de antihistaminicele de generaţia întâi106,107. Acestea au fost verificate în studii ce au utilizat doza cvadruplă faţă de cea recomandată de bilastină, cetirizină, ebastină, fexofenadină, levocetirizină şi rupatadină103,104,108–111.
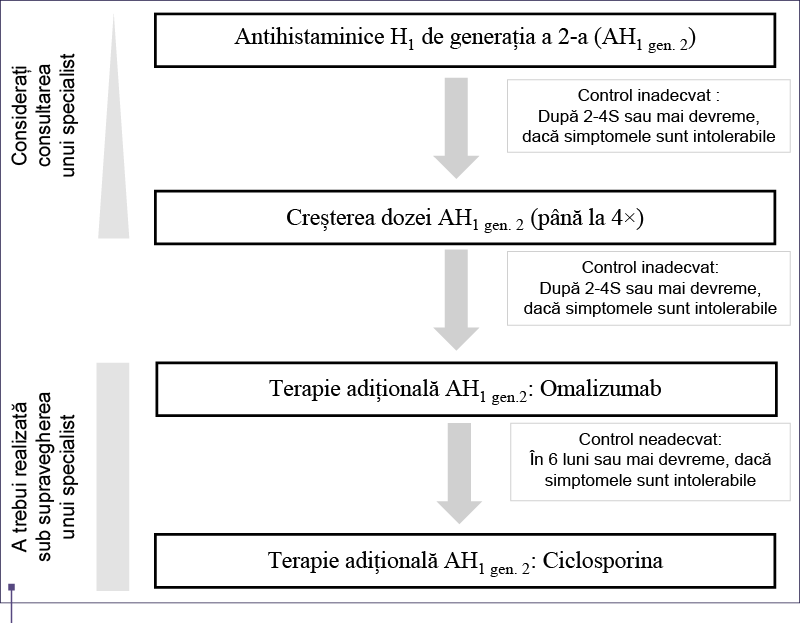
În concluzie, aceste studii sugerează că la majoritatea pacienţilor cu urticarie care nu răspund la dozele uzuale, creşterea dozelor aduce beneficii. Antihistaminicele moderne de generaţia a 2-a în doză standard reprezintă prima linie de tratament în urticarie, iar treapta a doua este reprezentată de creşterea dozelor (Figura 2).
|
Este doza cvadruplă de antihistaminice-H1 moderne, de generaţia a 2-a, utilă şi de preferat altor tratamente în urticarie (linia a doua de tratament)? |
||
|
Sugerăm creşterea dozelor de antihistaminice H1 de generaţia a 2-a până la o doză cvadruplă la pacienţii cu urticarie cronică care nu răspund la dozele standard (bazat pe dovezi şi consens) |
↑ |
>90% |
|
Dacă nu există o ameliorare, se pot lua în considerare doze mai mari de antihistaminice de geneneraţia a 2-a decât cele cvadruple? |
||
|
Nu recomandăm utilizarea dozelor mai mari decât cele standard în urticaria cronică (bazat pe dovezi şi consens) |
↓↓ |
>90% |
5.5. Alte posibilităţi terapeutice la pacienţii neresponsivi la antihistaminice
Omalizumabul (anti-IgE) s-a dovedit a fi foarte sigur şi eficient în tratamentul UCS112-117. Omalizumabul s-a dovedit eficient şi în UCInd118,119, inclusiv în urticaria colinergică120, urticaria la rece68,121, urticaria solară122, urticaria la cald123, dermografismul simptomatic67,124, şi urticaria tardivă indusă de presiune125. În UCS, omalizumabul previne dezvoltarea angioedemului126, îmbunatăţind semnificativ calitatea vieţii9,127, se poate administra pe termen îndelungat128 şi este eficient împotriva recăderilor după întrerupere128,129. Omalizumabul este eficient la doze între 150 şi 300 mg pe lună în UC. Doza este independentă de nivelul seric al IgE totale112. Doza recomandată în UCS este de 300 mg la fiecare 4 săptămâni. Doza autorizată şi durata tratamentul diferă între ţări.
|
Este Omalizumab util ca tratament suplimentar la pacienţii care nu răspund la doze mari de antihistaminice H1 (a III-a linie de tratament în urticarie)? |
||
|
Recomandăm adăugarea de Omalizumab* ca tratament suplimentar la pacienţii cu UC care nu răspund la doze mari de antihistaminice de generaţia a 2-a (bazat pe dovezi şi consens) * în prezent autorizat pentru urticarie |
↑↑ |
>90% |
Dacă se utilizează tratament cu corticosteroizi sistemici, sunt necesare doze de prednison cuprinse între 20 şi 50 mg/zi, dar există în acest caz reacţii adverse evidente pe termen lung. Există o recomandare puternică împotriva utilizării pe termen lung a corticosteroizilor în afara clinicilor de specialitate. În funcţie de ţară, trebuie menţionat că steroizii nu sunt nici ei autorizaţi pentru UC (ex, în Germania, prednisolonul este autorizat doar pentru urticarie acută). Cu toate acestea, pentru urticaria acută şi exacerbările acute ale UCS, o cură scurtă de corticosteroizi orali, de maximum 10 zile, poate fi totuşi utilă pentru a reduce durata/activitatea bolii.136,137. Cu toate acestea, nu sunt disponibile SRC bine structurate.
Ciclosporina A are de asemenea un efect direct, moderat, asupra eliberării mediatorilor din mastocite130,131. Eficienţa ciclosporinei A în combinaţie cu un antihistamininic H1 de generaţia a 2-a modern a fost demonstrată în studii placebo controlate132–134, precum şi în studii clinice controlate deschise135 în UCS, dar acest medicament nu poate fi recomandat ca tratament standard din cauza unei incidenţe mai mari a efectelor adverse133. Ciclosporina A se administreză off-label în urticarie şi este recomandată numai pacienţilor cu boală severă refractară la orice doză de antihistaminic şi omalizumab administrat în combinaţie. Cu toate acestea, ciclosporina A are un raport risc/beneficiu mult mai bun în comparaţie cu utilizarea pe termen lung a steroizilor.
Unele SRC anterioare au evaluat utilizarea de antagonoşti ai receptorilor de leucotriene. Studiile sunt dificil de comparat din cauza diferitelor populaţii studiate, de exemplu includerea numai a aspirinei şi a pacienţilor intoleranţi la aditivi alimentari sau excluderea pacienţilor pozitivi cu ASST. În general, nivelul dovezilor în ceea ce priveşte eficacitatea antagoniştilor receptorilor de leucotriene în urticarie este scăzut, dar este cel mai bun pentru montelukast.
|
Este Ciclosporina A utilă ca tratament suplimentar la pacienţii care nu răspund la doze mari de antihistaminice H1 (a III-a linie de tratament în urticarie)? |
||
|
Sugerăm adăugarea Ciclosporinei A ca tratament la pacienţii cu UC neresponsivi la antihistaminicele de generaţia a doua (bazat pe dovezi şi consens) |
↑ |
>90% |
|
Comentariul autorilor: aşa cum se arată în algoritmul de tratament bazat pe consens (Figura 2), care a fost votat mai târziu, s-a decis că Omalizumab trebuie încercat înaintea Ciclosporinei A, deoarece aceasta din urmă nu este autorizată pentru urticarie şi are un profil inferior de efecte adverse. |
|
Sunt antagoniştii leucotrienilor utili ca tratament suplimentar la pacienţii care nu răspund la doze mari de antihistaminice H1? |
||
|
Nu putem face o recomandare cu privire la montelukast ca tratament suplimentar la antihistaminicele H1 la pacienţii cu urticarie cronică fără răspuns la antihistaminicele H1 (bazat pe dovezi şi pe consens) |
0 |
>90% |
În prezent, corticosteroizii topici sunt folosiţi frecvent şi cu succes în multe boli alergice, dar în urticarie utilizarea lor topică nu este eficientă (cu o posibilă excepţie în ceea ce priveşte urticaria de presiune la nivel plantar ca terapie alternativă cu nivel scăzut de dovezi).
|
Ar trebui folosiţi corticosteroizii orali ca tratament suplimentar în urticarie? |
||
|
Nu recomandăm folosirea pe termen lung a corticosteroizilor sistemici în UC (bazat pe consens) |
↓↓ |
>90% |
|
Sugerăm luarea în considerare a unui tratament de scurtă durată cu glucocorticosteroizi sistemici la pacienţii cu exacerbare acută a UC (bazat pe consens) |
↑ |
|
Cu toate că antihistaminicele în doză până la cvadruplă faţă de cea recomandată de producător vor controla simptomele la majoritatea pacienţilor cu urticarie în practica generală, sunt necesare şi tratamente alternative pentru restul pacienţilor neresponsivi. Înainte de a trece la o terapie alternativă, se recomandă o perioadă de aşteptare cuprinsă între 1 şi 4 săptămâni pentru a permite eficacităţii depline să se instaleze.
Deoarece severitatea urticariei poate să varieze şi remisiunea spontană poate apărea în orice moment, se recomandă de asemenea reevaluarea necesităţii unui tratament continuu sau a unei medicaţii alternative la fiecare 3-6 luni.
Cu excepţia Omalizumabului şi a Ciclosporinei A, ambele având restricţii din cauza costului ridicat, multe dintre alternativele terapeutice, precum combinaţia dintre antihistaminice H1 moderne de generaţia a doua şi antagonişti ai receptorilor de leucotriene, sunt bazate pe studii clinice cu nivel scăzut de dovezi (Tabelul 8). Având în vedere nivelul de dovezi, liniile 3 şi 4 de tratament au astfel recomandare limitată (a se vedea algoritmul din figura 2).
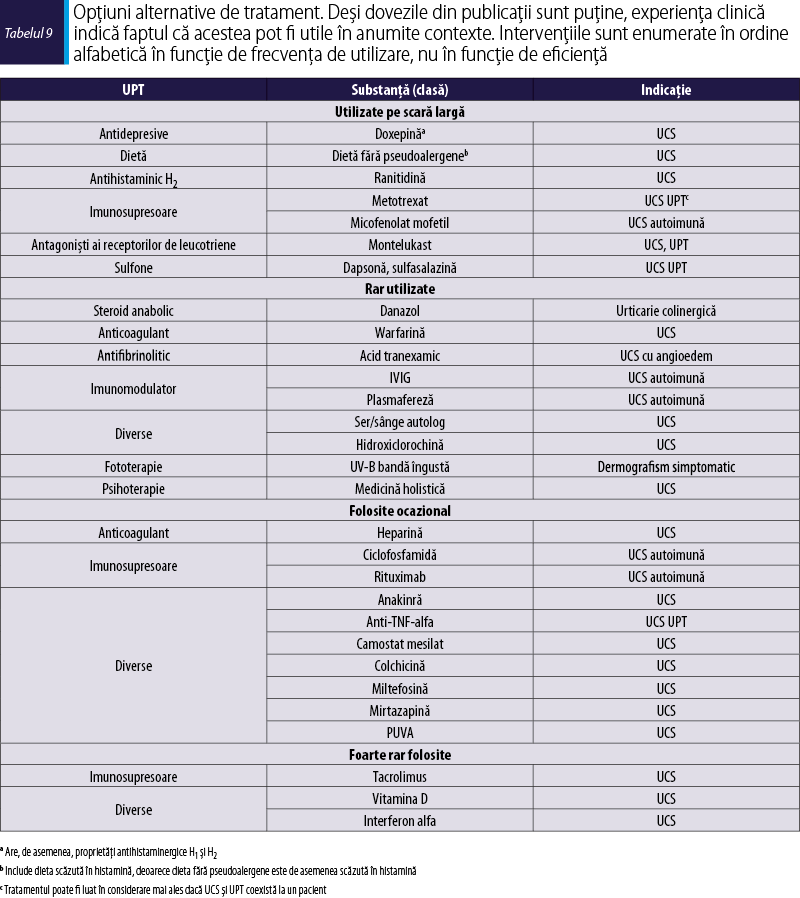
Antagoniştii H2 şi dapsona, recomandaţi în versiunea anterioară a ghidului, sunt actualmente percepuţi ca având niveluri de evidenţă prea scăzute pentru a le menţine ca recomandare în algoritm, dar ar putea avea totuşi relevanţă, deoarece sunt foarte rezonabili ca preţ în anumite sisteme de sănătate mai restrictive. Sulfasalazina, methotrexatul, interferonul, plasmafereza, fototerapia, imunoglobulinele intravenoase (IGIV), precum şi alte metode de tratament au nivel scăzut al dovezilor sau au fost publicate doar serii de cazuri2 (Tabelul 9). În pofida lipsei de dovezi publicate, toate aceste medicamente pot fi de valoare la anumiţi pacienţi în contextul clinic adecvat138.
|
Sunt antihistaminicele H2 utile ca terapie adjuvantă la pacienţii neresponsivi la doze mici sau mari de antihistaminice H1? |
||
|
Nu putem face o recomandare în ceea ce priveşte utilizarea sau evitarea utilizării combinate de antagonişti H1 şi H2 la pacienţii cu urticarie cronică. (bazat pe dovezi şi pe consens) |
0 |
>75% |
Antagoniştii factorului de necroză tumorală alfa (TNF-alfa)139 şi IGIV140–143, care au fost folosiţi cu succes în prezentări de cazuri, se recomandă la momentul actual să fie folosiţi doar în centrele specializate ca ultimă opţiune (adică anti-TNF-alfa pentru urticaria tardivă de presiune şi IGIV pentru UCS)144,145.
Pentru tratamentul UCS şi cel al dermografismului simptomatic, se pot adăuga tratamentului antihistaminic şi tratamente cu UV-B (bandă îngustă UV-B, TL01), UV-A şi PUVA timp de 1-3 luni146-148.
Unele alternative de tratament propuse anterior s-au dovedit a fi ineficiente în studiile dublu-orb, placebo controlate şi nu ar trebui să mai fie utilizate având în vedere că gradul lor de recomandare este scăzut. Acestea includ acidul tranexamic şi cromoglicatul de sodiu în UCS149,150, nifedipina în dermografismul simptomatic/urticarie factitia151, colchicina şi indometacinul în urticaria de presiune cu debut tardiv152,153. Cu toate acestea, este nevoie de mai multe studii pentru anumite subgrupuri de pacienţi, de exemplu Asero, et al.154 a publicat recent un studiu pilot la pacienţi cu niveluri ridicate de D-dimeri, care a arătat că heparina şi terapia cu acid tranexamic pot fi eficiente.
|
Ar putea fi recomandate alte opţiuni terapeutice ca tratament de linia a treia în urticarie? |
||
|
Nu putem face o recomandare cu privire la opţiunile suplimentare de tratament |
0 |
>90% |
5.6 Tratamentul grupelor speciale de populaţie
5.6.1. Copii
Mulţi clinicieni folosesc antihistaminice H1 de primă generaţie, sedative, ca primă alegere în tratamentul copiilor cu alergii, presupunând că profilul de siguranţă al acestor medicamente este mai cunoscut decât cel al antihistaminicelor H1 de generaţia a 2-a moderne, datorită unei experienţe mai îndelungate cu acestea. De asemenea, utilizarea de antihistaminice H1 de generaţia a 2-a moderne nu este autorizată pentru utilizarea la copii cu vârsta mai mică de 6 luni în multe ţări, în timp ce recomandările pentru antihistaminicele H1 de primă generaţie este uneori mai puţin clare, deoarece aceste medicamente au fost autorizate într-o perioadă în care legislaţia în industria farmaceutică era mai puţin strictă. În consecinţă, mulţi medici aleg antihistaminice de primă generaţie, care, aşa cum s-a menţionat, au un profil de siguranţă mai slab în comparaţie cu antihistaminicele H1 moderne de a 2-a generaţie. S-au făcut recomandări ferme de către grupul de experţi pentru a descuraja utilizarea antihistaminicelor de primă generaţie la sugari şi copii. Astfel, la copii, este recomandat acelaşi tratament de primă intenţie şi creşterea dozelor (ajustate la greutate şi vârstă) ca şi la adulţi. În populaţia pediatrică trebuie utilizate doar medicamente cu eficacitate şi siguranţă dovedită. Cetirizina155, desloratadina156,157, fexofenadina158, levocetirizina159, rupatadina160, bilastina161 şi loratadina155 au fost bine studiate la copii, iar siguranţa lor pe termen lung a fost bine stabilită la populaţia pediatrică. În plus, alegerea antihistaminicelor H1 de generaţia a 2-a la copii depinde de vârstă şi de disponibilitate, întrucât nu toate sunt disponibile sub formă de sirop sau comprimat orodispersabil, potrivite pentru aceştia.
|
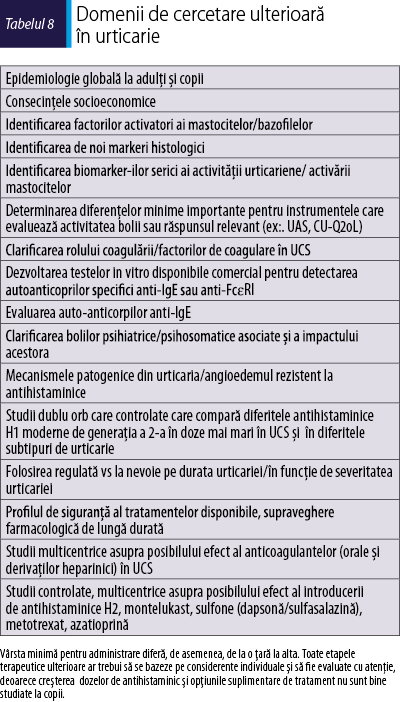
Epidemiologie globală la adulţi şi copii |
|
Consecinţele socioeconomice |
|
Identificarea factorilor activatori ai mastocitelor/bazofilelor |
|
Identificarea de noi markeri histologici |
|
Identificarea biomarker-ilor serici ai activităţii urticariene/ activării mastocitelor |
|
Determinarea diferenţelor minime importante pentru instrumentele care evaluează activitatea bolii sau răspunsul relevant (ex:. UAS, CU-Q2oL) |
|
Clarificarea rolului coagulării/factorilor de coagulare în UCS |
|
Dezvoltarea testelor in vitro disponibile comercial pentru detectarea autoanticoprilor specifici anti-IgE sau anti-FcɛRI |
|
Evaluarea auto-anticorpilor anti-IgE |
|
Clarificarea bolilor psihiatrice/psihosomatice asociate şi a impactului acestora |
|
Mecanismele patogenice din urticaria/angioedemul rezistent la antihistaminice |
|
Studii dublu orb care controlate care compară diferitele antihistaminice H1 moderne de generaţia a 2-a în doze mai mari în UCS şi în diferitele subtipuri de urticarie |
|
Folosirea regulată vs la nevoie pe durata urticariei/în funcţie de severitatea urticariei |
|
Profilul de siguranţă al tratamentelor disponibile, supraveghere farmacologică de lungă durată |
|
Studii multicentrice asupra posibilului efect al anticoagulantelor (orale şi derivaţilor heparinici) în UCS |
|
Studii controlate, multicentrice asupra posibilului efect al introducerii de antihistaminice H2, montelukast, sulfone (dapsonă/sulfasalazină), metotrexat, azatioprină |
Vârsta minimă pentru administrare diferă, de asemenea, de la o ţară la alta. Toate etapele terapeutice ulterioare ar trebui să se bazeze pe considerente individuale şi să fie evaluate cu atenţie, deoarece creşterea dozelor de antihistaminic şi opţiunile suplimentare de tratament nu sunt bine studiate la copii.
|
Ar trebui utilizată aceeaşi schemă de tratament la copii? |
||
|
Sugerăm utilizarea aceleiaşi scheme de tratament, cu precauţie la copiii cu urticarie cronică (bazat pe consens) |
↑ |
>90% |
5.6.2. Sarcină şi alăptare
În principiu, aceleaşi considerente se aplică şi femeilor însărcinate şi celor care alăptează. În general, utilizarea oricărui tratament sistemic trebuie evitat la femeile însărcinate, în special în primul trimestru de sarcină. Pe de altă parte, femeile însărcinate au dreptul la cea mai bună conduită terapeutică posibilă. Deşi siguranţa tratamentului nu a fost studiată în mod sistematic la femeile însărcinate care suferă de urticarie, trebuie subliniat faptul că posibilele efecte negative datorate nivelului crescut de histamină care apare în urticarie nu au fost studiate în sarcină. În ceea ce priveşte tratamentul, nu au fost raportate până în prezent defecte congenitale ale nou‑născuţilor la femeile care au folosit antihistaminice moderne de a doua generaţie în timpul sarcinii. Cu toate acestea, sunt disponibile numai studii de mărime mică din punctul de vedere al eşantionului pentru cetirizină162 şi o metaanaliză pentru loratadină163.
Mai mult, deoarece câteva antihistaminice moderne de a doua generaţie se eliberează acum fără prescripţie medicală, ele sunt utilizate pe scară largă atât în rinita alergică, dar şi în urticarie; se presupune că multe femei au folosit aceste medicamente în special la începutul sarcinii, cel puţin înainte de confirmarea ei. Cu toate acestea, întrucât în sarcină siguranţa este cea mai importantă şi obligatorie, sugestia pentru utilizarea antihistaminicelor moderne de generaţia a 2-a este de a prefera loratadina cu posibilă extrapolare la desloratadină şi cetirizină, cu o posibilă extrapolare la levocetirizină. Toate antihistaminicele H1 sunt excretate în laptele matern în concentraţii scăzute. Se recomandă utilizarea antihistaminicelor H1 de a doua generaţie, deoarece sugarii care sunt alăptaţi prezintă ocazional sedare din cauza antihistaminicelor H1 de generaţia întâi excretate prin laptele matern.
Doze crescute de antihistaminice moderne de generaţia a 2-a pot fi sugerate doar cu atenţie în sarcină, deoarece nu au fost efectuate studii de siguranţă, amintind că loratadina este metabolizată hepatic, ceea ce nu este cazul metabolitului său, desloratadina. Ar trebui evitate antihistaminicele H1 de primă generaţie100. Utilizarea de omalizumab în sarcină s-a dovedit a fi sigură şi până în prezent nu există nicio dovadă de teratogenitate164–166. Toate etapele ulterioare ar trebui să se bazeze pe considerente individuale, cu o preferinţă pentru medicamente care au un raport risc-beneficiu satisfăcător la gravide şi nou-născuţi în ceea ce priveşte teratogenitatea şi embriotoxicitatea. De exemplu, ciclosporina, deşi nu este teratogenică, este embriotoxică la modelele animale şi este asociată cu naşterea prematură şi cu greutatea scăzută la naştere la sugarii umani. Dacă beneficiile ciclosporinei în UC depăşesc riscurile la femeile însărcinate, acest lucru va trebui să fie determinat de la caz la caz. Cu toate acestea, toate deciziile ar trebui reevaluate în conformitate cu recomandările actuale publicate de autorităţile în vigoare.
|
Trebuie utilizată aceeaşi conduită terapeutică atât la femeile însărcinate cât şi în timpul alăptării? |
||
|
Sugerăm utilizarea aceleiaşi scheme de tratament cu precauţie atât la femeile însărcinate, cât şi la cele care alăptează după evaluarea raportului risc‑beneficiu. Nu trebuie utilizate medicamente contraindicate în sarcină (bazat pe consens) |
↑ |
>90% |
6. Nevoia de cercetări viitoare
Grupul de experţi şi participanţii au identificat mai multe domenii în care sunt necesare cercetări suplimentare. Aceste puncte sunt rezumate în tabelul 8.
Mulţumiri
Autorii mulţumesc medicilor şi specialiştilor care au contribuit la revizuirea şi actualizarea ghidurilor prin participarea activă la procesul democratic şi la discuţiile din cadrul celei de-a 5-a Reuniuni a Consensului Internaţional pentru Urticarie din 2016. Aceştia doresc să îşi exprime mulţumirile tuturor societăţilor naţionale pentru finanţarea delegaţilor lor şi următoarelor Societăţi, în special pentru contribuţia financiară suplimentară la costurile de îndeplinire şi lucrările de cercetare metodologică: EAACI, EADV, EDF, GA2LEN, WAO. De asemenea, îi mulţumim şi Tamarei Dörr pentru contribuţia substanţială în pregătirea acestui manuscris şi reţelei GA2LEN-UCARE (www.ga2len-ucare.com) pentru sprijinul ştiinţific.
Societăţi care ne susţin: AAAAI, Academia Americană de Alergologie, Astm şi Imunologie (susţinere prin comentarii); AAD, Academia Americană de Dermatologie; AAIITO, Asociaţia Italiană de Alergologi şi Imunologi din teritoriu şi spital; ACAAI, Colegiul American de Alergologie, Astm şi Imunologie; AEDV, Academia Spaniolă de Dermatologie şi Venerologie; APAAACI, Asociaţia Asia-Pacific de Alergologie şi Imunologie Clinică; ASBAI, Asociaţia Braziliană de Alergologie şi Imunopatologie; ASCIA, Societatea Australasiatică de Imunologie Clinică şi Alergologie; BAD, Asociaţia Britanică de Dermatologie; BSACI, Societatea Britanică de Alergologie şi Imunologie Clinică; CDA, Asociaţia Dermatologilor Chinezi; CMICA, Colegiul Mexican de Imunologie Clinică şi Alergologie; DDG, Societatea Germană de Dermatologie; DDS, Societatea Daneză de Dermatologie; DGAKI, Societatea Germană de Alergologie şi Imunologie Clinică; DSA, Societatea Daneză de Alergologie; DST, Societatea Thailandeză de Dermatologie; EAACI, Academia Europeană de Alergologie şi Imunologie Clinică; EDF, Forumul European de Dermatologie; EMBRN, Reţeaua Europeană de Cercetare a Mastocitului şi Bazofilului; ESCD, Societatea Europeană pentru Dermatita de Contact; GA2LEN, Reţeaua Europeană Globală de Alergologie şi Astm; IAACI, Asociaţia Israeliană de Alergologie şi Imunologie Clinică; IADVL, Asociaţia Indiană de Dermatologie, Venerologie şi Leprologie; JDA, Asociaţia Japoneză de Dermatologie; NVvA, Societatea Daneză de Alergologie (delegatul oficial a fost de acord cu acest ghid, dar la momentul publicării lui scrisoarea oficială de aprobare nu a fost primită. Dacă această scrisoare va fi primită mai târziu, se va publica o actualizare pe site-ul GA2LEN.); MSAI, Societatea Malayezeană de Alergologie şi Imunologie; ÖGDV, Societatea Austriacă de Dermatologie; PSA, Societatea Poloneză de Alergologie; RAACI, Asociaţia Rusă de Alergologie şi Imunologie Clinică; SBD, Societatea Braziliană de Dermatologie; SFD, Societatea Franceză de Dermatologie; SGAI, Societatea Elveţiană de Dermatologie şi Venerologie; SIAAIC, Societatea Italiană de Alergologie, Astm şi Imunologie Clinică; SIDeMaST, Societatea Italiană de Dermatologie Medicală, Chirurgicală şi Estetică şi de Boli Transmisibile Sexual; SPDV, Societatea Portugheză de Dermatologie şi Venerologie; TSD, Societatea Turcă de Dermatologie; UNEV, Reţeaua de Urticarie; WAO, Organizaţia Mondială de Alergologie.
Conflicte de interese
Acestea sunt doar conflictele de interese ale primului autor. Vă rugăm să verificaţi tabelul din secţiunea Metode, unde sunt prezentate în detaliu conflictele de interese ale tuturor autorilor
ORCID
T. Zuberbier http://orcid.org/0000-0002-1466-8875
R. Asero http://orcid.org/0000-0002-8277-1700
J. A. Bernstein http://orcid.org/0000-0002-3476-1196
Z. Brzoza http://orcid.org/0000-0002-1230-7013
M. Hide http://orcid.org/0000-0001-6183-6467
D. Larenas-Linnemann http://orcid.org/0000-0002-5713-5331
Bibliografie
-
Zuberbier T, Asero R, Bindslev-Jensen C, et al. EAACI/GA(2)LEN/ EDF/WAO guideline: definition, classification and diagnosis of urti-caria. Allergy 2009;64:1417-1426.
-
Zuberbier T, Asero R, Bindslev-Jensen C, et al. EAACI/GA(2)LEN/ EDF/WAO guideline: management of urticaria. Allergy 2009;64:1427-1443.
-
Zuberbier T, Aberer W, Asero R, et al. The EAACI/GA(2) LEN/EDF/ WAO Guideline for the definition, classification, diagnosis, and man-agement of urticaria: the 2013 revision and update. Allergy 2014;69:868-887.
-
Zuberbier T, Aberer W, Asero R, et al. Methods report on the development of the 2013 revision and update of the EAACI/GA2 LEN/EDF/WAO guideline for the definition, classification, diagnosis, and management of urticaria. Allergy 2014;69:e1-29.
-
Dressler C, Rosumeck S, Werner RN, Magerl M, Metz M, Maurer M, Nast A, Zuberbier T. Executive summary: methods and evidence report for the evidence- and consensus-based (S3) Guideline for the definition, classification, diagnosis, and management of urticaria - revision and update 2017. Allergy. 2018;73:1145-1146.
-
AGREE Next Steps Consortium. The AGREE II Instrument; 2009. http://www.agreetrust.org/. Accessed January 12, 2015.
-
Higgins JPT, Green S, Cochrane C. Cochrane handbook for system-atic reviews of interventions; 2011. http://www.cochrane-handb ook.org/
-
Guyatt GH, Oxman AD, Kunz R, et al. GRADE guidelines: 2. Fram-ing the question and deciding on important outcomes. J Clin Epi-demiol 2011;64:395-400.
-
Finlay AY, Kaplan AP, Beck LA, et al. Omalizumab substantially improves dermatology-related quality of life in patients with chronic spontaneous urticaria. J Eur Acad Dermatol Venereol 2017;31:1715-1721.
-
Atkins D, Best D, Briss PA, et al. Grading quality of evidence and strength of recommendations. BMJ 2004;328:1490.
-
GRADEpro GDT: GRADEpro Guideline Development Tool. McMas-ter University (developed by Evidence Prime, Inc.); 2015.
-
Jones J, Hunter D. Consensus methods for medical and health ser-vices research. BMJ 1995;311:376-380.
-
Haas N, Schadendorf D, Henz BM. Differential endothelial adhesion molecule expression in early and late whealing reactions. Int Arch Allergy Immunol 1998;115:210-214.
-
Peteiro C, Toribio J. Incidence of leukocytoclastic vasculitis in chronic idiopathic urticaria. Study of 100 cases. Am J Dermatopathol 1989;11:528-533.
-
Ito Y, Satoh T, Takayama K, Miyagishi C, Walls AF, Yokozeki H. Basophil recruitment and activation in inflammatory skin diseases. Allergy 2011;66:1107-1113.
-
Kay AB, Clark P, Maurer M, Ying S. Elevations in T-helper-2-initiating cytokines (interleukin-33, interleukin-25 and thymic stromal lymphopoietin) in lesional skin from chronic spontaneous (‘idiopathic’) urticaria. Br J Dermatol 2015;172:1294-1302.
-
Kay AB, Ying S, Ardelean E, et al. Calcitonin gene-related peptide and vascular endothelial growth factor are expressed in lesional but not uninvolved skin in chronic spontaneous urticaria. Clin Exp Allergy 2014;44:1053-1060.
-
Zuberbier T, Schadendorf D, Haas N, Hartmann K, Henz BM. Enhanced P-selectin expression in chronic and dermographic urticaria. Int Arch Allergy Immunol 1997;114:86-89.
-
Kay AB, Ying S, Ardelean E, et al. Elevations in vascular markers and eosinophils in chronic spontaneous urticarial weals with low-level persistence in uninvolved skin. Br J Dermatol 2014;171: 505-511.
-
Greaves MW. Chronic urticaria. N Engl J Med 1995;332:1767-1772.
-
Kaplan AP. Clinical practice. Chronic urticaria and angioedema. N Engl J Med 2002;346:175-179.
-
Hermes B, Prochazka AK, Haas N, Jurgovsky K, Sticherling M, Henz BM. Upregulation of TNF-alpha and IL-3 expression in lesional and uninvolved skin in different types of urticaria. J Allergy Clin Immunol 1999;103:307-314.
-
Maurer M, Weller K, Bindslev-Jensen C, et al. Unmet clinical needs in chronic spontaneous urticaria. A GA(2)LEN task force report. Allergy 2011;66:317-330.
-
Baiardini I, Braido F, Bindslev-Jensen C, et al. Recommendations for assessing patient-reported outcomes and health-related quality of life in patients with urticaria: a GA(2) LEN taskforce position paper. Allergy 2011;66:840-844.
-
Maurer M, Staubach P, Raap U, et al. H1-antihistamine-refractory chronic spontaneous urticaria: it’s worse than we thought – first results of the multicenter real-life AWARE study. Clin Exp Allergy 2017;47:684-692.
-
Maurer M, Staubach P, Raap U, Richter-Huhn G, Baier-Ebert M, Chapman-Rothe N. ATTENTUS, a German online survey of patients with chronic urticaria highlighting the burden of disease, unmet needs and real-life clinical practice. Br J Dermatol 2016;174:892-894.
-
Maurer M, Abuzakouk M, Berard F, et al. The burden of chronic spontaneous urticaria is substantial: real-world evidence from ASSURE-CSU. Allergy 2017;72:2005-2016.
-
O’Donnell BF, Lawlor F, Simpson J, Morgan M, Greaves MW. The impact of chronic urticaria on the quality of life. Br J Dermatol 1997;136:197-201.
-
Baiardini I, Giardini A, Pasquali M, et al. Quality of life and patients’ satisfaction in chronic urticaria and respiratory allergy. Allergy 2003;58:621-623.
-
Parisi CA, Ritchie C, Petriz N, Morelo Torres C. Direct medical costs of chronic urticaria in a private health organization of Buenos Aires, Argentina. Value Health Reg Issues 2016;11:57-59.
-
Broder MS, Raimundo K, Antonova E, Chang E. Resource use and costs in an insured population of patients with chronic idiopathic/ spontaneous urticaria. Am J Clin Dermatol 2015;16:313-321.
-
Graham J, McBride D, Stull D, et al. Cost utility of omalizumab compared with standard of care for the treatment of chronic spontaneous urticaria. Pharmacoeconomics 2016;34:815-827.
-
Zuberbier T, Maurer M. Urticaria: current opinions about etiology, diagnosis and therapy. Acta Derm Venereol 2007;87:196-205.
-
Kolkhir P, Church MK, Weller K, Metz M, Schmetzer O, Maurer M. Autoimmune chronic spontaneous urticaria: what we know and what we do not know. J Allergy Clin Immunol 2017;139:1772-1781.
-
Asero R, Tedeschi A, Marzano AV, Cugno M. Chronic urticaria: a focus on pathogenesis. F1000Res 2017;6:1095.
-
Kolkhir P, Balakirski G, Merk HF, Olisova O, Maurer M. Chronic spontaneous urticaria and internal parasites–a systematic review. Allergy 2016;71:308-322.
-
Imbalzano E, Casciaro M, Quartuccio S, et al. Association between urticaria and virus infections: a systematic review. Allergy Asthma Proc 2016;37:18-22.
-
Minciullo PL, Cascio A, Barberi G, Gangemi S. Urticaria and bacterial infections. Allergy Asthma Proc 2014;35:295-302.
-
Foti C, Nettis E, Cassano N, Di Mundo I, Vena GA. Acute allergic reactions to Anisakis simplex after ingestion of anchovies. Acta Derm Venereol 2002;82:121-123.
-
Ventura MT, Napolitano S, Menga R, Cecere R, Asero R. Anisakis simplex hypersensitivity is associated with chronic urticaria in endemic areas. Int Arch Allergy Immunol 2013;160:297-300.
-
Dionigi PC, Menezes MC, Forte WC. A prospective ten-year follow-up of patients with chronic urticaria. Allergol Immunopathol (Madr) 2016;44:286-291.
-
Shabrawy RM, Gharib K. Helicobacter pylori Infection as a risk factor in patients suffering from food allergy and urticaria. Egypt J Immunol 2016;23:67-75.
-
Curth HM, Dinter J, Nigemeier K, Kutting F, Hunzelmann N, Steffen HM. Effects of Helicobacter pylori eradication in chronic sponta-neous urticaria: results from a retrospective cohort study. Am J Clin Dermatol 2015;16:553-558.
-
Rasooly MM, Moye NA, Kirshenbaum AS. Helicobacter pylori: a significant and treatable cause of chronic urticaria and angioedema. Nurse Pract 2015;40:1-6.
-
Chen YJ, Wu CY, Shen JL, Chen TT, Chang YT. Cancer risk in patients with chronic urticaria: a population-based cohort study. Arch Dermatol 2012;148:103-108.
-
Konstantinou GN, Asero R, Maurer M, Sabroe RA, Schmid-Grendelmeier P, Grattan CE. EAACI/GA(2)LEN task force consensus report: the autologous serum skin test in urticaria. Allergy 2009;64:1256-1268.
-
Konstantinou GN, Asero R, Ferrer M, et al. EAACI taskforce position paper: evidence for autoimmune urticaria and proposal for defining diagnostic criteria. Allergy 2013;68:27-36.
-
Curto-Barredo L, Yelamos J, Gimeno R, Mojal S, Pujol RM, Gimenez-Arnau A. Basophil Activation Test identifies the patients with Chronic Spontaneous Urticaria suffering the most active disease. Immun Inflamm Dis 2016;4:441-445.
-
Netchiporouk E, Moreau L, Rahme E, Maurer M, Lejtenyi D, Ben-Shoshan M. Positive CD63 basophil activation tests are common in children with chronic spontaneous urticaria and linked to high disease activity. Int Arch Allergy Immunol 2016;171:81-88.
-
Kim Z, Choi BS, Kim JK, Won DI. Basophil markers for identification and activation in the indirect basophil activation test by flow cytometry for diagnosis of autoimmune urticaria. Ann Lab Med 2016;36:28-35.
-
Iqbal K, Bhargava K, Skov PS, Falkencrone S, Grattan CE. A positive serum basophil histamine release assay is a marker for ciclosporin-responsiveness in patients with chronic spontaneous urticaria. Clin Transl Allergy 2012;2:19.
-
Gericke J, Metz M, Ohanyan T, et al. Serum autoreactivity predicts time to response to omalizumab therapy in chronic spontaneous urticaria. J Allergy Clin Immunol 2017;139:1059-1061.
-
Grattan CEH, Dawn G, Gibbs S, Francis DM. Blood basophil numbers in chronic ordinary urticaria and healthy controls: diurnal variation, influence of loratadine and prednisolone and relationship to disease activity. Clin Exp Allergy 2003;33:337-341.
-
Eckman JA, Hamilton RG, Gober LM, Sterba PM, Saini SS. Basophil phenotypes in chronic idiopathic urticaria in relation to disease activity and autoantibodies. J Invest Dermatol 2008;128:1956-1963.
-
Saini SS, Omachi TA, Trzaskoma B, et al. Effect of omalizumab on blood basophil counts in patients with chronic idiopathic/spontaneous urticaria. J Invest Dermatol 2017;137:958-961.
-
Kolkhir P, Andre F, Church MK, Maurer M, Metz M. Potential blood biomarkers in chronic spontaneous urticaria. Clin Exp Allergy 2017;47:19-36.
-
Asero R, Marzano AV, Ferrucci S, Cugno M. D-dimer plasma levels parallel the clinical response to omalizumab in patients with severe chronic spontaneous urticaria. Int Arch Allergy Immunol 2017;172:40-44.
-
Mlynek A, Zalewska-Janowska A, Martus P, Staubach P, Zuberbier T, Maurer M. How to assess disease activity in patients with chronic urticaria? Allergy 2008;63:777-780.
-
Hawro T, Ohanyan T, Schoepke N, et al. Comparison and inter-pretability of the available urticaria activity scores. Allergy 2017;73:251-255.
-
Weller KG, Magerl M, Tohme N, et al. Development, validation and initial results of the angioedema activity score. Allergy 2013;68:1185-1192.
-
Ohanyan T, Schoepke N, Bolukbasi B, et al. Responsiveness and minimal important difference of the urticaria control test. J Allergy Clin Immunol 2017;140:1710-1713.
-
Weller K, Groffik A, Church MK, et al. Development and validation of the Urticaria Control Test: a patient-reported outcome instrument for assessing urticaria control. J Allergy Clin Immunol 2014;133:1365-1372.
-
Martinez-Escala ME, Curto-Barredo L, Carnero L, Pujol RM, Gime-nez-Arnau AM. Temperature thresholds in assessment of the clinical course of acquired cold contact urticaria: a prospective observational one-year study. Acta Derm Venereol 2015;95:278-282.
-
Abajian M, Curto-Barredo L, Krause K, et al. Rupatadine 20 mg and 40 mg are effective in reducing the symptoms of chronic cold urticaria. Acta Derm Venereol 2016;96:56-59.
-
Mlynek A, Magerl M, Siebenhaar F, et al. Results and relevance of critical temperature threshold testing in patients with acquired cold urticaria. Br J Dermatol 2010;162:198-200.
-
Koch K, Weller K, Werner A, Maurer M, Altrichter S. Antihistamine updosing reduces disease activity in patients with difficult-to-treat cholinergic urticaria. J Allergy Clin Immunol 2016;138:1483-1485.
-
Maurer M, Schutz A, Weller K, et al. Omalizumab is effective in symptomatic dermographism-results of a randomized placebo-controlled trial. J Allergy Clin Immunol 2017;140:870-873.
-
Metz M, Schutz A, Weller K, et al. Omalizumab is effective in cold urticaria-results of a randomized placebo-controlled trial. J Allergy Clin Immunol 2017;140:864-867.
-
Magerl M, Altrichter S, Borzova E, et al. The definition, diagnostic testing, and management of chronic inducible urticarias – the EAACI/GA(2) LEN/EDF/UNEV consensus recommendations 2016 update and revision. Allergy 2016;71:780-802.
-
Magerl M, Abajian M, Krause K, Altrichter S, Siebenhaar F, Church MK. An improved Peltier effect-based instrument for critical temperature threshold measurement in cold- and heat-induced urticaria. J Eur Acad Dermatol Venereol 2015;29:2043-2045.
-
Schoepke N, Abajian M, Church MK, Magerl M. Validation of a simplified provocation instrument for diagnosis and threshold testing of symptomatic dermographism. Clin Exp Dermatol 2015;40:399-403.
-
Mlynek A, Vieira dos Santos R, Ardelean E, et al. A novel, simple, validated and reproducible instrument for assessing provocation threshold levels in patients with symptomatic dermographism. Clin Exp Dermatol 2013;38:360-366.
-
Altrichter S, Salow J, Ardelean E, Church MK, Werner A, Maurer M. Development of a standardized pulse-controlled ergometry test for diagnosing and investigating cholinergic urticaria. J Dermatol Sci 2014;75:88-93.
-
Azkur D, Civelek E, Toyran M, et al. Clinical and etiologic evaluation of the children with chronic urticaria. Allergy Asthma Proc 2016;37:450-457.
-
Lee SJ, Ha EK, Jee HM, et al. Prevalence and risk factors of urticaria with a focus on chronic urticaria in children. Allergy Asthma Immunol Res 2017;9:212-219.
-
Church MK, Weller K, Stock P, Maurer M. Chronic spontaneous urticaria in children: itching for insight. Pediatr Allergy Immunol 2011;22:1-8.
-
Maurer M, Church MK, Weller K. Chronic urticaria in children – still itching for insight. JAMA Dermatol 2017;153:1221-1222.
-
Kuemmerle-Deschner JB, Ozen S, Tyrrell PN, et al. Diagnostic criteria for cryopyrin-associated periodic syndrome (CAPS). Ann Rheum Dis 2017;76:942-947.
-
Kowalski ML, Woessner K, Sanak M. Approaches to the diagnosis and management of patients with a history of nonsteroidal anti-inflammatory drug-related urticaria and angioedema. J Allergy Clin Immunol 2015;136:245-251.
-
Shakouri A, Compalati E, Lang DM, Khan DA. Effectiveness of Heli-cobacter pylori eradication in chronic urticaria: evidence-based analysis using the grading of recommendations assessment, development, and evaluation system. Curr Opin Allergy Clin Immunol 2010;10:362-369.
-
Ishaq S, Nunn L. Helicobacter pylori and gastric cancer: a state of the art review. Gastroenerol Hepatol Bed Bench 2015;8(Suppl1):6-14.
-
Henz BM, Zuberbier T. Causes of urticaria. In: Henz BM, Zuberbier T, Grabbe J, Monroe E, eds. Urticaria – clinical, diagnostic and therapeutic aspects. Berlin: Springer; 1998.
-
Ergon MC, ilknur T, Yucesoy M, Ozkan S. Candida spp. colonization and serum anticandidal antibody levels in patients with chronic urticaria. Clin Exp Dermatol 2007;32:740-743.
-
Zuberbier T, ChantraineKess S, Hartmann K, Czarnetzki BM. Pseudoallergen-free diet in the treatment of chronic urticaria – a prospective study. Acta Derm Venereol 1995;75:484-487.
-
Bruno G, Andreozzi P, Graf U. Exercise-induced urticaria-angioedema syndrome: a role in gastroesophageal reflux. In: Vena GA, Puddu P, eds. Proceedings of the international symposium on urticaria. Bari, Milan: Editrice CSH; 1998: 85-89.
-
Varghese R, Rajappa M, Chandrashekar L, et al. Association among stress, hypocortisolism, systemic inflammation, and disease severity in chronic urticaria. Ann Allergy Asthma Immunol 2016;116:344-348.
-
Kounis NG, Kounis GN, Soufras GD. Exercise-induced urticaria, cholinergic urticaria, and Kounis syndrome. J Pharmacol Pharmacother 2016;7:48-50.
-
Grattan CE, Francis DM, Slater NG, Barlow RJ, Greaves MW. Plasmapheresis for severe, unremitting, chronic urticaria. Lancet 1992;339:1078-1080.
-
Juhlin L. Recurrent urticaria: clinical investigation of 330 patients. Br J Dermatol 1981;104:369-381.
-
Pfrommer C, Bastl R, Vieths S, Ehlers I, Henz BM, Zuberbier T. Characterization of naturally occurring pseudoallergens causing chronic urticaria. J Allergy Clin Immunol 1996;97:367.
-
Pigatto PD, Valsecchi RH. Chronic urticaria: a mystery. Allergy 2000;55:306-308.
-
Bunselmeyer B, Laubach HJ, Schiller M, Stanke M, Luger TA, Brehler R. Incremental build-up food challenge–a new diagnostic approach to evaluate pseudoallergic reactions in chronic urticaria: a pilot study: stepwise food challenge in chronic urticaria. Clin Exp Allergy 2009;39:116-126.
-
Nettis E, Colanardi MC, Ferrannini A, Tursi A. Sodium benzoate-induced repeated episodes of acute urticaria/angioedema: randomized controlled trial. Br J Dermatol 2004;151:898-902.
-
Akoglu G, Atakan N, Cakir B, Kalayci O, Hayran M. Effects of low pseudoallergen diet on urticarial activity and leukotriene levels in chronic urticaria. Arch Dermatol Res 2012;304:257-262.
-
Wagner N, Dirk D, Peveling-Oberhag A, et al. A Popular myth – low-histamine diet improves chronic spontaneous urticaria – fact or fiction? J Eur Acad Dermatol Venereol 2016;31:650-655.
-
Beissert S, Stander H, Schwarz T. UVA rush hardening for the treatment of solar urticaria. J Am Acad Dermatol 2000;42:1030-1032.
-
Grob JJ, Auquier P, Dreyfus I, Ortonne JP. How to prescribe antihistamines for chronic idiopathic urticaria: desloratadine daily vs PRN and quality of life. Allergy 2009;64:605-612.
-
Weller K, Ardelean E, Scholz E, Martus P, Zuberbier T, Maurer M. Can on-demand non-sedating antihistamines improve urticaria symptoms? A double-blind, randomized, Single-dose study. Acta Derm Venereol 2013;93:168-174.
-
Vonakis BM, Saini SS. New concepts in chronic urticaria. Curr Opin Immunol 2008;20:709-716.
-
Church MK, Maurer M, Simons FE, et al. Risk of first-generation H (1)-antihistamines: a GA(2)LEN position paper. Allergy 2010;65:459-466.
-
Bousquet J, Khaltaev N, Cruz AA, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) 2008 update (in collaboration with the World Health Organization, GA(2)LEN and AllerGen). Allergy 2008;63(Suppl 86):8-160.
-
Kubo N, Senda M, Ohsumi Y, et al. Brain histamine H1 receptor occupancy of loratadine measured by positron emission topography: comparison of H1 receptor occupancy and proportional impairment ratio. Hum Psychopharmacol 2011;26:133-139.
-
Kontou-Fili K, Paleologos G, Herakleous M. Suppression of his-tamine-induced skin reactions by loratadine and cetirizine diHCl. Eur J Clin Pharmacol 1989;36:617-619.
-
Zuberbier T, Munzberger C, Haustein U, et al. Double-blind cross-over study of high-dose cetirizine in cholinergic urticaria. Dermatology 1996;193:324-327.
-
Kontou-Fili KK, Maniakatou G, Demaka P. Therapeutic effect of cetirizine 2 HCl in delayed pressure urticaria. Health Sci Rev 1989;3:23-25.
-
Wanderer AA, Ellis EF. Treatment of cold urticaria with cyproheptadine. J Allergy Clin Immunol 1971;48:366-371.
-
Kaplan AP, Gray L, Shaff RE, Horakova Z, Beaven MA. In vivo studies of mediator release in cold urticaria and cholinergic urticaria. J Allergy Clin Immunol 1975;55:394-402.
-
Staevska M, Popov TA, Kralimarkova T, et al. The effectiveness of levocetirizine and desloratadine in up to 4 times conventional doses in difficult-to-treat urticaria. J Allergy Clin Immunol 2010;125: 676-682.
-
Siebenhaar F, Degener F, Zuberbier T, Martus P, Maurer M. High-dose desloratadine decreases wheal volume and improves cold provocation thresholds compared with standard-dose treatment in patients with acquired cold urticaria: a randomized, placebo-con-trolled, crossover study. J Allergy Clin Immunol 2009;123:672-679.
-
Gimenez-Arnau A, Izquierdo I, Maurer M. The use of a responder analysis to identify clinically meaningful differences in chronic urticaria patients following placebo- controlled treatment with rupatadine 10 and 20 mg. J Eur Acad Dermatol Venereol 2009;23:1088-1091.
-
Guillen-Aguinaga S, Jauregui Presa I, Aguinaga-Ontoso E, Guillen-Grima F, Ferrer M. Updosing nonsedating antihistamines in patients with chronic spontaneous urticaria: a systematic review and meta-analysis. Br J Dermatol 2016;175:1153-1165.
-
Saini S, Rosen KE, Hsieh HJ, et al. A randomized, placebo-controlled, dose-ranging study of single-dose omalizumab in patients with H-1-antihistamine-refractory chronic idiopathic urticaria. J Allergy Clin Immunol 2011;128:567-U195.
-
Maurer M, Altrichter S, Bieber T, et al. Efficacy and safety of omalizumab in patients with chronic urticaria who exhibit IgE against thyroperoxidase. J Allergy Clin Immunol 2011;128:202-209.
-
Saini SS, Bindslev-Jensen C, Maurer M, et al. Efficacy and safety of omalizumab in patients with chronic idiopathic/spontaneous urticaria who remain symptomatic on H1 antihistamines: a randomized, placebo-controlled study. J Invest Dermatol 2015;135:67-75.
-
Maurer M, Rosen K, Hsieh HJ, et al. Omalizumab for the treatment of chronic idiopathic or spontaneous urticaria. N Engl J Med 2013;368:924-935.
-
Kaplan A, Ledford D, Ashby M, et al. Omalizumab in patients with symptomatic chronic idiopathic/spontaneous urticaria despite standard combination therapy. J Allergy Clin Immunol 2013;132:101-109.
-
Zhao ZT, Ji CM, Yu WJ, et al. Omalizumab for the treatment of chronic spontaneous urticaria: a meta-analysis of randomized clinical trials. J Allergy Clin Immunol 2016;137:1742-1750.
-
Maurer M, Metz M, Brehler R, et al. Omalizumab treatment in chronic inducible urticaria: a systematic review of published evidence. J Allergy Clin Immunol 2017; in press.
-
Metz M, Altrichter S, Ardelean E, et al. Anti-immunoglobulin E treatment of patients with recalcitrant physical urticaria. Int Arch Allergy Immunol 2011;154:177-180.
-
Metz M, Bergmann P, Zuberbier T, Maurer M. Successful treatment of cholinergic urticaria with anti-immunoglobulin E therapy. Allergy 2008;63:247-249.
-
Boyce JA. Successful treatment of cold-induced urticaria/anaphy-laxis with anti-IgE. J Allergy Clin Immunol 2006;117:1415-1418.
-
Guzelbey O, Ardelean E, Magerl M, Zuberbier T, Maurer M, Metz. Successful treatment of solar urticaria with anti-immunoglobulin therapy. Allergy 2008;63:1563-1565.
-
Bullerkotte U, Wieczorek D, Kapp A, Wedi B. Effective treatment of refractory severe heat urticaria with omalizumab. Allergy 2010;65:931-932.
-
Krause K, Ardelean E, Kessler B, et al. Antihistamine-resistant urticaria factitia successfully treated with anti-immunoglobulin E therapy. Allergy 2010;65:1494-1495.
-
Bindslev-Jensen C, Skov PS. Efficacy of omalizumab in delayed pressure urticaria: a case report. Allergy 2010;65:138-139.
-
Staubach P, Metz M, Chapman-Rothe N, et al. Effect of omalizumab on angioedema in H1 -antihistamine-resistant chronic spontaneous urticaria patients: results from X-ACT, a randomized controlled trial. Allergy 2016;71:1135-1144.
-
Maurer M, Sofen H, Ortiz B, Kianifard F, Gabriel S, Bernstein JA. Positive impact of omalizumab on angioedema and quality of life in patients with refractory chronic idiopathic/spontaneous urticaria: analyses according to the presence or absence of angioedema. J Eur Acad Dermatol Venereol 2017;31:1056-1063.
-
Maurer M, Kaplan A, Rosen K, et al. The XTEND-CIU study: long term use of Omalizumab in Chronic Idiopathic Urticaria. J Allergy Clin Immunol 2017; in press.
-
Metz M, Ohanyan T, Church MK, Maurer M. Retreatment with omalizumab results in rapid remission in chronic spontaneous and inducible urticaria. JAMA Dermatol 2014;150:288-290.
-
Stellato C, de Paulis A, Ciccarelli A, et al. Anti-inflammatory effect of cyclosporin A on human skin mast cells. J Invest Dermatol 1992;98:800-804.
-
Harrison CA, Bastan R, Peirce MJ, Munday MR, Peachell PT. Role of calcineurin in the regulation of human lung mast cell and basophil function by cyclosporine and FK506. Br J Pharmacol 2007;150:509-518.
-
Grattan CE, O’Donnell BF, Francis DM, et al. Randomized double-blind study of cyclosporin in chronic ‘idiopathic’ urticaria. Br J Der-matol 2000;143:365-372.
-
Vena GA, Cassano N, Colombo D, Peruzzi E, Pigatto P. Cyclosporine in chronic idiopathic urticaria: a double-blind, randomized, placebo-controlled trial. J Am Acad Dermatol 2006;55:705-709.
-
Kulthanan K, Chaweekulrat P, Komoltri C, et al. Cyclosporine for chronic spontaneous urticaria: a meta-analysis and systematic review. J Allergy Clin Immunol Pract 2017; in press.
-
Doshi DR, Weinberger MM. Experience with cyclosporine in children with chronic idiopathic urticaria. Pediatr Dermatol 2009;26:409-413.
-
Zuberbier T, Ifflander J, Semmler C, Henz BM. Acute urticaria: clinical aspects and therapeutic responsiveness. Acta Derm Venereol 1996;76:295-297.
-
Asero R, Tedeschi A. Usefulness of a short course of oral pred-nisone in antihistamine-resistant chronic urticaria: a retrospective analysis. J Investig Allergol Clin Immunol 2010;20:386-390.
-
Rutkowski K, Grattan CEH. How to manage chronic urticaria ‘be-yond’ guidelines: a practical algorithm. Clin Exp Allergy 2017;47:710-718.
-
Magerl M, Philipp S, Manasterski M, Friedrich M, Maurer M. Successful treatment of delayed pressure urticaria with anti-TNF-alpha. Allergy Clin Immunol 2007;119:752-754.
-
O’Donnell BF, Barr RM, Black AK, et al. Intravenous immunoglobulin in autoimmune chronic urticaria. Br J Dermatol 1998;138:101-106.
-
Dawn G, Urcelay M, Ah-Weng A, O’Neill SM, Douglas WS. Effect of high-dose intravenous immunoglobulin in delayed pressure urticaria. Br J Dermatol 2003;149:836-840.
-
Pereira C, Tavares B, Carrapatoso I, et al. Low-dose intravenous gammaglobulin in the treatment of severe autoimmune urticaria. Eur Ann Allergy Clin Immunol 2007;39:237-242.
-
Mitzel-Kaoukhov H, Staubach P, Muller-Brenne T. Effect of high-dose intravenous immunoglobulin treatment in therapy-resistant chronic spontaneous urticaria. Ann Allergy Asthma Immunol 2010;104:253-258.
-
Bangsgaard N, Skov L, Zachariae C. Treatment of refractory chronic spontaneous urticaria with adalimumab. Acta Derm Venereol 2017;97:524-525.
-
Sand FL, Thomsen SF. TNF-alpha inhibitors for chronic urticaria: experience in 20 patients. J Allergy (Cairo) 2013;2013:130905.
-
Hannuksela M, Kokkonen EL. Ultraviolet light therapy in chronic urticaria. Acta Derm Venereol 1985;65:449-450.
-
Borzova E, Rutherford A, Konstantinou GN, Leslie KS, Grattan CEH. Narrowband ultraviolet B phototherapy is beneficial in anti-histamine-resistant symptomatic dermographism: a pilot study. J Am Acad Dermatol 2008;59:752-757.
-
Engin B, Ozdemir M, Balevi A, Mevlitoglu I. Treatment of chronic urticaria with narrowband ultraviolet B phototherapy: a randomized controlled trial. Acta Derm Venereol 2008;88:247-251.
-
Thormann J, Laurberg G, Zachariae H. Oral sodium cromoglycate in chronic urticaria. Allergy 1980;35:139-141.
-
Laurberg G. Tranexamic acid (Cyklokapron) in chronic urticaria: a double-blind study. Acta Derm Venereol 1977;57:369-370.
-
Lawlor F, Ormerod AD, Greaves MW. Calcium antagonist in the treatment of symptomatic dermographism. Low-dose and high-dose studies with nifedipine. Dermatologica 1988;177:287-291.
-
Lawlor F, Black AK, Ward AM, Morris R, Greaves MW. Delayed pressure urticaria, objective evaluation of a variable disease using a dermographometer and assessment of treatment using colchicine. Br J Dermatol 1989;120:403-408.
-
Dover JS, Black AK, Ward AM, Greaves MW. Delayed pressure urticaria. Clinical features, laboratory investigations, and response to therapy of 44 patients. J Am Acad Dermatol 1988;18:1289-1298.
-
Asero R, Tedeschi A, Cugno M. Heparin and tranexamic Acid therapy may be effective in treatment-resistant chronic urticaria with elevated d-dimer: a pilot study. Int Arch Allergy Immunol 2010;152:384-389.
-
Nayak AS, Berger WE, LaForce CF, et al. Randomized, placebo-controlled study of cetirizine and loratadine in children with seasonal allergic rhinitis. Allergy Asthma Proc 2017;38:222-230.
-
Gupta S, Khalilieh S, Kantesaria B, Banfield C. Pharmacokinetics of desloratadine in children between 2 and 11 years of age. Br J Clin Pharmacol 2007;63:534-540.
-
Gupta SK, Kantesaria B, Banfield C, Wang Z. Desloratadine dose selection in children aged 6 months to 2 years: comparison of population pharmacokinetics between children and adults. Br J Clin Pharmacol 2007;64:174-184.
-
Meltzer EO, Scheinmann P, Rosado Pinto JE, et al. Safety and efficacy of oral fexofenadine in children with seasonal allergic rhinitis – a pooled analysis of three studies. Pediatr Allergy Immunol 2004;15:253-260.
-
Pampura AN, Papadopoulos NG, Spicak V, Kurzawa R. Evidence for clinical safety, efficacy, and parent and physician perceptions of levocetirizine for the treatment of children with allergic disease. Int Arch Allergy Immunol 2011;155:367-378.
-
Potter P, Mitha E, Barkai L, et al. Rupatadine is effective in the treatment of chronic spontaneous urticaria in children aged 2-years. Pediatr Allergy Immunol 2016;27:55-61.
-
Novak Z, Yanez A, Kiss I, et al. Safety and tolerability of bilastine 10 mg administered for 12 weeks in children with allergic diseases. Pediatr Allergy Immunol 2016;27:493-498.
-
Weber-Schoendorfer C, Schaefer C. The safety of cetirizine during pregnancy. A prospective observational cohort study. Reprod Toxicol 2008;26:19-23.
-
Schwarz EBMM, Nayak S, Koren G. Risk of hypospadias in off-spring of women using loratadine during pregnancy: a systematic review and meta-analysis. Drug Saf 2008;31:775-788.
-
Namazy J, Cabana MD, Scheuerle AE, et al. The Xolair Pregnancy Registry (EXPECT): the safety of omalizumab use during pregnancy. J Allergy Clin Immunol 2015;135:407-412.
-
Gonzalez-Medina M, Curto-Barredo L, Labrador-Horrillo M, Gimenez-Arnau A. Omalizumab use during pregnancy for chronic spontaneous urticaria (CSU): report of two cases. J Eur Acad Der-matol Venereol 2017;31:e245-e246.
-
Ghazanfar MN, Thomsen SF. Successful and safe treatment of chronic spontaneous urticaria with omalizumab in a woman during two consecutive pregnancies. Case Rep Med 2015;2015:368053.
-
Balshem H, Helfand M, Schunemann HJ, et al. GRADE guidelines: Rating the quality of evidence. J Clin Epidemiol 2011;64:401-
-
Maurer M. Cold urticaria. In: Saini SS, Callen J, editors. UpToDate. Boston, MA: Wolters Kluwer Health; 2014.





