SUPLIMENT TRATAMENTUL ÎN ALERGII
Evaluarea reacţiilor de hipersensibilitate la betalactamine
The assessment of hypersesibility reactions to betalactams
Abstract
Adverse drug reactions represent an important morbidity and mortality cause. The true prevalence and occurrence of the adverse drug reactions is not known. Females are predisposed to develop allergy to antibiotics more frequently. Hypersensitivity reactions to betalactams are classified as immediate or nonimmediate. Immediate reactions usually appear within one hour of drug-intake and are mediated by specific IgE antibodies. Nonimmediate reactions are those occurring more than one hour after drug intake, and can be T-cell mediated. Skin testing is the basic diagnostic tool, although in patients with a history of severe reactions, in vitro tests are recommended. Nevertheless, the drug provocation test is still necessary for diagnosis.Keywords
betalactamsdiagnosishypersensitivityanaphylaxisallergyskin testsRezumat
Reacţiile adverse medicamentoase reprezintă o cauză importantă de morbiditate şi mortalitate. Adevărata prevalență şi incidența reacţiilor adverse medicamentoase nu sunt cunoscute. Femeile au o predispoziţie crescută în dezvoltarea alergiilor la antibiotice. Reacţiile de hipersensibilitate la betalactamine sunt clasificate în imediate şi întârziate. Reacţiile imediate apar în prima oră de la administrarea medicamentului şi sunt IgE‑mediate. Cele întârziate apar după o oră de la administrare şi pot fi mediate de celulele T. Testele cutanate reprezintă principala investigaţie diagnostică, deşi la pacienţii cu istoric de reacţii severe se recomandă testele in vitro. Cu toate acestea, testul de provocare este încă necesar pentru diagnostic.Cuvinte Cheie
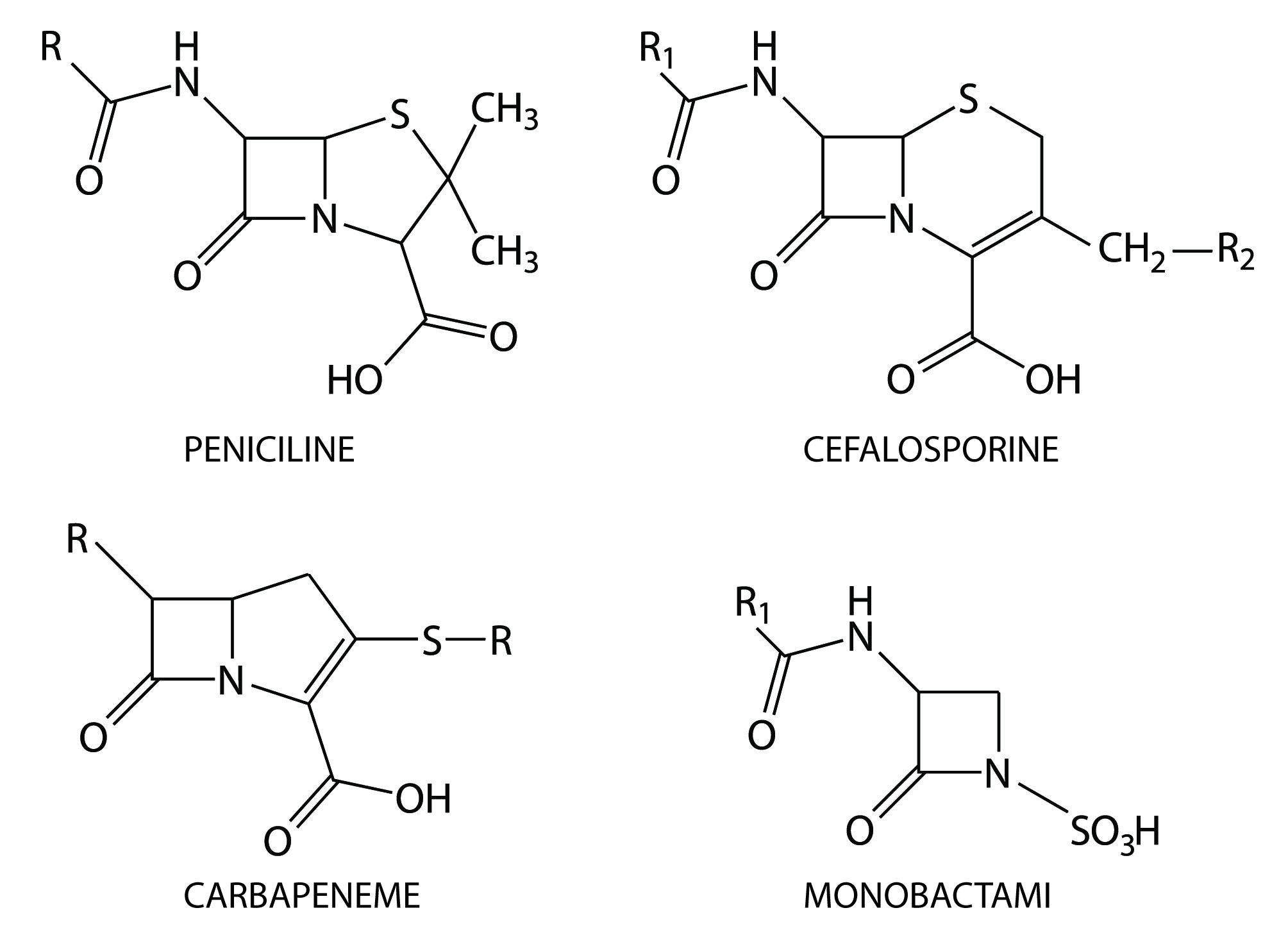
betalactaminediagnostichipersensibilitateanafilaxiealergieteste cutanateReacţiile alergice la betalactamine sunt cele mai frecvente cauze de reacţii adverse medicamentoase mediate prin mecanisme specifice imunologice, reprezentând o cauză importantă de mortalitate şi morbiditate, inclusiv în ţara noastră. Reacţiile pot apărea după administrarea oricărui antibiotic din această clasă disponibil pe piaţă, variind de la benzilpenicilină la alte betalactamine introduse recent în practica medicală, cum ar fi aztreonamul sau acidul clavulanic. Deşi procesul de producţie al betalactaminelor a fost îmbunătăţit în ultimii ani, numărul reacţiilor alergice nu a scăzut, probabil din cauza creşterii numărului de pacienţi cărora li se administrează această clasă de medicamente. Există o mare diversitate de structuri chimice care aparţin acestei clase de antibiotice, lucru care a generat mecanisme de recunoaştere ale acestora de către sistemul imunitar.
Patternul consumului de antibiotice s-a modificat semnificativ în timp. Un studiu recent cu privire la utilizarea generală a acestor medicamente în Europa a arătat că penicilina nu mai este cel mai frecvent folosit antibiotic, locul ei fiind luat treptat de alţi compuşi, ce variază de la ţară la ţară. Spre exemplu, amoxicilina este raportată ca fiind antibioticul cel mai frecvent folosit în Europa şi în Statele Unite ale Americii. Cefalosporinele reprezintă şi ele o cauză importantă a reacţiilor alergice.
Reacţiile alergice sau mediate imun, cum ar fi urticaria sau boala serului, au fost notate la începutul anilor ‘40, când penicilina a fost introdusă în tratamentele medicale. Prima raportare îi aparţine lui Lyons, care a constatat că 5,7% din soldaţii americani trataţi cu penicilină pentru infecţii chirurgicale prezentau urticarie. Primul articol privind reacţiile alergice la penicilină a fost publicat în 1946. Aceste reacţii alergice sau mediate imun se numesc astăzi reacţii de hipersensibilitate, conform clasificării lui Gell şi Coombs.
Răspunsurile imunologice la penicilină şi la alte antibiotice betalactamine pot fi clasificate pe larg în imediate şi întârziate, în funcţie de asocierea temporală dintre debutul simptomelor şi momentul administrării medicamentului. În timp ce răspunsurile imediate sunt IgE‑mediate şi apar în câteva minute până la o oră de la administrarea ultimei doze de medicament, reacţiile întârziate apar peste o oră de la administrarea ultimei doze, până la câteva zile. Reacţiile întârziate reprezintă un grup heterogen ca manifestări clinice şi mecanisme imunologice. O clasificare extinsă a reacţiilor întârziate induse medicamentos sau de hipersensibilitate de tip IV a fost propusă de Pichler. El a notat faptul că probabilitatea ca o reacţie să fie IgE‑mediată scade cu cât intervalul dintre debutul reacţiei şi momentul administrării medicamentului creşte. De reţinut însă că în anumite situaţii clinice este imposibil să se clasifice o reacţie alergică în funcţie doar de acest interval de timp.
Reacţiile alergice imediate şi non-imediate rămân o provocare pentru clinicieni, în mod particular atunci când testele cutanate sunt negative, în prezenţa unui istoric clinic sugestiv. În România, medicii specialişti alergologi se confruntă şi cu situaţia în care pacientul este testat de medici de alte specialităţi sau asistente medicale („testul la antibiotic din spital“), cu rezultat pozitiv (cel mai frecvent apărut prin mecanism iritativ atunci când nu se folosesc diluţiile corespunzătoare, standardizate), dar fără istoric sugestiv pentru reacţii alergice la medicamente şi fără teren atopic. În acest context, este simplu să înţelegem că testul nu prezintă sensibilitate şi specificitate semnificativă.
Date epidemiologice
Betalactaminele reprezintă una dintre cele mai frecvente cauze de reacţii adverse medicamentoase imediate sau întârziate. Prevalența hipersensibilităţii la penicilină în populaţia generală este necunoscută, neexistând studii prospective care să evalueze rata sensibilizărilor din timpul tratamentelor. Aproximativ 20% dintre pacienţii spitalizaţi afirmă reacţii alergice, dar numai 1-10% din aceşti pacienţi au demonstrată, in vivo sau in vitro, o reacţie de hipersensibilitate de tip I, se arată într-un studiu. Într-un studiu retrospectiv care a cuprins peste 1000 de copii şi adulţi care au primit lunar injecţii musculare cu penicilină G pe o perioadă de 3 ani, 3,2% au prezentat reacţii alergice, din care 0,2% anafilaxie. S-au raportat şi cazuri de reacţii alergice de contact sau prin expunere aeriană la particule aeropurtate, la personalul medical din laboratoare. De notat că amoxicilina şi ampicilina sunt asociate frecvent cu rash maculopapular, în special atunci când se administrează în infecţii virale. Se pare că femeile au o predispoziţie mai mare decât bărbaţii în dezvoltarea alergiilor la medicamente.
Anafilaxia
Se estimează că penicilina poate provoca reacţii anafilactice și este cauza a 0,7-10% dinre toate cazurile de anafilaxie. Cu fiecare tratament cu penicilină, rata anafilaxiei se estimează a fi între 0,015% şi 0,004%. Anafilaxia apare cel mai frecvent la adulţi între 20 şi 49 de ani, incidența fiind mult mai redusă în alte grupe de vârstă. Incidența anafilaxiei la cefalosporine nu este cunoscută, dar este categoric mai mică decât în cazul penicilinei, cu o rată de risc estimată între 0,0001% şi 0,1% pentru fiecare cură de tratament. În Europa, benzilpenicilina a fost gradual înlocuită cu aminopeniciline şi cefalosporine, din cauza schimbărilor în obiceiurile de prescriere.Riscul de deces prin şoc anafilactic în cazul penicilinei a fost estimat între 0,0015% şi 0,002% dintre pacienţii trataţi.
Factorii de risc pentru reacţiile de hipersensibilitate imediată la betalactamine nu sunt clarificați. Se consideră că cel mai important factor de risc este legat de structura chimică şi metabolismul medicamentului administrat. Betalactaminele acţionând ca haptene, devin în cursul metabolismului molecule imunogene.
Evaluare clinică
În evaluarea corectă a reacţiilor alergice la betalactamine, un rol important îl are istoricul detaliat, care poate fi obţinut de la pacient, martori sau părinţi, în cazul copiilor. Două puncte importante în anamneză sunt intervalul de timp între prima şi ultima administrare a medicamentului şi apariţia reacţiei şi tipul simptomelor, indiciu care ne ajută în clasificarea reacţiei alergice. Pacienţii cu reacţii alergice imediate dezvoltă simptome rapid după administrarea medicamentului, într-un interval de maximum o oră; după acest interval, probabilitatea ca reacţia să fie IgE‑mediată scade considerabil.Tabloul clinic tipic pentru reacţii imediate la betalactamine cuprinde urticaria, cu sau fără angioedem, şi anafilaxia. Urticaria este definită ca apariţia rapidă de papule pruriginoase pe diferite zone ale corpului. Anafilaxia este luată în considerare dacă apar câteva din următoarele simptome: pruritul palmelor sau al plantelor, care ulterior devine generalizat, eritem generalizat, urticarie, dispnee, dificultăţi de vorbire sau înghiţire, hipotensiune, tahicardie sau/şi pierderea conştienței. Urticaria poate reprezenta primul stadiu al anafilaxiei, care ulterior este urmată de manifestări respiratorii, gastrointestinale sau cardiovasculare.
Reactivitatea cutanată IgE‑mediată scade cu timpul, iar testele cutanate diagnostice pot deveni negative. Prin urmare, în interpretarea testelor cutanate negative trebuie luat în considerare timpul scurs de la apariţia reacţiei clinice până la evaluarea alergologică. Alte detalii de notat sunt: vârsta, sexul, istoricul personal de atopie, hipersensibilitate documentată la alte medicamente, istoric familial de alergii medicamentoase, medicaţia actuală a pacientului, bolile pentru care pacientul primeşte tratament, ultima dată la care pacientul a tolerat orice tip de antibiotic betalactaminic, câte zile şi ce doză s-a administrat la momentul reacţiei, ce medicamente s-au folosit pentru tratamentul reacţiei şi dacă pacientul a mai experimentat reacţii la betalactamine. Având în vedere importanţa anamnezei în diagnosticul alergiei la medicamente, foarte utile sunt chestionarele ENDA/EAACI în colectarea tuturor datelor anamnestice. Cu toate acestea, este dificilă obţinerea unui istoric clinic perfect. Cele două entităţi descrise, urticaria şi anafilaxia, se pot suprapune. Din păcate, de multe ori este dificil pentru pacient să-şi amintească detaliile solicitate, iar pentru medic să evalueze şi să clasifice perfect o reacţie alergică petrecută cu mult timp în urmă. Prin urmare, procedurile diagnostice trebuie să fie minuţioase şi stereotipe.
Testele cutanate
Deşi testele cutanate pentru diagnosticul reacţiilor alergice la betalactamine sunt foarte bine cunoscute, modul în care sunt efectuate diferă de la o ţară la alta, de la spital la spital şi chiar între doctorii din acelaşi spital. De când consumul de betalactamine diferă între ţări şi chiar între zonele aceleiaşi ţări, haptenele folosite pentru testele cutanate tind să sufere modificări. Iată necesitatea consultării ghidurilor ENDA/EAACI de către cadrele medicale care efectuează testări cutanate la antibiotice ca alternativă la consultul alergologic. Pe scurt, se folosesc trei metode clasice pentru testarea cutanată: prick, intradermică şi patch. Metoda prick se efectuează prin înţeparea pielii cu o lancetă specială prin soluţia de alergen. Dacă testul cu antibiotic are aceeaşi dimensiune cu a martorului negativ, urmează testul intradermic. Şi testul intradermic se efectuează alături de martor negativ, prin injectarea a 0,02-0,05 ml din soluţia cu haptenă pe partea volară a antebraţului. Rolul testării patch în diagnosticul reacţiilor imediate la betalactamine este minor şi nu este bine definit.Haptenele sunt definite ca structuri chimice care devin alergene numai după conjugarea cu molecule transportoare, in vivo sau in vitro. Spre exemplu, penicilinele şi derivaţii lor, aşa-numita mixtură de determinanţi minori (MDM), sunt haptene, în timp ce benzilpeniciloil poli-L-lizina (PPL) este conjugatul non-imunogenic al benzilpenicilinei cu poli-L-lizina. Deşi numărul determinanţilor minori ai penicilinei era mai mare, instabilitatea unora a restricţionat compoziţia MDM comercial la benzilpenicilină şi acid benzilpeniciloic. Apariţia reacţiilor specifice la catena laterală a necesitat folosirea şi a altor determinanţi, cum ar fi ai amoxicilinei şi ai cefalosporinelor. Există haptene comerciale pentru testări alergologice, cum ar fi MDM, PPL şi diferite cefalosporine, dar din păcate nu şi în România.
De notat concentraţiile maxime acceptate pentru testele alergologice prick şi intradermice la betalactamine: PPL 0,00005 mmol/L; MDM 0,02 mmol/L. În cazul pacienţilor cu istoric de reacţii severe sau cu riscuri crescute de reacţii la testarea alergologică, testele prick şi intradermice vor începe cu alergenul diluat de mii de ori, apoi concentraţia este crescută gradual până la apariţia răspunsului cutanat pozitiv sau până la atingerea concentraţiei maxime admise.
Citirea testării se face după 15-20 de minute, testul se raportează la martorul negativ, iar în cazul testului intradermic este necesară şi o citire tardivă, cu informarea pacientului asupra posibilităţii apariţiei unei reacţii în intervalul 24-48 de ore post-testare. Anumite medicamente trebuie întrerupte înainte de testare: antihistaminicele cu o săptămână înainte, betablocantele cu 48 de ore, pacientul nu trebuie să prezinte infecţii sau febră la momentul testării. După cum este bine cunoscut, aceste standarde nu sunt respectate atunci când se efectuează „testele alergologice“ pentru antibiotice în spitalele din România, ceea ce le invalidează rezultatele. Evident, testul de provocare rămâne standardul de aur în diagnosticul reacţiilor de hipersensibilitate la betalactamine.
Şi în cazul testării cutanate, ca şi în cursul testului de provocare, ne aşteptăm la provocarea reacţiilor de hipersensibilitate, motiv pentru care se recomandă efectuarea testărilor la medicamente în spital, cu consimţământul scris al pacientului şi cu trusa de urgenţă accesibilă. Aceste măsuri sunt necesare în mod deosebit atunci când reacţia originală a fost severă.
Simptomele clasice în timpul testării sunt prurit, urticarie cu/fără angioedem, eritem, răguşeală şi ameţeli care apar rapid după testele cutanate. Uneori, simptomatologia progresează către tahicardie, dureri abdominale, dispnee şi hipotensiune. De aceea, monitorizarea atentă a pacientului s-a dovedit utilă în controlul simptomelor. Un studiu efectuat între anii 1985 și 1995 a arătat că, după testarea intradermică cu doza maximă de penicilină, 11% dintre pacienţi, majoritatea cu test cutanat pozitiv, au dezvoltat reacţii sistemice la amoxicilină (50%), PPL (29%), MDM (15%) şi ampicilină (6%)(19).
Sensibilitatea şi specificitatea testelor cutanate la betalactamine nu sunt 100%, iar testul de provocare cu medicament nu poate fi utilizat întotdeauna ca un gold standard pentru clasificarea reacţiilor alergice. În plus, există situaţii în care pacientul prezintă istoric pozitiv, teste cutanate pozitive, dar test de provocare fals negativ. Din motive de siguranţă, se recomandă evitarea testului de provocare atunci când testele cutanate sunt pozitive. Astfel, valoarea predictivă pozitivă a testelor cutanate nu a fost determinată.
Rata de detecţie a testelor cutanate variază în diferite populaţii, alergia la penicilină fiind diagnosticată în aproximativ 69% din cazuri conform unor studii europene şi în 50% din cazuri conform unui recent studiu american. Se poate deduce astfel că testul de provocare medicamentoasă este necesar pentru a confirma sau exclude alergia. În studiile europene, diagnosticul alergiei medicamentoase este confirmat în o treime din cazuri, iar în studiile americane, în jumătate din cazuri. Sunt publicate protocoale pentru testul de provocare(30), dar paşii trebuie individualizaţi în funcţie de severitatea şi timingul reacţiei originale.
Teste in vitro
Există multe metode de laborator care ar putea fi de ajutor în diagnosticul alergiei la betalactamine, dar nu toate au fost evaluate şi standardizate. Cel mai bine studiate sunt cuantificarea IgE specifice in vitro, analiza serologică, ce nu presupune riscuri pentru pacient, de mare ajutor în cazul pacienţilor cu boli cutanate, de multe ori pozitive în cazul pacienţilor cu teste cutanate negative şi mai puţin costisitoare faţă de testele de provocare. Din păcate, sunt mai puţin sensibile faţă de testele cutanate. Activarea bazofilelor în sângele pacienţilor care au prezentat o reacţie alergică la betalactamine poate fi măsurată prin flow cytometrie, vizând markerii specifici ai bazofilelor CD63 sau CD203c. În ciuda specificităţii testului care atinge 93,3%, sensibilitatea BAT este doar 50%, deşi poate fi mai mare pentru cefalosporine(32,33). Aceste teste serologice sunt considerate complementare, iar în unele cazuri, de exemplu pacienţii cu reacţii alergice severe, testele in vitro ar trebui să reprezinte prima opţiune în evaluarea pacientului.Mediatorii inflamatori eliberaţi de mastocite şi bazofile în cursul reacţiei alergice pot fi detectaţi în sânge sau urină. Aceste determinări pot avea valoare diagnostică atunci când pacientul este evaluat în faza acută a reacţiei. Doi mediatori au fost extensiv studiaţi: histamina şi triptaza. Histamina este eliberată şi din mastocite, şi din bazofile, însă poate fi detectată în sânge doar câteva minute după reacţia alergică, fiind metabolizată rapid în N-metilhistamină, ce poate fi detectată în urină. De notat că niveluri crescute de N-metilhistamină pot fi detectate în urina subiecţilor nealergici în diverse situaţii; astfel, nu reprezintă o unealtă de diagnostic utilă în cazul alergiilor medicamentoase. Determinarea triptazei, eliberată exclusiv de celula mastocitară, este de ajutor în diagnosticul reacţiilor imediate la medicamente(31).
Reacţiile mediate de celulele T
Cele mai frecvente reacţii cutanate asociate administrării betalactaminelor sunt erupţiile maculopapulare şi exantemele morbiliforme(34). În acest tip de reacţie s-a demonstrat prezența celulelor T CD4+ la nivelul dermului perivascular şi niveluri similare de celule T CD4+ şi CD8+ la nivelul stratului dermoepitelial şi în epiderm(35). Aceste celule sunt activate şi exprimă niveluri crescute de homing-receptori, antigene limfocitare cutanate şi produc markeri citotoxici, cum ar fi perforine şi granzime(36,37). Patternul citokinelor şi chemokinelor este în principal Th1 (IFN-c şi TNF-a), deşi unii autori au indicat că IL-5 poate fi implicată în exantemul morbiliform(38). În alte entităţi clinice importante, cum ar fi pustuloza exantematoasă generalizată, sunt implicate celulele T şi neutrofilele(39). Patogenia sindromului Stevens-Johnson şi a necrolizei toxice epidermice a fost legată de apoptoza keratinocitelor epidermice, produsă de celulele T prin două căi: Fas/Fas ligand şi perforine-granzime. Patofiziologia reacţiilor la medicamente, rash cu eozinofilie şi simptome sistemice (sindromul DRESS), include eotaxina şi producţia de IL-5, care sunt importante în recrutarea eozinofilelor.Identificarea clinică a reacţiilor non-imediate la betalactamine este deseori dificilă, din cauza heterogenității manifestărilor clinice, care de multe ori se confundă cu ale bolilor infecţioase şi autoimune. Incidența reacţiilor alergice la betalactamine este mai scăzută în cazul copiilor, probabil prin pierderea mai rapidă a sensibilizării sau prin dozele cumulative de expunere mai mici.
Alergia la betalactamine a copiilor
Adevăratele reacţii alergice la betalactamine sunt mai puţin frecvente la copii faţă de adulţi(40). Copiii trataţi cu betalactamine dezvoltă frecvent rash cutanat, care este de obicei cu aspect urticarian. De cele mai multe ori, erupţia este considerată alergie medicamentoasă, dar în majoritatea cazurilor este datorată infecţiei virale (frecvent enterovirusuri), fiind foarte rar reprodusă la testele de provocare. Alergia la betalactamine este frecvent supradiagnosticată, acest lucru putând conduce la creşterea costurilor pentru sănătate şi rezistenţa la antibiotice (cu riscuri crescute pentru copii). Din păcate, nu există teste diagnostice in vitro care să facă distincţia între exantemul viral şi cel indus medicamentos.Cel mai frecvent raportată cauză de reacţii alergice la copii este amoxicilina. Majoritatea reacţiilor sunt reacţii cutanate non-imediate, ce apar la peste o oră de la administrarea unei doze, de severitate uşoară spre moderată, la copiii sub 4 ani(41,42). Nu există factori predispozanţi pentru alergia la betalactamine în cazul copiilor şi doar între 7% și 16% dintre copiii cu suspiciune de alergie la betalactamine se dovedesc a fi alergici la investigaţiile ulterioare.
Ca şi în cazul adulţilor, istoricul pacientului este esenţial pentru confirmarea diagnosticului. Simptomele clinice frecvente sunt rash-ul maculopapular (55%) şi urticaria (35%). Eritemul fix medicamentos este rar, iar sindromul Steven-Johnson este de obicei cauzat de infecţii virale. Eritemul multiform şi reacţiile boala serului-like nu sunt IgE mediate sau mediate celular, dar adesea apar din cauza unei infecţii virale.
Testele diagnostice sunt similare celor recomandate la adulţi, cu menţiunea că testele intradermice sunt mai dificil de efectuat la copiii mici. Testele cutanate nu sunt utile la copiii cu reacţii de hipersensibilitate non-IgE mediate şi non-T-cell mediate, cum ar fi eritemul multiform sau boala serului-like. IgE specifice cu reacţii imediate, în cazul copiilor, necesită investigaţii suplimentare. Testul de provocare orală este standardul de aur pentru diagnosticul alergiei la betalactamine şi o unealtă diagnostică utilă pentru erupţiile cutanate la copii. Prezintă riscuri scăzute în cazul copiilor fără istoric de anafilaxie şi trebuie luat în considerare la toţi copiii care dezvoltă erupţii cutanate în cursul tratamentelor.
Reacţiile alergice la betalactamine reprezintă o cauză importantă de reacţii imunologice la medicamente. Luând în considerare faptul că schimbările numărului de medicamente disponibile şi patternul consumului acestora au modificat sensibilitatea testelor diagnostice, este necesară adaptarea periodică a lumii medicale la aceste schimbări.
Bibliografie
- Fernandez-Rivas M., Perez Carral C., Cuevas M., Marti C., Moral A., Senent C.J. Selective allergic reactions to clavulanic acid. J Allergy Clin Immunol 1995; 95:748-750.
- Candarso A.I., Saez-Jiménez S.A., Vidal C., Rodríguez M. Aztreonam induced anaphylaxis. Lancet 1990; ii:746-747.
- Torres M.J., Romano A., Mayorga C., Moya M.C., Guzman A.E., Reche M., et al. Diagnostic evaluation of a large group of patients with immediate allergy to penicillins: the role of skin testing. Allergy 2001; 56:850-856.
- Torres M.J., Mayorga C., Leyva L., Guzman A., Cornejo-García J.A., Juarez C., Blanca M. Controlled administration of penicillin to patients with a positive history but negative skin and specific serum IgE tests. Clin Exp Allergy 2002; 32:270-276.
- Kaplan A.P. Urticaria and angioedema. In: Middleton Jr eds. Allergy principles and practice. 5th edn. Mosby, 1998: 1104-1122.
- Lieberman P. Anaphylaxis and anaphylactoid reactions. In: Middleton Jr Eds. Allergy principles and practice. 5th edn. Mosby, 1998: 1079-1092.
- Demoly P., Kropf R., Bircher A., Pichler W.J. Drug hypersensitivity questionnaire. Allergy 1999; 54:999-1003.
- Torres M.J., Mayorga C., Pamies R., Rodriquez J.L., Juarez C., Romano A., Blanca M. Immunological response to different determinants of benzylpenicillin, amoxicillin and ampicillin. Comparison between urticaria and anaphylactic shock. Allergy 1999; 54:936-943.
- Blanca M. Allergic reactions to penicillins. A changing world? Allergy 1995; 50:777-782.
- Cars O., Molstad S., Melander A. Variation in antibiotic use in the European Union. Lancet 2001; 357:1851-1853.
- Romano A., Quarantino D., Aimone-Gastin I., Mayorga C., Papa G., Venuti A et al. Cephalosporin allergy: characterization of unique and cross-reacting cephalosporin antigens. Int J Immunopathol Pharmacol 1997; 10:187-191.
- Lerch M., Pichler W.J. The immunological and clinical spectrum of delayed drug-induced exanthems. Curr Opin Allergy Clin Immunol 2004; 4:411-9.
- Richter A.G., Nasser S.M., Krishna M.T.A UK naţional survey of investigations for beta-lactam hypersensitivity - heterogeneity în practice and a need for naţional guidelines - on behalf of British Society for Allergy and Clinical Immunology (BSACI). Clin Exp Allergy 2013; 43:941-9.
- Gomez M.B., Torres M.J., Mayorga C. et al. Immediate allergic reactions to betalactams: facts and controversies. Curr Opin Allergy Clin Immunol 2004; 4:261-6.
- Kerr J.R. Penicillin allergy: a study of incidence as reported by patients. Br J Clin Pract 1994; 48:5-7.
- Shapiro S., Siskind V., Slone D., Lewis G.P., Jick H. Drug rash with ampicillin and other penicillins. Lancet 1969; 2:969-72.
- Idsoe O., Guthe T., Willcox R.R., De Weck AL. Nature and extent of penicillin side-reactions, with particular reference to fatalities from anaphylactic shock. Bull World Health Organ Geneva, Switzerland 1968; 38:159-88.
- Park M.A., Li J.T. Diagnosis and management of penicillin allergy. Mayo Clin Proc 2005; 80:405-10.
- Torres M.J., Romano A., Mayorga C., Moya M.C., Guzman A.E., Reche M., et al. Diagnostic evaluation of a large group of patients with immediate allergy to penicillins: the role of skin testing. Allergy 2001; 56:850-856.
- Lieberman P. Anaphylaxis and anaphylactoid reactions. In: Middleton Jr Eds. Allergy principles and practice. 5th edn. Mosby, 1998: 1079-1092.
- Parker C.W., de Weck A.L., Shapiro J., Kern M., Eisen H.N. The preparation and some properties of penicillenic acid derivatives relevant to penicillin hypersensitivity. J Exp Med 1962; 115:803-819.
- Levine B.B., Redmond A.P. Minor haptenic determinant specific reagins of penicillin hypersensitivity în man. Int Arch Allergy Appl Immunol 1969; 35:445-455.
- Sullivan T.J., Wedner J., Shatz G.S., Yecies L.D., Parker C.W. Skin testing to detect penicillin allergy. J Allergy Clin Immunol 1981; 68:171-180.
- Bircher A.J., Haldimann D., Weber J. CAST-ELISA testing for the diagnosis of immediate-type allergic reactions to betalactam antibiotics. Allergy Clin Immunol Int 1996; 8:109-110.
- Lebel B., Messaad D., Kvedariene V., Rongier M., Bousquet J., Demoly P. Cystenyl-leukotriene release test (CAST) in the diagnosis of immediate drug reactions. Allergy 2001; 56:688-692.
- Sanz M.L., Gamboa P.M., Antepara I., Uasuf C., Vila L., Garcia-Aviles C., et al. Flow cytometric basophil activation test by detection of CD63 expression in patients with immediate-type reactions to beta-lactam antibiotics. Clin Exp Allergy 2002; 32:277-286.
- Sabbah A., Lauret M.G., Maillard H. Preliminary study of basophil activation test for drug allergy using anti-membrane antibodies and flow cytometry. Allergie Immunol 1995; 27:276-277.
- Blanca M., Mayorga C., Torres M.J., Reche M., Moya M.C., Rodriguez J.L., et al. Clinical evaluation of Pharmacia CAP SystemTM RAST FEIA amoxicilloyl and benzylpenicilloyl in patients with penicillin allergy. Allergy 2001; 56:862-870.
- Macy E., Ngor E.W. Safely diagnosing clinically significant penicillin allergy using only penicilloyl-poly-lysine, penicillin, and oral amoxicillin. J Allergy Clin Immunol Pract 2013; 1:258-63.
- Messaad D., Sahla H., Benahmed S., Godard P., Bousquet J., Demoly P. Drug provocation tests in patients with a history suggesting an immediate drug hypersensitivity reaction. Ann Intern Med 2004; 140:1001-6.
- Fox S., Park M.A. Penicillin skin testing in the evaluation and management of penicillin allergy. Ann Allergy Asthma Immunol 2011; 106:1-7.
- Sanz M.L., Gamboa P.M., Antepara I. et al. Flow cytometric basophil activation test by detection of CD63 expression in patients with immediate-type reactions to betalactam antibiotics. Clin Exp Allergy 2002; 32:277-86.
- Torres M.J., Padial A., Mayorga C. et al. The diagnostic interpretation of basophil activation test în immediate allergic reactions to betalactams. Clin Exp Allergy 2004; 34:1768-75.
- Cohen A.D., Friger M., Sarov B., Halevy S. Which intercurrent infections are associated with maculopapular cutaneous drug reactions? A case-control study. Int J Dermatol 2001; 40:41-44.
- Yawalker N., Karlen S., Eqli F., Brand C.U., Qabee H.U., Dichlee W.J. et al. Infiltration of cytotoxic T cells in drug‑induced cutaneous eruptions. Clin Exp Allergy 2000; 30:847-855.
- Blanca M., Posadas S., Torres M.J., Leyva L., Mayorga C., Gonzalez L. et al. Expression of the skin-homing receptor in peripheral blood lymphocytes from subjects with non-immediate cutaneous allergic drug reactions. Allergy 2000; 55:998-1004.
- Posadas S.J., Padial A., Torres M.J., Mayorga C., Leyva L., Sanchez E. et al. Delayed reactions to drugs show levels of perforin, granzyme B, and Fas-L to be related to disease severity. J Allergy Clin Immunol 2002; 109:155-161.
- Fernandez T.D., Mayorga C., Torres M.J., Cornejo-Garcia J.A., López S., Chaves P. et al. Cytokine and chemokine expression in the skin from patients with maculopapular exanthema to drugs. Allergy 2008; 63:712-719.
- Padial M.A., Alvarez-Ferreira J., Tapia B., Blanco R., Mañas C., Blanca M. et al. Acute generalized exanthematous pustulosis associated with pseudoephedrine. Br J Dermatol 2004; 150:139-142.
- Ponvert C., Weilenmann C., Wassenberg J. et al. Allergy to betalactam antibiotics in children: a prospective followup study in retreated children after negative responses in skin and challenge tests. Allergy 2007; 62:42-6.
- Rebelo G.E., Fonseca J., Araujo L., Demoly P. Drug allergy claims in children: from self-reporting to confirmed diagnosis. Clin Exp Allergy 2008; 38:191-8.
- Lange L., Koningsbruggen S.V., Rietschel E. Questionnaire-based survey of lifetime-prevalence and character of allergic drug reactions in German children. Pediatr Allergy Immunol 2008; 19:634-8.
Articole din ediția curentă
SUPLIMENT TRATAMENTUL ÎN ALERGII
Tratamentul bolilor alergice în timpul sarcinii
Andreea Ioana Popescu
Bolile alergice, incluzând rinita/rinoconjunctivita alergică, astmul și urticaria, sunt afecţiuni frecvente care apar la adulţii tineri, prin urmare afectând femeile aflate la vârsta fertilă. Deşi, în mod ideal, gravidele nu ar trebui să primească tratament farmacologic, din cauza riscurilor pentru făt, uneor...
SUPLIMENT TRATAMENTUL ÎN ALERGII
Managementul farmacoterapeutic al afecţiunilor alergice și al altor reacţii de hipersensibilitate
Cristian Daniel Marineci
Reacțiile de hipersensibilitate sunt răspunsuri imune exagerate la antigeni străini. Simptomele reacțiilor alergice sunt combătute cu ajutorul antihistaminicelor H1, al stabilizatoarelor membranei mas...Articole din edițiile anterioare
SUPLIMENT TRATAMENTUL ÎN ALERGII
Tratamentul bolilor alergice în timpul sarcinii
Andreea Ioana Popescu
Bolile alergice, incluzând rinita/rinoconjunctivita alergică, astmul și urticaria, sunt afecţiuni frecvente care apar la adulţii tineri, prin urmare afectând femeile aflate la vârsta fertilă. Deşi, în mod ideal, gravidele nu ar trebui să primească tratament farmacologic, din cauza riscurilor pentru făt, uneor...
SUPLIMENT TRATAMENTUL ÎN ALERGII
Managementul farmacoterapeutic al afecţiunilor alergice și al altor reacţii de hipersensibilitate
Cristian Daniel Marineci
Reacțiile de hipersensibilitate sunt răspunsuri imune exagerate la antigeni străini. Simptomele reacțiilor alergice sunt combătute cu ajutorul antihistaminicelor H1, al stabilizatoarelor membranei mas...
RUBRICA SPECIALISTULUI