Din secretele longevităţii… nutraceuticele – partea a III-a Afecţiunile tiroidei
From the secrets of longevity... nutraceutics. Thyroid disorders – part III
Abstract
At the thyroid level, the fluctuations in hormone secretion primarily affect the patient’s metabolism. Therefore, thyroid disorders cause diseases of the cardiovascular system (hypertension, atherosclerosis) and increase the risk of cardiovascular accident. Bipolar mental disorders are also associated with endocrine diseases. Currently, there are no ways to stop the autoimmune process in chronic thyroiditis, but given the state of research, selenium therapy remains the only therapeutic alternative. Current national and international studies focus on assessing the status of selenium in patients with autoimmune thyroiditis and the role of selenium supplementation in the disease evolution.Keywords
thyroid disordersautoimmune diseasesseleniumRezumat
La nivel de tiroidă, fluctuaţiile secreţiei hormonale afectează în primul rând metabolismul pacientului. De aceea, afecţiunile tiroidiene cauzează boli ale sistemului cardiovascular (hiprtensiune arterială, ateroscleroză) şi duc la mărirea riscului de accident cardiovascular. Şi tulburările psihice bipolare sunt asociate cu bolile endocrine. În prezent nu există metode de a opri procesul autoimun în tiroidita cronică, dar având în vedere stadiul cercetărilor, tratamentul cu seleniu rămâne singura alternativă terapeutică. Studiile actuale, naţionale şi internaţionale, se axează pe evaluarea statusului seleniului la pacienţii cu tiroidită autoimună şi a rolului suplimentării cu seleniu asupra evoluţiei bolii.Cuvinte Cheie
afecţiuni tiroidieneboli autoimuneseleniuOboseala continuă, irascibilitatea şi episoadele de depresie nu sunt normale. Acestea sunt semne că pacientul trebuie să-şi examineze nivelul de TSH (hormonul de stimulare tiroidiană) din sânge. De cele mai multe ori, pacienţii cred că problemele cu care se confruntă sunt cauzate de stilul de viaţă dezordonat, însă specialiştii ar trebui să le recomande investigaţii endocrinologice pentru depistarea precoce a bolilor tiroidei şi pentru evitarea apariţiei complicaţiilor.
Bolile tiroidiene pot fi ţinute sub control, dar este foarte important ca acestea să fie depistate în stadiu incipient. De aceea, atât femeile, cât şi bărbaţii de peste 35 de ani trebuie să-şi testeze anual nivelul de TSH din sânge.
Asociaţia Pacienţilor cu Afecţiuni Autoimune (APAA) cere implementarea unui program naţional de screening pentru afecţiunile tiroidiene, care ar putea să ajute la conştientizarea faptului că simptome precum modificarea greutăţii, stările de anxietate sau depresia, insomnia, oboseala cronică (starea de oboseală care durează mai mult de 6 luni), însoţită de dureri ale muşchilor, migrene şi de probleme ale digestiei, iar la femei ciclul menstrual neregulat şi scăderea libidoului ar putea fi eliminate cu ajutorul unui tratament corect.
În anul 2010 s-au înregistrat 5 925 de cazuri noi de boli tiroidiene. În 2016, au fost depistate 12 577 de cazuri noi de hipotiroidie şi 9 575 de hipertiroidie, potrivit datelor Institutului Naţional de Sănătate Publică. 87,8% dintre pacienţii cu hipotiroidie sunt femei, iar în anul 2016, numărul de cazuri noi de hipotiroidie depistate în mediul urban a fost de două ori mai mare decât în zonele rurale(1) (figura 1).

Tiroida este o glandă în formă de fluture care nu cântăreşte mai mult de 30 de grame. Dimensiunea redusă este însă indirect proporţională cu importanţa sa pentru sănătate: influenţează modul în care funcţionează fiecare celulă, ţesut sau organ, de la muşchi, oase şi piele la tractul digestiv, creier, inimă şi multe altele.
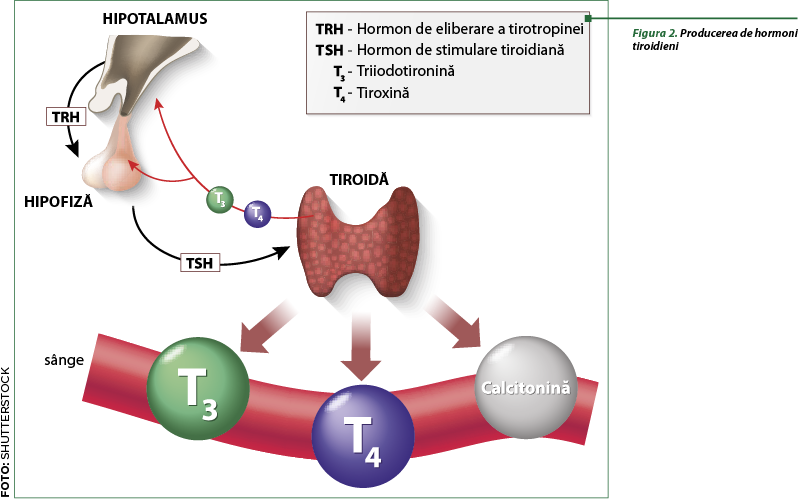
Glanda tiroidă îndeplineşte aceste roluri în primul rând prin secreţia hormonilor care controlează rapiditatea şi eficienţa cu care celulele transformă substanţele nutritive în energie (activitate chimică cunoscută sub numele de metabolism), astfel încât celulele să funcţioneze normal. Tiroida are nevoie de „combustibil” pentru a produce hormonii tiroidieni. Acest combustibil este iodul, care se găseşte în anumite alimente. Când acestea sunt consumate, iodul trece în sânge, pe urmă tiroida extrage din sânge acest ingredient necesar şi îl foloseşte pentru a produce două tipuri de hormoni tiroidieni: tiroxina (denumită T4, deoarece conţine 4 atomi de iod) şi triiodotironina (denumită T3, deoarece conţine 3 atomi de iod). Produsul glandei tiroide este, în principal, T4. Cea mai mare parte din hormonul T3 de care organismul are nevoie se obţine în afara glandei tiroide, în organe şi ţesuturi care utilizează T3 (ficatul, rinichii, creierul). Acestea transformă T4 (produs în glanda tiroidă) în T3, îndepărtând un atom de iod (figura 2).
Pe măsură ce glanda tiroidă produce hormonii tiroidieni, îi depozitează într-un număr mare de foliculi microscopici, cu aspect sferic. Când organismul are nevoie de hormoni tiroidieni, glanda tiroidă îi secretă în fluxul sangvin în cantităţi adecvate îndeplinirii nevoilor metabolice ale celulelor. Hormonii ajung uşor în interiorul celulelor care au nevoie de ei şi se ataşează de receptorii specifici, situaţi în nucleul acestora.
Funcţionarea glandei tiroide se află sub controlul glandei pituitare (hipofiza), care este situată la baza creierului. Hipofiza nu depăşeşte dimensiunea unui bob de mazăre, dar controlează funcţiile tiroidei şi ale altor glande aparţinând sistemului endocrin. Mesajele de la glanda pituitară către glanda tiroidă vin sub forma hormonului de stimulare tiroidiană (TSH, tirotropina). Un nivel ridicat de TSH determină tiroida să producă mai mulţi hormoni, după care cantitatea de TSH scade, ajungând la un nivel constant; un nivel scăzut de TSH avertizează tiroida să încetinească producţia. La adult, nivelul normal de TSH din sânge este între 0,45 şi 4,12 mlU/L.
Glanda pituitară poate răspunde direct hormonilor T4 care circulă în sânge, dar şi hipotalamusului, o regiune a creierului care produce propriul hormon – TRH (thyrotropin releasing hormone – hormon care eliberează tirotropina); iar TRH‑ul stimulează producţia de TSH în glanda pituitară. Această reţea de comunicare dintre hipotalamus, glanda pituitară şi glanda tiroidă este denumită axa hipotalamică-pituitară-tiroidiană (HPT) – figura 2.
Reţeaua de comunicare HPT este una foarte eficientă: în mod normal, glanda tiroidă eliberează cantitatea potrivită de hormoni tiroidieni pentru ca organismul să funcţioneze optim. Nivelurile de TSH se păstrează în general constante, dar răspund la cele mai mici schimbări ale nivelurilor de T4 şi viceversa.
Reţeaua HPT poate fi afectată în diverse moduri. De exemplu, factori externi precum bolile sau anumite medicamente pot să întrerupă „comunicarea”, după cum urmează:
glanda tiroidă nu produce suficienţi hormoni, încetinind astfel toate funcţiile organismului – afecţiunea este cunoscută ca hipotiroidism sau tiroidă hipoactivă;
glanda tiroidă produce prea mulţi hormoni, suprasolicitând organele – afecţiunea este cunoscută ca hipertiroidism sau tiroidă hiperactivă.
Când abordează boala tiroidiană, medicii încep prin a pune două întrebări: dacă glanda tiroidă produce o cantitate anormală de hormoni tiroidieni şi dacă există o modificare de structură a glandei tiroide (un nodul sau apariţia guşii). Deşi unul dintre aceste aspecte nu îl implică în mod obligatoriu pe celălalt, majoritatea afecţiunilor tiroidiene le includ pe ambele.
Majoritatea celor diagnosticaţi cu afecţiuni tiroidiene au în comun câteva caracteristici care îi plasează într-o categorie cu risc peste medie, şi anume: sexul feminin, un istoric familial de tiroidă hiperactivă sau hipoactivă, vârsta de peste 60 de ani, existenţa unei boli autoimune în istoricul familial, dacă femeia este însărcinată sau a născut în ultimele şase luni, dacă persoana este identificată cu un deficit de iod sau a fost expusă la cantităţi mari de radiaţii.
Numeroase studii arată că atât hipo-, cât şi hipertiroidismul au o incidenţă mai mare în cazul femeilor. Asociaţia Americană a Endocrinologilor Clinicieni (AACE) raportează că femeile sunt de 5 până la 8 ori mai expuse riscului de a suferi de o boală tiroidiană. Există dovezi care arată că hormonul estrogen afectează sistemul imunitar, în special globulele albe (limfocitele); limfocitele B, responsabile cu producţia de anticorpi, pot fi implicate în apariţia bolilor autoimune, inclusiv a afecţiunile tiroidiene.
Cercetările arată legătura dintre estrogen şi boala Basedow‑Graves (guşa exoftalmică); aceasta este rară înainte de pubertate, când nivelul estrogenului este scăzut. Se crede că influenţa estrogenului asupra sistemului imunitar are rol în instalarea altor boli autoimune (tiroidita Hashimoto – cauzată de un răspuns autoimun greşit care duce la un deficit de vitamina B12, ingredient esenţial în producerea de globule roşii).
Specialiştii susţin că fluctuaţiile nivelului de estrogen ar contribui la apariţia bolilor tiroidiene după menopauză, când nivelul hormonilor scade. Hipotiroidismul este frecvent în rândul persoanelor de peste 60 de ani, iar riscul creşte constant odată cu înaintarea în vârstă, în special în cazul femeilor, după cum s-a menţionat deja. Aceste scăderi ale nivelurilor hormonale coincid cu o creştere a anticorpilor care provoacă tiroidita Hashimoto.
Afecţiunile tiroidiene autoimune sunt transmise genetic. Până la 50% dintre rudele de gradul I ale pacienţilor cu aceste boli prezintă un risc de tiroidită autoimună. Existenţa unei afecţiuni tiroidiene autoimune induce riscul de a dezvolta şi altă boala autoimună: diabet de tip I, boala Addison, anemie pernicioasă (formă gravă de anemie care adesea afectează persoanele în vârstă care suferă de boala Graves sau de tiroidita Hashimoto), artrita reumatoidă, încărunţirea prematură (înainte de vârsta de 30 de ani) sau pierderea părului în smocuri (alopecia areată), vitiligo (leucoderma), care apare adesea în familiile cu un istoric de afecţiuni tiroidiene.
Iodul este singurul care contribuie semnificativ la declanşarea afecţiunilor tiroidiene (prea mult sau prea puţin iod). Unul dintre primele semne ale deficienţei de iod este apariţia guşii. Pe măsură ce tiroida încearcă să producă mai mulţi hormoni tiroidieni, aceasta se măreşte treptat. Deficitul sever de iod la copii duce la retard mintal şi la diferite grade de anormalitate în creştere şi dezvoltare.
Unele alimente, numite goitrogene, interferează cu absorbţia de iod a glandei tiroide. Acestea sunt: cartofii dulci, boabele de fasole Lima şi legumele crucifere (varza, conopida sau broccoli), cu menţiunea că ar trebui consumate în cantităţi extrem de mari pentru a reprezenta un risc.
Pe de altă parte, o cantitate prea mare de iod poate genera probleme acelor persoane care fie prezintă un risc ridicat de a dezvolta afecţiuni tiroidiene, fie suferă deja de una. Glanda tiroidă sănătoasă poate controla cantitatea de iod pe care o utilizează; dacă există un exces de iod, glanda îşi ajustează ritmul de producere a hormonilor, astfel încât continuă să producă o cantitate normală de hormoni tiroidieni. Dacă tiroida este deja mult prea activă, o cantitate prea mare de iod va determina glanda să reducă producţia de hormoni tiroidieni; totuşi, glanda nu poate controla cantitatea de iod care pătrunde în glandă, colectează iodul suplimentar şi începe să producă din nou prea mulţi hormoni tiroidieni.
Pentru bolnavii cu hipotiroidism cauzat de tiroidita Hashimoto, se presupune că un aport crescut de iod prin alimentaţie nu va fi de ajutor, ci dimpotrivă, acesta poate avea efectul opus. În perioada de sarcină sunt necesare 250 mcg de iod pe zi, deci multivitaminele administrate în perioada sarcinii şi alăptării trebuie să conţină suficient iod (cel puţin 150 mcg de iod), restul fiind luat din alimente. Însă nu trebuie depăşită doza recomandată, deoarece aportul zilnic >500 mcg poate fi dăunător pentru dezvoltarea fătului(2,3).
În ultimii ani a fost semnalată creşterea permanentă a incidenţei tireopatiilor autoimune.
Tiroidita autoimună este cea mai frecventă patologie tiroidiană, reprezentând o problemă de interes major în practica medicală, mai ales prin frecvenţă şi prognostic evolutiv către hipotiroidie, cu tratament substitutiv tiroidian ulterior, cel mai adesea permanent. Acest lucru implică orientarea spre studierea factorilor etiopatogenici şi identificarea unor factori suplimentari care să ajute în managementul terapeutic.
În prezent nu există metode de a opri procesul autoimun în tiroidita cronică autoimună, dar pe baza studiilor actuale, terapia cu seleniu, cu scopul de a reduce agresivitatea şi de a preveni disfuncţia tiroidiană autoimună, rămâne singura alternativă terapeutică (a cărei eficienţă necesită susţinere prin cercetări suplimentare).
Astfel, îmbunătăţirea ecogenităţii tiroidiene a fost remarcată în unele studii de suplimentare cu seleniu în tiroidita cronică autoimună. Ipoteza de lucru s-a axat pe evaluarea statusului seleniului la pacienţii cu tiroidită autoimună şi pe rolul suplimentării seleniului asupra evoluţiei bolii. Prima parte a cercetării a fost alcătuită dintr-un studiu prospectiv, intervenţional, randomizat, placebo-controlat, deschis, asupra suplimentării cu seleniu (100 µg/zi) versus placebo (timp de 3 luni) la pacienţii cu tiroidită autoimună şi status eutiroidian. Ţinând cont că aportul de seleniu este variabil în funcţie de regiunea geografică (tipul de sol) şi de concentraţiile din alimente (de asemenea, dependente de conţinutul în seleniu al solului), forma şi distribuţia seleniului în alimente (seleniul din plante are o biodisponibilitate mai mare decât cel din sursă animală), rezultatele determinărilor seleniului în respectivul studiu au fost dificil de integrat. S-au comparat rezultatele din studiul autohton cu rezultatele obţinute de alte ţări europene; acestea au variat în funcţie de aportul alimentar şi de compoziţia diferită a solului(4,5).
În Danemarca, un studiu comparativ la pacienţi evaluaţi înainte (1997-1998) şi după (2004-2005) introducerea suplimentării cu iod a găsit o corelaţie semnificativă între valorile scăzute ale seleniului şi creşterea riscului de guşă multinodulară (nu şi a riscului de noduli solitari)(5,6,7).
Astfel, pentru un management adecvat al afecţiunilor tiroidiene, ar fi utile produsele nutraceutice pe bază de seleniu. Datorită unei înalte biodisponibilităţi, poate fi luată în considerare şi drojdia cu seleniu, utilizabilă în alimente, suplimente alimentare sau medicamente. Exemplificăm prin produsul SelenoPrecise®, care conţine cantităţi semnificative şi omogene de seleniu organic uşor digerabil, în care conţinutul de compuşi de seleniu este cuprins între 1000 şi 1600 ppm. Produsul are un conţinut constant de l-selenometionină de cel puţin 55% din conţinutul total de seleniu, iar compuşii de seleniu anorganic nu depăşesc 1% din seleniul total, astfel încât are o mare biodisponibilitate (88,7%), demonstrată ştiinţific(8).
Studiile amintite au demonstrat că, în cazul tiroiditei autoimune, cu cât titrul anticorpilor este mai mare în momentul începerii suplimentării cu seleniu, cu atât tratamentul se dovedeşte mai eficient, scăderea nivelului anticorpilor antitiroidieni fiind obiectivul terapeutic prioritar.
Ţinând cont că în prezent nu există metode de a opri procesul autoimun în tiroidita cronică, iar tratamentul cu levotiroxină se adresează doar consecinţelor agresiunii autoimune, tratamentul cu seleniu se dovedeşte util la pacienţii cu deficit de seleniu confirmat. Impactul studiilor a fost semnificativ pentru sănătatea pacienţilor şi, probabil, pentru prognosticul evolutiv, aspect confirmat de parametrii biologici şi morfologici tiroidieni evaluaţi.
Ca perspective în aprofundarea problematicii în România, sunt dozarea seleniului din sol şi corelarea cu statusul seleniului în organism (evaluat atât în formă liberă, cât şi în selenoproteine – GPx). Un alt aspect care necesită evaluare suplimentară constă în faptul că la o doză de seleniu de 100 µg/zi s-a înregistrat o scădere a titrului anticorpilor antitiroidieni, dar nu semnificativă, ceea ce ar putea sugera că doza terapeutică ar trebui să fie mai mare decât doza de substituţie. Rezultatele terapeutice obţinute la doze mai mari ar deschide noi orizonturi pentru elaborarea unor programe eficiente de tratament al tiroiditei autoimune şi al complicaţiilor sale evolutive, având drept obiectiv ameliorarea şi îmbunătăţirea calităţii vieţii.
(va urma)
Bibliografie
-
Marinescu E. 20.12.2017. https://romanialibera.ro/lifestyle/bolile-tiroidei-numarul-pacientilor-s-a-triplat-in-ultimii-6-ani-702135.
-
https://www.reginamaria.ro/utile/dictionar-de-afectiuni/afectiuni-tiroidiene-generalitati.
-
www.health.harvard.edu – Thyroid Disease, Understanding hypothyroidism and hyperthyroidism, Harvard Medical School Special Health Report.
-
Stoica I, Vulpoi C. Rezumatul tezei de doctorat – Implicaţiile seleniului în patogeneza tiroiditei autoimmune, Facultatea de Medicină UMF „G. T. Popa”, Iaşi.
-
Gartner R, Gasnier BC, Dietrich JW, Krebs B, Angstwurm MW. Selenium supplementation in patients with autoimmune thyroiditis decreases thyroid peroxidase antibodies concentrations. Journal of Clin Endocr and Metab. 2002;87:1687–1691.
-
Zimmermann MB, Adou P, Torresani T, Zeder C, Hurrell RF. Effect of oral iodized oil on thyroid size and thyroid hormone metabolism in children with concurrent selenium and iodine deficiency. Eur J Clin Nutr. 2000;54(3):209-13.
-
Rasmussen LB, Schomburg L, Kohrle J, et al. Selenium status, thyroid volume, and multiple nodule formation in an area with mild iodine deficiency. Euro J of Endo. 2011;164:585-590.
-
Bugell S, Larsen EH, Sloth JJ, Flytlie K, Overvad K, Steenberg L, Moesgaard S. Absorption, excretion, and retention of selenium from a high selenium yeast in men with a high intake of selenium. Food & Nutrition Research. 2008;DOI:10.3402/fnr.v52i0.1642.