Implicarea farmacistului în managementul durerii
Pharmacist’s involvement in pain management
Abstract
There are many types of pain, and accordingly therapeutic approach to pain should be done more or less specifically. Patient individuality (comorbidity, preferences, mental state, social support) is conditioning therapeutic decisions. Appropriate opioid use is one of the most delicate clinical practice issues. Multimodal analgesia is the optimal current practice in pain management.Keywords
analgesicsNSAIDsadjuvant analgesic drugsacute painperioperative analgesiachronic painneuropathic paincancer painRezumat
Durerea e de mai multe feluri și, corespunzător, abordarea ei terapeutică se face diferit. Particularitățile pacientului (comorbiditate, preferințe, stare psihică, suport social) dictează deciziile terapeutice. Folosirea opioidelor este unul dintre cele mai delicate aspecte de practică clinică. Analgezia multimodală este considerată optimă în managementul actual al durerii.Cuvinte Cheie
analgeziceAINSanalgezice adjuvantedurere acutăanalgezie perioperatoriedurere cronicădurere neuropatădurere în cancerDurerea este una dintre provocările cele mai frecvente cu care se confruntă medicii și farmaciștii în procesul de îngrijire a sănătății pacienților, dacă ne gândim că este cea mai comună cauză pentru care oamenii se prezintă la medic. Durerea poate fi banală și trecătoare sau poate fi apăsătoare și debilitantă.
Progresul științelor medicale și farmaceutice pune la dispoziția noastră, în prezent, un arsenal redutabil de substanțe pe care le putem folosi pentru a vindeca durerea sau pentru a o atenua, atunci când vindecarea nu este un scop realist și tangibil.
Practica ține cont de aceste progrese și modelele de îngrijire vechi își arată limitările. Vom vedea în acest articol o variantă în care protocolul de tratament în trepte propus pe OMS în 1987(1) pentru durerea canceroasă poate fi îmbunătățit(2). Modelele actuale de protocol păstrează temeliile bune ale modelelor vechi, dar încorporează substanțele intrate recent în terapie, profită de avantajele unor formulări farmaceutice deosebite, de tehnologii revoluționare de administrare a substanțelor active și de manevre terapeutice inovatoare. Astfel, mai mulți pacienți pot beneficia de soluții mai bune, mai rapide și mai sigure de atenuare a suferințelor lor. Articolul trece în revistă comparativ diferite analgezice existente pe piața farmaceutică din România, discută principii de tratament pentru tipurile de durere cele mai frecvente și se încheie cu o sugestie asupra recomandărilor de principii vegetale, suplimente alimentare, dispozitive medicale și terapii complementare pe care le poate face farmacistul pacientului care acuză durere.
Definiția durerii
Durerea este o „experiență senzorială ori emoțională neplăcută, asociată unei distrucții tisulare actuale sau potențiale ori descrisă în termenii unei astfel de vătămări“(3). Durerea e subiectivă, iar oamenii variază mult în ceea ce privește toleranța lor la durere.
Durerea nociceptivă este durerea fiziologică și protectivă, iar durerea neuropată este durerea fiziopatologică și dăunătoare(3). Durerea acută este însoțită de anxietate și hiperactivare simpatică, pe când durerea cronică este însoțită de oboseală, de pierderea poftei de mâncare, de pierderea libidoului și de depresie. Durerea nociceptivă poate apărea atât la nivel somatic (piele, oase, încheieturi, mușchi, țesut conjunctiv), cât și la nivel visceral (organe interne)(4).
Componentele durerii nociceptive(3) Sunt etapele prin care durerea devine, pornind de la stimularea unor receptori, un act conștient.
Transducția are loc la nivelul nociceptorilor (receptori pentru durere), care răspund la interacțiunea cu un stimul dureros prin dezvoltarea unui potențial de acțiune care este apoi transmis către măduva spinării.
Transmisia este conducerea impulsului dureros prin fibre aferente A-d (groase, mielinizate, responsabile de apariția unei dureri ascuțite, bine localizate) sau C (subțiri, nemielinizate, responsabile de apariția unei dureri mai puțin intense, slab localizate). Talamusul joacă un rol de triaj al stimulilor dureroși care sunt conduși către structurile superioare ale SNC.
Percepția este procesul în care durerea devine o senzație conștientă, prin integrare la nivelul cortexului cerebral. Atât durerea acută, cât și durerea cronică sunt influențate de factori emoționali. Anxietatea, depresia, oboseala, furia și frica scad pragul percepției durerii. Opus, odihna, starea de spirit bună, simpatia, distragerea atenției și înțelegerea cresc pragul emoțional; de aceea este foarte importantă calitatea relațiilor dintre farmacist și pacient, pentru că, interacționând empatic cu pacientul, farmacistul poate participa la atenuarea durerii acestuia. Terapia comportamental-cognitivă, tehnicile de relaxare, de meditație și de imagerie mentală ghidată pot și ele ajuta în gestionarea durerii. Farmacistul are de oferit astfel de informații pacientului său suferind de dureri, pentru că astfel și rezultatele administrării medicamentelor în scopul atenuării durerii sunt mai bune.
Modularea durerii implică în principal sistemul opioid endogen, dar și alți neurotransmițători (serotonină, noradrenalină, acid g-aminobutiric GABA). Aceștia acționează la nivelul sistemului descendent de control al durerii, care pornește de la nivelul mezencefalului și inhibă transmiterea sinaptică la nivelul coarnelor măduvei spinării(3).
Scopurile terapiei durerii trebuie să fie individualizate pentru fiecare pacient, în funcție de tipul de durere și de circumstanțe. Strategiile folosite sunt atât farmacologice, cât și nefarmacologice.
În durerea acută, scopul intervenției este, de regulă, ameliorarea durerii, până la dispariția ei. În durerea cronică necanceroasă, obiectivele terapiei sunt îmbunătățirea capacității funcționale de zi cu zi a pacientului, încetinirea ratei deteriorării fizice, atenuarea perceperii durerii, creșterea senzației de bine a pacientului, cu păstrarea unor relații sociale și familiale bune și cu o dependență cât mai mică de terapia medicamentoasă. În durerea din cancer, scopul terapiei este de a scădea durerea astfel încât pacientul să aibă cât mai multă libertate de mișcare și de decizie și să suporte cât mai bine tratamentul antineoplazic(3).
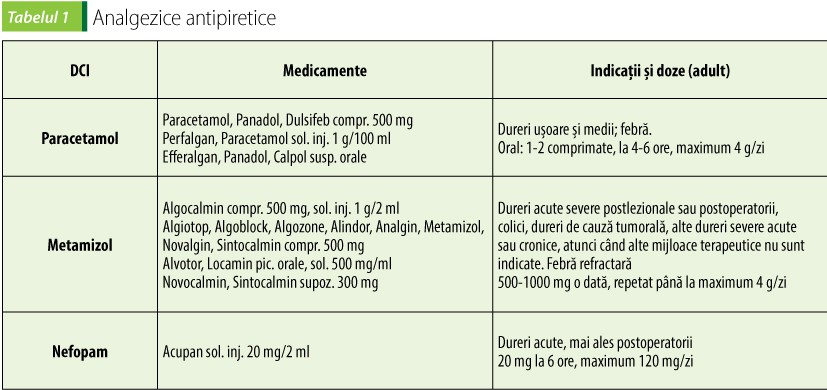
Medicația durerii acute(5)
Durerea acută este descrisă ca sfredelitoare, surdă, fluctuând în intensitate. Durerea acută apare prin traumă sau ca urmare a unei afecțiuni acute (colică renală, infarct acut de miocard). Este autolimitantă, pe măsură ce evenimentul cauzator își găsește vindecarea. Scopul tratamentului este să minimizeze răspunsurile fiziologice (tahicardie, dificultăți de respirație, spasme musculare), efectele adverse psihologice (anxietate) și să împiedice cronicizarea durerii (50% dintre pacienții care folosesc opioide pentru durere acută devin utilizatori cronici de opioide, pentru că durerea se cronicizează). Stabilirea scopurilor realiste este foarte importantă pentru reușita tratamentului. De multe ori, dispariția durerii nu e un scop realist(5).
În prezent, pentru tratarea durerii acute se folosesc analgezice nesteroidiene (AINS), analgezice-antipiretice, opioide puternice și anestezice locale(5). AINS (tabelele 2 și 3) și analgezicele-antipiretice (tabelul 1) blochează enzima ciclo-oxigenază (COX), cu împiedicarea formării prostaglandinelor implicate în nocicepție și inflamație. Opioidele produc analgezie spinală și supraspinală, acționând agonist pe receptorii opioizi. Anestezicele locale stabilizează membranele neuronale, împiedicând formarea și conducerea impulsului dureros(6).
Motive pentru a folosi analgezice neopioide:
- sunt eficiente – AINS scad cu 50% intensitatea durerii moderat-severe în cazul a 33-50% dintre pacienți; paracetamol 1000 mg face același lucru în cazul a 25-33% dintre pacienți(5);
- permit folosirea unei doze mai mici de opioid, atunci când se apelează la opioid, în cazurile mai severe;
- nu dau toleranță, dependență și nu produc abstinență la oprirea tratamentului;
- reacțiile adverse sunt în general mai ușoare decât cele date de morfinomimetice.
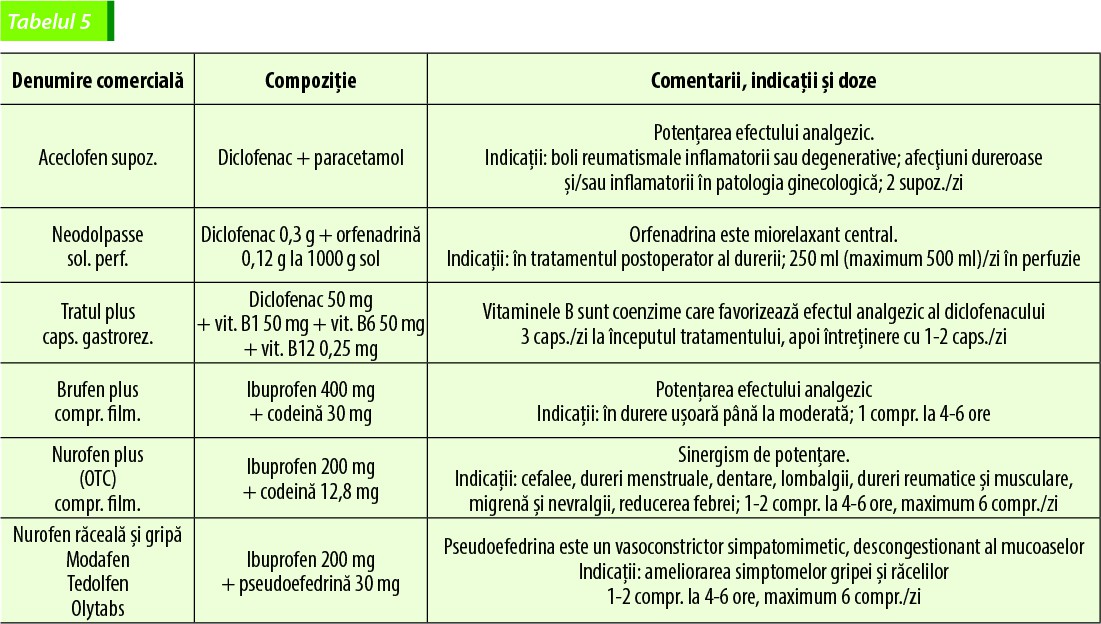
Există multe asocieri fixe de analgezice antipiretice cu alte substanțe, a căror eficacitate e îmbunătățită și profilul reacțiilor adverse e scăzut.
De exemplu, pentru potențarea efectului analgezic, paracetamolul se asociază cu codeină (Ultracod, Paradoren) sau cu tramadol (Zaldiar, Doreta, Linerol, Palgotal, Traumobol).
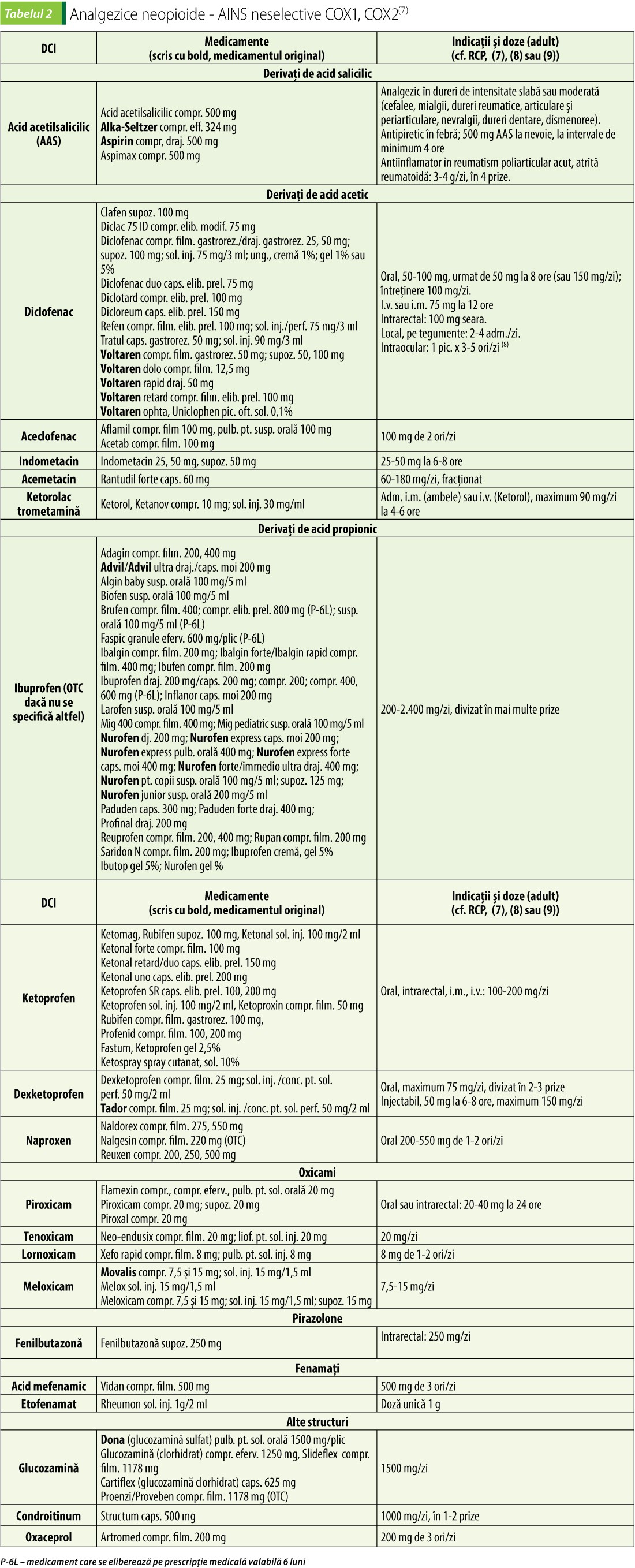
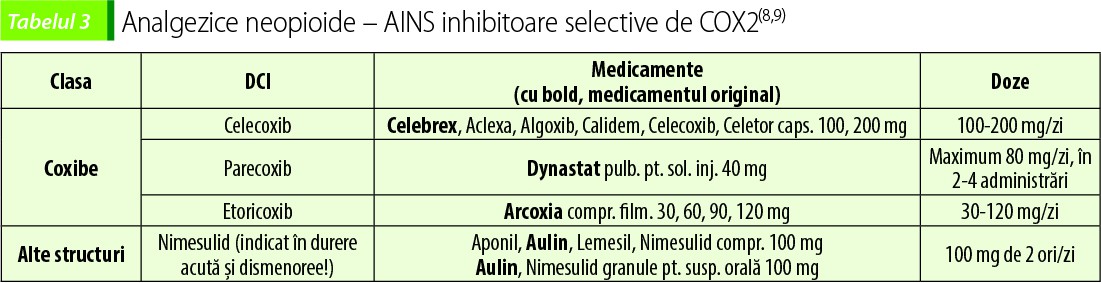
Analgezice neopioide – AINS inhibitoare neselective de COX(7)
Dozele din tabelele 2 și 3 sunt cele uzuale; pentru doze destinate unor indicații particulare, consultați RCP-ul; durata tratamentului poate fi și ea diferită, în funcție de tipul afecțiunii, acută sau cronică. Ca regulă generală de siguranță, reacţiile adverse pot fi reduse la minimum utilizând cea mai mică doză eficace pentru cea mai scurtă perioadă necesară controlării simptomelor.
Ca regulă generală, analgezicele și AINS care sunt OTC-uri nu trebuie administrate pentru mai mult de 3-5 zile fără a se consulta medicul, deoarece se consideră că, dacă durerea nu se ameliorează în acest interval de timp, sunt necesare investigații suplimentare. Pe de altă parte, folosirea pe durată mai lungă a acestor medicamente poate să le crească nivelul de toxicitate, necesitând monitorizare specializată.
Preparatele topice conținând AINS sunt folosite în diferite afecțiuni dureroase cu componentă inflamatorie: reumatism muscular, periartrită scapulo-humerală, lumbago, tenosinovită, bursită; spondiloză, osteoartrită. Se aplică pe pielea intactă prin masaj ușor, de regulă de 1 până la 4 ori/zi.
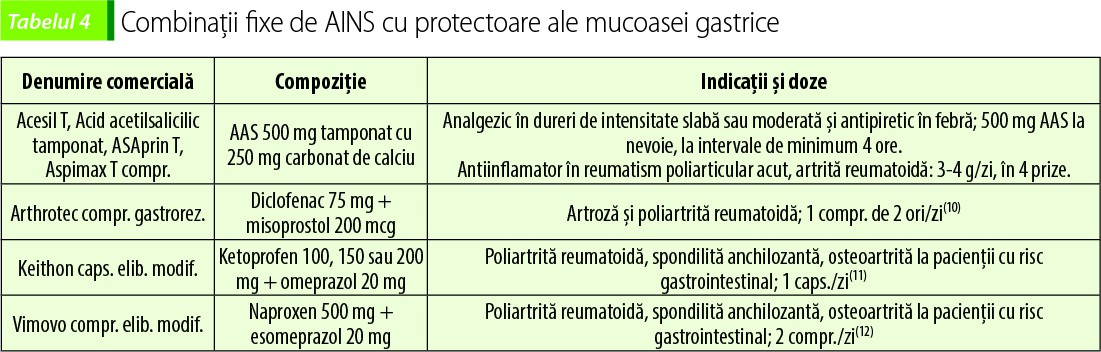
Riscul ulcerelor și al sângerărilor gastrointestinale pentru persoanele peste 65 de ani este de 3-4 ori mai mare decât pentru cei de vârstă mijlocie(7). Pentru a asigura protecție față de tulburările gastrointestinale, mai ales la pacienţii cu risc de apariţie a ulcerului gastric şi/sau duodenal ca urmare a administrării AINS, acestea se asociază cu un protector al mucoasei gastrice (analog de prostaglandină sau inhibitor al pompei de protoni); există asocieri fixe de astfel de substanțe (tabelul 4).
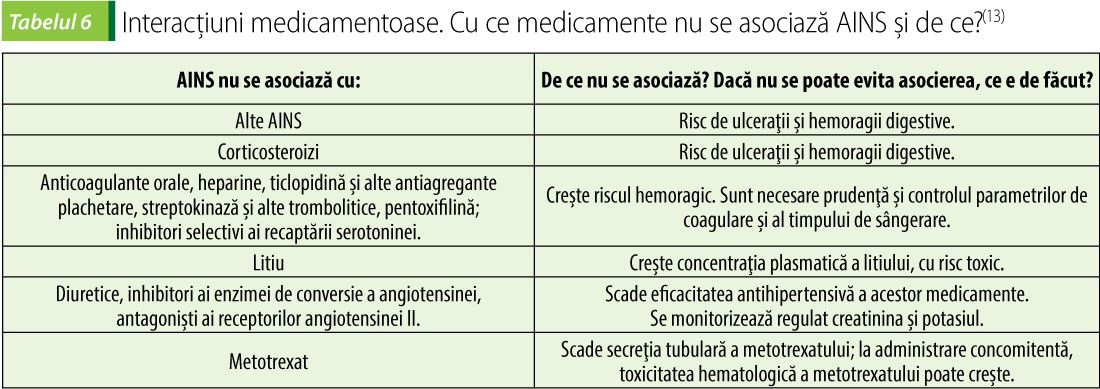
AINS sunt contraindicate la persoane cu antecedente de hipersensibilitate (chiar încrucișată) la antiinflamatoare nesteroidiene sau cu teren alergic; la pacienți cu ulcer gastric sau duodenal activ, cu diateze hemoragice, antecedente de astm bronşic indus de administrarea de AINS. Nu se folosesc în ultimul trimestru de sarcină. Nu se folosesc în insuficiențe grave ale căilor de epurare (insuficiență renală, insuficiență hepatică)(13).
Efectele negative ale AINS în cel de-al treilea trimestru de sarcină se datorează blocării sintezei prostaglandinelor. Consecutiv, se pot instala toxicitate cardiopulmonară (cu închiderea prematură a ductului arterial şi hipertensiune pulmonară); disfuncţie renală, care poate progresa la insuficienţă renală cu oligohidroamnios; prelungire posibilă a timpului de sângerare; inhibare a contracţiilor uterine, determinând întârzierea sau prelungirea travaliului.
Reacțiile adverse ale AINS sunt de tipul: sângerări diverse – hematemeză, melenă, hemoragii digestive oculte (eventual cu anemie feriprivă), epistaxis, gingivoragii, purpură; riscul hemoragic chirurgical este crescut; iritaţie gastrică (dureri abdominale, pirozis, greaţă, vărsături); posibilă activare a ulcerului gastroduodenal. Sunt posibile reacţii alergice, manifestate îndeosebi prin urticarie, edeme, rareori astm bronşic sau reacţii anafilactice. La copiii trataţi cu acid acetilsalicilic în scop analgezic şi antipiretic poate să apară sindrom Reye (encefalopatie şi afectare hepatică)(6).
Dacă AINS sau paracetamolul nu au fost suficiente pentru atenuarea durerilor acute moderat-severe (dureri dentare, dureri postoperatorii, dureri consecutive traumei, dureri musculo-scheletice), pacientului i se poate administra un opiod puternic, oral (morfină, oxicodonă), într-o formă farmaceutică cu cedare imediată (Sevredol compr. film. 10, 20 mg). Acesta temperează reacția emoțională și trebuie luat pe o perioadă cât mai scurtă (5).
Dacă pacientul nu poate înghiți și are dureri moderat-severe (postoperatorii, după chirurgie invazivă, traumă majoră sau IAM), i se administrează un opioid parenteral (i.v., epidural, intratecal). Se recomandă asocierea cu un alt nonopioid. Nu se folosește morfina la alergici la morfină, pacienți postinfarct cu bradicardie, infarct ventricular drept, hipotensiune, confuzie. Dispozitivele PCA (Patient Controlled Analgesia) sunt preferate administrării în perfuzie sau în bolus; cu PCA se obține o analgezie mai bună, crește tolerabilitatea, iar pacientul este mulțumit că își controlează singur durerea(5). Se pot folosi morfina, sol. inj. 2% și petidină (Mialgin, sol. inj. 100 mg/2 ml).
Anestezicele locale (bupivacaină, ropivacaină, lidocaină) se administrează epidural, spinal (intratecal), în bloc nervos periferic sau în infiltrații locale. Se folosesc preoperatoriu la pacienții obezi sau cu boală pulmonară, care sunt mai sensibili la opioide și la anestezia generală. Scad cantitatea de opioid necesară analgeziei.
Analgezia perioperativă
Durerea care apare ca urmare a intervențiilor chirurgicale necesită analgezie multimodală. Ghidul american din 2016 de Management al Durerii Postoperatorii(14) face următoarele recomandări:
- Clinicianul trebuie să furnizeze educație adaptată situației individuale a pacientului, centrată pe pacient și pe familia acestuia. Educația include informații despre opțiunile de tratament pentru managementul durerii postoperatorii, cu stabilirea obiectivelor intervențiilor analgezice și întocmirea unui plan al acestora.
- Analgezia folosită să fie multimodală, adică să folosească o varietate de metode și tehnici analgezice combinate cu intervenții nefarmacologice, pentru a se obține un efect aditiv sau sinergic.
- Opioidele nu sunt neapărat necesare la toți bolnavii operați; e de dorit să se evite folosirea opioidelor atunci când se poate, deoarece unele studii au arătat că folosirea perioperativă a opioidelor este asociată creșterii posibilității de a folosi ulterior opioide pe termen lung. Uneori este suficientă administrarea regulată, continuă (around the clock) a analgezicelor neopioide. Efecte analgezice mai bune se obțin când se combină simultan mai multe medicamente care acționează diferit sau când se folosesc aceleași medicamente administrate prin tehnici diferite (de exemplu, lidocaină administrată sistemic și epidural).
- Dacă e posibil, se preferă administrarea orală a opioidelor față de administrarea intravenoasă. Atunci când calea orală nu e disponibilă, se folosește Analgezia Controlată de Pacient (PCA – Patient Controlled Analgesia). Această metodă folosește o pompă acționată de pacient, care trimite, printr‑un cateter plasat intravenos, cantități presetate de analgezic în corpul pacientului. Pompa poate avea un flux bazal de analgezic (nu la pacienții naivi în ceea ce privește administrarea opioidelor); doza bazală este suplimentată de pacient sau de cineva care îl îngrijește, prin apăsarea unui buton. Avantajele PCA sunt că pun pacientul în controlul durerii sale; pacientul nu mai este supus unor administrări dureroase de analgezice; se reduce timpul în care pacientul are dureri, pentru că nu mai e nevoie de intervenția unui cadru medical care să administreze analgezicul; scad dozele de opioid folosite, iar efectul analgezic e mai bun.
- Dacă e nevoie de administrare parenterală, se recomandă evitarea administrării intramusculare, dureroase.
- Analgezia postoperatorie multimodală presupune folosirea paracetamolului sau a AINS, pentru că există studii care arată că durerea postoperatorie și consumul de opioide sunt mai mici după paracetamol sau AINS decât după opioid.
- Medicația preoperatorie cu celecoxib, 200-400 mg, cu 30-60 de minute înainte de operație, scade consumul de opioid după operație și reduce intensitatea durerii. Nu se administrează celecoxib înaintea unui by-pass coronarian, din cauza riscului cardiovascular intrinsec al medicamentului.
- Administrare preoperatorie de 600-1.200 mg gabapentin sau 150-300 mg pregabalin, cu 1-2 ore înaintea intervențiilor chirurgicale majore sau asociate cu durere intensă.
- Se poate folosi preoperator și ketamina, administrată intravenos. Anestezicele locale (AL) folosite epidural (neuraxial) sau administrate prin infiltrație sunt de folosit în cazul anesteziei multimodale. Tehnici noi de administrare prin infiltrație a AL de tipul bupivacainei folosesc pompe cu elastomeri. Acestea sunt un fel de balonașe pline cu soluție de anestezic, având un cateter cu mai multe orificii, prin care anestezicul local este introdus în zona operată. Eliberarea anestezicului se face constant, evitând astfel limitarea clasică impusă de durata scurtă de acțiune a AL. Administrarea AL înaintea operației reduce cantitatea de analgezic și anestezic folosită intraoperator; se realizează astfel o analgezie preemptivă, cu blocarea efectelor receptorilor NMDA de eliberare a mediatorilor proinflamatori(15).
Medicația durerii cronice
Durerea cronică este durerea care apare mai mult de trei luni, care persistă mai mult de o lună după vindecarea unor leziuni acute sau care acompaniază o leziune care nu se vindecă. Cauzele durerii cronice sunt boli cronice (cancer, diabet, artrită), traumatisme (hernii de disc, rupturi de ligament) sau tulburări dureroase primare (durere neuropată, fibromialgie, cefalee)(7).
Durerea neuropată este un tip de durere cronică. Durerea neuropată este cauzată de o vătămare a nervilor periferici sau a sistemului nervos central. Anticonvulsivantele și antidepresivele sunt de elecție în abordarea durerii neuropate periferice, dar se pot folosi și opioide, și agenți topici. Când vătămarea este centrală, simptomele pot fi periferice, iar medicamentele sunt puțin eficace(4).
Componenta neuropată a durerii apare frecvent în neuropatiile diabetice dureroase, nevralgiile postherpetice, durerea neoplazică, vătămări ale măduvei spinării, sindromul durerii regionale complexe, scleroza multiplă, nevralgia de trigemen, durerea post-AVC, durerea asociată infecției cu HIV(16).
Medicația durerii neuropate
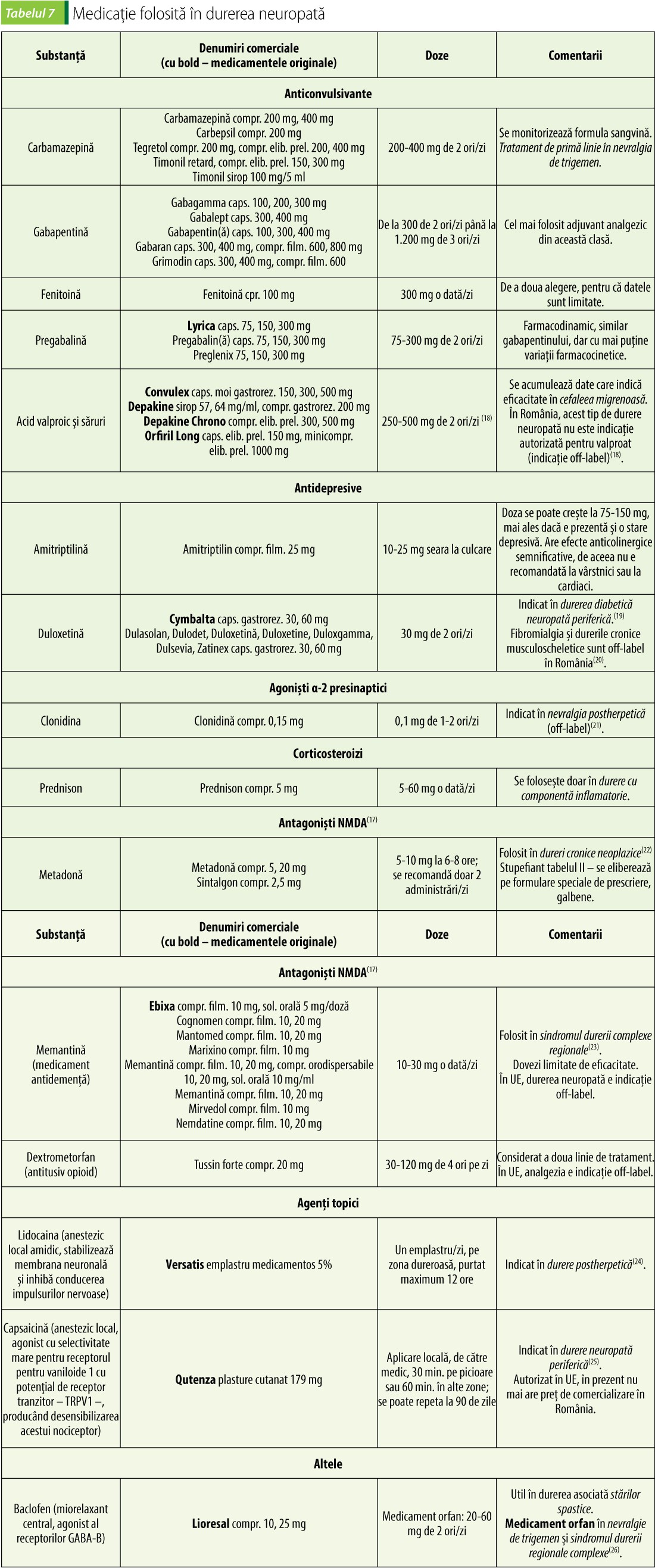
Analgezicele adjuvante sunt medicamente consacrate pentru o altă indicație terapeutică (anticonvulsivante, antidepresive, agoniști centrali a-2 presinaptici, corticosteroizi etc.), dar s-a observat și studiile clinice au confirmat că pot fi folosite cu succes în situații în care analgezicele clasice nu sunt suficiente. În anumite situații sunt chiar tratamente de primă alegere (tabelul 7).
În pofida eficacității de necontestat a analgezicelor opioide, care constituie medicația de elecție în durerea moderată și severă, un studiu al American Pain Society din 1998 arată că cel puțin 40% dintre pacienții tratați cu opioide pentru durere moderată sau severă nu obțin ameliorări satisfăcătoare. Această ineficacitate terapeutică se poate datora rezistenței la opioide sau durerii neuropate. Rezistența la opioide se întâlnește în durerea neoplazică, în neuropatii, în sindromul durerii complexe regionale, în durere postherpetică sau pancreatită. În aceste situații se pot folosi antagoniștii NMDA (N-metil-d-aspartat). Stimularea receptorilor NMDA de către glutamatul eliberat la stimuli dureroși este asociată hiperalgeziei, durerii neuropate și funcționalității scăzute a receptorilor opioizi. Metadona, analgezic opioid agonist µ, k și d, este și un puternic blocant al receptorilor NMDA; se poate folosi ca înlocuitor al altor opioide când acestea nu (mai) sunt eficiente sau dacă au determinat reacții adverse limitatoare ale creșterii dozei. Este însă greu maniabilă, deoarece are un timp de înjumătățire lung și variabil, necesită monitorizare EKG, pentru că prelungește intervalul QT și este incriminată în multe interacțiuni medicamentoase; stabilirea dozelor echianalgezice în comparație cu morfina este dificilă. Ketamina este un antagonist NMDA puternic, astfel încât incidența efectelor adverse este mare; halucinațiile și stările mentale disociative limitează folosirea ketaminei, deși este eficientă în tratarea durerilor refractare la tratament. Memantina și dextrometorfanul blochează mai puțin receptorii NMDA, având în consecință reacții adverse mai puțin severe: amețeli, tulburări de vedere, bufeuri; din păcate, și eficacitatea ca analgezice este mai mică(17).
Medicația durerii în cancer
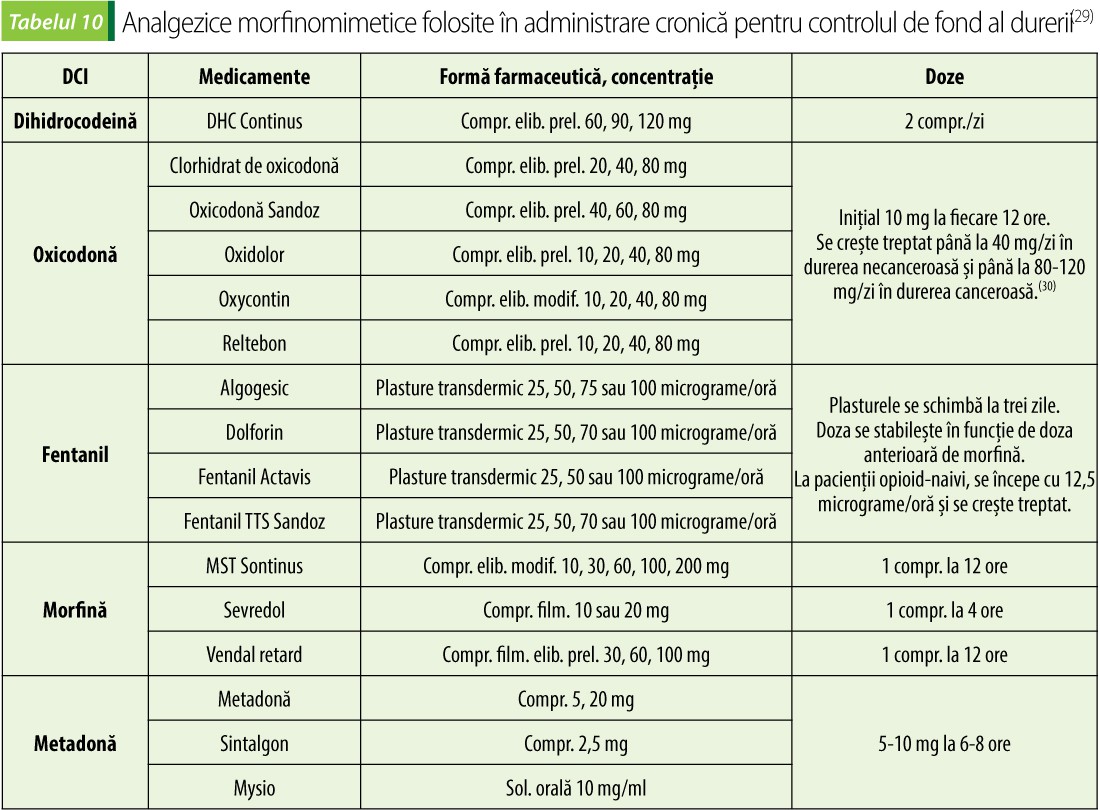
Analgezice morfinomimetice
Morfinomimeticele, prin acțiune agonistă la nivelul receptorilor µ, d și k, împiedică transmiterea impulsurilor nociceptive pe căile spino-talamice și talamo-corticale. Împiedică perceperea durerii la nivel talamic și cortical, cu creșterea pragurilor de percepere a durerii și de reacţie la durere, cu înlăturarea reacţiilor psihice, vegetative și somatice.
Pe lângă acțiunea analgezică, opioidele produc inhibiţie a SNC, cu sedare și somnolenţă, precum și diminuarea capacităţii de concentrare. Deprimă centrul respirator bulbar, producând deprimare respiratorie și deprimare a centrului tusei, cu efect antitusiv util. Stimulează centrul vomei, din aria postrema, cu apariția de grețuri și vărsături. Scad tranzitul intestinal și produc constipaţie, prin creșterea tonusului mușchilor netezi ai tubului digestiv și prin scăderea peristaltismului, prin scăderea secreţiilor digestive și prin contracția sfincterelor.
La nivel renal, determină tendinţă la retenţie urinară, prin creșterea tonusului sfincterului, a vezicii urinare, a detrusorului și a ureterelor(6).
Paranteza care urmează se referă la principii de folosire corectă a analgezicelor opiode(27).
Limitarea folosirii opioidelor în durerea acută. Opioidele nu sunt medicamente de primă alegere pentru multe tipuri de durere acută. Se prescriu doar pentru perioada anticipată de dureri severe, urmând a se face trecerea cât se poate de repede la analgezice neopioide OTC-uri. Nu se folosesc formele cu cedare controlată în durerea acută(27).
Limitarea folosirii opioidelor pentru durerile de spate. Pentru durerile acute de spate, se consideră că opioidele nu au rezultate mai bune decât AINS. Abordarea durerilor acute de spate se face farmacologic (tabelul 8) și nefarmacologic. Rolul intervențiilor este să reducă durerea și efectele ei asupra activității de zi cu zi, nu neapărat să elimine total durerea. Pacienții trebuie sfătuiți să rămână activi. Pacienții pot aplica comprese calde sau reci, eventual alternându-le. Ei trebuie consiliați asupra folosirii acestora, pentru a nu se arde, mai ales cei care au sensibilitatea termică afectată; compresele nu se aplică direct pe piele și se țin 15-20 de minute. Dacă durerea ține mai mult de patru săptămâni, pacienților cu risc mare de cronicizare a durerii lombare (cei cu stare generală proastă, depresivii, maladaptativii, cei cu dureri severe) li se recomandă fizioterapie. Toți pacienții cu durere de spate mai lungă de patru săptămâni pot recurge la yoga, masaj, acupunctură(28).
Dacă durerea se cronicizează, se poate încerca administrarea de amitriptilină sau duloxetină.
Folosirea opioidelor cronice doar în afecțiuni potrivite. Opioidele administrate cronic sunt eficiente în durerile moderat-severe care nu răspund la altă medicație: osteoartrită neresponsivă la paracetamol sau AINS, durere neuropată neresponsivă la antidepresive triciclice sau anticonvulsivante. În general, se evită opioidele cronice în durerea pelviană, fibromialgie, cefalee, migrenă, dureri de spate, sindromul intestinului iritabil(27).
Identificarea pacienților cu risc de folosire neadecvată a opioidelor. Factorii de risc care predispun la abuzul de opioide sunt: vârsta (tinerii au factor de risc mai mare decât adulții), boală psihiatrică în antecedente, istoric personal sau familial de abuz de substanțe; aceștia trebuie evaluați. Pacientul care prezintă comportament de căutare de drog (cere insistent un anumit produs, susține că e alergic sau nu tolerează anumite produse) este un posibil toxicoman(27).
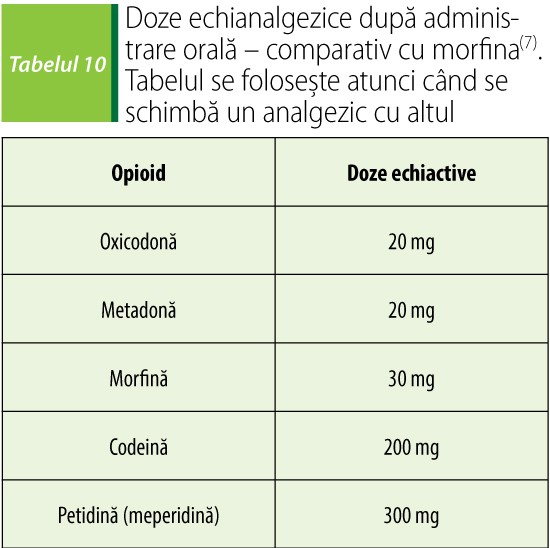
Reducerea riscului de supradoză. Pacienții trebuie evaluați în ceea ce privește depresia, ideația suicidară sau alte probleme psihiatrice. Opioidele se prescriu și se eliberează în cantități limitate; aceste cantități pot fi și mai mici, în cazul pacienților cu riscuri. Se evită asocierile cu alte deprimante SNC (benzodiazepine, barbiturice, miorelaxante etc.). Tratamentul se începe cu doze mici dintr-un opioid cu durată scurtă de acțiune (oxicodonă 5 mg la 4-6 ore). Opioidele cu durată lungă de acțiune nu sunt mai sigure sau mai eficiente decât cele cu durată scurtă de acțiune – au risc de supradoză de două ori mai mare decât cele cu durată scurtă de acțiune. Opioidele cu durată lungă de acțiune se păstrează pentru pacienții cu dureri severe continue, la care opioidele cu durată scurtă au fost eficace. La doze peste 100 mg/zi de morfină administrată oral, riscul de supradoză crește semnificativ. Trecerea de la un opioid la altul necesită atenție sporită și se face în funcție de dozele echianalgezice. Pacientul trebuie consiliat să nu mestece, să nu rupă sau să nu zdrobească formele farmaceutice cu cedare modificată(27).
Gestionarea așteptărilor pacientului. Scopurile terapiei trebuie agreate de profesionistul în sănătate și pacient. În cazul durerii cronice, scopul principal al terapiei este îmbunătățirea sau menținerea funcționalității. Pacientul trebuie avertizat că reducerea durerii cu 30% și ameliorarea funcțională cu 30% reprezintă un succes al terapiei durerii cronice. Pacientul trebuie să înțeleagă că administrarea de opioide se face numai pe un interval de timp limitat(27).
Educarea pacientului. Pacientului trebuie să i se prezinte alternativele terapeutice. Consilierea pacientului se face și referitor la faptul că nu trebuie să consume alcool pe perioada tratamentului cu opioide și că nu trebuie să conducă dacă se instalează somnolența. Pacientul trebuie să fie informat despre riscurile consumului cronic de opioide (hipogonadism, apnee de somn, toleranță, hiperalgezie, dependență și sindrom de abstinență). Pacientul și cei care îl îngrijesc trebuie să știe cum să păstreze la loc sigur opioidele și ce să facă cu cantitățile nefolosite(27).
Prevenirea și identificarea folosirii improprii. În durerile cronice necanceroase se recomandă ca pacientul să se angajeze să folosească opioidele o perioadă limitată. Aderența la tratament (și abuzul de medicamente este o formă de neaderență, deși pacientul ia mai mult de 100% din medicamentele sale) se poate determina pe baza numărării pastilelor și prin testarea unor specimene de urină, periodic, dar și inopinat(27).
Evaluarea corespunzătoare a terapiei cu opioide. Pacientul care ia opioide trebuie să fie evaluat periodic de medicul său, ca și la creșteri ale dozei administrate. Ineficacitatea dozei administrate se poate datora folosirii necorespunzătoare sau instalării hiperalgeziei (sensibilizare la durere produsă de opioide)(27).
Folosirea corespunzătoare a terapiei adjuvante. Înainte de a folosi opioide, se încearcă folosirea dozelor mari de analgezice neopioide. Terapia comportamental-cognitivă, exercițiile aerobe și stretchingul sunt utile. Este nevoie de un regim de somn adecvat. Comorbiditățile trebuie tratate. Constipația se previne cu laxative osmotice sau stimulante, fluide, fibre și exerciții fizice(27).
Întreruperea tratamentului. Se scade doza sau se întrerupe tratamentul prin scăderea treptată a dozelor, dacă substanța nu e eficientă, apar efecte adverse intolerabile, semne de intoxicație, supradoză, opioidul e folosit în alte scopuri sau hiperalgezie suspectată(27).
Oferirea de tratament în cazul în care s-a instalat dependența de opioide. Se folosesc substanțe de tip metadonă sau asocierea buprenorfină-naloxon (Suboxone compr. sublinguale). Buprenorfina este un agonist-antagonist mixt, stimulând receptorii µ și d și blocând receptorii k, în timp ce naloxon este antagonist competitiv al receptorilor opioizi(6).
Prin definiție, se consideră că a apărut toleranță la opioide în cazul pacienților care primesc, cel puțin o săptămână, cel puțin 60 mg/zi morfină oral sau 25 mcg/oră fentanil transdermal sau 30 mg/zi oxicodonă oral sau un alt opioid în doză echianalgezică(31).
În situația în care un pacient aflat sub tratament cronic cu opioide experimentează dureri fulgurante (breakthrough pain), acestea se tratează cu opioide de urgență, cu latență și durată scurtă de acțiune, de exemplu fentanilul condiționat sub formă de comprimate sublinguale (Lunaldin). Acestea se iau la nevoie, își fac repede efectul și controlează durerea bruscă și violentă.
Reacții adverse ale morfinomimeticelor
Morfinomimeticele pot produce dependență și folosire în scopuri ilicite, ca droguri. Însă au și alte efecte adverse, unele severe. Pot produce deprimare respiratorie, cresc riscul de apariție a fracturilor provocate de căderi, produc hipogonadism, cresc sensibilitatea la durere, determină constipație și impactarea materiilor fecale, cresc riscul apariției cariilor dentare, deoarece determină uscăciunea gurii. Riscul de supradoză apare nu doar la cei care abuzează de medicamente sau la cei care le folosesc în scop suicid, ci și la cei care folosesc opioidele prescrise de medic, mai ales la utilizare concomitentă cu alte deprimante SNC (benzodiazepine, alcool)(32,7).
Analgezicele morfinomimetice care blochează receptorii µ de la nivel intestinal produc constipație. Măsurile de urmat pentru reducerea acestui efect advers pot fi prezentate de farmacist. Un laxativ osmotic (lactuloză) poate fi administrat regulat; laxativele osmotice sunt bine tolerate chiar și în administrare prelungită și produc crampe intestinale mai puțin decât laxativele iritante intestinale (de tipul bisacodilului, antracenozidele din Senna). Bisacodilul se poate folosi dacă laxativele osmotice nu sunt eficiente. Dacă nici una dintre aceste intervenții nu e eficientă, constipația produsă de opioide se poate combate cu un antagonist opioid intestinal de tipul metilnaltrexonului (Relistor, sol. inj. pentru administrare subcutanată), care împiedică legarea agoniștilor opioizi de receptorii lor intestinali, păstrând astfel motilitatea intestinală, fără afectarea efectului analgezic(33).
Consiliați pacienții asupra importanței stilului de viață pentru un tranzit intestinal normal (suficiente fibre și lichide în alimentație; creșterea activității fizice, dacă e posibil; orar de defecare, după micul dejun, fără grabă sau fără neeliminarea scaunului când survine reflexul de defecare etc.)(34).
Contraindicațiile morfinei (Sevredol)
Hipersensibilitate cunoscută la morfină sau la oricare dintre excipienţi, depresie respiratorie, astm bronşic, stază bronşică, insuficienţă respiratorie decompensată în absenţa respiraţiei asistate, traumatism cranian acut, cu hipertensiune intracraniană în absenţa respiraţiei asistate, epilepsie necontrolată terapeutic, ileus paralitic, abdomen acut, rectocolită ulcero-hemoragică, evacuare gastrică întârziată, boli hepatice acute, insuficienţă hepatică gravă cu encefalopatie.
Este contraindicat tratamentul concomitent cu buprenorfină, nalbufină şi pentazocină, tratament concomitent cu inhibitori de monoaminooxidază (IMAO) sau la mai puţin de două săptămâni de la întreruperea lui.
Nu se recomandă în timpul sarcinii şi alăptării. Nu se recomandă copiilor cu vârsta mai mică de 3 ani.
De asemenea, este contraindicată utilizarea morfinei la conducătorii auto(35).
Particularitățile geriatrice ale tratamentului cu analgezice opioide apar deoarece la vârstnici opioidele au timp de înjumătățire mai lung și efect analgezic mai intens, comparativ cu adultul. Administrate pe perioade scurte în dureri cronice, reduc durerea și îmbunătățesc mobilitatea, dar afectează negativ funcțiile mintale. Constipația și retenția urinară produse de opioide sunt mai severe la bătrâni. Riscul de fracturi, datorat sedării și confuziei, e mai mare după opioide decât după AINS(7).
Din cauza riscului de adicție, abuz și folosire necorespunzătoare a opioidelor, chiar la dozele recomandate, și pentru că formele cu cedare controlată au risc mai mare de supradozare, acestea se recomandă a fi folosite la pacienții pentru care analgezicele neopioide sau opioidele cu cedare imediată nu sunt eficiente ori nu sunt tolerate. Formele farmaceutice cu cedare controlată nu sunt indicate pentru durerea acută sau pentru tratament la nevoie (PRN; pro re nata)(31). Un avantaj al formelor farmaceutice cu cedare controlată este că, din ele, substanțele active sunt greu de reconstituit pentru administrare parenterală, fiind deci mai greu de deturnat de la scopul lor terapeutic către folosirea recreațională.
Eliberarea produselor care conțin substanțe psihotrope este strict reglementată prin Legea 339/2005 privind regimul juridic al plantelor, substanțelor și preparatelor stupefiante și psihotrope și de Legea 179/2012 pentru modificarea și completarea Legii 339/2005 și normele lor de aplicare. Conform acestor acte normative, opioidele se încadrează în lista TAB II și se eliberează pe formulare de prescripție galbene.
Scara analgezică în cancer
Organizația Mondială a Sănătății (OMS) a elaborat în 1987 o „scară“ analgezică folosită pentru intervenții eficiente de atenuare a durerii care apare în cancer. Conform acestui protocol, durerea apărută în cancer se tratează oral cu medicamente în următoarea succesiune:
- analgezice neopioide (AAS, paracetamol);
- opioide slabe (codeină);
- opioide puternice (morfină),
la toate treptele putându-se adăuga adjuvante pentru calmarea anxietății.
Pentru a asigura analgezie optimă, medicamentele se administrează la fiecare 3-6 ore, și nu la nevoie.
Metoda propusă de OMS este considerată accesibilă ca preț și cu eficacitate de 80-90%(1).
Cu timpul, scării analgezice a OMS i s-au găsit limitările. Scara clasică OMS se consideră în prezent că furnizează analgezie eficace la 70-80% dintre pacienți, pentru că nu permite inițierea tratamentului direct cu trepte superioare. În plus, multe dintre intervențiile analgezice recente, precum și multe substanțe consacrate deja în practică, nu sunt folosite de scara analgezică OMS(2).
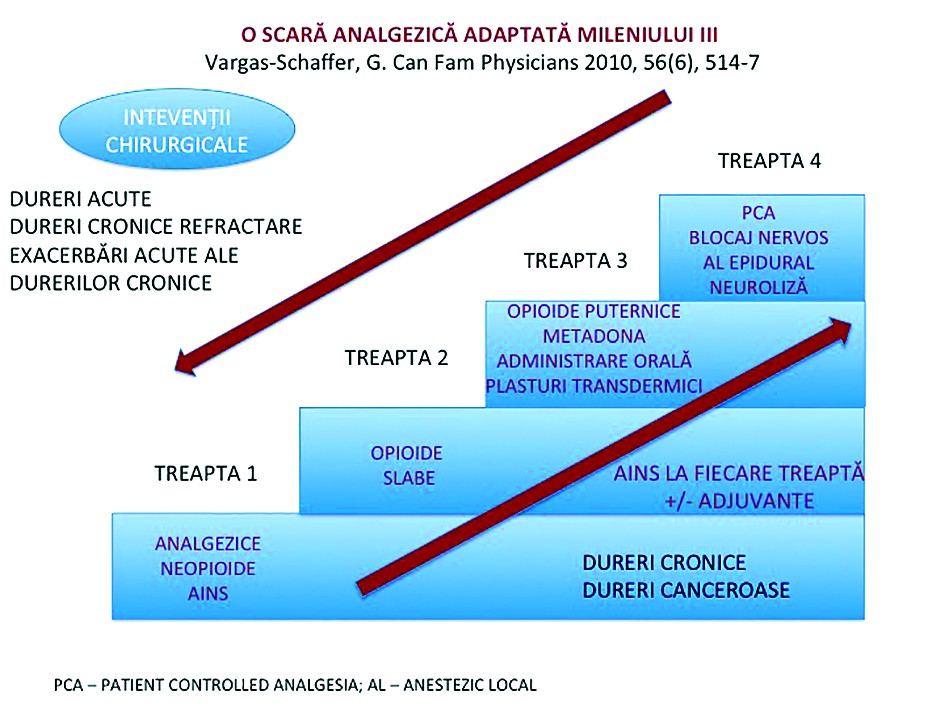
În figura 1 este prezentată o astfel de adaptare a scării analgezice OMS pentru durerea acută, durerea cronică necanceroasă și durerea neoplazică.
Noua scară are patru trepte și oferă mai multă flexibilitate; se poate iniția analgezia de la orice treaptă; scara poate fi urcată sau coborâtă după tipul și intensitatea durerii. A patra treaptă conține proceduri neurochirurgicale, precum stimularea cerebrală, sau tehnici invazive, precum blocajul nervos ori neuroliza. Tot aici se regăsește și metoda PCA de autoadministrare a analgezicului în raport cu nevoile pacientului prin intermediul unui dispozitiv de tip pompă. Apar și substanțe noi – tramadol, oxicodonă, buprenorfină –, și forme farmaceutice și căi de administrare noi: plasturii transdermici. Metadona apare pe treapta a treia a scării, pentru că este folosită în tratarea durerii neoplazice, a durerii cronice necanceroase și a durerii neuropate refractare(2).
Plante, suplimente alimentare și alte practici complementare(36,37)
Durerea fiind atât de prezentă în viața oamenilor, nu e de mirare că produsele de origine naturală (comercializate sub forma suplimentelor alimentare sau a dispozitivelor medicale) sunt atât de folosite. Mulți oameni au o reacție de aversiune față de medicamentele de sinteză și preferă remediile naturale. Cunoașterea aprofundată de către farmacist a terapiilor alternative și a principiilor active naturale îl face pe acesta un mai bun consilier al pacientului afectat de dureri. În continuare vom trece în revistă unele dintre cele mai folosite astfel de remedii. Produsele comerciale de origine naturală enumerate în text sunt suplimente alimentare notificate IBA sau dispozitive medicale înregistrate la ANMDM.
Plante și extracte din plante cu acțiune antiinflamatoare. Atenție la interacțiuni cu alte medicamente, pentru că aceste principii vegetale au, cel puțin teoretic, și efectele adverse ale antiinflamatoarelor. De aceea pot favoriza sângerările, la asociere cu alte medicamente antitrombotice.
Bromelaina (Ananas comosus) este o enzimă proteolitică din ananas despre care se consideră că are proprietăți antiinflamatoare prin reducerea migrării și activării leucocitelor. Reduce durerea în osteoartrite, deși nu este clar dacă poate atinge concentrații plasmatice suficiente pentru a avea efect terapeutic. Se găsește în produse precum Bromelain 500 mg, Bromelaină 800 GDU. OTC-ul Wobenzym conține bromelaină (bromelină), alături de alte enzime, și este adjuvant în stări inflamatorii de natură traumatică sau consecutive intervenţiilor chirurgicale minore, administrându-se 2-3 drajeuri de 3 ori pe zi înaintea meselor(38).
Gheara-mâței (Uncaria guaianensis) inhibă prostaglandina PGE2 și factorul de necroză tumorală a și poate fi eficientă în osteoartrite, reducând durerea asociată mișcării și rigiditatea. Se găsește în produse precum Cat’s Claw 485 mg, 500 mg etc.
Gheara-diavolului (Harpagophytum procumbens) conține harpagozidă care inhibă COX și lipooxigenaza, având efecte utile în durerea din osteoartrită. Există studii conform cărora 50-100 mg de harpagozidă zilnic reduc durerea de spate similar cu rofecoxib 12,5 mg/zi (Vioxx, coxibă a cărei autorizație de punere pe piață a fost retrasă în 2004 din cauza riscului cardiovascular crescut, dar care este un antiinflamator și analgezic eficient)(39). Se folosesc atât preparate topice (Artiglio diavolo, Balsam Gheara-diavolului etc.), cât și sistemice (Gheara-diavolului caps., Harpagophyton caps., Devil’s Claw caps., Harpagin caps. etc).
Turmericul (Curcuma longa) conține curcumină, despre care se pare că are activitate antiinflamatorie prin inhibarea COX2, a prostaglandinelor și a leucotrienelor, putând reduce durerea în osteoartrită și în artrită reumatoidă. Produse comerciale: Curcumin95 C3 complex, Turmeric (Curcuma longa) 720 mg, Curcumin plus capsule vegetale, Curcuma 3X, Curcumin Forte – Turmeric extract cu 95% Curcuminoide 500 Mg etc.
Scoarța de salcie (Salix sp.) conține salicină, care se biotransformă în acid salicilic, cu acțiune antinflamatoare, analgezică și antiagregant plachetară. Pe piața din România se găsește în produsele Salix, Salix 500, Salix Extract (100 mg salicină) – Aspirina vegetală etc.
Remediii naturale cu acțiune antidepresivă. În asociere cu medicamente care acționează stimulant la nivelul transmisiei serotoninergice (tramadol, antidepresive etc.), pot determina apariția sindromului serotoninergic.
5-HTP (5-hidroxitriptofan) și L-triptofan sunt convertiți în organism la serotonină și studii neconcludente susțin că au efect analgezic în durerea neuropată. Există un supliment înregistrat la IBA, 5-HTP 98% (5-hidroxitriptofan 98%), deși în anii 1989-1990 L-triptofanul a fost asociat cu apariția sindromului eosinofilie-mialgie, cu rată de mortalitate mare.
Extractul de sunătoare a fost testat pentru acţiunea analgezică în durerea neuropată, dar studiile nu sunt concludente. Se găsește în Extract de sunătoare, extract uleios de sunătoare presat la rece, tinctură de sunătoare, Hypericum extract de sunătoare, ST John’s Wort Organika 450 mg. Remotiv este un OTC conținând extract uscat de Hyperici herba, indicat pentru ameliorarea stărilor depresive ușoare; stimulează transmisiile serotoninergică și adrenergică. Este un inductor enzimatic puternic, cu numeroase interacțiuni farmacocinetice.
Remediile iritante determină iritație și stimulare a țesutului nervos, care în timp conduc la depleția și inhibarea reacumulării de substanță P în nervii senzitivi. Apare diminuarea răspunsului la stimuli dureroși, cu ameliorarea durerii.
Camforul (rășină de Cinnamomum camphora) este folosit în diferite preparate topice, pentru atenuarea durerii acute ușoare produse de înțepături de insectă, arsuri minore, hemoroizi. Se folosesc alcoolul camforat 10%, plasturi antireumatici cu camfor etc.
Capsicum (Capsicum spp) conține capsaicină, utilă după aplicare topică în durerile din osteoartrită. Este disponibil sub forma unui extract alcoolic de ardei iute (Capsicum) și ca plasturi antireumatici.
Alte remedii naturale
Condroitin sulfat este unul dintre cele mai folosite produse naturale pentru combaterea durerii, participând la formarea matricei celulare. Intră în compoziția multor preparate antialgice care conțin și glucozamină, eventual și MSM.
Glucozamin sulfatul participă la formarea lichidului sinovial. Sulfatul de glucozamină are eficacitate mai mare decât clorhidratul de glucozamină. Conform unor studii, 1.500 mg/zi de glucozamin sulfat au efecte analgezice comparabile cu ale 1.200 mg/zi de ibuprofen(40) sau paracetamol 1.000 mg de 3 ori/zi(41). Efectul analgezic al glucozaminei pare că durează mai mult decât efectul acestor substanțe cu care a fost comparată, dar apare mai greu(36). Se administrează 1.500 mg/zi, preferabil doză unică. Intră în compoziția Glucozamin Condroitin Hyaluronic acid, Condartrox, Proveben, Bonefactor etc.
Metilsulfonilmetan (MSM) pare să aibă efecte favorabile în osteoartrită; are și efecte serotoninergice, putând să favorizeze instalarea fazei maniacale la pacienții cu tulburări bipolare.
S-adenozilmetionina (SAM) pare să crească sinteza de proteoglicani în celulele cartilaginoase, stimulând creșterea și regenerarea cartilajului.
Marijuana (Cannabis sativa) începe să intre în arsenalul terapeutic de combatere a durerii severe (în SUA), acționând la nivelul receptorilor canabinoizi, deși este mai degrabă cunoscută pentru folosirea ei în scop recreațional.
Deși folosite în medicina tradițională de multă vreme, remediilor naturale le lipsesc cel mai adesea studii clinice de calitate pe baza cărora farmacistul să poată face recomandări de calitate.
O sumară indicație de recomandare pentru farmaciști în ceea ce privește oferirea de remedii naturale pentru ameliorarea durerilor pacienților poate fi structurată astfel(36):
Recomandați produse cu camfor (pentru durere), Capsicum, Glucozamin sulfat, SAM; există studii care arată că, probabil, sunt eficiente și sigure.
- Nu recomandați produse cu camfor (pentru osteoartrită), Condroitin sulfat, Turmeric sau activități precum acupunctura, balneoterapia, masajul, reflexologia, yoga; acestea sunt probabil sigure, însă doar posibil eficace și nu pot înlocui tratamente dovedite a fi eficiente.
- Nu recomandați tehnici de relaxare precum imageria ghidată sau meditația; acestea sunt probabil sigure, dar în favoarea lor dispunem de insuficiente dovezi de eficiență.
- Nu recomandați 5-HTP, gheara-mâței, gheara-diavolului, MSM, urzică vie, scoarță de salcie; ele sunt doar posibil eficiente și posibil sigure.
- Nu recomandați produse cu bromelaină, glucozamină clorhidrat sau activități precum terapia Reiki; deși sunt posibil sigure, nu există suficiente dovezi de eficacitate.
- Recomandați împotriva folosirii ca analgezice a extractului de sunătoare (posibil ineficient și generator de interacțiuni medicamentoase multiple), a L‑triptofanului (istoric de reacții adverse) și marijuanei, posibil eficientă, dar și posibil nesigură.
Omul suferind are dreptul să beneficieze de îngrijirea optimă pe care o poate furniza o societate, într-un anumit loc și la un anumit moment de timp. Pentru aceasta, medicii și farmaciștii au datoria să își exercite cât mai bine profesia și să utilizeze toate instrumentele pe care le au la dispoziție.
Bibliografie
- WHO. WHO’s cancer pain ladder for adults. Available from: http://www.who.int/cancer/palliative/painladder/en/ .
- Vargas-Schaffer G. Is the WHO analgesic ladder still valid? Twenty-four years of experience. Can Fam Physicians. 2010; 56(6): pp.. 514-517.
- Baumann T, Herndon C, Strickland J. Pain Management. In Pharmacotherapy: A Pathophysiologic Approach, Ninth Edition. Excerpt From: Posey, L. Michael. „Pharmacotherapy: A Pathophysiologic Approach, Ninth Edition: McGraw-Hill Education; 2014.
- Kral L, Virginia G. Pain and Its Management. In Alldredge B, editor. Koda-Kimble and Young’s Applied Therapeutics: The Clinical Use of Drugs.: Lippincot Williams&Wilkins; 2012. pp. 112-146.
- Cupp M. Analgesics for Acute Pain. Pharmacist’s Letter / Prescriber’s letter. 2014 November.
- Cristea AN. Tratat de farmacologie. I ed.: Editura Medicală; 2006.
- Chirița C, Marineci CD. Agenda Medicală 2016 - Ediția de buzunar: Editura Medicală; 2016.
- Markman J, Narasimhan SK. Treatment of Pain. In Merck Manual Professional Version. [Online].; 2014 [cited 2016 October 9 [accesat 10.10.2016]. Available from: https://www.merckmanuals.com/professional/neurologic-disorders/pain/treatment-of-pain .
- Dobrescu D, Negreș Simona. Memomed; 2016.
- ANMDM. RCP Arthrotec.; 2016 [http://www.anm.ro/_/_RCP/rcp_5640_24.08.05.pdf?s_den_com=arthrotec&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=2819 accesat 14.10.2016].
- ANMDM. RCP Keithon.; 2016 [http://www.anm.ro/_/_RCP/rcp_1541_02.04.09.pdf?s_den_com=Keithon&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=17481 accesat 15.10.2016].
- ANMDM. RCP Vimovo.; 2015 [http://www.anm.ro/_/_RCP/rcp_3440_20.05.11.pdf?s_den_com=Vimovo&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=36907 accesat 15.10.2016].
- ANMDM. RCP Naldorex.; 2015 [http://www.anm.ro/_/_RCP/rcp_4952_18.09.12.pdf?s_den_com=naldorex+&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=22493 accesat 10.10.2016].
- Chou R, Gordon D, de Leon-Casasola Oea. Management of Postoperative Pain: A Clinical Practice Guideline From the American Pain Society, the American Society of Regional Anesthesia and Pain Medicine, and the American Society of Anesthesiologists’ Committee on Regional Anesthesia, Executive Committee, and Administrative Council. J Pain. 2016 February; 17(2): pp. 131-157.
- Whiteman A, Bajaj S, Hasan M. Novel Techniques of Local Anaesthetic Infiltration. BJA Education. 2011; 11(5): pp. 167-171.
- Linn J. Medical Approach to the Management of Neuropathic Pain. The Transverse Myelitis Association Newsletter. 2007; 7(2).
- ANMDM. RCP Orfiril Long - acid valproic și săruri.; 2016 [http://www.anm.ro/_/_RCP/RCP_8680_23.02.16.pdf?s_den_com=orfiril&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=24949 accesat 15.10.2015].
- Jamero D, Borghol A, Vo N, Hawawini F. The Emerging Role of NMDA Antagonists in Pain Management [accesat 01.10.2016]. Available from: http://www.medscape.com/viewarticle/744071 .
- EMA. EPAR Cymbalta.: EPAR Cymbalta; 2016 [http://www.ema.europa.eu/docs/ro_RO/document_library/EPAR_-_Product_Information/human/000572/WC500036781.pdf accesat 15.10.2016].
- Medscape Reference. Cymbalta (duloxetine) dosing, indications, interactions, adverse effects and more. [http://reference.medscape.com/drug/cymbalta-duloxetine-342960 accesat 15.10.2016].
- Medscape Reference. Catapres (clonidine) dosing, indications, interactions, adverse effects and more. [http://reference.medscape.com/drug/catapres-tts-clonidine-342382 accesat 15.10.2016].
- ANMDM. RCP Sintalgon - metadonă.; 2015 [http://www.anm.ro/_/_RCP/RCP_8411_23.11.15.pdf?s_den_com=&s_dci=methadon&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=20805 accesat 15.10.2016].
- Sinis N, Birmauer N, Gustin, Sylvia, Schwarz A, Bredanger S, et al. Memantine Treatment of Complex Regional Pain Syndrome. Clin J Pain. 2007; 23: pp. 237-243.
- ANMDM. RCP Versatis - lidocaină. [http://www.anm.ro/_/_RCP/rcp_5736_09.08.13.pdf?s_den_com=versatis&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=36722 accesat 15.10.2016].
- EMA. EPAR Qutenza.; 2015 [http://www.ema.europa.eu/docs/ro_RO/document_library/EPAR_-_Product_Information/human/000909/WC500040453.pdf accesat 10.10.2016].
- Medscape Reference. Lioresal, Gablofen (baclofen) dosing, indications, interactions, adverse effects and more. [Online]. [accesat 10.10.2016]. Available from: http://reference.medscape.com/drug/lioresal-baclofen-343335 .
- Cupp M. PL Detail-Document, Treatment of Acute Low Back Pain. Pharmacist’s Letter. 2013 December; 29(12).
- Cupp M. PL Detail-Document Appropriate Opioid Use. Pharmacist’s Letter/Prescriber’s Letter. 2016 May.
- Chou R, Fanciullo G, Fine Pea. Clinical guidelines for the use of chronic opioid therapy in chronic noncancer pain. J Pain. 2009 February; 10(2): pp. 113-130.
- ANMDM. RCP Oxycontin.; 2012 [http://www.anm.ro/_/_RCP/rcp_4282_10.02.12.pdf?s_den_com=oxycontin&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=25382 accesat 17.10.2016].
- Medscape Reference. MC Contin, Astramorph (morphine) dosind, indications, interactions, adverse effects and more. [cited 2016 October [http://reference.medscape.com/drug/ms-contin-astramorph-morphine-343319 accesat 16.10.2016].
- PHYSICIANS FOR RESPONSIBLE OPIOID PRESCRIBING. [Online]. [cited 2016 October 10. Available from: http://www.supportprop.org/wp-content/uploads/2014/01/PROP_OpioidPrescribing.pdf .
- EMA. EPAR Relistor. [http://www.ema.europa.eu/docs/ro_RO/document_library/EPAR_-_Product_Information/human/000870/WC500050562.pdfaccesat].
- Hester S. PL Detail-Document Treatment of Constipation in Adults. Pharmacist’s Letter/Prescriber’s Letter. 2015 June.
- ANMBM. RCP Sevredol - morfina. [http://www.anm.ro/_/_RCP/rcp_7772_29.12.06.pdf?s_den_com=sevredol&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=31856 accesat 10.10.2011].
- Natural Medicines in the Clinical Management of Pain. http://pharmacistsletter.therapeuticresearch.com/ce/ceCourse.aspx?cs=&s=PL&pc=15-106&pm=0&quiz=1&searchid=58499041#keywordanchor accesat 15.10.2016.
- ANMDM. RCP Wobenzym.; 2005 [http://www.anm.ro/_/_RCP/RCP_1760_08.03.01.pdf?s_den_com=wobenzym&s_dci=&s_firm_tar_d=&s_forma_farm=&s_cod_atc=&s_cim=&anmPageSize=&ID=37568 accesat 16.10.2016].
- Institutul Național de Cercetare-Dezvoltare pentru Bioresurse Alimentare - IBA București. Lista suplimentelor alimentare notificate în conformitate cu ordinul nr. 244/401/2005. [Online].; 2016 [cited 2016 October 16 [http://www.bioresurse.ro/sites/default/files/notificari/notificari244.pdf].
- Gagnier J, Chrubasik S, Manheimer E. Harpgophytum procumbens for osteoarthritis and low back pain: a systematic review.. BMC Complement Altern Med. 2004 Semptember; 15(4): p. 13.
- Vaz L. Double-blind clinical evaluation of the relative efficacy of ibuprofen and glucosamine sulphate in the management of osteoarthrosis of the knee in out-patients. Curr Med Res Opin. 1982; 8(3): pp. 145-9.
- Herrero-Beaumont G, Ivorra J, Del Carmen Trabado M, Blanco F, Benito P, Martín Mola E, et al. Glucosamine sulfate in the treatment of knee osteoarthritis symptoms: a randomized, double-blind, placebo-controlled study using acetaminophen as a side comparator. Arthritis Rheum. 2007 February; 56(2): pp. 555-67.
- Chou R. Clinical Guidelines for the Use of Chronic Opioid Therapy in Chronic Noncancer Pain [Document].; 2009.