Imunoterapeutice
Immunotherapeutics
Abstract
Lately, one of the most developed therapeutic areas has been that of drugs that display their therapeutic effects by involving the immune system. Monoclonal antibodies are the most well-known such drugs. Immunotherapeutic agents are drugs of biological origin. This feature comes along with advantages and disadvantages. The targeted mechanism of action gives them specificity. However, the risks of hypersensitivity and side effects involving the immune system should not be neglected. Immunotherapeutic agents are indicated in a wide range of diseases, from inflammatory or autoimmune diseases to cancers, but also in infections or as antidotes in drug overdoses. Antineoplastic immunotherapy uses drugs that restore the antitumor function of the immune system, affected by cancers, allowing to obtain remarkable therapeutic results, both by destroying tumor cells and by inducing a long-lasting antitumor immune response.Keywords
monoclonal antibodiesantineoplasticimmunosuppressive drugsimmunomodulatorsRezumat
Una dintre ariile terapeutice cu cea mai spectaculoasă dezvoltare în ultimii ani este cea a medicamentelor care îşi exercită efectele terapeutice prin implicarea sistemului imunitar – imunoterapeuticele. Anticorpii monoclonali sunt cele mai cunoscute astfel de medicamente. Imunoterapeuticele sunt medicamente de provenienţă biologică. Această caracteristică vine cu avantaje şi dezavantaje; faptul că acţionează ţintit le conferă specificitate de acţiune. Riscurile de hipersensibilitate şi de reacţii adverse implicând sistemul imunitar nu sunt însă de neglijat. Imunoterapeuticele sunt indicate într-o gamă largă de afecţiuni, de la boli inflamatorii sau autoimune la cancere, dar şi la infecţii ori ca antidoturi în supradozări cu medicamente. Imunoterapia antineoplazică foloseşte medicamente care restabilesc funcţia antitumorală a sistemului imunitar, afectată în cancere, permiţând obţinerea unor rezultate terapeutice remarcabile, atât prin distrugerea celulelor tumorale, cât şi prin inducerea unui răspuns imunitar antitumoral de durată.Cuvinte Cheie
anticorpi monoclonaliantineoplaziceimunosupresoareimunomodulatoareAbrevieri
ADN – Acid dezoxiribonucleic
ALK – Kinaza limfomului anaplastic
ALL – Leucemie acută limfoblastică
AM – Anticorp monoclonal
APC – Celule prezentatoare de antigen (antigen presenting cells)
APP – Autorizaţie de punere pe piaţă
CD – Clusteri de diferenţiere (cluster of differentiation)
CHOP – Schemă terapeutică antineoplazică alcătuită din ciclofosfamidă, doxorubicină, vincristină, prednisolon
CTLA – Cytotoxic T-lymphocyte antigen
EMA – Agenţia Europeană pentru Medicamente
DMARD – Antireumatice modificatoare de boală (disease modifying anti-rheumatic drugs)
EGFR – Receptori ai factorului de creştere epidermic (epidermic growth factor receptors)
ERB-B – Familie de receptori asemănători EGFR
FOLFIRI – Schemă terapeutică antineoplazică alcătuită din leucovorin (acid folinic), fluorouracil şi irinotecan
FOLFOX – Schemă terapeutică antineoplazică alcătuită din leucovorin (acid folinic), fluorouracil şi oxaliplatin
G-CSF – Factor stimulator al coloniilor de granulocite şi macrofage
GM-CSF – Factor de creştere al coloniilor de granulocite şi macrofage
HER2 – Receptorul 2 al factorului de creştere epidermică
HLA – Human leukocyte antigen (denumirea veche a MCH)
ICAM – Moleculă de adeziune intercelulară
IL – Interleukine
INF – Interferon
MCH – Complex major de histocompatibilitate (major histocompatibility complex)
NK – Celule Natural Killer – celule care determină apoptoza celulelor infectate cu patogeni sau a celulelor anormale, asigurând o parte importantă a imunităţii înnăscute
UE – Uniunea Europeană
VEGF – Factor de creştere endotelial vascular
Medicamentele care îşi manifestă efectele terapeutice folosind sau modificând mecanisme imune sunt considerate imunoterapeutice.
În această categorie, care se dezvoltă spectaculos în ultimul timp ca urmare a progreselor realizate de imunologie şi genetică, intră următoarele clase de medicamente: anticorpi monoclonali, proteine de fuziune, receptori solubili ai citokinelor, citokine recombinante(1).
Răspunsul imun şi inflamaţia
Rolul sistemului imunitar uman este de a ne proteja organismul împotriva a ceea ce este străin şi nociv (substanţe, bacterii şi virusuri), precum şi a oricăror celule anormale care ar putea apărea în corp. Pe lângă sistemul imunitar, şi alte structuri ale organismului iau parte la această apărare: bariere fizice şi chimice faţă de infecţie, precum şi mecanisme biologice şi celulare de răspuns. Prima linie de apărare împotriva microorganismelor invadatoare implică barierele fizice reprezentate de piele şi de mucoase; mucoasele sunt acoperite de secreţii vâscoase, care captează invadatorii. Enzime precum lizozimul se găsesc pe mucoase şi degradează microorganismele. Cele care reuşesc să străbată această primă linie de apărare şi pătrund în circulaţia sistemică sunt atacate de fagocite şi de celule natural killer, care acţionează nespecific, fiind componente ale imunităţii înnăscute. Frecvent, simultan se declanşează un răspuns inflamator important şi poate să apară febra, şi acestea având un rol protector. Mecanismele imunităţii dobândite se declanşează şi ele, cu implicarea limfocitelor T şi B, conducând la efecte citotoxice directe şi mediate de anticorpi, precum şi la apariţia memoriei imunitare(2).
Componentele sistemului imunitar
Antigenele
Antigenele sunt substanţele care pot induce un răspuns imunitar: molecule specifice localizate pe bacterii, virusuri, polen, plante, venin de insecte sau ţesut transplantat. Regiunea specifică a antigenului care iniţiază răspunsul imunitar se numeşte epitop. Cele mai puternice antigene sunt macromolecule complexe, de regulă proteine sau glucide. Haptenele sunt molecule mici care pot declanşa un răspuns imunitar numai după legarea de o macromoleculă‑cărăuş(2).
Complexul major de histocompatibilitate
Complexul major de histocompatibilitate (MCH – major histocompatibility complex) este un set de glicoproteine aflat pe suprafaţa celulelor, unic fiecărei persoane. Iniţial, MCH a fost denumit antigenul leucocitar uman (human leucocyte antigen; HLA) pentru că a fost prima dată identificat pe suprafaţa leucocitelor(2).
Pe celule există două tipuri distincte de MCH:
-
MCH I se găseşte pe suprafaţa tuturor celulelor nucleate ale organismului, având rolul de a le marca pe acestea ca self, pentru a nu fi atacate de sistemul imunitar. Celulele infectate cu virusuri suferă modificări la nivelul MCH I, cu exprimarea unor antigene virale, ceea ce face ca celula să fie marcată ca infectată, deci necesitând implicarea sistemului imunitar pentru a o distruge(2).
-
MCH II se află în principal pe suprafaţa macrofagelor şi a altor celule imune, având rolul de a prezenta antigenul străin altor celule ale sistemului imunitar, pentru a le activa pe acestea. Macrofagele care exprimă la suprafaţa lor antigene provenite din distrugerea patogenilor în cadrul răspunsului imunitar înnăscut, legate de MCH II, poartă numele de celule prezentatoare de antigen (APC – antigen presenting cells)(2).
Monocitele şi macrofagele
Monocitele sunt produse în măduva osoasă şi circulă pe cale sangvină, migrând în ţesuturi la nivelul leziunii. În ţesuturi, monocitele se maturează în macrofage, celule fagocitice care înglobează şi distrug patogenul şi alte particule străine, exprimând apoi la suprafaţa lor, prin intermediul MCH II, antigenele acestora. Aceste APC sunt apoi recunoscute de limfocite Thelper specifice, care ulterior activează alte limfocite pentru a ataca şi distruge orice particulă străină care exprimă acel antigen. Macrofagele produc de asemenea şi citokine, precum interleukina-1, cu rol de a potenţa răspunsul imunitar(2).
Limfocitele
Limfocitele provin din celulele stem ale măduvei osoase; în funcţie de locul unde se maturează şi de rolurile pe care le au, limfocitele sunt de două tipuri, limfocite T şi limfocite B. Limfocitele T se maturează în timus şi au rol în imunitatea mediată celular. Şi ele sunt de mai multe tipuri. Limfocitele Thelper exprimă la suprafaţa lor CD4. Clusterii de diferenţiere (CD) sunt seturi unice de proteine care identifică diferite limfocite, având rol important în comunicarea şi semnalizarea celulară. Aceste clustere de diferenţiere sunt folosite ca ţinte antigenice ale unor anticorpi monoclonali, fiind zone pe care aceste medicamente le recunosc şi de care se leagă în mod specific, declanşând efecte care duc la distrugerea acelor celule care poartă antigenul specific. Limfocitele Thelper se activează când iau contact cu antigene expuse pe APC; odată activate, secretă citokine care stimulează activitatea macrofagelor, a celulelor T citotoxice şi a celulelor NK. Tot limfocitele Thelper activate stimulează diferenţierea limfocitelor B, cu producere de anticorpi(2).
Limfocitele T citotoxice (celulele T citotoxice) exprimă pe suprafaţa lor CD8 şi sunt activate de citokine secretate de limfocitele Thelper. Recunosc şi se leagă de antigenul expus de celulele infectate prin intermediul MCH I. Celulele T citotoxice distrug direct celulele infectate, prin intermediul perforinelor, citokinelor citotoxice şi al enzimelor citolitice pe care le eliberează(2).
Limfocitele B furnizează imunitatea mediată umoral. După interacţiunea cu un antigen, sub influenţa citokinelor eliberate de celulele Thelper, limfocitele B se transformă în celule plasmatice (plasmocite) care produc anticorpi. O parte din limfocitele B activate se transformă în celule B cu memorie, care persistă mult în organism, fiind capabile ca la o ulterioară întâlnire cu antigenul specific să îl recunoască şi să secrete rapid anticorpi, asigurând un răspuns imunitar eficient şi mai rapid decât cel dezvoltat la primul contact cu antigenul(2).
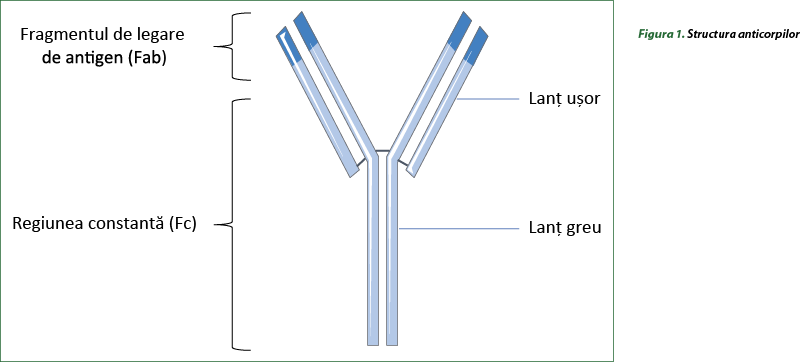
Anticorpii
Anticorpii sunt proteine globulare produse de plasmocite (limfocitele B activate). Anticorpii, denumiţi şi imunoglobuline, recunosc şi se leagă specific de antigene virale, bacteriene sau de toxine, participând la inactivarea acestora. Anticorpii sunt alcătuiţi dintr-o regiune constantă (FC) cu rol structural, aceeaşi pentru toţi anticorpii, şi o regiune variabilă (Fab – antigen binding fragment), care este porţiunea la nivelul căreia se leagă de antigenul specific (figura 1). Au fost identificate cinci clase de anticorpi:
-
IgA sunt anticorpii predominanţi în secreţii (salivă, secreţii respiratorii, lapte), asigurând protecţia mucoaselor. 10-15% dintre anticorpi sunt IgA.
-
IgG – 80% dintre anticorpii umani sunt IgG, care asigură efecte antivirale, antibacteriene şi împotriva toxinelor. IgG străbat placenta şi asigură protecţie nou-născutului în primele luni de viaţă.
-
IgM sunt cei mai mari anticorpi, având o structură pentamerică. Sunt primii anticorpi care apar în timpul răspunsului imunitar (apoi, prin recombinare isotipică, apar IgG). Aproximativ 10% dintre anticorpi sunt IgM, aceştia fiind responsabili de imunitatea naturală (cum ar fi reacţiile generate de incompatibilitatea dintre grupe sangvine).
-
IgE sunt ataşate mastocitelor şi sunt implicate în reacţii de hipersensibilitate de tip I, cu eliberare de histamină (atopiile sunt caracterizate de un răspuns exagerat mediat de IgE). Mai puţin de 1% dintre anticorpi sunt IgE.
-
IgM sunt necesari pentru maturarea limfocitelor M, rolul lor fiind încă incomplet cunoscut. Şi ei sunt în cantitate mică, reprezentând mai puţin de 1% din totalul anticorpilor(2).
Celulele natural killer (NK)
Sunt un tip nespecific de limfocite care distrug toate celulele invadatoare (cele care nu exprimă MHC I) şi pe cele infectate (care au MHC I alterat) pe care le întâlnesc, cu ajutorul substanţelor citotoxice pe care le secretă; de asemenea, eliberează citokine, care atrag alte componente ale sistemului imunitar la locul traumei. Pot distruge şi celule marcate ca periculoase, odată cu legarea de anticorpi(2).
În procesul denumit citotoxicitate celulară dependentă de anticorpi, macrofagele şi celulele NK distrug celule de care sunt legaţi anticorpi, proces declanşat de interacţiunea dintre anticorp şi receptorii Fc exprimaţi pe celulele efectoare(3).
Citokinele
Citokinele sunt proteine mici produse în principal de limfocitele T şi de macrofage. Rolurile lor sunt de comunicare intercelulară, dar şi efectoare (mediază inflamaţia, au activitate antivirală, stimulează regenerarea tisulară). Principalele citokine sunt chemokinele, interleukinele, interferonii, factorii de necroză tumorală, factorii de creştere (tisulară, vasculară etc.), factorii de stimulare a coloniilor hematopoietice. Rolurile lor în răspunsul imunitar şi modul în care sunt ele afectate de anticorpii monoclonali folosiţi în terapie vor fi detaliate pe parcursul lucrării.
Sistemul complement
Este alcătuit din peste 20 de proteine care se găsesc în plasmă în stare inactivă (zimogeni) sau care se află la suprafaţa unor celule. Activarea acestor proteine se face în cascadă, pe mai multe căi, iar funcţiile imunitare ale complementului apar prin participare la degranularea mastocitară, promovarea lizei bacteriilor şi opsonizarea sau neutralizarea bacteriilor(2).
Anticorpi monoclonali şi alte imunoterapeutice
Anticorpii monoclonali (AM) sunt imunoglobuline produse exogen pornind de la o singură celulă-părinte. AM recunosc şi se leagă de un anumit antigen specific, ceea ce îi face să fie terapii ţintite. Spre deosebire de AM, anticorpii formaţi în organism ca urmare a unei infecţii sunt anticorpi policlonali, proveniţi din celule-părinte diferite şi care se pot lega de mai mulţi determinanţi antigenici.
Medicamentele cu AM sunt preparate omogene de anticorpi sau fragmente de anticorpi în care secvenţele de proteine ale fiecărui anticorp din produs sunt identice ca secvenţă proteică şi, prin urmare, se aşteaptă ca fiecare anticorp să aibă acelaşi loc de recunoaştere de antigen, aceeaşi afinitate şi aceleaşi interacţiuni şi efecte biologice. Acest lucru distinge AM de anticorpii policlonali, care sunt secvenţe eterogene de proteine şi recunosc epitopi diferiţi de pe un antigen(4).
După modul lor de obţinere şi după caracteristicile lor, AM se clasifică în patru categorii: murini, himerici, humanizaţi şi umani.
Anticorpii monoclonali murini. Aceştia se obţin prin injectarea şoarecilor cu antigenul-ţintă, colectarea splinei animalului pentru a obţine celule B (care produc anticorpi specifici acelui antigen), fuzionarea acestor celule cu celule imortalizate de mielom de şoarece şi cultivarea acestor hibridoame, cu recoltarea anticorpilor produşi(1).
Aceste hibridoame clonate se pot propaga continuu şi pot produce cantităţi nelimitate de anticorpi monoclonali.
Utilizarea clinică a anticorpilor murini este limitată de producerea anticorpilor umani împotriva materialului provenit de la şoarece, apariţia bolii serului (un tip de reacţie de hipersensibilitate de tipul III, cu formarea de complexe imune) şi eliminarea relativ rapidă din organismul omului(1).
Pentru diminuarea acestor probleme au fost creaţi, prin tehnologia ADN‑ului recombinant, anticorpi monoclonali care conţin porţiuni umane şi porţiuni murine. După obţinerea hibridomului care produce anticorpi faţă de antigenul urmărit, ADN-ul întregului fragment variabil al anticorpului de şoarece sau numai a unei porţiuni a acestui fragment este combinat cu ADN care codează imunoglobuline umane. ADN-ul rezultat este plasat în culturi celulare care exprimă astfel gena dorită, cu producerea de AM intenţionat. Dacă întreaga porţiune variabilă provine de la şoarece, anticorpul rezultat este un anticorp himeric; dacă gena de şoarece codează numai porţiunea hipervariabilă a anticorpului, acesta este un anticorp umanizat(1).
Metoda hibridomului a condus la alte tehnologii de obţinere a anticorpilor, des folosite în prezent. Celulele producătoare de anticorpi obţinute direct de la animale sau pacienţi imunizaţi sunt izolate şi eventual modificate, iar apoi genele care codează anticorpii de interes sunt transplantate în linii celulare producătoare de anticorpi(5).
În dezvoltarea AM se pot folosi librării fagice, obţinute prin introducerea în bacteriofagi (virusuri care infectează bacteriile) a anumitor secvenţe genetice, fiecare clonă de bacteriofag producând un singur anticorp sau un singur fragment de anticorp. Colecţiile de anticorpi obţinute prin astfel de tehnici moleculare pot fi examinate in vitro pentru legarea de un antigen ţintă, alegându-se AM dorit(6).
AM umanizaţi sau cei himerici se obţin prin inginerie genetică, folosind tehnologia ADN‑ului recombinant pentru a realiza substituţii de aminoacizi care fac AM mai asemănători cu secvenţa umană. Distincţia dintre un anticorp umanizat şi unul hibrid este una fină. În general, anticorpii monoclonali himerici conţin peste 65% secvenţă umană, iar anticorpii umanizaţi, peste 90% secvenţă umană. Anticorpii himerici sunt, în general, cei în care fragmentul constant al moleculei de imunoglobulină este o secvenţă umană, iar regiunea determinantă de complementaritate – de origine animală. În anticorpii monoclonali umanizaţi, partea nonumană este şi mai redusă cantitativ, dar în continuare părţi mici, dar critice ale regiunii determinante de complementaritate sunt de provenienţă animală, iar regiunile constante mai mari ale lanţurilor grele şi uşoare de imunoglobulină sunt derivate de la om. Există în prezent tehnologii care generează anticorpi umani (complet umanizaţi), folosiţi în terapie(4).
Anticorpii bifuncţionali sau bispecifici conţin două lanţuri de imunoglobulină cu specificitate diferită care au fost fuzionate într-o singură moleculă de anticorp. Exemple de astfel de anticorpi sunt emicizumab, blinatumumab sau catumaxomab, medicamente care se pot lega de două ţinte antigenice(7).
Conjugaţii anticorp-medicament sunt complexe antigen-medicament clasic (de regulă, citostatic), care se utilizează pentru a livra un medicament sau o toxină într-un anumit loc – de exemplu, la nivelul unei tumori. Exemple de astfel de medicamente sunt inozutumab ozogamicin, brentuximab vedotin sau trastuzumab emtansin.
Proteinele fuzionate cu fragmentul cristalizabil al unei imunoglobuline umane se folosesc şi ele ca terapii ţintite biologice. Uneori, proteina are rol de receptor solubil. Exemple sunt abatacept şi etanercept(4).
Nomenclatura anticorpilor monoclonali
Numele anticorpilor monoclonali se termină cu sufixul -mab, ceea ce îi face uşor de recunoscut în multitudinea de DCI-uri. La un prefix aleator, şi distinctiv pentru fiecare anticorp, se adaugă subrădăcina A (tabelul 1), care desemnează ţinta asupra căreia acţionează anticorpul, apoi subrădăcina B (tabelul 2), care semnifică sursa anticorpului, urmată de sufixul -mab. Din 2017 s-a renunţat la cea de-a doua subrădăcină, cea care indica originea anticorpului şi modificările, pentru a nu introduce artificial ideea de superioritate a unui anticorp faţă de altul; toţi anticorpii utilizaţi în terapie sunt evaluaţi după aceleaşi standarde, iar din punct de vedere terapeutic, nu contează dacă un anticorp este himeric sau uman(8).
Deci numele anticorpului monoclonal se formează astfel:
Prefix + subrădăcina A + (subrădăcina B) + mab.
Nomenclatura anterioară anului 2017 sugera că imunogenitatea anticorpilor nonumani ar putea fi redusă într-o ordine secvenţială de la anticorpi murini la cei himerici şi apoi la cei umanizaţi prin creşterea fracţiunii de secvenţe umane. Datele experimentale nu au fost convingătoare în acest sens, de aceea s-a renunţat la subrădăcina B, fără a se modifica numele medicamentelor deja intrate în uz(8).
Mecanismul de acţiune al AM
Se leagă specific de un antigen şi în general blochează funcţia celulei care îl exprimă sau marchează celula respectivă pentru distrugere. Unii dintre AM au capacitatea de a stimula sistemul imunitar, prin ridicarea unor piedici în funcţionarea acestuia sau recrutarea altor celule imunitare şi molecule, precum sistemul complement, care participă şi ele la uciderea celulelor-ţintă.
Farmacocinetica
Anticorpii monoclonali sunt molecule mari, care se administrează parenteral, intravenos sau subcutanat.
Retenţia în ţesuturi depinde de afinitatea pentru ţintă. Cei mai mulţi AM sunt eliminaţi cu ajutorul macrofagelor reticuloendoteliale. Timpii de înjumătăţire ai AM sunt destul de variabili, de la două zile la câteva săptămâni. Ca regulă generală, anticorpii sunt relativ stabili în circulaţie şi pot fi administraţi o dată pe săptămână sau la intervale mai mari. Durata activităţii biologice poate diferi substanţial de timpul de înjumătăţire, date fiind efectele şi proprietăţile diferite ale celulei-ţintă(4).
Plasmafereza (procedura de circulaţie a sângelui unui pacient într-un sistem închis extracorporal prin care este eliminată plasma autologă, cu returnarea componentelor celulare către pacient şi transfuzia plasmei donate) şi schimbul de plasmă elimină proteinele plasmatice din sângele pacientului şi, odată cu acestea, şi AM. Acest lucru poate duce la scăderea disponibilului de AM. Hemodializa nu elimină AM din circulaţie(4).


Reacţii adverse
Reacţii adverse mediate imunologic
Reacţiile legate de administrare (perfuzie) se manifestă cu febră, frisoane, rigiditate; pot să apară hiperemie facială, angioedem, bronhospasm, vărsături, greaţă, urticarie/erupţie cutanată, fatigabilitate, cefalee, iritaţie faringiană, rinită, prurit, durere, tahicardie, hipertensiune arterială, hipotensiune arterială, dispnee, dispepsie, astenie şi aspecte ale sindromului de liză tumorală(10). De regulă, aceste reacţii adverse sunt moderate, dar pot evolua, rar, până la şoc anafilactic, care poate pune în pericol viaţa. Pentru limitarea acestor reacţii adverse de hipersensibilitate se poate face premedicaţie cu un antihistaminic H1.
Pe lângă reacţiile legate de perfuzare, alte reacţii adverse pot apărea, prin perturbarea echilibrului imunitar normal dintre activitatea imună şi toleranţa imună. AM pot avea reacţii adverse dermatologice, gastrointestinale, endocrine şi alte reacţii inflamatorii. Imunosupresia poate fi uneori severă; unele infecţii latente (hepatită B, tuberculoză) se pot reactiva. Răspunsul la vaccinare poate fi perturbat(4).
Alte efecte adverse
Unii dintre AM pot avea reacţii adverse secundare mecanismului de acţiune. De exemplu, abciximab are acţiune antiagregant plachetară care poate duce la sângerări, trastuzumab poate produce toxicitate cardiacă, despre care se crede că este legată de rolul cardioprotector mediat de HER2, iar cetuximab, un inhibitor al factorului de creştere epidermică, determină toxicitate dermatologică, cu acnee şi alte leziuni cutanate(4).
Sindromul de eliberare de citokine
Sindromul de eliberare a citokinelor este o reacţie imunitară severă, care poate apărea la persoanele tratate pentru anumite afecţiuni maligne.
În continuare, prezentăm anticorpii monoclonali şi alte imunoterapeutice, clasificate în funcţie de antigenul de care se leagă şi/sau de utilizarea terapeutică.
AM care acţionează la nivel cardiovascular
AM împotriva receptorilor glicoproteici IIb/IIIa
Abciximab
Abciximab este un AM himeric care se leagă de receptorii glicoproteici IIb/IIIa aflaţi pe suprafaţa trombocitelor, având efect antiagregant plachetar. Este indicat pentru prevenirea complicaţiilor ischemice cardiace la pacienţii supuşi intervenţiei coronare percutanate sau la anumiţi pacienţi cu risc ridicat, prezentând sindrom coronarian acut(1).
AM împotriva factorului Von Willebrand
Caplacizumab
Caplacizumab constă într-un fragment variabil bivalent cu afinitate ridicată pentru factorul Von Willebrand. Legarea sa blochează interacţiunea dintre acesta şi trombocite, care joacă un rol central în trombozele microvasculare, cum sunt cele care apar la pacienţii cu purpură trombocitopenică trombotică(4).
Caplacizumab (Cablivi®, pulb. pt. sol. inj. 10 mg) este indicat în purpura trombocitopenică trombotică dobândită, în asociere cu plasmafereză şi tratament imunosupresor(11).
AM împotriva unor factori ai coagulării
Emicizumab
Emicizumab este un AM bispecific. Acesta se leagă de doi factori ai coagulării (factorul IXa şi factorul X), luând locul factorului VIII activat (deficitar în hemofilie A) în cascada coagulării.
Emicizumab (Hemlibra®, sol. inj. 60 mg, 105 mg) este indicat în profilaxia de rutină a episoadelor de sângerare la pacienţi cu hemofilie A (deficienţă congenitală de factor VIII al coagulării), cu sau fără inhibitori de factor VIII(12).
AM împotriva proprotein convertazei subtilizin kexină tipul 9 (PCSK9)
Alirocumab şi evolocumab
Alirocumab (Praluent®, sol. inj. în seringă/stilou injectabil preumplut 75 mg, 150 mg) şi evolocumab (Repatha®, sol. inj. în pen preumplut 140 mg) sunt AM care se leagă de PCSK9 circulant, împiedicând legarea acestuia de receptorului hepatic al lipoproteinelor cu densitate scăzută (LDL). Astfel, este prevenită degradarea mediată de PCSK9 a acestor receptori pentru LDL, cu creşterea captării la nivel hepatic a LDL, deci cu creşterea metabolizării colesterolului şi cu scăderea concentraţiilor de LDL-colesterol(13).
Inhibitorii PCSK9 sunt indicaţi pentru:
-
scăderea LDL-colesterolului, ca adjuvant la dietă şi statine, la adulţi cu hipercolesterolemie heterozigotă familială sau cu boală cardiovasculară aterosclerotică (ambii);
-
reducerea riscului cardiovascular la pacienţii cu boală coronariană (evolocumab)(1).
AM împotriva unor componente aflate pe suprafaţa celulară
Mulţi dintre AM care ţintesc componente celulare se folosesc ca antineoplazice ţintite. Antigenele tumorale sunt secvenţe proteice alterate, hiperexprimate, care au suferit mutaţii, aflate pe celulele canceroase, şi care pot fi recunoscute de limfocitele T(4).
AM anti-CD19
Blinatumomab
Blinatumomab este un antineoplazic indicat în leucemii limfoblastice acute cu precursori de limfocite B care exprimă CD19. Blinatumomab este un AM bispecific, care se leagă de CD19 de pe suprafaţa celulelor B şi de clusterul de diferenţiere CD3 de pe suprafaţa limfocitelor T. Este favorizată astfel eliberarea de enzime proteolitice care distrug celula-ţintă; alte mecanisme imunologice implicate în efectul antineoplazic al blinatumomabului sunt eliberarea de citokine proinflamatorii, proliferarea limfocitelor T şi supraexpresia tranzitorie a moleculelor de adeziune celulară(14).
Blinatumomab (Blincyto®, pulb. pt. conc. pt. sol. perf. 38,5 mcg) este indicat în leucemia limfoblastică acută cu precursori de celule B(14).
AM anti-CD20
Molecula CD20 este o fosfoproteină transmembranară exprimată la nivelul limfocitelor B, în stadiul de trecere de la limfocită pre-B la limfocită B matură. Molecula CD20 este exprimată şi pe o mică parte din limfocitele T activate.
Legarea AM la CD20 induce liza celulelor B CD20+ sau a limfocitelor T. Distrugerea celulelor la care s-a legat AM se face prin citotoxicitate dependentă de complement şi, într-o măsură mai mică, prin citotoxicitate mediată celular dependentă de anticorpi. AM anti-CD20 se folosesc ca antitumorale şi imunosupresoare(15).
Rituximab
După legarea de antigenul CD20 exprimat pe limfocitele B (normale sau maligne), rituximab mediază citotoxicitatea mediată de complement şi citotoxicitatea mediată de anticorpi, cu distrugerea celulelor de care s-a legat; promovează, de asemenea, apoptoza acestor celule(10).
Rituximab (Blitzima®, MabThera®, Rixathon® conc. pt. sol. perf. 100 mg, 500 mg; MabThera® sol. inj. 1400 mg, 1600 mg(13)) este folosit ca antineoplazic în diferite cancere hematologice sau ca imunosupresor, medicament modificator de boală în afecţiuni autoimune. Este indicat în:
-
limfoame foliculare non-Hodgkin, stadiul III-IV, chimiorezistente sau care au recidivat de două sau mai multe ori după chimioterapie; se asociază cu scheme complexe cistostatice, de exemplu CHOP (ciclofosfamidă, doxorubicină, vincristină, prednisolon);
-
leucemie limfocitară cronică;
-
granulomatoză cu poliangeită (boala Wegener) şi poliangeită microscopică, în asociere cu corticosteroizi;
-
poliartrită reumatoidă, în asociere cu metotrexat;
-
pemfigus vulgar moderat-sever(10).
Obinutuzumab
Obinutuzumab (Gazyvaro®, conc. pt. sol. perf. 1000 mg) este un AM tip IgG1, recombinant, umanizat şi glicomodificat, care determină moartea directă a celulelor tumorale de care se leagă prin intermediul antigenului CD20. Distruge celulele tumorale şi prin citotoxicitate celulară şi fagocitoză, dependente de anticorpi. Modificarea prin glicoinginerie a anticorpului face ca acesta să aibă o afinitate mai mare faţă de celulele natural killer, macrofage şi monocite, mediind atacul acestora împotriva celulei tumorale(16).
Obinutuzumab este indicat în:
-
leucemie limfocitară cronică, în asociere cu clorambucil, la pacienţi netrataţi anterior şi cu comorbidităţi care nu permit administrarea unei cure complete de fludarabină;
-
limfom folicular. În forme avansate, netratate anterior, se asociază cu chimioterapie şi după inducerea răspunsului se trece la tratament de întreţinere doar cu obinutuzumab. În limfoame care nu au răspuns la tratament sau au progresat în timpul sau în interval de 6 luni după tratamentul cu rituximab, se asociază cu bendamustină(16).
Ofatumumab
Ofatumumab este un AM complet uman, care, după legare prin intermediul CD20 la limfocite B (aflate în tranziţia către forme mature) şi limfocite T, determină distrugerea acestor celule, în principal prin citotoxicitate mediată de complement(15).
Ofatumumab este indicat în:
-
leucemie limfocitară cronică (LLC) (Arzerra®, conc. pt. sol. perf. 1000 mg – retras de pe piaţă în UE);
-
LLC netratată anterior, la pacienţii la care tratamentul pe bază de fludarabină este considerat inadecvat; se asociază clorambucilului;
-
tratamentul prelungit al LLC la pacienţii cu răspuns complet sau parţial după regimuri medicamentoase pentru boală recurentă sau progresivă;
-
LLC refractară la fludarabină şi alemtuzumab;
-
LLC recidivată (utilizată cu fludarabină şi ciclofosfamidă)(13);
-
forme recidivante de scleroză multiplă (Kesimpta®)(15).
Tositumomab legat de iod radioactiv
Tositumomab radioiod este un exemplu de AM care livrează iod radioactiv celulelor canceroase, pe care le identifică precis şi de care leagă la nivelul CD20. Este indicat în limfom folicular CD20+ refractar şi recidivat şi în limfom non-Hodgkin care a progresat în timpul sau după terapia cu rituximab(1).
Ibritumomab tiuxetan
Este un AM care livrează izotopul ytriu 90 [90Y] limfocitelor B care exprimă CD20, de care se leagă; izotopul emite particule β, care distrug celulele-ţintă, dar şi celulele învecinate.
Ibritumomab tiuxetan (Zevalin®, kit pentru preparate radiofarmaceutice pentru perfuzie) este indicat, după marcare radioactivă, în:
-
limfom folicular, după inducerea remisiunii, ca terapie de consolidare;
-
limfom non-Hodgkin cu celule B, cu celule exprimând CD20, recidivant sau refractar la rituximab(17).
Ocrelizumab
Ocrelizumab este un AM umanizat care, după legare de limfocite B la nivelul CD20, determină imunomodulare prin reducerea numărului şi funcţiilor acestora.
Ocrelizumab (Ocrevus®, conc. pt. sol. perf. 300 mg) este un medicament folosit în scleroza multiplă, forme recurente sau forme primar progresive(13).
AM anti-CD22
Inotuzumab ozogamicin
Inotuzumab ozogamicin este un conjugat anticorp-medicament. Antigenul monoclonal umanizat, de tip IgG4, recunoaşte în mod specific CD22 uman. Molecula mică cu care e conjugat, N-acetil-gama-calicheamicină, este un produs citotoxic, care realizează alterări ale ADN-ului, cu oprirea ciclului celular şi moarte celulară prin apoptoză(13).
Inotuzumab ozogamicin (Besponsa®, pulb. pt. conc. pt. sol. perf. 1 mg) este indicat în leucemia acută limfoblastică recidivată sau refractară cu precursori de celule B pozitive pentru CD22, la adulţi.
AM anti-CD30
Brentuximab vedotin
Brentuximab vedotin este un complex alcătuit dintr-un anticorp monoclonal anti-CD30 şi un medicament citotoxic, monometil auristatin E, care opreşte diviziunea celulelor canceroase care exprimă proteina CD30.
Brentuximab vedotin (Adcetris®, pulb. pt. conc. pt. sol. perf. 50 mg) este indicat în:
-
limfom Hodgkin CD30+ (cazuri avansate, recidivate ori refractare);
-
limfom anaplastic cu celule mari sistemic, recidivat sau refractar;
-
limfom cutanat cu celule T(13).
AM anti-CD38
Daratumomab
Daratumomab este un AM complet uman, de tip IgG1κ, care se leagă de celulele tumorale prin intermediul CD38 exprimat la suprafaţa acestora, afectându‑le funcţii importante, precum adeziunea celulară şi activitatea de semnalizare şi enzimatică. Induce astfel liza celulelor tumorale prin citotoxicitate dependentă de complement, citotoxicitate mediată celular dependentă de anticorpi şi fagocitoza celulară dependentă de anticorpi în tumorile care exprimă CD38(13).
Daratumomab (Darzalex®, sol. inj. 1800 mg, conc. pt. sol. perf. 100 mg, 400 mg) este indicat în mielomul multiplu, în monoterapie sau asociat altor antineoplazice, în funcţie de stadiul bolii şi de istoricul medicamentelor cu care a fost tratat anterior mielomul(13).
Isatuximab
Isatuximab (Saclisa®, conc. pt. sol. perf. 100 mg, 500 mg) are un mecanism de acţiune similar daratumomabului şi se foloseşte tot în mielom multiplu(18).
AM anti-CD33
Gemtuximab ozogamicin
Gemtuximab ozogamicin este un conjugat anticorp-medicament. Gemtuximab se leagă la nivelul CD33 de blaştii mieloizi leucemici şi de celulele normale imature din linia mielomonocitară, cărora le livrează citotoxicul (N-acetil gama calicheamicina), care determină moartea celulei tumorale(19).
Gemtuximab ozogamicin (Mylotarg®, pulb. pt. conc. pt. sol. perf. 5 mg) este indicat în leucemia mieloidă acută cu CD33 pozitiv, în asociere cu daunorubicină şi citarabină, la pacienţi de peste 15 ani, netrataţi anterior; nu se foloseşte în forma promielocitară a acestei leucemii(19).
AM împotriva CD52 exprimat pe limfocitele B
Alemtuzumab
Alemtuzumab, după legare prin intermediul CD52 de pe suprafaţa celulară a limfocitelor T şi B, determină citoliză celulară dependentă de anticorpi şi liză mediată de complement, cu efect imunomodulator util în scleroza multiplă(13).
Alemtuzumab (Lemtrada®, conc. pt. sol. perf. 12 mg) este indicat în:
-
leucemie limfocitică cronică cu celule B, refractară la tratamente standard;
-
scleroză multiplă recurentă la pacienţi care au avut un răspuns inadecvat la cel puţin două medicamente anterioare(1).
AM împotriva SLAMF 7
Elotuzumab
Elotuzumab este un AM umanizat care se leagă specific de proteina membrul 7 al familiei de molecule de semnalizare a activării limfocitare (SLAMF7), proteină semnificativ crescută în mielom. Această proteină se află şi pe celulele NK şi pe alte componente ale sistemului imunitar, a căror activitate antitumorală o favorizează(20).
Elotuzumab (Empliciti®, conc. pt. sol. perf. 300 mg, 400 mg) se foloseşte în mielomul multiplu(1).
AM împotriva glicolipidei GD2
Dinutuximab
Se foloseşte în neuroblastom, în asociere cu IL-2(21). După legare de gangliozidul 2, care este bine exprimat pe celulele de neuroblastom, dinutuximab induce citotoxicitate mediată de complement şi citotoxicitate mediată de anticorpi, cu liza celulelor de care s-a legat(21).
AM împotriva RANK-ligandului
Denosumab
Denosumab este un AM uman care se leagă de ligandul RANKL, împiedicând interacţiunea acestuia cu receptorul RANK de pe suprafaţa precursorilor osteoclastelor şi a osteoclastelor. Împiedicarea acestei interacţiuni previne formarea osteoclastelor, efectele resorbtive osoase ale acestora, precum şi supravieţuirea lor(13).
Denosumab este indicat în:
-
osteoporoză (Prolia®, sol. inj. în seringă preumplută 60 mg);
-
la femei în postmenopauză şi la bărbaţi cu risc crescut;
-
tratamentul pierderii de masă osoasă după ablaţie hormonală la bărbaţi cu cancer de prostată sau asociată corticoterapiei sistemice îndelungate (Prolia®);
-
la adulţi cu cancere avansate, cu afectare osoasă, pentru prevenirea unor evenimente negative asociate sistemului osos (fractură patologică, iradiere la nivel osos, compresie la nivelul coloanei vertebrale sau intervenţie chirurgicală la nivel osos) (Xgeva®, sol. inj. 120 mg);
-
tumori osoase cu celule gigant (Xgeva®)(13).
AM anti-sclerostină
Romosozumab
Romosozumab este un AM care inhibă sclerostina, o proteină care scade formarea de masă osoasă. Romosozumab stimulează producţia matricei osoase de către osteoblaste şi determină recrutarea celulelor osteoprogenitoare. AM modifică şi expresia mediatorilor osteoclastelor, scăzând resorbţia osoasă(22).
Romosozumab (Evenity®, sol. inj. în stilou preumplut 105 mg) este indicat în osteoporoza severă la femeile în postmenopauză, cu risc crescut de fracturi(22).
Anticorpi monoclonali care acţionează împotriva unor compuşi solubili sau a receptorilor acestora
AM împotriva receptorilor factorului de creştere epidermică (EGFR)
Receptorul factorului de creştere epidermică este un receptor membranar cu activitate tirozin‑kinazică ce joacă un rol important în controlul căilor de transducţie celulară, atât în celulele normale, cât şi în cele canceroase.
Interacţiunea EGFR cu liganzii săi endogeni (factorul de creştere epidermică EGF, factorul de creştere transforming growth factor alpha, neuregulina etc.) duce la formare homodimerilor EGFR-EGFR sau a heterodimerilor alcătuiţi din EGFR şi un receptor epidermic uman HER (EGFR-HER1, EGFR-HER2 sau EGFR-HER3); formarea acestor dimeri duce la schimbări conformaţionale ale porţiunii intracelulare a EGFR, care capătă activitate tirozin-kinazică. Sunt astfel favorizate proliferarea celulară, pe calea protein‑kinazei mitogen-activate (MAPK) şi ras-activate, precum şi progresia prin ciclul celular şi supravieţuirea celulară, pe calea fosfatidilinositol‑3‑kinazei (PI3K) şi a protein‑kinazei B (Akt). Se pare că EGFR se pot transloca şi în nucleu, acţionând apoi ca factori de transcripţie(23).
Activarea receptorilor factorului de creştere epidermică EGFR a fost corelată cu progresia malignă, inducerea angiogenezei şi inhibarea apoptozei sau a morţii celulare. Acest receptor este supraexprimat într-o varietate de tumori umane: cancer de cap şi gât, sân, plămân, colorectal, prostată, rinichi, pancreas, ovar, creier şi vezică urinară(23).
AM anti‑EGFR (cetuximab, panitumumab, necitumumab) sunt anticorpi neutralizanţi care se leagă de domeniul extracelular al EGFR în starea sa inactivă; concurează cu legarea ligandului prin împiedicarea interacţiunii acestuia cu regiunea sa de legare de pe receptor şi, prin urmare, blochează activarea tirozin kinazei indusă de ligand. Aceşti AM promovează internalizarea(23).
Cetuximab
Cetuximab (Erbitux®, sol. inj. 100 mg) este un AM himeric care blochează EGFR, fiind indicat în:
cancer colorectal metastatic care prezintă gena RAS de tip sălbatic şi care exprimă EGFR, în asociere cu chimioterapia pe bază de irinotecan sau ca tratament de primă linie în combinaţie cu FOLFOX ori ca monoterapie, după eşecul tratamentului cu oxaliplatină şi irinotecan şi la pacienţii intoleranţi la irinotecan;
cancer cu celule scuamoase al capului şi gâtului, în asociere cu radioterapie (pentru boala local avansată) sau în asociere cu compuşi de platină în cancerul recurent şi/sau metastatic(24).
Panitumumab
Panitumumab (Vectibix®, conc. pt. sol. perf. 100 mg, 400 mg) este un AM de tip IgG2, în totalitate uman, recombinant, care se leagă de receptorul pentru factorul de creştere epidermică, ducând la internalizarea receptorului, la inhibarea creşterii celulare, la inducerea apoptozei şi la scăderea producerii de IL-8 şi de factor de creştere endotelial vascular(25).
Panitumumab este indicat în tratamentul cancerului metastatic de colon, la pacienţii fără mutaţii ale genei RAS(25).
Necitumumab
Necitumumab (Portrazza®, conc. pt. sol. perf. 800 mg) este indicat în neoplasmul pulmonar scuamos, altul decât cel cu celule mici, avansat local sau metastatic, care exprimă receptorul factorului de creştere epidermică; se asociază gemcitabinei şi cisplatinei(26).
AM împotriva receptorului epidermal uman 2 (HER2)
Trastuzumab
Trastuzumab este un AM umanizat, antireceptor al factorului de creştere epidermal uman 2 (HER2). Legarea trastuzumabului de acest receptor împiedică activarea lui, cu inhibarea proliferării celulelor tumorale care exprimă HER2 în exces. Celulele tumorale sunt ucise şi prin citotoxicitate mediată celular dependentă de anticorpi, fenomen stimulat de trastuzumab(27).
Trastuzumab (Herzuma®, Kanjinti®, Ogivri®, Ontruzant®, Trazimera®, Zercepac® pulb. pt. conc. pt. sol. perf. 150 mg, 420 mg) este indicat în:
-
cancerul mamar incipient sau metastatic, HER2 pozitiv, în monoterapie, în asociere sau după alte intervenţii terapeutice;
-
cancerul gastric sau al joncţiunii gastroesofagiene metastatic, care exprimă HER2 în exces(27).
-
Formularea Herceptin® în sol. inj. (600 mg/5 ml) este destinat administrării subcutanate, conţinând hialuronidază, care creşte dispersia şi absorbţia medicamentului(27).
Trastuzumab emtansinum
Trastuzumab emtansin (Kadcyla®, pulb. pt. conc. pt. sol. perf. 100 mg, 160 mg) este un conjugat anticorp-medicament, indicat în cancerul mamar incipient sau metastazat, HER2 pozitiv. Conjugarea substanţei citotoxice DM1 (un inhibitor al microtubulilor, care împiedică mitoza) la trastuzumab conferă selectivitate agentului citotoxic pentru celulele tumorale care exprimă în exces HER2, crescând astfel eliberarea intracelulară a DM1 direct în celulele maligne. După legarea de HER2, trastuzumab emtamsin suferă internalizare mediată de receptor şi degradare lizozomală, cu eliberarea cataboliţilor citotoxici care conţin DM1(28).
Pertuzumab
Pertuzumab (Perjeta®, conc. pt. sol. perf. 420 mg) este un AM umanizat, de tip IgG1, produs în celule ovariene de hamster chinezesc prin tehnologia ADN‑ului recombinant.
Pertuzumab blochează heterodimerizarea ligand-dependentă a receptorului 2 al factorului de creştere epidermal uman (HER2) cu alţi membri ai familiei HER, inclusiv EGFR, HER3 şi HER4. Ca urmare, inhibă semnalizarea intracelulară iniţiată de liganzi şi stopează creşterea celulelor şi le determină apoptoza. Cele două căi de semnalizare importante perturbate sunt MAP (protein-kinaza activată de mitogeni) şi PI3K (fosfoinositol 3-kinaza). Mediază citotoxicitatea mediată celular dependentă de anticorpi(29).
Pertuzumab este indicat în neoplasmul mamar metastatic HER2-pozitiv sau recurent local inoperabil, în asociere cu trastuzumab şi docetaxel, la adulţi netrataţi anterior cu medicamente anti-HER2 sau chimioterapie(29).
Asocierea pertuzumab cu trastuzumab majorează semnificativ activitatea antitumorală în modele de xenogrefă cu HER2 exprimat în exces. De aceea a fost dezvoltată combinaţia fixă Phesgo®, sol. inj. 600/1200 mg pertuzumab şi 600 mg trastuzumab, care este indicat în cancerul mamar HER2 pozitiv, incipient sau metastazat(30).
AM împotriva factorului de creştere endotelial vascular
Factorii de creştere ai endoteliului vascular (VEGF‑A, VEGF-B, VEGF-C şi VEGF-D) acţionează la nivelul unor receptori membranari, fiind implicaţi în angiogeneză (formarea vaselor de sânge din vase de sânge preexistente), vasodilaţie, limfangiogeneză şi chemotaxie şi se leagă de receptori. Receptorul 2 pentru factorul de creştere a endoteliului vascular (VEGF) este mediatorul principal al angiogenezei induse de VEGF.
Bevacizumab
Bevacizumab (Avastin®, Mvasi®, Zirabev® conc. pt. sol. perf. 100 mg, 400 mg) este un AM recombinant uman care se leagă de factorul de creştere endotelial vascular, inhibând angiogeneza celulelor tumorale, care sunt astfel private de aportul de sânge şi principii nutritive.
Bevacizumab are următoarele indicaţii:
-
asociat chimioterapiei pe bază de fluoropirimidine, este indicat în tratamentul de primă linie al cancerului de colon sau rect metastazat;
-
reprezintă tratamentul de primă linie al neoplasmului mamar metastazat, în asociere cu paclitaxel;
-
asociat capecitabinei, este indicat în tratamentul de primă linie al neoplasmului mamar metastazat, dacă tratamentul cu taxani sau antracicline nu este adecvat;
-
în asociere cu chimioterapie cu săruri de platină, este indicat pentru tratamentul de primă linie al neoplasmului bronhopulmonar, altul decât cel cu celule mici, diferit de tipul histologic cu celule predominant scuamoase, avansat inoperabil, metastazat sau recurent;
-
în asociere cu erlotinib, este indicat pentru tratamentul de primă linie al neoplasmului bronhopulmonar, altul decât cel cu celule mici, diferit de tipul histologic cu celule scuamoase, avansat inoperabil, metastazat sau recurent, cu mutaţii activatoare ale receptorului pentru factorul de creştere epidermal;
-
în asociere cu interferon alfa-2a, este indicat pentru tratamentul de primă linie al neoplasmului renal avansat şi/sau metastazat;
-
în asociere cu carboplatină şi paclitaxel, este indicat ca tratament de primă linie al neoplasmului ovarian epitelial, neoplasmului trompelor uterine sau neoplasmului peritoneal primar în stadii avansate;
-
în asociere cu carboplatină şi gemcitabină sau paclitaxel, este indicat pentru tratamentul primei recidive de neoplasm ovarian epitelial, neoplasm al trompelor uterine sau neoplasm peritoneal primar.
-
în asociere cu paclitaxel, topotecan sau doxorubicină lipozomală polietilenglicată, este indicat pentru tratamentul neoplasmului ovarian epitelial, neoplasmului trompelor uterine sau neoplasmului peritoneal primar, recurente, rezistente la chimioterapia cu săruri de platină, la pacienţi cărora nu li s-au administrat mai mult de două scheme chimioterapice;
-
în asociere cu paclitaxel şi cisplatină sau topotecan, este indicat pentru tratamentul carcinomului de col uterin persistent, recurent sau metastazat.
Ranibizumab
Ranibizumab (Lucentis®, sol. inj. 10 mg/ml) este fragmentul de legare de antigen al unui AM recombinant care se leagă şi inhibă factorul de creştere endotelial vascular A. Ranibizumab inhibă legarea acestui factor de creştere de receptorii săi şi suprimă neovascularizarea. Medicamentul este utilizat în tratamentul unor forme de degenerescenţă maculară legată de vârstă, când încetineşte pierderea vederii(31).
Ramucirumab
Ramucirumab (Cyramza®, conc. pt. sol. perf. 100 mg) este un AM care vizează receptorii VEGFR-2. Este indicat în:
-
neoplasm gastric în stadiu avansat sau adenocarcinom de joncţiune gastroesofagiană;
-
cancer colorectal metastatic;
-
cancer pulmonar fără celule mici, avansat la nivel local sau metastatic(13).
Aflibercept
Aflibercept este o proteină recombinantă de fuziune, formată din porţiuni ale domeniilor extracelulare ale receptorilor 1 şi 2 ai VEGF (factorul endotelial de creştere vasculară) uman, fuzionate cu porţiunea Fc a IgG1 umane. Afliberceptul acţionează ca un receptor-capcană, solubil, care se leagă de VEGF-A şi de factorul placentar de creştere (PlGF), cu afinitate superioară receptorilor naturali ai acestora şi, astfel, poate inhiba legarea şi activarea acestor receptori înrudiţi ai VEGF. Determină astfel scăderea neovascularizaţiei patologice coroidale şi scăderea îngroşării retinei.
În administrare intravitroasă, aflibercept (Eylea®, sol. inj. 40 mg/ml) este indicat în:
-
forma neovasculară de degenerescenţă maculară legată de vârstă;
-
afectarea acuităţii vizuale determinată de edemul macular secundar ocluziei venei retinei;
-
afectarea acuităţii vizuale determinată de edemul macular diabetic;
-
afectarea acuităţii vizuale determinată de neovascularizaţia coroidală miopică(13).
În administrare intravenoasă, aflibercept (Zaltrap®, conc. pt. sol. perf. 100 mg, 200 mg) este indicat în cancerul colorectal metastazat, în asociere cu schema chimioterapeutică FOLFIRI la adulţi la care boala a progresat în timpul administrării unei scheme de tratament conţinând oxaliplatină sau care sunt intoleranţi la aceasta(13).
Brolucizumab
Brolucizumab este un AM umanizat care se leagă de VEGF-A, blocând interacţiunea acestuia cu receptorii săi VEGFR-1 şi VEGFR-2. Este astfel suprimată proliferarea celulară endotelială, reducând neovascularizaţia patologică şi scăzând permeabilitatea vasculară(32).
Brolucizumab (Beovu®, sol. inj. în seringă preumplută 120 mg/ml) este indicat în forma neovasculară a degenerescenţei maculare legate de vârstă(32).
AM împotriva factorului de creştere a fibroblaştilor
Burosumab
Burosumab (Crysvita®) acţionează în metabolismul calciului şi al fosforului, fiind indicat în hipofosfatemie X-linkată, la copii şi adolescenţi în creştere. Hipofosfatemia X-linkată este o afecţiune genetică, cu supraexprimarea factorului 23 de creştere a fibroblaştilor, caracterizată de concentraţii plasmatice scăzute de fosfat şi a formei active a vitaminei D, calcitriolul, cu apariţia rahitismului(33).
Burosumab este un anticorp monoclonal IgG1 uman recombinant antifactor de creştere fibroblastic 23. După legarea de acest factor de creştere, determină reabsorbţia fosfatului la nivel renal, restabilind nivelurile normale de fosfat în sânge. Scopul tratamentului este de a corecta rahitismul sau osteomalacia, anomaliile radiografice şi deformările de la nivelul scheletului(33).
În numărul următor, vom continua discuţia despre anticorpi monoclonali şi alte medicamente biologice.
Bibliografie
-
Delves PJ. Immunitherapeutics. Last full review/revision Apr 2020. Merck Manual. Professional Version. p. https://www.merckmanuals.com/professional/immunolo.
-
Zdanowicz MM. Essentials of pathophysiology for pharmacy. Routledge; 2019. 228 p.
-
Melero I, Hervas-Stubbs S, Glennie M, Pardoll DM, Chen L. Immunostimulatory monoclonal antibodies for cancer therapy. Nat Rev Cancer. 2007;7(2):95–106.
-
Manis JP. Overview of therapeutic monoclonal antibodies. Last updated 16 Dec. 2020. www.uptodate.com.
-
Rajewsky K. The advent and rise of monoclonal antibodies. Nature. 2019;575(7781):47–9.
-
Zhao A, Tohidkia MR, Siegel DL, Coukos G, Omidi Y. Phage antibody display libraries: a powerful antibody discovery platform for immunotherapy. Crit Rev Biotechnol. 2016;36(2):276–89.
-
Cooper V, Metcalf L, Versnel J, Upton J, Walker S, Horne R. Patient-reported side effects, concerns and adherence to corticosteroid treatment for asthma, and comparison with physician estimates of side-effect prevalence: a UK-wide, cross-sectional study. NPJ Prim care Respir Med. 2015;25:15026.
-
Mayrhofer P, Kunert R. Nomenclature of humanized mAbs: Early concepts, current challenges and future perspectives. Hum Antibodies. 2019;27(1):37–51.
-
Angus DC, Birmingham MC, Balk RA, Scannon PJ, Collins D, Kruse JA, et al. E5 murine monoclonal antiendotoxin antibody in gram-negative sepsis: A randomized controlled trial. J Am Med Assoc. 2000;283(13):1723–30.
-
EMA/CHMP. MabThera (rituximab). Rezumatul caracteristicilor produsului. Ultima actualizare martie 2021.
-
EMA/CHMP. Cablivi (caplacizumab). Rezumatul caracteristicilor produsului. Ultima actualizare noiembrie 2020.
-
EMA/CHMP. Hemlibra (emicizumab). Rezumatul caracteristicilor produsului. Ultima actualizare decembrie 2020.
-
Chiriţă C, Marineci CD. Agenda medicală. Bucureşti: Editura Medicală; 2021.
-
EMA/CHMP. Blincyto (blinatumomab). Rezumatul caracteristicilor produsului. Ultima actualizare ianuarie 2021.
-
EMA/CHMP. Kesimpta (ofatumumab). Rezumatul caracteristicilor produsului. Ultima actualizare aprilie 2021.
-
EMA/CHMP. Gazyvaro (obinutuzumab). Rezumatul caracteristicilor produsului. Ultima actualizare ianuarie 2021.
-
EMA/CHMP. Zevalin (ibritumomab tiuxetan). Rezumatul caracteristicilor produsului. Ultima actualizare martie 2020.
-
EMA/CHMP. Sarclisa (isatuximab). Rezumatul caracteristicilor produsului. Ultima actualizare iunie 2020.
-
EMA/CHMP. Mylotarg (gemtuzumab ozogamicin). Rezumatul caracteristicilor produsului. Ultima actualizare decembrie 2021.
-
EMA/CHMP. Empliciti (eculizumab). Rezumatul caracteristicilor produsului. Ultima actualizare februarie 2021.
-
EMA/CHMP. Qarziba (dinutuximab). Rezumatul Caracteristicilor Produsului. Ultima actualizare ianuarie 2020.
-
EMA/CHMP. Evenity (romosozumab). Rezumatul caracteristicilor produsului. Ultima actualizare februarie 2020.
-
Martinelli E, De Palma R, Orditura M, De Vita F, Ciardiello F. Anti-epidermal growth factor receptor monoclonal antibodies in cancer therapy. Clin Exp Immunol. 2009;158(1):1–9.
-
EMA/CHMP. Erbitux (cetuximab). Rezumatul caracteristicilor produsului. Ultima actualizare ianuarie 2020.
-
EMA/CHMP. Vectibix (panitumomab). Rezumatul caracteristicilor produsului. Ultima actualizare ianuarie 2020.
-
EMA/CHMP. Portrazza (necitumumab). Rezumatul caracteristicilor produsului. Ultima actualizare decembrie 2016.
-
EMA/CHMP. Herceptin (trastuzumab). Rezumatul caracteristicilor produsului. Ultima actualizare aprilie 2021.
-
EMA/CHMP. Kadcyla (trastuzumab emtansin). Rezumatul caracteristicilor produsului. Ultima actualizare ianuarie 2020.
-
EMA/CHMP. Perjeta (pertuzumab). Rezumatul caractersticilor produsului. Ultima actualizare iunie 2020.
-
EMA/CHMP. Phesgo. Rezumatul caractersticilor produsului. Ultima actualizare ianuarie 2021.
-
EMA/CHMP. Lucentis (ranibizumab). Rezumatul caracteristicilor produsului. Ultima actualizare octombrie 2020.
-
EMA/CHMP. Beovu (brocilizumab). Rezumantul caracteristicilor produsului. Ultima actualizare februarie 2021.
-
EMA/CHMP. Crysvita (burosumab). Rezumatul caracteristicilor produsului. Ultima actualizare februarie 2021.





