Vaccinarea anti-COVID-19
COVID-19 vaccines
Abstract
The COVID-19 pandemic is the most important public health challenge facing humankind in the 3rd millennium to date. It also has myriad of economic, political and social implications. In addition to behavioral measures, vaccines are the solution to limit the number of cases of infections. The scientific community has mobilized exemplary, and with the financial and regulatory support of states, in less than a year since the sequencing of the SARS-CoV-2 genome, dozens of vaccines have reached advanced stages of clinical testing, some of which being already authorized for use in vaccination campaigns unprecedented in history. This paper reviews the anti-COVID vaccines currently in use, along with some having the potential to be authorized soon. The mechanisms of immunogenic action of vaccines and the platforms that enabled their development are discussed. Results from clinical trials investigating the efficacy and safety of vaccines are presented. The success of stopping the pandemic through vaccination currently depends on several factors. The availability of vaccines, in sufficient quantities to vaccinate billions of people, is a challenge. Some of the vaccines have restrictive storage conditions, making it difficult to use them in less developed parts of the world. People’s acceptance of immunization is also a decisive factor. The hesitant attitude towards vaccination is not a new phenomenon, and it seems that important refusal rates are also being reached towards COVID‑19 vaccination. Nondiscriminatory attitudes, nonmandatory vaccination and education campaigns are considered to be optimal strategies for increasing the acceptance rate of vaccination. In order to achieve herd immunity, it’s important that high percentages of the population be vaccinated. How high this level should be is unknown yet. Also, there are many questions that we have not yet answered. The emergence of viral variants, on which vaccines are less effective, is one of the most important impediments that have arisen against successful curbing the pandemic.Keywords
SARS-CoV-2COVID-19vaccineRezumat
Pandemia de COVID-19 este cea mai importantă provocare de sănătate publică cu care omenirea s-a confruntat în mileniul al treilea, până în prezent. Implicaţiile ei se extind inclusiv în sferele economice, politice şi sociale. Pe lângă măsurile comportamentale, vaccinurile sunt soluţia pentru limitarea numărului de îmbolnăviri şi stoparea pandemiei. Comunitatea ştiinţifică s-a mobilizat exemplar şi, cu sprijinul financiar şi de reglementare al statelor, în mai puţin de un an de la secvenţierea genomului SARS-CoV-2, zeci de vaccinuri au ajuns în faze avansate de testare clinică, câteva dintre acestea fiind deja autorizate pentru a fi folosite în campanii de vaccinare fără precedent în istorie. Lucrarea trece în revistă vaccinurile anti-COVID-19 folosite în prezent, dar şi unele cu potenţial de a fi autorizate în curând. Se discută mecanismele acţiunii imunogene ale vaccinurilor şi platformele care au permis dezvoltarea acestora. Sunt prezentate rezultate ale studiilor clinice care au investigat eficacitatea şi siguranţa vaccinurilor. Succesul stopării pandemiei prin vaccinare depinde în prezent de mai mulţi factori. Disponibilitatea vaccinurilor în cantitate suficientă pentru a fi vaccinaţi miliarde de oameni este o provocare. Unele dintre vaccinuri au condiţii de stocare restrictive, ceea ce face dificilă utilizarea lor în anumite părţi ale lumii, mai puţin dezvoltate. Acceptarea de către oameni a imunizării este de asemenea un factor decisiv. Atitudinea ezitantă faţă de vaccinare nu este un fenomen nou şi se pare că şi faţă de vaccinarea anti-COVID-19 se ating cote importante de refuz. Atitudinea nediscriminativă, neimpunerea obligativităţii vaccinării şi campaniile de educare se consideră că sunt strategiile optime de creştere a ratei de acceptare a vaccinării. Este important ca procente mari din populaţie să se vaccineze pentru a se atinge imunitatea de grup, dar încă este neclar cât de ridicat trebuie să fie acest nivel. Sunt însă multe întrebări la care nu avem încă răspuns. Apariţia variantelor virale asupra cărora vaccinurile sunt mai puţin eficiente este unul dintre cele mai importante impedimente apărute în lupta vaccinurilor cu pandemia.Cuvinte Cheie
SARS-CoV-2COVID-19vaccinVaccinurile care previn infecţia cu SARS-CoV-2 şi/sau afecţiunea produsă de acesta, COVID-19, sunt considerate cea mai promiţătoare abordare pentru a stopa pandemia declanşată în 2020 de noul tip de coronavirus. Acestea, suplimentar măsurilor de distanţare socială, de purtatul măştii, de igiena tusei şi de spălatul frecvent pe mâini, par a contribui la scăderea numărului de cazuri, cu speranţe îndreptăţite de a transforma pandemia în focare epidemice de infectări cu SARS-CoV-2.
La nivel mondial, numărul de doze de vaccin administrate depăşeşte la începutul lui martie de 2-3 ori numărul de infecţii, iar raportul creşte vertiginos de la zi la zi(1).
SARS-CoV-2
SARS-CoV-2 este un coronavirus ARN monocatenar încapsulat aparţinând familiei Coronaviridae. Coronavirusurile infectează păsările şi mamiferele, cauzând o serie de simptome, de la tulburări respiratorii la tulburări gastrointestinale. Unele coronavirusuri sezoniere relativ frecvente infectează oamenii, provocând afecţiuni respiratorii uşoare precum răceala comună. Anterior actualei pandemii, au fost raportate două epidemii cu letalitate mare cauzate de coronavirusuri umane – şi anume, sindromul respirator acut sever (SARS, cauzat de SARS-CoV-1, în 2002, cu mortalitate de aproximativ 9%) şi sindromul respirator din Orientul Mijlociu (MERS, cauzat de MERS-CoV, în 2012, cu mortalitate mai mare, de circa 40%)(2).
Epidemiologie
Până la 12 martie 2021 s-au înregistrat la nivel mondial peste 118,5 milioane de cazuri de infecţii cu SARS-CoV-2, dintre care mai mult de 2,6 milioane s-au soldat cu deces(3).
În primele două săptămâni din martie 2021, după şase săptămâni consecutive de scădere a numărului de cazuri, acesta a început să crească din nou faţă de săptămâna anterioară, cu 7% în prima săptămână (2,6 milioane de cazuri noi) şi cu 2% în cea de-a doua (2,7 milioane de cazuri noi). Numărul de decese continuă să scadă în ultimele şase săptămâni, înregistrându-se săptămânal câte o scădere de 6% faţă de săptămâna precedentă(4).
Imunitatea faţă de SARS-CoV-2
După infecţia cu SARS-CoV-2, majoritatea pacienţilor dezvoltă anticorpi produşi de limfocitele B activate în procesul imun. Aceşti anticorpi conferă imunitate antivirală prin mai multe mecanisme:
-
neutralizare virală
-
citotoxicitate celulară dependentă de anticorpi
-
fagocitoză celulară dependentă de anticorpi
-
activare a complementului dependentă de anticorpi(2).
Se crede că un nivel mai înalt al anticorpilor neutralizanţi conferă o imunitate mai bună, deşi nu se ştie în prezent cât de mare trebuie să fie titrul de anticorpi pentru a oferi imunitate şi nici cât timp persistă în sânge nivelurile protectoare de anticorpi. Citokinele, defensinele şi alţi anticorpi nespecifici pot avea şi ei un rol protector(5).
Vaccinurile anti-COVID-19 folosesc ca ţintă antigenică în principal proteina spike. Asemănător vaccinurilor clasice, sunt dezvoltate vaccinuri anti-COVID-19 care conţin fie virus viu atenuat, fie virus inactivat, fie fragmente proteice. O altă strategie de inducere a imunităţii împotriva SARS-CoV-2 este folosirea de material genetic, ADN sau ARNmesager, care comandă în organismul vaccinatului sinteza ribozomală de proteine spike, faţă de care ulterior sistemul imunitar al vaccinatului dezvoltă răspuns imun.
Situaţia la zi a autorizării vaccinurilor
Vaccinurile cu rezultate promiţătoare în testele preclinice intră în testare clinică, pe subiecţi umani. Iniţial, în studii clinice de fază 1, vaccinul este administrat unui număr mic de persoane, în general sănătoase, pentru a evalua siguranţa sa la doze diferite şi pentru a obţine informaţii iniţiale despre efectele imunogene ale acestuia la om. Dacă profilul de siguranţă al vaccinului, rezultat din studiile de fază 1, este favorabil, se trece la studii clinice de fază 2, care includ mai multe persoane, unde diferite doze sunt testate pe sute de persoane cu stare de sănătate de obicei diferită şi din diferite grupuri demografice, în studii randomizate controlate. Aceste studii oferă informaţii suplimentare privind reacţiile adverse şi riscurile asociate, examinează relaţia dintre doza administrată şi răspunsul imun şi pot furniza informaţii iniţiale privind eficacitatea vaccinului. În studii clinice de fază 3, vaccinul este administrat în general la mii de persoane în studii randomizate, controlate, care implică grupuri demografice largi (cât mai asemănătoare populaţiei destinate utilizării vaccinului) şi care generează informaţii privind eficacitatea şi date suplimentare importante privind siguranţa. Această fază oferă informaţii suplimentare despre răspunsul imun la persoanele care primesc vaccinul în comparaţie cu cele care primesc un control, cum ar fi o substanţă placebo(6).
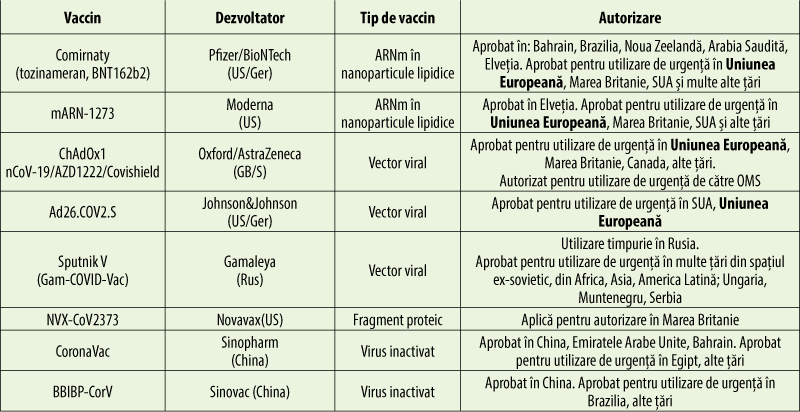
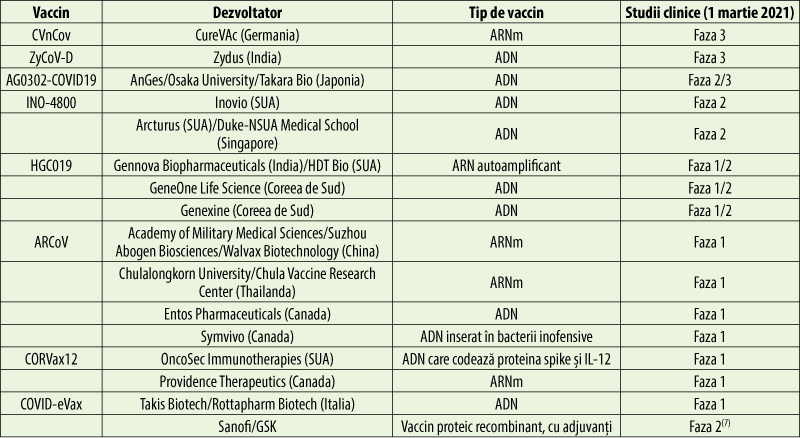
Tipuri de vaccinuri anti-COVID
Dezvoltarea vaccinurilor anti-COVID‑19 foloseşte platforme clasice de producere a vaccinurilor, dar şi tehnologii moderne, care transferă informaţie genetică.
Proteina S (spike) este antigenul imunodominant al virusului SARS-CoV-2, anticorpii neutralizanţi ataşându-se şi blocând în special domeniul de legare de receptori al subunităţii S1 a acestei proteine. Este împiedicată astfel legarea virusului de receptorul ACE2 şi consecutiv intrarea virusului în celulă. Majoritatea vaccinurilor anti-COVID-19 determină exprimarea în organismul vaccinatului a proteinei S, care declanşează răspunsul imun protector. Acesta constă în producere de anticorpi neutralizanţi şi generare de imunitate mediată de limfocitele T(8).
Vaccinuri cu virus viu atenuat
Sunt în diferite faze ale testării preclinice vaccinuri cu virus viu atenuat, incapabil de a produce boala la persoanele imunocompetente. Aceste vaccinuri sunt înalt imunogene, pentru că se replică în organismul vaccinatului; din acest motiv, nu necesită adjuvanţi în formulare. Sunt dificil de obţinut, deoarece necesită creşterea virusului în unităţi cu un grad de biosecuritate ridicat; atenuarea trebuie atent realizată, pentru a se îndepărta factorii de virulenţă(2).
Vaccinurile cu patogeni vii atenuaţi sunt în general contraindicate imunocompromişilor şi gravidelor(2). Condiţiile de păstrare sunt de asemenea restrictive în cazul acestui tip de vaccinuri, dar acest aspect logistic este oricum unul sensibil pentru toate vaccinurile anti-COVID-19 existente în prezent(2).
Teoretic, un vaccin cu virus viu atenuat destinat administrării intranazale ar putea oferi şi imunitate locală, la nivelul mucoaselor, împiedicând intrarea patogenului în organism(2).
Vaccinuri cu virus inactivat
Vaccinurile inactivate sunt produse prin creşterea virusului în unităţi de producţie cu nivel înalt de securitate biologică şi apoi omorârea sau inactivarea lui, astfel încât să nu se mai poată replica. Se poate folosi apoi întregul virus sau fragmente obţinute după dezmembrarea lui, urmând apoi separarea şi purificarea preparatului. Aceste vaccinuri sunt mai sigure decât vaccinurile cu virus viu atenuat, deoarece nu se pot replica, dar nu sunt la fel de imunogenice, de aceea necesită uzual adjuvanţi(2).
Sinopharm
Compania Farmaceutică Naţională Chineză Sinopharm şi institutele de cercetare din Wuhan şi din Beijing au dezvoltat un vaccin cu virus întreg inactivat, sigur şi imunogenic. Rezultatele studiilor clinice de fază 3 nu sunt încă disponibile, dar se pare că ar avea o eficacitate de aproximativ 80%(8).
CoronaVac
Sinovac Biotech, o companie privată chineză, a dezvoltat un vaccin cu virus inactivat pentru care studiile din Brazilia şi Turcia au arătat că are grade de protecţie diferite (în jur de 50% eficacitate în Brazilia şi peste 80% în Turcia), în parte pentru că studiile au avut un design diferit. Vaccinul este în prezent folosit în Asia şi America de Sud(1).
Vaccinuri cu proteine sau subunităţi proteice
Sunt vaccinuri care conţin proteine cu rol antigenic ale noului coronavirus. Unele vaccinuri conţin proteine întregi, iar altele, doar fragmente proteice, unele dintre ele fiind învelite în nanoparticule. Vaccinurile recombinante sunt alcătuite din proteine virale obţinute prin tehnica ADN recombinant în diferite celule (de drojdii, de insecte, de mamifere). Sunt mai uşor de produs decât vaccinurile cu patogen inactivat sau atenuat, pentru că nu necesită cultivarea virusului.
NVX-CoV2373
Vaccinul dezvoltat de compania americană Novavax conţine proteina spike introdusă într-o matrice specială. Rezultate ale unor studii clinice randomizate, placebo-controlate, încă nepublicate, dar comunicate de producător, arată următoarele rezultate ale administrării de două doze de vaccin, la 21 de zile(9):
-
în Marea Britanie, eficacitatea vaccinului a fost de 89,3% (IÎ 95%; 75,2‑95,4%, rezultate interimare); în acest studiu clinic de fază 3 au fost incluşi în jur de 15000 de adulţi, dintre care 25% de peste 65 de ani, iar datele preliminare arată că mai mult de 50% din cazurile de boală sunt atribuite variantei britanice B.1.1.7. Eficacitatea exactă a vaccinului asupra acestei variante urmează a fi investigată în continuare, rezultatele preliminare arătând că ar fi mai mare de 85%. Procentajul evenimentelor adverse care au necesitat intervenţie medicală a fost similară în rândul vaccinaţilor (2,7%) şi al celor care au primit placebo (2,8%);
-
în Africa de Sud, eficacitatea vaccinului a fost de 49,4% (IÎ 95%; 6,1‑72,8%), 93% din cazurile de COVID-19 înregistrate datorându-se variantei 501Y.V2, tulpină care determină rate mai mari de reinfectare, aproximativ o treime dintre participanţii la studiu având deja istoric de COVID-19.
Obiectivul principal evaluat în aceste studii a fost apariţia bolii COVID-19, uşoară, moderată sau severă, diagnosticată prin PCR la mai mult de 7 zile după a doua doză de vaccin(9).
Novavax lucrează deja la vaccinuri care să conţină antigene provenite de la mai multe tulpini virale, pe care intenţionează să le evalueze în studii clinice din trimestrul al II-lea din 2021(9).
Vaccinuri ARNmesager
Vaccinurile cu ARNmesager constau dintr-un fragment de catenă de ARN care codifică producerea proteinei S. Ele reprezintă o alternativă promiţătoare la modalităţile convenţionale de producere a vaccinurilor, datorită potenţei lor ridicate, capacităţii de dezvoltare rapidă şi cu costurilor reduse de producţie, care s-ar putea dovedi esenţiale pentru accesibilitatea globală a unui vaccin pandemic împotriva COVID-19. Ele au, de asemenea, un profil bun de siguranţă, deoarece acestea nu sunt realizate cu agent patogen şi nu se integrează în ADN-ul gazdei(2).
În prezent sunt autorizate pentru folosire de urgenţă, în Uniunea Europeană, Marea Britanie şi Statele Unite ale Americii, vaccinurile cu ARNmesager dezvoltate de Pfizer/BioNTech şi de Moderna.
Autorizarea de către FDA pentru folosire de urgenţă s-a bazat pe rezultate care arată că vaccinul Moderna are o eficacitate de până la 80% la două săptămâni după prima doză, iar vaccinul Pfizer/BioNTech are o eficacitate de minimumum 50% după prima doză(8).
Vaccinurile Pfizer/BioNTech şi Moderna sunt vaccinuri care conţin ARNmesager înglobat în nanoparticule lipidice. Ajuns în organismul vaccinatului, ARNmesager determină sinteza glicoproteinei spike în stare prefuzionată a SARS-CoV-2, faţă de care se declanşează răspunsul imun, astfel încât, la un contact ulterior cu virusul, organismul declanşează mult mai rapid mecanismele de apărare.
Ambele vaccinuri autorizate se administrează intramuscular, în două doze.
Intervalul recomandat între administrări este de 21 de zile pentru vaccinul Pfizer/BioNTech şi de 28 de zile, pentru vaccinul Moderna. Se recomandă administrarea celei de-a doua doze cât mai precis la aceste intervale; se admite o administrare mai devreme cu 4 zile faţă de data preconizată a celei de-a doua doze. Dacă întârzierea nu se poate evita, a doua doză trebuie totuşi administrată la maximumum 6 săptămâni după prima, în prezent existând doar date limitate privind eficacitatea acestor vaccinuri în situaţia în care a doua doză este întârziată peste această perioadă(6).
Este de urmărit evoluţia situaţiei din Marea Britanie, care a decis să amâne până la 12 săptămâni administrarea celei de-a doua doze din vaccinul Pfizer/BioNTech, cu scopul de a furniza unui număr cât mai mare de oameni protecţia oferită de prima doză de vaccin, în condiţiile în care cantitatea de vaccin nu este suficientă. Există deja voci care contestă această decizie şi cer revenirea la intervalul de trei săptămâni, care este cel validat de testele clinice de fază 3(10). Se pare că există diferenţe cantitative semnificative în ceea ce priveşte producţia şi persistenţa anticorpilor neutralizanţi: vaccinurile cu ARNm prezintă scăderi marcate ale concentraţiilor anticorpilor neutralizanţi la sfârşitul primei luni după vaccinare, la toate grupurile de vârstă, scăderi care continuă în lipsa administrării celei de-a doua doze, cu riscul unei imunităţi reduse, în special la persoanele în vârstă, fragile; se discută despre faptul dacă nu cumva această protecţie parţială creşte riscul apariţiei unor noi variante de virus.
Comirnaty (tozinameran, BNT162b2)
Vaccinul conţine ARNmesager (reprezentat de nucleozide modificate) încapsulat în nanoparticule lipidice pentru a fi protejat de biodegradarea rapidă. Este destinat persoanelor de peste 16 ani; se administrează intramuscular, preferabil în muşchiul deltoid, în două doze, la 21 de zile distanţă(11).
Într-un studiu amplu de fază 3, placebo-controlat, acest vaccin a avut o eficacitate de 95% (IÎ 95%; 90,3‑97,6%) în prevenirea, începând cu a şaptea zi după administrarea celei de-a doua doze, a COVID-19 simptomatic(12). Studiul a inclus peste 36000 de participanţi cu vârsta de minimum 16 ani, iar analiza s-a făcut după înregistrarea a 170 de cazuri confirmate de COVID-19 (8 în grupul vaccinat şi 162 în grupul placebo). Nouă din cele zece cazuri severe care au apărut în timpul studiului au fost în grupul placebo. În rândul adulţilor de peste 65 ani care au avut alte comorbidităţi sau obezitate, eficacitatea vaccinului a fost de 91,7% (IÎ 95%; 44,2‑99,8%). Incidenţa COVID-19 în grupul vaccinat a început să scadă în raport cu rata din grupul placebo la aproximativ două săptămâni după prima doză(12).
Rezultatele studiilor clinice se confirmă şi în studii observaţionale realizate după începerea campaniilor de vaccinare în diferite ţări. Într-un studiu din Israel, care a inclus aproape 570 000 de persoane vaccinate cu BNT162b2 şi un număr egal de martori nevaccinaţi cu caracteristici similare grupului vaccinat, eficacitatea estimată a vaccinului după cel puţin 7 zile de la a doua doză a fost de 92% pentru infecţia documentată cu SARS-CoV-2, 94% pentru COVID-19 simptomatic, 92% pentru COVID-19 sever şi de 87% pentru COVID-19 care a necesitat spitalizare(13).
Imunogenicitatea vaccinului se datorează inducerii de anticorpi neutralizanţi şi care împiedică legarea virusului de receptorii membranari, în concentraţii similare celor care apar în plasma convalescenţilor(14). Se pare că persoanele vaccinate cu acest vaccin dezvoltă anticorpi şi împotriva tulpinii B.1.1.7, variantă virală mai contagioasă şi mai periculoasă apărută în Marea Britanie(15); capacitatea de a dezvolta anticorpi neutralizanţi faţă de varianta B.1.351 din Africa de Sud este însă mult mai mică(16).
Reacţiile adverse evidenţiate în cazul studiilor clinice care au stat la baza autorizării acestui vaccin, la care au participat 21744 de persoane care au primit una sau două doze de vaccin, au fost următoarele:
-
foarte frecvente (frecvenţă de peste 10%): cefalee; artralgie, mialgie; durere sau tumefiere la locul administrării; fatigabilitate, frisoane, febră (cu frecvenţă mai mare după a doua doză);
-
frecvente (frecvenţă de 1-10%) – greaţă; eritem la locul administrării;
-
mai puţin frecvente (frecvenţă de 0,1-1%) – limfadenopatie; insomnie; dureri la nivelul extremităţilor; stare generală de rău; prurit la locul administrării;
-
rare (frecvenţă de 0,01-0,1%) – paralizie facială periferică acută.
-
cu frecvenţă necunoscută – anafilaxie; hipersensibilitate(11).
După vaccinarea masivă în SUA, CDC estimează că frecvenţa reacţiilor anafilactice pentru acest vaccin este de 11 cazuri la 1 milion de doze administrate(17).
mARN-1273
Într-un studiu amplu de fază 3, controlat cu placebo, realizat la aproape 30 000 de participanţi cu vârsta de 18 ani şi peste, cu o urmărire mediană de două luni după vaccinare, vaccinul dezvoltat de Moderna a avut o eficacitate în prevenirea COVID-19 simptomatic după minimum 14 zile de la a doua doză de 94,1% (IÎ 95%; 89,3‑96,8%)(18). Efectul a fost evaluat după înregistrarea a 196 de cazuri confirmate de COVID-19 (11 în grupul vaccinat şi 185 în grupul placebo). În rândul adulţilor cu vârsta peste 65 de ani, eficacitatea vaccinului a fost de 86,4% (IÎ 95%; 61,4‑95,5%). S-au înregistrat 30 de cazuri severe, toate acestea apărând în grupul placebo. Din datele raportate după urmărirea timp de o lună de la prima doză administrată a aproximativ 2 000 de participanţi, eficacitatea vaccinului după administrarea unei singure doze a fost de 80,2% (IÎ 95%; 55,2‑92,5%); din cauza duratei scurte de urmărire, durata de protecţie conferită de o singură doză rămâne incertă(18).
Siguranţa vaccinului Moderna a fost evaluată într‑un studiu clinic de fază 3 în care 15 185 de participanţi au primit vaccinul, iar 15 166 de participanţi au primit placebo. Au fost semnalate următoarele reacţii adverse:
-
foarte frecvente (frecvenţă de peste 10%) – limfadenopatie; cefalee; greaţă, vărsături; artralgie, mialgie; durere şi tumefiere la locul administrării; fatigabilitate, frisoane, febră;
-
frecvente (frecvenţă de 1-10%) – erupţii cutanate tranzitorii; eritem, urticarie sau erupţii la locul administrării;
-
mai puţin frecvente (frecvenţă de 0,1-1%) – prurit la locul administrării;
-
rare (frecvenţă de 0,01-0,1%) – paralizie facială periferică acută; tumefiere la nivelul feţei.
-
cu frecvenţă necunoscută – anafilaxie; hipersensibilitate(19).
Vaccinuri ADN
Diferite vaccinuri ADN sunt în studii clinice, pentru conferire de imunitate împotriva infecţiei cu noul coronavirus, dar şi cu alţi patogeni. Vaccinurile pe bază de ADN sunt stabile şi sigure la utilizare. Vaccinurile ADN conţin plasmide (elemente extracromozomiale care constau în fragmente mici de ADN circular) care promovează expresia proteinei-ţintă în organismul vaccinatului. Cantităţi mari de ADN plasmidic stabil pot fi generate în Escherichia coli, ceea ce constituie un avantaj major de producţie. Vaccinurile ADN au adesea imunogenitate scăzută şi au nevoie de dispozitive speciale de livrare, cum ar fi electroporatoarele (dispozitive care generează intrarea vaccinului în celule prin intermediul curentului electric, aplicat pe pielea vaccinatului), care limitează utilizarea acestora. Vaccinurile ADN conduc la inducerea celulelor CD4+ şi CD8+ şi la producţia de anticorpi specifici antigenului(2).
Vaccinuri cu vectori virali
Vectorii virali au fost utilizaţi pentru administrarea vaccinurilor datorită capacităţii lor de a infecta celulele şi de a livra produsul genetic care codează diferite proteine antigenice, pentru a produce imunitate la nivelul persoanei vacinate după administrare intramusculară de obicei. În timp ce vaccinurile cu subunităţi proteice produc o imunitate umorală mai bună, vaccinurile cu vectori virali sunt capabile să inducă o imunitate mai robustă mediată celular, suplimentar dezvoltării de anticorpi(2).
Virusurile folosite ca vectori virali sunt de obicei modificate genetic pentru a le reduce virulenţa sau a le face incompetente din punct de vedere replicativ. Adenovirusurile şi poxvirusurile sunt cei mai utilizaţi vectori virali care nu se reproduc. Adenovirusurile umane sunt cei mai frecvenţi vectori virali nonreplicativi, fiind utilizaţi pentru dezvoltarea vaccinului împotriva SARS-CoV-2. În timp ce vectorii de tip adenovirus sunt bine toleraţi şi foarte imunogeni la majoritatea oamenilor, imunitatea preexistentă la vectorul viral poate împiedica inducerea imunităţii faţă de noul coronavirus, în special după doze repetate. Adenovirusurile animale pot fi folosite ca vectori în loc de cei umani pentru a depăşi această problemă, acesta fiind motivul pentru care Universitatea Oxford/AstraZeneca a ales adenovirusul de cimpanzeu ca vector pentru vaccinul chAdOx1 nCoV-19/AZD1222)(2).
ChAdOx1 nCoV-19/AZD1222/Covishield
Universitatea din Oxford şi compania AstraZeneca au dezvoltat şi produc un vaccin cu vector viral. Un studiu clinic de fază 3 a arătat că vaccinul are o eficacitate de 82,4%, la administrarea a două doze, intramuscular, spaţiate la 12 săptămâni. Se pare că vaccinul nu protejează doar faţă de COVID-19, ci ar scădea şi transmiterea infecţiei(20).
Alte studii clinice, de fază 1 şi 2, indică răspunsuri imune importante, cu creşteri ale imunităţii celulare, marcate de creşteri ale numărului de celule T îndreptate specific împotriva SARS-CoV-2, la 1-2 săptămâni după vaccinare(10).
Analiza rezultatelor intermediare ale unui studiu randomizat multinaţional de fază 3, cu peste 11000 de participanţi, a arătat o eficacitate de 70,4% (IÎ 95%; 54,8‑80,6%) a acestui vaccin în prevenirea COVID-19 simptomatic, la cel puţin 14 zile după a doua doză. Au fost înregistrate 30 de cazuri confirmate de COVID-19 în grupul vaccinal şi 101 în grupul martor, urmărirea mediană fiind de două luni după vaccinare. 10 participanţi au fost spitalizaţi pentru COVID-19, dintre care doi au dezvoltat forme severe de boală; toţi erau în grupul de control. Un subgrup de participanţi (alcătuit din 2741 de subiecţi) a primit din greşeală o doză mai mică de vaccin pentru prima dintre cele două doze, iar eficacitatea globală a vaccinului în acest subgrup a fost mai mare, de 90% (IÎ 95%; 67,4‑97%), comparativ cu cea înregistrată la participanţii cărora li s-a administrat doza completă, la care s-a înregistrat o eficacitate de 62,1% (IÎ 95%; 41‑75,7%). Motivele acestei diferenţe sunt incerte, iar diferenţa nu este semnificativă din punct de vedere statistic. Diferenţele în ceea ce priveşte substanţa administrată lotului de control (vaccin meningococic pentru ambele doze în unele zone geografice ale studiului, faţă de vaccin meningococic pentru o doză şi ser fiziologic pentru cealaltă doză, în alte zone) şi intervalul dintre administrările celor două doze de vaccin contribuie şi mai mult la incertitudinile care planează asupra vaccinului dezvoltat de Universitatea din Oxford în colaborare cu AstraZeneca(20).
Alte studii au arătat că administrarea celei de-a doua doze la 12 săptămâni sau mai târziu după prima a fost asociată cu o eficacitate mai mare a vaccinului decât administrarea acesteia la mai puţin de 6 săptămâni (eficacitate de 81% faţă de 55%). Aceste constatări susţin prelungirea intervalului dintre administrări la 12 săptămâni(21).
Siguranţa vaccinului Oxford/AstraZeneca a fost evaluată în vederea autorizării medicamentului într‑un studiu clinic de fază 3 în care 12 021 de participanţi au primit cel puţin o doză de vaccin, iar 15 166 de participanţi au primit placebo. Au fost raportate următoarele reacţii adverse:
-
foarte frecvente (frecvenţă de peste 10%) – cefalee; greaţă; artralgie, mialgie; durere, sensibilitate, prurit, echimoze, căldură la locul administrării; fatigabilitate, frisoane, febră, stare generală de rău;
-
frecvente (frecvenţă de 1-10%) – vărsături, diaree; tumefiere, erupţii la locul administrării;
-
mai puţin frecvente (frecvenţă de 0,1-1%) – limfadenopatie; apetit alimentar scăzut; ameţeli, somnolenţă; hiperhidroză; prurit, erupţii cutanate tranzitorii;
-
rare (frecvenţă de 0,01-0,1%) – paralizie facială periferică acută; tumefiere la nivelul feţei(22).
Ad26.COV2.S
Vaccinul dezvoltat de Janssen/Johnson&Johnson este recent autorizat pentru folosire de urgenţă în SUA (27 februarie 2021) şi în Uniunea Europeană (11 martie 2021) şi este diferit de celelalte deja intrate în uz prin aceea că se administrează în doză unică. Acest lucru poate creşte mult accesibilitatea la vaccin.
Vaccinul conţine un adenovirus serotip 26 (Ad26) recombinant, incompetent replicativ. Vectorul conţine secvenţe genetice care codifică în întregime o formă stabilizată a proteinei S a SARS-CoV-2(23).
Eficacitatea vaccinului a fost evaluată într-un studiu clinic de fază 3, care a înrolat în jur de 40000 de subiecţi de peste 18 ani; după administrare în doză unică, vaccinul a avut o eficacitate de 66,9% (IÎ 95%; 59‑73,4%) în prevenirea COVID-19 moderată până la severă sau critică, după 14 zile de la vaccinare. Analiza rezultatelor s-a încheiat după raportarea a 464 de cazuri, dintre care 116 s-au înregistrat în grupul vaccinaţilor, iar 348 în grupul placebo. Eficacitatea vaccinului a variat în funcţie de regiune, ca urmare a variantelor virale dominante: 74% în Statele Unite, 66% în Brazilia (unde predomină varianta P.2) şi 52% în Africa de Sud (unde cele mai multe infecţii au fost cauzate de varianta B.1.351). Totuşi, eficacitatea vaccinului împotriva formelor severe sau critice de COVID-19 a fost similară(24).
Autorităţile de reglementare au evaluat siguranţa vaccinului Janssen/Johnson&Johnson, analizând rezultatele unui studiu clinic de fază 3 în care 21 895 de pacienţi de peste 18 ani au primit vaccinul. În acest studiu, frecvenţa de apariţie a reacţiilor adverse a fost:
-
foarte frecvente (frecvenţă de peste 10%) – cefalee; greaţă; mialgie; fatigabilitate; durere la locul administrării;
-
frecvente (frecvenţă de 1-10%) – tuse; artralgie; febră; eritem şi tumefiere la locul injectării; frisoane;
-
mai puţin frecvente (frecvenţă de 0,1-1%) – tremor; strănut, durere orofaringiană; rash, hiperhidroză; slăbiciune musculară, dureri ale extremităţilor; dureri de spate; astenie; stare generală de rău;
-
rare (frecvenţă de 0,01-0,1%) – hipersensibilitate; urticarie;
-
cu frecvenţă necunoscută – anafilaxie(25).
Sputnik V – Gam-COVID-Vac
Rezultatele unui studiu clinic de fază 3 au arătat că vaccinul produs de Gamaleya Reasearch Institute (Rusia) are o eficacitate de 91,6%(26). Vaccinul, denumit iniţial Gam-COVID-Vac, conţine o combinaţie de două adenovirusuri Ad26 (conţinut în prima doză) şi Ad5 (conţinut în a doua doză). Această folosire intenţionează să evite situaţia în care sistemul imunitar dezvoltă imunitate la vectorul viral şi îl distruge înainte ca acesta să declanşeze răspunsul imun faţă de proteinele coronavirusului, a căror sinteză este comandată de materialul genetic introdus în vectorul viral.
Vaccinul se administrează intramuscular, la un interval de trei săptămâni între doze. Se condiţionează congelat, dar în prezent se lucrează la o formulare care să fie stabilă la refrigerare. În studiul clinic de fază 3 publicat în The Lancet, grupul vaccinat nu a prezentat evenimente adverse severe semnificativ diferite faţă de grupul martor(26).
În martie 2021 vaccinul este folosit în multe ţări ale lumii, iar EMA a început evaluarea lui în vederea folosirii de urgenţă. Institutul rus de cercetare are parteneriate cu AstraZeneca pentru a cerceta dacă o eventuală combinare celor două vaccinuri poate creşte eficacitatea vaccinului AstraZeneca. A fost demarat, de asemenea, un studiu clinic pentru a testa eficacitatea unei doze unice a unei versiuni a vaccinului, denumită Sputnik Light(1).
Finalizarea seriei de vaccinare cu două doze
Până în prezent, nu sunt raportate rezultate ale unor studii clinice care să fi combinat vaccinuri diferite administrate aceleiaşi persoane, de aceea se recomandă finalizarea seriei de vaccinare cu vaccinul cu care s-a făcut prima doză, în lipsa situaţiei în care pacientul face reacţie anafilactică la vaccin, situaţie în care se poate lua în calcul administrarea celei de-a doua doze dintr-un alt vaccin, în funcţie de situaţie(6).
Calendarul vaccinării anti-COVID-19 în raport cu alte vaccinări
Deoarece deocamdată nu sunt disponibile date specifice, se recomandă ca seria de vaccinuri anti-COVID-19 să se administreze în mod obişnuit singură, cu un interval minimum de 14 zile înainte sau după administrarea oricărui alt vaccin(27).
Vaccinarea pacienţilor care au fost infectaţi cu SARS-CoV-2
Dacă în cursul COVID-19 pacienţii au fost trataţi cu plasmă de convalescent sau cu anticorpi monoclonali, vaccinarea anti-COVID-19 se face la minimum 90 de zile după un astfel de tratament(6).
Mai multe studii mici au sugerat că, după o singură doză de vaccin ARNm, persoanele cu dovezi de infecţie anterioară cu SARS-CoV-2 pot dezvolta niveluri substanţial mai mari de anticorpi blocanţi şi neutralizanţi, comparativ cu cei care nu au trecut prin infecţie. Este incert dacă această constatare se traduce printr-un răspuns protector durabil cu o singură doză de vaccin la persoanele infectate anterior(28,29).
Persoanele cu antecedente de infecţie cu SARS-CoV-2 pot prezenta, de asemenea, mai multe efecte adverse locale şi sistemice (de exemplu, febră, frisoane, mialgii, oboseală) după prima doză de vaccin decât cele care nu fost anterior infectate cu acest virus(6).
Vaccinarea anti-COVID-19 se poate întârzia la pacienţii care s-au refăcut după COVID-19, deoarece aceştia au, în primele luni după infecţie, imunitate naturală; astfel, vaccinul poate fi disponibil celor neprotejaţi. Se discută de asemenea ca o singură doză de vaccin să fie suficientă pentru a asigura imunitate celor care au făcut COVID-19, dar deocamdată nu sunt studii suficiente pentru o astfel de recomandare.
Sarcina şi alăptarea
Riscul de boală severă cauzată de infecţia cu SARS‑CoV‑2 este crescut la pacientele gravide. Decizia de vaccinare în timpul sarcinii trebuie individualizată, luând în considerare riscurile individuale de infecţie şi boală severă(6).
Nu există date care să contraindice administrarea vaccinurilor anti-COVID‑19 la gravide sau la femei care alăptează. Studiile clinice care au dus la autorizarea pentru folosirea de urgenţă a vaccinurilor anti-COVID-19 nu au inclus gravide sau femei care alăptează. Un număr foarte mic de femei au rămas gravide după ce au primit vaccinul în timpul studiilor clinice. Nu s-au semnalat probleme, dar deocamdată nu se poate trage o concluzie, deoarece sunt puţine astfel de situaţii disponibile pentru analiză.
Până în prezent, nu sunt raportate rezultate ale studiilor clinice care evaluează eficacitatea şi siguranţa vaccinării anti-COVID-19 la gravide, dar acestea sunt în desfăşurare (de exemplu, studiul NCT04754594 realizat de Pfizer/BioNTech a fost demarat la sfârşitul lui februarie 2021 şi îşi propune să înroleze aproximativ 4 000 de gravide între 24 şi 34 de săptămâni de gestaţie)(30). Studiile preclinice de toxicitate asupra procesului de reproducere şi dezvoltare embrionară arată lipsa oricăror efecte adverse la şoarece.
Nu există date privind siguranţa vaccinurilor anti-COVID-19 la femeile care alăptează sau efectele vaccinurilor asupra sugarilor alăptaţi sau asupra producţiei ori excreţiei de lapte. Deoarece vaccinurile fără virus viu atenuat nu prezintă niciun risc pentru mamele care alăptează sau pentru sugarii acestora, vaccinurile împotriva COVID-19 nu sunt considerate un risc pentru acestea. De aceea, femeile care alăptează pot alege să fie vaccinate. Iniţierea alăptării nu trebuie întârziată ca urmare a vaccinării, iar alăptarea nu trebuie întreruptă la pacienţii vaccinaţi(6).
Pacienţii imunocompromişi
Conform CDC, persoanele imunocompromise se pot vaccina împotriva COVID-19 dacă nu au vreuna dintre contraindicaţiile generale ale vaccinului ales. Pacienţii trebuie consiliaţi cu privire la profilul necunoscut de siguranţă a vaccinului şi eficacitatea în populaţiile imunocompromise, precum şi referitor la posibilitatea ca răspunsul imun dezvoltat să fie insuficient, fiind în continuare necesare masca şi distanţarea socială. Acest lucru este valabil mai ales la:
-
pacienţii cu leucemie limfocitară cronică;
-
cei care primesc în mod activ terapie cu anticorpi monoclonali anti-CD20 (rituximab, ocrelizumab), inhibitori de tirozin kinază Bruton (ibrutinib);
-
cei cu transplant de celule hematopoietice;
-
cei sub tratament cu terapii celulare, cum ar fi receptorul antigenului chimeric (CAR)-T (tisagenlecleucel)(6).
Pacienţii imunocompromişi, precum cei cărora li se administrează corticosteroizi sau medicamente anti-TNF (etanercept, infliximab, adalimumab, certolizumab, golimumab), pacienţii cu afecţiuni maligne hematologice sau pacienţii cu deficit de celule B, pot să nu prezinte răspuns imun robust după vaccinare şi/sau să aibă nevoie de vaccinări suplimentare de rapel(31). Deşi imunogenitatea şi eficacitatea vaccinurilor sunt încă incerte la aceşti pacienţi, potenţialul de COVID-19 sever la aceştia depăşeşte incertitudinile.
Conform Society for Immunotherapy of Cancer, toţi pacienţii cu cancer care primesc imunoterapie aprobată sau investigaţională ca parte a regimului lor de tratament, fie ca standard de îngrijire, fie ca parte a studiilor clinice şi fără o contraindicaţie generală la vaccinare, ar trebui sau ar putea primi vaccinare SARS-CoV-2 autorizată când le este pusă la dispoziţie(31).
Colegiul American de Reumatologie consideră că beneficiul vaccinării anti-COVID-19 pentru pacienţii cu afecţiuni reumatice sau musculoscheletale depăşeşte riscul potenţial de apariţie a autoimunităţii şi că, în absenţa alergiilor cunoscute la componentele vaccinului, nu există contraindicaţii suplimentare cunoscute pentru pacienţii cu boli reumatice autoimune şi inflamatorii. Aceşti pacienţi trebuie să discute cu medicul lor curant despre oportunitatea vaccinării şi, în funcţie de tratamentul de fond al afecţiunii, pot fi luate anumite măsuri. De exemplu, le poate fi sugerată programarea vaccinării, astfel încât seria de vaccinare să fie iniţiată cu aproximativ patru săptămâni înainte de următoarea doză programată de rituximab şi întârzierea administrării rituximabului cu două-patru săptămâni după terminarea vaccinării, dacă activitatea bolii o permite(32).
Contraindicaţii şi precauţii
Persoanelor cu alergie cunoscută la polietilenglicol, polisorbat sau alt ingredient al vaccinului le sunt contraindicate vaccinurile anti-COVID-19(6).
Vaccinarea trebuie amânată la persoanele cu boală acută severă însoţită de febră sau cu infecţie acută. Prezenţa unei infecţii minore şi/sau a febrei scăzute nu constituie un motiv de amânare a vaccinării.
Reacţii adverse. Monitorizarea, gestionarea şi raportarea acestora
După administrarea vaccinului, pacientul rămâne sub supraveghere medicală 15 minute, pentru a se monitoriza semnele şi simptomele anafilaxiei sau ale unor reacţii vasovagale datorate anxietăţii şi a se interveni prompt în cazul apariţiei acestora. Se supraveghează 30 de minute persoanele cu antecedente anafilactice, indiferent de cauză, cei cu istoric de reacţii adverse alergice, indiferent de severitate, la un vaccin sau la administrarea injectabilă a unui medicament, precum şi la cei care au contraindicaţie la un tip de vaccin anti-COVID-19 şi sunt vaccinaţi cu un alt vaccin similar(6).
Reacţii anafilactice
Apar în general la 15-30 de minute după administrarea vaccinului. În cursul monitorizării care se practică în cele 15-30 de minute după vaccinare se urmăresc:
-
senzaţia de colaps iminent;
-
simptome cutanate (prezente la aproximativ 90% din cazurile de anafilaxie) – prurit, urticarie, eritem, angioedem;
-
confuzie, dezorientare, ameţeală, slăbiciune, pierderea cunoştinţei;
-
scurtarea respiraţiei, wheezing, bronhospasm, stridor, hipoxie;
-
hipotensiune, tahicardie(6).
Pot apărea şi simptome gastrointestinale (greaţă, vomă, diaree, dureri abdominale), creşterea bruscă a secreţiilor nazale, oculare, salivare, precum şi incontinenţă urinară.
Dacă se suspectează declanşarea anafilaxiei la vaccin, se intervine de urgenţă:
-
se evaluează competenţa căilor respiratorii, respiraţia, circulaţia şi starea de conştienţă;
-
se apelează serviciile de urgenţă;
-
se poziţionează pacientul culcat, cu faţa în sus şi cu picioarele ridicate (dacă pacientul nu vomită şi nu are căile respiratorii obstruate);
-
se administrează imediat 0,3 mg (maximum 0,5 mg) de adrenalină, din seringi preumplute sau stilou autoinjector, intramuscular. Doza de adrenalină se poate repeta la fiecare 5-15 minute dacă simptomele nu se îmbunătăţesc, până la sosirea echipajului de urgenţă, căruia i se comunică cantitatea de adrenalină administrată. Dată fiind gravitatea situaţiei, în anafilaxie nu există contraindicaţii la administrarea adrenalinei(27).
Antihistaminicele şi bronhodilatatoarele nu tratează obstrucţia căilor respiratorii sau hipotensiunea arterială şi, prin urmare, nu sunt tratamente de primă linie pentru anafilaxie. Ele pot ameliora urticaria şi mâncărimea sau simptomele de detresă respiratorie şi se pot administra în anafilaxie, dar numai după adrenalină. Nu se recomandă administrarea de antihistaminice înainte de vaccinarea anti-COVID-19, deoarece nu previn anafilaxia, iar utilizarea lor profilactică poate masca simptomele cutanate, ceea ce poate duce la o întârziere în diagnosticarea şi gestionarea anafilaxiei(27).
Reacţii vasovagale
Unii dintre vaccinaţi dezvoltă în primele 15 minute după vaccinare reacţii care se datorează stimulării excesive a sistemului nervos vegetativ parasimpatic. Apar:
-
senzaţie de cald sau de frig;
-
paloare, transpiraţii, piele umedă, senzaţie căldură la nivelul feţei;
-
ameţeli, sincopă, slăbiciune, perturbarea vederii (senzaţie de lumini pâlpâitoare, vedere în tunel), modificări ale auzului;
-
tahipnee (dacă apare şi anxietate);
-
posibil bradicardie şi hipotensiune arterială în timpul sincopei;
-
greaţă, vomă(6).
Aceste simptome apar mai ales la persoanele tinere şi la cei emotivi. Nu contraindică administrarea celei de-a doua doze.
Raportarea reacţiilor adverse
Pentru evaluarea cât mai corectă a incidenţei evenimentelor nedorite asociate vaccinării anti-COVID-19, când vaccinurile se folosesc în masă, este de dorit ca raportarea reacţiilor adverse să se facă ori de câte ori acestea apar. Aşa se pot detecta şi cuantifica şi reacţiile adverse rare. Autorităţile de reglementare în domeniul medicamentului pun la dispoziţie instrumente online de raportare a acestor reacţii adverse. În România, raportarea se poate face de către pacient sau de către un furnizor de servicii de sănătate (medic, farmacist, medic dentist, asistent medical, asistent de farmacie), online, pe pagina ANMDMR https://covid19.anm.ro.
Activitatea de farmacovigilenţă este importantă, pentru că ea poate conduce la măsuri prompte. Detectarea rapidă a unor evenimente nedorite poate duce la decizii de întrerupere a administrării unui anumit vaccin, pentru investigaţii suplimentare şi cercetarea relaţiilor dintre administrarea vaccinului (sau a unui lot dintr-un vaccin) şi un anumit efect advers. Gestionarea acestor decizii este foarte importantă, pentru că, pe de o parte, se poate împiedica apariţia altor reacţii adverse similare (dacă există relaţie de cauzalitate între vaccin şi reacţia adversă), pe de altă parte se păstrează încrederea populaţiei în vaccinuri, prin transparenţa asupra întregului proces decizional. Întreruperea vaccinării nu este de dorit să se facă decât strict până la clarificarea situaţiei, pentru că altfel este întârziată realizarea protecţiei oferite de vaccinul respectiv împotriva COVID-19, într-o perioadă în care cantitatea de vaccin este oricum insuficientă pentru nevoile întregii populaţii.
Variante ale SARS-CoV-2 şi efectelor lor asupra propagării pandemiei
În decembrie 2020, o creştere neaşteptată a cazurilor raportate de COVID-19 a fost atribuită apariţiei noilor variante de SARS-CoV-2 501Y.V1 (B.1.1.7) în Marea Britanie şi 501Y.V2 (B.1.351) în Africa de Sud. Ambele variante au suferit o mutaţie în domeniul de legare de receptori al proteinelor spike, care face, probabil, virusul cu mai transmisibil. Suplimentar, varianta V2 are încă două mutaţii (E484K şi K417N) în proteina spike, care conferă potenţialul de a fi mai rezistentă faţă de anticorpi. Alte mutaţii (N501Y, E484K şi K417T) au fost identificate în Brazilia, unde circulă varianta P.1 (501Y.V3). Vaccinurile anti-COVID-19 actuale par a proteja în grade mai mici împotriva infecţiilor sau bolii produse de aceste noi variante ale SARS-CoV-2, de aceea apariţia variantelor complică şi întârzie stingerea pandemiei prin vaccinare. Se lucrează deja la variante de vaccin conţinând material genetic care să codifice proteine ale noilor variante virale(33).
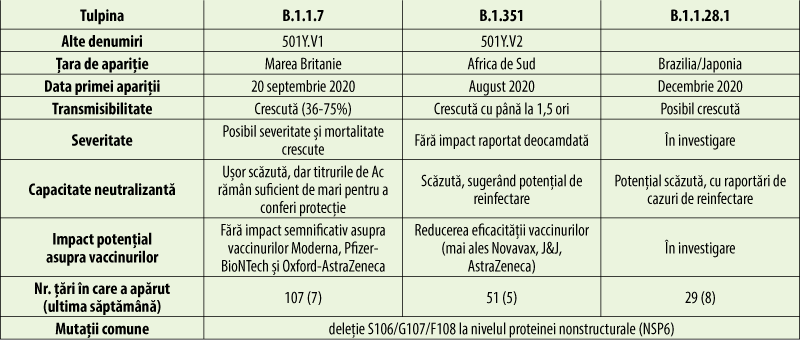
Consilierea pacientului asupra riscurilor şi beneficiilor asociate vaccinării anti-COVID‑19, asupra a ceea ce trebuie să facă pacientul şi să nu facă înainte şi după vaccinare, precum şi combaterea atitudinii ezitante faţă de vaccinare sunt alte activităţi în care farmacistul, alături de alţi profesionişti în sănătate, este dator să se implice.
Bibliografie
- Zimmer C, Corum J, Sui-Lee W. Coronavirus Vaccine Tracker. https://www.nytimes.com/interactive/2020/science/coronavirus-vaccine-tracker.html. Accesat 03/2021. New York Times. 2021.
- Flanagan KL, Best E, Crawford NW, Giles M, Koirala A, Macartney K, et al. Progress and Pitfalls in the Quest for Effective SARS-CoV-2 (COVID-19) Vaccines. Front Immunol. 2020;11:2410.
- COVID-19 Dashboard, Center for Systems Science and Engineering, Johns Hopkins University; https://www.arcgis.com/apps/opsdashboard/index.html#/bda7594740fd40299423467b48e9ecf6. Accesat 03/2021.
- WHO. Weekly epidemiological update - 09 March 2021. https://www.who.int/publications/m/item/weekly-epidemiological-update---2-march-2021. Accesat 03/2021.
- Rojas M, Rodríguez Y, Monsalve DM, Acosta-Ampudia Y, Camacho B, Gallo JE, et al. Convalescent plasma in COVID-19: Possible mechanisms of action. Autoimmun Rev. 2020;19(7):102554.
- CDC. Interim Clinical Considerations for Use of COVID-19 Vaccines. https://www.cdc.gov/vaccines/covid-19/info-by-product/clinical-considerations.html. Accesat 03/2021.
- Sanofi. Updates on our COVID-19 Vaccines - Sanofi. https://www.sanofi.com/en/our-covid-19-vaccine-candidates. Accesat 03/2021.
- Creech CB, Walker SC, Samuels RJ. SARS-CoV-2 Vaccines. JAMA. 2021; Feb.26.
- Novavax. Announcement of UK and South Africa Trial Results. https://www.novavax.com/sites/default/files/2021-01/UK-SouthAfrica-Trial-Results--FINAL.pdf. Accesat 03/2021.
- Robertson JFR, Sewell HF, Stewart M. Delayed second dose of the BNT162b2 vaccine: innovation or misguided conjecture? Lancet (London, England). 2021;397(10277):879–80.
- CHMP. EPAR Comirnaty, INN-COVID-19 mRNA Vaccine (nucleoside-modified). Last update 25.02.2021.
- Polack FP, Thomas SJ, Kitchin N, Absalon J, Gurtman A, Lockhart S, et al. Safety and Efficacy of the BNT162b2 mRNA COVID-19 Vaccine. N Engl J Med. 2020;383(27):2603–15.
- Dagan N, Barda N, Kepten E, Miron O, Perchik S, Katz MA, et al. BNT162b2 mRNA COVID-19 Vaccine in a Nationwide Mass Vaccination Setting. N Engl J Med. 2021;NEJMoa2101765.
- Walsh EE, Frenck RW, Falsey AR, Kitchin N, Absalon J, Gurtman A, et al. Safety and Immunogenicity of Two RNA-Based COVID-19 Vaccine Candidates. N Engl J Med. 2020;383(25):2439–50.
- Muik A, Wallisch A-K, Sänger B, Swanson KA, Mühl J, Chen W, et al. Neutralization of SARS-CoV-2 lineage B.1.1.7 pseudovirus by BNT162b2 vaccine-elicited human sera. Science. 2021;371(6534):1152–3.
- Zhou D, Dejnirattisai W, Supasa P, Liu C, Mentzer AJ, Ginn HM, et al. Evidence of escape of SARS-CoV-2 variant B.1.351 from natural and vaccine induced sera. Cell. 2021; Feb 23.
- CDC. Allergic Reactions Including Anaphylaxis After Receipt of the First Dose of Pfizer-BioNTech COVID-19 Vaccine – United States, December 14–23, 2020. MMWR Morb Mortal Wkly Rep. 2021;70(2):46–51.
- Baden LR, El Sahly HM, Essink B, Kotloff K, Frey S, Novak R, et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. N Engl J Med. 2021;384(5):403–16.
- CHMP. EPAR. COVID-19 Vaccine Moderna, Common name-COVID-19 mRNA Vaccine (nucleoside modified). Last update 26.01.2021.
- Voysey M, Clemens SAC, Madhi SA, Weckx LY, Folegatti PM, Aley PK, et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet. 2021;397(10269):99–111.
- Voysey M, Costa Clemens SA, Madhi SA, Weckx LY, Folegatti PM, Aley PK, et al. Single-dose administration and the influence of the timing of the booster dose on immunogenicity and efficacy of ChAdOx1 nCoV-19 (AZD1222) vaccine: a pooled analysis of four randomised trials. Lancet (London, England). 2021;397(10277):881–91.
- CHMP. EPAR. COVID-19 Vaccine AstraZeneca, COVID 19 Vaccine (ChAdOx1 S [recombinant]). Last update 26.01.2021.
- Sadoff J, Le Gars M, Shukarev G, Heerwegh D, Truyers C, Groot AM de, et al. Interim Results of a Phase 1–2a Trial of Ad26.COV2.S COVID-19 Vaccine. N Eng J Med. 2021; https://doi.org/101056/NEJMoa2034201.
- Vaccines and Related Biological Products Advisory Committee February 26 2021 Meeting Briefing Document- FDA. FDA Briefing Document. Janssen AD26.COV2.2 Vaccine for tha Prevention of COVID-19. 2021.
- CHMP. EPAR: COVID-19 vaccine Janssen 5737 - PI_clean_EN. Last update 11.03.2021.
- Logunov DY, Dolzhikova IV, Shcheblyakov DV, Tukhvatulin AI, Zubkova OV, Dzharullaeva AS, et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. Lancet (London, England). 2021;397(10275):671–81.
- CDC. Interim Considerations: Preparing for the Potential Management of Anaphylaxis after COVID-19 Vaccination (last updated March 3, 2021). https://www.cdc.gov/vaccines/covid-19/clinical-considerations/managing-anaphylaxis.html. Accesat 03.2021.
- Saadat S, Tehrani ZR, Logue J, Newman M, Frieman MB, Harris AD, et al. Binding and Neutralization Antibody Titers After a Single Vaccine Dose in Health Care Workers Previously Infected With SARS-CoV-2. JAMA. 2021;
- Prendecki M, Clarke C, Brown J, Cox A, Gleeson S, Guckian M, et al. Effect of previous SARS-CoV-2 infection on humoral and T-cell responses to single-dose BNT162b2 vaccine. Lancet (London, England). 2021;
- Www.clinicaltrials.com. https://www.clinicaltrials.gov/ct2/results?recrs=ab&cond=&term=NCT04754594&cntry=&state=&city=&dist=. https://www.clinicaltrials.gov/ct2/results?recrs=a. https://www.clinicaltrials.gov/ct2/results?recrs=ab&cond=&term=NCT04754594&cntry=&state=&city=&dist=. Accesat 03/2021.
- SITC Statement on SARS-CoV-2 Vaccination and Cancer Immunotherapy - Society for Immunotherapy of Cancer (SITC). https://www.sitcancer.org/aboutsitc/press-releases/2020/sitc-statement-sars-cov-2-vaccination-cancer-immunotherapy. Accesat 03/2021.
- American College for Rheumatology. COVID-19 Vaccine Clinical Guidance Summary for Patients with Rheumatic and Musculoskeletal Diseases. https://www.rheumatology.org/Portals/0/Files/COVID-19-Vaccine-Clinical-Guidance-Rheumatic-Diseases-Summary.pdf. Accesat 03/2021.
- Fontanet A, Autran B, Lina B, Kieny MP, Karim SSA, Sridhar D. SARS-CoV-2 variants and ending the COVID-19 pandemic. Lancet (London, England). 2021;397(10278):952–4.





