Background. Antiretroviral treatment represents the corner-stone of a better life quality and for preventing transmission in HIV infected persons. It is still at debate the effect on children born to HIV infected women, exposed to HIV, to other associated infections and to antiretrovirals. Materials and Methods. We analyzed the birth defects in perinatal HIV exposed children followed-up for 7 years. We assessed: child gender, mother’s age at birth, exposure to antiretroviral before and during pregnancy. Results. Among 244 studied children we identified 10 cases of severe malformations: complex heart defect, Hirschsprung disease, anal imperforation, Dandy Walker Syndrome, gangliosidosis, Niemann Pick syndrome, true hermaphroditism, congenital mixedema, gastroschisis and cleft lip. Two children died during first year of life due to malformations. None of the children with severe birth defects were HIV infected. Conclusion. The rate of severe birth defects in studied children was relatively high. Better strategies for the prevention of congenital anomalies are needed.
Defecte congenitale severe la copiii expuşi vertical la infecţia HIV. Serie de cazuri
Severe birth defects in HIV verically exposed children. Case series
First published: 15 septembrie 2015
Editorial Group: MEDICHUB MEDIA
Abstract
Rezumat
Introducere. Tratamentul antiretroviral reprezintă piatra de temelie pentru o mai bună calitate a vieţii şi pentru prevenirea transmiterii infecţiei HIV. Este încă în discuţie efectul asupra copiilor expuşi HIV, precum şi la alte infecţii asociate sau la antiretrovirale. Material şi metodă. Am analizat defectele congenitale apărute la copiii expuşi perinatal HIV pe o perioadă de 7 ani. Am luat în considerare: sexul copilului, vârsta mamei la naştere, expunerea la antiretrovirale înainte şi în cursul sarcinii. Rezultate. Din 244 de copii studiaţi am identificat 10 cazuri de malformaţii severe: respectiv câte un caz de malformaţie cardiacă complexă, boală Hirschsprung, imperforaţie anală, sindrom Dandy Walker, gangliozidoză, sindrom Niemann Pick, hermafroditism adevărat, mixedem congenital, gastroschizis şi cheiloschizis. Concluzii. Rata malformaţiilor congenitale severe a fost relativ crescută la pacienţii studiaţi. Este necesară îmbunătăţirea strategiilor de prevenire a malformaţiilor.
Introducere
Introducerea terapiei antiretrovirale combinate (cART) a reprezentat un moment de cotitură pentru pacienţii cu infecţie HIV, deoarece a determinat creşterea supravieţuirii prin scăderea mortalităţii şi morbidităţii acestei afecţiuni, precum şi scăderea riscului de transmitere orizontală şi verticală a HIV(1,2).
Utilizarea medicamentelor antiretrovirale este grevată de reacţii adverse care pot apărea la începutul terapiei, dar şi după mai mulţi ani, având în vedere că terapia infecţiei HIV este un tratament cronic pe toată durata vieţii(3,4).
Una din problemele importante legate de reacţiile adverse ale terapiei antiretrovirale este efectul teratogen al acestora, având în vedere că aceste medicamente sunt recomandate în sarcină pentru prevenirea transmiterii infecţiei la produsul de concepţie.
Pe acest subiect au fost publicate date contradictorii. Un studiu de cohortă derulat în Franţa a cuprins peste 13.000 de nou-născuţi de mame seropozitive care au fost monitorizate în 90 de centre între anii 1994 şi 2010. Cercetătorii francezi au arătat că există un risc mai mare de defecte congenitale cardiace în cazul copiilor expuşi din primul trimestru de sarcină la zidovudină, medicament care este recomandat încă de la începutul anilor 1990 pentru profilaxia transmiterii verticale HIV(5).
De asemenea, autorii francezi au evidenţiat o asociere semnificativă între utilizarea efavirenzului în primul trimestru de sarcină şi defectele congenitale de tub neural, motiv pentru care această moleculă nu este recomandată în sarcină de ghidurile europene de tratament(6).
Un alt studiu publicat de cercetători italieni cuprinzând peste 1.200 de copii evaluaţi între 2001 şi 2011 nu a găsit asociere semnificativă din punct de vedere statistic între nici unul din medicamentele antiretrovirale şi malformaţii la copii născuţi de femei HIV pozitive(7).
În acest articol ne propunem să prezentăm experienţa Secţiei de Imunodepresie Copii din cadrul Institutului Naţional de Boli Infecţioase „Matei Balş”, Bucureşti, privind defectele congenitale severe la copiii expuşi perinatal infecţiei HIV şi la medicaţia antiretrovirală.
Material şi metodă
Am analizat datele consemnate în foile de observaţie ale tuturor copiilor născuţi în perioada 1 ianuarie 2006 - 31 decembrie 2012 de femei diagnosticate cu infecţie HIV şi evaluaţi în clinica noastră. Diagnosticul de infecţie HIV în cazul mamelor s-a bazat pe două teste ELISA şi confirmare western blot. Conform Ghidului Naţional de Management al Infecţiei HIV, copiii născuţi de femei HIV pozitive sunt evaluaţi periodic timp de 18 luni postnatal. Diagnosticul de copil expus, dar neinfectat HIV se bazează pe negativarea testelor serologice ELISA pentru HIV în decursul a 18 luni după naştere şi niveluri ale ARN HIV nedetectabile la toate evaluările. Diagnosticul de infecţie HIV cu transmitere verticală de la mamă la copil a fost susţinut de niveluri detectabile ale ARN HIV în ser la oricare dintre determinările efectuate postnatal la copii. Informaţiile extrase din documentele medicale au fost: sexul copilului, data naşterii, date clinice privind defecte congenitale, investigaţii imagistice care să susţină diagnosticul malformaţiilor identificate clinic, teste ELISA şi determinarea nivelului ARN HIV periodic 18 luni postnatal. În ceea ce priveşte mamele copiilor studiaţi am notat: vârsta la momentul naşterii, istoricul infecţiei HIV şi cel terapeutic.
Am identificat copii cu defecte congenitale severe, respectiv cele care pun în pericol viaţa pacienţilor sau au impact important asupra stării de sănătate folosind definiţia şi clasificarea Centrului pentru Controlul şi Prevenirea Bolilor din Statele Unite ale Americii (CDC pentru anomaliile congenitale majore(8,9,10)).
Menţionăm că măsurile de prevenire a transmiterii verticale a infecţiei HIV conform Ghidului Naţional şi al celui European(6,11) cuprind: tratamentul antiretroviral al femeii gravide, naştere prin cezariană programată, interzicerea alăptării şi administrarea de zidovudină şi lamivudină nou-născutului timp de 6 săptămâni imediat după naştere. De asemenea, copiii sunt monitorizaţi periodic până la vârsta de 18 luni, aşa cum am precizat anterior.
Rezultate şi discuţii
Am identificat 244 de copii expuşi perinatal infecţiei HIV născuţi în perioada 1.01.2006 - 31.12.2012 care au fost evaluaţi în clinica noastră. Rata globală a malformaţiilor a fost de 39,34% (96/244), cele mai frecvente fiind cele cardiovasculare (47/96 cazuri), reprezentând aproximativ jumătate din totalul malformaţiilor, urmate de cele musculoscheletale (24/96), neurologice (20/96), urogenitale (13/96) , cele mai rare fiind cele digestive (3/96), metabolice (2/96) şi alte anomaliile cromozomiale (2/96). Aceste date au fost deja publicate, fiind prezentate la Conferinţa privind Terapia HIV care a avut loc la Glasgow, Marea Britanie, în noiembrie 2014(12).
Folosind definiţia CDC pentru malformaţii severe pe parcursul celor 7 ani, am identificat 10 copii cu malformaţii severe: un caz de cheiloschizis, un caz de hermafroditism adevărat, unul de gangliozidoză, un caz de megacolon aganglionic congenital total (boala Hirschsprung), unul de imperforaţie anală, unul de malformaţie cardiacă complexă, un caz de agenezie de corp calos (sindrom Dandy Walker), un caz de boală lipozomală (sindrom Niemann Pick) şi un caz de mixedem congenital. Precizăm că nici unul din aceşti copii cu malformaţii severe nu a asociat şi infecţie HIV, toţi fiind seronegativi şi cu ARN HIV nedetectabil la vârsta de 18 luni.
Cazul 1. Pacientul diagnosticat cu cheiloschizis şi malformaţii ale pavilionului urechii drepte este un băiat născut în anul 2006 la termen, prin operaţie cezariană programată şi cu greutate normală la naştere (3.000 g). Mama copilului avea vârsta de 17 ani la naştere, fiind diagnosticată cu infecţie HIV cu doi ani anterior. Pacienta nu a fost aderentă la tratament antiretroviral pe parcursul sarcinii, astfel că am considerat cazul neexpus la medicaţie.
Factorii de risc asociaţi cazurilor de cheiloschizis sunt genetici, factori de mediu la care femeia gravidă este expusă, cum ar fi fumatul şi unele medicamente neurotrope (acid valproic) în primul trimestru de sarcină, sau diabetul matern. Nici unul dintre aceşti factori nu a fost identificat în acest caz(2).
Rata cazurilor de cheiloschizis în Statele Unite ale Americii este de 6,45(2), iar în Europa, de aproximativ 8 cazuri la 10.000 de naşteri(13). În ceea ce priveşte rata în România, nu sunt publicate date recente, riscul fiind apreciat de aproximativ 3%(14).
Cazul 2. Al doilea caz este o fetiţă născută în anul 2007, de asemenea la termen, prin operaţie cezariană programată, cu greutate normală (2.500 g). Mama a născut la vârsta de 23 de ani, la aproximativ 3 ani de la diagnosticarea cu infecţie HIV şi a primit tratament pe parcursul sarcinii, iniţiat de la diagnostic cu combinaţia în doză fixă zidovudină, lamivudină la care s-a asociat nelfinavir (conform Ghidului de tratament al infecţiei HIV la momentul diagnosticului şi la momentul naşterii). Copilul a fost diagnosticat cu sindrom Niemann Pick pe baza medulogramei şi a manifestărilor clinice: hepatosplenomegalie şi retard psihomotor evidenţiat încă din prima lună de viaţă.
Sindromul Niemann Pick este o tezaurismoză transmisă autozomal recesiv, foarte rară 1/120.000 naşteri(15), care este caracterizată de manifestări viscerale, neurologice şi psihiatrice(16), iar tratamentul actual vizează numai încetinirea evoluţiei bolii. În cazul prezentat de noi, evoluţia este marcată de întârziere de dezvoltare neuromotorie, dar prognosticul pe termen lung este rezervat, supravieţuirea fiind de până la maximum 25 de ani(16).
Cazul 3. Băiat născut în anul 2011 la termen, prin operaţie cezariană programată, cu greutate la naştere de 3.300 g, la examenul clinic la naştere prezenta perimetru cranian crescut, motiv pentru care se efectuează ecografie transfontanelară, care evidenţiază malformaţie cerebrală complexă: agenezie corp calos, dilatare moderată a ventriculilor trei şi patru, hipoplazie vermis cerebelos, fosa posterioară de dimensiuni crescute, modificări caracteristice sindromului Dandy-Walker (figura 1). Evaluarea neurologică în dinamică în primul an de viaţă arată retard neuropsihomotor moderat, fără semne de hipertensiune intracraniană. Electroencefalograma efectuată la vârsta de un an a evidenţiat descărcări de unde delta. Pacientul a rămas în supraveghere neurochirurgicală.
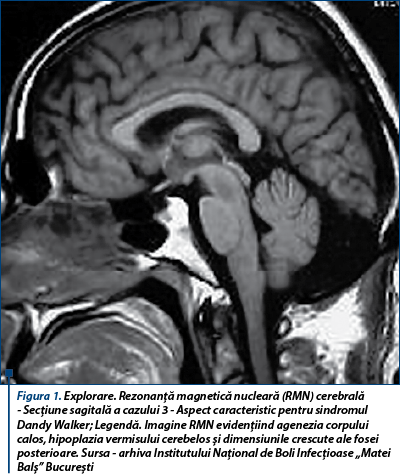
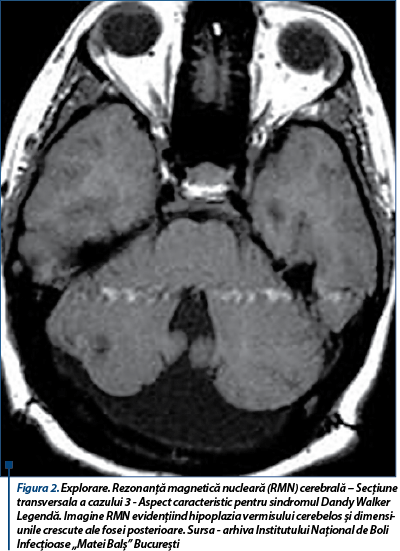
Mama copilului a născut la vârsta de 21 de ani, fiind diagnosticată cu infecţie HIV şi hepatită cronică B de la vârsta de 14 ani, fiind în tratament antiretroviral cu zidovudină, lamivudină şi nevirapină, medicamente recomandate gravidelor şi nici unul dintre ele nu a fost asociat cu anomalii cerebrale. Menţionăm că tatăl copilului este şi el seropozitiv HIV.
Rata acestei malformaţii este de aproximativ 1/30.000 naşteri(17). Deşi este cea mai frecventă malformaţie cerebeloasă, nu au fost identificate gene specifice. Rata scăzută a incidenţei bolii în familiile pacienţilor sugerează un determinism poligenic(18). Boala poate avea manifestări clinice variabile, de la uşoare la severe, fiind marcată de ataxie cerebeloasă, jumătate dintre cazuri având retard psihomotor şi uneori şi hidrocefalie, semne clinice prezente la cazul prezentat mai sus(19).
Cazul 4. În continuare vă prezentăm cazul unui copil de sex masculin născut în anul 2009, la termen, cu greutatea de 3.900 g, prin operaţie cezariană programată. A fost diagnosticat cu malformaţie cardiacă complexă pe baza semnelor clinice şi a investigaţiilor imagistice. Ecografia cardiacă efectuată la vârsta de două săptămâni a arătat: diametrul ventriculului stâng (VS) - 17 mm, al ventricului drept (VD) - 14 mm, diametrul aortei la nivelul inelului - 11 mm, grosimea septului interventricular - 5 mm, defect septal ventricular mic perimembranar - 2 mm, grosimea peretelui posterior al VS - 5 mm, valve sigmoide aortice displazice cu flux turbulent transvalvular cu gradient de 116 mmHg, la nivelul tractului de ieşire al VS se observă o zonă de hipertrofie musculară de 4 mm, precum şi aspect de foramen ovale patent. Concluzie: stenoză aortică subvalvulară şi valvulară, hipertrofie biventriculară, hipertrofie de sept interventricular, defect septal ventricular şi foramen ovale. Copilul a fost îndrumat pentru corectarea chirurgicală a malformaţiei.
Mama copilului a fost diagnosticată cu infecţie HIV de la vârsta de 1 an şi a născut la vârsta de 19 ani. A primit tratament antiretroviral timp de 10 ani, cu trei combinaţii terapeutice, astfel: zidovudină şi lamivudină 6 luni (martie - august 1999), la care s-a adăugat nelfinavir pentru o perioadă de aproximativ nouă luni (august 1999 - iunie 2000), urmată de combinaţia: didanosină, stavudină, indinavir, din noiembrie 2001 până în octombrie 2008, când s-a iniţiat schema recomandată în sarcină zidovudină - lamivudină, combinaţie în doză fixă, asociată cu lopinavir boostat cu norvir.
Având în vedere faptul că unele studii(5) au arătat asocierea malformaţiilor cardiace cu expunerea la zidovudină în sarcină, precum şi faptul că mama are un istoric terapeutic încărcat, nu putem exclude ipoteza că medicaţia antiretrovirală este unul din factorii asociaţi malformaţiei cardiace în acest caz. De asemenea, mama este fumătoare, dar nu a consumat alcool sau droguri în cursul sarcinii, factori de risc dovediţi a fi asociaţi cu anomaliile congenitale cardiace(20). Alţi factori de risc asociaţi malformaţiilor cardiace sunt deficitul de acid folic, bolile materne, cum ar fi diabetul, obezitatea, bolile febrile şi expunerea la unele medicamente (antidepresivele, antihipertensivele şi antibioticele)(20).
Rata malformaţiilor cardiace în SUA este de aproximativ 1%, un sfert dintre cazuri fiind forme severe de boală(21). Datele privind incidenţa malformaţiilor cardiace în ţara noastră sunt limitate(22), la nivel european fiind raportate 71 de cazuri la 10.000 de naşteri, iar forme severe, 19 cazuri la 10.000 de naşteri(13).
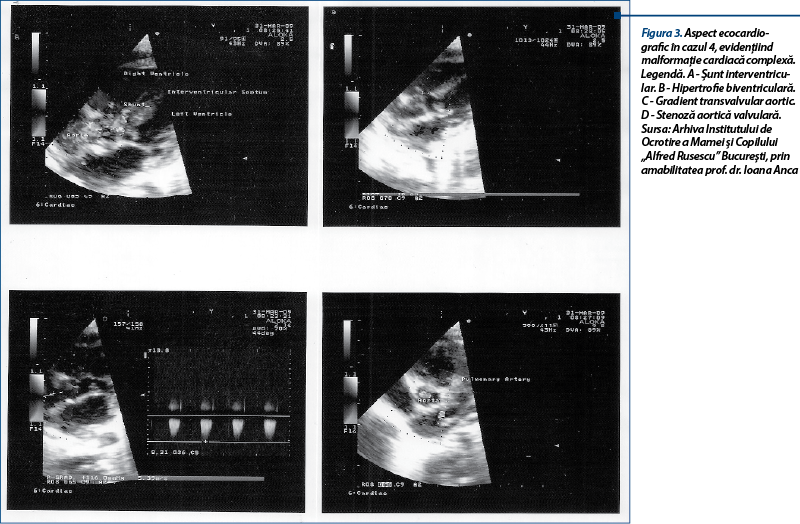
Cazul 5. Următorul caz este cel al unui băiat născut spontan după 33 de săptămâni de gestaţie, în martie 2012, fiind primul copil, provenit din sarcina nedispensarizată, cu greutatea de 1.800 g. În primele 24 de ore de viaţă a suferit o intervenţie chirurgicală de urgenţă la Spitalul Clinic de Copii „M.S. Curie” din Bucureşti pentru imperforaţie anală, cu evoluţie ulterioară favorabilă. Ambii părinţi erau diagnosticaţi cu infecţie HIV. Mama a născut la vârsta de 21 de ani, fiind în tratament antiretroviral încă de la vârsta de 9 ani, primind în această perioadă mai multe combinaţii medicamentoase, respectiv: zidovudină, lamivudină, nevirapină până în 2003, apoi stavudină, lamivudină, nelfinavir trei ani (2004-2007), urmat de combinaţia fixă zidovudină, lamivudină, ziagen plus efavirenz 2 ani (2007-2009), apoi combinaţie în doză fixă lamivudină, abacavir, plus atazanavir boostat cu norvir.
Rata malformaţiilor anorectale la nivel european este de aproximativ 3 cazuri la 10.000 de naşteri(13). Factorii de risc asociaţi malformaţiilor anorectale sunt bolile materne: diabet, obezitate, toxicele (fumatul)(23). Şi în acest caz putem considera infecţia HIV şi tratamentul antiretroviral matern factori de risc pentru apariţia acestui tip de malformaţie la produsul de concepţie.
Cazul 6: Fetiţă născută spontan tot în anul 2012, la 34 de săptămâni, cu greutatea de 2.430 g. Evoluţia postpartum a fost nefavorabilă: vărsături fecaloide, distensie abdominală, absenţa tranzitului şi peritonită meconială la 72 de ore de viaţă, motiv pentru care se practică rezecţia ileonului terminal cu ileo şi colostomă la Spitalul Clinic de Copii „Grigore Alexandrescu”, Bucureşti. Irigografia efectuată postoperator evidenţiază: rect, sigmoid, colon descendent şi transvers cu calibru foarte redus, cu topografie normală, substanţa de contrast se exteriorizează prin locostomă, iar la administrarea substanţei de contrast în amonte pe ileostomă se observă intestin subţire cu calibru normal şi traiect tortuos. Examenul histopatologic susţine diagnosticul de megacolon congenital aganglionic forma totală (boala Hirschsprung). În aprilie 2013, copilul beneficiază de colectomie totală, ileoanastomoză procedeu Soave la Spitalul Clinic de Copii „M.S. Curie”, Bucureşti, cu evoluţie favorabilă postoperator.
Mama a fost diagnosticată în luna a 7-a de sarcină cu infecţie HIV, VHC şi sifilis latent, fiind consumatoare de heroină. A primit terapie antiretrovirală pentru o scurtă perioadă de câteva săptămâni, deoarece travaliul se declanşează prematur.
Rata bolii Hirschsprung forma totală în Europa este de 1 caz la 10.000 de naşteri(13). Fiind tot o malformaţie digestivă, factorii de risc asociaţi sunt cei deja descrişi în cazul anterior. Şi în acest caz putem susţine o legătură între starea de sănătate a mamei, inclusiv consumul de droguri ilegale, şi apariţia afecţiunii congenitale la copil.
Cazul 7. Următorul caz pe care îl prezentăm este cel al unei fetiţe născute spontan, la termen, cu greutatea de 2.550 g, fiind al patrulea copil al unei femei diagnosticate la naştere cu infecţie HIV, hepatită cronică B şi C, consumatoare de droguri intravenoase (heroină şi etnobotanice) şi lues în antecedente. La momentul evaluării în clinica noastră, copilul prezenta hepatosplenomegalie importantă, motiv pentru care s-au efectuat investigaţii imagistice hematologice serologice şi genetice în colaborare cu Institutul de Ocrotire a Mamei şi Copilului „Alfred Rusescu” din Bucureşti.
Examenul frotiului de sânge periferic a evidenţiat frecvente limfocite cu vacuole în citoplasmă, cu aspect sugestiv pentru boală metabolică lipozomală. Ecografia transfontanelară a arătat ventriculomegalie uşoară, cu asimetrie, ventriculul stâng fiind mai mare în dimensiuni faţă de cel drept. Ecografia cardiacă a evidenţiat defect septal atrial, foramen ovale, microcalcificări pe cuspa septală aortică.
Consultul genetic (dr. Vasilica Plăiaşu) descrie facies dismorfic, cu urechi jos implantate, hipertrofie gingivală, limba cu depozite amiloidozice, hipertonia membrelor superioare şi inferioare, hipotonie axială, retard global în dezvoltare, tulburare de coordonare motorie de tip central, nistagmus orizontal, strabism convergent intermitent, sugerând diagnosticul de boală lizozomală, gangliozidoză tip 1 sau mucopolizaharodoză. Acest diagnostic este susţinut de determinările activităţii enzimatice pentru betagalactozidază, realizată pe leucocite preparate la Laboratorul Centogene Rostock Germania, care a evidenţiat activitate enzimatică sever redusă. Respectiv nivelul de activitate pentru beta-galactozidază a fost sub 1 nmol/MU/mg proteină (N: 119-659), iar cel al beta-hexozaminidazei a fost de 4,672 nmol/MU/mg proteină (N: 1905-5641).
Pacienta a avut o evoluţie nefavorabilă, marcată de agravarea simptomelor neurologice şi a decedat la vârsta de 10 luni.
Gangliozidoza, sau boala Tay Sacks, este o boală autozomal recesivă degenerativă, neurologică, determinată de acumularea de glicolipide la nivelul sistemului nervos central. Este foarte rară, de 1 caz la 100.000-200.000 de naşteri. Forma infantilă cu debut la vârsta de sugar, ca în cazul prezentat mai sus, are prognostic infaust, decesul survenind în primii ani de viaţă(24,25).
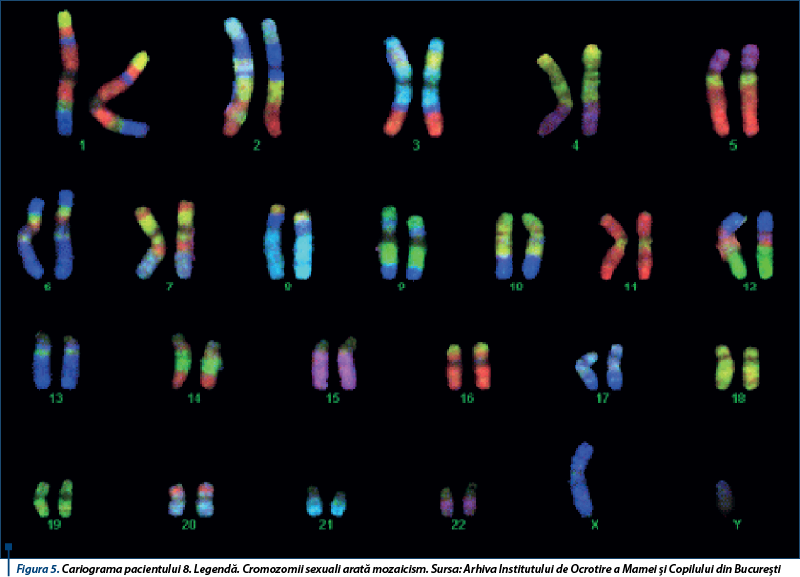
Cazul 8. Copilul a fost născut în anul 2010, la termen (38 săptămâni), prin cezariană programată, greutatea 2.800 g, ambii părinţi fiind HIV pozitivi. Examenul clinic a evidenţiat: organe genitale externe cu aspect de labioscrot, micropenie (~1 cm), absenţa testicului stâng în scrot şi orificiul uretral la nivelul vârful penisului. Investigaţiile genetice au evidenţiat mozaicism 45X0/46XY, ceea ce a condus la diagnosticul de hermafroditism adevărat sau disgenezie gonadală. Detaliile investigaţiilor genetice privind acest caz au fost publicate(26) în revista „Acta Endocrinologica” în anul 2011.
În acest caz, nivelul hormonilor sexuali a fost în limite normale, iar cultura de fibroblaşti din dermul genital a evidenţiat receptori androgenici şi pentru 5-alfa-reductază. Pacientul a beneficiat de intervenţie chirurgicală, care a extras ovotestisul aflat în canalul inghinal stâng, apoi reconstrucţie a organelor genitale externe cu fenotip masculin. Evoluţia postoperatorie a fost favorabilă, copilul având o dezvoltare fizică şi neuropsihomotorie normală.
Ambii părinţi fac parte din cohorta pediatrică românească(11), diagnosticaţi în copilărie, care au primit terapie antiretrovirală. Mama a fost diagnosticată cu infecţie HIV la vârsta de 7 ani şi a primit multiple combinaţii antiretrovirale anterior şi în cursul sarcinii (zidovudină, dideoxicitozină, dideoxiinozină, stavudină, efavirenz, indinavir, epivir, ziagen, lopinavir boostat cu norvir, combinaţie fixă zidovudină, lamivudină şi lopinavir, norvir) şi a născut la vârsta de 21 de ani. Tatăl este şi el diagnosticat cu infecţie HIV de la vârsta de 6 ani, primind mai multe scheme antiretrovirale (dideoxicitozină şi zidovudină doi ani, apoi zidovudină, emtricitabină şi efavirenz). De menţionat că ambii părinţi aveau nivelul ARN HIV nedetectabil de aproximativ 10 ani.
Disgenezia ovotesticulară reprezintă aproximativ 10% din toate anomaliile congenitale caracterizate de ambiguitate sexuală şi este determinată de anomalii cromozomiale(27).
Factorii de risc asociaţi sau cauzele acestei anomalii congenitale nu sunt cunoscute(28), astfel că este greu de apreciat dacă terapia antiretrovirală de lungă durată a avut sau nu o contribuţie în cazul prezentat, totuşi nu poate fi exclusă această ipoteză.
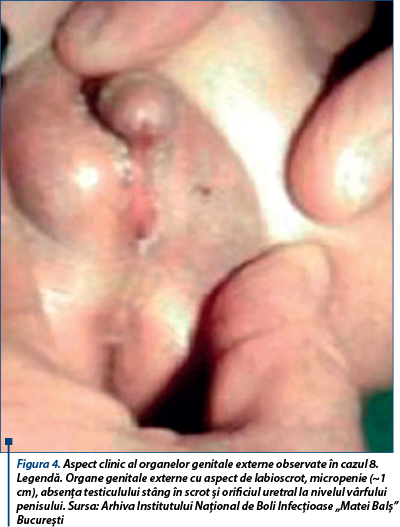
Cazul 9. Fetiţă născută în anul 2010 la 9 luni prin operaţie cezariană, GN=3.000 g. A prezentat icter prelungit neonatal formă severă, nivelul maxim de 15 mg/dl al bilirubinei fiind atins în a 5-a zi de viaţă. La examenul clinic se remarcă aspect infiltrat al tegumentelor, gât scurt, urechi jos implantate, fante palpebrale mongoloide, disfonie, macroglosie, AV=116 bătai/minut, suflu sistolic gr III-IV, parasternal stâng. Investigaţiile de laborator arată niveluri scăzute ale hormonilor tiroidieni T3=0,44 ng/mL (N=0,6-1,81 ng/ml), T4=2.5 ug/dl (N=4,5-11,5 ug/dl), FT3=1,35 pg/nL (N= 2,3-4,2 pg/nl), FT4=0,13 ng/dl (N=0,89-1,76 ng/dl) cu niveluri crescute ale TSH >150.00 UiU/mL (N=0,35-5,5 U/ml). Ecografia cardiacă evidenţiază defect septal atrial şi persistenţă de canal arterial. Examenul neurologic la vârsta de 3 ani şi 4 luni arată întârziere în achiziţia de limbaj (vocabular sărac), nu foloseşte persoana întâi şi are deficit de achiziţii cognitive (nu ştie culorile sau literele). Mama avea 22 de ani la naştere, fiind depistată cu infecţie HIV cu 9 ani anterior şi primise tratament ARV de la diagnosticare, ultima schemă fiind cea recomandată în sarcină, respectiv zidovudină-lamivudină, combinaţie în doză fixă, asociată lopinavirului boostat cu norvir.
Rata hipotiroidismului congenital în Europa este de aproximativ 1 caz la 400 de naşteri(29), fiind cea mai frecventă boală endocrină la copii. Este o boală genetică, transmisă autozomal recesiv şi se poate datora disgenezei glandei tiroide, a hipotalamusului sau deficitului de sinteză al hormonilor tiroidieni(30).
Deficitul de hormoni tiroidieni are efect asupra dezvoltării neuropsihice a copilului(31), iar terapia de substituţie reprezintă fundamentul îmbunătăţirii achiziţiilor cognitive. În cazul prezentat, copilul are un deficit de dezvoltare neuropsihică moderat, în ciuda iniţierii precoce a terapiei de substituţie cu levotiroxină.
Cazul 10. Al doilea caz cu evoluţie nefavorabilă este cel al unei fetiţe născute prematur în anul 2010, diagnosticată cu malformaţie severă a peretelui abdominal - gastroschizis, cu hernierea viscerelor abdominale, care a decedat la două săptămâni după naştere din cauza complicaţiilor septice. Mama copilului este cunoscută cu infecţie HIV din anul 2006, fiind în tratament antiretroviral.
Incidenţa acestei malformaţii în populaţia generală în Europa este de aproximativ 3 cazuri la 10.000 de naşteri. De cele mai multe ori, evoluţia este favorabilă după terapia chirurgicală, dar nu şi în cazul prezentat(32). Factorii de risc asociaţi sunt toxicele, cum ar fi fumatul şi utilizarea de droguri ilicite, dar sunt puţine date în literatura de specialitate privind acest aspect, motiv pentru care şi în acest caz nu poate fi argumentată implicarea medicaţiei antiretrovirale în apariţia malformaţiei, dar nici nu poate fi exclusă o legătură cauză-efect.
Concluzii
Malformaţiile congenitale severe au cel mai adesea cauze multiple, fiind greu de asociat de multe ori cu anumiţi factori de mediu. Sunt puţine date în literatură privind efectul teratogen al infecţiei HIV şi al medicaţiei antiretrovirale, acesta fiind motivul principal al publicării prezentului articol.
Din experienţa clinicii noastre rezultă o rată neaşteptat de mare a malformaţiilor în general (39%), precum şi a celor severe cu impact major asupra dezvoltării copiilor expuşi la infecţia HIV şi la antiretrovirale (4%, respectiv 10/244 de cazuri).
Doar două dintre cazurile identificate de noi au avut o evoluţie nefavorabilă prin deces, dar şi deficitul de dezvoltare neuropsihomotorie prezentă în alte patru cazuri reprezintă o problemă importantă de sănătate, care aduce costuri suplimentare şi îngrijiri speciale pentru aceşti copii, mai ales în cazul copilului cu sindrom Niemann Pick.
În 8 din 10 cazuri prezentate, copii au fost expuşi medicamentelor antiretrovirale şi această asociere nu trebuie neglijată, ci trebuie investigată pe cohorte mai largi de pacienţi pentru a putea identifica cu mai mare acurateţe factorii de risc şi impactul infecţiei HIV şi a medicamentelor antiretrovirale asupra produsului de concepţie.
Un alt aspect important pe care dorim să-l menţionăm este că pentru diagnosticul şi tratamentul corect al pacienţilor a fost nevoie de colaborare interdisciplinară, fiind implicate mai multe unităţi medicale din Bucureşti.
De asemenea, considerăm că trebuie dezvoltate strategii la nivel naţional pentru consiliere genetică preconcepţie, pentru monitorizarea corectă a sarcinii în populaţia generală, dar şi la femeile seropozitive, pentru a putea îmbunătăţi prognosticul în rândul copiilor.
Mulţumiri: Mulţumiri pacienţilor şi părinţilor acestora, personalului medical din Institutul Naţional de Boli Infecţioase „Matei Balş” şi al Institutului de Ocrotire a Mamei şi Copilului „Alfred Rusescu”, în mod special dr. Vasilica Plăieşu şi dr. Florin Brezan.
Această lucrare este efectuată în cadrul Programului Operaţional Sectorial pentru Dezvoltarea Resurselor Umane (POSDRU), finanţat din Fondul Social European şi Guvernul României prin contractul POSDRU/159/1.5/S/137390.
Bibliografie
-
May M, Sterne JA, Sabin C, Costagliola D, Justice AC, et al. (2007) Prognosis of HIV-1-infected patients up to 5 years after initiation of HAART: collaborative analysis of prospective studies. AIDS 21: 1185–1197.
-
Parker SE, Mai CT, Canfield MA, et al. Updated national birth prevalence estimates for selected birth defects in the United States, 2004-2006. Birth Defects Research Part A - Clinical and Molecular Teratology. 2010;88:1008-1016.
-
Louie JK, Hsu LC, Osmond DH, et al. Trends in causes of death among persons with acquired immunodeficiency syndrome in the era of highly active antiretroviral therapy, San Francisco, 1994–1998. J Infect Dis 2002;186(7):1023-7.
-
Madeddu G, Rezza G, Mura MS. Trends in the European HIV/AIDS epidemic: a perspective from Italy. Expert Rev Anti Infect Ther. 2009 Feb;7(1):25-36).
-
Sibiude J, Mandelbrot L, Blanche S, et al. Association between Prenatal Exposure to Antiretroviral Therapy and Birth Defects: An Analysis of the French Perinatal Cohort Study (ANRS CO1/CO11). Menéndez C, ed. PLoS Medicine. 2014;11(4):e1001635. doi:10.1371/journal.pmed.1001635.
-
http://www.eacsociety.org/guidelines/eacs-guidelines/eacs-guidelines.html
-
Floridia M, Mastroiacovo P, Tamburrini E, Tibaldi C, Todros T, Crepaldi A, Sansone M, Fiscon M,Liuzzi G, Guerra B, Vimercati A, Vichi F, Vicini I, Pinnetti C, Marconi A, Ravizza M. Birth defects in a national cohort of pregnant women with HIV infection in Italy, 2001–2011. BJOG2013;120:1466–1476.
-
National Center on Birth Defects and Developmental Disabilities, CDC. State birth defects surveillance program directory. Birth Defects Res Part A Clin Mol Teratol 2006;76:837-93.
-
CDC. Update on Overall Prevalence of Major Birth Defects - Atlanta, Georgia, 1978-2005. MMWR 2008;57(01):1-5.
-
Correa A, Cragan JD, Kucik ME, et al. Metropolitan Atlanta Congenital Defects Program: 40th anniversary edition surveillance report. Reporting birth defects surveillance data 1968-2003. Birth Defects Res A Clin Mol Teratol 2007;79:65--186.
-
www.cnlas.ro.
-
Maria Tudor ASevere birth defects in children perinatal exposed to HIV from a “real-world” setting: Infectious Diseases National Institute, Bucharest, Romania. Journal of the International AIDS Society. 2014;17(4Suppl 3):19699. doi:10.7448/IAS.17.4.19699).
-
Khoshnood B, Greenlees R, Loane M, Dolk H on behalf of the EUROCAT Project Management Committee and a EUROCAT Working Group (2011), „Paper 2: EUROCAT public health indicators for congenital anomalies in Europe”, Birth Defects Research (Part A), Vol 91, pp S16-S22. [doi:10.1002/bdra.20776].
-
Tudose, C., Lacatusu, C., Bara, I. C., Tudose, M., & Bara, I. (2007). Estimation of recurrence risk and genetic counselling of families with evidence of isolated (unsyndromic) cleft lip and palate in Suceava county, Romania. Analele Stiintifice Ale Universitatii „Al.I.Cuza” Din Iasi.(Serie Noua).Sectiunea 2.a.Genetica Si Biologie Moleculara,8(1).
-
Mengel E, Klunemann H, Lourenco C, et al. Niemann-Pick disease type C symptomatology: an expert-based clinical description. Orphanet Journal of Rare Diseases. 2013;8:166-166.
-
Ory DS. The niemann-pick disease genes: Regulators of cellular cholesterol homeostasis. Trends Cardiovasc Med. 2004;14:66-72.
-
Ferraris A, Bernardini L, Sabolic Avramovska V, et al. Dandy-Walker malformation and Wisconsin syndrome: novel cases add further insight into the genotype-phenotype correlations of 3q23q25 deletions. Orphanet Journal of Rare Diseases. 2013;8:75. doi:10.1186/1750-1172-8-75).
-
Blank MC, Grinberg I, Aryee E, et al. Multiple developmental programs are altered by loss of Zic1 and Zic4 to cause Dandy-Walker malformation cerebellar pathogenesis. Development (Cambridge, England). 2011;138(6):1207-1216. doi:10.1242/ dev 054114.
-
Grinberg I, Northrup H, Ardinger H, Prasad C, Dobyns WB, Millen KJ, Heterozygous deletion of the linked genes ZIC1 and ZIC4 is involved in Dandy-Walker malformation.. Nat Genet. 2004 Oct; 36(10):1053-5.
-
Patel SS, Burns TL. Nongenetic Risk Factors and Congenital Heart Defects. Pediatr Cardiol. 2013;34:1535-1555.
-
Reller MD, Strickland MJ, Riehle-Colarusso T, Mahle WT, Correa A. Prevalence of congenital heart defects in Atlanta, 1998-2005. J Pediatr.2008;153:807-13.
-
Togănel, Rodica; Făgărăşan, Amalia; Paşc, Sorina; Gozar, Liliana; Muntean, Iolanda; Şuteu, Carmen; Blesneac, Cristina; Előd, K. (2010). Registrul regional al malformaţiilor cardiace congenitale. Revista Română de Cardiologie 2010; 25(4): 235-241.
-
Cretolle C, Rousseau V, Lottmann H, et al. Anorectal Malformations. Archives de Pediatrie. 2013;20:S19-S27).
-
Kalpathy S. Krishnamoorthy, M.D., Florian Eichler, M.D., Otto Rapalino, M.D., and Matthew P. Frosch, M.D., Ph.D. Case 14-2014 — An 11-Month-Old Girl with Developmental Delay. N Engl J Med 2014; 370:1830-1841May 8, 2014DOI: 10.1056/NEJMcpc1305987).
-
Sandhoff K, Harzer K. Gangliosides and gangliosidoses: Principles of molecular and metabolic pathogenesis. Journal of Neuroscience. 2013;33:10195-10208).
-
Cristea C, Plaiasu V, Ochiana D, Neagu RD, Gherlan I, Mardarescu M. Sexual ambiguity associated with „in utero” antiretroviral exposure. Acta Endocrinol. 2011;7:551-559.
-
Krstić ZD, Smoljanić Ž, Vukanić D, Varinac D, Janjić G. True hermaphroditism: 10 years’ experience. Pediatr Surg Int. 2000;16:580-583.
-
Walker, A., Walker, J., Adams, S., Shi, E., McGlynn, M. and Verge, C. (2000), True hermaphroditism. Journal of Paediatrics and Child Health, 36: 69–73. doi: 10.1046/j.1440-1754.2000.00432.x.
-
Toublanc, J. (1992) Comparison of epidemiological data on congenital hypothyroidism in Europe with those of other parts of the world. Hormone Research, 38, 230–235.
-
Park SM, Chatterjee VKK. Genetics of congenital hypothyroidism. J Med Genet. 2005;42:379-389.
-
Selva, K.A., Harper, A., Downs, A., Blasco, P.A. & Lafranchi, S.H. (2005) Neurodevelopmental outcomes in congenital hypothyroidism: comparison of initial t4 dose and time to reach target T4 and TSH. Journal of Pediatrics, 147, 775–780.
-
Holland AJA, Walker K, Badawi N. Gastroschisis: an update. Pediatr Surg Int. 2010;26:871-878.).