Aprecierea fibrozei hepatice la copil prin teste neinvazive
Assessing liver fibrosis in children through non-invasive tests
Abstract
Hepatic fibrosis accompanies innevitably the evolution of chronic hepatitis. In diagnostic protocols, staging and treatment, the assessment of hepatic fibrosis is absolutely mandatory in the correct therapeutic approach. Liver biopsy is an invasive method with risks in children. Currently there are a number of non-invasive tests that offer the correct staging of fibrosis and are admitted in the therapeutic decision and monitoring of chronic hepatitis in children.
Keywords
fibrosischronic hepatitischildRezumat
Fibroza hepatică însoţeşte în mod implacabil evoluţia hepatitelor cronice. În protocoalele de diagnostic, stadializare şi tratament, aprecierea fibrozei hepatice este absolut obligatorie în gestul terapeutic corect. Biopsia hepatică este o metodă invazivă, cu riscuri la copil. În prezent există o serie de teste neinvazive ce oferă stadializarea corectă a fibrozei şi care sunt admise în decizia terapeutică şi de monitorizare a hepatitelor cronice la copil.
Cuvinte Cheie
fibrozăhepatită cronicăcopilBiopsia hepatică (BH) în diagnosticul şi evaluarea pacienţilor cu afecţiuni hepatice şi-a pierdut întâietatea în ultimii ani, testele genetice, moleculare şi enzimatice, neinvazive, fiind în multe cazuri suficiente pentru un diagnostic etiologic(1).
Stadializarea fibrozei hepatice sau a cirozei se face din ce în ce mai frecvent folosind diverşi indici sau sisteme de scoruri bazate pe teste biochimice, markeri serologici sau metode imagistice, cu performanţe diferite.
În pediatrie, sunt folosite în prezent numeroase teste neinvazive de apreciere a fibrozei hepatice prin extrapolare din patologia adultului, fără a exista suficiente studii pediatrice de validare. Avantajele acestor tehnici comparativ cu biopsia hepatică sunt: o înaltă reproductibilitate şi fiabilitate, sunt complet neinvazive, sunt mai puţin costisitoare şi fără complicaţii, evaluează fibroza hepatică în întregul ficat, dar dezavantajele majore sunt legate de imposibilitatea diagnosticului etiologic, slaba discriminare între stadiile intermediare de fibroză şi de faptul că pot fi influenţate de diferite condiţii hepatice sau extrahepatice, precum obezitatea sau steatoza(1).
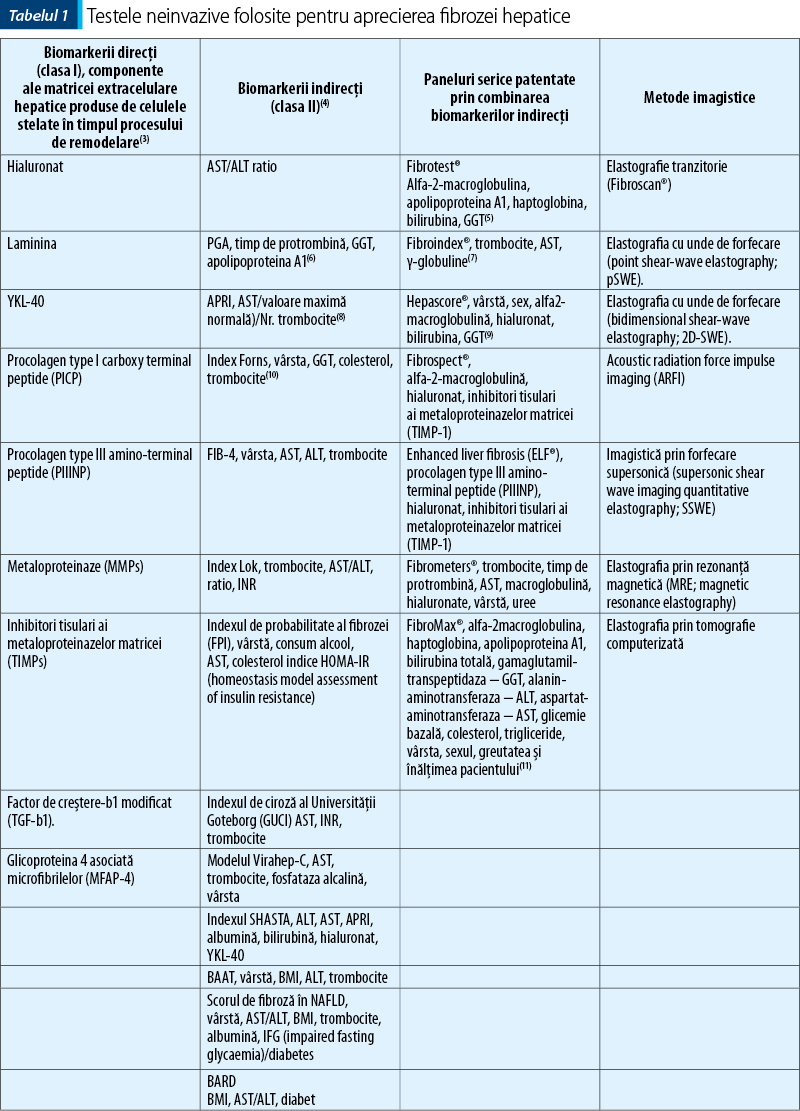
Pentru aprecierea şi stadializarea fibrozei hepatice se pot folosi biomarkeri serici indirecţi (clasa II) sau direcţi (clasa I), sau numeroase tehnici imagistice. Markerii indirecţi (clasa II) rezultă prin combinarea unor teste serologice uzuale după un algoritm specific fiecăruia (tabelul 1)(2).
Testul FibroTest-ActiTest® (FT/AT) este unul dintre cele mai validate scoruri pentru evaluarea fibrozei în hepatitele cronice virale, cuprinzând pentru calcul vârsta, sexul, nivelul seric al haptoglobinei, apolipoproteinei A1, GGT, a2-macroglobulinei şi bilirubinei totale(5).
Se obţin astfel două scoruri, unul pentru fibroză şi unul pentru activitatea necroinflamatorie, cu valori cuprinse între 0 şi 1 (de la absenţa bolii la fibroză sau activitate necroinflamatorie severă). Testul este validat şi la copil, de la vârsta de 12 ani, dar corelaţia cu aspectul histologic este mai puternică pentru activitatea necroinflamatorie decât pentru fibroză(12,13).
Unele afecţiuni, precum citoliza hepatică acută, hemoliza acută, inflamaţii acute sau colestaza extrahepatică, pot inflluenţa acurateţea rezultatului(14).
Testul FibroMax® este o combinaţie de cinci teste neinvazive diferite: FibroTest, ActiTest, SteatoTest, NashTest şi AshTest, pentru a evalua gradul afectării hepatice.
-
FibroTest evaluează gradul fibrozei (F0-F4, conform scorului METAVIR).
-
ActiTest evaluează activitatea necroinflamatorie (A0-A3, conform scorului METAVIR).
-
SteatoTest evaluează steatoza hepatică (S0-S3).
-
NashTest evaluează prezenţa steatohepatitei non-alcoolice la pacienţii obezi (N0: „NOT NASH”, N1: „Borderline NASH” şi N2: „NASH”).
-
AshTest evaluează gradul afectării hepatice la pacienţii cu consum excesiv de etanol (H0-H3)(14,15).
Testul are aceleaşi limite de eroare ca şi FibroTest-ActiTest®, dar pentru vârsta pediatrică nu este validat.
Testul Fibrometer® este un alt panel patentat, indisponibil în România.
Tehnicile imagistice de apreciere a fibrozei hepatice cuprind:
-
Elastografia hepatică tranzitorie (TE), prin FibroScan® (Vibration-controlled transient elastography), utilizează ultrasunetele cu frecvenţă de 5 MHz sau unde elastice de frecvenţă joasă (50 Hz) pentru măsurarea rigidităţii hepatice, fiind o tehnică neinvazivă, rapidă, simplă şi reproductibilă. Se foloseşte o vibraţie de mică amplitudine, care este transmisă prin transductor în ţesutul hepatic, şi se măsoară ulterior rapiditatea de propagare a undelor elastice prin ficat. Măsurătorile se pot efectua până la o adâncime în ţesut de 25-65 mm de la tegument. Velocitatea undei propagate este legată în mod direct de elasticitatea staturilor parcurse: dacă ţesutul este dur, deci mai fibrotic, undele elastice se propagă mai repede(16).
Rezultatul este media aritmetică a zece măsurători valide; limitele de măsurare sunt 2,5-75 kPa, valorile de 4,5-5,4 kPa fiind valorile cutoff ale normalului la copil(17,18).
Valoarea-limită validată ca fiind patologică diferă în funcţie de etiologia afecţiunii hepatice şi este, în medie, 7,2 kPa pentru fibroza semnificativă, 12,5 kPa pentru fibroza severă şi peste 17,6 kPa pentru ciroză(19,20).
Pentru populaţia adultă s-a realizat o serie de corelaţii între valorile obţinute la FibroScan şi posibilele complicaţii legate de fibroza hepatică, astfel: valoarea >17 kPa este un factor de predicţie a hipertensiunii portale şi valoarea rigidităţii hepatice >19,2 kPa prezice prezenţa varicelor esofagiene mari (Paquet-grade ≥II)(21).
Asociaţia Americană de Gastroenterologie recomandă elastografia ca metodă de ales pentru evaluarea fibrozei la pacienţii cu hepatită cronică VHB sau VHC, dar pentru fibroza asociată steatozei hepatice recomandă utilizarea rezonanţei magnetice(21).
Acurateţea şi reproductibilitatea măsurătorilor sunt dependente de o serie de factori: obezitatea cu BMI ≥25 kg/m2, prezenţa steatozei hepatice sau a fibrozei uşoare, colestaza extrahepatică, insuficienţa cardiacă cu congestie hepatică şi presiune venoasă centrală ridicată, anestezia generală, mesele bogate cu mai puţin de trei ore înaintea examinării, vârsta mică a pacienţilor care prezintă spaţii intercostale înguste, prezenţa nodulilor de regenerare cirotici, dar şi de experienţa medicului examinator. Se consideră că experienţa necesară se câştigă după efectuarea a minimum 500 de examinări. Dificultăţi tehnice legate de această metodă imagistică sunt prezente în special la sugar şi copilul mic, unde nu pot fi evitate la examinare vasele sangvine şi biliare, din cauza ferestrei reduse de examinare prin spaţiile intercostale mici, fiind necesară adaptarea sondei de examinare(18).
În funcţie de afecţiune, există valori diferite patologice stabilite prin studii multiple, cunoscute ca Fibroscan scoring card (figura 1, tabelul 2)(22,23).
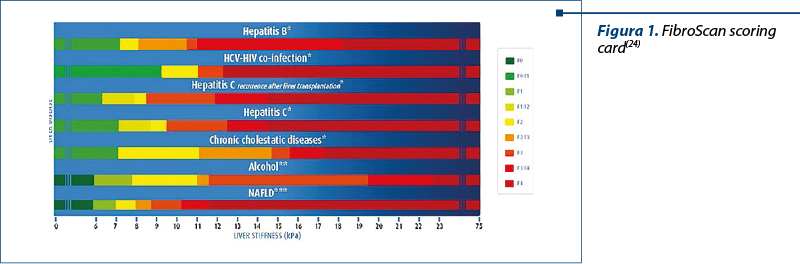
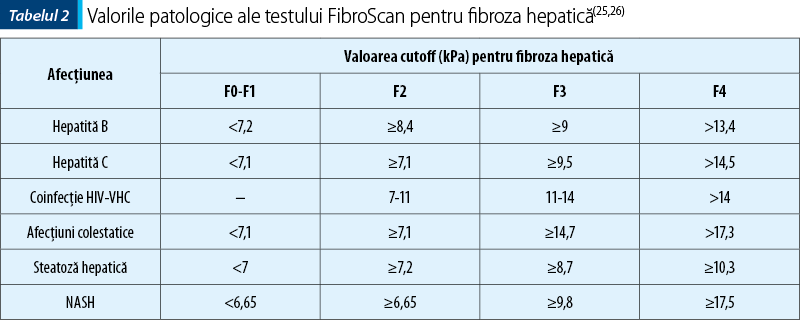
Asociaţia Americană de Gastroenterologie consideră pentru confirmarea cirozei hepatice valoarea cutoff în cazul hepatitei cronice cu VHC 12,5 kPa şi 11 kPa pentru hepatita cronică B(21).
-
Acoustic radiation force impulse imaging (ARFI; shear wave velocity – SWV – quantification) este o tehnică neinvazivă, uşor de efectuat, rapidă, reproductibilă, ce foloseşte echipament de ecografie cu pulsaţii acustice de scurtă durată (push-pulses) emise cu o frecvenţă de 2,6 MHz(27).
Se creează unde de forfecare prin compresia indusă de o pulsaţie, acestea fiind transmise perpendicular pe şesut şi apoi captate de un sistem de achiziţie pulse-echo pentru ultrasunete. Velocitatea de propagare a acestor unde este măsurată într-o arie de interes (region of interest; ROI) de 5 mm x 10 mm, localizată până la 8 cm în profunzime. Prin această tehnică este evaluat un volum hepatic mai mic decât cel evaluat prin elastografie(3).
Velocitatea undei este mai mare atunci când străbate un ţesut mai rigid, deci viteza undei de forfecare creşte în cazurile de fibroză hepatică marcată, ceea ce face ca această tehnică să evalueze mai fidel fibroza avansată (F3-F4). Fibroza mai puţin severă este apreciată cu mai mare acurateţe prin elastometrie. Rezultatele sunt exprimate în m/s, valorile măsurabile fiind cuprinse între 0,5 şi 4,4 m/s. Ca şi în cazul elastometriei, acurateţea este mai mică la pacienţii obezi (BMI ≥25 kg/m2) şi în prezenţa ascitei(28).
Valorile normale la copil sunt aceleaşi între 0 şi 10 ani, apoi se modifică conform celor de la adult, iar cutofful de diagnostic pentru fibroza hepatică semnificativă este 1,34 m/s pentru F≥2, 1,55-1,61 m/s pentru fibroza avansată (F≥3) şi 1,87-2,37 m/s pentru ciroză(29,30).
-
Elastografia cu unde de forfecare (shear-wave elastography; SWE) este o tehnică cu două variante de realizare: point shear wave elastography (pSWE), care măsoară rigiditatea ţesutului hepatic şi viteza undei de forfecare într-un singur punct, şi 2D SWE, prin care se obţine o hartă colorată a rigidităţii ţesutului sau a vitezei undelor de forfecare în zona de interes. Pentru o mai bună acurateţe se pot face mai multe măsurători(31).
Această tehnică reprezintă o elastografie bidimensională în timp real, cu aprecierea rigidităţii hepatice cantitativ, în kPa, având avantajul unei mai bune localizări a ariei de interes, cu evaluarea mai fidelă a fibrozei(32).
Cele trei metode neinvazive de apreciere a fibrozei hepatice, TE, ARFI şi SWE, au rezultate similare în ceea ce priveşte evaluarea gradului de fibroză hepatică(33), dar SWE are acurateţe mai mare în diagnosticul cirozei, iar TE apreciază mai bine stadiile incipiente şi moderate ale fibrozei(34).
-
Imagistica prin forfecare supersonică (supersonic shear wave imaging quantitative elastography – SSWE) este o tehnică bazată pe folosirea ultrasunetelor pentru vizualizarea în timp real a proprietăţilor elastice ale ţesuturilor moi. Metoda constă în folosirea unor fascicule concentrate de ultrasunete, cu obţinerea unor surse de vibraţii mecanice care vor radia ca unde de forfecare cu frecvenţă mică în interiorul ţesuturilor. Undele de forfecare rezultate vor interfera, creând două valuri importante de forfecare plană care se propagă şi sunt distorsionate din cauza heterogenităţii ţesuturilor. Un scanner ultrarapid este capabil să genereze undele şi să capteze imaginile undelor de forfecare rezultate cu o viteză supersonică (5000 cadre/sec.) şi elasticitatea de forfecare a mediului poate fi înregistrată cantitativ, cu cartografierea elasticităţii ţesuturilor în mai puţin de 20 ms(35).
Rezultatele se exprimă în kPa, iar valorile normale sunt 6±1,4 kPa, dar pot fi influenţate de BMI şi de vârsta pacienţilor(36). Tehnica poate fi aplicată pentru evaluarea fibrozei şi la copil, având avantajul că rezultatele nu sunt influenţate de respiraţie(37).
Aprecierea fibrozei hepatice prin această tehnică determină rezultate comparabile cu cele obţinute prin TE sau ARFI(38).
-
Elastografia prin rezonanţă magnetică (magnetic resonance elastography; MRE) foloseşte unde sonore de frecvenţă mică (60 Hz) pentru a induce unde de forfecare în ţesutul hepatic, vizualiate prin folosirea unei secvenţe cu contrast de fază modificată. Se măsoară în plus viteza de propagare a undelor prin executarea unui RMN cu un aparat cu soft modificat. Undele sonore sunt generate de un subwoofer („driver activ”) în afara camerei de scanare şi sunt transmise la un disc de plastic („driver pasiv”) securizat de o bandă elastică deasupra părţii superioare drepte a abdomenului anterior, pe grilajul costal, iar datele obţinute sunt interpretate de un aparat de RMN cu soft special. Această tehnică poate discrimina fidel între stadiile de fibroză moderată şi cele de fibroză uşoară la adult, dar studiile pediatrice sunt limitate, metoda nefiind validată în pediatrie.
Avantajele majore ale acestei tehnici constau în reproductibilitatea rezultatelor şi în posibilitatea unei evaluări globale a rigidităţii ficatului, chiar şi la pacienţii obezi(39), iar dezavantajele constau în senzaţia neplăcută de trepidaţie din cauza vibraţiilor resimţite atunci când undele sunt generate, necesitatea sedării, costul ridicat şi accesabilitatea redusă(40).
MRE se poate realiza rapid, într-o perioadă de timp ce corespunde la 1-4 respiraţii; în studiile clinice în care a fost folosită nu a necesitat sedare până la vârsta de 4 luni, dar a necesitat sedare/anestezie la copiii mai mari(31).
Studiile efectuate până în prezent consideră o valoare normală de 2,71 kPa la copil(41).
Evaluarea neinvazivă a fibrozei hepatice este una dintre metodele care au evoluat cel mai rapid în ultimii ani. În ciuda numeroaselor avantaje, a existat mult timp şi încă există o rezistenţă clară la acceptarea stadializării fibrozei hepatice prin tehnici neinvazive la copil, deoarece lipseşte o validare externă suficientă pentru unele dintre metodele propuse. Numărul metodelor propuse este din ce în ce mai mare şi, practic, nu există timp pentru a le valida sau a le testa pe toate şi, nu în ultimul rând, mulţi hepatologi consideră încă biopsia hepatică indispensabilă.
Conflict of interests: The author declares no conflict of interests.
Bibliografie
- Dezsofi A, Baumann U, Dhawan A, et al. Liver Biopsy in Children: Position Paper of the ESPGHAN Hepatology Committee. J Pediatr. Gastroenterol. Nutr. 2015; 60 (3):408-20.
- Păcurar D, Ion G. Hepatitele cronice la copil. In: Plesca Doina Anca (ed.): Curs de Pediatrie pentru studenţi. Editura Universitară „Carol Davila”. 2017;, Bucureşti, vol 1:146-157.
- Papastergiou V, Tsochatzis, E, Burroughs AK. Non-invasive assessment of liver fibrosis. Annals of Gastroenterology. 2012; 25:218-231.
- Gressner OA, Weiskirchen R, Gressner AM. Biomarkers of liver fibrosis: clinical translation of molecular pathogenesis or based on liver-dependent malfunction tests. Clin Chim Acta. 2007; 381:107-113.
- Imbert-Bismut F, Ratziu V, Pieroni L, et al. Biochemical markers of liver fibrosis in patients with hepatitis C virus infection: a prospective study. Lancet. 2001; 357:1069-1075.
- Nguyen-Khac E, Chatelain D, Tramier B, et al. Assessment of asymptomatic liver fibrosis in alcoholic patients using fibroscan: prospective comparison with seven non-invasive laboratory tests. Aliment Pharmacol Ther. 2008; 28:1188-1198.
- Koda M, Matunaga Y, Kawakami M, et al. FibroIndex, a practical index for predicting significant fibrosis in patients with chronic hepatitis C. Hepatology. 2007; 45:297-306.
- Wai CT, Greenson JK, Fontana RJ, et al. A simple noninvasive index can predict both significant fibrosis and cirrhosis in patients with chronic hepatitis C. Hepatology. 2003; 38:518-526.
- Adams LA, Bulsara M, Rossi E, et al. Hepascore: an accurate validated predictor of liver fibrosis in chronic hepatitis C infection. Clin Chem. 2005; 51:1867-1873.
- Forns X, Ampurdanes S, Llovet JM, et al. Identification of chronic hepatitis C patients without hepatic fibrosis by a simple predictive model. Hepatology. 2002; 36; 986-992.
- Morra R, Munteanu M, Imbert-Bismut F, et al. FibroMax: Towards a new universal marker of hepatic disease? Expert Rev Mol Diagn. 2007; Sept., 7(5):481-90.
- Poynard T, Morra R, Halfon P, et al. Meta-Analyses of FibroTest Diagnostic Value in Chronic Liver Disease. BMJ Gastroenterology. 2007; 7:40.
- Pokorska-Śpiewak M, Kowalik-Mikołajewska B, Aniszewska M, et al. Non-invasive evaluation of the liver disease severity in children with chronic viral hepatitis using FibroTest and ActiTest - comparison with histopathological assessment. Clin Exp Hepatol. 2017; Dec., 3(4):187-193.
- Laborator Synevo. Referinţele specifice tehnologiei de lucru utilizate, 2010. Catalog.
- Poynard T, Vlad Ratziu V, Naveau S et al. The diagnostic value of biomarkers (SteatoTest) for the prediction of liver steatosis. Comp Hepatol. 2005; 4:10.
- Sandrin L, Fourquet B, Hasquenoph JM, et al. Transient elastography: a new noninvasive method for assessment of hepatic fibrosis. Ultrasound Med Biol. 2003; 29:1705-1713.
- Roulot D, Czernichow S, Le Clesiau H, et al. Liver stiffness values in apparently healthy subjects: influence of gender and metabolic syndrome. J Hepatol. 2008; 48:606-613.
- Goldschmidt I et al. Application and limitations of transient liver elastography in children. J Pediatr Gastroenterol Nutr. 2013; 57,109–13.
- Castera L, Forns X, Alberti A. Non-invasive evaluation of liver fibrosis using transient elastography. J Hepatol. 2008; 48:835-847.
- J Foucher, E Chanteloup, J Vergniol, et al. Diagnosis of cirrhosis by transient elastography (FibroScan): a prospective study. Gut. 2006 ; Mar 55(3):403-408.
- Lim KL, Flamm SL, Singh S, et al. American Gastroenterological Association Institute Guideline on the Role of Elastography in the Evaluation of Liver Fibrosis. Gastroenterology. 2017; 152:1536-1543.
- Tapper BE, Laurent Castera L, Afdhal NH. FibroScan (Vibration-Controlled Transient Elastography): Where Does It Stand in the United States Practice. Clinical Gastroenterology and Hepatology. 2015; 13:27-36.
- Yoshioka K, Kawabe N, Hashimoto S. Transient elastography: applications and limitations. Hepatol Res. 2008; Volume 38, Issue 11, November, Pages 1063-1068.
- https://hepatitiscnewdrugs.blogspot.ro/p/fibroscan-scoring-card-understanding. html, updated dec 2017
- Coco B, Oliveri F, Maina AM, et al. Transient elastography: a new surrogate marker of liver fibrosis influenced by major changes of transaminases. Journal of viral hepatology. 2007; 14 (5):360-369.
- Fraquelli M, Rigamonti C, Casazza G, et al. Reproducibility of transient elastography in the evaluation of liver fibrosis in patients with chronic liver disease. Gut. 2007; Jul 56(7):968-73.
- Lupsor M, Badea R, Ştefănescu H, et al. Performance of a new elastographic method (ARFI technology) compared to unidimensional transient elastography in the noninvasive assessment of chronic hepatitis C. Preliminary results. J Gastrointestin Liver Dis. 2009;18:303-310.
- Sporea I, Sirli RL, Deleanu A, et al. Acoustic radiation force impulse elastography as compared to transient elastography and liver biopsy in patients with chronic hepatopathies. Ultraschall Med. 2011 ; Jan, 32 Suppl 1:S46-52.
- Schiavon LL, Luz J Schiavon N, José de Carvalho-Filho R. Non-invasive diagnosis of liver fibrosis in chronic hepatitis C. World J Gastroenterol. 2014; Mar 21, 20(11): 2854-2866.
- Hu X, Qiu L, Liu D, Qian L. Acoustic Radiation Force Impulse (ARFI) Elastography for non-invasive evaluation of hepatic fibrosis in chronic hepatitis B and C patients: a systematic review and meta-analysis. Med Ultrason. 2017; Jan 31, 19(1):23-31.
- Serai SD, Trout AT, Sirlin CB. Elastography to assess the stage of liver fibrosis in children: concepts, opportunities, and challenges. Clin. Liver Dis. 2017; 9:5-10.
- Zaleska-Dorobisz U, Pawluś A, Kucharska M, Inglot M. SWE elastography in assessment of liver fibrosis. Postepy Hig Med Dosw (Online). 2015; Feb 15; 69:221-6.
- Gerber L, Kasper D, Fitting D, et al. Assessment of liver fibrosis with 2-D shear wave elastography in comparison to transient elastography and acoustic radiation force impulse imaging in patients with chronic liver disease. Ultrasound Med Biol. 2015; Sep 41(9):2350-9.
- Bisnar VJ et al. Comparison of the Accuracy of Shear Wave Elastography and Acoustic Radiation Force Impulse in Determining Liver Fibrosis among Patients with Chronic Liver Disease. EC Gastroenterology and Digestive System. 2017; 3:88-99.
- Bercoff J, Tanter M, Fink M. Supersonic shear imaging: a new technique for soft tissue elasticity mapping. IEEE Trans Ultrason Ferroelectr Freq Control. 2004; Apr; 51(4):396-409.
- Sirli R, Bota S, Sporea I, et al. Liver stiffness measurements by means of supersonic shear imaging in patients without known liver pathology. Ultrasound Med Biol. 2013; Aug, 39(8):1362-7.
- Yoon HM, Cho YA, Kim JR, et al. Real-time two-dimensional Shear-wave elastography for liver stiffness in children: Interobserver variation and effect of breathing technique. Eur J Radiol. 2017; Dec, 97:53-58.
- Lee MS, Bae JM, Joo SK, et al. Prospective comparison among transient elastography, supersonic shear imaging, and ARFI imaging for predicting fibrosis in nonalcoholic fatty liver disease. PLoS One. 2017; Nov 27, 12(11):e0188321.
- Serai SD, Yin M, Wang H, et al. Cross-vendor validation of liver magnetic resonance elastography. Abdom Imaging. 2015; 40:789-794.
- Serai SD, Towbin AJ, Podberesky DJ. Pediatric liver MR elastography. Dig Dis Sci. 2012; 57:2713-2719.
- Xanthakos SA, Podberesky DJ, Serai SD, et al. Use of magnetic resonance elastography to assess hepatic fibrosis in children with chronic liver disease. J Pediatr. 2014; Jan.,vol. 164, Issue 1, 186-188.



