Managementul clinic și de diagnostic al sindromului Cushing la câine
Abstract
The therapeutic approach in hyperadrenocorticism is essential in managing this pathological condition, helping in the control, through adequate medication, of this disease. Periodic check-ups and paraclinical exams represent a major component in establishing or changing, if necessary, the dosages of elected drugs, but also in evaluating the patients’ response to therapeutic plan.Keywords
therapeutic managementHACdogRezumat
Abordarea terapeutică a hiperadrenocorticismului prezintă o mare importanță în managementul acestei condiții patologice, deoarece permite menținerea sub control, prin medicație corespunzătoare, a acestei afecțiuni. Controalele periodice și examenele paraclinice reprezintă o coordonată majoră în stabilirea sau modificarea, unde este cazul, a dozelor din schema terapeutică, dar și în evaluarea răspunsului la tratamentul prestabilit.Cuvinte Cheie
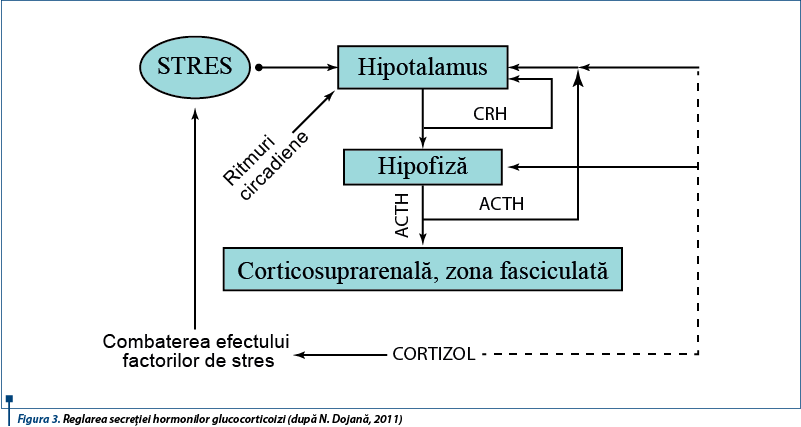
management terapeuticHACcâineSindromul Cushing (hiperadrenocorticismul) presupune o secreţie excesivă de cortizol, putând fi hipofizo-dependent (frecvent procese neoplazice de tipul microadenoamelor și mai rar adenocarcinoame) sau corticodependent, din cauza unor tumori primare la nivelul corticosuprarenalei, mai rar hiperplaziei bilaterale. Mai poate fi provocat de leziuni diencefalice sau de administrări prelungite de glucocorticoizi (hiperadrenocorticism iatrogenic).
În caz de tumori corticosuprarenale (maligne sau benigne) se instituie hiperglicemie prin neoglucogeneză crescută, crește secreţia de insulină, ceea ce determină o sinteză crescută de grăsimi, cu instalarea obezităţii (adipozitate centripetă).
Factorii care determină aceste dereglări pot fi de origine endocrină (tiroidieni - medicaţie excesivă cu extracte tiroidiene, săruri de iod, inflamaţii sau neoplasme tiroidiene, sau hipofizari - adenom bazofil al adenohipofizei, ce duce la o secreţie de tireotrop) sau de origine nervoasă, precum excitaţiile nervoase grave, encefalitele, formaţiunile tumorale, distonii neurovegetative.
Sindromul Cushing poate fi hipofizo-dependent (frecvent procese neoplazice de tipul microadenoamelor și mai rar adenocarcinoame) sau datorat unor tumori primare la nivelul corticosuprarenalei ori hiperplaziei bilaterale. Mai poate fi provocat de leziuni diencefalice sau de administrări prelungite de glucocorticoizi (hiperadrenocorticism iatrogenic).
Glucocorticoizii:
- Stabilizează membrana celulară.
- Scad permeabilitatea capilară și măresc vasoconstricția.
- Acțiune orexigenă - stimulează apetitul.
- Stimulează secreția glandelor fundice și de tripsină.
- Stimulează secreția de tripsină.
- Cresc depozitele de grăsime și de glicogen în hepatocite.
- Suprimă activitatea sistemului imunitar.
- Cresc depozitele de grăsime, în special în abdomen.
- Determină slăbirea mușchilor și atrofia lor.
- Determină subțierea pielii.
HAC de origine hipofizară:
- Micro- și macroadenoame, adenocarcinoame.
- Secreție de ACTH în exces, cortizol în exces.
- Hiperplazie suprarenală bilaterală.
HAC de origine suprarenală:
- Tumori ale corticalei suprarenalelor.
- Nu sunt întotdeauna funcționale.
- În 10% din cazuri sunt bilaterale.
- 50% sunt adenoame benigne, 50% sunt adenocarcinoame maligne.
- 50% din tumori se mineralizează.
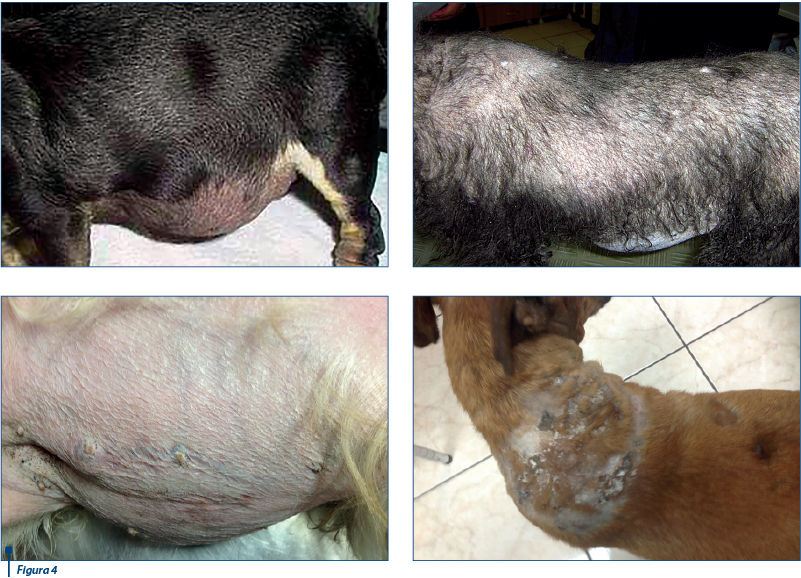
Clinic, se înregistrează constant PU/PD, polifagia, ptoza abdominală, îngroșarea pielii, alopecie simetrică dorsală bilaterală, slăbiciune musculară, obezitate, tulburări sexuale, hipercheratoză și calcinoză cutanată, calcificări ectopice, sensibilitate la infecţii, hipertensiune arterială, slăbiciune musculară (cu amiotrofie), rareori tulburări nervoase și exoftalmie.
Poliuria este un semn clinic extrem de comun în sindromul Cushing, densitatea urinară este <1.020 (în peste 75% din cazuri, iatrogene sau „naturale”), dar poate scădea chiar la 1.001. Cauza poliuriei este deficitul secundar și reversibil de ADH (diabet insipid central).
La aceasta se mai adaugă intoleranţă la căldură, osteoporoză, hipercalcemie, hiperglicemie, creșterea corticosteroizilor plasmatici și urinari.
Analizele de laborator evidenţiază constant creșteri ale activităţii fosfatazei alcaline și transaminazelor serice (în special ALAT), ale valorilor colesterolului seric și scăderea sau situarea la limita inferioară a valorilor ureei serice.
Modificări paraclinice
- Hipertensiune
- Proteinurie
- Tromboembolism
- Neutrofilie, monocitoză, limfopenie
- ALP mărit
- ALT ușor mărit
- Colesterol, trigliceride mărite
- 10% din cazuri au diabet.
Examen de urină
- Densitatea este mai mică de 1.015-1.020
- Poate concentra până la 1.025-1.035
- Proteinurie frecventă
- Sediment inactiv
- 46% din cazuri au infecții ale tractului urinar inferior.
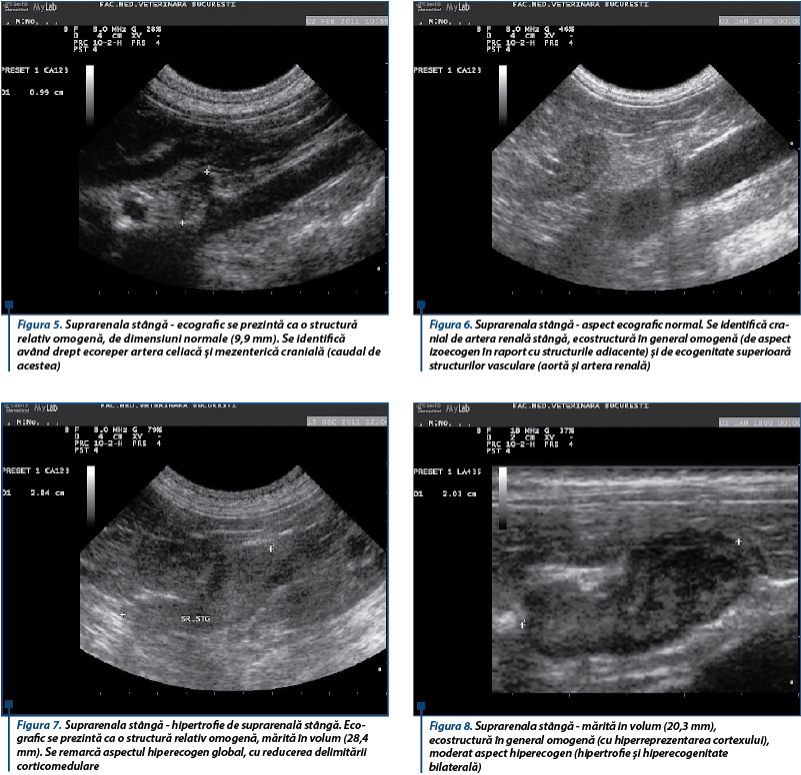
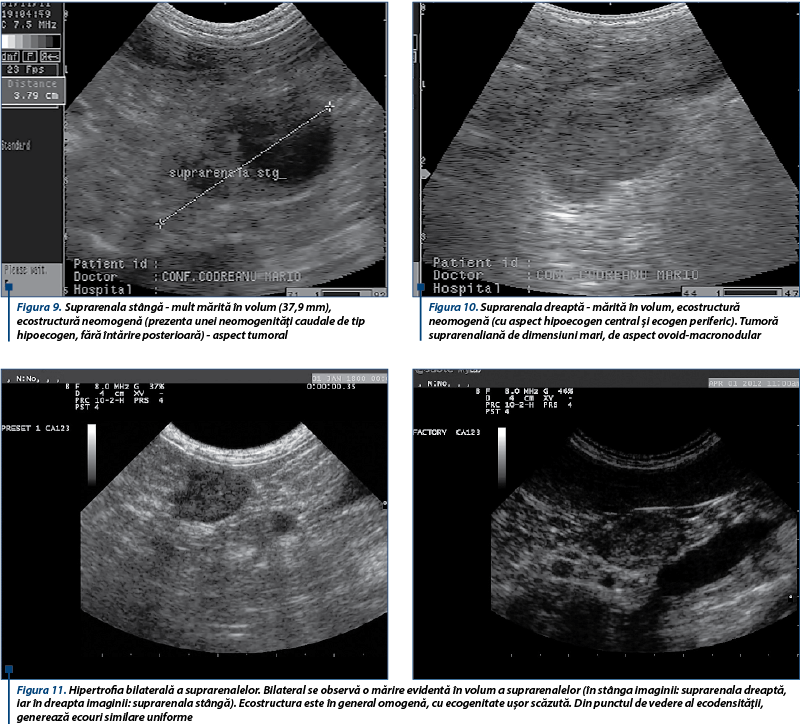
Evaluarea ecografică permite cu mare ușurinţă aprecierea modificărilor de volum, topografie, contur, ecostructură și ecogenitate, cu importanţă și semnificaţie diagnostică ridicată.
Pentru examinarea ecografică, se poziţionează pacientul în decubit dorsal sau lateral, recomandându-se vizualizarea suprarenalelor în axul lung (plan sagital și plan dorsal) și în axul scurt, vizând morfologic lungimea, grosimea (aspectul ventral/dorsal) și înălțimea (medial spre lateral). Pentru identificarea și aprecierea suprarenalei stângi (mai ușor) se recomandă obținerea unei imagini sagitale a rinichiului stâng, ulterior prin înclinarea sondei se identifică aorta cu cele două ramuri ale arterei celiace și arterei mezenterice craniale, iar caudal de acestea și anterior de artera renală stângă se află suprarenala stângă. Lungimea suprarenalelor este corelată cu talia și vârsta animalului, în mod obișnuit, înălțimea neavând aceeași corelație directă. Suprarenala stângă are următoarele repere dimensionale: lungime 17,4 mm (13,2-26,3), înălțime 4,1 mm (3-5,2), iar cea dreaptă: lungime 16,7 mm (12,4-22,6) și înălțime 4,3 mm (3,1-6).
Sunt organe pereche, plate, bilobate, la câine suprarenala stângă având formă de arahidă, iar suprarenala dreaptă având formă de săgeată. Din punct de vedere ecografic, sunt hipoecogene și omogene (deseori au o ecogenitate similară cu a vaselor de sânge din vecinătate), se pot distinge foarte greu (Dopplerul poate ajuta la identificare), iar joncțiunea corticomedulară se poate distinge cu o sondă de înaltă frecvență (peste 7,5 MHz). Ambele suprarenale sunt localizate cranial și medial față de rinichi, suprarenala stângă se află caudal de cele două ramuri ale aortei (artera celiacă și artera mezenterică cranială) și cranial de artera renală stângă, iar suprarenala dreaptă se află adiacent sau peste suprafața venei cave caudale.
Criteriile ecografice de apreciere a dimensiunii recunosc: mărire unilaterală simetrică, mărire unilaterală asimetrică, mărire bilaterală simetrică și mărire bilaterală asimetrică (simetria se face prin compararea polului caudal față de cel cranial al unei suprarenale).
Diagnosticul imagistic (radiografic, ecografic și computer tomografic) poate confirma existenţa substratului lezional suspicionat.
Dominantele clinice sunt suficient de sugestive pentru suspicionarea diagnosticului: sindromul PU-PD, alopecia simetrică dorsală, ptoza abdominală, hepatomegalia, polifagia, slăbiciunea musculară (amiotrofia), tulburări ale ciclului estral (anestru)/atrofie testiculară, hiperpigmentarea, calcificările cutanate (calcinoza).
Paraclinic, cu specificitate ridicată sunt și creșteri ale activităţii ALAT și ASAT, hiperlipidemia, scăderea nivelului ureei serice, hiperglicemia, hipofosfatemia, scăderea densităţii urinare (<1.015-1.020) și proteinuria.
Confirmarea presupune teste funcţionale hipofizare și ale suprarenalelor: testul de stimulare cu ACTH și testul cu dexametazonă.
Testul de stimulare cu ACTH
Acesta presupune măsurarea răspunsului suprarenalelor la stimularea cu ACTH (cortrosyn, synacthen). Recoltarea probelor se face cu două ore înainte și după administrarea a 2,2 UI/kg cortrosyn/synacthen. Valoarea normală a cortizolului este 0,5-6 mg/dl, iar post-administrare: 6-17 mg/dl. Valorile de peste 22 mg/dl confirmă hiperadrenocorticismul.
Testul cu dexametazonă
La câinele sănătos, concentraţia cortizolului plasmatic scade la 2-3 ore după administrarea dexametazonei și rămâne scăzută timp de 24-48 de ore. La câinii cu hiperadrenocorticism, suprarenalele sunt rezistente la efectul supresor al dexametazonei (0,01 mg/kg - probe recoltate înainte cu 4 ore și, respectiv, după 8 ore de la administrarea i.v.). La câinele sănătos, concentraţia cortizolului este mai mică de 1,4 mg/dl, la 4 și 8 ore de la administrarea dexametazonei. În situaţiile în care concentraţia cortizolului, la 8 ore după administrare, este egală sau mai mare de 1,4 mg/dl, se confirmă prezenţa hiperadrenocorticismului.
În cazul HAC de origine hipofizară, examenul ecografic al suprarenalelor se folosește pentru a diferenţia sindromul Cushing hipofizar de tumorile suprarenaliene (glandele suprarenale pot avea dimensiuni în limite fiziologice), și nu pentru a diagnostica HAC.
În HAC de origine suprarenală (formaţiuni tumorale de suprarenală) se constată imposibilitatea diferenţierii între formaţiunea tumorală de corticală, pheocromocitom, leziuni metastatice, hiperplazie și ţesut normal doar prin examinarea ecografică, ecogenitatea putând apărea fie omogenă, fie mixtă.
Tratamentul HAC presupune abordarea terapeutică pentru ambele forme (central și periferic), însă, practic, singura modalitate de „vindecare” a bolii Cushing este îndepărtarea tumorii glandei suprarenale (în cazul în care aceasta este dependentă de formaţiunea tumorală și în absenţa metastazelor). Cu toate acestea, tehnicile chirurgicale de îndepărtare a formaţiunilor tumorale pituitare la canide sunt încă supuse studiului, astfel încât intervenţia chirurgicală nu este o opţiune în prezent.
Printre opţiunile schemei de tratament disponibile în prezent se regăsesc Lysodren (Mitotan, o,p’-DDD), Vetoryl (Trilostane, Modrenal), Ketoconazol (Nizoral). În 2008, Trilostane (Vetoryl) a fost singurul medicament aprobat de FDA (Food and Drug Administration) pentru a trata atât sindromul Cushing corticodependent, cât și cel periferic. Acesta acţionează prin stoparea producerii de cortizol la nivelul glandei suprarenale. Și Seleginina (Anipryl) este aprobată de FDA pentru tratamentul bolii Cushing la câine, dar este recomandată doar în cazurile de boală dependentă de glanda pituitară, fără complicaţii. Doza iniţială este 0,45 mg/0,5 kg/zi. Dacă nu se observă rezultate după o perioadă de 2 luni, se poate crește doza la 0,9 mg/0,5 kg/zi. Se poate recurge și la folosirea chimioterapicelor de uz uman, Mitotan (Lysodren), ce distrug straturile glandei suprarenale care produc cortizol, nefiind însă eficiente în sindromul Cushing periferic. Administrarea acestui chimioterapic necesită monitorizare atentă și poate avea efecte secundare severe. Perioada de inducţie este 50 mg/kg/zi, divizate în două administrări pe zi. După perioada de inducţie se administrează 25-50 mg/kg/săptămână (se poate, de asemenea, diviza în mai multe administrări).
Bibliografie
1. Barker, E.N., Campbell, S., Tebb, A.J., Neiger, R., Herrtage, M.E., Reid, S.W.J., Ramsey IK. (2005) - A comparison of the survival times of dogs treated with mitotane or trilostane for pituitary-dependent hyper-adrenocorticism. J. Vet. Intern. Med. 19, 810-815.
2. Benchekroun, G., de Fornel-Thibaud, P., Lafarge, S., Gomes, E., Begon, D., Delisle, F., Moraillon, R., Heripet, D., Maurey, C., Rosenberg, D. (2008). Trilostane therapy for hyperadrenocorticism in three dogs with adrenocortical metastasis. Vet. Rec. 163, 190-192.
3. Bourdeau I, Lampron A, Costa MH, Tadjine M, Lacroix A. (2007) – Adrenocorticotropic hormone-independent Cushing’s syndrome. Curr Opin Endocrinol Diabetes Obes. 2007 Jun;14(3):219-25.
4. Clemente, M., De Andrés, P.J., Arenas, C., Melián, C., Morales, M., Pérez-Alenza, M.D. (2007). Comparison of non-selective adrenocorticolysis with mitotane or trilostane for the treatment of dogs with pituitary-dependent hyperadrenocorticism. Vet. Rec.161, 805-809.
5. Codreanu M. (2008) - Sindromul poliuro-polidipsic. abordare clinică și terapeutică diferenţiată la câine și pisică, 12 nov 2008 – Sinaia, Simpozionul A.M.V.A.C.
6. Codreanu M. și col. (2009) – Studiu privind importanţa examenului ecografic în diagnosticul afecţiunilor suprarenalelor la câine, Lucr. știinţifice, vol.52(11), p.483-486, Iași.
7. Codreanu M. și col. (2011) - Relevanţa examenului ecografic al suprarenalelor În sindromul Cushing la câine, Congresul Naţional de Medicină Veterinară, București.
8. Ettinger J. Stphen; Feldman C. Edward (2010) - Textbook of Veterinary Internal Medicine - seventh edition – vol II.
9. Feldman E. (2005) - An update on the diagnosis of Cushing’s Syndrome in Dogs, Presented at the Wisconsin Veterinary Medical Association Convention, Madison, Wisconsin.
10. Galac, S., Buijtels, J., Mol, J., Kooistra, H. (2010) - Effects of trilostane treatment on the pituitary-adrenocortical and renin-aldosterone axis in dogs with pituitary-dependent hypercortisolism. Vet. J. 183, 75-80.
11. Galac, S., Reusch, C.E., Kooistra, H.S., Rijnberk A. (2010) - Adrenals. In: Rijnberk, A., Kooistra, H.S., eds. Clinical Endocrinology of Dogs and Cats, 2nd ed. Hannover, Germany, Schlütersche. pp. 93-154.
12. Lahera Vargas M, da Costa CV. (2009) - Prevalence, etiology and clinical findings of Cushing’s syndrome, Endocrinol Nutr. 2009 Jan; 56(1):32-9. Epub 2009 Mar 1.
13. Marin (Ivașcu) Gabriela, Maria Crivineanu, M. Codreanu (2011) – Study regarding the relevance of ultrasound examination in uterine diseases – associated with polyuria-polydipsia syndrome in bitch - “Contribution of the scientific research to veterinary medicine progress”, FMV București.
14. Marin (Ivașcu) Gabriela, Maria Crivineanu, M. Codreanu (2012) – Clinical and paraclinical changes in Cushing`s syndrome in dogs, Simpozionul “Contribution of the scientific research to veterinary medicine progress”, FMV, București.
15. Peterson ME. (2011) - What’s the Differential Diagnosis of Polydipsia and Polyuria in Dogs and Cats? Veterinary endocrinology.
16. Sieber-Ruckstuhl, N., Boretti, F., Wenger, M., Maser-Gluth, C., Reusch, C. (2006) - Cortisol, aldosterone, cortisol precursor, androgen and endogenous ACTH concentrations in dogs with pituitary-dependent hyperadrenocorticism treated with trilostane. Domest. Anim. Endocrinol, 31, 63-75.
17. Vaessen, M., Kooistra, H.S., Mol, J.A., Rijnberk, A. (2004). Urinary corticoid: creatinine ratios in healthy pet dogs after oral low-dose dexamethasone suppression tests. Vet. Rec. 155, 518-521.
18. Van der Vlugt-Meijer, R.H., Meij, B.P., van den Ingh, T.S.G.A.M., Voorhout, G. (2003) - Dynamic computed tomography of the pituitary gland in dogs with pituitary-dependent hyperadrenocorticism. J. Vet. Intern. Med. 17, 773-780.
19. Witt, A.L., Neiger, R. (2004). Adrenocorticotropic hormone levels in dogs with pituitary-dependent hyperadrenocorticism following trilostane therapy. Vet. Rec. 154, 399-400.
20. Wood, F.D., Pollard, R.E., Uerling, M., Feldman, E. (2007). Diagnostic imaging findings and endocrine test results in dogs with pituitary-dependent hyperadreno-corticism that did or did not have neurologic abnormalities: 157 cases (1989-2005). J. Am. Vet. Med. Assoc. 231, 1081-1085.
