Managementul urgenţelor oncologice veterinare
Management of veterinary oncologic emergencies
Abstract
The emergency situation in oncology can be defined as a pathological condition determined by the clinical evolution of cancerous paraneoplastic syndromes or a consequence of the chemotherapy disease (metabolic, hematological, neurological, motor). Assessing the diagnosis and performing specific therapy should be rapid and address the syndromes in the order of their severity. The diagnosis of the oncology patient’s emergency must be determined in the order of priority and type of emergency: morphological or obstructive paraneoplastic syndromes caused by solid tumors with organ and/or metabolic compression caused by functional failure of tissues or organs; chemotherapy disease toxicity induced through iatropathy, following the administration of chemotherapy medication. The objectives in solving oncological emergencies are the diagnosis of the cause, the clinical and paraclinical evaluation and very rapid therapy. Paraneoplastic syndromes may be due only to primary or associated tumors of lymph node invasion, visceral metastases, or may be the consequence of established therapies: surgical, chemotherapy, hormonal. Oncology emergency may be aggravated by preexisting liver disease, kidney disease, hematologic disease, neurological disease, disease evolution or therapy-associated. The urgency of oncological therapy is to control pain, restore blood volum, to amend the paraneoplastic symptoms (anemia, cachexia, thrombocytopenia, lymphopenia) and eventually restore the morphostructural palliative integrity of affected tissues. The choice of therapeutic strategy and the combination of techniques and methods are made personalized according to the clinical condition of the oncology patient at the time of diagnosis by anamnesis, general physical examination, TNM clinical staging, monitoring of vital functions, histopathological type and the appreciation of the response to the therapies already performed.Keywords
oncologyemergencyparaneoplasticchemotherapydiseaseRezumat
Situaţia de urgenţă în oncologie poate fi definită ca o afecţiune patologică determinată de evoluţia clinică a sindroamelor paraneoplazice canceroase sau o consecinţă a bolii chimioterapice (metabolice, hematologice, neurologice, motorii). Evaluarea diagnosticului şi efectuarea terapiei specifice ar trebui să fie rapide şi să se refere la sindroame în ordinea gravităţii lor. Diagnosticul de urgenţă al pacientului oncologic trebuie determinat în ordinea priorităţii şi a tipului de urgenţă: sindroame paraneoplastice morfologice sau obstructive cauzate de tumori solide, cu compresie de organe şi/sau metabolice, cauzate de eşecul funcţional al ţesuturilor sau al organelor; boala citostatică indusă prin iatropatie după administrarea chimioterapiei. Obiectivele de rezolvare a situaţiilor de urgenţă oncologice sunt diagnosticarea cauzei, evaluarea clinică şi paraclinică şi terapia foarte rapidă. Sindroamele paraneoplazice se pot datora tumorilor primare sau asociate ale invaziei limfopatologice, metastazelor viscerale sau, poate, sunt consecinţa terapiilor stabilite: chirurgicale, chimioterapice, hormonale. Boala canceroasă poate fi agravată de afecţiuni hepatice preexistente, afecţiuni renale, afecţiuni hematologice, afecţiuni neurologice, de evoluţia bolii sau terapia asociată. Urgenţa terapiei oncologice este aceea de a controla durerea, de a restabili volumul sângelui, de a controla simptomele paraneoplazice (anemie, caşexie, trombocitopenie, limfopenie) şi, eventual, de a restabili integritatea paliativă morfostructurală a ţesuturilor afectate. Alegerea strategiei terapeutice şi combinaţia dintre tehnici şi metode se fac personalizate, în funcţie de starea clinică a pacientului oncologic la momentul diagnosticării prin anamneză, de evaluarea generală a examinării fizice, stadializarea clinică a TNM, monitorizarea funcţiilor vitale, tipul histopatologic şi de aprecierea răspunsului la terapiile deja efectuate.Cuvinte Cheie
oncologieurgenţeparaneoplazicchimioterapieboalăIntroducere
Urgenţa oncologică reprezintă o condiţie acută determinată de cancer sau de tratamentul oncologic, necesitând o intervenţie rapidă pentru a preveni moartea sau instalarea unor disfuncţii severe permanente. Înainte de a stabili un plan terapeutic adecvat, se vor preciza stadializarea şi răspunsul la tratamentul actual, precum şi prognosticul general. În funcţie de tabloul clinic, urgenţa poate fi datorată unor tumori primare, adenopatiilor, metastazelor, tratamentului, unei noi condiţii sau agravării unei condiţii preexistente, fără relaţie cu boala canceroasă.
Urgenţele oncologice ar putea fi clasificate în:
-
urgenţe obstructive sau structurale datorate tumorilor înlocuitoare de spaţiu (durerea);
-
urgenţe datorate problemelor metabolice sau hormonale (caşexia, anemia);
-
urgenţe secundare tratamentului oncologic (boala citostatică).
Efectele terapiilor asociate (chimioterapie citostatică, radio-, imuno-, hormonoterapie, inclusiv chirurgia oncologică) induc cumulativ agravarea unor stări patologice, preexistente, ca sindroame paraneoplazice, dar pot fi şi generatoare a unora noi, sub forma efectelor secundare, reacţii de apărare sau adverse, în urma interacţiunii celulelor tumorale sau sănătoase cu substanţele citostatice sau cu produşii de metabolism rezultaţi.
Rezultate şi discuţii
Urgenţe oncologice structurale şi obstructive:
-
Sindromul de compresiune venoasă
-
Sindromul de compresiune medulară
-
Boala tromboembolică.
Sindromul de compresiune venoasă (SCV) apare odată ce tumora comprimă vena în traseul său. Obstrucţia venoasă poate fi datorată compresiei, invaziei, trombozei sau fibrozei venei. Rezultă o creştere a presiunii venoase centrale şi apariţia circulaţiei colaterale frecvent cu derivaţie. Deşi este considerată o urgenţă clasică, rareori pune imediat viaţa în pericol, însă urgenţa poate deveni reală prin inducerea unei creşteri a presiunii intracraniene, cu edem cerebral. Tumorile maligne primare, cancerele bronhopulmonare, limfoamele şi tumorile mediastinale şi metastazele sunt responsabile de peste 80% din toate cazurile de SCV.
Cauzele non-maligne sunt deosebit de rare şi includ: tuberculoza, fibroza mediastinală post-iradiere sau idiopatică, o cauză cu frecvenţă în creştere la pacientul oncologic fiind utilizarea pe scară tot mai largă a cateterelor venoase centrale.
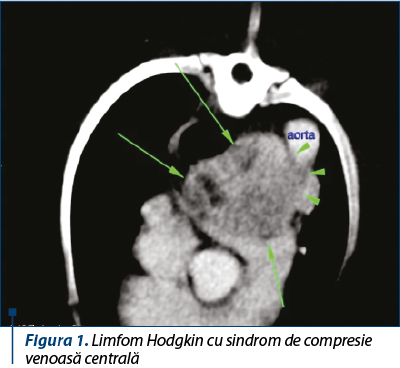
Diagnosticul se stabileşte clinic relativ uşor; în stadiile iniţiale, SCV poate fi confundat cu insuficienţa cardiacă (trăsătura de diferenţiere fiind absenţa pulsaţiilor jugularelor şi absenţa tahicardiei şi a galopului).
Simptomele sugestive pentru SCV constau în edemul progresiv al gâtului, urmat de edemul facial şi al braţului, dispneea asociată cu compresia traheală, edemul capului, gâtului şi toracelui (edem în pelerină), ectazii venoase superficiale pe faţa anterioară a toracelui.
Proceduri care pot fi utilizate în diagnostic sunt: radiografia, bronhoscopia, toracotomia minimă sau toracoscopia, venografia, examenul CT şi examenul RMN.
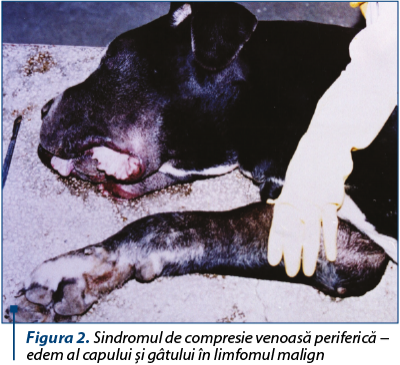
Dacă diagnosticul de certitudine nu poate fi stabilit imediat, tratamentul activ se poate amâna până la efectuarea unei investigaţii mai amănunţite. Amânarea este chiar indicată la tineret, la care sunt suspectate şi alte etiologii. Iniţial pacienţii pot fi trataţi simptomatic cu oxigenoterapie pentru dispnee, furosemid 20-40 de miligrame intravenos, pentru a reduce edemul, şi dexametazonă sau hidrocortizon în doze mari pentru reducerea inflamaţiei. Odată diagnosticul stabilit, pacientul trebuie tratat prin:
-
radioterapie (mai ales dacă afecţiunea primară este un cancer bronhopulmonar non-microcelular)
-
chimioterapie, dacă se presupune că tumora este un limfom sau o tumoră germinală.
Sindromul de compresie medulară este o adevărată urgenţă oncologică şi survine la 1-5% din pacienţii cu cancere sistemice, atunci când tumora primară sau metastazele determină un efect de masă sau compresiune spinală cu deficit neurologic. Amânarea terapiei poate conduce la instalarea unei paralizii ireversibile, la pierderea funcţiilor intestinale şi ale vezicii urinare. Aceasta, din cauza în special a metastazelor situate în afara durei mater (95%), care invadează coloana vertebrală. Localizarea cea mai frecventă este toracică (70%), urmată de cea lombosacrată (20%) şi cervicală (10%). Între 10% şi 40% din cazuri sunt multifocale, implicarea primară a spaţiilor epidurale fiind mai puţin frecventă. Deşi compresiunea medulară apare într-o varietate foarte largă de neoplazii, cel mai frecvent implicate sunt: cancerul de prostată, de plămâni, metastazele cu punct de plecare neprecizat, neoplasmul renal, limfomul, mielomul şi melanomul.
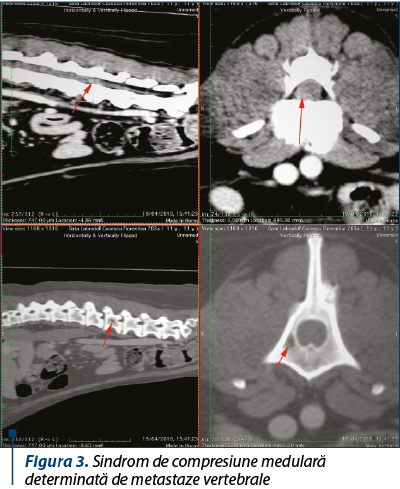
Primul pas în diagnosticul paraclinic îl constituie istoricul şi examenul neurologic, semnele precoce fiind: durere localizată la nivelul coloanei sau al orificiilor radiculare (>90%), tuse, strănut, încordarea muşchilor.
În ceea ce priveşte semnele intermediare şi tardive, acestea sunt reprezentate de: astenia accentuată, precedată sau însoţită de tulburări senzoriale, tulburări de mers, retenţie de urină, constipaţie.
După apariţia acestor simptome, compresiunea medulară progresează de obicei rapid, determinând, în lipsa tratamentului, paralizie ireversibilă în câteva ore sau zile.
Examenul fizic poate evidenţia localizarea durerii la nivelul vertebrelor implicate sau al teritoriului de distribuţie al nervului implicat, senzaţia de consistenţă scăzută la palpare sau percuţie a splinei de la nivelul metastazei, astenie musculară, spasticitate, reflexe osteotendinoase anormale, tulburări senzoriale.
Investigaţiile imagistice utile sunt:
-
Radiografia vertebrală – mai mult de 66% din pacienţii care vin cu compresiune medulară prezintă anomalii osoase pe radiografiile convenţionale, ce constau în eroziuni sau dispariţia pediculilor osoşi, colapsul parţial sau complet al corpilor vertebrali, prezenţa de mase paraspinale de ţesut moale.
-
Imagistica prin rezonanţă magnetică – un semnal anormal, fără prezenţa spaţiului corespunzător discului intervertebral, sugerează posibilitatea unei infecţii, fiind eficientă evaluarea compresiunii medulare toracice.
Examenul CT şi mielografia confirmă diagnosticul clinic.
Obiectivele tratamentului – recuperarea şi menţinerea funcţiei neurologice normale, controlul local al tumorii, stabilizarea coloanei vertebrale, controlul durerii şi evitarea complicaţiilor. Alegerea tratamentului depinde de starea pacientului în momentul diagnosticului, de posibilitatea obţinerii diagnosticului histologic, de evoluţia clinică a bolii, tipul de neoplazie, localizarea la nivelul coloanei vertebrale, stabilitatea coloanei şi de tratamentul anterior.
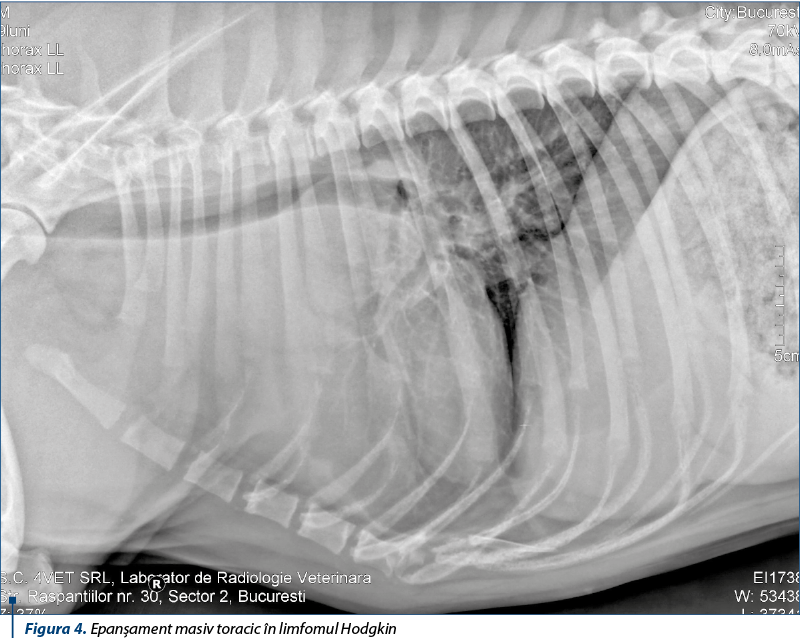
Boala tromboembolică (BTE)
Tromboza asociată cancerului este recunoscută ca o cauză frecventă de mortalitate şi morbiditate la pacienţii cu boală malignă. Boala tromboembolică, cunoscută şi sub termenul de tromboembolism venos (TEV), include un spectru larg de manifestări, de la cea mai frecventă – tromboza venoasă acută (TVA) – la cele mai severe – tromboza venoasă profundă (TVP) şi embolia pulmonară (EP).
Riscul crescut de tromboză este datorat eliberării de către tumoră a unui factor tisular cu efect procoagulant, responsabil pentru declanşarea cascadei de coagulare extrinsecă. Riscul cel mai crescut este asociat cu tumorile cerebrale, ovariene, pancreatice, prostatice, pulmonare şi renale. Factorii de risc asociaţi cu BTE pot fi clasificaţi ca:
Endogeni
-
Activitate procoagulantă tumorală (ţesut tumoral, factor tisular)
-
Răspunsul inflamator (factorul de necroză tumorală, interleukina 1)
-
Anomalii de coagulare (trombocitoză, activare plachetară, creşterea nivelului de fibrinogen, activarea coagulării).
Extrinseci
-
Agenţii citotoxici, terapia hormonală, factorii de creştere hematopoietici (risc de TVP: 2-30%)
-
Radioterapia (risc de TVP: 3-8%)
-
Staza venoasă (compresie extrinsecă, mobilitate redusă, spitalizarea îndelungată)
-
Traumatismul venos sau arterial (cateterele - risc de TVP: 10-50%, risc de EP: 1-5%)
-
Intervenţiile chirurgicale prelungite.
Pleurezia prezintă incidenţă crescută în cancerul pulmonar, ovarian şi în limfoame maligne. Cauzele sunt: pleurezita carcinomatoasă sau metastazele pleurale, care reprezintă perturbarea fluxului limfatic, insuficienţa cardiacă sau deficitul proteic.
Terapia constă în administrarea de citostatice pe cale generală (carboplatin, gemcitabină, holoxan), asociate cu diuretice osmotice (manitol) sau de ansă (furosemid).
Oncohematopatologia
Modificările liniei sangvine albe în limfoame
În majoritatea cazurilor, limfoamele câinelui sunt aleucemice, cel puţin la începutul maladiei, şi nu se găsesc semne sangvine ale afecţiunii; pentru Parodi (1972), doar 20% din cazuri erau semnalate printr-o leucemie. Această leucemie e variabilă şi imprevizibilă, aparent fără legătură cu distribuţia tumorală, cu excepţia infiltraţiilor difuze ale măduvei osoase, care sunt invariabil reflectate prin variaţii în sângele periferic. Într-un stadiu avansat al maladiei, o treime din cazurile de leucoză limfoidă ar fi leucemice, după Lombard (1968).
Obişnuit, numărul celulelor albe este puţin crescut la început, apoi se manifestă o leucocitoză moderată, de 20.000-30.000 (Altman). Această leucocitoză înseamnă un răspuns exagerat al măduvei. Dar, în formele leucemice, numărul globulelor albe este mult crescut: 150.000 (Jacquier), 320.000-629.000 (Conceicao), 580.000 (De Schepper), 1.079.000 (Backgren).
Formula leucocitară suferă, de asemenea, mari variaţii în formele leucemice sau aleucemice. În formele aleucemice, formula leucocitară permite punerea în evidenţă a unei neutrofilii, cel mai adesea cu indicele Arneth deviat spre stânga.
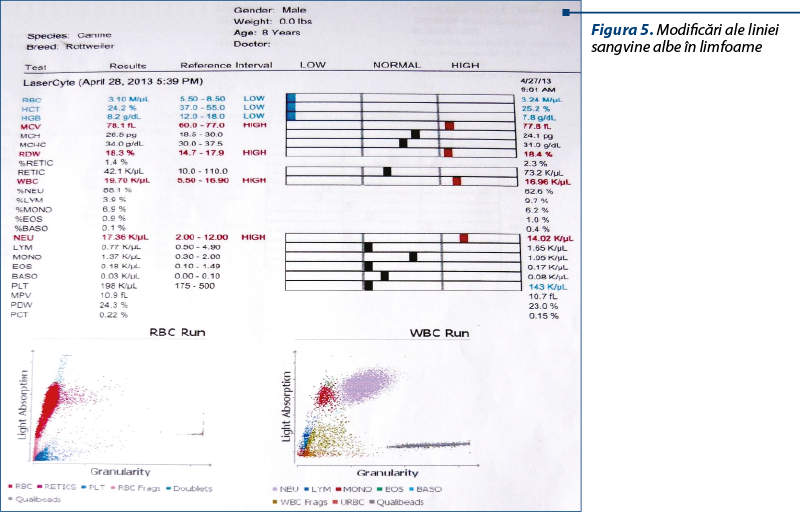
Această neutrofilie este explicabilă printr-un răspuns exagerat al măduvei osoase la progresia tumorii şi la fenomenul de necroză; poate, de asemenea, apărea o mielopoieză la nivelul splinei şi ficatului, care, asociată activităţii măduvei osoase, explică această neutrofilie, mai ales în timpul perioadei de agravare a maladiei. Pentru Meier, această neutrofilie, care regresează adeseori după utilizarea antibioticelor, ar fi din cauza suprainfecţiilor frecvente. În celelalte cazuri observăm, paradoxal, o limfopenie. O limfocitoză poate surveni izolată sau asociată neutrofiliei (Backgren). Howard, într-o formă cutanată, constată o eozinofilie care atinge 31% înainte de a reveni la 10-15%. În formele leucemice, observăm o limfocitoză foarte marcantă, aceste celule putând atinge 99% din celulele albe, ca într-un caz citat de De Schepper, cu 580.000 de globule albe. Este vorba deci, cel mai adesea, de limfoblaşti rotunzi, voluminoşi, cu nucleu bazofil excentric, cu o cromatină fin dispersată, fără condensări, cu nucleoli sau fără, a căror citoplasmă redusă este albastru-bleu palid, putând prezenta o zonă Golgi perinucleară clară. Aceste celule sunt fragile şi se sparg uşor când se realizează etalarea, dând celule în paner sau pete.
Frecvent, leucocitele prezente sunt celule reticulare cu caractere morfologice histiocitare. Uneori, în cazul invadării măduvei de către celule neoplazice, înlocuirea acesteia cu ţesut neoplazic sau mieloptizia provoacă pasajul în sânge al celulelor imature, mielocite, metamielocite sau mieloblaşti, care, în absenţa altor examene pentru precizarea diagnosticului, pot antrena o confuzie cu o leucoză mieloidă.
Modificările liniei sangvine roşii
Într-un stadiu avansat al maladiei, constatăm o anemie normocromă, normocitară; numărul globulelor roşii poate scădea sub 2.000.000/mm³ (Niemand). Nivelul hemoglobinei relevat de Backgren era inferior valorii de 11,5 g/100 ml la 40% dintre câini. Această anemie se explică printr-o stare proastă a câinilor, dar şi prin faptul că serul câinilor cu limfosarcon are o activitate hemolitică crescută. La un câine, Wall găseşte un hematocrit de 14%.
Modificările plachetelor sangvine
În leucozele avansate, trombocitopenia este o regulă, numărul plachetelor poate fi foarte scăzut: 102.000/mm³ (De Schepper, 1974), sub 50.000/mm³ (Mac Coy, 1950). Această trombocitopenie explică accidentele hemoragice constatate în cazul limfoamelor avansate. Pentru Lombard (1968), această trompocitopenie nu ţine de o insuficienţă a trombocitopoiezei.
Viteza de sedimentare
Este obişnuit crescută, dar moderată în limfom, o creştere notabilă putând atinge 100 mm la prima oră; poate fi pusă în relaţie cu infecţiile intercurente sau cu fazele evoluţiei maladiei. O viteză de sedimentare importantă este nefavorabilă pentru prognostic pentru că ea semnifică evoluţia afecţiunii sau o complicaţie infecţioasă asociată unei anemii intense cel mai adesea.
Terapia este de substituţie prin transfuzie de homogrup sau prin administrare de factori specifici de stimulare a hematopoiezei pe linia sangvină afectată.
Urgenţele oncologice metabolice
Sindromul de caşexie canceroasă este o manifestare clinică şi metabolică paraneoplazică patognomonică a bolii canceroase în ansamblul ei, caracterizată prin afectări ponderale grave ale organismului în cauză, neimpunându-se implicarea afecţiunilor gastrointestinale. Alterările induse de cancer în metabolismul energetic al gazdei sau caşexia canceroasă sunt probabil cele mai comune sindroame paraneoplazice în medicina umană şi veterinară. Caşexia este specifică fazelor avansate, terminale, ale bolii canceroase, fiind determinată de o pronunţată alterare metabolică sistemică, având drept consecinţă afectarea metabolismului protidic. Este determinată în special de tumorile maligne cu localizare digestivă, pulmonară sau a aparatului reproducător. Terapia se bazează pe administrarea hranei speciale adecvate şi a aminoacizilor esenţiali perfuzabili.
Modificări biochimice sangvine
Transaminazele (ALT - GPT)
Prezintă variaţii nespecifice şi neregulate. Valorile găsite variază de la normal la 900 U.S.F., dar cel mai comun dozajele permit determinarea unor niveluri de 120-400 U.S.F.
Colesterolemia
Apare mai ales în afectările organice. Hipercolesterolemia este frecventă, dar nu invariabilă în insuficienţa hepatică.
Electroforeza proteinelor serice
Pentru Guelfi, leucozele câinelui nu se asociază decât cu perturbări prea inconstante şi variabile pentru a fi interesante, semnele nefiind modificate decât la sfârşitul evoluţiei şi în cursul diverselor complicaţii.
P. Groulade, J. Groulade şi C. Ollivier consideră că această tehnică are o valoare de prognostic. Modificările sunt foarte discrete la început, dar în cursul unei faze evolutive notăm o scădere a albuminelor, acompaniată cel mai adesea de o creştere a a2-globulinelor, în timp ce g-globulinele se diminuează. Groulade semnalează în cazul leucozelor limfoide cronice o creştere a g-globulinelor, dar această formă este dificil de definit clinic la câine. Howard, într-o formă cutanată, semnalează o hipergamaglobulinemie cu un nivel de b-globuline la limita superioară.
Hipoalbuminemia reprezintă principala cauză a reducerii nivelului seric al calciului la pacienţii cu boală severă. Alcaloza prin hiperalcalinizare conduce la creşterea calciului legat de proteine şi determină reducerea consecutivă a nivelului de calciu ionizat care trebuie măsurat. Administrarea de plasmă integrală sau compuşi medicamentoşi cu aminoacizi poate corecta deficitul de albumină serică.
Glicemia
Este normală în majoritatea cazurilor, dar uneori constatăm o hipoglicemie netă (De Schepper, 1974), fără ca pentru aceasta să apară simptome legate de scăderea nivelului glucozei sangvine.
Hipoglicemia. La om, tumorile din cavitatea toracică sau abdominală sunt asociate cu hipoglicemie, aceasta fiind datorată producerii unei substanţe analoge insulinei (Somals, 1963) sau utilizării excesive de glucoză de către marile mase tumorale, cu un deficit în glucogeneză (Tashima, 1968). Această deficienţă a glucogenezei ar fi cauzată de o afectare hepatică, împiedicând funcţia glicogenică şi antienzimatică antiinsulină, din cauza unei compresiuni a vaselor sau nervilor.
Calcemia şi fosfatemia
Hipocalcemia este o manifestare directă a hiperfosfatemiei, fiind definită ca un nivel al calciului seric mai redus de 2,1 mmoli/l; totuşi, numai 10% dintre aceşti pacienţi prezintă diminuarea calciului ionizat. Hipocalcemia poate provoca uneori simptome semnificative clinic: spasme musculare sau, în cazurile mai grave, tetanie, spasm laringian sau convulsii.
Hipercalcemia, definită drept creşterea concentraţiei serice a calciului ionizat peste limitele normale, este cea mai frecventă perturbare metabolică la pacienţii cu cancer, putând surveni în asociere cu metastazele osoase, dar şi în absenţa oricărei afectări directe; trebuie diferenţiată de creşterea nivelurilor de calciu seric prin hiperparatiroidism.
Hiperkaliemia reprezintă principala perturbare electrolitică potenţial fatală, definită ca o creştere a nivelului plasmatic al potasiului peste 5 mmoli/l, din cauza eliberării detritusurilor celulare prin liza celulară. Cele mai severe manifestări sunt aritmia ventriculară, creşterea amplitudinii undei T, adesea cu aspect ascuţit, alungirea intervalelor PR şi QRS, blocuri A-V şi flutter.
Hiponatremia este o anomalie cu potenţial letal cu cauze multiple. Hiponatremia prin supraîncărcare volemică este cauzată de acumularea de fluide în compartimentul extracelular, prin reducerea volumului circulant. În cea de-a doua situaţie, este o manifestare a unei varietăţi de boli. Sindromul secreţiei inadecvate de hormon antidiuretic trebuie luat în considerare.
Uremia şi creatinemia
Sunt crescute în tumori hematopoietice sau sarcoame, semnalând un defect de funcţionare renală, până la o prăbuşire completă a acestor organe. Creşterea nivelului ureei şi creatininei sangvine înrăutăţeşte prognosticul. Trebuie investigată sistematic, pentru că ele pot semnala o insuficienţă renală; există cazuri particulare în care se observă o hipercalcemie cu normofosfatemie, neasociate cu o tulburare de epurare renală. Este vorba de un fenomen endocrin paraneoplazic, în genul pseudohiperparatiroidismului. Aceste sindroame endocrine paraneoplazice au fost descrise la om în hematosarcoame şi alte tumori. La câine, Osborne şi col. (1973) au studiat acest fenomen, iar De Schepper semnalează un caz care poate fi asociat acestui sindrom. Nivelul calciului seric crescut este deseori asociat cu limfomul cu celule T (Putro 2001). În limfoame, hipercalcemia poate fi din cauza metastazelor osoase, şi în acest caz este asociată cu o hiperfosforemie, pentru că osteoliza este astfel crescută, încât rinichii şi intestinul sunt incapabili de a resorbi electroliţii sangvini. În cazul pseudohiperparatiroidismului, calcemia este crescută, dar există hipofosfatemie şi fără metastaze osoase. Acest sindrom are loc din pricina secretării de către ţesutul tumoral a unei particule hormonale comparabile parathormonului. Apariţia unui asemenea sindrom înrăutăţeşte prognosticul, pentru că hipercalcemia severă antrenează o hipercalciurie şi tulburări renale secundare unei nefrocalcinoze, rapid letale. Un asemenea sindrom trebuie diferenţiat de un hiperparatiroidism primar sau unul secundar, renal, deoarece conduita terapeutică va fi diferită.
Fosfatazele alcaline
Sunt markeri tumorali sangvini indirecţi, permiţând şi aprecierea afectării hepatice; creşterea lor presupune şi că ficatul va detoxifia atunci mai greu organismul de produsele utilizate pentru tratament şi de produsele de degradare a celulelor tumorale distruse.
Lactodehidrogenaze
Sunt crescute în limfosarcomul câinelui, mai ales fracţiunea LDH3. Valorile normale, care sunt 50-80 U/ml, ajung pentru câinii limfomatoşi la 125-400 U/ml. Boni (1972) citează chiar o valoare de 1300 U/ml într-un caz.
Analizele de urină
Densitatea urinei
În formele renale sau cu afectare renală se constată hipostenurie, adică o lipsă de concentraţie, care se manifestă prin scăderea densităţii.
Proteinuria
Este frecventă în afectările renale; este adesea asociată cu hematurie, când leziunile renale sunt importante.
Bilirubinuria
Apare în timpul invaziei ficatului de către procesul neoplazic.
De fapt, aceste variaţii urinare semnalează diseminarea cancerului şi nu sunt caracteristice afecţiunii (Ducos de Lahitte, 1977).
Imunosupresia în oncologie
La o serie de afecţiuni maligne, ca de exemplu leucemiile acute, leucemiile cronice sau mielomul multiplu, există imunodepresie constantă, independentă de tratamentul efectuat. Este de presupus că imunodeficienţa la aceste boli este dată de interferenţa celulelor maligne cu celulele corespunzătoare normale, prin producerea unor factori supresori de transfer (Roitt, 1994), nefiind vorba de obicei (în lipsa unei afecţiuni imunodepresive cunoscute anterior) de imunodepresie, care să preceadă afecţiunea respectivă.
În cazul bolii Hodgkin există o scădere a imunităţii celulare încă din stadiile I şi II ale bolii. Ulterior, se semnalează disfuncţii în activitatea macrofagelor, monocitelor şi a celulelor B. „Imunitatea tumorală” este însă modificată, răspunsul în anticorpi la diverse antigene este scăzut. Se consideră totuşi că depresia imunităţii tumorale este tranzitorie, putând reveni la normal după tratament. În ansamblu, profilul imunitar al bolii Hodgkin se caracterizează prin: scăderea capacităţii limfocitului T de a reacţiona la mitogeni, creşterea activităţii limfocitelor T supresoare, raportul CD4/CD8 diminuat, scăderea activităţii celulelor natural killer.
Limfoamele non-hodgkiene prezintă, de asemenea, deficit atât pe linie T, cât şi pe linie B, imunodeficitul fiind influenţat de tipul de celulă (T sau B) care proliferează.
Leucemiile acute sunt caracterizate prin producerea şi acumularea de leucocite anormal maturate. Se constată blocarea maturării celulelor mieloide sau limfoide în stadiile primare de evoluţie, respectiv la nivelul stadiului de blast. Aceste celule imature se vor infiltra în sângele periferic, măduvă şi ulterior în ţesuturi. Liniile de limfocite care proliferează pot fi T (sau pre-T), limfocite B (sau pre-B) în aproximativ 80% din cazuri sau limfocite nule în 20% din cazuri. Deficitul imun se instalează progresiv, mai ales prin înlocuirea clonelor normale de limfocite cu clone tumorale, care sunt alcătuite din limfocite imature, incapabile de exercitarea funcţiei lor imunitare. Există şi presupunerea că ar fi inhibate clonele normale de cele tumorale prin factori supresori.
În leucemiile cronice, imunodeficitul este cel mai puţin bine exprimat, din cauza proliferării mai lente a clonelor (sau clonei) tumorale, precum şi a faptului că celulele care proliferează sunt blocate din dezvoltare în fazele imature. În cazul leucemiei limfatice cronice, în 90% din cazuri, proliferarea este a limfocitelor B, celulele anormale reprezentând o singură clonă. De cele mai multe ori, se poate întâlni reducerea valorilor imunoglobulinelor M, urmată de reducerea IgG şi IgA. Deficienţe în funcţionalitatea limfocitelor T şi B sunt frecvente. Există tendinţa de a dezvolta şi alte tipuri de cancere.
Urgenţele secundare tratamentului oncologic – boala citostatică:
-
Sindromul de icter indus
-
Emeza
-
Sindromul enteric
-
Nefrita interstiţială acută
-
Sindromul de cistită hemoragică
-
Sindromul hematocitotoxic central
-
Sindromul hematocitotoxic periferic
-
Imunosupresia citostatică
-
Trombocitopenia
-
Sindromul lizei tumorale acute.
Boala citostatică reprezintă totalitatea sindroamelor patologice induse de medicaţia citostatică organismului canceros. Întregul complex de simptome care apar consecutiv acţiunii neselective asupra întregului organism a terapiei citostatice a fost denumit prin analogie cu efectele bolii de iradiere. Tratamentul cu chimioterapice citostatice presupune doze mari, la limita toxicităţii minime pentru fiecare drog, determinând o boală citostatică cu simptomatologie şi intensitate diferită: slabă, moderată sau severă.
Sindromul de icter indus reprezintă sindromul de acumulare în exces a bilirubinei conjugate în ţesuturi sau în curentul sangvin. Clinic se evidenţiază icter la nivelul pielii pigmentate, mucoaselor, scleroticii şi palatului moale.
Icterul se prezintă sub forma:
-
Prehepatică – determinată de anemie autoimună hemolitică
-
Hepatică – determinată de supradozarea medicamentoasă a citostaticelor din grupa alkilanţilor
-
Posthepatică – indusă de tumori ale vezicii biliare
-
Extrahepatică – determinată de stenoza compresivă a canalului coledoc.
Emeza reprezintă simptomul caracteristic de reflux al conţinutului gastric, determinat de afectarea tubului digestiv. Aceasta poate fi:
-
Precoce – determinată de administrarea unui citostatic pe cale orală cu absorbţie digestivă (ciclofosfamidă)
-
Tardivă – se declanşează în urma unor tratamente îndelungate cu antimetabolitul 5-fluorouracil
-
Ultraprecoce – se bazează pe reflexul pavlovian în urma experienţelor avute înainte de administrarea citostaticelor.
Sindromul enteric se bazează pe existenţa a două acţiuni la nivelul tranzitului intestinal: diareea şi constipaţia.
Diareea apare consecutiv acţiunii iritative locale a unor citostatice sau tratamente parenterale în doze mari şi pe perioade îndelungate, care accentuează peristaltismul.
Constipaţia apare în urma tratamentului cu antimitotice, determinând tulburări ale tranzitului intestinal.
Nefrita interstiţială acută
Histologic, se constată proliferare limfoplasmocitară şi rare granulocite periglomerular, peritubular şi perivascular. În spaţiul capsulei Bowman apare uneori material proteic, iar în glomerul, proliferare endotelială.
Sindromul hematocitotoxic central
Efectul depresiv asupra celor trei sisteme hematoformatoare, respectiv mielomonocitar, limfo- şi megacariocitopoietic, constituie un indicator obiectiv al aprecierii efectului terapiei citostatice asupra celor stem. Substanţele medicamentoase citostatice, inhibitoare ale mitozei în special, au un efect limitat asupra celulelor sangvine mature diferenţiate (eritrocite, granulocite, monocite, trombocite, limfocite) circulante.
Sindromul hematocitotoxic periferic
Evaluând modificările citologice din sângele periferic comparativ cu cele de la nivelul măduvei hematopoietice, se observă o evoluţie în oglindă. Astfel, numărul granulocitelor din sângele periferic este în scădere după administrarea fiecărui citostatic, iar fenomenul reconversiei este vizibil după 48 de ore de la tratament (prin mobilizarea rezervelor celulare din limfonoduri, pentru ca după 11 zile alterările să fie mai dramatice).
Sindromul de cistită hemoragică reprezintă sindromul patogenic determinat de administrarea în doze mari şi repetate a ciclofosfamidei ca agent alkilant, iar degradarea oxidativă a acesteia determină apariţia unor metaboliţi urotoxici la nivel hepatic sub formă de acroleină şi cloroacetaldehidă.
Imunosupresia citostatică reprezintă un sindrom care afectează iniţial imunitatea mediată celular şi apoi cea mediată umoral, fiind datorată unor mecanisme precum: inhibarea proliferării la nivelul celulelor stem, distrugerea celulelor imunocompetente circulante sau fixe, diminuarea concentraţiei de anticorpi circulanţi.
Trombocitopenia este determinată de citoliza megacariocitară la nivel medular central prin efect inhibitor metabolic. Clinic, se manifestă printr-un sindrom de purpură hemoragică, consecutiv administrării de ciclofosfamidă sau busulfan.
Sindromul lizei tumorale acute reprezintă un sindrom postterapeutic citostatic observat la câine consecutiv polichimioterapiei citostatice, tumorilor maligne voluminoase, limfoamelor non-hodgkiniene în stadiul IV, cu visceralizare şi leucemii în stadii avansate. Se datorează lizei rapide a celulelor tumorale, care eliberează cantităţi mari de potasiu şi fosfor în circulaţia generală. Se caracterizează prin aspecte de tip anafilactic, iar manifestările cuprind: colaps cardiovascular, bradicardie, tahipnee, deshidratare.
Concluzii
Urgenţele oncologice se diferenţiază de cele obişnuite din cauza gravităţii extreme a bolii, sindroamele paraneoplazice suprapunându-se peste efectele bolii citostatice.
Alterările metabolice oncologice sunt direct proporţionale cu stadiile evolutive ale bolii.
Hematopatologia neoplazică se caracterizează prin anemie, trombocitopenie şi granulocitoză, asociate cu imunosupresie.
Caşexia canceroasă este sindromul asociat stadiilor clinice avansate, fiind cel mai complex, însumând toate sindroamele paraneoplazice metabolice, insuficienţa hepato-renală fiind de obicei urgenţa majoră a pacienţilor cu neoplasme maligne în faze terminale.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Andres FA. Descripcion de tres casos clinicos de osteosarcomas en perros. Revista clinica de pequenos animales. 1997; 17 (4), 227-235.
- Bacci G, Picci P, Ferrari S et al. Primary chemotherapy and delayed surgery for non-metastatic osteosarcoma of the extremitites. Results in 164 patients preoperatively treated with high doses of methotrexate followed by cisplatin and doxorubicin. Cancer. 1993 Dec 1; 72(11):3227-38
- Baker R, Lunsden JH. Color atlas of cytology of the dog and cat. Mosby Inc. 2000; 199-208.
- Bohndorf K. Magnetic resonance imaging of primary tumors and tumours-like lesions of the bone. Skeletal Radiology. October 1986, Volume 15, Issue 7, 511–517.
- Crînganu D. Patologia animalelor de companie. Oncologie generală, ed. a II-a revizuită şi adăugită. Editura Printech, 2009.
- Crînganu D, Crivineanu M. Terapie oncologică veterinară. Editura Printech, 2009.
- Cooley DM, Waters DJ. Skeletal neoplasms in small dogs: a retrospective study and literature review. Journal of Am. Animal Hospital Association. 1997; 33 (1), 11-23.
- Drelise F, Devauchelle P. Les osteosarcomes du chien. Le point veterinaire. 1996; 27 (2), 65-67.
- Eilber FR, Rosen G. Adjuvant chemotherapy for osteosarcoma. Semin Oncol. 1989 Aug; 16(4):312-22.
- Flores AJ. Osteosarcoma osteogenico: descripcion de un caso clinico. Medicina Veterinaria. 1996; 13 (2), 124-127.
- La Rue SM, Withdrow SJ, Wrigley RH. Radiographic Bone Surveys in the evaluation of primary bone tumors in dogs. J Am Vet Med Assoc. 1986.
- Morton MM, Townsend CM. Limb salvage from a multidisciplinary treatment approach for skeletal and soft tissue sarcoma of the extremity. Ann Surg. 1976 Sep; 184(3):268-78.
- Matthieusen DT, Clark GN, Orsher RJ, Pardo AO, Glennon J, Patnaik AK. En bloc resection of primary rob tumors in 40 dogs. Vet Surg. 1992 May-Jun; 21(3):201-4.
- Pastorino U, Valente M, Santoro A et al. Results of a salvage surgery for metastatic sarcomas. Ann Oncol. 1990 Jul; 1(4):269-73.
- Stevenson S. Fracture-associated sarcoma. Vet. Clin. North. Am. Small Animal Pract. 1991 Jul; 21(4):859-72.
- Teracini B, Glickman LT. Host-related risk factors for canine osteosarcoma. The veterinary Journal. 1998; 156 (1), 31-39.
- White RAS. Manual of small animal oncology. British Small Animal Veterinary Association. 1991; 265-280.
- Yasko AW, Somlo MD. Bone sarcomas in cancer management. 1996.

