Schizophrenia is rightly considered the most severe psychiatric disorder, in which the therapeutic results are still below the expectations predicted after the development of clinical farmacology and after using in clinical practice various molecules with antipsychotic effect. The low-quality results are even more surprising, as the diagnostic accuracy based on statistical nosographic criteria became better and more frequent, and the biological and translational psychiatry allowed the development of multifactorial pathogenic models. The practical reality puts the clinician into a real intelectual dilemma, because the statistical nosographic criteria are not supported by the explicative pathogenic models. As a result, in current practice the symptomatic therapeutic strategies are predominant, the pathogenic interventions being scotomized. In these circumstances, the presentation of some clinico-biological argument is intended to get the nosographic model closer to the medical model of the diseases, calling for reflection on the therapeutic decision on schizophrenia.
Modele patogenice diferenţiate implicate în evoluţia defavorabilă a schizofreniei
Differential pathogenic models involved in the unfavorable evolution of schizophrenia
First published: 27 aprilie 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Psih.52.1.2018.1630
Abstract
Rezumat
Schizofrenia este considerată, pe bună dreptate, cea mai severă tulburare psihiatrică, în care rezultatele terapeutice sunt încă sub aşteptările previzionate prin dezvoltarea farmacologiei clinice şi prin utilizarea în practica terapeutică a unei diversităţi de molecule cu efect antipsihotic. Rezultatele de slabă calitate sunt cu atât mai surprinzătoare, cu cât acurateţea diagnostică bazată pe criterii nosografice de tip statistic a câştigat în amplitudine şi în utilizare, iar psihiatria biologică şi translaţională a permis elaborarea unor modele patogenice multifactoriale. Realitatea practică pune clinicianul într-o veritabilă dilemă intelectuală, întrucât criteriile nosografice de tip statistic nu sunt susţinute de modele explicative patogenice. În consecinţă, predomină în practica curentă strategiile terapeutice de tip simptomatic, scotomizându-se intervenţiile de tip patogenic. În aceste condiţii, prezentarea unor argumente clinico-biologice urmăreşte apropierea modelului nosografic de modelul medical al bolilor, îndemnând la reflecţii asupra deciziei terapeutice în schizofrenie.
Dezvoltarea psihofarmacologiei clinice a permis, pe baza studiilor translaţionale, implementarea modelelor patogenice în schizofrenie, demonstrându-se o variabilitate importantă a acestora, confirmându-se anticiparea lui E. Bleuler, care nu a vorbit despre schizofrenie, ci despre grupul schizofreniilor.
Facem precizarea că în momentul actual există, practic, o ruptură între conceptul descriptiv nosografic, reprezentat de manualele de diagnostic statistic ICD 10 şi DSM 5, care uniformizează conceptul teoretic al schizofreniei şi stabilesc criterii diagnostice care, în opinia noastră, nu acoperă modelele patogenice ale tulburării psihiatrice majore care este schizofrenia. Această discrepanţă conduce la eludarea principiilor medicale generale în intervenţia terapeutică, principii care se adresează specific unui conflict etiopatogenic, şi nu rezultantei epifenomenale a acestui conflict. Constanţa fenomenelor simptomatice poate fi rezultanta unor modele patogenice diferite, ceea ce conduce la intervenţii terapeutice predominant simptomatice, care pot rezolva un simptom sau un set de simptome, dar nu rezolvă conflictul etiopatogenic, determinând evoluţii defavorabile sau chiar rezistenţă terapeutică (figura 1).
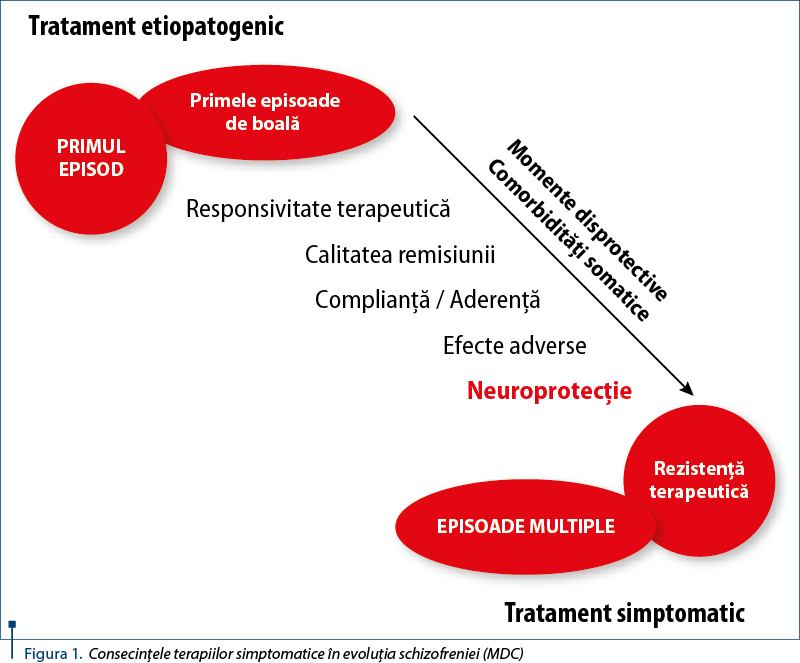
Recunoaşterea modelului medical al bolii în tulburarea schizofrenică permite evaluarea corectă a fiecărui caz în parte, în funcţie de parametrii psihopatologici, neurobiologici, dar şi de implicarea unor factori de comorbiditate somatici care particularizează, practic, fiecare pacient şi reprezintă, din punctul nostru de vedere, baza conceptului de medicină personalizată.
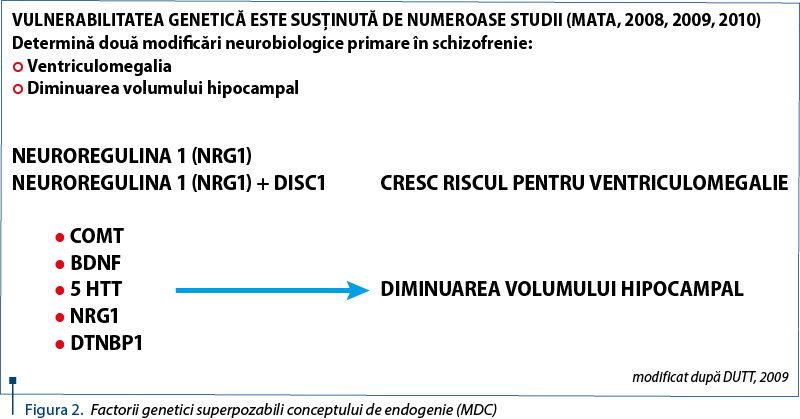
Integritatea structurală şi funcţională cerebrală reprezintă o variantă apropiată de vechiul concept de „endogenie” în care dominanţa factorilor genetici determină vulnerabilitatea genetică (figura 2), susţinută de numeroase studii care corelează varianţele genetice cu două modificări neurobiologice primare în schizofrenie:
- ventriculomegalia – element semnalat de şcoala germană de psihiatrie condusă de Huber încă din 1960, ca factor de predicţie a evoluţiei defavorabile a schizofreniei şi a rezistenţei terapeutice. Ventriculomegalia poate fi interpretată ca o consecinţă a encefalopatiei hipoxice-ischemice şi a leucomalaciei periventriculare sau a modificărilor de tip vascular de la nivelul substanţei albe, apărute pe parcursul evoluţiei bolii şi în legătură cauzală potenţială cu mecanismele vasculare de tip leucoaraiozic favorizate de disfuncţia endotelială, activarea microglială şi a proceselor proinflamatoare sau de patologia vasculară cerebrală, consecinţă a sindromului cardiometabolic sau a diabetului zaharat (comorbidităţi considerate ca efecte adverse ale medicaţiei psihotrope);
- diminuarea volumului hipocampal – marker biologic al deficitului cognitiv, consecinţă a activărilor glutamatergice primare, hiperglutamatergia determinând apoptoza şi disconectivitatea între zonele hipocampale CA1 (cornul lui Amon 1) şi CA3, precum şi la nivelul girusului dentat (DG). Volumul hipocampal poate fi diminuat şi prin mecanisme de activare glutamatergică secundare generate de hipercortizolemia endogenă, consecinţă a stresului, prin hiperactivitatea axei hipotalamo-hipofizo-corticosuprarenaliene (Axa HPA) sau a apoptozei generate de blocajul excesiv al receptorilor de tip D2, prin intervenţia terapeutică excesivă şi pe termen lung cu substanţe antipsihotice (figura 3).
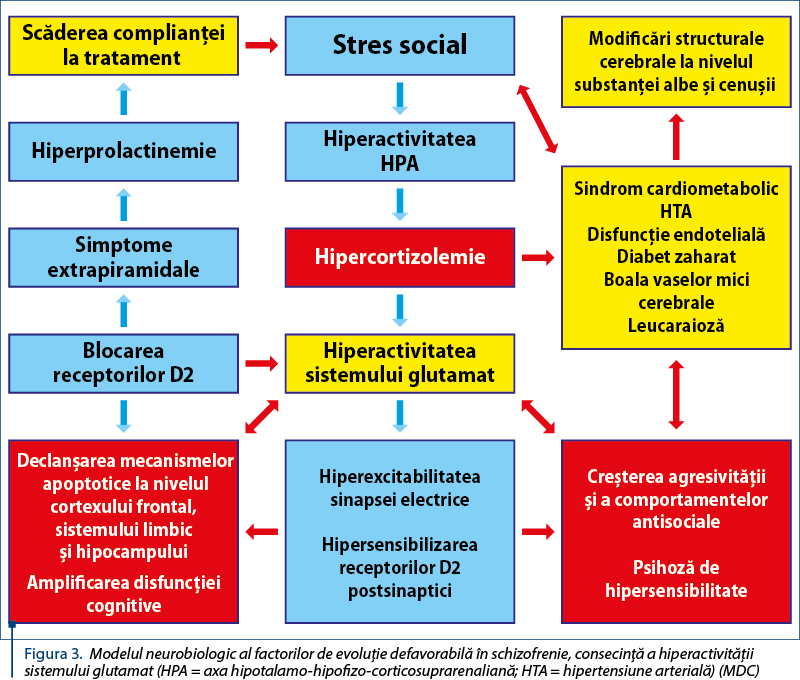
Studiile epidemiologice au evidenţiat factori genetici importanţi care determină în principal o disconectivitate primară la nivelul circuitelor cognitive de tip integrativ, în care informaţia cognitivă este rezultanta prelucrării datelor senzitivo-senzoriale trecute prin filtrul învăţării/experienţei mnezice („learning memory”) şi confruntate cu memoria de lucru, flexibilitatea decizională şi coloratura afectiv-emoţională. Toate aceste date de neuropsihologie beneficiază, în condiţiile normalităţii, de procesul de reechilibrare prin interrelaţionare reciprocă, determinând o expresie comportamentală şi un nivel de funcţionalitate socială armonic cu cerinţele etico-sociale. Acest proces integrativ „normal” al informaţiei cognitive este consecinţa rezervei conective individuale, dependentă de conservarea zonelor de neurogeneză de la nivelul periventricular şi al zonei granulare subventriculare, precum şi al zonei granulare de la nivelul girusului dentat al hipocampului.
Alterarea integrităţii structurale şi funcţionale cerebrale, consecinţă a modelului etipatogenic de tipul anomaliilor de neurodezvoltare, determină disconectivitatea secundară, în care vulnerabilitatea circuitelor cognitive de tip integrativ este mult mai evidentă, fiind semnalate precoce semne neurologice minime anterioare oricărei intervenţii terapeutice cu substanţe psihotrope, semne de tip piramidal şi extrapiramidal, ataxie cerebeloasă, dificultăţi de coordonare în mişcările fine şi a mersului, precum şi deficite de învăţare, consecinţă a microleziunilor focale din sistemul limbic şi cortexul fronto-temporo-parietal, cu apariţia fenomenelor de tip dislexic şi dispraxic, pe modelul sindromului de minimă leziune cerebrală.
Aprioric, disconectivitatea primară necesită implicarea neuroregulinei 1 (NRG1), structură celulară de adeziune moleculară codată la nivelul genei NRG1, şi a „Disrupted in schizophrenia 1” (DISC 1), structură proteică cu varianţă genetică la nivelul genei DISC1, care pot fi factorii genetici care controlează rezerva de conectivitate prin asigurarea unei neurogeneze de tip compensator care poate reechilibra deficitele circuitelor cognitiv integrative. Depistarea precoce a varianţelor genetice NRG1 şi DISC1 poate anunţa o alterare a capacităţii de reechilibrare conectivă. În această situaţie, se impune din partea clinicianului o abordare terapeutică care să nu permită agravarea alterării neurogenezei sau perturbarea capacităţilor de neuroprotecţie.
Acceptând premisa de lucru validată de majoritatea ghidurilor terapeutice, dar în dezacord cu conceptul psihofarmacologic al adecvanţei terapeutice, care urmăreşte abordul patogenic, în prezenţa fenomenelor psihotice de tip pozitiv (halucinaţii, delir, dezorganizare comportamentală), se vor utiliza antipsihotice cu capacitate de blocare predominant la nivelul receptorilor de tip D2 ai excesului dopaminergic. Utilizarea pe termen lung a acestei strategii terapeutice atrage după sine modificări ale constantei de neurotransmisie dopaminergică, determinând efecte neurobiologice defavorabile:
Dezechilibrarea între mecanismele fazice de eliberare a dopaminei din structurile de emergenţă (aria tegmentului ventral – ATV şi substanţa neagră – SN), fenomen care va conduce la o hipodopaminergie globală într-o primă fază, cu epuizarea cvasitotală a capacităţilor de eliberare a dopaminei, moment în care se declanşează activitatea hiperglutamatergică, având consecinţe defavorabile clinic (reactivarea simptomelor psihotice pozitive) şi biologice cerebrale (declanşarea mecanismelor apoptotice), cu pierderi neuronale şi ale integrităţii funcţionale a unităţii neuron-astroglie, susţinere vasculară şi metabolică (figura 4).
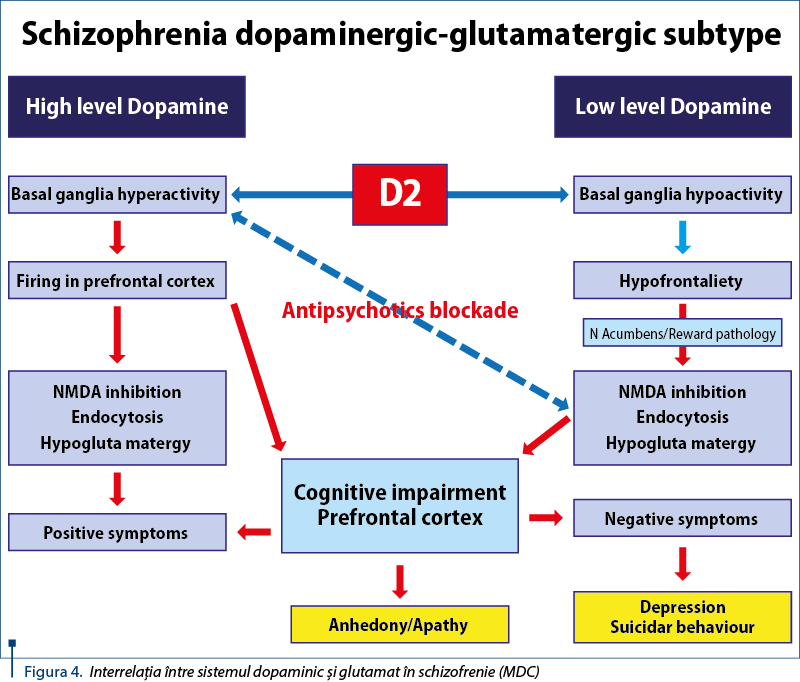
Consecinţele hipodopaminergiei pot fi multiple: de tip neuropsihologic (persistenţa simptomelor negative, intensificarea deficitului cognitiv şi a depresiei, inclusiv a comportamentului suicidar), neurologic (fenomene extrapiramidale, parkinsonism, distonie, acatisie) şi endocrin (hiperprolactinemia, cu creşterea riscului cardiovascular, de neoplasm mamar, de osteoporoză şi creşterea comportamentului de tip agresiv).
Hipodopaminergia se va manifesta la nivelul nucleului accumbens, determinând disfuncţionalitatea mecanismelor de tip „reward”, fenomene implicate în creşterea comportamentelor adictive faţă de mâncare (obezitate, sindrom cardiometabolic), droguri ilicite şi alcool, adicţie sexuală (comportament antisocial de risc, prin posibilitate de contaminare a pacienţilor cu boli transmisibile prin contact sexual – HIV, hepatită tip C, sifilis etc.), gambling patologic, cu consecinţe financiare dezastruoase pentru pacient şi familia sa. În plan psihopatologic, lipsa recompensei determină amplificarea anhedoniei, apatiei şi depresiei, conturând un tablou deficitar de tip lob frontal, precum şi adicţia la droguri ilicite şi alcool, încadrându-se în criteriile nosografice ale patologiei de tip dual.
Este momentul în care este activat sistemul glutamatergic, cu consecinţe neurobiologice dominate de alterările structurale cerebrale, determinate de declanşarea mecanismelor de tip apoptotic.
Disfuncţia integrativă şi conectivă a hipocampului
Declanşarea hiperactivităţii sistemului glutamat la nivelul hipocampului determină în zonele de conectivitate interhipocampică CA1-DG un sindrom metabolic şi de hiperperfuzie vasculară (faza de hipercompensare), care poate fi corelat cu creşterea aspectelor de tip disritmic şi iritativ la evaluarea electroencefalografică (EEG).
Apariţia pe înregistrările EEG a undelor rapide cu hipersincronism de tip Gamma constituie un important marker de tip electrofiziologic, care indică iminenta trecere de la stadiul prodromal la stadiul psihotic, cu alterarea comunicării emisferice şi aplatizarea elementelor electrice, care indică asimetria interemisferică. Scăderea asimetriei interemisferice în cadrul evaluărilor electrofiziologice este considerată ca marker endofenotipal pentru schizofrenie. Prezenţa unor modificări electroencefalografice de tip disritmic, iritativ sau a hipersincronismului Gamma poate anticipa o evoluţie defavorabilă de tip deficitar a schizofreniei.
Etapa patologică propriu-zisă (episodul psihotic acut) este corelată cu hiperactivitatea dopaminică, în special la primele episoade de boală.
Hiperactivitatea sistemului dopaminic se manifestă predominant la nivelul mezolimbic, iar prin activitatea crescută a sistemului glutamatergic se realizează un fenomen de firing excesiv al neuronilor dopaminergici din zona prefrontală, fenomen care este asociat cu apariţia sindromului de hipoperfuzie vasculară şi metabolic, cu amplificarea stresului oxidativ şi declanşarea fenomenelor de excitocitoză şi apoptoză la nivelul cortexului prefrontal şi al conexiunilor acestuia cu circuitele talamocerebeloase.
În lipsa intervenţiei terapeutice adecvate, care să realizeze reechilibrarea transmisiei dopaminice şi să scadă hiperexcitabilitatea pre- şi postsinaptică a sistemului neuronal glutamatergic (timostabilizatoarele din clasa anticonvulsivantelor, modulatorii receptorilor NMDA şi activatori ai sistemului glicin-serină), nu se va putea realiza o reechilibrare a constantelor de neurotransmisie între etajul cortical şi cel subcortical, procesul apoptotic determinând leziuni neuronale progresive care pot fi evidenţiate la evaluările neuroimagistice, devenind indicatori de prognostic defavorabil:
- atrofia cortexului frontal şi a cerebelului
- scăderea volumului hipocampal, cu scăderea capacităţilor cognitive
- pierderea conectivităţii sistemului limbic prin atrofia zonei bazolaterale a amigdalei cerebrale (zonă dopamino-dependentă) şi a circuitului cortico-limbic poate prezice riscul unor manifestări cu caracter antisocial prin creşterea agresivităţii şi a manifestărilor violente de tip impulsiv, exploziv, manifestări care sunt asemănătoare cu tulburările comportamentale ale epilepsiei.
Disfuncţia cognitivă integrativă a hipocampului în schizofrenie, consecinţă a hiperactivităţii sistemului glutamat, poate fi previzionată de indicatori clinico-anamnestici şi paraclinici. Principalii indicatori de acest tip sunt:
- prezenţa în antecedente a encefalopatiei hipoxice – ischemice – hiperglutamatergice a nou-născutului, afecţiune asociată cu creşterea excitotoxicităţii şi a disfuncţiei sistemului de neurotransmisie glutamatergic;
- prezenţa unor manifestări paroxistice neurologice sau EEG (crize convulsive febrile cu anomalii disritmice; iritative EEG – distonia mioclonică);
- existenţa în antecedentele pacientului a terapiilor electroconvulsivante, terapii ce, în mod surprinzător, îşi menţin indicaţiile la un nivel procentual ridicat (55,6%) în unele ţări;
- identificarea în antecedente a unor crize glicemice severe sau a unor manifestări de tip hipertensiune ortostatică, traumatisme craniene minore, dar repetate, care pot determina disfuncţia axonală şi a unor fenomene de hipoxie severă, consecutivă unor evenimente infecţioase respiratorii sau unor disfuncţii cardiovasculare.
Evoluţia de lungă durată a schizofreniei, cu multiple recăderi psihotice şi remisiuni incomplete de tip deficitar, amplifică factorii de risc pentru agravarea disfuncţiei cognitiv-integrative a hipocampului şi amplifică disfuncţionalitatea socială şi riscul pentru manifestări comportamentale antisociale, scăzând calitatea vieţii pacienţilor, prin amplificarea stigmei.
Considerăm că se impune, ca fiind o condiţie de bună practică farmacologică în tratamentul schizofreniei, adecvarea strategiilor terapeutice prin individualizarea modelelor neurobiologice diferenţiate, strategii terapeutice care trebuie să aibă ca ţinte principale recâştigarea controlului şi echilibrului pentru transmisia dopaminergică şi limitarea activităţii excesive a sistemului glutamat sau a hipercortizolemiei produse prin condiţii de stres social.
Conflict de interese: Autorii declară că nu au conflict de interese, iar materialul prezentat reprezintă opinii personale rezultate din experienţa clinică, nefiind rezultatul transpunerii unor date copiate din lucrări de specialitate.
Bibliografie
- Tsai G, Goff DC, Chang RW, Flood BSJ, Baer L, Coyle JT. Markers of Glutamatergic Neurotransmission and Oxidative Stress Associated with Tardive Dyskinesia. Am J Psychiatry. 1998;155:1207–1213.
- Tseng KY, O’Donnell P. Dopamine–Glutamate Interactions Controlling Prefrontal Cortical Pyramidal Cell Excitability Involve Multiple Signaling Mechanisms. The Journal of Neuroscience. June 2, 2004;24(22):5131–5139.
- Rosell DR, Siever LJ. The neurobiology of aggression and violence – CNS Spectrums, page 1 of 26. © Cambridge University Press. 2015;doi:10.1017/S109285291500019X.
- Allen KA, Brandon DH. Hypoxic Ischemic Encephalopathy: Pathophysiology and Experimental Treatments. Newborn Infant Nurs Rev. 2011 September 1;11(3): 125–133. doi:10.1053/j.nainr.2011.07.004.
- Johnson M. Excitotoxicity in neonatal hypoxia. Developmental Disabilities Research Reviews. 2001 Vol.7, 4. 2001;229-234.
- Lieberman JA, Girgis RR, Brucato G, Moore H, Provenzano F, Kegeles L, Javitt D, Kantrowitz J, Wall MM, Corcoran CM, Schobel SA, Small SA. Hippocampal dysfunction in the pathophysiology of schizophrenia: a selective review and hypothesis for early detection and intervention. Molecular Psychiatry 2017; 00, 1–9 www.nature.com/mp.
- Leiknes KA, von Schweder LJ, Hoie B. Contemporary use and practice of electroconvulsive therapy worldwide. Brain and Behavior. 2012;2(3): 283–345 doi: 10.1002/brb3.37.
- Manchanda R, Malla A, Harricharan R, Cortese L, Takhar J. EEG Abnormalities and Outcome in First-Episode Psychosis. Can J Psychiatry, Vol 48, No 11. December 2003.
- Floresco SB, Todd CL, Grace AA. Glutamatergic Afferents from the Hippocampus to the Nucleus Accumbens Regulate Activity of Ventral Tegmental Area Dopamine Neurons. The Journal of Neuroscience. 2001;21(13):4915–4922.
- Zhang L, Doyon WM, Clark JJ, Phillips PEM, Dani JA. Controls of Tonic and Phasic Dopamine Transmission in the Dorsal and Ventral Striatum. Mol Pharmacol. 2009; 76:396–404.