Migraine is a complex neurological pathology that has a major negative impact on people’s health and quality of life. At the same time, it is a global health problem, for which a definitive therapeutic management has not yet been established. This uncertainty is explained by the multilateral aspect of the pathophysiology of migraine, the individual nature of the clinical manifestations presented by patients, as well as the diversity of the level of effectiveness of available treatments. Therefore, the identification of optimal anti-migraine treatment options should be based on the following principles: understanding and capitalizing on the multifactorial pathogenetic specificity of migraine and the individualized approach to patients. Thus, this combination, together with a productive dialogue between the doctor, the patient and his family, will generate positive results in the treatment of migraine.
Aspecte contemporane în managementul farmacologic al migrenei
Contemporary aspects in pharmacological management of migraine
First published: 14 aprilie 2022
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Farm.205.2.2022.6288
Abstract
Rezumat
Migrena reprezintă o patologie neurologică foarte complexă, care are un impact negativ major asupra sănătăţii şi a calităţii vieţii oamenilor. Totodată, este o problemă de sănătate globală, pentru care încă nu a fost stabilit un management terapeutic definitiv. Incertitudinea dată se explică prin aspectul multilateral al fiziopatologiei migrenei, prin caracterul individual al manifestărilor clinice prezentate de către pacienţi, precum şi prin diversitatea nivelului de eficacitate al tratamentelor disponibile. Prin urmare, identificarea opţiunilor terapeutice antimigrenoase optime ar trebui să se bazeze pe următoarele principii: înţelegerea şi valorificarea specificului patogenetic multifactorial al migrenei şi abordarea individualizată a pacienţilor. Astfel, această combinaţie, alături de un dialog productiv între medic, pacient şi familia acestuia, va genera rezultate pozitive în tratamentul migrenei.
Introducere
Migrena reprezintă o cefalee primară episodică, cu localizare hemicranică şi caracter pulsatil. Este caracterizată prin diverse combinaţii de tulburări neurologice, gastrointestinale şi vegetative. Din punct de vedere fiziopatologic, este o cascadă complexă de evenimente neurovasculare şi biochimice, care determină vasodilatare şi inflamaţie neurogenă, neinfecţioasă, a vaselor meningeale(1,2).
Conform datelor epidemiologice, migrena afectează aproximativ 15% din populaţia globală(1,2) şi este cea mai invalidantă şi a doua cea mai răspândită dintre toate tulburările neurologice la nivel mondial(4,5), iar OMS clasifică migrena pe locul 19 în privinţa dizabilităţii pentru ambele sexe(6).
Migrena este divizată în patru faze: premonitorie (prodrom), aura, cefaleea şi postdromul (de rezoluţie). Fiecare etapă are o anumită durată: prodromul – până la 72 de ore, aura – până la 60 de minute, cefaleea – de la 4 la 72 de ore, postdromul – până la 24 de ore. Acestea se pot manifesta într-o ordine secvenţială liniară, dar, în majoritatea cazurilor, fazele migrenei arată o suprapunere semnificativă, astfel încât ordonarea liniară este atât atractivă, cât şi înşelătoare prin simplitatea sa(14).
Fiziopatologia migrenei
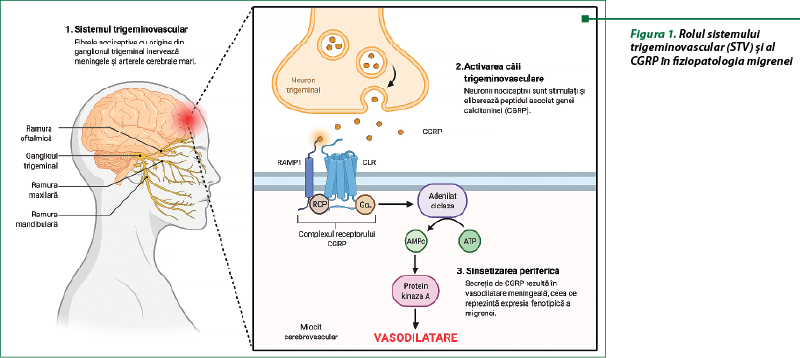
În conformitate cu studiile recente, sistemul trigeminovascular (STV) are un rol esenţial în declanşarea migrenei(3). Neuronii fibrelor nociceptive, cu origine în ganglionul trigeminal, care inervează meningele şi arterele cerebrale mari, sunt stimulaţi şi eliberează substanţe vasoactive(3). Secreţia acestor mediatori (peptidul vasoactiv intestinal, oxidul nitric, peptidul asociat genei calcitoninei – CGRP, peptidul activator al adenilat-ciclazei pituitare etc.) declanşează o cascadă de evenimente intracelulare la nivel de miocit cerebrovascular, determinând vasodilataţie meningeală – expresia fenotipică a migrenei. De asemenea, acţiunea neuromediatorilor, cu origine din STV, asupra structurilor subcorticale explică, din punct de vedere fiziopatologic, simptomele asociate crizelor migrenoase (aura)(10). Studiile neuroimagistice (PET 15O-H20) arată o creştere a fluxului sangvin cerebral (FSC) în structuri subcorticale specifice, în timpul fazei premonitorii şi de aură(8.9). Când aceste substanţe biologice interesează nucleul tractului solitar, pacientul acuză greaţă şi vomă; locus coeruleus – stres psihologic, dereglări în regimul somn-veghe, dezechilibru ortostatic, instabilitate emoţională; nucleii pulvinari din talamus – dereglări vizuale, fotofobie.
Factorii-trigger ai migrenei
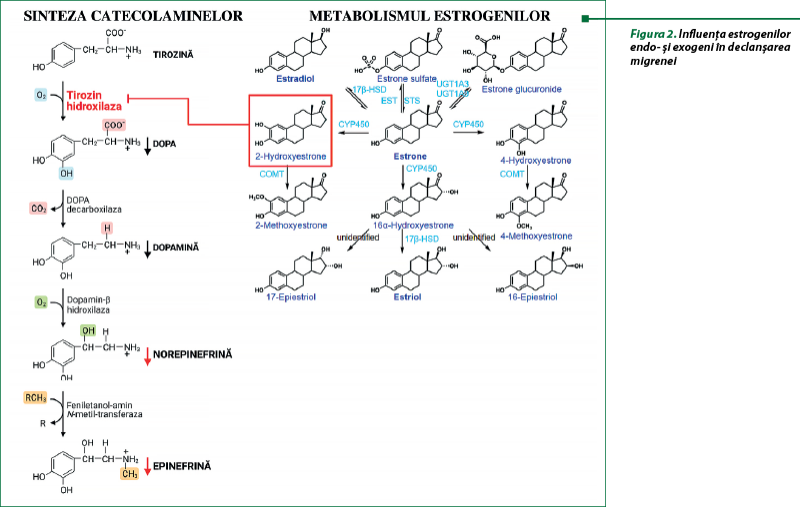
Numeroase studii elucidează factorii precipitanţi ai migrenei, precum şi rolul acestora în cronicizarea cefalalgiei respective(7). Influenţa estrogenilor endogeni şi exogeni, expunerea macroorganismului la tiramină şi tirozină, în diverse situaţii clinice sunt exemple elocvente de factori-trigger ai migrenei. Analizând rolul hormonilor sexuali feminini, statistica ne arată faptul că, în perioada prepubertară, pentru fete şi băieţi, prevalenţa migrenei este de 4%; la adulţi, rata femeilor devine de două-trei ori mai mare (18% – F, 6% – B); la 20% dintre femei, migrena debutează la pubertate (60% dintre aceste femei; ulterior, au crize migrenoase în perioada perimenstruală); două treimi din femeile cu migrenă anterioară remarcă o ameliorare odată cu menopauza fiziologică(1,6). Fiziopatologic, acest fenomen se explică prin inhibarea enzimei tirozin-hidroxilază de către un metabolit al estrogenului, 2-hidroxiestrona, dereglându-se astfel lanţul de sinteză a catecolaminelor. Ca rezultat, apare scăderea concentraţiei adrenalinei şi noradrenalinei, ulterior cu micşorarea efectului vasopresor, manifestându-se vasodilatarea meningeală – nucleul evenimentelor neurovasculare în migrenă. Prin urmare, la pacientele cu migrenă sau cu predispoziţie migrenoasă, se administrează cu precauţie contraceptivele orale combinate şi terapia hormonală de substituţie(1).
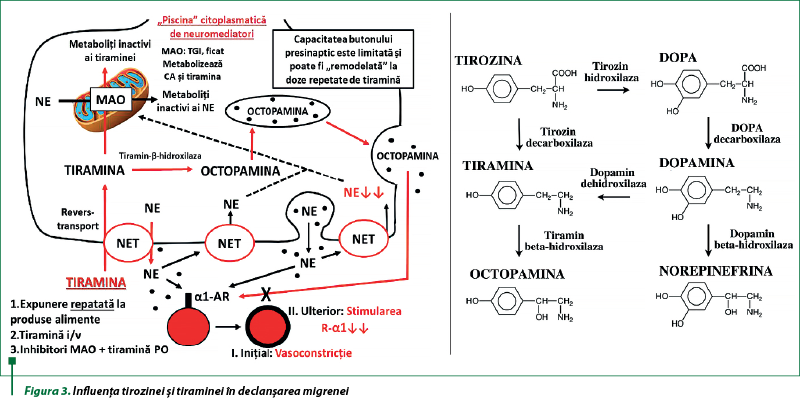
De asemenea, vasodilatarea meningeală este provocată şi de contactul organismului uman cu tiramina şi cu tirozina (consum alimentar repetat şi consecutiv; administrarea tiraminei intravenos sau administrarea internă în asociere cu inhibitori MAO). Surse importante de tirozină şi tiramină sunt caşcavalul maturat, ciocolata neagră, fructele de avocado, fructele uscate, murăturile, vinul roşu etc. Din moment ce este captată în butonul presinaptic, tiramina, fiind în exces, este metabolizată insuficient de către enzima mitocondrială monoamin-oxidază (MAO). Excesul de tiramină este metabolizat de către enzima citoplasmatică tiramin-β-hidroxilază, transformându-se în octopamină. Ulterior, octopamina substituie neuromediatorii vasopresori din veziculele butonului presinaptic (de exemplu, norepinefrina). La început, avalanşa de norepinefrină eliberată din vezicule determină o creştere a rezistenţei periferice vasculare prin vasoconstricţie, însă, după ce se epuizează, se remarcă vasodilataţia, deoarece octopamina nu are afinitate pentru receptorii α1-adrenergici şi nu-i poate stimula pentru a produce vasoconstricţie. Deci pacienţii cu migrenă trebuie să evite contactul cu tiramina şi tirozina, atât alimentar, cât şi farmacologic, pentru a limita riscul de declanşare a crizelor migrenoase.
Managementul terapeutic
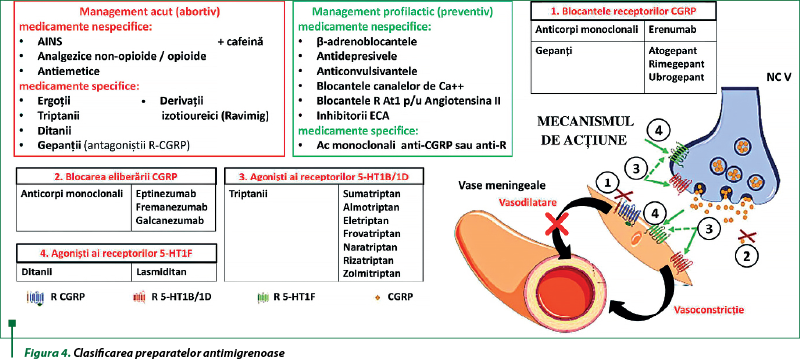
Conform protocoalelor şi studiilor clinice, terapia antimigrenoasă de succes reprezintă o combinaţie dintre managementul nefarmacologic (acupunctură, biofeedback, terapie cognitiv‑comportamentală, terapie de relaxare, stimulare magnetică cerebrală, stimulare electrică transcraniană, stimularea nervului vag etc.)(2,13) şi managementul farmacologic, conform FDA şi EMA: acut specific – ergoţii, triptanii, ditanii, gepanţii, derivaţii izotioureici; acut nespecific – AINS, analgezicele opioide/nonopioide, antiemeticele şi/sau cafeină; profilactic specific – anticorpii monoclonali anti-CGRP sau antireceptorul-CGRP; profilactic nespecific – antidepresivele, β-adrenoblocantele, anticonvulsivantele, blocantele canalelor ionilor de calciu, blocantele receptorilor pentru angiotensina II, inhibitorii enzimei de conversie a angiotensinei(10,11,14). Actualităţile terapeutice relevă multiple ţinte ale preparatelor farmacologice noi, acestea fiind centrate spre modularea activităţii neuronale, mediată prin intermediul receptorilor 5-HT1B, 5-HT1D, 5-HT1F şi α1, R-CGRP(10,12). Acţiunea medicamentelor specifice antimigrenoase rezultă în limitarea neuroinflamaţiei şi a vasodilataţiei meningeale, reducându-se hiperexcitabilitatea indusă de neuromediatorii proinflamatori şi vasodilatatori asupra structurilor subcorticale, responsabile de simptomatica migrenei(1,14). Clasele de medicamente menţionate au indicaţii şi contraindicaţii specifice şi diverse, motiv pentru care putem adapta administrarea antimigrenoaselor conform necesităţilor individuale ale pacienţilor, ceea ce reprezintă un punct forte pentru tendinţa actuală de medicină individualizată. Managementul terapeutic specific abortiv şi specific profilactic demonstrează eficacitate în tratamentul antimigrenos, conform studiilor clinice internaţionale şi naţionale(2,13,14). Chiar dacă opţiunile terapeutice menţionate ameliorează starea pacienţilor şi calitatea vieţii, utilizarea inadecvată a medicamentelor poate duce la cronicizarea migrenei(7).
Concluzii
Ultimele descoperiri efectuate în farmacoterapia antimigrenoasă sunt un argument persuasiv care demonstrează importanţa evaluării migrenei în context patogenetic amplu. Esenţa multifactorială specifică migrenei reprezintă cheia managementului terapeutic de succes al acestei patologii. Dacă tratamentul este administrat corect, atât farmacologic, cât şi nefarmacologic, luându-se în calcul o abordare individualizată a pacientului, prognosticul este favorabil. Contrar acestui fapt, managementul neeficient al migrenei şi absenţa înlăturării factorilor-trigger duc la cronicizarea patologiei, cu repercusiuni nefavorabile pentru sănătatea pacientului.
Bibliografie
-
Moldovanu I, Dodick DW, Odobescu S. Cefaleele, durerile faciale şi cervicale: diagnostic şi tratament. Chişinău. 2007.
-
Migrena: diagnostic şi tratament, Protocol clinic instituţional, INN (2018).
-
Ashina M. Migraine. N Engl J Med. 2020 Nov 5;383(19):1866-1876. doi: 10.1056/NEJMra1915327.
-
GBD 2016 Neurology Collaborators. Global, regional, and national burden of neurological disorders, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol. 2019 May;18(5):459-480. doi: 10.1016/S1474-4422(18)30499-X.
-
GBD 2016 Headache Collaborators. Global, regional, and national burden of migraine and tension-type headache, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol. 2018;17, 954–976.
-
Steiner TJ, Scher AI, Stewart WF, Kolodner K, Liberman J, Lipton RB. The prevalence and disability burden of adult migraine in England and their relationships to age, gender and ethnicity. Cephalalgia. 2003;23(7):519-27.
-
Moldovanu I, Odobescu S, Craciun C. Chronic migraine with and without medication overuse: the role of drug phobia and associated factors (according to the data of Headache Centre, Chisinau, the Republic of Moldova). Cephalalgia. 2008; 28(11):1229-33.
-
Weiller C, May A, Limmroth V, Juptner M, Kaube H, Schayck RV, Coenen HH, Diener HC. Brain stem activation in spontaneous human migraine attacks. Nat Med. 1995 Jul;1(7):658-60. doi: 10.1038/nm0795-658.
-
Maniyar FH, Sprenger T, Monteith T, Schankin C, Goadsby PJ. Brain activations in the premonitory phase of nitroglycerin triggered migraine attacks. Brain. 2014 Jan;137(Pt 1):232-41. doi: 10.1093/brain/awt320.
-
Goadsby PJ, Holland PR, Martins-Oliveira M, Hoffmann J, Schankin C, Akerman S. Pathophysiology of Migraine: A Disorder of Sensory Processing. Physiol Rev. 2017 Apr;97(2):553-622. Published online 2017 Feb 8. doi: 10.1152/physrev.00034.2015: 10.1152/physrev.00034.2015; https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5539409/?report=printable
-
Teză de doctorat Rezumat „Cercetări asupra managementului terapeutic al migrenei”, conducător, prof. univ. dr. Florica Popescu PhD, student Mihaela Bianca Anoaica, Universitatea de Medicină şi Farmacie Craiova.
-
De Vries T, Villalón CM, MaassenVanDenBrink A. Pharmacological treatment of migraine: CGRP and 5-HT beyond the triptans. Pharmacol Ther. 2020 Jul;211:107528. doi: 10.1016/j.pharmthera.2020.107528.
-
„Migrena”, Protocol clinic naţional, PCN- 284, Chişinău, 2017.
-
Mavridis T , Breza M, Deligianni CI, Mitsikostas DD. Therapeutic Management: When and What. In: Kozubski, W. , editor. Migraine [Internet]. London: IntechOpen; 2020. Available fat: https://www.intechopen.com/chapters/72737. doi: 10.5772/intechopen.93096.
Articole din ediţiile anterioare
Migrena, adesea mai mult decât o durere de cap
Migrena este un tip de cefalee care diminuează profund calitatea vieţii. Se manifestă cu atacuri migrenoase, cu sau fără aură. Se deosebeşte de alt...