Iod povidona demonstrează activitate virucidă in vitro rapid instalată împotriva SARS-CoV-2, virusul responsabil de apariţia COVID-19
Povidone-iodine demonstrates rapid in vitro virucidal activity against SARS-CoV-2, the virus causing COVID-19 disease
Abstract
Introduction. As of 22 June 2020, Severe Acute Respiratory Syndrome (SARS)-coronavirus (CoV)-2 has infected more than 8.95 million people worldwide, causing >468,000 deaths. The virus is transmitted through respiratory droplets and physical contact from contaminated surfaces to the mucosa. Hand hygiene and oral decontamination among other measures are key to preventing the spread of the virus. We report the in vitro virucidal activity of topical and oral povidone-iodine (PVP-I) products against SARS-CoV-2.Method. Suspension assays were used to assess the virucidal activity of PVP-I against SARS-CoV-2. Products were tested at a contact time of 30 s for virucidal activity. Viral titres were calculated using the Spearman‑Kärber method and reported as median tissue culture infectious dose (TCID50)/mL.
Results. All four products [antiseptic solution (PVP-I 10%), skin cleanser (PVP-I 7.5%), gargle and mouth wash (PVP-I 1%) and throat spray (PVP-I 0.45%)] achieved ≥ 99.99% virucidal activity against SARS-CoV-2, corresponding to ≥ 4 log10 reduction of virus titre, within 30 s of contact.
Conclusions. This study provides evidence of rapid and effective virucidal activity of PVP-I against SARS-CoV-2. PVP-I-based products are widely available for medical and personal use for hand hygiene and oral decontamination, and could be readily integrated into the coronavirus disease (COVID-19) infection control measures in hospital and community settings.
Keywords
anti-infective agentsCOVID-19povidone-iodinePVP-ISARS-CoV-2upper respiratory tract infectionsvirusesRezumat
Introducere. La data de 22 iunie 2020, SARS-CoV-2, ce determină COVID-19, a infectat mai mult de 8,95 milioane de oameni din întreaga lume, determinând peste 468.000 de decese. Virusul se transmite pe cale respiratorie, prin picături de secreţie eliberate prin tuse şi strănut şi prin contactul fizic dintre suprafeţele contaminate şi mucoase. Alături de alte măsuri, igiena mâinilor şi decontaminarea orală sunt măsuri-cheie pentru prevenirea răspândirii virusului. Raportăm activitatea virucidă in vitro a produselor topice şi orale pe bază de iod povidonă (PVP-I) împotriva SARS-CoV-2.Metodă. A fost utilizată testarea cantitativă a suspensiei pentru evaluarea activităţii virucide a PVP-I împotriva SARS-CoV-2. Produsele au fost testate la un timp de contact de 30 de secunde pentru activitate virucidă. Titrurile virale au fost calculate prin metoda Spearman-Kärber şi au fost raportate ca doză infecţioasă medie a culturii de ţesuturi (TCID50)/ml.
Rezultate. Toate cele patru produse [soluţie cutanată antiseptică (PVP-I 10%), soluţie cutanată antiseptică de curăţare (PVP-I 7,5%), gargarism şi apă de gură (PVP-I 1%), precum şi spray pentru gât (PVP-I 0,45%)] au demonstrat o activitate virucidă ≥99,99% împotriva SARS-CoV-2, corespunzând unei reduceri cu ≥4 log10 a titrului viral, în termen de 30 de secunde de la contact.
Concluzii. Acest studiu oferă dovezi ale activităţii virucide eficace şi rapide a PVP-I împotriva SARS-CoV-2. Produsele pe bază de PVP-I sunt disponibile pe scară largă pentru uz medical şi personal, pentru igiena mâinilor şi decontaminarea orală, şi ar putea fi uşor integrate în măsurile de control al COVID-19, atât în mediul spitalicesc, cât şi în cel comunitar.
Cuvinte Cheie
agenţi antiinfecţioşiCOVID-19iod povidonăPVP-ISARS-CoV-2infecţii de tract respirator superiorvirusuriIntroducere
Boala coronavirus 2019 (COVID-19), cauzată de SARS-CoV-2, a fost declarată pandemică de Organizaţia Mondială a Sănătăţii (OMS) în data de 11 martie 2020(1). Numărul infecţiilor a crescut exponenţial într-o perioadă scurtă(2). Până la 22 iunie 2020, virusul s-a răspândit rapid şi a infectat cel puţin 8,95 milioane de oameni la nivel mondial, provocând peste 468.000 de decese(3). SARS-CoV-2 este un virus ARN anvelopat monocatenar, cu polaritate pozitivă, şi aparţine aceleiaşi clase de beta-coronavirusuri ca SARS-CoV şi Sindromul Respirator al Orientului Mijlociu (MERS)-CoV, responsabile de epidemiile SARS din 2003 şi respectiv MERS din 2012(4,5).
Dovezile actuale indică faptul că transmiterea de la om la om are loc în principal prin picături respiratorii din tuse sau strănut şi/sau prin contact fizic(6). Deoarece virusul poate persista pe suprafeţe contaminate timp de mai multe zile(7), infecţia poate să apară indirect prin transferul de virus de la aceste suprafeţe sau mâini către mucoasa gurii, nasului sau ochilor. Astfel, măsurile de control al infecţiilor, cum ar fi dezinfectarea suprafeţelor şi o bună igienă personală şi a mâinilor, sunt importante pentru a limita răspândirea virusului.
Iod povidona (PVP-I; polivinilpirolidona iodată) este un complex solubil în apă de povidonă, o moleculă purtătoare, şi iod, care are o activitate microbicidă puternică. Formulările pe bază de PVP-I au fost utilizate pe scară largă timp de peste 60 de ani datorită activităţii antimicrobiene cu spectru larg şi profilului de siguranţă bine determinat(8,9).
PVP-I se află pe lista medicamentelor esenţiale întocmită de OMS, care identifică medicamente importante necesare unui sistem funcţional de asistenţă medicală. Apa de gură pe bază de PVP-I este, de asemenea, inclusă în planul de cercetare şi dezvoltare al OMS pentru terapii experimentale împotriva COVID-19, de aceea ar fi important să se demonstreze activitatea sa antivirală directă împotriva virusului(10). În plus faţă de activitatea largă antibacteriană şi antifungică, PVP-I a demonstrat o activitate in vitro împotriva unei serii de virusuri(11), inclusiv SARS-CoV(12) şi MERS-CoV(13). În acest studiu am evaluat activitatea virucidă a patru produse pe bază de PVP-I împotriva SARS-CoV-2, utilizând o testare cantitativă după un timp de expunere de 30 de secunde.
Metodă
Patru produse pe bază de PVP-I [Betadine® soluţie cutanată antiseptică (PVP-I 10%), Betadine® soluţie cutanată antiseptică de curăţare (PVP-I 7,5%), Betadine® gargarism şi apă de gură (PVP-I 1,0%) şi Betadine® spray pentru gât (PVP-I 0,45%)] au fost testate la facilitatea de producţie cu nivel 3 de biosiguranţă animală de la Şcoala Medicală Duke-NUS din Singapore. Betadine® gargarism şi apă de gură a fost testată atât nediluată, cât şi în diluţie 1:2.
Produsele pentru testare au fost furnizate de către Mundipharma Singapore Holding. Activitatea virucidă a produselor pe bază de PVP-I faţă de SARS-CoV-2 a fost evaluată într-o analiză ce a determinat timpul de inactivare a virusului, adaptând protocolul din metodologia de testare a dezinfectanţilor EN14476, care a fost utilizată anterior pentru a testa eficacitatea produselor Betadine® în cazul SARS-CoV şi MERS-CoV. O reducere ≥4 log10 (99,99%) a titrului viral reprezintă o activitate virucidă eficientă conform standardelor europene(9,12). Acest articol nu conţine studii cu subiecţi umani sau cu animale, efectuate de vreunul dintre autori.
Cultura virală
SARS-CoV-2 (hCoV-19/Singapore/2/2020) a fost propagat în celulele Vero-E6 (American Type Culture Collection). Celulele-gazdă Vero-E6 au fost menţinute în mediul Dulbecco Eagle modificat, conţinând 5% ser fetal bovin (DMEM-5% FBS). Pentru a pregăti stocurile de virus, monostraturile cu celule confluente au fost infectate cu SARS-CoV-2 şi incubate la 37°C, 5% CO2, timp de până la 7 zile. Când efectele citopatice (CPE) au fost evidente microscopic, supernatantul a fost recoltat, clarificat prin centrifugare şi păstrat la -80°C.
Test de citotoxicitate a PVP-I
Citotoxicitatea PVP-I a fost testată prin incubarea celulelor Vero-E6 neinfectate cu câte zece diluţii seriale ale produselor de test PVP-I în FEM DMEM-5%. După incubarea la 37°C timp de patru zile, au fost observate CPE la fiecare diluţie pentru a determina concentraţia cea mai mică de PVP-I, la care efectele citotoxice au lipsit.
PVP-I – testul timpului necesar de inactivare a virusului
Expunerea virusului la produsele pe bază de PVP-I a fost efectuată la 21°C timp de 30 de secunde, pentru a evalua eficacitatea dezinfectantului, aşa cum s-a descris anterior(13). S-a amestecat o cantitate de 100 µl de virus cu 700 µl produs de test PVP-I, în prezenţa a 200 µl de soluţie salină tamponată cu fosfat (PBS) care conţine 0,3 g/l BSA ca substanţă interferentă.
Au fost incluse controalele virusului cu 700 µl de PBS în locul produselor pe bază de PVP-I. După timpul de contact prevăzut, reacţia PVP-I a fost oprită prin transferul de 100-µl alicote la 900 µl DMEM-5% FBS. Imediat, s-au efectuat zece diluţii seriale şi s-au utilizat 100 µl din fiecare diluţie pentru a inocula celulele Vero-E6 (în patru exemplare) într-o placă cu microtitru cu 96 de godeuri. Datorită titrării imediate, nu s-a putut produce niciun efect secundar al produsului de testare, aşa cum s-a descris anterior(9). Plăcile au fost incubate la 37°C timp de patru zile înainte de evaluarea CPE. Titrurile virale au fost calculate ca doză medie infecţioasă a culturii ţesuturilor (TCID50/ml), folosind metoda Spearman‑Kärber(14,15).
Rezultate
Testul timpului necesar pentru inactivarea virusului a fost efectuat după prima evaluare a citotoxicităţii produselor pentru celulele Vero-E6. Soluţia cutanată antiseptică, dezinfectantul pentru mâini, spray-ul pentru gât şi gargarism/apa de gură nu au fost citotoxice pentru Vero-E6 la diluţiile ≥1:100 şi soluţia cutanată antiseptică de curăţare la diluţiile ≥1:1000. Acest lucru a fost luat în considerare atunci când s-a efectuat testul de inactivare a virusului.
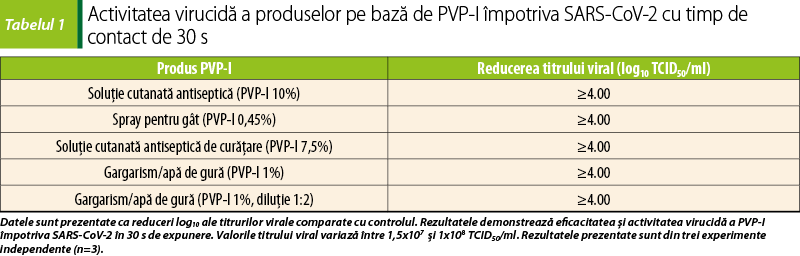
Testarea iniţială a fost efectuată la 120 de secunde pentru a evalua eficacitatea diferitelor produse pe bază de PVP-I împotriva SARS-CoV-2 şi pentru a optimiza testul (tabelul 1). Nu au fost observate CPE după expunerea SARS-CoV-2 la produsele pe bază de PVP-I. Datorită citotoxicităţii produselor în celulele Vero-E6, limita de detectare a testului a fost de 3x103 TCID50/ml. Acest lucru a demonstrat că toate produsele de testare au fost eficiente împotriva SARS-CoV-2 după două minute. Pentru a determina activitatea virucidă a produsului (reducerea cu
≥4 log10 a titrurilor virale), eficacitatea produselor pe bază de PVP-I împotriva SARS-CoV-2 a fost testată la un timp de expunere de 30 s, conform Ghidurilor Agenţiei Europene pentru Produse Chimice (ECHA)(16), pentru a demonstra eficacitatea virucidă a dezinfectanţilor pentru utilizare în spitale şi acasă.
Toate produsele pe bază de PVP-I testate la 30 de secunde au demonstrat o reducere cu ≥4 log10 a titrurilor SARS-CoV-2, corespunzând unei inactivări virale de ≥99,99% pentru toate produsele testate, indicând o activitate virucidă rapidă(16) şi, de asemenea, respectând reperele de timp ECHA pentru eficacitatea dezinfectanţilor (tabelul 1).
Discuţie
În prezent, nu sunt stabilite terapii eficace sau vaccinuri împotriva infecţiei cu SARS-CoV-2, în ciuda multitudinii de studii clinice în curs de desfăşurare(17). Prin urmare, tratamentul pentru pacienţii cu COVID-19 se bazează în cea mai mare parte pe tratament de susţinere, ventilaţie mecanică şi/sau medicamente utilizate anterior împotriva altor coronavirusuri(17). La fel ca SARS-CoV, SARS-CoV-2 părea să se răspândească iniţial prin transmiterea picăturilor şi prin contact direct/indirect cu persoane infectate simptomatice. Cu toate acestea, persoanele infectate, asimptomatice şi cele presimptomatice, cu SARS-CoV-2 pot transmite virusul(18). Mai mult, virusul pare să fie mult mai contagios în comparaţie cu SARS-CoV(19).
Pe lângă distanţarea fizică, măsurile preventive, precum igiena personală şi dezinfectarea frecventă a suprafeţelor atinse în permanenţă în spaţiile publice, alături de măsurile luate privind sănătatea publică sunt intervenţii nonterapeutice importante pentru a reduce riscul de transmitere de la persoană la persoană în cadrul comunităţii şi pentru a proteja angajaţii din sistemul sanitar. Formulările testate au diferite roluri complementare în controlul infecţiilor, inclusiv igiena mâinilor şi igiena orală. În primul rând, protocoalele recomandate de OMS(6) în ceea ce priveşte igiena mâinilor pot fi augmentate prin utilizarea de dezinfectanţi cu activitate dovedită in vitro împotriva SARS-CoV-2, aşa cum s-a demonstrat cu PVP-I în acest studiu.
Un studiu anterior de simulare a igienei mâinilor a demonstrat o eficacitate in vivo superioară a PVP‑I în comparaţie cu săpunul moale sau clorhexidina împotriva norovirusului murin nepatogen (MNV)(20). MNV, un virus neanvelopat, a fost utilizat ca model de virus‑test în simulări in vivo din motive de biosecuritate, şi se ştie că este mai rezistent la antiseptice decât virusurile anvelopate, cum ar fi coronavirusurile(20).
În al doilea rând, având în vedere potenţialul pentru infecţia cu SARS-CoV-2 prin mucoasa bucală şi nazală, pe lângă măşti, măsurile de igienă respiratorie suplimentară, precum spray-urile pentru gât sau soluţiile pentru gargară, se consideră că reduc riscul de transmitere a SARS-CoV-2 pe aceste căi(9). Ghiduri ale mai multor organizaţii, inclusiv Asociaţia Dentară Australiană şi Centrele din SUA pentru Controlul şi Prevenirea Bolilor, referitoare la COVID-19, au recomandat utilizarea spălăturilor bucale preprocedural cu produse precum PVP-I(21,22). Un studiu realizat în Japonia a arătat că, la pacienţii cu boli respiratorii cronice, incidenţa episoadelor de exacerbare acută a infecţiilor respiratorii cronice a scăzut semnificativ după începerea utilizării regulate a iod povidonei pentru gargară(23). Studii recente au arătat că SARS-CoV-2 este mai contagios în stadiile precoce ale bolii, iar transmiterea are loc mai ales la nivelul tractului respirator superior(24,25). Luând în considerare aceşti factori, atât spălarea frecventă a mâinilor, cât şi igiena orală prin gargară ar putea ajuta la reducerea la minimum a riscului de infecţii(26).
Un studiu recent a testat stabilitatea SARS-CoV-2 în diferite condiţii de mediu, inclusiv expunerea la iod povidonă şi la alţi dezinfectanţi, pentru 5, 15 şi 30 de minute(7). Rezultatele au arătat că SARS-CoV-2 ar putea rămâne viabil timp de 6-7 zile pe unele suprafeţe (oţel inoxidabil şi plastic), dar că ar putea fi inactivat de o serie de dezinfectanţi obişnuiţi. Virusul a fost nedetectabil după o perioadă de expunere de minimum 5 minute la iod povidonă (7,5%), indicând astfel o potenţială utilizare a acesteia din urmă în cadrul procedurilor de dezinfecţie(7). Studiile anterioare care au testat eficacitatea produselor cu iod povidonă în eliminarea SARS-CoV şi MERS-CoV au demonstrat activitate virucidă rapidă în prezenţa unor substraturi interferente cum sunt eritrocitele, pentru a simula contaminarea organică (condiţii neigienice). Nu a fost observată nicio diferenţă în eliminarea virusurilor în condiţii igienice versus neigienice, indicând faptul că substanţele interferente nu determină reducerea activităţii antivirale a iod povidonei(9,13).
În aceste studii, iod povidona a demonstrat inactivarea rapidă (reducere log10 a titrurilor virale ≥4) a SARS‑CoV şi MERS-CoV într-un timp de contact de 15 secunde.
Concluzii
Activitatea virucidă rapidă a iod povidonei împotriva SARS-CoV-2, precum şi spectrul larg al acţiunii antimicrobiene sugerează importanţa sa în controlul infecţiilor. Ca o măsură de protecţie suplimentară echipamentului de protecţie personală (Personal Protective Equipment; PPE), aceste produse pot contribui la reducerea transmiterii bolii.
Iod povidona este uşor de administrat şi este utilizată atât în spitale, cât şi în comunităţi, de peste 60 de ani, putând fi astfel uşor integrată în protocoalele existente pentru controlul infecţiilor.
Produsele pe bază de iod povidonă pot face parte din măsurile de control al infecţiilor în timpul pandemiei de COVID-19(27–29).
În concluzie, utilizarea produselor pe bază de iod povidonă poate spori măsurile de igienă şi sănătate pentru a reduce răspândirea SARS-CoV-2 în colectivităţi. n
MULŢUMIRI. Adresăm mulţumiri echipei Duke-NUS Medical School ABSL3 pentru managementul logistic.
Finanţare. Acest studiu, suportul editorial şi taxele aferente publicării acestui manuscris au fost finanţate de Mundipharma Singapore Holding Pte. Limited.
Asistenţa editorială. Asistenţa editorială în pregătirea acestui articol a fost oferită de Sen Kwan Tay, Tech-Observer Asia-Pacific Pte Ltd.
Drepturi de autor. Toţi autorii menţionaţi corespund criteriilor International Committee of Medical Journal Editors (ICMJE) privind drepturile de autor pentru acest studiu şi îşi asumă responsabilitatea pentru integritatea prezentei lucrări în totalitatea ei şi şi-au dat acordul pentru publicarea acestei versiuni.
Contribuţiile autorilor. Danielle E. Anderson, Maren Eggers, Harsha Arumugam, Abhishek Ananthanarayanan, Timothy M. Jenkins şi Yacine Hadjiat au realizat designul studiului şi au coordonat activităţile de cercetare. Danielle E. Anderson, Velraj Sivalingam şi Adrian Eng Zheng Kang au condus experimentele. Danielle E. Anderson, Velraj Sivalingam şi Adrian Eng Zheng Kang au efectuat analizele. Abhishek Ananthanarayanan, Harsha Arumugam, Yacine Hadjiat, Timothy M. Jenkins, Maren Eggers şi Danielle E. Anderson au redactat documentul.
Publicare prealabilă. O versiune fără revizuire de specialitate a acestui articol a fost disponibilă în avans, începând cu data de 10 iunie 2020, la adresa ResearchSquare: https://www.researchsquare.-com/article/rs-34544/v1.
Declararea conflictelor de interese. Abhishek Ananthanarayanan, Harsha Arumugam, Timothy M. Jenkins şi Yacine Hadjiat sunt angajaţi ai Mundipharma. Danielle E. Anderson, Velraj Sivalingam şi Adrian Eng Zheng Kang au încheiat contracte de prestări servicii cu Mundipharma pentru acest studiu. Maren Eggers este consultant şi lector pentru Mundipharma.
Conformitatea cu ghidurile de etică. Acest articol nu conţine studii efectuate pe animale sau subiecţi umani.
Disponibilitatea datelor. Toate datele generate sau analizate în timpul acestui studiu sunt incluse în articolul publicat sau sunt disponibile sub formă de fişiere cu informaţii suplimentare.
Acces liber. Acest articol este sub licenţa internaţională Creative Commons Attribution-NonCommercial 4.0, care permite orice utilizare necomercială, partajare, adaptare, distribuire şi reproducere în orice mediu sau format, în condiţiile în care se face referirea cuvenită la sursă şi autori, se pune la dispoziţie un link către licenţa privind drepturile de autor şi se menţionează dacă au fost efectuate modificări. Imaginile sau alte materiale ale unor terţe părţi sunt incluse în licenţa privind drepturile de autor ale articolului, dacă nu există o altă menţiune. În cazul unui material care nu este inclus în licenţă, iar utilizarea respectivului material nu este permisă de reglementările legale sau depăşeşte aria de utilizare permisă, va trebui obţinută permisiunea de utilizare direct de la deţinătorul licenţei. O copie a acestei licenţe este disponibilă la adresa http://creativecommons.org/licenses/by-nc/4.0/.
Bibliografie
-
World Health Organisation. WHO Director General’s opening remarks at the media briefing on COVID-19 - 11 March 2020: World Health Organisation. 2020. https://www.who.int/dg/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19—11-march-2020. Accessed 11 May 2020.
-
Zhao S, Lin Q, Ran J, et al. Preliminary estimation of the basic reproduction number of novel coronavirus (2019-nCoV) in China, from 2019 to 2020: a data-driven analysis in the early phase of the out-break. Int J Infect Dis. 2020;92:214-7.
-
Johns Hopkins University and Medicine. Coronavirus Resource Center: John Hopkins University. 2020. https://coronavirus.jhu.edu/map.html. Accessed 22 June 2020.
-
Corman VM, Muth D, Niemeyer D, Drosten C. Hosts and sources of endemic human coronaviruses. Adv Virus Res. 2018;100:163-88.
-
Zhu N, Zhang D, Wang W, et al. A novel coronavirus from patients with pneumonia in China, 2019. N Engl J Med. 2020;382(8):727-33.
-
World Health Organisation. Interim recommendations on obligatory hand hygiene against transmission of COVID-19: World Health Organization. 2020. https://www.who.int/who-documents-detail/interim-recommendations-on-obligatory-hand-hygiene-against-transmission-of-covid-19. Accessed 18 Apr 2020.
-
Chin AWH, Chu JTS, Perera MRA, et al. Stability of SARS-CoV-2 in different environmental conditions. Lancet Microbe. 2020;1:e10.
-
Vogt PM, Hauser J, Mueller S, Bosse B, Hopp M. Efficacy of conventional and liposomal povidone-iodine in infected mesh skin grafts: an exploratory study. Infect Dis Ther. 2017;6(4):545–55.
-
Eggers M, Koburger-Janssen T, Eickmann M, Zorn J. In vitro bactericidal and virucidal efficacy of povidone-iodine gargle/mouthwash against respiratory and oral tract pathogens. Infect Dis Ther. 2018;7(2): 249–59.
-
World Health Organisation. WHO R&D Blueprint COVID 19 Experimental Treatments: World Health Organisation. 2020. https://www.who.int/docs/ default-source/coronaviruse/covid-classification-of- treatment-types-rev.pdf. Accessed 18 May 2020.
-
Kawana R, Kitamura T, Nakagomi O, et al. Inactivation of human viruses by povidone-iodine in comparison with other antiseptics. Dermatology. 1997;195(Suppl 2):29–35.
-
Kariwa H, Fujii N, Takashima I. Inactivation of SARS coronavirus by means of povidone-iodine, physical conditions and chemical reagents. Dermatology. 2006;212(Suppl 1):119–23.
-
Eggers M, Eickmann M, Zorn J. Rapid and effective virucidal activity of povidone-iodine products against middle east respiratory syndrome coronavirus (MERS-CoV) and modified vaccinia virus Ankara (MVA). Infect Dis Ther. 2015;4(4):491–501.
-
Spearman C. The method of ‘right and wrong cases’ (‘constant stimuli’) without Gauss’s formulae. Br J Psychol. 1908;2:227–42.
-
Kärber G. Beitrag zur kollektiven Behandlung pharmakologischer Reihenversuche. Archiv Exper Pathol Pharmakol. 1931;162:480–3.
-
Comité Européen de Normalisation. EN14476:2013?A1:2015: Chemical disinfectants and antiseptics. Quantitative suspension test for the evaluation of virucidal activity in the medical area. Test method and requirements (Phase 2/Step 1) 2015.
-
Cascella M, Rajnik M, Cuomo A, Dulebohn SC, Di Napoli R. Features, evaluation and treatment coronavirus (COVID-19). Treasure Island, FL: Stat- Pearls; 2020.
-
Bai Y, Yao L, Wei T, et al. Presumed asymptomatic carrier transmission of COVID-19. JAMA. 2020;323(14):1406–7.
-
Sanche S, Lin YT, Xu C, Romero-Severson E, Hengartner N, Ke R. High contagiousness and rapid spread of severe acute respiratory syndrome coronavirus 2. Emerg Infect Dis. 2020;26(7):1470–7.
-
Eggers M, Koburger-Janssen T, Ward LS, Newby C, Müller S. Bactericidal and virucidal activity of povidone-iodine and chlorhexidine gluconate cleansers in an in vivo hand hygiene clinical simulation study. Infect Dis Ther. 2018;7(2):235–47.
-
Australian Dental Association. Managing COVID-19 Guidelines. 2020. https://www.ada.org.au/ Covid-19-Portal/Cards/Dental-Profesionals/ Guidelines-and-Risk-Factors/Just-an-information- Card. Accessed 21 June 2020.
-
Centers for Disease Control and Prevention. Guidance for dental settings: interim infection prevention and control guidance for dental settings during the COVID-19 response: centers for disease control and prevention. 2020. https://www.cdc.gov/ coronavirus/2019-ncov/hcp/dental-settings.html. Accessed 21 June 2020.
-
Nagatake T, Ahmed K, Oishi K. Prevention of respiratory infections by povidone-iodine gargle. Dermatology. 2002;204(Suppl 1):32–6.
-
Wölfel R, Corman VM, Guggemos W, et al. Virological assessment of hospitalized patients with COVID-2019. Nature. 2020;581(7809):465–9.
-
To KK, Tsang OT, Leung WS, et al. Temporal profiles of viral load in posterior oropharyngeal saliva samples and serum antibody responses during infection by SARS-CoV-2: an observational cohort study. Lancet Infect Dis. 2020;20(5):565–74.
-
Gui D, Pepe G, Magalini S. Just one more hygiene practice in COVID-19. Eur Rev Med Pharmacol Sci. 2020;24(7):3438–9.
-
O’Donnell VB, Thomas D, Stanton R, et al. Potential role of oral rinses targeting the viral lipid envelope in SARS-CoV-2 infection. Function. 2020;1: zqaa002.
-
Mady LJ, Kubik MW, Baddour K, Snyderman CH, Rowan NR. Consideration of povidone-iodine as a public health intervention for COVID-19: Utilization as ‘‘Personal Protective Equipment’’ for frontline providers exposed in high-risk head and neck and skull base oncology care. Oral Oncol. 2020;105: 104724.
-
Kirk-Bayley J, Challacombe S, Sunkaraneni S, Combes J. The use of povidone iodine nasal spray and mouthwash during the current COVID-19 pandemic may reduce cross infection and protect healthcare workers. 2020. https://doi.org/10.2139/ ssrn.3563092.





