Gravida cu hepatită cronică virală B, în practica medicului de familie
Primary care management of hepatitis B in pregnant women
Abstract
Hepatitis B virus (HBV) infection during pregnancy presents a particular situation that requires an effective approach, so that the risk of transmission of infection during pregnancy at the time of birth and during the lactation period is limited. The paper proposes a monitoring algorithm by which the physician family can provide optimal care to these patients.Keywords
pregnant womanhepatitis B virusRezumat
Gravida cu hepatită B constituie o situație particulară, care necesită o abordare eficientă, astfel încât riscul transmiterii infecției în timpul sarcinii, în momentul nașterii și în perioada de alăptare să fie limitat. Lucrarea își propune să prezinte un algoritm de monitorizare prin care medicul de familie să poată asigura o îngrijire optimă unei astfel de paciente.Cuvinte Cheie
gravidăvirus hepatitic BHepatita virală B are o prevalență de 3,5% în țara noastră, conform datelor statistice din 2008, ceea ce ne încadrează ca zonă cu prevalență intermediară a acestei maladii. Prevalența a început să scadă odată cu introducerea vaccinării antihepatitice în programul național.
Hepatita virală B reprezintă o afecțiune hepatică gravă, cu evoluție către ciroză, mai rapidă în timp, comparativ cu hepatita virală C. Aproximativ 20% din infecțiile acute cu virus B evoluează către forme cronice de boală, iar dintre acestea, aproximativ 2% ajung să dezvolte cancer hepatic. Coinfecția cu virus D crește rata mortalității. Terapia antivirală specifică limitează infecția, cu negativarea viremiei în timpul tratamentului. Întreruperea acestuia este urmată de recăderea bolii.
Luând în considerare cele de mai sus, cel mai important gest în combaterea acestei maladii este vaccinarea antihepatitică de la naștere, în maternitate, de preferat în primele 12 ore de viață, cu asigurarea unui titru protector de anticorpi. Astfel se reduce numărul de persoane infectate, lucru confirmat și de practică, după introducerea vaccinării antihepatitice în programul național. Medicul de familie este direct implicat în vaccinarea sugarului, copiilor, dar și a contacților, fiind astfel o verigă importantă a acestui proces (figura 1).
În practică ne întâlnim cu următoarele situații de infecție cronică:
- gravidă cunoscută cu infecție cronică cu virus B;
- gravidă depistată în timpul sarcinii cu virus B.

Abordarea celor două situații este similară.
În general, sarcina este bine tolerată la femeile cu infecție cronică cu virus hepatitic B (VHB) cu afectare hepatică ușoară, iar fătul are o dezvoltare normală. Analizele utile monitorizării gravidei cu virus hepatic B sunt:
1. Transaminazele (TGP și TGO), care evaluează funcția hepatică. Dublarea TGP impune inițierea terapiei antivirale specifice.
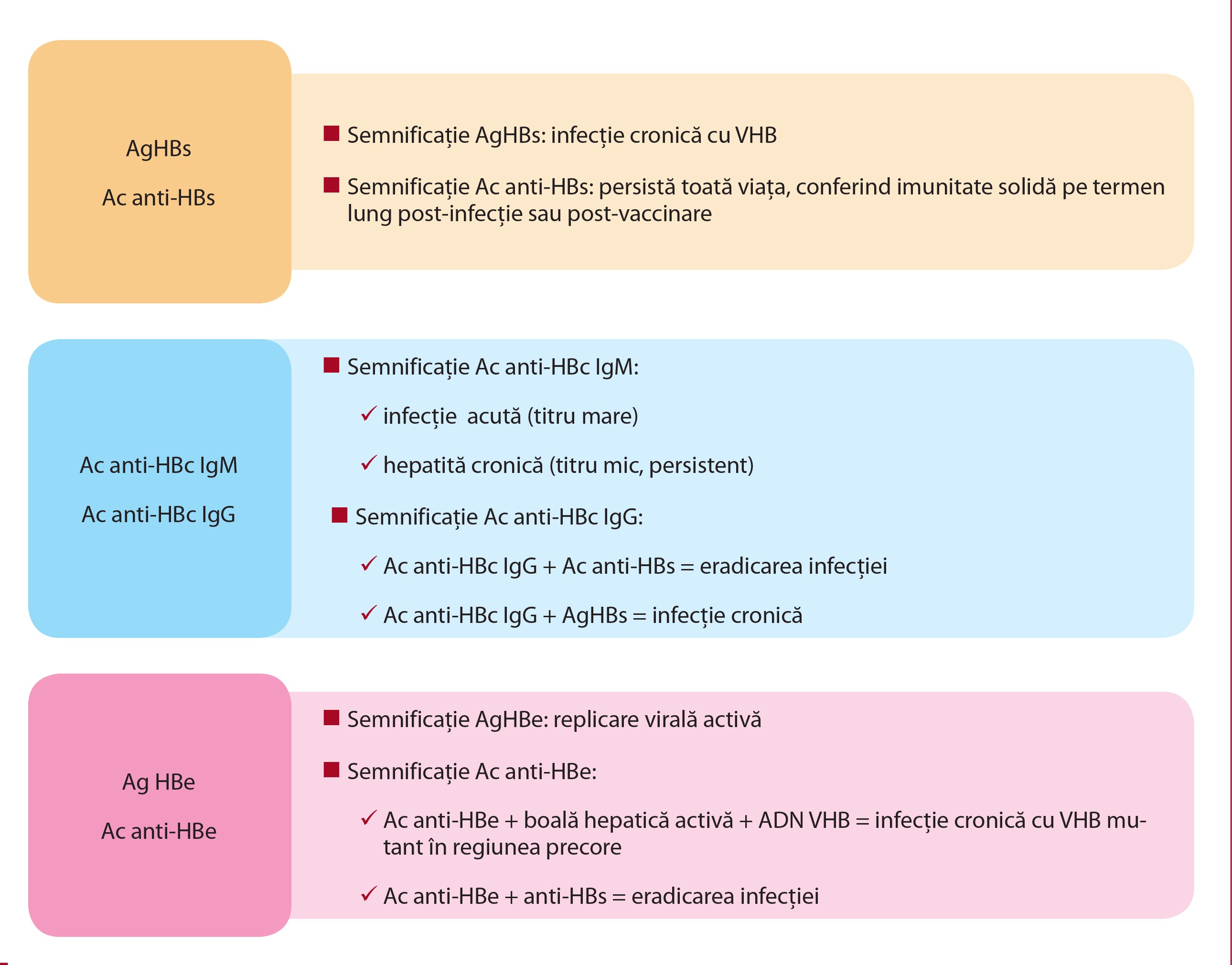
2. Perechea de antigen/anticorp AgHBe/AcHBe, care dă informații despre replicarea virală, prezența antigenului relevând replicarea activă a virusului, semn de agravare a afecțiunii (figura 2).
3. Viremia (ADN viral), care contribuie la decizia inițierii terapiei antivirale specifice. Viremia ridicată indică replicare virală înaltă, chiar dacă TGP are valori normale, și, de aceea, în al treilea trimestru (săptămânile 26-28) de sarcină, dacă viremia este >106 copii/mL, trebuie inițiată terapia antivirală, acest lucru prevenind transmiterea materno-fetală.
În mod fiziologic, albumina serică și hematocritul scad, iar fosfataza alcalină și alfa-fetoproteina pot fi crescute la gravide, de aceea nu le putem folosi la evaluarea funcției hepatice.
Poate o femeie cu virus hepatic B, în tratament antiviral, să păstreze sarcina?
Dacă gravida nu are ciroză, se poate face tranziție de pe o medicație cu potențial teratogen pe medicație sigură de administrat în timpul sarcinii, însă acest lucru trebuie decis numai de medicul curant hepatolog.
În ce situații primește terapie antivirală o gravidă cu hepatită cronică B?
Inițierea terapiei se face în funcție de următorii factori:
- Prezența/absența cirozei
- Titrul AgHBe/AcHBe
- Titrul viremiei
- Nivelul transaminazelor.
Medicamentul administrat la gravide în ultimul trimestru de sarcină este tenofovir disoproxil fumarat ca terapie princeps. Se poate utiliza și lamivudină.
Tratamentul va fi inițiat și monitorizat atent de către medicul hepatolog curant (gastroenterolog sau specialist de boli infecțioase).
O mamă cu hepatită cronică B poate alăpta?
Conform datelor medicale actuale, copiii care au primit la naștere (în primele 12 ore de viață) imunoglobulină specifică și prima doză de vaccin antihepatitic pot fi alăptați. Deși ADN-ul viral B a fost detectat în colostru, nu s-a putut demonstra o relație între alăptare și infecția cronică virală dezvoltată la copil.
Mama trebuie avertizată să nu alăpteze dacă observă sângerare la nivelul mameloanelor. Folosirea unei tetine de silicon reduce această posibilitate.
Mama trebuie avertizată să nu doneze laptele matern.
Studiile medicale disponibile în acest moment nu au ajuns la o concluzie privind siguranța alăptării în timpul tratamentului antiviral.
Medicația recomandată în tratamentul hepatitei cronice B sunt analogii nucleozidici, care însă trebuie evitați în cursul alăptării, deoarece se excretă în laptele matern. Singurul medicament care se excretă în doze foarte reduse este tenofovirul disoproxil fumarat, iar acesta nu are efecte toxice asupra copilului.

Transmiterea perinatală a infecției cu VHB
Riscul de transmitere a virusului hepatic B de la mame cu AgHbs pozitiv la făt este de peste 90% în lipsa imunizării active și pasive. Transmiterea virusului este posibilă intrauterin, în timpul nașterii și după naștere, prin alăptare. Riscul transmiterii este redus prin screeningul hepatitei B la gravide, vaccinarea antihepatitică începând din maternitate (în primele 12 ore de viață), și prin folosirea profilactică a imunoglobulinei specifice la nou-născuții cu mame cu AgHbs pozitiv. Riscul de transmitere este mai ridicat la femei cu AgHbs și AgHBe pozitive, viremia >106 copii/mL sau la femei cu vârsta <25 de ani.Riscul de transmitere este cel mai ridicat în momentul nașterii, atunci când secrețiile și sângele din canalul cervical vin în contact cu mucoasa membranelor copilului. Cel mai important factor în transmiterea verticală a infecției, în ciuda unei profilaxii corect făcute la naștere, îl reprezintă statusul de AgHBe pozitiv și/sau viremia crescută la mamă. Transmiterea transplacentară și transmiterea în timpul procedurilor obstetricale sunt cauze rare de infecție, iar alăptarea naturală nu reprezintă un risc major în transmiterea infecției. Beneficiul cezarienei în protecția împotriva transmiterii infecției nu este clar stabilit (figura 3).
Bibliografie
1. Giles M., Visvanathan K., Lewin S., et al. Clinical and virological predictors of hepatic flares in pregnant women with chronic hepatitis B. Gut 2015; 64:1810.
2. Nguyen G., Garcia R.T., Nguyen N., et al. Clinical course of hepatitis B virus infection during pregnancy. Aliment Pharmacol Ther 2009; 29:755.
3. Tan H.H., Lui H.F., Chow W.C. Chronic hepatitis B virus (HBV) infection in pregnancy. Hepatol Int 2008; 2:370.
4. Söderström A., Norkrans G., Lindh M. Hepatitis B virus DNA during pregnancy and post-partum: aspects on vertical transmission. Scand J Infect Dis 2003; 35:814.
5. Wong S., Chan L.Y., Yu V., Ho L. Hepatitis B carrier and perinatal outcome in singleton pregnancy. Am J Perinatol 1999; 16:485.
6. Tse K.Y., Ho L.F., Lao T. The impact of maternal HBsAg carrier status on pregnancy outcomes: a case-control study. J Hepatol 2005; 43:771.
7. Terrault N.A., Bzowej N.H., Chang K.M., et al. AASLD guidelines for treatment of chronic hepatitis B. Hepatology 2016; 63:261.
8. Society for Maternal-Fetal Medicine (SMFM), Dionne-Odom J., Tita A.T., Silverman N.S. #38: Hepatitis B in pregnancy screening, treatment, and prevention of vertical transmission. Am J Obstet Gynecol 2016; 214:6.
9. American Academy of Pediatrics. Hepatitis B. In: Red Book: 2015 Report of the Committee on Infectious Diseases, 30th ed, Kimberlin D.W., Brady M.T., Jackson M.A., Long SS (Eds), American Academy of Pediatrics, Elk Grove Village, IL 2015. p. 400.
10. Cundy K.C., Sueoka C., Lynch G.R., et al. Pharmacokinetics and bioavailability of the anti-human immunodeficiency virus nucleotide analog 9-[(R)-2-(phosphonomethoxy)propyl]adenine (PMPA) in dogs. Antimicrob Agents Chemother 1998; 42:687.
11. Van Rompay K.K., Hamilton M., Kearney B., Bischofberger N. Pharmacokinetics of tenofovir in breast milk of lactating rhesus macaques. Antimicrob Agents Chemother 2005; 49:2093.
12. Ehrhardt S., Xie C., Guo N., et al. Breastfeeding while taking lamivudine or tenofovir disoproxil fumarate: a review of the evidence. Clin Infect Dis 2015; 60:275.
13. Gouraud A., Millaret A., Bernard N., et al. Tenofovir exposure through breast feeding: Serum concentrations in neonates and clinical follow-up. Fundam Clin Pharmacol. 2012;26 (Suppl 1):9.
14. Ganne-Carrie N., Causse X., Zarski J.P. et al. Efficacy and safety results of tenofovir DF (TDF) treatment from the first trimester in HBV pregnant women in real-life clinical practice. Hepatology. 2013;58 (Suppl 1):664A-5A.
15. Lactmed. Tenofovir. http://toxnet.nlm.nih.gov/cgi-bin/sis/search2/f?./temp/~SOkg2H:1.
16. Stevens C.E., Beasley R.P., Tsui J., Lee W.C. Vertical transmission of hepatitis B antigen in Taiwan. N Engl J Med 1975; 292:771.
17. Schillie S., Walker T., Veselsky S., et al. Outcomes of infants born to women infected with hepatitis B. Pediatrics 2015; 135:e1141.
18. Stevens C.E., Toy P.T., Tong M.J., et al. Perinatal hepatitis B virus transmission in the United States. Prevention by passive-active immunization. JAMA 1985; 253:1740.
19. Chen H.L., Lin L.H., Hu F.C., et al. Effects of maternal screening and universal immunization to prevent mother-to-infant transmission of HBV. Gastroenterology 2012; 142:773.
20. Guidelines for Perinatal Care. In: American Academy of Pediatrics and American College of Obstetricians and Gynecologists, 4th ed, Washington, DC 1997. p.286.
21. Pan C.Q., Duan Z., Dai E., et al. Tenofovir to Prevent Hepatitis B Transmission in Mothers with High Viral Load. N Engl J Med 2016; 374:2324.
22. The antiretroviral pregnancy registry. http://www.apregistry.com/forms/interim_report.pdf (Accessed on January 18, 2017).
