Importanţa şi aplicaţiile unor analize de laborator în infertilitatea la căţea (review)
The importance and use of some laboratory tests in bitch infertility (review)
Abstract
The present study is a summary of some laboratory means and methods, used in the investigation of cases that can be linked to reproductive diseases and pathology, respectively infertility, in bitches. Possible causes and serological, cytological, bacteriological, immunological evaluations will be discussed with the purpose of emphasizing the events taking place during oestrus surveillance, the correct management and the optimum breeding conditions in bitch, as well as identifying syncopes in evaluating these.Keywords
infertilitycytologyserologyimmunopathologyRezumat
Studiul de faţă este un rezumat al unor metode şi mijloace paraclinice de laborator implicate în investigarea unor cazuri ce pot fi încadrate în domeniul tulburărilor şi al patologiei reproducţiei, pe tema infertilităţii la căţea. Vor fi enumerate şi dezbătute cauze posibile şi evaluări de ordin serologic, citologic, bacteriologic, imunologic, cu intenţia evidenţierii şi aducerii în atenţie a cascadei de evenimente implicate în monitorizarea estrală, bunul management şi condiţiile optime de montă la căţea, precum şi identificarea sincopelor în evaluarea acestora.Cuvinte Cheie
infertilitatecitologieserologieimunopatologieInfertilitatea poate fi considerată reversul fertilităţii şi exprimă incapacitatea femelelor, mature sexual, de a se reproduce. Aceasta este considerată o tulburare pasageră, reversibilă, spre deosebire de sterilitate, care reprezintă tulburarea definitivă şi ireversibilă a funcţiei de reproducţie. Factorii cauzali ai acestor stări patologice pot acţiona din primele faze ale dezvoltării unui nou organism, începând cu stadiul de zigot, apoi în fazele organogenezei embrionare şi ale dezvoltării fetale, iar apoi în viaţa extrauterină (de la fătare până la pubertate şi apoi în perioada genitală). Ancheta ginecologică urmăreşte cunoaşterea individuală a fiecărui animal şi încadrarea lui într-o stare fiziologică sau patologică din punct de vedere reproductiv, să se cunoască situaţia generală a principalilor indici de reproducţie, precum şi măsurile care trebuie aplicate de urgenţă pentru îmbunătăţirea acestora. Deoarece este posibilă interferarea acţiunii mai multor factori nocivi ce pot îngreuna punerea unui diagnostic etiologic, trebuie ca specialistul să examineze animalul cu un deosebit discernământ.
Înainte de ancheta ginecologică propriu-zisă, trebuie să se analizeze următoarele elemente: alimentaţia, igiena, condiţiile de întreţinere, mişcarea şi odihna efectivului, situaţia epidemiologică, executarea însămânţărilor artificiale etc. Elementele pe baza cărora se execută ancheta ginecologică sunt: anamneza şi examenul clinic intern şi extern (Bîrţoiu A., Seiciu F., 2006).
Unele dintre cele mai comune simptome ce apar la căţelele inabile în a se reproduce ar fi estrul neregulat, incapacitatea de concepţie, greutate în a stabili contactul sexual, precum şi pierderea gestaţiei. Pentru a numi fertilitate în limite normale la căţea cu capacitate reproductivă de pui sănătoşi, este nevoie de un estru normal şi regulat, cu un aparat reproducător sănătos, ovule normale, hormoni reproductivi în limite optime şi constante, fertilizare fără anormalităţi de către spermatozoid, reacţia pozitivă a mediului de implementare a zigotului format, nidarea lui în endometru, plasarea normală a placentei, iar pentru susţinerea unei gestaţii până la termen, concentraţii stabile de progesteron. Toate aceste condiţii trebuie menţinute la nivel optim pe tot parcursul celor două luni de gestaţie, altfel procesul reproducţiei se alterează, rezultând infertilitatea (Fontbonne A., 2006).
Infertilitatea poate afecta căţele de toate vârstele, dar tinde să îşi facă apariţia în rândul celor geriatrice. Pentru căţele ce trec de 6 ani, cauza frecventă este hiperplazia cistică endometrială. Căţele ce au avut în antecendente infecţii uterine pot dezvolta şi ele dificultăţi în implantarea ovulului fecundat. Dar, în cele mai multe cazuri, o cauză majoră a infertilităţii o constituie inseminările în perioada greşită a estrului. Rasele de câini predispuse la insuficienţe tiroidiene au o prevalenţă mai mare în ceea ce priveşte problemele de fertilitate. Rasele cu risc particular de hipotiroidism sunt Boxerii, Dobermanii, Teckelii, Golden Retrieverii, Dogul german, Setterii irlandezi, Schnautzerii pitici şi Caniche-ul.
Alte criterii ce pot juca un rol în scăderea posibilităţii de reproducţie la căţele sunt:
- herpes virus canin;
- infecţii cu Toxoplasma spp.;
- anticorpii antispermatici;
- anticorpii antimüllerieni;
- hiperadenocorticism;
- hipotiroidism;
- funcţii ovariene dereglate;
- aberaţii cromozomiale;
- infecţii sistemice virale sau parazitare;
- factorii de infertilitate la câinele mascul;
- infecţii uterine subclinice;
- Brucella canis;
- lipsa stimulării înainte de actul copulator în vederea inducerii ovulaţiei căţelei.
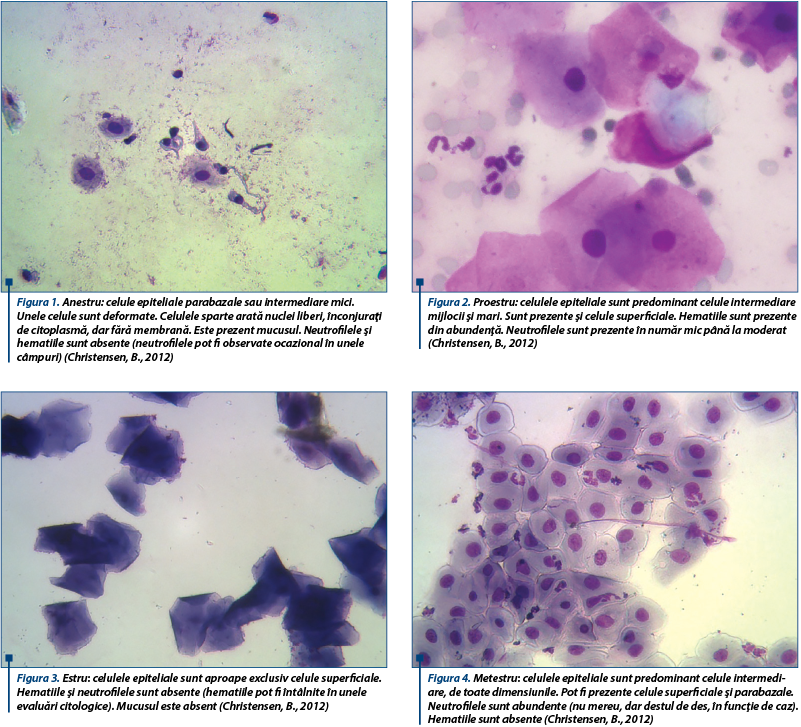
Principala metodă de verificare a stadiului estral al căţelei este citologia vaginală.
Toate schimbările observate în citologia vaginală pe perioada estrului căţelei sunt datorate modificărilor concentraţiei de estrogeni din organism. Înţelegerea mecanismului prin care apar aceste modificări şi efectele lor consecutive vizibile în citologie într-un cadru clinic vor ajuta clinicianul în întocmirea unui grafic al ciclurilor normale şi anormale. Estrogenul este produs pe calea steroidogenică, începând cu celulele tecale, unde diverse enzime fac conversia colesterolului în diferiţi pregnani şi eventual în hormoni androgeni androstendioni, transportaţi ulterior de-a lungul membranei bazale în celulele granuloasei (Okkens et al., 2006).
Determinarea progesteronului seric
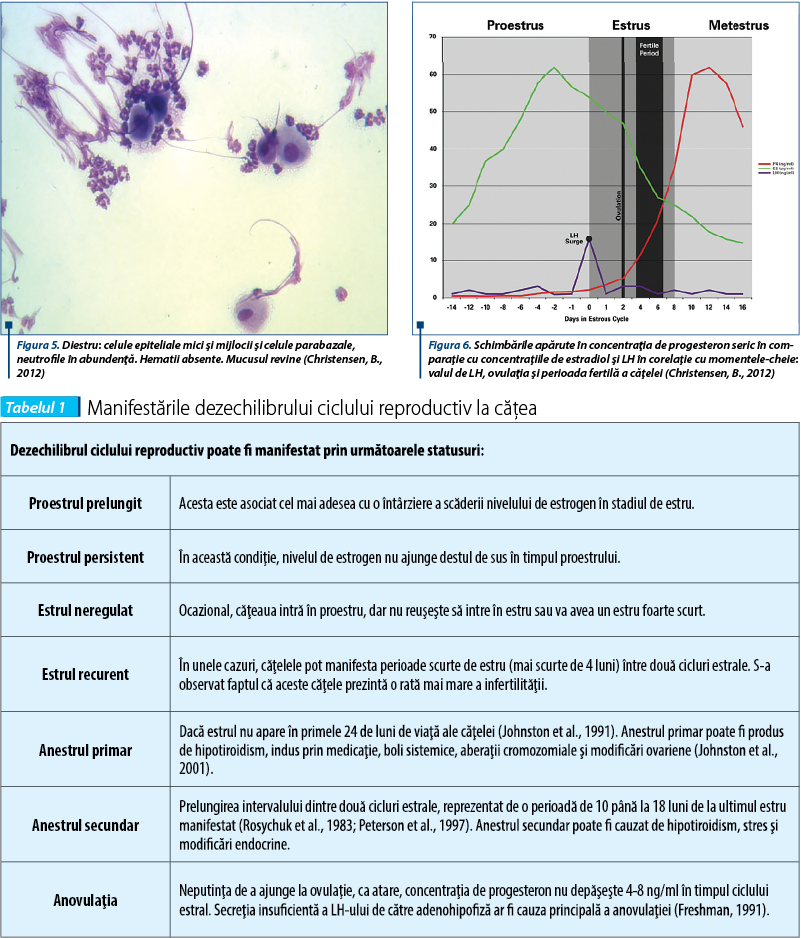
La căţea, progesteronul provine iniţial din ţesutul luteal ovarian. În timpul anestrului, concentraţiile bazale ale progesteronului seric sunt în mod normal mai mici de 1 ng/mL.
În timpul proestrului apare luteinizarea preovulatorie în unele celule foliculare, ca atare, înainte cu câteva zile înainte de ovulaţie, acestea îşi schimbă producţia de estrogen în producţie de progesteron (Concannon, P.W., 2006). Concentraţiile serice de progesteron în timpul proestrului cresc încet în jurul valorii de 1 ng/mL, unde se stabilizează pentru câteva zile până la aproape două săptămâni. La un moment dat, concentraţiile încep să crească din nou şi vor ajunge în jurul valorii de 5 ng/mL înainte de momentul ovulaţiei căţelei (Concannon, P.W., 1977). Odată pornită această creştere a progesteronului, rata de creştere a acestuia rămâne constantă în rândul căţelelor şi deci clinicianul poate corela evenimentele fiziologice ale vârfului de secreţie a LH-ului, ovulaţia şi începutul perioadei fertile cu nişte concentraţii corespunzătoare de progesteron seric.
Anomalii genetice
Există animale hermafrodite cu modificările specifice la nivel genital, fapt asociat cu aberaţii cromozomiale, gonadale şi fenotipice sexuale (Meyers - Wallen, 1993).
Aneuploidia, care reprezintă o aberaţie cromozomială în meioză sau în mitoză, ce rezultă în trisomie sau monosomie, este o altă cauză importantă de infertilitate la căţea. Mutaţiile genetice ce afectează dezvoltarea unui câine pot apărea în timpul unuia dintre cele 3 puncte de bază în concepţie: 1) în timpul stabilirii cromozomiale a genului - monosomie (XO), trisomie (XXX sau XXY) sau chimerism (unele celule XX, altele XY la acelaşi individ); 2) când se face traducerea de la nivel cromozomial a genului la nivel gonadal (discrepanţa între sexul cromozomial real şi cel al organelor reproducătoare reieşite, de exemplu ovarele căţelei sunt XY, şi nu XX); 3) în timpul dezvoltării tractului reproducător şi a organelor (apariţie externă de femelă, dar cu organe reproducătoare de mascul). Când una dintre aceste situaţii apare, funcţia reproducătoare normală este inhibată şi se instalează o stare permanentă şi ireversibilă de anestru (Breen et al., 2001).
Anomalii de diferenţiere sexuală: ooforita limfocitică, chisturile luteale ovariene, insuficienţa pituitară, aplazia ovariană/hipoplazia.
Sindromul Dezechilibrului Atipic de Cortizol-Estrogeni (ACEIS) identifică prezenţa cortizolului inactiv sau insuficient ce permite producerea unei cantităţi mari de adeno-estrogeni. Acest exces nu numai că se leagă la receptorul hormonului tiroidian, dar dereglează şi sistemul imunitar, care nu mai protejează pacientul. Creşterea estrogenului total apare, deci, ca urmare a dezechilibrului dat de stratul mijlociu al corticalei adeno-hipofizei cu producţie de cortizol. Acest dezechilibru poate fi cauzat de o deficienţă, de o legare sau de o inactivare a cortizolului, un nivel mare în concentraţie sau aproape inexistent al acestuia (Plechner, A.J., 2004).
Influenţa nutriţiei în infertilitate
Când o dietă este prea bogată în carbohidraţi, care fac conversie în zaharuri (cereale, amidonul din cartofi, mazăre, morcovi şi cartofi dulci, precum şi zaharuri simple, precum miere, fructe şi fructoză), această dietă face ca nivelul de zaharuri din organism să crească. Acest fapt, în schimb, face ca insulina să fie eliberată pentru a scădea nivelul zahărului. Atunci când nivelul zahărului scade, cortizolul este eliberat pentru a ajuta la creşterea nivelului de zahăr. Această reacţie are efect de bumerang, cu un efect de du-te-vino, ceea ce poate provoca extenuarea insulinică. Acest flux afectează nivelurile de estrogen, progesteron şi testosteron. Când cortizolul este eliberat în mod repetat ca răspuns la o dietă plină de zaharuri, acesta concurează cu progesteronul pentru aceiaşi receptori şi cortizolul câştiga de fiecare dată. Iar progesteronul este esenţial pentru fertilitate (Olson, L., 2015).
Hipotiroidismul
Hipotiroidismul este asociat cu infertilitatea şi este caracterizat prin anestru, neregularităţi în ciclul estral şi sângerări proestrale prelungite (Johnson, 1980; Nesbitt et al., 1980). Problemele de reproducţie asociate hipotiroidismului sunt cauzate de nivelul ridicat de prolactină serică (Chastin și Ganjam, 1986).
Hormonul anti-müllerian
Hormonul anti-müllerian (AMH), o glicoproteină homodimerică membră a familiei factorului de transformare a creşterii b (TGF-b), denumit şi substanţa inhibitorie mülleriană, a fost studiat în principal pentru rolul său de reglare a diferenţierii sexului masculin în perioada embrionară. Astfel, hormonul produs de către celulele Sertoli ale testiculului fetal induce regresia ductelor mülleriene, elementele primordiale ale tractului reproductiv feminin, şi prin aceasta contribuie la dezvoltarea normală a organelor genitale masculine. Odată cu începerea pubertăţii, AMH, la fel ca şi inhibina B, este produs de celulele stratului granulos ale foliculilor de creştere din ovar, şi nu de către foliculii primordiali, nici de către foliculii antrali în faza finală de creştere (aflaţi sub reglarea directă a FSH). Datorită exprimării specifice la nivelul celulelor stratului granulos din foliculii de creştere neselecţionaţi (foliculii primari şi secundari potenţial fertili), AMH constituie un marker ideal pentru estimarea rezervei ovariene (Visser et al., 2006).
O expresie AMH scăzută la nivelul foliculilor va diminua pragul pentru FSH, ceea ce face ca foliculii să-şi continue creşterea şi să ovuleze în ciclul următor (Durlinger et al., 1999; Durlinger, 2002).
Sindromul de pseudogestaţie
Sindromul de pseudogestaţie este prezent la căţele negestante după 6-12 săptămâni de estru şi este caracterizat prin semne de edem vulvar, lactaţie şi creşterea în mărime a glandei mamare (Jones et al., 1988).
Neoplaziile vaginale
Neoplaziile vaginale sunt cele mai răspândite tipuri de tumori ale sistemului reproducător la căţea (Manothaiudom et al., 1991). Cele mai importante neoplazii vaginale sunt: carcinom tranziţional celular al uretrei (TCC), tumori venerice transmisibile (TVT), carcinom scuamo-celular (SCC), leiomiom şi fibropapilom. Aceste tumori vaginale sunt prezente de obicei la căţeaua geriatrică, exceptând cele venerice prezente în mod obişnuit la tineret.
Metodele uzuale de diagnostic pentru aceste tumori sunt examenul fizic, panelul complet de analize, palparea (examinare digitală), vaginoscopia, citologia vaginală şi biopsia chirurgicală.
Bazele imunologice ale infertilităţii
Răspunsul imunitar patologic este una dintre etiologiile infertilităţii, chiar dacă până în acest moment nu există foarte multe dovezi. Obiectivul principal al studierii acestei etiologii ar fi sintetizarea datelor despre toleranţa antigenică, pierderea acesteia, patogeneza imunitară ce induce infertilitate şi diagnosticul de laborator al acesteia (Smith et al, 1999).
Autoimunitatea şi ţinte antigenice în patologia ovariană
Implicarea mecanismelor autoimune în încetarea prematură a funcţiei ovariene a fost pusă în dezbatere de numeroşi specialişti. În unele patologii ovariene, precum infertilitatea idiopatică, sindromul polichistic ovarian sau endometrita, au fost sugerate mecanisme asemănătoare. În orice caz, rolul exact al autoimunităţii în fiziopatologia acestor boli rămâne încă la nivel de controverse. Diagnosticul bolii ovariene autoimune se bazează pe ancheta clinică, biologică şi histologică, dar un interes special se acordă autoanticorpilor antiovarieni.
Ca ţinte sunt implicate enzime steroidogene, gonadotropinele şi receptorii lor, corpul luteal, zona pellucida şi ovocitul, care sunt investigate în continuare.
Toleranţa femelei la antigenele spermatice
Tractul genital la femelă este căptuşit cu celulele de componentă imunologică ce fagocitează spermatozoizii şi le procesează antigenele pentru recunoaştere imunitară. Acest mecanism poate fi influenţat de următorii factori:
n din numărul mare de spermatozoizi eliberaţi în partea superioară a vaginului, este posibil ca doar o mică parte, imunologic diferită faţă de majoritatea rămasă, să capete acces la tubii fallopieni; eliminarea spermei din tractul genital reduce numărul celor ce vor câştiga acces la sistemul imun; degradarea antigenelor spermatice de către enzimele extracelulare specifice uterului; fagocitoza spermatozoizilor de către celulele somatice şi macrofage, atracţia chemotactică pentru macrofage şi neutrofile în cervixul uterin şi în cavitatea peritoneală; legarea nespecifică a imunoglobulinelor sau a anticorpilor natural nepatogenici la spermatozoizii maturi, ca acţiune preliminară până la fagocitoza acestora. Acest mecanism poate, în schimb, creşte fagocitoza şi imunogenicitatea; prezenţa factorilor imunosupresori în sperma şi în lichidul folicular etc.
Boala autoimună
Atât pentru testicule, cât şi pentru ovare, apare în momentul în care balanţa înclină în favoarea celulelor T reactive patogenic la self, prin: 1. depleţia celulelor T supresoare (regulatorii) şi 2. activarea celulelor T reactive patogenic la self.
În ovar, structurile recunoscute de autoanticorpi includ: ovocitul şi foliculii, zona pellucida, celulele granuloasei, celulele tecale, celulele luteale şi receptorii pentru gonadotropina corionică. Un rol al hiperstimulării ovariene înainte de fertilizări in vitro în producţia de autoanticorpi ovarieni ar fi posibil, la fel şi o traumă repetată asupra ovarului de extracţie a unui ovocit în vederea fertilizării in vitro (Agarwal et al., 2007).
Anticorpii antispermatici (ASA)
Faptul că sperma poate induce apariţia anticorpilor este bine cunoscut încă din 1899. ASA sunt detectabili la 7-15% din masculi şi la 13-80% din femelele cu infertilitate inexplicabilă.
Poţi fi găsiţi în ser, lichid seminal, pe suprafaţa spermatozoizilor, în mucus cervical. Fac parte din clasa de imunoglobuline IgG, IgM şi IgA.
Testarea în laborator a infertilităţii imunologice
Până în acest moment, foarte puţine teste de analiză a imunităţii mediate celular au fost prezentate. Acest lucru se datorează complexităţii sistemului imunitar celular, precum şi componentelor ce mediază infertilitatea, asupra cărora încă se lucrează la definire şi elaborare. Când există suspiciunea de infertilitate produsă de ASA (infertilitate inexplicabilă), poate fi folosit unul dintre testele disponibile. Acestea se împart în 5 grupe:
Teste de aglutinare - macro: Test de aglutinare în gel (GAT); Reacţia mixtă anti-globulină (MAR); Testul immunobead® este o procedură specifică, folosită în detecţia prezenţei anticorpilor IgG, IgM şi IgA, care demonstrează ce zonă a spermatiei (cap, gât sau coadă) afectează autoanticorpii. Sperma este combinată cu particule de poliacrilamidă, anterior căptuşite fie cu anti-IgG, anti-IgM sau anti-IgA.
Fluorescenţa anticorpilor: imunofluorescenţa (IF); citometria în flux.
Colorimetrie: Enzyme-linked immunosorbent assay (ELISA).
Evaluare radioimună: Testul prin antiglobuline radiomarcate.
Fiecare dintre aceste teste are avantaje şi dezavantaje. Pentru o evaluare completă, indicată este folosirea tuturor acestor teste ce pot oferi localizarea, izotipul şi cuantificarea legăturilor dintre anticorpi.
Insuficienţa luteală la căţea, ca o consecinţă a răspunsului autoimun la progesteron
Scurtarea ciclului estral, moartea embrionică şi avortul, toate acestea pot fi asociate cu o secreţie insuficientă de progesteron de către corpul luteal al căţelei. Se verifică concentraţia de progesteron, prolactina şi relaxina în faza hipoluteică şi controlul în timpul gestaţiei şi în perioada unui ciclului estral negestant. Mai mult, anticorpii canini antiprogesteron au fost analizaţi din cauza posibilei pierderi embrionare asociate cu modificările hormonale, corelate cu răspunsul anticorpilor hormonali (Jenny K. et al., 2006).
Diagnosticul diferenţial
Diagnosticul diferenţial pentru infertilitate se face între probleme de management şi protocol clinic de delimitare în timp a ovulaţiei, căţele care ulterior nu au permis montarea sau nu au prins monta după o montă forţată sau inseminare artificială, verificarea în timpul perioadei fertile a managementului defectuos din partea crescătorilor.
Perioadele de receptivitate şi fertilitate în timpul estrului variază semnificativ în rândul căţelelor normale şi chiar de la individ la individ la cicluri următoare. Aceste perioade pot să nu coincidă cu alegerea iniţială a timpului optim de montă, la a zecea - a 14-a zi de la primele scurgeri sangvinolente vaginale. Protocoalele de stabilire a momentului ovulaţiei folosind citologia vaginală, vaginoscopia repetată şi verificarea concentraţiilor de progesteron şi LH sunt folositoare în identificarea perioadei fertile, când ar trebui instituită monta, permiţând un management corect al montelor. Clinicianul trebuie să aibă în vedere faptul că un moment optim al ovulaţiei nu poate fi stabilit decât atunci când se face corelarea tuturor rezultatelor examenelor şi ale testelor aferente (Jenny K. et al., 2006).
Bibliografie
1. Agarwal, S. and Naik, S., 2007: Fundamentals of Immunogenetics: Principles and Practices. International Book Distributing Co (Publishing Division), Lucknow., pp. 217-228.
2. Bîrţoiu A., Seiciu F., 2006: Tratat de Patologia reproducţiei la animale, Ed. Bic All, Bucureşti.
3. Breen, M., et al., 2001: Chromosome-specific single-locus FISH probes allow anchorage of an 1800-marker integrated radiation-hybrid/linkage map of the domestic dog genome to all chromosomes. Genome Research 11.10: 1784-1795.
4. Chastin C.B., Ganjam V.K., 1986: Clinical Endocrinology of Companion Animals. Lea & Febiger, Philadelphia., Pp. 140.
5. Christensen, Bruce W., 2012: The physiology of ovulation timing in the bitch, Veterinary Clinical Sciences, College of Veterinary Medicine, Iowa State University, Ames, IA.
6. Concannon P.W., 2009: Endocrinologic control of normal canine ovarian function. Reprod Domest Anim; 44:3-15.
7. Concannon P.W., 2010: Reproductive cycles of the domestic bitch. Anim Reprod Sci;doi:10.1016/janireprosci.2010.08.028.
8. Durlinger, A.L.L. et al., 2002: Regulation of ovarian function: the role of Anti-Müllerian hormone. Reproduction, 124, 601-609.
9. Feldman E.C., Nelson R.W., 2004: Ovarian cycle and vaginal cytology. In. Canine and feline endocrinology and reproduction. Eds: R.W.B. Kersey. Saunders, Philadelphia. pp. 752-774.
10. Fontbonne, A., 2006: R–Reproduction/ Infertility in the bitch - World Congress WSAVA/FECAVA/CSAVA, IVIS proceedings/lecture 24, Paris, France, pp. 679 -682.
11. Fontbonne, A., Claire Sarrazin, B. Polack, 2010; Neosporosis in dogs: consequences on reproduction?, Bulletin de l’Academie Veterinaire, France, Vol 163 - N°2.
12. Jenny A. Visser, et al., 2006: Anti-Müllerian hormone: a new marker for ovarian function. Reproduction, 131 1-9.
13. Krachudel, Jenny, et al., 2013: Luteal insufficiency in bitches as a consequence of an autoimmune response against progesterone?.Theriogenology 79.9: 1278-1283.
14. Smith D.A. and Germolec D. R., 1999: Introduction to immunology and auto-immunity. Environ Health Perspect ; 107 Suppl. 5: 661-5.



