Non-cystic fibrosis bronchiectasis (NCFB) is still an important cause of chronic suppurative lung disease in low-income countries and among disadvantaged populations of high-income countries. Bronchiectasis is defined as a dilatation of the airway (bronchi, bronchioles), accompanied by inflammatory destruction of bronchial and peribronchial tissue. The pathogenesis is thought to be the breakdown of local lung defenses, leading to infection, inflammation, bronchial obstruction, airway damage, ineffective mucociliary clearance and persistent retention of secretions infection. Bronchiectasis should be suspected if a child has chronic cough and recurrent chest infections. High-resolution chest computed tomography (HRCT) is necessary as chest radiography is not sensitive for detecting early disease. An underlying cause for bronchiectasis cannot be determined in all patients. The treatment is based on optimizing airway clearance techniques and intermittent courses of antibiotics for pulmonary exacerbations. Surgery is an option for localized bronchiectasis. Lung transplantation might only be an option in patients with advanced lung disease and declining lung function.
Bronşiectaziile non-fibroză chistică – diagnostic şi management terapeutic
Non-cystic fibrosis bronchiectasis – diagnosis and therapeutic management
First published: 28 decembrie 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Pedi.52.4.2018.2153
Abstract
Rezumat
Bronşiectaziile non-fibroză chistică (NCFB) sunt încă o cauză importantă de boală pulmonară supurativă cronică, în ţările slab dezvoltate şi în rândul populaţiei dezavantajate din ţările dezvoltate. Bronşiectazia se defineşte prin dilatarea căilor respiratorii (bronhii, bronhiole), asociată cu un proces distructiv inflamator al bronhiei şi al ţesutului peribronşic. Patogeneza se consideră a avea legătură cu deficienţa mecanismelor pulmonare locale de apărare, conducând la infecţie, inflamaţie, obstrucţie bronşică, distrucţia căilor respiratorii, clearance mucociliar ineficient, retenţia şi persistenţa secreţiilor infectate. Bronşiectazia trebuie suspectată dacă un copil are tuse cronică productivă şi infecţii respiratorii recurente. Tomografia computerizată de înaltă rezoluţie (HRCT) este necesară, deoarece radiografia pulmonară nu este sensibilă în detectarea bolii precoce. O cauză subiacentă a bronşiectaziei nu poate fi întotdeauna determinată. Tratamentul se bazează pe optimizarea tehnicilor de clearance al căilor respiratorii şi cure intermitente de antibiotice în exacerbările pulmonare. Chirurgia este o opţiune pentru bronşiectaziile localizate. Transplantul pulmonar poate fi singura opţiune la pacienţii cu boală pulmonară avansată şi declinul funcţiei pulmonare.
Introducere
În anul 1819, Rene Laennec, inventatorul stetoscopului, a descris prima dată bronşiectazia la pacienţii cu tuberculoză pulmonară sau sechele de pneumonie. Bronşiectazia a fost ulterior folosită ca un termen morfologic pentru a descrie dilatarea căilor respiratorii, susţinută de semne clinice şi radiologice.
Bronşiectazia ilustrează descrierea patologică a unui proces de boală care poate avea cauze multiple şi se caracterizează prin dilatarea anormală a bronhiilor sau bronhiolelor, asociată cu îngroşarea pereţilor acestora.
Cea mai comună cauză de bronşiectazie în copilărie este fibroza chistică, dar există şi alte numeroase cauze. Bronşiectaziile non-fibroză chistică (NCFB) reprezintă încă o cauză importantă de boală cronică supurativă pulmonară în ţările în curs de dezvoltare şi în cadrul populaţiei dezavantajate din ţările dezvoltate. O scădere a prevalenţei a fost observată începând cu 1950 în ţările dezvoltate, odată cu îmbunătăţirea sistemului de sănătate şi a accesului la acesta, cu introducerea pe scară largă a vaccinării şi cu folosirea precoce a antibioticelor.
Fiziopatologie
Bronşiectazia se defineşte prin dilatarea căilor respiratorii (bronhii, bronhiole), asociată cu un proces distructiv inflamator la nivelul bronhiei şi al ţesutului peribronşic. Iniţial s-a crezut că este ireversibilă, dar în prezent există evidenţe clare că unele bronşiectazii apărute în copilărie se pot remite.
Etiologia NCFB este variabilă, dar mecanismul fiziopatologic comun presupune infecţie, inflamaţie şi distrucţie tisulară. Dacă injuria asupra căilor respiratorii este severă sau recurentă, afectarea acestora devine ireversibilă şi se autoîntreţine.
Patogeneza se consideră că are legătură cu afectarea mecanismelor locale de apărare pulmonară, conducând la apariţia infecţiei, inflamaţiei şi obstrucţiei bronşice, cu afectarea mecanismelor de clearance mucociliar, ceea ce determină retenţia secreţiilor şi persistenţa infecţiei.
Răspunsul inflamator excesiv de la nivelul căilor respiratorii, stimulat de încărcătura bacteriană, determină o creştere a producţiei de citokine proinflamatorii şi activarea necontrolată a mediatorilor celulari, conducând la afectarea severă a căilor respiratorii.
Etiologie
Nu se poate determina întotdeauna cauza bronşiectaziei. Investigaţiile amănunţite pot identifica etiologia în 60-70% din cazuri. Îmbunătăţirea tehnicilor de diagnostic pentru cele mai subtile anomalii imunologice şi posibilitatea identificării defectului ciliar primar au dus la scăderea procentului de cazuri idiopatice.
Perioada dintre primele simptome şi diagnostic este uneori destul de lungă pentru a putea dovedi cauzalitatea. Printre etiologiile identificate în copilărie, infecţiile severe se află pe primul loc. Astfel, infecţia cu virusurile gripale, adenovirusuri, virusul rujeolei, dar şi cu Bordetella pertussis pot determina apariţia de bronşiectazii. Infecţii bacteriene severe cu Streptococcus pneumoniae, Staphylococcus aureus sau cu Mycobacterium tuberculosis sunt, de asemenea, incriminate.
Dintre sindroamele de imunodeficienţă asociate frecvent cu bronşiectazii sunt menţionate: agamaglobulinemia, imunodeficienţa comună variabilă, deficitele de IgA şi subclase de IgG, hiper-IgE, boala granulomatoasă cronică, sindromul ataxie-telangiectazie.
Diskinezia ciliară primară poate fi o cauză de infecţii recurente încă de la vârsta de sugar şi trebuie luată în considerare. Mai rar, pot apărea bronşiectazii post-obstrucţie, ca în aspiraţia de corp străin neglijată sau în obstrucţia prin compresie tumorală sau adenopatie. Sindromul de aspiraţie cronică asociat unor afecţiuni neurologice sau patologiei de reflux se caracterizează de repetate pneumonii de aspiraţie, cu pneumonii recurente şi bronşiectazii.
Bolile de colagen şi vasculitele, cum ar fi sarcoidoza, sunt menţionate mai rar în etiologia NCFB, alături de sindroame care asociază anomalii congenitale ale căilor respiratorii, respectiv sindromul Williams-Campbell (absenţă de cartilaj) şi sindromul Mounier-Kuhn (traheobronhomegalie). În cadrul etiologiilor mai rare sunt menţionate şi sindromul Ehler-Danlos, sindromul Marfan, sindromul Young şi sindromul unghiilor galbene.
Formele atipice de fibroză chistică sunt dificil de diagnosticat – statisticile arată că evaluarea complexă în centre specializate identifică aproximativ 20% dintre acestea.
Manifestări clinice
Copilul cu bronşiectazii se prezintă pentru tuse productivă persistentă şi infecţii respiratorii recurente. Unii pacienţi pot avea wheezing recurent, iar un procent mic pot prezenta hemoptizii. Pneumonia recurentă sau persistentă este una dintre principalele cauze pentru care pacientul se prezintă la medic. În lipsa exacerbărilor, examenul clinic pulmonar poate fi normal în formele uşoare, până la momentul în care anomaliile căilor aeriene devin semnificative. Pe măsură ce boala avansează, examenul clinic relevă diminuarea murmurului vezicular şi se pot ausculta raluri crepitante în inspir. De asemenea, poate apărea wheezing expirator când există o afectare severă a căilor respiratorii.
Hipocratismul digital poate fi prezent la copiii cu forme moderate sau severe de NCFB, fiind de cele mai multe ori legat de o evoluţie îndelungată, cu frecvente exacerbări, şi nu de o extindere a bolii. Dispneea şi cianoza apar tardiv în evoluţie sau în exacerbări severe. În formele cu evoluţie îndelungată se constată semne de hipertensiune pulmonară secundară şi cord pulmonar cronic. Otita medie recurentă, falimentul creşterii, refluxul gastroesofagian, rinite şi otite recurente din perioada neonatală, dar şi intoleranţa la efort sau hemoptizia pot fi motive de prezentare şi internare în centre specializate, în vederea evaluării.
Suspiciunea de NCFB trebuie luată în considerare în următoarele condiţii: tuse cronică umedă sau productivă, cu durata de cel puţin opt săptămâni, astm bronşic neresponsiv la tratament, rezoluţie incompletă a pneumoniei după tratament sau pneumonie recurentă, raluri crepitante persistente, aparent neexplicate, sau hemoptizii.
Imagistica
Radiografia pulmonară poate arăta semne de îngroşare a pereţilor bronşici sau/şi dilatarea căilor respiratorii, realizând imagini tubulare mai mult sau mai puţin paralele, uneori „în şine de tramvai” sau „fagure de miere” (bronhii dilatate cu conţinut aerian în mijlocul unui parenchim atelectatic). Examenul radiologic este nespecific în multe cazuri, iar o radiografie pulmonară normală nu exclude diagnosticul.
Diagnosticul definitiv de NCFB este susţinut de tomografia computerizată pulmonară de înaltă rezoluţie (HRCT), tehnică imagistică ce a înlocuit bronhografia şi reprezintă gold standard pentru diagnosticul bronşiectaziilor, având o sensibilitate de 97%. Bronşiectazia este prezentă dacă diametrul intern luminal este uşor mai mare decât cel al vasului de sânge adiacent (semnul inelului cu pecete – figura 1). Îngroşarea peribronşică este prezentă dacă grosimea peretelui este egală sau mai mare decât diametrul vasului adiacent (figura 2). Pe parcursul efectuării HRCT se evaluează zonele de impactări mucoide, bronşiectaziile, respectiv abcesele sau dilataţiile saculare, se poate evalua arborele bronşic şi divizarea acestuia sau prezenţa unor condensări, pleurezii sau abcese (figura 3).
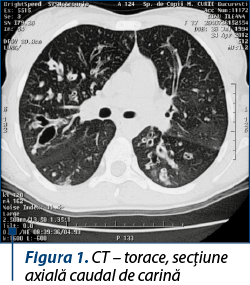
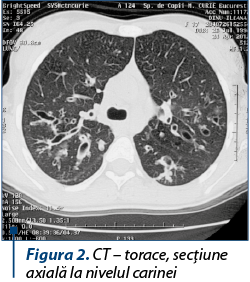
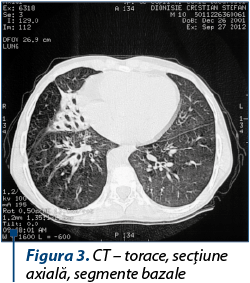
Rezonanţa magnetică nucleară (RMN) pulmonară este o nouă metodă care se poate utiliza în diagnosticul NCFB. Studiile au arătat că RMN-ul pulmonar furnizează date echivalente cu HRCT în ceea ce priveşte diagnosticul şi determinarea extinderii bolii pulmonare la copiii cu bronşiectazii non-fibroză chistică.
Testele funcţionale pulmonare efectuate de copiii de peste 5 ani pot arăta o disfuncţie ventilatorie obstructivă, restrictivă sau mixtă.
Spirometria nu aduce informaţii pentru diagnostic, dar poate servi ca marker de progresie a bolii. Nu se foloseşte în detectarea precoce a bronşiectaziilor şi a defectelor căilor respiratorii. S-a constatat că funcţia pulmonară la copiii cu NCFB scade semnificativ în timp, în ciuda unui tratament adecvat.
Microbiologia
Cultura de spută reprezintă standardul de evaluare a colonizării şi infecţiei în NCFB (uneori se apelează la sputa indusă când nu se poate obţine expectoraţia). Cei mai frecvenţi germeni izolaţi din spută sunt: Hemophilus influenzae, Pseudomonas aeruginosa, Streptococcus pneumoniae, Staphylococcus aureus şi Moraxella catarrhalis.
Evaluare diagnostică în vederea stabilirii etiologiei
După confirmarea imagistică a diagnosticului de bronşiectazie, trebuie evaluată cauza subiacentă a acesteia, prin efectuarea unor investigaţii mai mult sau mai puţin invazive. Localizarea bronşiectaziilor pe HRCT poate sugera etiologia. Astfel, prezenţa acestora unilateral, în lobul superior, poate sugera etiologia tuberculoasă, în timp ce prezenţa bilaterală în lobii superiori este caracteristică fibrozei chistice. Bronşiectaziile centrale sunt caracteristice aspergilozei bronhopulmonare alergice (ABPA), iar cele focale din lobii inferiori apar după aspiraţii de corp străin. Afectarea multilobară se întâlneşte după pneumonii virale, pneumonii recurente de aspiraţie sau asociate bolilor sistemice, imunodeficienţelor şi patologiei ciliare primare.
Tuturor copiilor cu bronşiectazii li se va efectua testul sudorii, pentru a exclude fibroza chistică (FC), necesitând cel puţin două teste. Dacă valoarea testului este normală sau borderline şi gradul de suspiciune este mare, se va efectua analiza genetică, necesitând uneori un test extins. Screeningul normal al imunodeficienţelor include determinări cantitative ale imunoglobulinelor IgA, IgM, IgG, alături de subclase de IgG şi nivelul complementului. Determinările specifice imunologice includ, de asemenea, dozarea nivelului anticorpilor postvaccinali, răspunsul la dozele booster, evaluări ale imunităţii mediate celular sau teste care evaluează funcţia neutrofilelor. Testarea HIV este necesară dacă există suspiciunea legată de boală.
Tuberculoza pulmonară trebuie exclusă prin efectuarea intradermoreacţiei la tuberculină, dar şi a frotiului şi a analizei genetice (PCR), care vor fi efectuate din secreţiile obţinute la bronhoscopie. Rezultatul culturilor pentru bacilul Koch este tardiv. La copiii mai mari se mai poate efectua testul Quantiferon, respectiv dozarea interferonului gama. Se cunoaşte faptul că la copiii cu NCFB cauza postinfecţioasă este frecventă, dar uneori momentul diagnosticului este tardiv şi astfel de cauze pot fi puse greu în evidenţă. Serologiile unor anticorpi în dinamică, alături de istoric, pot susţine diagnosticul etiologic. Bronhoscopia cu bronhoscop flexibil evidenţiază obstrucţia căilor respiratorii, face o inspecţie vizuală a mucoasei acestora şi colectează secreţii de la acest nivel. Uneori se poate face un lavaj bronhoalveolar (LBA), din care se fac frotiuri şi culturi. Prezenţa unor germeni ca Pseudomonas aeruginosa este important de stabilit, atât în diagnosticul etiologiei, cât şi în managementul terapeutic al exacerbărilor.
Patologia de reflux sau aspiraţie cronică va beneficia de evaluare atentă, fiind necesare tranzit baritat, pH-metrie esofagiană sau videofluoroscopie.
Diskinezia ciliară primară poate fi diagnosticată prin studii în microscopie electronică a probelor obţinute din biopsie ciliară şi periaj bronşic efectuate în centre specializate. Aspergiloza bronhopulmonară alergică va trebui exclusă prin serologii specifice.
Pentru cauze foarte rare care implică patologii autoimune inflamatorii, colagenoze sau vasculite se vor face teste specifice în funcţie de anamneză şi de alte semne clinice prezente.
În cazuri rare au fost raportate în etiologia NCFB astmul netratat, necontrolat terapeutic sau corp străin nediagnosticat.
Management terapeutic
Scopul tratamentului este controlul simptomelor, prevenirea progresiei bolii şi asigurarea unei creşteri şi dezvoltări normale. Când identificăm cauza bronşiectaziei, managementul specific va fi direcţionat asupra acesteia. Nu există consens în tratamentul NCFB. Recomandările de management se bazează pe evidenţe extrapolate din studiile efectuate la copiii cu bronşiectazii din FC. Recomandările generale trebuie respectate şi adaptate fiecărui pacient în parte.
Fizioterapia toracică şi exerciţiile, alături de gimnastica respiratorie sunt esenţiale în favorizarea clearance-ului secreţiilor din căile respiratorii, având rolul de a scădea numărul de exacerbări şi de a încetini declinul funcţiei pulmonare. Se folosesc diferite metode manuale sau mecanice: tapotajul toracic, drenajul postural, oscilaţii de înaltă frecvenţă ale căilor aeriene, presiune expiratorie pozitivă etc. Tratamentul mucolitic, adjuvant al fizioterapiei, foloseşte inhalaţii cu soluţii saline hipertone sau cu dornază. Deşi se folosesc uneori, nu sunt suficiente studii care să arate eficienţa acestor tratamente în NCFB. Tratamentul antiinflamator foloseşte corticosteroizi în administrare sistemică în timpul exacerbărilor cu insuficienţă respiratorie sau în ABPA. Administrarea corticosteroizilor inhalatori nu beneficiază de suficiente studii la copii, care să le arate eficienţa, deşi studiile efectuate la adulţi au demonstrat o îmbunătăţire a calităţii vieţii. Tratamentul nu se recomandă de rutină, cu excepţia pacienţilor care prezintă simptome de hiperreactivitate bronşică. Tratamentul bronhodilatator este indicat la pacienţii cu hiperreactivitate bronşică; s-a constatat că îmbunătăţeşte mişcările cililor, facilitând clearance-ul mucusului şi secreţiilor. Tratamentul antibiotic va fi recomandat şi utilizat în exacerbări, pe cale sistemică şi/sau inhalatorie. Se vor utiliza antibiotice conform antibiogramei faţă de germenii izolaţi din culturile de spută sau lichidul de LBA, în doze mari şi pentru perioade lungi. În cazul infecţiei cu Pseudomonas aeruginosa, regimurile de tratament vor fi aceleaşi ca în cazul pacienţilor cu fibroză chistică.
Unii autori au propus administrări repetate de antibiotice, în scop profilactic, însă cei mai mulţi consideră că acestea ar putea duce la rezistenţa germenilor faţă de antibioterapie. În plus, nu s-au dovedit eficiente în ceea ce priveşte prevenţia exacerbărilor. Este permisă o singură excepţie, respectiv folosirea azitromicinei, în cure de lungă durată, trei zile pe săptămână. Studiile au dovedit efectul antiinflamator al acesteia (scăderea numărului de neutrofile şi a IL8 în lichidul de LBA), având un rol important de reducere a numărului de exacerbări şi de menţinere a funcţiei pulmonare.
Antibioticele inhalatorii se folosesc mai ales în cazul infecţiei/colonizării cu Pseudomonas aeruginosa, conform protocoalelor de la FC. Nu există date suficiente pentru recomandarea tratamentului cu antagonişti de receptori de leucotriene, carbocisteină, manitol sau methilxantine.
Tratamentul chirurgical se recomandă la cei cu forme localizate, care prezintă simptome semnificative persistente, neresponsive la tratament; se recomandă, de asemenea, în cazul pacienţilor care prezintă hemoptizii masive neresponsive la embolizarea arterei bronşice.
Transplantul pulmonar poate fi singura opţiune la pacienţii cu boală pulmonară avansată şi declin sever al funcţiei pulmonare. Nu există ghiduri specifice pentru indicaţia de transplant; se aplică aceleaşi criterii recomandate în cazul pacienţilor cu FC. Managementul infecţiilor este cheia unei evoluţii favorabile posttransplant.
Profilaxie şi prognostic
Se recomandă vaccinarea antigripală anuală şi antipneumococică potrivit schemelor de vaccinare. Copiii se vor vaccina antirujeolă şi antipertussis, având în vedere incidenţa NCFB postinfecţioase.
Exacerbările infecţioase vor fi atent monitorizate şi tratate conform sensibilităţii germenilor identificaţi. Infecţia cronică cu Pseudomonas este legată de un prognostic nefavorabil.
Simptomele nocturne şi hipoxemia afectează calitatea somnului (apnee de somn), iar copiii pot prezenta afectarea creşterii, deficienţă de învăţat şi dezvoltare emoţională deficitară. Copiii cu NCFB vor fi monitorizaţi regulat în ceea ce priveşte simptomatologia, examenul clinic, creşterea, starea de nutriţie şi funcţia pulmonară, pentru că, în timp, s-a observat la aceşti copii declinul funcţiei pulmonare, deşi schemele terapeutice utilizate au fost corespunzătoare.
Când există suspiciune de bronşiectazie, se va indica efectuarea de HRCT, pentru un diagnostic corect al bolii încă din stadiile incipiente. Acest lucru va permite tratamentul corect al exacerbărilor şi monitorizarea bolii. Sunt descrise şi cazuri de reversibilitate a bronşiectaziilor în copilărie, mai ales dacă există o cauză subiacentă care beneficiază de tratament.
Conflict of interests: The author declares no conflict of interests.
Bibliografie
- Bastardo CM, Sounnappa S, Stanojevic S et al. Non CF – fibrosis bronchiectasis in childhood: longitudinal growth and lung function. Thorax. 2009; 64; 246- 251.
- Chaleners JD, Chotirmall SH. Bronchiectasis: new therapies and new perspectives. Lancet Respir Med. 2018.
- Chang AB, Oppenheimer JJ, Weiberger MM et al. Children with chronic wet or productive cough – treatment and investigations: a systematic review. Chest. 2016;149;120 -142.
- Chang AB, Children with chronic cough: when is watchful waiting appropriate; Development of likelihood ratios for assessing children with chronic cough. Chest. 2015; 147; 745-753.
- Douros CM. Alexopoulous E, Nicopoulous A. Bronchoscopic and high resolution CT findings in children with chronic cough. Chest. 2011; 140; 317- 323.
- Goyal V, Grimmwood K, Master IB et al. State of the art: pediatric bronchiectasis. Pediatric Pulmonolog. 2016; 51, 450-469.
- Greenberger PA, Bush RK, Demin JG et al. Allergic bronchopulmonary aspergillosis. J Allergy Clin Immunol Pract. 2014;2; 703-708.
- Hull J, Forton J, Thomson A. Paediatric Respiratory Medicine, Oxford specialist in paediatrics; Non cystic fibrosis bronchiectasis. 2015;387-395.
- Rademacher J, Ringshausen FC. Prevention and treatment of exacerbations of non-CF–bronchiectasis: The spectrum of bronchial infection. European Respiratory monograph. 2013;127-137.
- Lucas JS, Barbato A, Collins SA et al. European Respiratory Society Guidelines for the diagnosis of primary cilliary dyskinesia. Eur Respir J. 2017:49.
- O’Grady KF, Drescher BJ, Goyal V et al. Chronic cough postacute respiratory illness in children: a cohort study. Arch Dis Child. 2017; 102; 1044–1048.
- Pasteur MC, Bilton D, Hill AT. British Thoracic Society Bronchiectasis non-CF Guideline Group, British Thoracic Society guideline for non-CF bronchiectasis, 2018, Thorax 65(suppl); 11-58.
- Pizzuto SJ, Hare K M, Upham JV et al. Bronchiectasis in children; current concepts in immunology and microbiology. Front Pediatr. 2017;5; 123.
- Wikson R, Hansell DM, Loebinger MR. Definition and aetiology of non-CF-bronchiectasis. The spectrum of bronchial infection. European Respiratory monograph. 2013;107-120.
- Singleton RJ, Valery PC, Morris P et al. Indigenous children from three countries with non CF fibrosis chronic suppurative lung disease/bronchiectasis. Pediatric Pulmonol. 2014; 49; 184-200.
Articole din ediţiile anterioare
Rolul biomarkerilor în patologia pulmonară din fibroza chistică (mucoviscidoza)
Biomarkerii reprezintă indicatori cuantificabili, care ajută la susţinerea diagnosticului sau a evaluărilor unei anumite patologii. Biomarkerii p...
Asthma: from complex pathophysiology to histological changes
Astmul este cea mai frecventă afecţiune pulmonară cronică şi afectează aproximativ 15-20% din populaţie în ţările dezvoltate, în timp ce rata est...