Hepatic encephalopathy (EH) is a syndrome involving a series of neuropsychiatric abnormalities in patients with hepatocellular damage and/or portosystemic venous shunts in the absence of other cerebral diseases. It is the late consequence of portal hypertension with a high degree of spontaneous or surgically created portosystemic shunts. The pathogenic substrate is the diffuse disturbance of cerebral metabolism due to insufficient processing or shunting of the liver by intestinal toxic nitric products. The clinical evaluation by psychometric tests may reveal minimal EH for an adequate early management and preservation of the integrity of cerebral functions in patients with cirrhosis.
Encefalopatia hepatică – consideraţii actuale
Hepatic encephalopathy - current considerations
First published: 28 mai 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Pedi.54.2.2019.2435
Abstract
Rezumat
Encefalopatia hepatică (EH) reprezintă un sindrom ce cuprinde o serie de anormalităţi neuropsihice la pacienţi cu afectare hepatocelulară sau/şi şunturi venoase portosistemice, în absenţa altor afecţiuni cerebrale. EH este consecinţa tardivă a hipertensiunii portale cu grad crescut de şunturi portosistemice spontane sau create chirurgical şi are ca substrat perturbarea difuză a metabolismului cerebral ca urmare a prelucrării insuficiente sau a şuntării ficatului de către produşii toxici azotaţi de origine intestinală. Evaluarea clinică prin teste psihometrice poate evidenţia EH minimă pentru un management precoce adecvat şi păstrarea, pe cât posibil, a integrităţii funcţiilor cerebrale la pacienţii cu ciroză.
Introducere
În cursul evoluţiei cirogene a hepatopatiilor cronice, surprinderea apariţiei fenomenelor ce ţin de complicaţiile hipertensiunii portale reprezintă un moment esenţial. Manifestările digestive, neurologice, renale şi pulmonare ale hipertensiunii portale pot surprinde clinicianul prin gravitate, iar managementul optim al acestora este o condiţie necesară în evoluţia pacienţilor.
Encefalopatia hepatică (EH) reprezintă un sindrom ce cuprinde o serie de anormalităţi neuropsihice la pacienţi cu afectare hepatocelulară sau/şi şunturi venoase portosistemice, în absenţa altor afecţiuni cerebrale(1,2).
EH este consecinţa tardivă a hipertensiunii portale cu grad crescut de şunturi portosistemice spontane sau create chirurgical şi are ca substrat perturbarea difuză a metabolismului cerebral, ca urmare a metabolizării insuficiente sau a şuntării ficatului de către produşii toxici azotaţi de origine intestinală(3).
Termenul de encefalopatie portosistemică este frecvent utilizat ca sinonim pentru encefalopatia hepatică.
Encefalopatia hepatică clinic manifestă este prezentă la 28% din pacienţii cu ciroză hepatică(4), iar dacă se includ şi formele subclinice, până la 70% dintre pacienţii cu ciroză hepatică prezintă diferite grade de EH(5). Circa 30% dintre cei cu ciroză hepatică decedează în sau prin EH severă. În cazul pacienţilor cu şunturi portocave sau spleno-renale distale, EH se dezvoltă la aproximativ 24-53%(3,5).
Encefalopatia hepatică ia frecvent aspect acut, este adesea secundară unei hemoragii digestive, tratamentului cu diuretice (alcaloză hipocloremică), sedative sau unei infecţii, unui regim hiperproteic ori hipoxiei prin hipovolemie.
EH se diferenţiază de encefalopatia hepatică din insuficienţa hepatică fulminantă, în care pacientul nu are o boală hepatică în antecedente, şi de encefalopatia hepatică pseudoportală (prin sedative, alcaloză, hipoglicemie) cu amoniac seric normal.
Patogeneza encefalopatiei hepatice
O serie de teorii au fost propuse pentru a explica evoluţia EH la pacienţii cu ciroză. Unii cercetători susţin faptul că encefalopatia hepatică este o tulburare a funcţiei astrocitelor.
Astrocitele sunt celule ale sistemului nervos central de mari dimensiuni, de formă stelată, care controlează mediul chimic din jurul neuronilor, fiind implicate şi în răspunsurile imune ale ţesutului nervos. Acestea furnizează celulelor nervoase energia de care au nevoie pentru a putea funcţiona prin redirecţionarea sângelui cu aport în oxigen şi glucoză. Sunt cele mai mari dintre nevroglii, au numeroase prelungiri şi nucleu sferoidal situat central.
Astrocitele sunt unite prin joncţiuni de tip gap, formând astfel un sinciţiu funcţional. O creştere a concentraţiei de calciu intracelular se poate propaga în acest sinciţiu. Ca răspândire, astrocitele reprezintă aproximativ o treime din volumul cortical. Ele joacă un rol-cheie în controlul barierei hematoencefalice, sunt implicate în menţinerea homeostaziei electrolitice şi în furnizarea de nutrienţi şi precursori ai neurotransmiţătorilor la neuroni. De asemenea, ele joacă un rol în detoxifierea unor substanţe chimice, inclusiv a amoniacului(6).
Se presupune că substanţele neurotoxice, inclusiv amoniacul şi manganul, pot penetra sistemul nervos central (SNC) în insuficienţa hepatică. Aceste substanţe neurotoxice pot contribui la modificări morfologice ale astrocitelor. În ciroză, astrocitele pot suferi modificări conformaţionale prin balonizare, dezvoltă un nucleu palid mare şi marginalizarea cromatinei.
Modificările astrocitelor în insuficienţa hepatică acută sunt similare celor din maladia Alzheimer, dar balonizarea este mult mai importantă, consecinţa macroscopică fiind edemul cerebral, presiunea intracraniană crescută şi posibila herniere cerebrală.
La sfârsitul anilor 1990, cercetători de la Universitatea din Nebraska au raportat hipertensiune intracraniană la 12 pacienţi cu ciroză avansată şi comă hepatică de gradul 4 pe o perioadă de 6 ani(7). Edemul cerebral a fost evidenţiat prin tomografie computerizată (CT) la 9 din 12 pacienţi. Pacienţii au răspuns într-o primă fază la terapii specifice şi nespecifice (poziţionare la 45 de grade, hiperventilare, manitol intravenos, comă indusă de fenobarbital), dar aceste măsuri nu au avut efect pe termen lung, în condiţiile în care insuficienţa hepatică cronică nu era rezolvată.
Există şi o componentă genetică în encefalopatia hepatică. Sunt modificate gene care codifică o gamă largă de proteine de transport, a căror expresie poate creşte sau poate scădea. De exemplu, gena care codifică receptorul benzodiazepinic de tip periferic este crescută atât în ciroză, cât şi în insuficienţa hepatică acută, iar astfel de modificări genetice pot duce, în cele din urmă, la afectarea neurotransmisiei(8).
Encefalopatia hepatică poate fi, de asemenea, considerată o tulburare din cauza substanţelor neurotoxice acumulate în creier. Neurotoxinele incriminate includ acizi graşi cu catenă scurtă, mercaptani, falşi neurotransmiţători (tiramină, octopamină, beta-feniletanolamine), mangan, amoniac şi acid gama-aminobutiric (GABA).
Ipoteza amoniacului
Amoniacul este produs în tractul gastrointestinal prin degradarea bacteriană a aminelor, aminoacizilor, purinelor şi ureei. Enterocitele transformă, de asemenea, glutamina în glutamat şi amoniac prin activitatea glutaminazei. În mod normal, amoniacul este detoxifiat în ficat prin conversia în uree în cadrul ciclului Krebs-Henseleit(9).
Doi factori contribuie la hiperamonemia din ciroza hepatică:
a.scăderea masei hepatocitelor funcţionale duce la reducerea posibilităţilor de detoxifiere a amoniacului prin procesele de mai sus;
b.circulaţia portosistemică poate îndepărta sângele care conţine amoniac de ficat, trimiţându-l în circulaţia sistemică.
Muşchii scheletici nu posedă aparatele enzimatice ale ciclului ureei, dar conţin glutamină sintetază. Activitatea glutamin-sintetazei în muşchi creşte de fapt în ciroză cu şunturi portosistemice. Astfel, muşchiul scheletic este un loc important pentru metabolizarea amoniacului în ciroză. Cu toate acestea, pierderea musculară care se observă la pacienţii cu ciroză avansată poate potenţa hiperamonemia.
Amoniacul are efecte neurotoxice multiple. Acesta poate modifica transportul şi metabolizarea aminoacizilor, apei şi electroliţilor în astrocite şi neuroni şi utilizarea energiei în creier. Amoniacul poate inhiba generarea excitaţiei şi a potenţialelor postsinaptice inhibitoare. Inflamaţia (sistemică, neuroinflamaţia, endotoxinemia) asociată cu amoniacul pare să joace un rol important în encefalopatia hepatică la pacienţii cu ciroză, aspect susţinut de faptul că diferite terapii antiinflamatorii reprezintă o abordare terapeutică potenţială(10). Observaţia clinică susţine faptul că tratamentele care reduc nivelurile de amoniac din sânge pot îmbunătăţi simptomele encefalopatiei hepatice.
Există şi argumente contra rolului amoniacului seric în encefalopatia hepatică. Unul din acestea este observaţia că aproximativ 10% dintre pacienţii cu encefalopatie clinic manifestă au niveluri normale de amoniac seric. Mulţi pacienţi cu ciroză prezintă niveluri ridicate ale amoniemiei, fără a se evidenţia encefalopatia. De asemenea, amoniacul nu induce modificările clasice electroencefalografice (EEG) asociate cu encefalopatia hepatică atunci când este administrat la pacienţii cu ciroză.
Ipoteza GABA
GABA (acidul gama-aminobutiric) este o substanţă neuroinhibitoare produsă în tractul gastrointestinal. Este considerat a fi unul dintre cei mai importanţi mediatori inhibitori centrali. Cele mai mari concentraţii de GABA au fost găsite în globus pallidus, hipotalamus, substanţa neagră, nucleii cerebeloşi, substanţa cenuşie periapeductală, nucleul caudat şi talamusul medial. Dintre toate sinapsele nervoase din creier, se presupune că 24-45% sunt GABA-ergice. De peste 20 de ani s-a afirmat că encefalopatia hepatică a fost rezultatul creşterii tonusului GABA-ergic în creier. Cu toate acestea, studii experimentale mai noi schimbă percepţiile privind activitatea complexului receptor GABA în ciroză(8,11).
Complexul receptor GABA conţine situsuri de legare pentru GABA, benzodiazepine şi barbiturice. Se credea că nivelurile crescute de GABA şi benzodiazepine endogene din plasmă trec prin bariera hematoencefalică extrapermeabilă, iar ulterior legarea GABA şi a benzodiazepinelor la un complex receptor GABA neuronal suprasensibil permite influxul de ioni de clor în neuronii postsinaptici, conducând la generarea unui potenţial postsinaptic inhibitor.
Noi cercetări au demonstrat că nu există schimbări în nivelul GABA sau al benzodiazepinelor la nivelul SNC şi nici în sensibilitatea receptorilor complexului receptor GABA(11).
Administrarea flumazenilului, un antagonist al receptorului benzodiazepinic, ar putea îmbunătăţi funcţia mentală la pacienţii cu encefalopatie hepatică, dar studii recente arată că flumazenilul îmbunătăţeşte funcţia mentală doar la un procent mic de pacienţi cu ciroză.
Complexul receptorului neuronal GABA conţine şi un situs de legare pentru neurosteroizi, iar unii cercetători susţin că neurosteroizii joacă un rol-cheie în encefalopatia hepatică(12).
În modelele experimentale, neurotoxinele, cum ar fi amoniacul şi manganul, cresc producţia receptorului benzodiazepinic de tip periferic (peripheral-type benzodiazepine receptor – PTBR) în astrocite. PTBR, la rândul său, stimulează transformarea colesterolului în pregnenolon la neurosteroizi. Neurosteroizii sunt apoi eliberaţi din astrocite. Ei sunt capabili să se lege la receptorul lor în complexul receptorului GABA neuronal şi pot creşte neurotransmisia inhibitoare(13).
Un studiu a comparat nivelurile diferitelor substanţe chimice din ţesuturile cerebrale la autopsiile pacienţilor cu ciroză care au decedat fie în comă hepatică, fie fără evidenţierea encefalopatiei hepatice. Niveluri ridicate de alopregnanolon, metabolitul neuroactiv al pregnenolonei, au fost găsite în ţesutul cerebral al pacienţilor cu comă hepatică. Nivelurile cerebrale de liganzi ai receptorilor benzodiazepinici nu au fost semnificativ crescute la pacienţii cu sau fără comă. Această constatare susţine rolul neurosteroizilor în encefalopatia hepatică(14).
Reversibilitatea encefalopatiei hepatice
Clasic, encefalopatia hepatică este considerată o afecţiune reversibilă. Starea clinică a pacienţilor pare să se îmbunătăţească fie cu terapie medicamentoasă (de exemplu, lactuloză sau rifaximină), fie în urma transplantului hepatic. Cu toate acestea, un studiu recent a evaluat pacienţii cu ciroză care s-au recuperat aparent dintr-un episod de encefalopatie hepatică manifestă. După testarea psihometrică corespunzătoare, s-a descoperit că aceşti pacienţi cu ameliorare clinică au prezentat o insuficienţă cognitivă reziduală în comparaţie cu pacienţii cirotici cu encefalopatie hepatică minimă sau fără encefalopatie(15).
În 2009, Sotil şi colaboratorii au evaluat 39 de pacienţi care au avut transplant hepatic cu aproximativ 1,5 ani înainte de studiu. Cei 25 de pacienţi care au prezentat encefalopatie hepatică înainte de transplant au avut rezultate mai slabe la testele psihometrice decât cei 14 pacienţi fără antecedente de encefalopatie manifestă înainte de transplant(16).
În 2011, Garcia-Martinez şi colaboratorii au evaluat funcţia cognitivă la 52 de pacienţi care au suferit transplant hepatic. Funcţia cognitivă globală după transplant a fost mai gravă la pacienţii cu antecedente de ciroză indusă de alcool, pacienţi cu diabet zaharat şi pacienţi cu antecedente de encefalopatie hepatică înainte de transplant. În plus, volumul creierului (evaluat prin imagistică prin rezonanţă magnetică – IRM) după transplant a fost mai mic la pacienţii cu antecedente de encefalopatie hepatică înainte de transplant decât la pacienţii fără encefalopatie manifestă(17).
Evaluarea clinică a encefalopatiei hepatice
Diagnosticul pozitiv se bazează pe asocierea simptomatologiei neuropsihice la un pacient cu ciroză hepatică. Neexistând nicio metodă specifică de diagnostic pentru EH, este obligatorie excluderea altor cauze de encefalopatie la un pacient cirotic, ceea ce presupune un diagnostic diferenţial atent. Diagnosticul de encefalopatie hepatică este în esenţă un diagnostic de excludere.
În EH, tabloul clinic este polimorf şi este determinat de severitatea bolii hepatice şi de expresivitatea hipertensiunii portale(1,3). Semnele insuficienţei hepatice sunt informative, dar nespecifice, astfel încât absenţa lor nu exclude diagnosticul de EH. Foetor hepaticus – respiraţia cu miros caracteristic, dulceag (asemănat cu mirosul de ficat crud), considerat a fi cauzat de mercaptanii din aerul expirat, este frecvent întâlnită, are specificitate mare pentru insuficienţa hepatică şi de obicei se corelează cu severitatea encefalopatiei. Semnele cutanate de insuficienţă hepatocelulară (icter, steluţe vasculare, eritroză palmară, buze carminate, unghii albe), sindromul hemoragipar (epistaxis, gingivoragii, echimoze cutanate) şi sindromul ascitoedematos sunt, de asemenea, prezente în EH.
Prezenţa semnelor de hipertensiune portală este constantă – circulaţie colaterală abdominală, varice esofagiene, ascită(1,3). Manifestările neurologice şi psihiatrice(2) au o mare variabilitate şi nu sunt specifice encefalopatiei hepatice.
Tabloul clinic se poate instala brusc sau insidios, cele mai precoce simptome fiind reprezentate de modificările de comportament şi de reducerea uşoară a funcţiilor intelectuale. Accentuarea encefalopatiei conduce la modificări ale conştienţei, ale funcţiilor motorii, modificarea semnificativă a funcţiilor intelectuale şi instalarea progresivă a comei hepatice. Există şi modificări ale personalităţii, pacienţii sunt iritabili, fără interes pentru anturaj, simptomatologie asemănătoare sindromului de lob frontal. Uneori prezintă comportament bizar, stări euforice alternând cu stări depresive, limbaj vulgar şi neglijarea igienei personale. În stadiile iniţiale ale EH apar şi modificări ale conştienţei, cu inversarea ritmului somnului, cu insomnie nocturnă şi somnolenţă diurnă, care se accentuează progresiv în stadiile avansate până la comă. Dintre modificările intelectului, atenţia este deficitară, cu imposibilitate de a se concentra, ulterior apare apraxia (de exemplu, sunt incapabili să reproducă un desen simplu); progresiv apar dificultăţi în efectuarea calculelor simple, tulburări de memorie, se modifică scrisul (urmărirea zilnică a scrisului permite aprecierea evoluţiei bolii).
Cel mai precoce semn neurologic este flapping tremorul (asterixis). Acesta apare în stadiile iniţiale ale encefalopatiei şi este absent când se instalează coma. Deşi constant întâlnit, nu este totuşi specific cirozei hepatice. Prezenţa semnelor neurologice de focar nu este caracteristică EH.
Odată cu agravarea encefalopatiei, tabloul neurologic devine complex, cu modificări de tonus muscular, modificări ale reflexelor osteotendinoase, devierea conjugată a ochilor, cecitate corticală tranzitorie, manifestări extrapiramidale.
În prezent, cea mai utilizată scală de gradare a EH o reprezintă criteriile West Haven, bazate exclusiv pe criterii clinice, în speţă pe evaluarea stării mentale; există astfel 5 grade de encefalopatie hepatică, prezentate în tabelul 1.
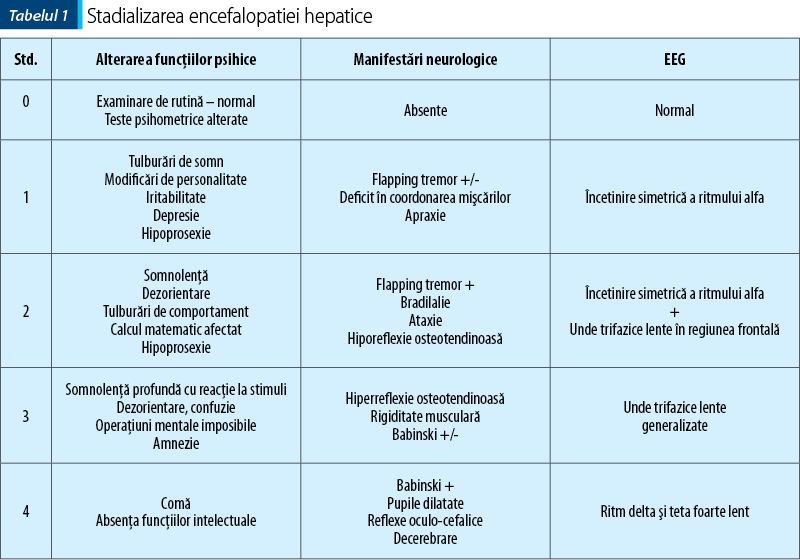
Managementul encefalopatiei hepatice
Abordarea encefalopatiei hepatice se realizează în funcţie de severitatea manifestărilor clinice şi de certitudinea diagnosticului bolii de bază. De exemplu, la un pacient cu ciroză cunoscută care asociază şi uşoară scădere a capacităţii de concentrare şi a performanţelor şcolare, testarea psihometrică poate evidenţia encefalopatie minimă, iar iniţierea lactulozei şi rifaximinei, cu evaluare atentă, periodică, reprezintă opţiunea terapeutică de urmat. Un pacient care se prezintă în unitatea de primiri urgenţe cu encefalopatie hepatică severă sau comă necesită o abordare diferită. Recomandările generale de management al EH includ:
-
excluderea altor cauze non-hepatice ale funcţiei mentale alterate;
-
evaluarea amoniemiei este obligatorie la orice pacient cunoscut cu ciroză hepatică;
-
evitarea comorbidităţilor precipitante ale EH: hipovolemia, alte dezechilibre metabolice, sângerări gastrointestinale, infecţii, constipaţie; acestea trebuie manageriate specific;
-
evitarea medicamentelor care deprimă funcţia sistemului nervos central, în special benzodiazepinele. Pacienţii cu agitaţie severă şi encefalopatie hepatică pot primi haloperidol ca sedativ;
-
pacienţii cu encefalopatie severă (grad 3 sau 4) care prezintă risc de aspiraţie trebuie intubaţi profilactic în unitatea de terapie intensivă.
Cele mai multe terapii actuale sunt concepute pentru a trata hiperamonemia, care este un semn distinctiv al majorităţii cazurilor de encefalopatie hepatică.
Modificări dietetice
În secolul XX, dietele cu conţinut scăzut de proteine au fost în mod obişnuit recomandate pacienţilor cu ciroză, în speranţa scăderii producţiei intestinale de amoniac şi pentru prevenirea exacerbărilor encefalopatiei hepatice. O consecinţă evidentă a fost agravarea malnutriţiei preexistente a proteinelor şi a energiei, iar restricţia proteică este rareori justificată la pacienţii cu ciroză şi encefalopatie hepatică persistentă.
Dietele care conţin proteine vegetale par a fi mai bine tolerate decât dietele bogate în proteine animale, în special proteine derivate din carnea roşie. Acest lucru se realizează prin conţinutul crescut de fibre şi niveluri scăzute de aminoacizi aromatici, care ar inhiba neurotransmisia dopaminergică şi agravează encefalopatia hepatică (fiind precursori ai neurotransmiţătorilor falşi tiramină şi octopamină).
Aminoacizii cu catenă ramificată (BCAA) au efect benefic asupra encefalopatiei hepatice, dar nu şi asupra mortalităţii, calităţii vieţii sau a parametrilor nutriţionali(18).
Laxativele
Lactuloza (beta-galactozidofructoza) şi lactitolul (beta-galactozidosorbitolul) sunt dizaharide neabsorbabile, fiind utilizate de la începutul anilor 1970. Sunt degradate de bacteriile intestinale la acid lactic şi alţi acizi organici. Lactuloza pare să inhibe producţia de amoniac intestinal prin transformare în acid lactic şi acid acetic, cu rezultat în acidifierea lumenului intestinal. În acest mediu are loc conversia amoniacului (NH3) în amoniu (NH4+); din cauza impermeabilităţii relative a membranei, ionii NH4+ nu sunt absorbiţi. Acidifierea mediului intestinal inhibă bacteriile coliforme amoniacogene, ceea ce duce la creşterea nivelului lactobacililor nonamonogeni. Lactuloza funcţionează şi ca laxativ, reducând încărcătura bacteriană colonică(19,20).
Doza de lactuloză poate fi modificată, testându-se toleranţa pacientului şi tranzitul intestinal (maximum 2-4 scaune în 24 de ore). La adolescenţi se poate începe cu 30 ml oral, zilnic sau de două ori pe zi. Reducerea dozelor se realizează în caz de diaree, crampe abdominale sau balonare. Trebuie acordată însă o mare atenţie atunci când se prescrie lactuloza, deoarece supradozajul poate duce la ileus, diaree severă, tulburări electrolitice şi hipovolemie. Hipovolemia poate fi suficient de gravă pentru a induce simptomele de encefalopatie hepatică.
La pacienţii cu encefalopatie hepatică minimă, lactuloza a fost mai eficace decât placebo în ceea ce priveşte îmbunătăţirea performanţei pacientului în cadrul testelor psihometrice(21,22). Lactuloza a fost studiată şi în studii mari randomizate ca prevenţie secundară pentru encefalopatia hepatică recurentă la pacienţii cu ciroză(23,24).
Lactuloza este utilizată şi ca profilaxie primară, deşi studii extensive pentru această idee sunt încă necesare. O metaanaliză din 2013 a confirmat utilitatea lactulozei în tratamentul encefalopatiei hepatice(25).
Antibioticele
Neomicina şi alte antibiotice, cum ar fi metronidazolul, vancomicina, chinolonele orale, sunt administrate pentru efectul de scădere a concentraţiei de bacterii amoniacogene în colon. Doza iniţială de neomicină la adolescenţi şi adulţi este de 250 mg pe cale orală de 2-4 ori pe zi. Neomicina este de obicei utilizată ulterior iniţierii tratamentului cu lactuloză. Tratamentul pe termen lung cu neomicină prezintă risc de ototoxicitate şi nefrotoxicitate.
Rifaximina, un derivat neabsorbabil al rifampicinei, a fost utilizat în Europa de peste 20 de ani pentru multe afecţiuni gastrointestinale. Studii clinice au demonstrat că rifaximina în doză de 400 mg administrată oral de 3 ori pe zi a fost la fel de eficace ca lactuloza sau lactitolul la ameliorarea simptomelor encefalopatiei hepatice(26,27). Rifaximina a avut un profil de tolerabilitate comparabil cu placebo.
Encefalopatia hepatică minimă
Encefalopatia hepatică minimă descrie o disfuncţie cognitivă uşoară prezentă la mai mult de 70% dintre pacienţii cu ciroză(28). Poate fi sugerată de atenţie scăzută, tulburări în luarea deciziilor, viteză scăzută de reacţie şi de modificări ale funcţiei vizuale. Este detectată doar prin teste psihometrice (testul de conectare numerică, testul simbolului cifrelor, timpul de reacţie la lumină sau sunet etc.). Encefalopatia hepatică minimă este cel mai probabil rezultatul hiperamonemiei, iar modificările neurologice pot fi ameliorate prin administrarea de lactuloză(29).
Studiu clinic
Am realizat un studiu clinic în vederea aprecierii incidenţei EH la un lot de copii cu ciroză hepatică de diverse etiologii, la o parte din aceştia fiind realizată şi splenectomie cu sau fără şunt chirurgical.
Studiul retrospectiv a fost realizat pe un lot de 47 de copii diagnosticaţi cu ciroză hepatică în Clinica II Pediatrie Iaşi pe o perioadă de 7 ani (2010-2016). Etiologia cirozei hepatice a fost stabilită prin anamneză şi consultarea foilor de observaţie. Criteriile West Haven au fost utilizate pentru a aprecia stadiul clinic al EH. Encefalopatia hepatică minimă a fost evaluată utilizând o baterie de teste psihometrice de tip PHES, care a cuprins: Number Connection Tests (NCT) A and B, Digit Symbol Test (DST), Serial Dotting Test, Line Drawing Test (figura 1). Scorul Z pentru aprecierea EH a fost determinat folosind un calculator online disponibil gratuit la http://www.redeh.org/TEST_phes.htm.
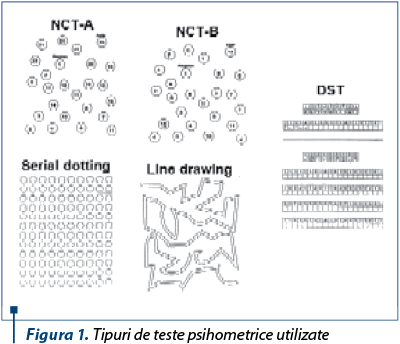
Encefalopatia hepatică minimă a fost diagnosticată pentru un scor Z≤-5.
Analiza statistică a fost realizată cu Statistical Package for Social Sciences (SPSS, version 13.0, SPSS Inc., Chicago, USA).
Rezultate
Din cei 47 de copii, testarea psihometrică a fost efectuată la 34 dintre aceştia, la care bateria de teste psihometrice a putut fi aplicată.
Vârsta medie a pacienţilor a fost 12,3±4,05 ani (0-18 ani), majoritatea diagnosticaţi cu ciroză hepatică la vârste de peste 10 ani, după evoluţia prelungită a unei hepatopatii cronice. Raportul pe sexe în lotul de studiu a fost F/M=1/1,32.
Pacienţii cu ciroză hepatică diagnosticată la vârstă mică (3 cazuri), de cauză malformativă sau infecţioasă, au fost încadraţi, conform criteriilor clinice modificate pentru această vârstă, în stadiul I de EH.
Alţi 5 copii cu vârste mai mari au fost încadraţi, de asemenea, în stadiul I de EH după criteriile West Haven.
Encefalopatia hepatică minimă a fost evaluată la copii începând de la vârsta şcolară prin bateria de teste PHES. Fiecare pacient a completat toate cinci categoriile de teste psihometrice, după instrucţiuni clare şi monitorizare atentă. Niciun pacient din cei care au realizat testarea psihometrică nu prezenta semne clinice specifice pentru a fi încadrat într-un grad superior de EH.
Rezultatele testelor au fost introduse în calculatorul online, împreună cu vârsta pacienţilor şi gradul de şcolarizare pentru fiecare.
Rezultatul în ansamblu al testării psihometrice a fost exprimat prin calculul scorului Z pentru bateria de teste PHES.
Valorile între -4 şi +15 au fost considerate normale, sugerând absenţa EH minime. Scorul Z≤-5 a confirmat diagnosticul de EH minimă.
Rezultatele din figura 2 arată faptul că la o treime din cazuri s-a constatat absenţa EH, iar în aproape jumătate din cazuri s-a constatat prezenţa EH minime, care a putut fi decelată doar prin testare psihometrică, de unde se observă importanţa procedurii.
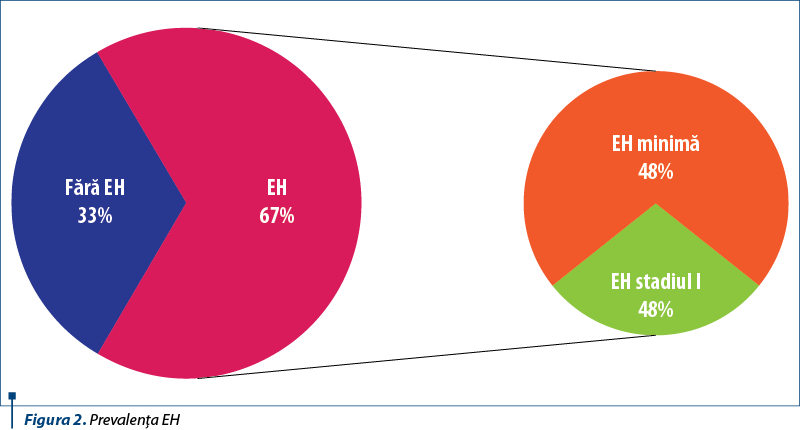
Splenectomia s-a impus ca necesitate terapeutică chirurgicală la 18 pacienţi, la 11 din aceştia fiind însoţită de şunt portosistemic. Evoluţia postoperatorie a acestor pacienţi a fost favorabilă pe perioada urmărită, fiind necesare monitorizări ulterioare pe termen lung.

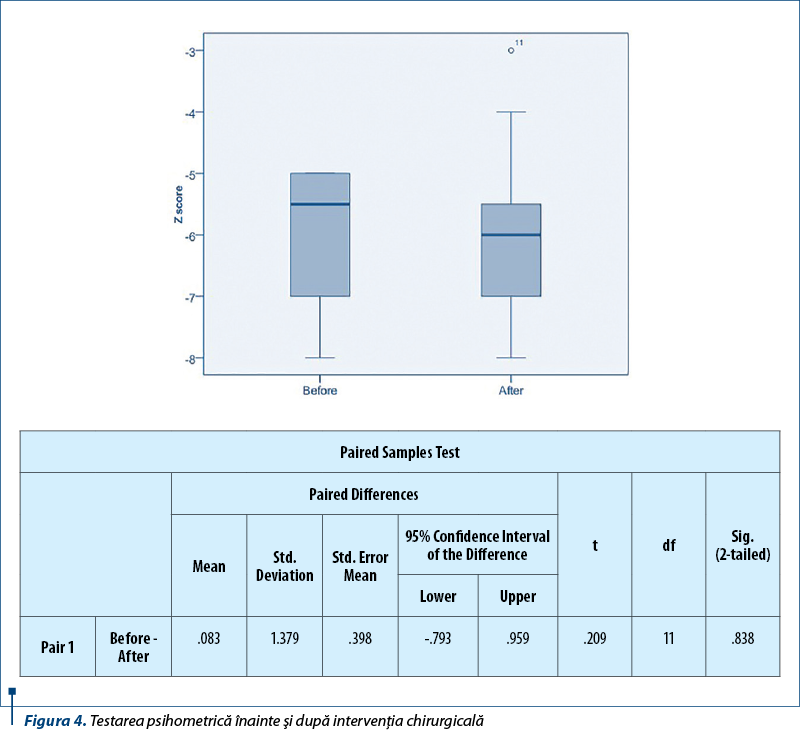
Testarea psihometrică a fost realizată la 12 pacienţi înainte şi după intervenţia chirurgicală, urmărindu-se impactul asupra EH. Testul statistic aplicat a fost nesemnificativ, deci, conform cu datele din literatură, nu au existat diferenţe semnificative în variaţia scorului Z la aceşti copii.
Drept concluzie a studiului, splenectomia, cu sau fără şunt, are o eficienţă relativă la pacienţii cu hipertensiune portală, ameliorând doar parametrii hematologici.
Prin urmare, encefalopatia hepatică trebuie evaluată prin teste psihometrice la orice pacient cu ciroză hepatică, iar încadrarea acesteia reprezintă un element de monitorizare şi evoluţie a bolii. Metoda de evaluare nu este complicată, necesitând doar rigurozitate şi atenţie din partea clinicianului. Detectarea encefalopatiei hepatice încă din stadiile incipiente permite o mai bună urmărire a bolii, deşi tehnicile chirurgicale de şunt portosistemic sau transplantul hepatic nu ameliorează encefalopatia hepatică.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Sherlock S, Dooley J. Hepatic Encephalopathy. In: Sherlock S, Dooley J. Disease of the Liver and Billiary System, ed 11. Blackwell Science Publishing, 2002; 93-111.
- Ferenci P, Lockwood A, Mullen K et al. Hepatic encephalopathy – Definition, nomenclature, diagnosis, and quantification: Final report of the Working Party at the 11th World Congress of Gastroenterology, Vienna, 1998. Hepatology. 2002; 35:716-721.
- Mas, A. Hepatic Encephalopathy: From Pathophysiology to Treatment. Digestion. 2006; 73 (Suppl.1): 86-93.
- Cervera JL. Hepatic encephalopathy: A review. Ann Hepatol. 2003; 2(3): 122-130.
- Fitz JG. Hepatic encephalopathy, hepatopulmonary syndromes, hepatorenal syndrome, coagulopathy and endocrine complications of liver disease. In: Feldman M, Friedman LS and Sleisenger MH (eds.). Sleisenger and Fordtran’s Gastrointestinal and Liver Disease, Ed 7. Philadelphia: WB Saunders, 2002,1543-1565.
- Brusilow SW. Hyperammonemic encephalopathy. Medicine (Baltimore). 2002 May; 81(3):240-9.
- Donovan JP, Schafer DF, Shaw BW Jr, et al. Cerebral oedema and increased intracranial pressure in chronic liver disease. Lancet. 1998 Mar 7; 351(9104): 719-21.
- Butterworth RF. Pathogenesis of hepatic encephalopathy: new insights from neuroimaging and molecular studies. J Hepatol. 2003 Aug; 39(2):278-85.
- Chatauret N, Butterworth RF. Effects of liver failure on inter-organ trafficking of ammonia: implications for the treatment of hepatic encephalopathy.
- J Gastroenterol Hepatol. 2004; 19:S219-223.
- Luo M, Guo JY, Cao WK. Inflammation: A novel target of current therapies for hepatic encephalopathy in liver cirrhosis. World J Gastroenterol. 2015 Nov 7; 21(41):11815-24.
- Ahboucha S, Butterworth RF. Pathophysiology of hepatic encephalopathy: a new look at GABA from the molecular standpoint. Metab Brain Dis. 2004 Dec; 19(3-4):331-43.
- Butterworth RF. Neurosteroids in hepatic encephalopathy: Novel insights and new therapeutic opportunities. J Steroid Biochem Mol Biol. 2016 Jun; 160:94-7.
- Butterworth RF. The astrocytic (“peripheral-type“) benzodiazepine receptor: role in the pathogenesis of portal-systemic encephalopathy. Neurochem Int. 2000 Apr; 36(4-5):411-6.
- Ahboucha S, Pomier-Layrargues G, Mamer O, et al. Increased levels of pregnenolone and its neuroactive metabolite allopregnanolone in autopsied brain tissue from cirrhotic patients who died in hepatic coma. Neurochem Int. 2006 Sep; 49(4):372-8.
- Bajaj JS, Schubert CM, Heuman DM, et al. Persistence of cognitive impairment after resolution of overt hepatic encephalopathy. Gastroenterology. 2010 Jun; 138(7):2332-40.
- Sotil EU, Gottstein J, Ayala E, Randolph C, Blei AT. Impact of preoperative overt hepatic encephalopathy on neurocognitive function after liver transplantation. Liver Transpl. 2009 Feb; 15(2):184-92.
- Garcia-Martinez R, Rovira A, Alonso J, et al. Hepatic encephalopathy is associated with posttransplant cognitive function and brain volume. Liver Transpl. 2011 Jan. 17(1):38-46.
- Gluud LL, Dam G, Les I, et al. Branched-chain amino acids for people with hepatic encephalopathy. Cochrane Database Syst Rev. 2015 Sep 17; 9:CD001939.
- Sharma P, Agrawal A, Sharma BC, Sarin SK. Prophylaxis of hepatic encephalopathy in acute variceal bleed: a randomized controlled trial of lactulose versus no lactulose. J Gastroenterol Hepatol. 2011 Jun; 26(6):996-1003.
- Frederick RT. Current concepts in the pathophysiology and management of hepatic encephalopathy. Gastroenterol Hepatol (N Y). 2011 Apr; 7(4):222-33.
- Prasad S, Dhiman RK, Duseja A, Chawla YK, Sharma A, Agarwal R. Lactulose improves cognitive functions and health-related quality of life in patients with cirrhosis who have minimal hepatic encephalopathy. Hepatology. 2007 Mar; 45(3):549-59.
- Mittal VV, Sharma BC, Sharma P, Sarin SK. A randomized controlled trial comparing lactulose, probiotics, and L-ornithine L-aspartate in treatment of minimal hepatic encephalopathy. Eur J Gastroenterol Hepatol. 2011 Aug; 23(8):725-32.
- Sharma BC, Sharma P, Agrawal A, Sarin SK. Secondary prophylaxis of hepatic encephalopathy: an open-label randomized controlled trial of lactulose versus placebo. Gastroenterology. 2009 Sep; 137(3):885-91, 891.e1.
- Agrawal A, Sharma BC, Sharma P, Sarin SK. Secondary prophylaxis of hepatic encephalopathy in cirrhosis: an open-label, randomized controlled trial of lactulose, probiotics, and no therapy. Am J Gastroenterol. 2012 Jul; 107(7):1043-50.
- Gluud LL, Dam G, Borre M, et al. Lactulose, rifaximin or branched chain amino acids for hepatic encephalopathy: what is the evidence? Metab Brain Dis. 2013 Jun; 28(2):221-5.
- Mas A, Rodes J, Sunyer L, et al. Comparison of rifaximin and lactitol in the treatment of acute hepatic encephalopathy: results of a randomized, double-blind, double-dummy, controlled clinical trial. J Hepatol. 2003 Jan; 38(1):51-8.
- Miglio F, Valpiani D, Rossellini SR, et al. Rifaximin, a non-absorbable rifamycin, for the treatment of hepatic encephalopathy. A double-blind, randomised trial. Curr Med Res Opin. 1997; 13(10):593-601.
- Butterworth RF. Editorial: rifaximin and minimal hepatic encephalopathy. Am J Gastroenterol. 2011 Feb; 106(2):317-8.
- Weissenborn K, Ennen JC, Schomerus H, Ruckert N, Hecker H. Neuropsychological characterization of hepatic encephalopathy. J Hepatol. 2001 May; 34(5):768-73.
Articole din ediţiile anterioare
Portal cavernoma in children – complications and evolution
Tromboza de venă portă este o afecţiune rară, dar reprezintă o cauză importantă de hipertensiune portală în patologia pediatrică. Principalii facto...