Anesthesia and intense care for patients with intracranial pathology undergoing surgery or imaging diagnosis is a challenge for practitioners. There is a need for extensive knowledge of the physiology and physiopathology, based on concepts as changes of intracranial pressure (IP), blood flow control (BFC) and cerebrospinal fluid production (CFS), and effects on the body. The key to success are the choice of anesthesia protocol and intensive therapy tailored to the particularities of the case, the knowledge of risks and the management of possible complications.
Consideraţii privind anestezia şi terapia intensivă pentru pacienţii cu patologie intracraniană
Considerations on anesthesia and intensive care for patients with intracranial pathology
First published: 20 noiembrie 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/PV.29.8.2017.1255
Abstract
Rezumat
Anestezia și terapia intensivă pentru pacienții cu patologie intracraniană supuși intervențiilor chirurgicale sau celor de diagnostic imagistic reprezintă o provocare pentru practicieni. Este necesar un bagaj vast de cunoștințe din domeniul fiziologiei și fiziopatologiei, la baza căruia stau noțiunile legate de dinamica presiunii intracraniene (PI), controlul fluxului sangvin (FSC), producția fluidului cerebrospinal (FCS) și efectele asupra organismului. Cheia succesului este reprezentată de alegerea protocolului de anestezie și terapie intensivă adaptate particularităților cazului, cunoașterea riscurilor și gestionarea eventualelor complicații.
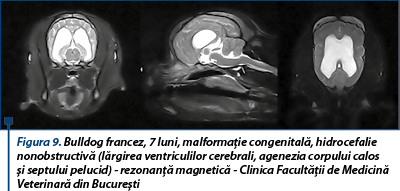
Pacienții cu patologie intracraniană (neoplazii, afecțiuni congenitale, patologie posttraumatică) supuși intervențiilor chirurgicale sau celor de diagnostic imagistic (electroencefalografie - EEG, mielografie, CT, RMN), necesită o atenție sporită și protocoale de anestezie - terapie intensivă specifice. Varietatea etiologiilor și manifestărilor clinice impune cunoașterea în detaliu a fiziologiei și fiziopatologiei cu implicare la acest nivel, pentru a putea gestiona corespunzător cazurile și a aprecia corect riscurile asociate anesteziei.
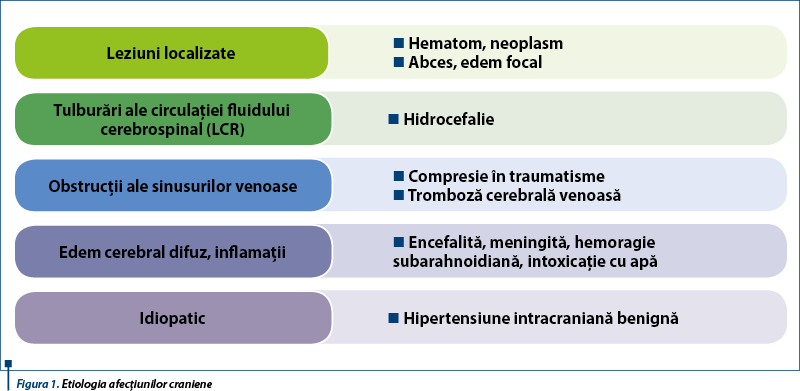
Fluxul sangvin către SNC este controlat printr-un sistem unic de autoreglare, care determină presiunea perfuziei cerebrale (PPC), respectiv gradientul de presiune necesar pentru a trimite fluxul sangvin către creier. Orice modificare a fluxului sangvin cerebral influențează presiunea intracraniană.
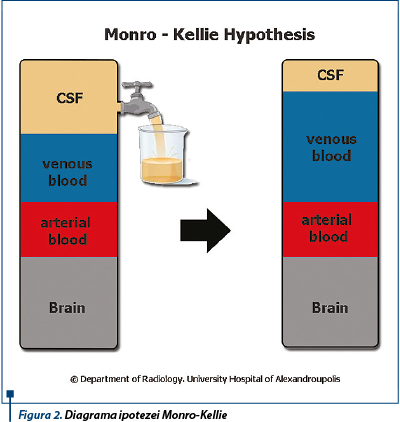
Presiunea intracraniană (PIC) este menținută de cele trei componente ale spațiului intracranian: țesut cerebral (80-85%), volum de sânge cerebral (5-8%), fluid cerebrospinal (7-10%). Craniul este o incintă închisă, nedilatabilă. Creșterea volumului oricărui component (edem, hidrocefalie, dezvoltarea proceselor patologice: hematom, tumoră) este urmată de scăderea volumului altui component sau se asociază cu creșterea presiunii intracraniene (ipoteza Monro-Kellie; figura 2). Fluidul cerebrospinal umple sistemul ventricular cerebral, spațiile subarahnoidiene cerebrale și medulare. Orice obstrucție a secreției/absorbției lui determină creșterea presiunii intracraniene.
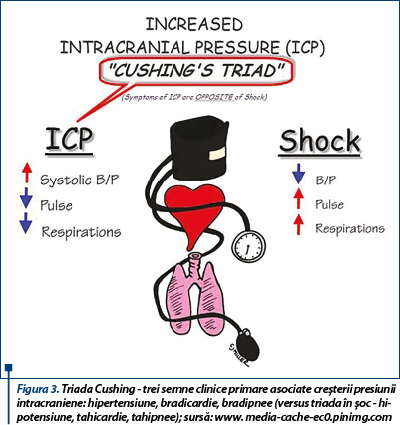
Creșterea presiunii intracraniene determină creșterea presiunii arteriale medii (MAP) pentru a menține perfuzia cerebrală. Astfel apare reflexul Cushing și scad pulsul și frecvența cardiacă, răspuns al creșterii rezistenței vasculare sistemice. Creșterea rapidă, necontrolată, a presiunii intracraniene determină hipertensiune arterială, bradicardie, tulburări respiratorii, în final herniere cerebrală, compresie, pierderea cunoștinței și exitus.
Managementul anestezic al pacienților cu presiune intracraniană crescută vizează scăderea volumului celor trei compartimente. Volumul sangvin și cel al fluidului cerebrospinal se adaptează cel mai ușor la modificarea presiunii intracraniene.
Neuroanestezia: examinarea preanestezică trebuie percepută ca primă etapă a protocolului anestezic, facilitând ierarhizarea problemelor pacientului și încadrarea sa într-o grupă de risc. Un examen preanestezic cât mai complet trebuie realizat minimizând factorii de stres, evitând metodele de contenţie brutale, manevrele inutile și zgomotele puternice. Evaluarea pacientului se va realiza din punctul de vedere al istoricului medical, al examenului clinic specific complet, astfel încât să se stabilească protocolul anestezic și grupa de risc în care se plasează acesta (clasificarea ASA a pacienților, adaptare pentru medicina veterinară).
În cazul pacienților convulsivi se pot produce creșterea necesarului de oxigen, acidoză lactică în țesutul cerebral, modificări ale fluxului sangvin cerebral, pierderea autoreglării fluxului sangvin cerebral și creșterea necesarului energetic cerebral. Sedarea se va corela cu eventualele tratamente antiepileptice.

După traumatismele craniene, creierul își poate intensifica activitatea metabolică (hipermetabolism cerebral), astfel încât pacienții hipoeuglicemici vor compensa greu hipermetabolismul cerebral și se poate produce criza metabolică (hipoglicemie). Măsurile de terapie intensivă vizează menținerea glicemiei la valori ușor crescute (100-180 mg/dl) pentru această categorie de pacienți, în vederea evitării crizei metabolice hipoglicemice.
Stabilizarea perianestezică în urgențe neurologice presupune protocoale complexe, dependente de severitatea cazului, de la resuscitare cardiopulmonară și cerebrală (suport vital de bază) și continuând cu suportul vital avansat (monitorizare, medicație specifică etc.). Pentru controlul crizelor pacienților cu patologie intracraniană se pot administra antiepileptice, barbiturice (reduc metabolismul cerebral și fluxul sangvin cerebral) și medicație cu efect sedativ (scade presiunea IC, scade necesarul metabolic cerebral). Deosebit de importante sunt monitorizarea și controlul tensiunii arteriale. Manoperele de stabilizare în urgență se pot completa cu puncție și aspirare lentă a fluidului cerebrospinal (ventriculostomă) sau craniectomie decompresivă.
Pregătirea pacientului pentru neurochirurgie presupune poziționarea cu extremitatea cefalică peste nivelul inimii, cu gâtul în poziție neutră, pentru maximizarea drenării venoase cerebrale. Ridicarea excesivă determină un risc crescut de embolie gazoasă venoasă (aer). Atenție la detalii: ocluzia venei jugulare (stază directă sau indirectă cu zgardă, catetere) poate determina rapid creșterea presiunii intracraniene. Se va evita încălzirea excesivă a pacientului, ideal acesta menținându-se ușor hipotermic (32-35°C) prin lipsa încălzirii/răcire.

Administrarea fluidelor se va face cu discernământ, ratele mari fiind asociate cu creșterea presiunii venoase centrale, flux sangvin scăzut și risc crescut pentru producerea edemului cerebral. Recomandările sunt de a administra cristaloide izotone la o rată maximă de 3 ml/kg/h, cu bolusuri de soluții hipertonice saline la nevoie (pentru scăderea presiunii intracraniene).
Diureticele sunt indicate pentru cazurile cu presiune intracraniană crescută sau edem cerebral, administrate în scheme terapeutice complexe (manitol 0,5-1 g/kg bolus i.v., lent în 20 minute sau 1-2 mg/kg/min, furosemid 1-8 mg/kg bolus i.v. sau CRI 0,1-1 mg/kg/min, la 15 minute după administrarea manitolului).
Particularitățile anesteziei pentru pacienții cu afecțiuni intracraniene vizează monitorizarea și controlul depresiei SNC, ratei de metabolizare cerebrală a oxigenului și necesarului de oxigen. În timpul anesteziei trebuie gestionate optim oxigenarea, nivelul EtCO2, nivelul presiunii arteriale și respectiv fluxul sangvin venos cerebral.
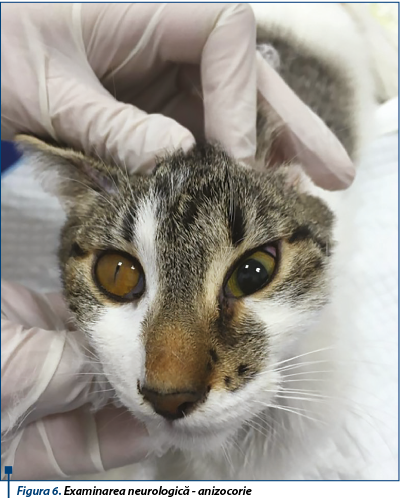
O atenție sporită este necesară în alegerea protocolului optim de anestezie și analgezie, corelat cu statusul ASA al pacientului și cu efectele medicației utilizate. În acest sens, pentru premedicație se pot utiliza barbiturice (reduc MAP și PIC, sunt utile în menținerea perfuziei cerebrale, a autoreglării, a răspunsului la variația CO2), opioide (reduc discret perfuzia și metabolismul cerebral, induc hipoventilație și indirect creșterea PIC), benzodiazepine (reduc ușor perfuzia cerebrală). Ketamina determină creșterea ratei de metabolizare cerebrală a oxigenului și secundar crește fluxul cerebral și PIC. Nu se administrează ca medicație unică, folosindu-se cu precauție doar în combinații care blochează acest efect (cu benzodiazepinice, izofluran, propofol). Lidocaina administrată în faza de menținere a anesteziei are efect de stabilizare membranară și consecutiv determină reducerea necesarului energetic pentru menținerea integrității membranare.

Inducția anesteziei se poate realiza cu propofol (reduce metabolismul cerebral, vasoconstricție, scade fluxul sangvin cerebral și PIC), etomidat (de evitat la epilepitici, pentru că activează focarele de criză, este util pentru examinarea EEG), combinații fentanyl cu propofol (se reduce PIC la intubare).
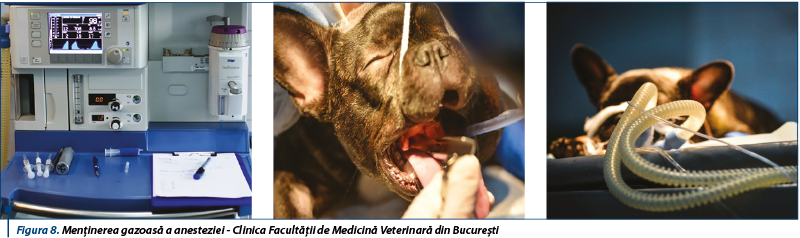
Menținerea anesteziei cu utilizarea anestezicelor gazoase (izofluran, sevofluran) reduce semnificativ rata metabolică cerebrală (necesarul de oxigen la nivel cerebral). Acestea favorizează vasodilatația cerebrală și augmentarea fluxului sangvin cerebral, cu reducerea presiunii sangvine. În condițiile asigurării ventilației eficiente, răspunsul la variațiile CO2 este menținut.
Există diferențe semnificative între efectul diferitelor anestezice volatile utilizate și valoarea MAC-ului la care sunt utilizate (MAC - minimum alveolar concentration). Semnificația clinică a efectelor izofluranului asupra ratei de metabolizare cerebrală și presiunii intracraniene se produce la o valoare a MAC de 1,5-2 (la MAC 1 apare supresia ratei metabolice cu 25%). Sevofluranul are un impact major asupra fluxului sangvin cerebral și PIC peste MAC 1 (reduce rata metabolică cerebrală cu 38% la MAC 1). Sevofluranul are un potențial redus de a determina crize epileptiforme și se va utiliza cu prudență la pacienții epileptici.
Utilizarea relaxantelor nondepolarizante (vecuronium/rocuronium/atracurium) acționează prin eliberare de histamine, vasodilatație cerebrală și creșterea PIC, scăderea TA și reducerea presiunii perfuziei intracerebrale. Atunci când sunt utilizate în protocoale de anestezie, se ajustează dozele și rata și se evită hipotensiunea!
Complicațiile anestezice pentru pacienții cu patologie intracraniană supuși anesteziei în vederea procedurilor de diagnostic imagistic (electroencefalografie, mielografie, CT, RMN) se pot produce imediat sau tardiv și se manifestă pornind de la reacții alergice (atenție la substanțele de contrast utilizate) până la convulsii, hipertermie, hiperestezie, vomă, meningită, bradicardie, asistolă etc.
Bibliografie
2. Costea R. Anesthesia considerations for critically ill patients. EJCAP volume 26 (3), 2016.
3. Costea, Ruxandra, et al. Contributions to the peri-operative supportive care and anesthesia for urogenital surgeries in small animals. Scientific Works. Series C. Veterinary Medicine, 2013, 59.3: 72-73.
4. Eriksson, Lars I. Miller's Anesthesia,. Vol. 1. Elsevier Health Sciences, 2009.
5. Mutch, W. A. C., et al. Neuroanesthesia Adjunct Therapy (Mannitol and Hyperventilation) Is as Effective as Cerebrospinal Fluid Drainage for Prevention of Paraplegia After Descending Thoracic Aortic Cross-Clamping in the Dog. Survey of Anesthesiology, 1996, 40.5: 329.
6. Shores, Andy. Neuroanesthesia: A review of the effects of anesthetic agents on cerebral blood flow and intracranial pressure in the dog. Veterinary Surgery, 1985, 14.3: 257-263.
Articole din ediţiile anterioare
Hipertensiunea pulmonară - diagnostic și tratament
Hipertensiunea pulmonară (HTP) este un sindrom clinic cu etiologie plurifactorială, caracterizat prin creșterea persistentă a presiunii arteriale p...
Hipertensiunea arterială la pisici
Hipertensiunea arterială este o boală comună la pisicile geriatrice, frecvent diagnosticată în asociere cu alte afecţiuni, cum ar fi boala renală c...
Studiul retinopatiilor şi coroidopatiilor la pisicile hipertensive
Hipertensiunea arterială sistemică este definită ca o creştere persistentă a tensiunii arteriale peste valorile de referinţă ale speciilor. Poate r...