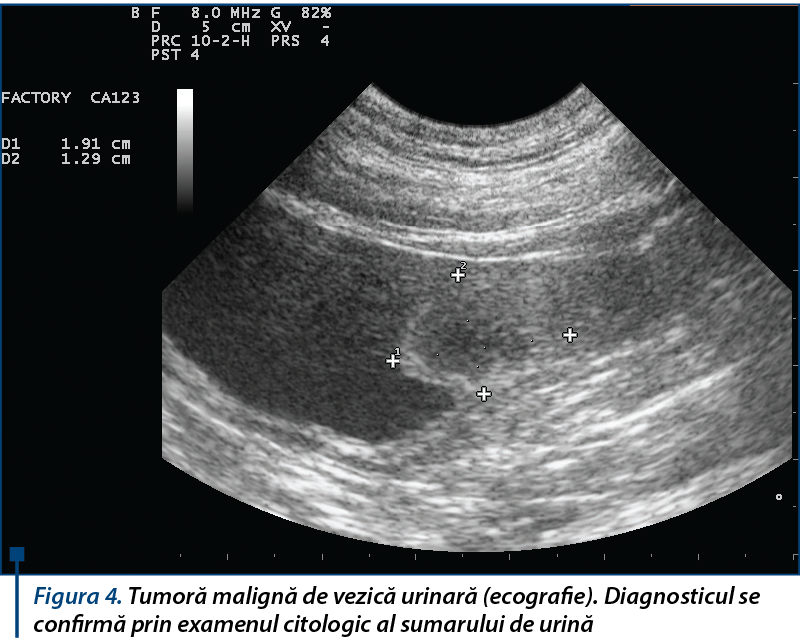
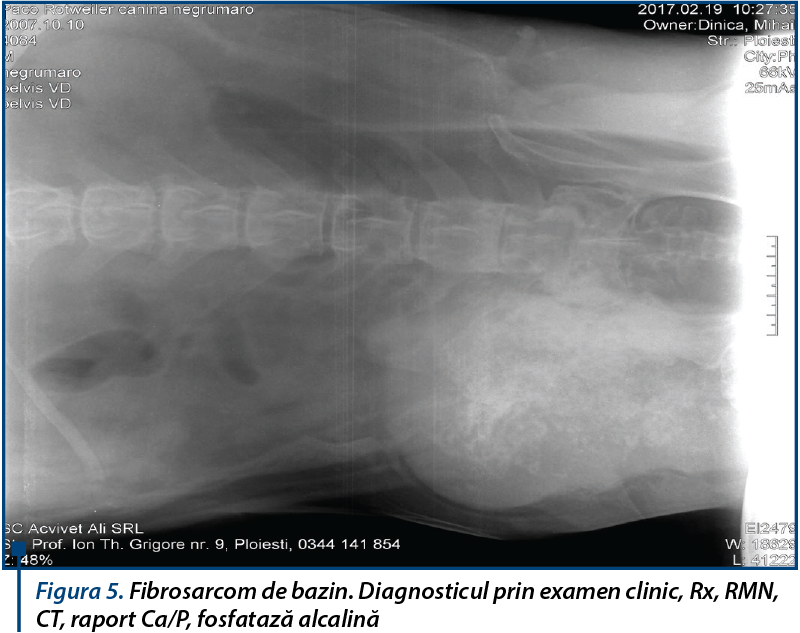
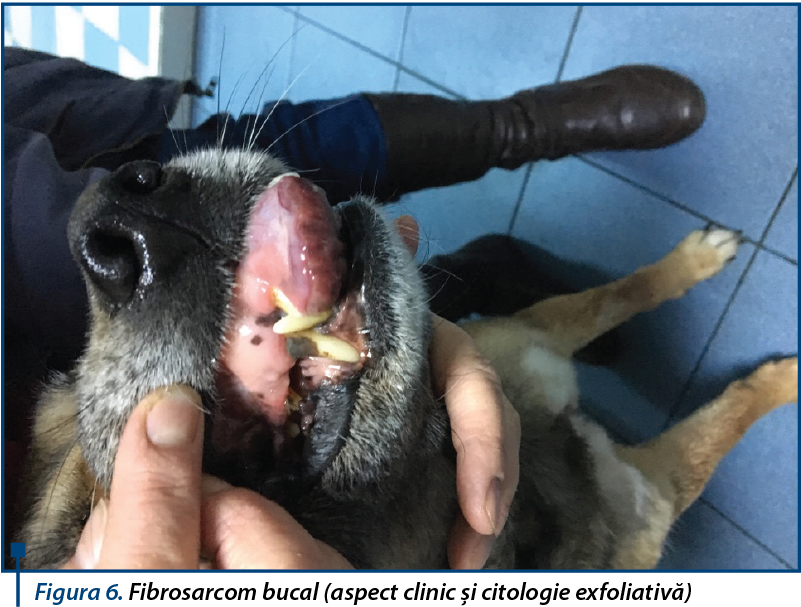
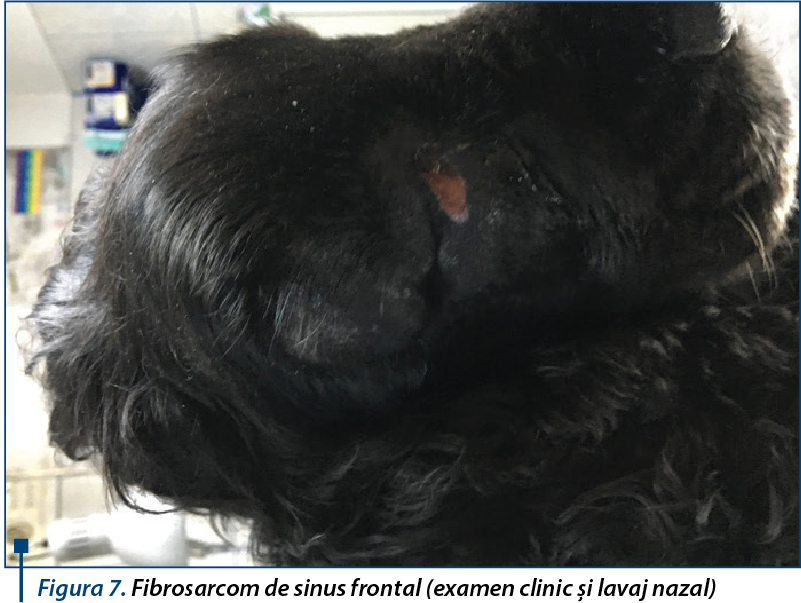
The oncological diagnosis represents a complex process, with several stages and a multi disciplinary approach through which we establish the existence of a neoplastic process, benign or malignant, the stage of malignancy, clinical stage and overall disease. This evaluation is important in the individual protocol therapy established for the animal patient. Each disease diagnosis requires corroborating the results from clinical investigations, but especially paraclinical methods. The oncological evaluation of the patient includes, first of all, hematological tests, blood biochemistry, urinalysis, complete endoscopic examination, ultrasound, thermography, X-ray, magnetic resonance and nuclear medicine methods, cytological and histological, endocrine, immunological and immunohistochemical markers. In the clinical context, a stage interpretation of the results confirms the nature of the proliferative process, and thus a potential therapeutic conduct. The differential diagnosis of animals’ oncopathology has the same complex issues as in human oncology, in many cases clinical signs expressed in animals being atypical or insufficient to establish a certain diagnosis because of their general feature regardless of malignancy, insidious occurance, without obvious clinical manifestations to motivate diagnostic investigations. A close monitoring of the animal for a period is necessary in expectation. Periodic screening for pets over 6-7 years of age as an early way for the detection of malignancies developed de novo or for borderline lesion (border disease) is crucial for a successful treatment. It is to be avoided by any means the invasive oncological cytopathology diagnostic procedures (fine needle aspiration biopsy and incision biopsy), which should be replaced with alternative, non-invasive and conservative procedures like tumor markers, exfoliative citology and imaging evaluation, especially in cases with suspicion of malignancy developed in intense vascularized and nonencapsulated tissue.
Diagnosticul multimodal în neoplazii
The multimodal diagnosis of neoplasias
First published: 10 aprilie 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/PV.26.1.2017.576
Abstract
Rezumat
Diagnosticul în oncologie reprezintă un proces complex, cu mai multe stadii şi o abordare multidisciplinară, în urma căruia stabilim existenţa unui proces neoplazic, benign sau malign, stadiul malignităţii şi stadiul clinic al bolii în ansamblu. Această evaluare este importantă în protocolul terapeutic individualizat pentru fiecare animal. Diagnosticul fiecărei boli necesită coroborarea rezultatelor investigaţiilor clinice, dar mai ales metode paraclinice de examinare. Evaluarea oncologică a pacientului include, în primul rând, examene hematologice, de biochimie a sângelui, analiza urinei, examinare completă endoscopică, ecografie, termografie, examene radiologice, RMN sau alte metode de medicină nucleară, markeri citologici, histochimici, endocrini, imunologici şi imunohistochimici. În contextul clinic, interpretarea stadializată a rezultatelor confirmă natura procesului proliferativ, sugerând o posibilă abordare terapeutică. Diagnosticul diferenţial al patologiei oncologice la animale prezintă aceleaşi dificultăţi ca şi în oncologia umană, în numeroase cazuri simptomele clinice ale animalelor fiind atipice sau insuficiente pentru a pune un diagnostic de certitudine, din cauza caracteristicilor generale indiferent de malignitate, a apariţiei insidioase, fără manifestări clinice evidente pentru a motiva investigaţii diagnostice. Este necesară o monitorizare în expectativă, atentă, a animalului, pentru o perioadă. Screeningul periodic al animalelor de peste 6-7 ani, ca metodă de detectare precoce a malignităţilor apărute de novo sau a leziunilor borderline, este crucial pentru a institui un tratament eficient. Trebuie evitate cu orice preţ procedurile diagnostice de citopatologie oncologică invazivă (biopsia aspirativă cu ac fin şi biopsia incizională), care trebuie înlocuite cu proceduri alternative, neinvazive şi conservative, precum markerii tumorali, citologia exfoliativă şi evaluarea imagistică, mai ales în cazuri cu suspiciune de malignitate dezvoltată în ţesuturi intens vascularizate şi neîncapsulate
Diagnosticul oncologic trebuie să reprezinte un mijloc de stabilire a naturii, extinderii și mai ales a tipului formațiunii neoplazice, și nu un scop în sine care trebuie atins cu orice preț pentru sănătatea și viața animalului.
Evitarea când se poate a mijloacelor sângeroase, invazive, de diagnostic și înlocuirea lor cu tehnici alternative, non-invazive și conservative, sunt de preferat, markerii oncologici fiind în general suficient de utili în stabilirea diagnosticului diferențial.
În prezent, se urmărește alinierea oncologiei veterinare la modelul celei umane, motivată de interesul crescând pentru oncologia comparată ca o componentă a conceptului de medicină ca o singură știință.
Termenul de diagnostic provine din limba greacă (diagnosis, unde dia = prin și gnosis = a cunoaște) și reprezintă concluzia reieșită în urma coroborării rezultatelor tuturor mijloacelor de examinare utilizate, ceea ce, practic, definește starea clinică a pacientului la momentului examinării.
Diagnosticul oncopatiilor la animale ridică aceleași probleme complexe ca și la om: stabilirea precoce a certitudinii prezenței bolii canceroase într-un organism este dificilă, deoarece caracteristica generală a cancerului, indiferent de gradul de malignitate, este apariția insidioasă, fără manifestări clinice evidente, care să motiveze investigația de diagnostic. La aceasta se adaugă și faptul că, la o mare parte din procesele tumorale, momentul exprimării clinice, respectiv al atingerii unei mase de celule tumorale de 10 x 9, este deja tardiv pentru a influența major terapeutic evoluția lor. Aceasta presupune că diagnosticul precoce ar trebui să preceadă acest moment, respectiv boala să fie depistată în faza infraclinică, fapt ce a determinat și determină o continuă perfecționare și mai ales o lărgire a metodelor de investigație.
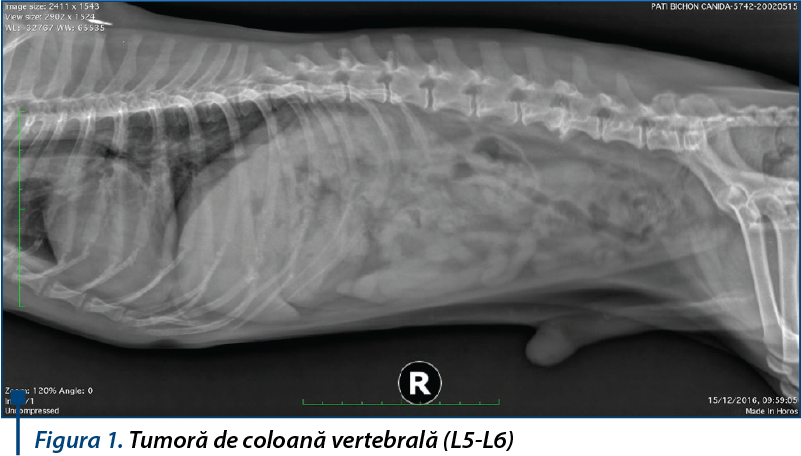
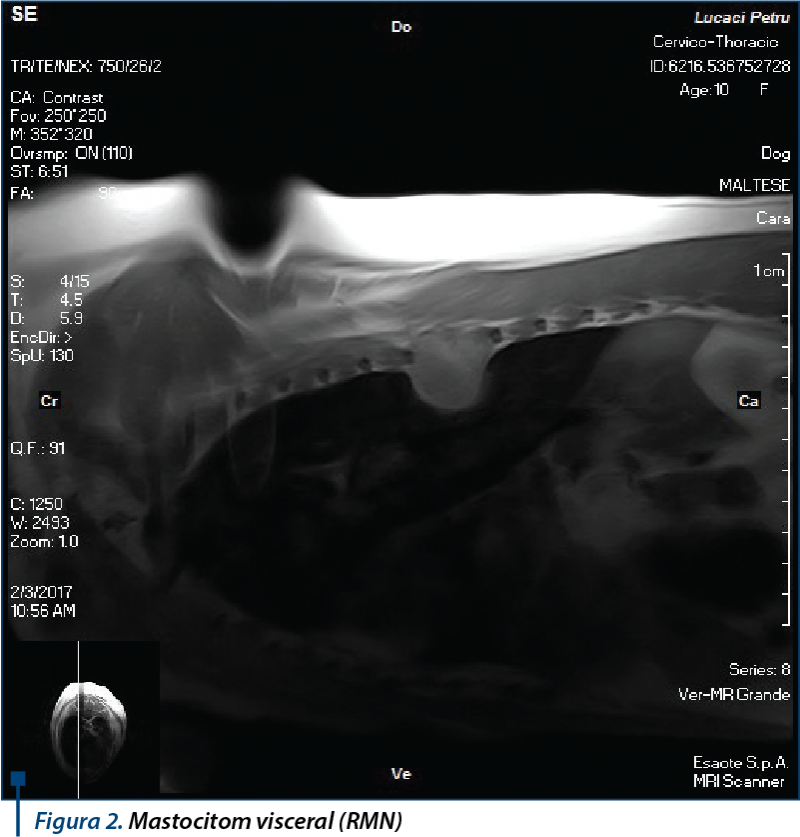

Clasificarea diagnosticului oncologic
Stabilirea diagnosticului fiecărei afecțiuni neoplazice impune folosirea metodelor combinate de investigație clinică și paraclinică, interpretarea corectă a acestor rezultate ducând la stabilirea tipului de manifestare patologică, a eventualelor cauze și implicit a conduitei terapeutice. O importanță deosebită o are și realizarea diagnosticului diferențial, în multe situații semnele clinice exprimate de animal fiind atipice sau insuficiente pentru stabilirea unui diagnostic cert, fiind nevoie de o perioadă cu supraveghere expectativă îndeaproape a animalului.
În raport cu scopul urmărit, diagnosticul clinic completat de cel paraclinic permite evaluarea următoarelor sindroame și simptome:
Simptomatic - pe baza semnelor de boală prezentate de animal; în cazul unei neoplazii, presupune cunoașterea și interpretarea diferitelor simptome care pot fi evidențiate.
-
Simptome funcționale (modificarea funcției unui organ); de exemplu:
- șchiopătarea - diagnostic diferențial radiologic, CT, între osteită și osteosarcom;
- vomă, disfagie - diagnostic diferențial ecografic, RMN (tumori hepatice, splenice);
- tuse, dispnee - diagnostic diferențial radiologic, CT (tumori la nivel pulmonar sau prezența metastazelor la nivelul aparatului pulmonar).
- Simptome morfologice - prezența unei neoformațiuni vizibile cu ochiul liber - peste 10 x 9 celule (de exemplu, tumoră mamară, tumoră Sticker, papilom bucal) - sau depistarea acesteia la examenul radiologic, ecografic sau cu alt mijloc de vizualizare (formațiuni de diferite dimensiuni și forme la nivelul unor viscere sau structuri interne).
- Simptome locale ale tumorii primare - modificări locale consecutive dezvoltării locale a unei formațiuni (în stadiu incipient; nu există decât tumor și functio laesa, nu și rubor, calor, dolor).
- Simptome generale - implicarea întregului organism în procesul patologic (cum ar fi tumorile extrem de agresive sau tumori cu prezență veche în organism, care alterează în timp homeostazia).
- Simptome patognomonice prezente, de regulă, în cazul localizărilor externe.
- Simptome tipice caracteristice unor localizări, dar pentru precizarea diagnosticului se coroborează și cu alte semne (de exemplu, adenopatia).
- Simptome atipice sau nespecifice care pot ajuta la orientarea examenului.
- Simptome ciudate - manifestări care pot deruta medicul.
- Simptome constante (șchiopătura în cazul osteosarcomului) și inconstante (ascita în cazul hepatocarcinomului).
- Simptome directe de la locul modificării și indirecte, de la distanță.
- Simptome obiective (cele evidențiate în urma examenului clinic) și subiective (deduse în urma manifestărilor individului, cum ar fi reacția de apărare la palparea unui ficat afectat).
-
Topografic - localizarea directă sau indirectă a modificării leziunii, tulburării, realizată cu ajutorul mijloacelor de vizualizare:
- medicină nucleară - radioscopia, radiografia, RMN, tomografia
- ultrasonoscopia, ultrasonografia (ecografia)
- termografia.
- Anatomic - stabilirea organului sau structurii afectate; mostre de țesut sau organ. Confirmarea se realizează prin examen citologic și histopatologic.
- Funcțional - urmărește evidențierea funcțiilor unui sistem sau aparat care sunt alterate. Precedă modificările morfologice; prin teste funcționale, în funcție de aparatul sau sistemul afectat.
- Etiologic - dacă se cunoaște existența unor factori oncoactivi sau chiar de ordin genetic (factori fizici/chimici implicați, inclusiv toxine; factori virali/parazitari; factori traumatici; factori favorizanți/predispozanți).
- Direct - pe baza semnelor constatate la examinarea clinică a animalului.
- Indirect - semnalarea modificărilor cu ajutorul unor aparate sau determinări de laborator:
- calitative (aspecte citologice, markeri serici, biochimie)
- cantitative - HLG, examen biochimic sangvin.
De urină - cantitative și calitative.
Colecții lichidiene (sinovie, ascită, LCR).
Examenul clinic și de laborator al materiilor fecale.
Examen ecografic, termografic, EKG.
Examen radiologic, endoscopic, RMN, CT, endoscopic.
Examenul citologic, histopatologic.
- Diferențial - are un rol deosebit pentru diagnosticul oncopatiilor: de exemplu, osteită - osteosarcom (proces inflamator - proces neoplazic) sau retroversie vaginală - tumora Sticker; de altfel, în toate afecțiunile cu simptomatologie puțin specifică, efectuarea unui diagnostic diferențial este foarte importantă.
- Expectativ - ținerea animalului sub observație pentru a fi depistate anumite semne mai slab exprimate inițial.

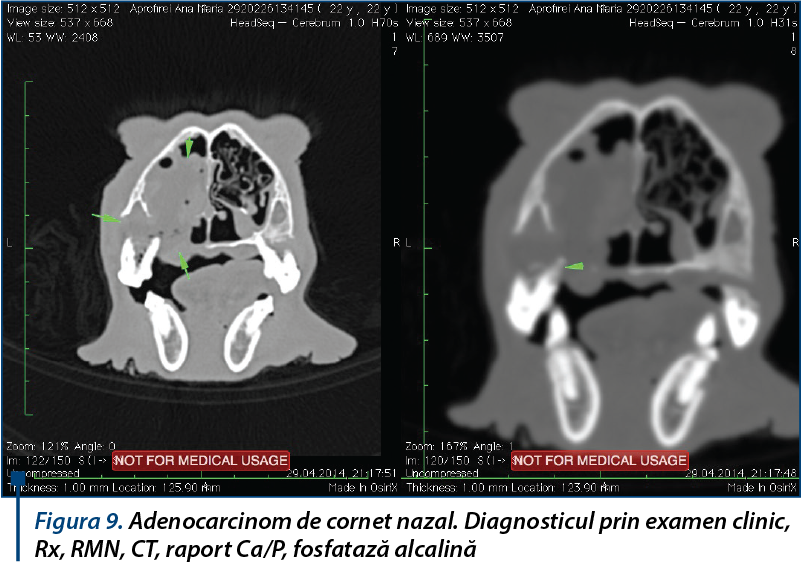

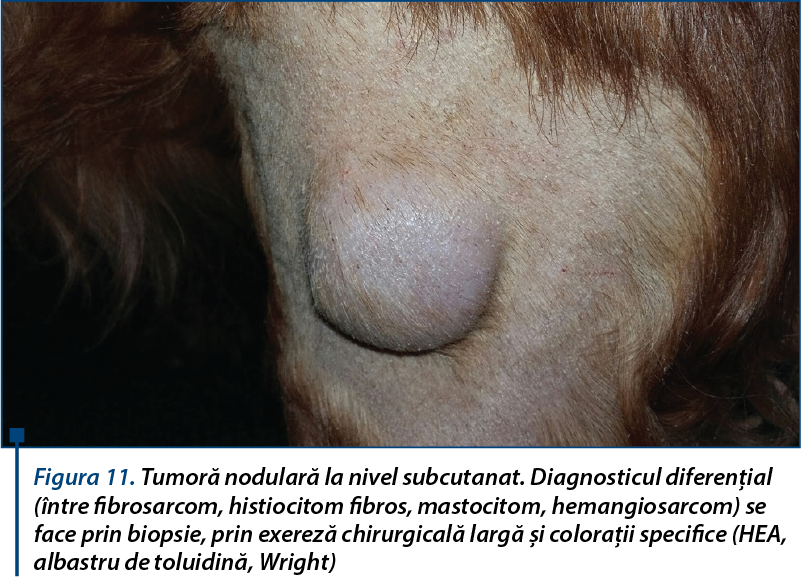
Aspecte urmărite de diagnosticul oncologic veterinar multidisciplinar
Ca și în medicina umană, diagnosticul oncologic veterinar presupune o serie de etape obligatorii și succesive, corelând tehnici de investigație multidisciplinare.
Întreaga metodologie uzitată are în vedere stabilirea corectă a trei deziderate:
1. Localizarea procesului tumoral - aceasta ridicând o serie de probleme în cazul localizărilor profunde sau „ascunse”. Se realizează prin examen clinic obiectiv, fiind ușor de aplicat în cazul localizărilor externe, utilizându-se metodele semiologice clasice. Se bazează pe examenul obiectiv al animalului coroborat cu mijloace de investigație de laborator (biochimice și hematologice), urmărindu-se ca prin datele obținute să se stabilească diagnosticul și implicit conduita terapeutică adecvată.
2. Evaluarea extensiei tumorale - examenul clinic obiectiv, ca examen morfologic, urmărește doar aspecte privind dinamica în timp a dezvoltării procesului tumoral, fără a furniza date privind natura și extensia (invazia loco-regională profundă sau prezența unor metastaze). De aceea el trebuie obligatoriu asociat inițial cu metode de diagnostic prin vizualizare (tehnici imagistice optice, electronice, ultrasonografice și ale medicinei nucleare) și ulterior cu examenele paraclinice de diagnostic.
3. Identificarea naturii histopatologice și a gradului de diferențiere se realizează printr-o multitudine de tehnici, în funcție de localizarea topografică și aspectul macroscopic al formațiunii suspecte:
- recoltarea de probe citopatologice sau histopatologice se realizează prin mijloace sângeroase, tehnicile și situațiile fiind evaluate individual, pentru a micșora la maximum riscul diseminării loco-regionale și metastatice;
- citologie exfoliativă pentru neoplazii superficiale de piele sau mucoase (raclare, endoscopie, lavaj) și lactocitograma;
- puncție aspirativă cu ac fin din tumora primară, limfadenogramă, metastaze, medulogramă;
- biopsii excizionale intra- sau preoperatorii.
4. Stabilirea tipului histopatologic și a originii embrionare prin markeri tumorali - markerii tumorali sunt elemente de semnalizare cu rol în screeningul de diagnostic, prognostic, monitorizare terapeutică și postterapeutică în boala canceroasă.
Markerul celular, în general, poate fi și un caracter morfologic (formă, dimensiune, anumiți receptori prezenți sau absenți) sau funcțional (biochimic - de exemplu, enzimă), particular pentru o anumită populație celulară. Sunt produși biologici rezultați din metabolismul celulelor tumorale maligne, dar pot fi și consecința activității unor celule normale (în proliferare rapidă) sau implicate în diverse procese patologice benigne, motiv pentru care rezultatele fals-pozitive sunt frecvente. În urma hipersintezei sunt eliberați în sânge sau urină, structural fiind constituiți din proteine specifice (enzime, izoenzime ale ciclului pentozofosfat), hormoni endo- și ectopici, diferiți metaboliți (colesterol, poliamine, resturi de ADN), produși oncofetali (sintetizați în condiții normale în perioada embrionară și fetală), antigene tumorale specifice sau antigene asociate tumorilor.
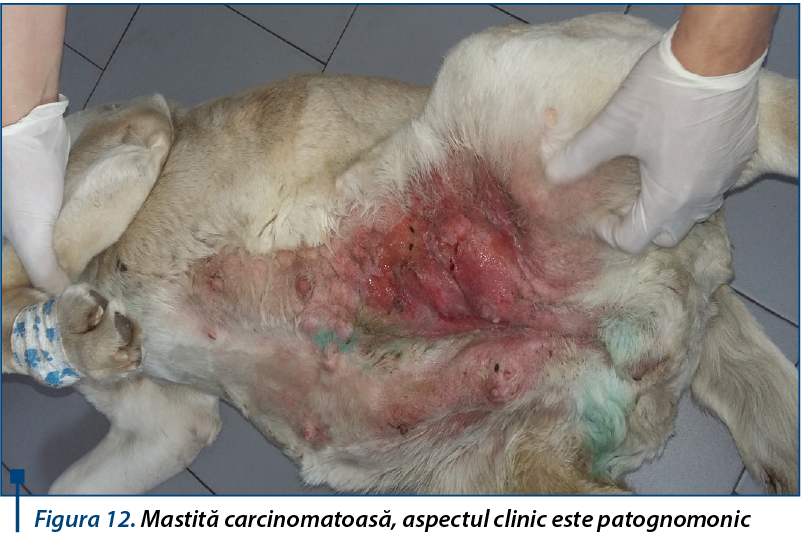
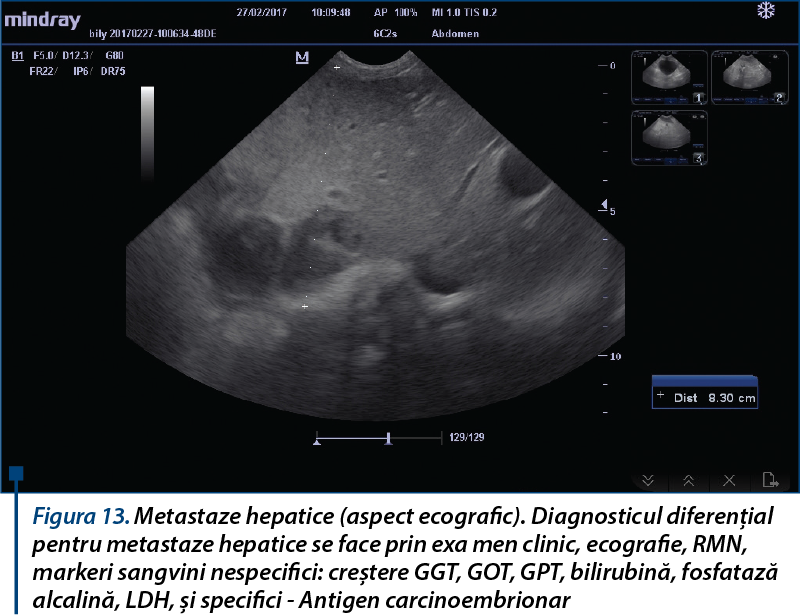

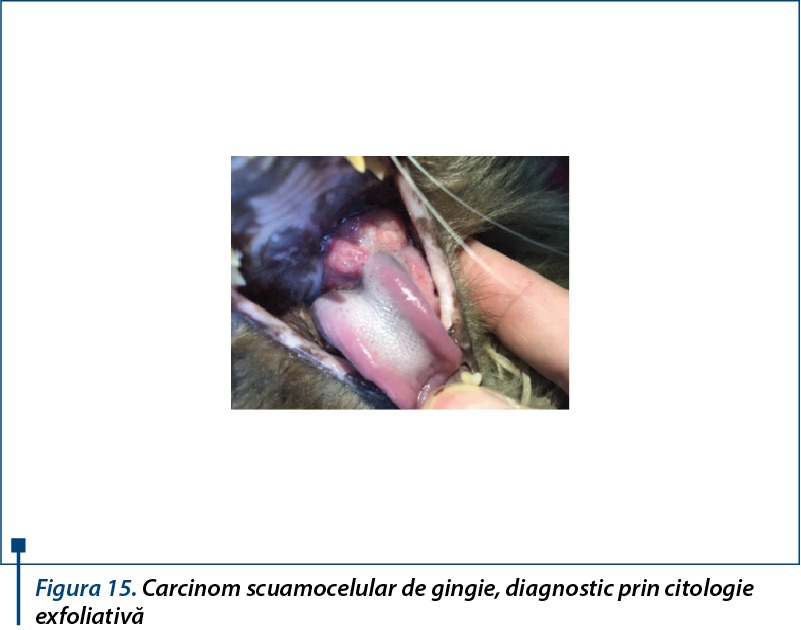
Este important de subliniat faptul că populațiile celulare tumorale sunt eterogene, iar în evoluția tumorii intervin procese de selecție a unor subpopulații care au comportament biologic diferit față de celulele canceroase parentale și numai unele dintre variantele celulare își câștigă capacitatea de secreție. De aceea, cantitatea de substanță marker elaborată de tumoră nu se corelează întotdeauna cu volumul ei. În plus, există tumori capabile să secrete mai multe tipuri de markeri. La fel, apariția de metastaze se bazează pe selecția și migrarea unor variante celulare având un potențial crescut de metastazare, dar care își pot pierde capacitatea de elaborare a markerilor; de aceea, unele metastaze ale unei tumori primare, producătoare de marker, pot să nu fie însoțite de creșterea valorii acestuia. În cazul celulelor neoplazice, poate apărea în mod frecvent sinteza de izoenzime sau de proteine de tip fetal, ca și cea de antigene tumorale (alpha 1 fetoproteina în carcinoame hepatice; alpha 2 fetoproteina în unele reticulosarcoame și leucemii). Acestea fac parte din categoria glicoproteinelor tumorale onco-fetale care se formează în etapa timpurie a dezvoltării embrionare în anumite țesuturi, dar sinteza lor este stopată postnatal în mod normal. Ceea ce este important la acești markeri este că fenotipul tumoral este diferit de cel embrionar.
Nivelul markerilor în sânge depinde de vascularizația masei tumorale, difuzibilitatea substanței, modul de eliberare din celulă, durata de viață a materialului sintetizat. Dacă markerul este antigenic și induce o reacție imună în organism, prin fixarea pe receptorul corespunzător specific, acest fenomen poate fi depistat, iar prezența celulelor tumorale va fi sesizată precoce, înaintea dezvoltării tumorii primare. În același fel se pot depista precoce (înaintea apariției clinice a tumorii primare), în anumite tipuri tumorale, recidiva postoperatorie sau chiar metastazele.
Utilitatea clinică a markerilor tumorali
Au valoare enormă diagnostică și paraclinică, putând fi detectați concomitent atât cei sangvini, în hemopatiile maligne, cât și cei serici, în cazul metastazelor, sau morfologici ai tumorii primare solide.
Depistarea precoce a modificărilor markerilor tumorali maligni permite o instituire a terapiei în stadiile incipiente, cu evitarea mijloacelor sângeroase și invazive de diagnostic, cu monitorizarea efectelor terapeutice și asigurarea unui interval de supraviețuire mai lung și în condiții de confort biologic.
-
Diagnosticul precoce al cancerului în faze preclinice (To-T in situ) prin determinarea:
- unor markeri oncologici la populația cunoscută cu risc înalt pentru un anumit tip de cancer (ex.: depistarea supraexprimării genei HER2-neu la anumite familii cu incidență mare a cancerelor genitale la femele);
- localizării unor cancere primare sau metastaze oculte (decelare radioimună folosindu-se anticorpi markeri corespunzători, marcați radioactiv, și evidențierea fixării lor prin explorare scintigrafică computerizată).
- Indicator preoperator al volumului tumoral, al stadializării și extinderii bolii (prin monitorizare TNM).
- Monitorizarea tratamentului (evaluarea rezultatelor terapeutice, decelarea precoce a recidivelor și/sau metastazelor) - bolnavii la care inițial au fost constatate niveluri ridicate ale unui marker și la care valorile au revenit la normal pot fi monitorizați pentru evoluția bolii prin determinarea dinamică a acestuia. Reapariția în postoperator și menținerea unor niveluri ridicate ale markerului determinat sugerează rezecție incompletă, prezența recidivelor sau a metastazelor.
- Evaluarea prognosticului - dacă în momentul diagnosticării unor tumori maligne există niveluri crescute ale unor markeri, aceasta se corelează frecvent cu invazii masive loco-regionale și/sau metastaze precoce.
Clasificarea markerilor tumorali
Markerii tumorali ai organismului canceros sunt rezultați în urma evoluției clinice a bolii și ca o consecință a dezvoltării celulelor tumorale maligne diferite de cele normale, precum și datorită sindroamelor paraneoplazice.
1. Markerii tumorali morfologici convenționali (de linia I) sunt cei care pot fi depistați la nivelul organismului canceros prin examenele de diagnostic:
- Clinici (funcționali) - se referă la statusul de performanță al animalului canceros, corespondentul Indicelui Karnofsky de la om.
- Morfologici (referitori la tumora primară). Dimensiunile tumorii primare, respectiv dimensionali (T), număr de limfocentri invadați neoplazic (N), prezența și numărul metastazelor (M), invazia capilarelor limfatice a sistemului circulator venos, a epanșamentelor, respectiv evaluarea clinică prin sistemul TNM, gradul de diferențiere histologică; numărul limfocentrilor invadați; statusul receptorilor hormonali.
- Tisulari, reprezentați de: gradingul histopatologic (G1-G3), pentru tumori solide, gradingul citologic Babeș-Papanicolau (CIN 1-4) pentru citologia exfoliativă, nivelul de invazie Clark (1-4) al dermului în cazul melanomului malign.
Majoritatea caracterelor cito-morfofuncționale și elementele constitutive ale celulelor normale sunt regăsite în celulele neoplazice, în diferite proporții, totuși cele maligne prezintă un ansamblu de particularități care permit caracterizarea și recunoașterea lor în raport cu țesutul de origine. Abaterea de la morfologia celulară normală constituie atipia celulară, caracter general al neoplaziilor maligne.
2. Markerii celulari tumorali funcționali, respectiv specifici (de linia a II-a):
Aceștia indică prezența celulelor tumorale în organism și sunt elemente de semnalizare în screeningul de diagnostic, monitorizarea terapeutică și postterapeutică.
Se clasifică, după natura lor, în: morfologici, enzimatici, imunologici, genetici, receptori pentru diverse proteine, markeri hormonali.
Markerii genetici: activitatea citoproliferativă; gradul de ploidia (cuantificarea ADN-ului tumoral); expresia și amplificarea unor oncogene (Her 2 Neu, BRCA1, BRCA2).
Markerii imunologici - receptorii factorilor de creștere: EGF - factor de creștere epidermali; IGF1 - factor de creștere insulinic; IGF alpha și beta - factori de transformare tumorală; FGF - factor fibroblastic de creștere; GRP - bombesina.
Markeri de invazivitate și metastazare - catepsina D
Biomarkeri tumorali circulanți:
- TPA - antigen polipeptidic tisular;
- CA-15 -3 - biomarkeri de natură mucinică.
Markeri de chimiorezistență:
- MDR1 și MDR2 - genele rezistenței multidrog;
- GST - II - gena rezistenței pleiotrope la chimioterapie.
3. Markeri tumorali patognomonici
- morfologici: celulele multinucleate Sternberg Paltouf Reed, celula Hodgkin;
- anomalii genetice, cum ar fi translocația Philadelphia, în leucemia mieloidă cronică;
- biochimice serice: anticorpii himerici, proteina M (monoclonală), ca fragment imunoglobulinic, sau proteina Bence-Jones în macroglobulinemia Waldenstrom (Plasmocitom).
Proteine: poliaminele (putresceina, spermidina, spermina); K – cazeina și feritina.
Enzime și izoenzime: fosfataza alcalină placentară (izoenzima Regan) și fosfataza alcalină osoasă; fosfataza acidă prostatică și fosfataza acidă limfocitară.
Glicoziltransferaze (fucoziltransferaza, sialiltransferaza, galactoziltransferaza), 5̀-nucleotidaza; aspartat și alanin transferază; gamma - glutamiltransferază, fosfohexozotransferază, lactatdehidrogenază; dezoxinucleotidil transferază terminală.
Proteine oncofetale sau de diferențiere: CEA (antigenul carcimo-embrionar); AFP (alpha - 1 - fetoproteină); POA (antigenul oncofetal pancreatic); TA - 4 (antigenul tumoral - 4); CALA (antigenul comun al leucemiilor limfatice acute sau antigenul Greaves); EME (antigenul de membrană epitelială); BOFA (antigenul beta-oncofetal).
Hormoni și hormoni ectopici: ACTH sau precursori ai ACTH (big - ACTH); LPH (beta lipotropină); MSH (hormonul melanostimulator); glucagonul (factorul hiperglicemiant), calcitonina tiroidiană, gastrina, eritropoetina.
Gonadotrofine hipofizare: FSH (hormonul foliculo-stimulant), LH (hormonul luteotrop), prolactina; ADH (hormonul antidiuretic), PTH (hormonul paratiroidian), TSH (hormonul tireotrop), LATS (substanța tireostimulatoare cu acțiune lentă), HPF (factorul hipoglicemiant insulin-like).
Hormonii placentari ectopici: beta HCG (gonadotrofina corionică).
Proteine fiziologice cu procente crescute: calcitonina, GH (hormonul de creștere); CFS (factorul de stimulare a formării de colonii), AUP (arginina, vasopresina), VIP (peptide intestinale vasoactive), serotonina, histamina.
Spre deosebire de alte stări patologice, în oncologie nu este suficient să se stabilească prezența unei neoplazii, aceasta find insuficientă pentru luarea deciziei terapeutice privind tratamentul multidisciplinar obligatoriu la pacienții cu cancer, iar aprecierea prognostică devine foarte relativă. Din aceste motive, se impune stabilirea cât mai precisă și precoce a extensiei reale a bolii, stadiul clinic de dezvoltare (TNM), natura embriogenezică a țesutului malignizat, gradul de citodiferențiere tumorală, folosind o gamă foarte largă de investigații clinice, dar și paraclinice: ultrasonografice, termografice, radiologice, rezonanța magnetică și metodele medicinei nucleare, endoscopice, citologice și histopatologice, endocrinologice, imunologice, inclusiv prin markeri.
Bibliografie
2. Dan Crînganu. Patologia animalelor de companie – oncologie generală, ediţia a II-a, Edit. Printech, 2009.
3. Jubb K.V.F., Kennedy P.C., Palmer N. (1993). Pathology of domestic animals. Fourth Edition, vol. I, Academic Press, Inc. Hartcourt Brace Javanovich.
4. Drelise F., Devauchelle P. (1996). Les osteosarcomes du chien. Le point veterinaire.
5. Baba A.I. Oncologie comparată, Ed. Academiei Române, Bucureşti, 2002.
6. Coomer Alastair R., Liptak Julius M. Canine histiocytic diseases, Compendium Continuing Education Vet 2008 Apr; 30(4): 202-4, 208-16; quiz 216-17.
7. Fulmer Amanda K., Mauldin Glenna E. Canine histiocytic neoplasia: An overview, Can Vet J 2007; 48:1041–1050.
8. Gross Thelma Lee, Ihrke Peter J., Walder Emily J., Affolter Verena K. Skin Diseases of the Dog and Cat Clinical and Histopathological Diagnosis, 2nd ed., Ed. Blackwell Science, 2005, pp. 323-325, 837-852.
9. Hahn Kevin A. (2002), Veterinary Oncology, Butterworth-Heinemann, Woburn, USA.
10. Kim D.Y., Royal A.B., Villamil J.A. (2009). Disseminated Melanoma in a Dog with Involvement of Leptomeninges and Bone Marrow, Veterinary Pathology vol. 46, no. 1, 80-83.
11. Kuding Simon T., Seguin Bernard (2012), Veterinary Surgical Oncology, Wiley-Blackwell, Oregon, USA.
12. Martinez C.M., Penafiel-Verdu C., Vilafranca M., Ramirez G., Mendez-Gallego M., Buendia A.J., Sanchez J. (2011). Cyclooxygenase-2 Expression is Related with Localization, Proliferation, and Overall Survival in Caninre Melanocytic Neoplasms, Veterinary Pathology vol. 48, no. 6, 1204-1211.
13. Ramos-Vara J.A., Beissenherz M.E., Miller M.A., Johnson G.C., Pace L.W., Fard A., Kottler S.J. (2000). Retrospective Study of 338 Canine Oral Melanomas with Clinical, Histological, and Immunohistochemical Review of 129 Cases, Veterinary Pathology, vol 37, no 6, 597-608.
14. Simon T. Kudding, Bernard Seguin (2012). Veterinary Surgical Oncology, Wiley-Blackwell, Iowa, USA.
15. Smith S.H., Goldschmidt M.H., McManus P.M.(2002). A Comparative Review of Melanocytic Neoplasms, Veterinary Pathology, vol 39, no. 6, 651-678.
16. Stephen J. Withrow, David M. Vail (2007), Witrow & McEwens Small Animal Clinical Oncology, Saunders, Missouri, USA.
17. Yamada N., Mori T., Murakami M., Noguchi S., Sakai H., Akao Y., Maruo K. (2012). Fascin-1 expression in canine cutaneous and oral melanocytic tumors, Veterinary and Comparative Oncology, vol 10, issue 4, 303–311.
18. http://www.marvistavet.com/html/oral_squamous_cell_carcinoma_f.html
19. http://www.nativeremedies.com/petalive/articles/nasal-tumor-dogs.html;
20. http://www.vetsurgerycentral.com/oncology_nasal_tumors.htm
21. http://www.epathology.ro/patologie-generala/tumori-maligne/tumori-mezenchimale-maligne.html?start=4
22. http://www.caninecancer.com/Osteosarcoma.html
Articole din ediţiile anterioare
Carcinomul scuamocelular la pisică − diagnostic diferenţial şi abordare terapeutică multimodală
Carcinomul scuamocelular la pisică este o afecţiune care poate fi tratată dacă este diagnosticată precoce. Din acest considerent sunt extrem de imp...
Fibrosarcoamele la câini
Fibrosarcomul poate să apară la orice vârstă şi ocupă locul al treilea ca frecvență la câine. La această formă de cancer sunt mai predispuse rasele...