The taxonomy of Psittaciformes order classifies families such as Loriinae (lory parrots or false parrots), Cacatuidae (parrots with crest and nymphs) and Psittacidae (true parrots and parrakeets). The ever-increasing desire to obtain specimens with plumage and especially with a spectacular chromatics lead in many cases to the reproduction by repeated inbreds and in very close kinship (even repetitive generations of mother-son or father-daughter matings), causing secondary changes in the metabolism and immune system of the obtained birds, characteristics transmitted to the next generations. The breeding conditions are not always correlated with the needs of these species, in many cases the knowledge about the eco-biology of captive-grown psittacins being rather poor, which leads to an increase in their sensitivity. In recent years, we are confronted in the clinic of these species with extremely diverse pathologies or metabolic changes that have never been described or even observed in wild parrots. Among the psittacines’ bacterioses, the pseudomonosis is an important disease because of its increasing frequency of diagnosis, in both owners and professional breeders. One particular feature is the sensitivity that many psittacine species exhibit both to Pseudomonas aeruginosa and Pseudomonas fluorescens. The two bacterial species (Pseudomonas aeruginosa and Pseudomonas fluorescens) exhibit resistance to the action of many antibiotics and have the ability to synthesize numerous substances present in the cell structure, toxins and many other factors that interfere with virulence. The disease appears as a well-defined clinical entity that evolves with dominant digestive disorders or sepsis. The faeces are green or with white urates on the edge, with a heavy or liquid consistency. In the association with Pseudomonas fluorescence, there are even found green-leek color and respiratory symptomatology. The diagnosis of Pseudomonas spp. infection in birds is based on the anatomoclinical data and is confirmed by bacteriological examination. The clinical diagnosis is difficult and is not very valuable. The septicemic forms of the disease are difficult to diagnose because, apart from disrupting the general condition, birds have no characteristic signs.
Pseudomonozele psitacinelor
Psittacines pseudomonosis
First published: 18 decembrie 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/PV.33.4.2018.2109
Abstract
Rezumat
Ordinul Psittaciformes încadrează taxonomic familiile: Loriinae (papagali Lori sau falşii peruşi), Cacatuidae (papagalii cu creastă şi peruşii nimfă) şi Psittacidae (papagali şi peruşi adevăraţi). Dorinţa tot mai mare de a obţine exemplare cu penaj şi în special cu o cromatică spectaculoasă a însemnat în multe situaţii reproducerea prin consangvinizare repetată şi în grade de rudenie extrem de apropiate (chiar repetarea pe mai multe generaţii a împerecherilor mamă-fiu sau tată-fiică), determinându-se în plan secundar modificări importante în metabolismul şi sistemul imunitar al produşilor obţinuţi, caracteristici care s-au transmis generaţiilor următoare. Condiţiile de întreţinere nu sunt întotdeauna corelate cu necesităţile speciilor respective, în multe cazuri cunoştinţele despre ecobiologia psitacinelor crescute în captivitate fiind destul de sărace, acestea ducând la o accentuare a sensibilităţii lor. În ultimii ani ne confruntăm în clinica acestor specii de păsări cu patologii extrem de diverse sau cu modificări metabolice care nu au fost niciodată descrise sau măcar observate la papagalii aflaţi în sălbăticie. Între bacteriozele psitacinelor, pseudomonozele ocupă un loc important prin frecvenţa tot mai ridicată cu care sunt diagnosticate, atât la psitacine ale iubitorilor amatori, cât şi în crescătoriile unor profesionişti. O particularitate o reprezintă şi sensibilitatea pe care multe specii de psitacine o manifestă atât la Pseudomonas aeruginosa, cât şi la Pseudomonas fluorescens, în diferite situaţii constatându-se în aceeaşi comunitate sindrom respirator produs de Pseudomonas fluorescens şi sindrom digestiv determinat de Pseudomonas aeruginosa. Boala apare ca o entitate clinică bine definită, care evoluează dominant cu tulburări digestive sau septicemie. Fecalele sunt verzi sau coafate pe margine cu uraţi, cu o consistenţă păstoasă sau lichidă. Diagnosticul se bazează pe date anatomoclinice şi este confirmat prin examen bacteriologic. Diagnosticul clinic este dificil de stabilit. Formele septicemice ale bolii sunt greu de diagnosticat, deoarece, în afară de perturbarea stării generale, păsările nu au semne caracteristice.
Abordarea unui subiect referitor la bacteriozele psitacinelor este importantă deoarece, pe de o parte, frecvenţa bolilor infecţioase, în general, la păsările de colivie şi volieră este într-o creştere accelerată, iar pe de altă parte, pentru că greşelile de diagnostic (implicit intervenţia terapeutică) sunt destul de dese. Ordinul Psittaciformes încadrează taxonomic familiile: Loriinae (papagali Lori sau falşii peruşi), Cacatuidae (papagalii cu creastă şi peruşii nimfă) şi Psittacidae (papagali şi peruşi adevăraţi). Condiţiile de întreţinere nu sunt întotdeauna corelate cu necesităţile speciilor respective, în multe cazuri cunoştinţele despre ecobiologia psitacinelor crescute în captivitate fiind destul de sărace. În ultimii ani ne confruntăm în clinica acestor specii de păsări cu patologii extrem de diverse sau cu modificări metabolice care nu au fost niciodată descrise sau măcar observate la speciile de papagali aflaţi în sălbăticie. Diagnosticarea corectă, utilizând metodele imagistice şi citohistologice actuale, permite o intervenţie terapeutică rapidă şi cu rezultate pozitive.
Între bacteriozele psitacinelor, pseudomonozele ocupă un loc important prin frecvenţa tot mai ridicată cu care sunt diagnosticate, atât la psitacine ale iubitorilor amatori, cât şi în crescătoriile unor profesionişti. O particularitate o reprezintă şi sensibilitatea pe care multe specii de psitacine o manifestă atât la Pseudomonas aeruginosa, cât şi la Pseudomonas fluorescens, în diferite situaţii constatându-se în aceeaşi comunitate sindrom respirator produs de Pseudomonas fluorescens şi sindrom digestiv determinat de Pseudomonas aeruginosa. Speciile din genul Pseudomonas sunt capabile să se adapteze şi să supravieţuiască în mai multe habitate, graţie capacităţii metabolice complexe. Ele pot utiliza un număr mare de componenţi organici prezenţi în mediile naturale, contribuind prin activitatea metabolică la circuitul materiei organice în natură. Mai mult, pot să supravieţuiască cu nevoi nutritive minime şi să se dezvolte la temperaturi de până la 42oC. Cerinţele nutritive minime şi capacitatea de a fi tolerante faţă de numeroşi factori fizici contribuie la succesul ecologic al pseudomonadelor şi ca agenţi patogeni. În afara infecţiilor respiratorii, pseudomonadele s-au dovedit a fi implicate şi în infecţiile pielii şi ale ţesuturilor moi, în endocardite, în infecţii gastrointestinale, în infecţii ale sistemului nervos central, în otite, în cheratite, în infecţii ale tractusului urinar şi în infecţii ale oaselor şi articulaţiilor.
Cele două specii bacteriene (P. aeruginosa şi P. fluorescens) prezintă rezistenţă la acţiunea multor antibiotice şi au capacitatea de a sintetiza numeroase substanţe prezente în structura celulei, toxine şi numeroşi alţi factori ce interferează cu virulenţa. Structurile asociate acestora includ pilii, care se presupune că acţionează ca adezine, permiţând ataşarea bacteriei de celulele epiteliale ale gazdei. Date care susţin acest punct de vedere sugerează că mutantele lipsite de pili manifestă o virulenţă scăzută pentru animalele de laborator. Mai mult, pilii purificaţi şi anticorpii blochează ataşarea bacteriei de celulele epiteliale. În anumite condiţii, aceste bacterii sunt capabile să sintetizeze un strat gros, cu aspect mucoid, cu rol important în determinarea infecţiilor respiratorii cronice, fapt demonstrat de frecvenţa ridicată a tulpinilor de Pseudomonas aeruginosa ce prezintă în jurul celulelor învelişul mucos, caracteristic. Un alt argument în ceea ce priveşte importanţa fenotipului mucoid în determinarea infecţiilor respiratorii se referă la observaţia că tulpinile non-mucoide reintroduse în pulmonii şobolanilor se transformă rapid în fenotipul mucoid.
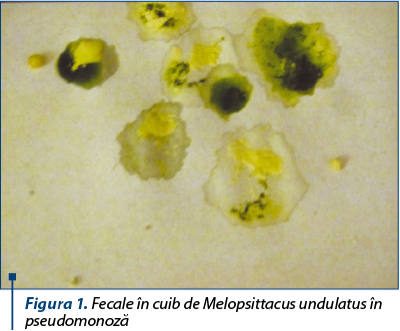
În afara factorilor deja descrişi, Pseudomonas aeruginosa este capabilă de a secreta şi alţi produşi ce intervin în manifestarea funcţiei de patogenitate. În timp ce structurile anatomice prezente pe suprafaţa celulelor bacteriene ajută la evitarea acţiunilor de apărare ale gazdei, capacitatea bacteriei de a invada ţesuturile gazdelor naturale receptive se datorează sintezei unor compuşi extracelulari care neutralizează acţiunea factorilor nespecifici sau/şi specifici de apărare ai gazdei, iar în final determină alterarea ţesuturilor colonizate de bacterie. Din categoria exoproduselor sintetizate de această bacterie fac parte enzimele şi toxinele care vor fi prezentate şi descrise în cele ce urmează. Cele mai importante substanţe sintetizate de Pseudomoas aeruginosa, în cursul metabolismului ei, sunt proteazele extracelulare şi exotoxina A. Până în prezent au fost identificate şi descrise trei tipuri de proteaze extracelulare, denumite Las A elastaza (Las A), Las B elastaza (Las B) şi proteaza alcalină. Dintre acestea, elastaza Las B este considerată sursa majoră a activităţii elastazice la Pseudomonas aeruginosa, iar contribuţia ei în patogeneza infecţiei şi în deteriorarea ţesuturilor a fost evidenţiată prin apariţia leziunilor hemoragice de pe pielea animalelor infectate. Cercetări recente au demonstrat că proteaza alcalină (alt metabolit sintetizat de tulpinile de Pseudomonas aeruginosa) este capabilă să degradeze laminina şi alte substraturi asemănătoare, contribuind prin aceasta la agravarea leziunilor tisulare şi permiţând difuziunea bacteriei în ţesuturile învecinate. Exotoxina A este cel mai toxic produs pe care tulpinile patogene de Pseudomonas aeruginosa îl pot sintetiza în cursul multiplicării lor. Toxina este o ADP-ribosiltransferază, cu acţiune similară toxinei difterice, ce intervine în inhibarea proceselor de biosinteză ale proteinelor celulare gazdă.
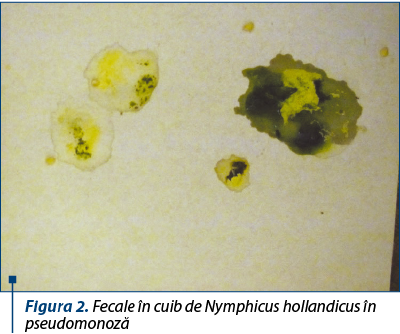
Cu toate că Pseudomonas aeruginosa este capabilă să producă un număr mare de toxine şi enzime, ea este considerată un patogen ocazional, fiind în măsură să cauzeze îmbolnăviri numai la indivizi compromişi din punctul de vedere al statusului lor imunitar. În situaţiile în care homeostazia organismului gazdă este alterată, ca în cazul arsurilor întinse sau al chimioterapiei supresive, bacteria colonizează ţesuturile şi provoacă infecţii localizate, ce se pot generaliza uşor. Odată cu multiplicarea bacteriei şi cu sinteza produselor toxice, bacteria îşi pierde statutul de saprofit şi devine un patogen serios, adesea fatal.

Pentru speciile de psitacine, Pseudomonas aeruginosa este reprezentantul genului cu cea mai mare importanţă, putând determina infecţii sistemice şi localizate. Acestea pot apărea la pui, tineret sau adulţi, iar uneori se constată (în special la Loriinae) pierderea capacităţii de ecloziune. Faptul că bacteria este prezentă în apă, sol şi pe suprafaţa plantelor lărgeşte mult posibilităţile de diseminare şi, totodată, posibilităţile de contaminare. În general, apariţia bolii este favorizată de igiena necorespunzătoare, de alimentaţia defectuoasă, de tratamentele îndelungate cu antibiotice faţă de care Pseudomonas spp. este rezistent şi de menţinerea ouălor din cuib în condiţii improprii. Adesea, Pseudomonas aeruginosa participă ca germen de infecţie secundară sau asociat altor infecţii bacteriene sau virale (micoplasmice, colibacilare, hemofilice). Este un germen ubicuitar, care se poate izola din solul umed, apa de băut, beţele din colivie sau volieră care sunt menţinute umede sau de pe plantele din mediul în care sunt cazate păsările. În plus, este şi un epifit al mucoaselor respiratorii şi digestive, de unde este eliminat, contaminând mediul ambiant, de unde ajunge din nou pe mucoasele animalelor, închizându-se astfel circuitul germenului în natură, chiar şi fără a include în lanţ păsările bolnave. În multe situaţii, calea de pornire o constituie hrănirea păsărilor sălbatice pe pervazul ferestrelor sau pe terasă, de unde bacteria este preluată de proprietar sau se aerosolizează. Este posibilă şi transmiterea verticală a bolii, dar nu transovarian, ci ca urmare a contaminării cojii ouălor, fie în oviduct sau cloacă, fie după eliminare cu germeni din mediul ambiant, care, în anumite condiţii, pot pătrunde în interiorul oului. În astfel de cazuri apare fie mortalitatea embrionară, fie îmbolnăvirea puilor în primele zile de viaţă. În cuib, infectarea se poate realiza şi pe cale respiratorie sau digestivă, sursa primară fiind reprezentată de primii pui bolnavi, care ulterior o vor transmite şi fraţilor mai mici.

Boala apare ca o entitate clinică bine conturată, ce evoluează cu tulburări dominant digestive sau cu forme septicemice. Fecalele au o culoare verzuie, marcate pe margine cu uraţi albi, cu o consistenţă păstoasă. În cazul asocierii cu Pseudomonas fluorescens se constată chiar o culoare verde-praz şi asocierea cu simptome respiratorii. Evoluţia este de regulă rapidă, putând apărea în câteva zile diarei apoase, cu o coloraţie verde strident. La puii în vârstă de câteva zile, boala evoluează de obicei septicemic, în multe cazuri forma digestivă fiind inaparentă clinic. Puii rezultaţi din ouă infectate se îmbolnăvesc la puţin timp după ecloziune, prezentând febră, anorexie, somnolenţă, conjunctivită, jetaj, diaree, slăbire progresivă, tulburări nervoase şi moarte după 3-4 zile de boală în proporţie de până la 25% din efectiv. Pe măsura înaintării în vârstă, sensibilitatea la infecţia piocianică se reduce simţitor, iar simptomele mai evidente sunt cele digestive: diaree cu fecale galben-deschis la culoare la debut, apoi cu nuanţe verzi-albăstrui sau albastru, albastru-brun.
La psitacinele adulte, boala se manifestă mai ales prin tulburări digestive şi foarte rar prin semne nervoase. Păsările prezintă diaree cu fecale pigmentate, anorexie, anemie, imobilitate, caşexie, diminuarea constantă a capacităţii de mişcare sau chiar somnolenţă. Dacă nu se intervine, pot să apară manifestări nervoase cu tremurături ale extremităţilor, reducerea acuităţii vizuale şi auditive şi contracţii clonice ale membrelor. Evoluţia este cronică şi pot apărea simptome respiratorii (dispnee, pneumonie, aerosaculită) şi moarte în 1-2 săptămâni. În alte situaţii, la speciile de peruşi (în special peruşul ondulat, inseparabili şi peruşi nimfă), boala se manifestă prin abatere, tristeţe, anorexie, diaree cu fecale pigmentate verde intens, caşexie, iar la unii indivizi prin tulburări nervoase (convulsii, paralizii), boala cu evoluţie acută ducând la moarte în 24-48 de ore. Asocierile cu Pseudomonas fluorescens pot provoca apariţia de procese difteroide cu localizare bucală şi faringiană. La speciile de Rosella şi Pionites pot apărea manifestări atât de tip digestiv, cât şi respiratorii, ascită, diaree, iar în final necroze hepatice, evoluţia fiind cronică, mulţi indivizi murind după 7-10 zile.

Stabilirea diagnosticului infecţiei cu Pseudomonas spp. la păsări se face pe baza datelor anatomoclinice şi se confirmă prin examen bacteriologic. Diagnosticul clinic este dificil şi are valoare redusă. Formele septicemice de boală sunt greu de diagnosticat deoarece, în afara perturbării stării generale, păsările nu prezintă semne caracteristice. În general, diagnosticul clinic are în vedere următoarele elemente: prezenţa simptomelor digestive, diaree cu fecale pigmentate în galben-verde, cu irizaţii albăstrui, reducerea apetitului sau anorexie, slăbire progresivă, tulburări nervoase, anemie.
Diagnosticul anatomopatologic nu aduce prea multe date în plus. La tineretul îmbrăcat în penaj şi la psitacinele adulte se are în vedere aspectul verzui-albastru al conţinutului stomacal, intestinal şi uneori la cromatica verzuie a ficatului. Prezenţa lichidului ascitic şi modificările hepatice pot aduce suspiciunea de pseudomonoză. De asemenea, aerosaculita şi modificările pulmonare, asociate uneori cu depozite pe mucoasele respiratorii, pot reprezenta elemente care să atragă suspiciunea.
Diagnosticul de laborator se bazează pe examenul bacteriologic, care este singurul în măsură să stabilească un diagnostic de certitudine. Examenul bacterioscopic al materialelor patologice nu este util pentru diagnosticul etiologic, deoarece prezenţa unor cocobacili Gram-negativi chiar şi în frotiurile din sânge nu poate sugera decât existenţa unei infecţii bacteriene. Examenul histopatologic are valoare redusă întrucât nu poate evidenţia decât leziuni fără semnificaţie deosebită la nivelul stomacului glandular: îngroşarea stratului mucos, hiperplazia foliculilor glandulari şi descuamarea straturilor superficiale ale mucoasei. Culturile se fac din organe, îndeosebi din ficat, din intestin şi ingluviu, din sacul vitelin neresorbit, din pulmon, sinusuri şi măduva hematogenă. Examenul bacteriologic este numai aparent uşor, pentru că în realitate, în afara identificării ca atare a germenului, bacteriologul este pus adesea în faţa situaţiei dificile de a diferenţia tulpinile comensale de cele parazite. În cazurile în care creşte în cultură pură din exsudate şi lichide organice (hemocultură, exsudat pleural, auricular etc.) sau din măduvă osoasă, acest examen este cât se poate de semnificativ. În alte cazuri, cum ar fi cazul infecţiilor urinare şi intestinale, se obţin culturi mixte, îngreunându-se izolarea lui. Pentru izolare, mai ales în astfel de situaţii, se folosesc medii selective, ce conţin în compoziţia lor chimică substanţe ce inhibă dezvoltarea altor specii bacteriene. După identificarea certă a tulpinii de Pseudomonas aeruginosa izolată, urmează, în unele cazuri, cea mai dificilă problemă: aprecierea dacă tulpina respectivă aparţine tipului comensal sau celui patogen. În vederea acestei aprecieri, datele obţinute în laborator trebuie coroborate cu datele epizootologice, clinice şi anatomopatologice. Aprecierea unui anumit tip într-o anumită colectivitate este făcută prin lizotipie şi/sau serotipaj şi activitate piocianică.

Conduita terapeutică trebuie să includă antibioterapia sau chimioterapia. Comportarea acestor specii bacteriene faţă de acţiunea antibioticelor rămâne una din problemele mereu actuale în patologie şi în acest sens se dovedeşte rezistenţa naturală a bacteriei faţă de majoritatea antibioticelor disponibile, dobândirea relativ frecventă a rezistenţei la antibioticele faţă de care bacteria era iniţial sensibilă, precum şi toxicitatea ridicată a antibioticelor eficiente pentru organismul supus tratamentului. Activitatea antibioticelor faţă de Pseudomonas aeruginosa este în funcţie de capacitatea acestora de a penetra prin peretele celular, de rezistenţa la acţiunea inactivantă a enzimelor bacteriene şi de afinitatea antibioticului pentru anumite structuri ale celulei. La rândul său, Pseudomonas aeruginosa poate contracara acţiunea antibioticelor prin unul din următoarele mecanisme: elaborarea unor sisteme alternative care îl înlocuiesc sau substituie pe cel care este inhibat; reducerea activităţii enzimei-ţintă, care îşi păstrează structura normală şi substituirea activităţii ei prin alte rute metabolice; excluderea inhibitorului de la nivelul locurilor-ţintă prin reducerea permeabilităţii peretelui celular sau producerea unor macromolecule de suprafaţă; distrugerea antibioticului prin hidroliză şi substituirea unor grupuri chimice ale antibioticului. Rezistenţa speciei la acţiunea antibioticelor îşi are un corespondent genetic; în mod obişnuit, mai mult de 95% din informaţia genetică este conţinută în cromozomi şi numai între 1% şi 5% în plasmide. S-a constatat, de asemenea, că în general nu există o concordanţă deplină între sensibilitatea manifestată in vitro de Pseudomonas aeruginosa şi cea in vivo.
Clorinarea şi acidifierea apei, singure sau în asociere, reduc mult posibilitatea de contaminare pe cale bucală şi contribuie la reducerea stării de purtător. Acidifierea apei până la un pH de 2,5 şi clorinarea până la 10 ppm au fost folosite cu rezultate foarte bune, fără a se observa vreo influenţă negativă asupra păsărilor.
Ca mijloace specifice de profilaxie, se poate utiliza vaccinarea. Aceasta este posibilă, germenul fiind în măsură să confere o imunitate omologă destul de solidă faţă de tulpina utilizată la prepararea vaccinului. În condiţii de laborator s-a demonstrat posibilitatea obţinerii unei imunităţi faţă de tulpini înrudite serologic şi chiar slabă imunitate heterologă. Rezultatele cele mai bune au fost obţinute prin inocularea a trei doze de vaccin polivalent inactivat prin formol, urmată de inocularea unei doze de vaccin polivalent viu. În prezent, vaccinurile anti-Pseudomonas monovalente şi heptavalente sunt considerate cele mai bune, în special în spaţiile unde sunt cazate asociaţii de păsări (parcuri zoologice, crescătorii sau voliere mari). S-a demonstrat eficienţa vaccinului polivalent anti-Pseudomonas, preparat împotriva a 16 serotipuri de Pseudomonas aeruginosa, dar numai la păsări adulte, iar imunitatea nu se transferă pe verticală.
Conflict of interests: The author declares no conflict of interests.
Bibliografie
- Andriole VT. Pseudomonas bacteremia: Can antibiotic therapy improve survival? J Lab Clin Med. 1979; 94:196-200.
- Baltch AL, Griffh PE. Pseudomonas aeruginosa bacteremia: a clinical study of 75 birds. Am J Med Sci. 1997;274:119-120.
- Bodey GP Jadeja L, Elting L. Pseudomonas bacteremia. Retrospective analysis of 410 episodes. Arch Intern Med. 1985;145;1621-1629.
- Bross JE. Combination therapy versus monotherapy for Pseudomonas aeruginosa septicemia [Letter]. Am J Med. 1991;90:135.
- Flick MR, Cluff LE. Pseudomonas bacteremia. Review of 108 cases. Am J Med. 1976;60:501-508.
- Foldenauer U, Simova-Curd S, Nitzl D, Bogdanova A, Zollinger E, Hatt JM. Analysis of exhaled breath condensate in a mixed population of psittacine birds. Journal of Avian Medicine and Surgery, 2010; vol. 24, nr. 3, pp. 185-191.
- Hilf M, Yu VL, Sharp J, Zuravleff JJ, Korvick JA, Muder RR. Antibiotic therapy for Pseudomonas aeruginosa bacteremia: outcome correlation in a prospective study of 200 birds. Am J Med. 1989;87:540-546.
- Lechi A, Arosio E, Pancera P, et al. Pseudomonas septicaemia. A review of 60 cases observed in a veterinary hospital. J Hosp Infect. 1984;5:29-37.
- Pass DA, Perry RA. The pathology of psittacine beak and feather disease. Australian Veterinary Journal, 2008; vol. 61, nr. 3, pp. 69-74.
- Vidal F, Mensa J, Almela M, et al. Epidemiology and outcome of Pseudomonas aeruginosa bacteremia, with special emphasis on the influence on antibiotic treatment. Analysis of 189 episodes. Arch Intern Med. 1996; 156:2121-2126.
Articole din ediţiile anterioare
Carcinomul scuamocelular la pisică − diagnostic diferenţial şi abordare terapeutică multimodală
Carcinomul scuamocelular la pisică este o afecţiune care poate fi tratată dacă este diagnosticată precoce. Din acest considerent sunt extrem de imp...
Orientări clinico-terapeutice în patologia testudidelor de companie
În multe situații, creșterea în captivitate a unor specii de broaște țestoase nu se corelează cu necesitățile de hrănire și microclimat, conducând...
Update cu privire la tratamentul parvovirusurilor
Canine parvoviruses are non-enveloped DNA viruses which require rapidly divided cells to reproduce. Currently, most worldwide cases with clinical ...
Obiective în abordarea terapeutică a vomei la câine
Vomitarea este expulzarea conținutului gastric și/sau intestinal, prin mișcări coordonate ale componentelor gastrointestinale, ale sistemului nervo...