Organizarea activităţii în clinicile de alergologie în contextul pandemiei de COVID-19
Organizing the activity in allergology clinics in the context of the COVID-19 pandemic
Abstract
COVID-19 is the disease associated with severe acute respiratory syndrome 2 coronavirus (SARS-CoV-2). This is a new strain of coronavirus, which was first detected in humans in December 2019 in Wuhan, China. It spread rapidly around the world and was declared a pandemic by the World Health Organization (WHO) on March 11, 2020. SARS-CoV-2 is a contagious virus, social distancing being the key intervention in reducing its spread. Therefore, urgent changes to health care procedures, including the implementation of remote services, were needed in order to prevent the spread of the virus.Organizations such as EAACI or WAO have developed international recommendations on the reorganization of activity in allergy and immunology clinics. The main recommendations include the use of telemedicine, restricting clinical consultations to reduce face-to-face interactions, and delaying procedures, especially aerosol-generating ones. It is also recommended to continue the prescribed therapy for allergic diseases, including inhaled and oral corticosteroids or biological treatments.
Keywords
COVID-19allergy practicetelemedicineEAACI recommendationsRezumat
COVID-19 este boala asociată coronavirusului sindromului respirator acut sever 2 (SARS-CoV-2). Aceasta este o nouă tulpină de coronavirus, care a fost depistată la oameni pentru prima dată în decembrie 2019 în Wuhan, China. S-a răspândit rapid în întreaga lume şi a fost declarată pandemie de Organizaţia Mondială a Sănătăţii (OMS) la 11 martie 2020. SARS-CoV-2 este un virus contagios, distanţarea socială reprezentând intervenţia-cheie în reducerea răspândirii acestuia. Prin urmare, au fost necesare modificări urgente ale procedurilor de îngrijire a sănătăţii, inclusiv implementarea de servicii la distanţă, pentru a preveni răspândirea virusului.Organizaţii precum EAACI sau WAO au elaborat recomandări internaţionale cu privire la reorganizarea activităţii în clinicile de alergologie şi imunologie. Printre principalele recomandări se numără utilizarea telemedicinei, restricţionarea consulturilor în clinică pentru a reduce interacţiunile faţă în faţă şi întârzierea unor proceduri, în special a celor generatoare de aerosoli. De asemenea, se recomandă continuarea terapiei prescrise pentru bolile alergice, inclusiv a corticosteroizilor inhalatori şi orali sau a tratamentelor biologice.
Cuvinte Cheie
COVID-19alergologietelemedicinărecomandări EAACIIntroducere
Clinicile de alergologie şi imunologie au fost nevoite să se supună unor modificări în practica de zi cu zi, conform recomandărilor Academiei Europene pentru Alergologie şi Imunologie Clinică (EAACI), în contextul pandemiei de COVID‑19, încercând să asigure siguranţa personalului medical şi a pacienţilor, fără a scădea calitatea actului medical. În prezent există date limitate cu privire la implementarea acestor măsuri în clinicile de alergologie în România. O mai bună informare cu privire la aceste recomandări şi înţelegerea raţionamentelor pe care se bazează acestea vor ajuta la implementarea unui plan standardizat de activitate în clinicile de alergologie, care ar putea fi utilizat şi în contextul altor evenimente similare locale sau globale.
COVID‑19: evoluţie clinică la pacienţii alergici
Coronavirusurile – la fel ca alte virusuri cu tropism la nivelul mucoasei respiratorii, precum rinovirusurile sau virusul sinciţial respirator – se pot asocia cu agravarea exacerbărilor astmului prin stimularea producţiei de citokine de tip 2 în celulele epiteliale infectate (Gaspar-Marques et al., 2021). O altă caracteristică a bolilor alergice este că acestea pot predispune la infecţii virale sau la un clearance viral deficitar din cauza producţiei întârziate şi deficitare a interferonului de tip I şi III şi/sau a afectării funcţiei barierei epiteliale prin leziuni induse viral.
Până în prezent sunt disponibile cunoştinţe limitate cu privire la evoluţia infecţiilor cu SARS-CoV‑2 la pacienţii alergici comparativ cu cei nonalergici. Trei studii din Wuhan, China, au raportat boli alergice (astm, rinită alergică, dermatită atopică, urticarie sau hipersensibilitate la medicamente) printre comorbidităţile pacienţilor cu COVID‑19 (Pfaar et al., 2021). Pe de altă parte, într-un studiu din Lombardia, Italia, care a inclus peste 1500 de pacienţi, 13% dintre pacienţii cu COVID‑19 internaţi la terapie intensivă au avut astm. În niciunul dintre aceste studii nu s-a raportat o evoluţie prelungită sau agravată a bolii la pacienţii cu boli alergice, comparativ cu cazurile nonalergice incluse. În SUA s-au constatat prevalenţe mai crescute ale astmului la pacienţii adulţi spitalizaţi cu COVID‑19, în special la cei cu vârste cuprinse între 18 şi 49 de ani. Cu toate acestea, nu au fost disponibile informaţii cu privire la etiologia alergică sau nealergică a acestuia (Lombardi et al., 2021). Un raport preliminar recent a sugerat scăderea nivelurilor receptorilor ACE-2 în inflamaţia de tip 2, care ar putea arunca o nouă lumină asupra rolului imunităţii de tip 2 în infecţiile cu SARS‑CoV‑2 şi evoluţia COVID‑19. Cu toate acestea, sunt necesare mai multe dovezi ştiinţifice pentru a răspunde la întrebarea dacă bolile alergice sau tratamentul bolilor alergice ar putea predispune pacienţii la dezvoltarea COVID‑19 şi la o evoluţie mai gravă a bolii (Pfaar et al., 2021).
Consideraţii specifice în gestionarea diferitelor boli alergice
Simptomele tipice ale COVID‑19 includ stare generală de rău, febră, probleme respiratorii, în special tuse şi dispnee. Acestea prezintă atât similitudini, cât şi deosebiri faţă de rinita alergică, astmul alergic, gripă şi virozele comune (figura 1).
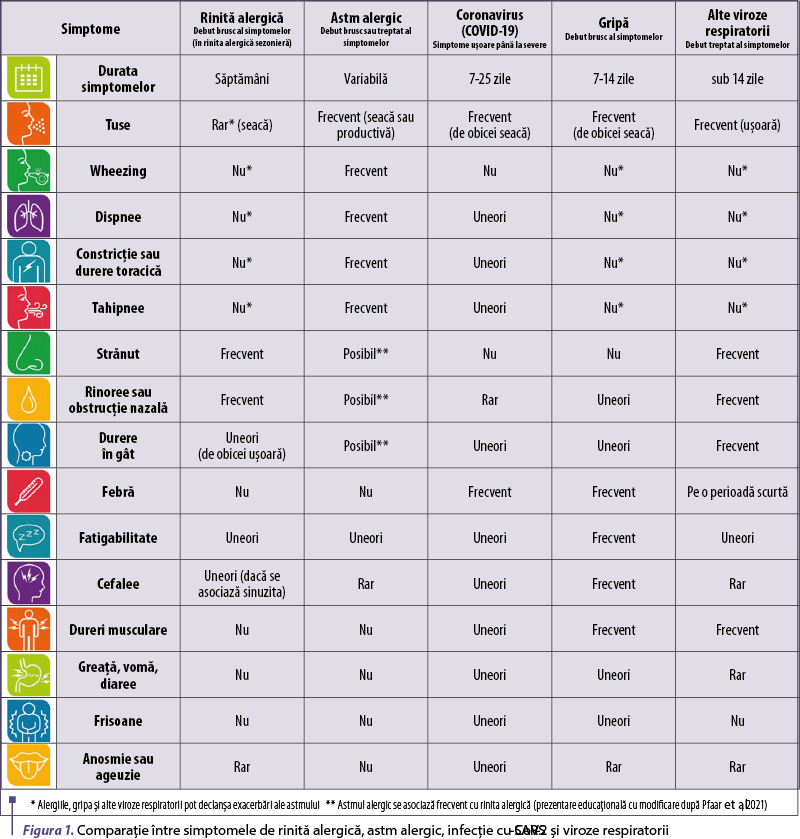
Potrivit OMS, pacienţii cu risc de a dezvolta COVID‑19 sau cu COVID‑19 diagnosticat ar trebui să îşi continue tratamentul pentru orice altă boală (aceasta include şi boala alergică), în conformitate cu recomandările specifice actuale. O atenţie specială ar trebui acordată interferenţei medicamentelor cu COVID‑19 sau invers. În general, se recomandă ca pacienţii să aibă o cantitate de medicamente suficientă pentru cel puţin 14 zile de carantină. În cazul în care sunt puse în aplicare măsuri mai stricte sau pentru perioade mai lungi de izolare, trebuie luată în considerare disponibilitatea medicamentelor şi potenţialii înlocuitori ai tratamentelor actuale, în cazul în care nu se pot obţine anumite medicamente. Pacienţii ar trebui să aibă un plan de acţiune pentru a se asigura că aceste probleme sunt acoperite.
Telemedicina s-a dovedit a fi utilă, dar nu poate înlocui toate consultaţiile în persoană, în special cele obligatorii pentru administrarea imunoterapiei alergenice subcutanate. Cu toate acestea, înainte de consultarea faţă în faţă pot fi clarificate printr-o consultaţie de telemedicină întrebările care identifică contraindicaţii ale terapiei. Multe dintre substanţele biologice utilizate pentru tratamentul bolilor alergice (de exemplu, omalizumab, benralizumab, mepolizumab şi dupilumab) sunt înregistrate pentru autoadministrare dacă pacienţii sunt instruiţi în mod adecvat privind tehnica de injectare şi în evaluarea şi gestionarea efectelor secundare. În timpul vizitelor de telemedicină, tehnicile de injecţie pot fi reverificate şi se poate răspunde la întrebările pacienţilor cu privire la tratament. De asemenea, pot fi discutate rezultatele testelor funcţionale pulmonare şi managementul controlului bolii, iar tratamentele pot fi adaptate.
Pacienţii pot fi instruiţi şi cu privire la măsurile de evitare a alergenelor şi la modalităţile de tratament. Aceştia pot arăta medicamentele pe care le au la domiciliu şi pot fi instruiţi cu privire la tehnicile de utilizare a inhalatoarelor şi a spray-urilor nazale. Pacienţii care suferă de anafilaxie pot fi instruiţi în utilizarea autoinjectoarelor cu adrenalină. Toate aceste informaţii cresc siguranţa şi pot îmbunătăţi şi calitatea vieţii pacientului.
Ca regulă generală, pacienţii cu boală alergică severă care se află pe terapii biologice şi au infecţie cu SARS‑CoV‑2 ar trebui să le întrerupă. Administrarea terapiei biologice trebuie reiniţiată după rezoluţia infecţiei cu SARS‑CoV‑2. Managementul adecvat şi tratamentul de fond al bolii alergice (corticosteroizi inhalatori sau alte medicamente) trebuie continuate conform prescrierii.
Rinoconjunctivita alergică (RA)
Există cunoştinţe limitate despre relaţia dintre susceptibilitatea la infecţia cu SARS‑CoV‑2, riscul de dezvoltare a formelor severe de COVID‑19 şi RA. S-a demonstrat că expresia ACE2, receptorul SARS‑CoV‑2, în celulele epiteliale nazale este mai scăzută la pacienţii cu RA şi astm alergic decât la persoanele sănătoase (Qiu et al., 2021). Se consideră că probabil RA nu creşte susceptibilitatea de a dezvolta COVID‑19 şi nici riscul de a dezvolta forme severe, dar sunt necesare mai multe studii pentru confirmarea acestor observaţii (Suzaki et al., 2021).
S-a raportat iniţial că „preparatele corticosteroide” aplicate local (corticosteroizi intranazali) pot creşte riscul de a dezvolta COVID‑19 sau pot provoca o evoluţie mai severă a bolii. Această opinie a îngrijorat numeroşi pacienţi care suferă de RA, rinosinuzită cronică sau astm (Lombardi et al., 2021). Protocolul actual al ARIA şi EAACI privind tratamentul rinitei alergice afirmă că INCS reprezintă standardul terapeutic pentru tratamentul RA, indiferent de simptome şi inflamaţii. În dozele aprobate, INCS nu creşte riscul de infecţie cu SARS‑CoV‑2 şi nici nu declanşează o evoluţie mai severă a COVID‑19. Reducerea inflamaţiei alergice a mucoasei prin INCS poate chiar să scurteze durata şi să scadă severitatea simptomelor în infecţiile virale ale tractului respirator superior la pacienţii cu RA, dar pare să nu aibă efecte marcante asupra simptomelor virozelor comune la pacienţii fără RA (Qiu et al., 2021). Prin urmare, se recomandă ca pacienţii cu RA să continue utilizarea regulată a INCS în doza prescrisă individual şi nu se recomandă ca aceştia să schimbe sau chiar să oprească tratamentul fără a consulta medicul. Întreruperea INCS poate agrava simptomele RA, inducând rinoree crescută şi strănut, ceea ce poate favoriza transmiterea virală a picăturilor de la pacienţii infectaţi cu SARS‑CoV‑2 la persoanele sănătoase. În plus, agravarea RA poate declanşa o exacerbare a astmului, care este considerat factor de risc pentru evoluţia severă a COVID‑19. Corticosteroizii sistemici în general au mai multe efecte adverse dacă se administrează pe termen lung. Pentru RA, aceştia ar trebui utilizaţi cu mai multă precauţie în timpul pandemiei actuale de COVID‑19 şi numai când nu sunt disponibile alternative terapeutice, din cauza riscului de imunosupresie temporară, care ar creşte riscul de a contracta o infecţie cu SARS‑CoV‑2 sau de progresie la boală severă.
Astmul alergic
Până în prezent, există foarte puţine informaţii disponibile cu privire la pacienţii cu astm şi COVID‑19. În general, s-a demonstrat că virusurile, inclusiv rinovirusurile şi virusurile sinciţiale respiratorii, induc episoade de astm sau exacerbări. Infecţiile şi colonizarea bacteriană au fost, de asemenea, asociate cu exacerbarea şi wheezingul, efecte care pot fi independente sau un cofactori cu virusurile. În plus, anumiţi indivizi pot avea o predispoziţie genetică spre wheezing indus viral şi spre dezvoltarea astmului. Rămâne de văzut dacă acest lucru se aplică şi infecţiei cu SARS‑CoV‑2. Cu toate acestea, bolile alergice ale căilor respiratorii, inclusiv astmul, nu par să reprezinte un factor de risc pentru COVID‑19 sau pentru o evoluţie clinică severă (Hosoki et al., 2020); cu toate acestea, contribuţia sa efectivă la risc poate depinde de prezenţa altor factori de mediu şi de comportament (de exemplu, fumatul, comorbidităţile), de tipul şi severitatea astmului (de exemplu, fenotipuri de astm non-tip 2, astm necontrolat), de tratamentele pentru astm şi de respectarea terapiei. Pacienţii imunocompromişi – inclusiv persoanele în vârstă, cei cu diabet zaharat sau cei sub corticoterapie sistemică – pot prezenta un risc crescut de infecţie şi o evoluţie mai severă a COVID‑19 (Lombardi et al., 2021).
Controlul optim al bolii este prima apărare împotriva factorilor declanşatori ai exacerbărilor astmului. Terapia de întreţinere cu bronhodilatatoare şi corticosteroizi inhalatori nu trebuie oprită în timpul pandemiei COVID‑19. Întreruperea tratamentului poate induce un risc crescut de agravare a simptomelor astmului şi exacerbări acute ale căilor respiratorii. În plus, riscul ca astmul să se deterioreze într-o manieră ameninţătoare şi să necesite vizite neprogramate la medic sau internări – potenţial responsabile pentru contactul cu pacienţii cu COVID‑19 – este mult mai periculos pentru pacienţii astmatici decât un posibil risc crescut de infecţie cu SARS‑CoV‑2 datorată unei imunodepresii teoretice locale induse de corticosteroizii inhalatori. Având în vedere lipsa dovezilor că aceştia afectează negativ evoluţia COVID‑19, experţii şi societăţile profesionale din domeniul respirator şi alergologic – inclusiv Global Initiative for Asthma (GINA), Academia Americană de Alergie, Astm şi Imunologie (AAAAI), Societatea Respiratorie Europeană (ERS) şi EAACI – subliniază importanţa controlului bolilor.
În afară de măsurile de evitare aplicabile în general, emise de guverne, societăţile recomandă ca pacienţii să continue administrarea medicamentelor care conţin corticosteroizi şi alte terapii de întreţinere (inclusiv terapii biologice), aşa cum este detaliat în planul lor personal de astm, şi să solicite ajutor medical în cazul deteriorării controlului bolii (Hosoki et al., 2020). O întrerupere a substanţelor biologice poate duce la o înrăutăţire a bolii de bază, care, la rândul său, ar putea avea un impact negativ asupra evoluţiei unei infecţii cu SARS‑CoV‑2. Exacerbările astmului cauzate de virusuri apar mai rar sau sunt mai puţin severe sub tratament biologic, aşa cum s-a demonstrat pentru omalizumab, dar nu există suficiente informaţii în contextul COVID‑19. Cu toate acestea, când este autorizată de organismele internaţionale de reglementare (de exemplu, Agenţia Europeană pentru Medicamente şi Administraţia SUA pentru Alimente şi Medicamente – FDA), autoadministrarea trebuie întotdeauna recomandată pentru a reduce expunerea la medii cu risc ridicat, cum ar fi spitalele şi clinicile. În absenţa terapiei biologice, pacienţilor, în special celor cu astm sever, ar trebui să li se recomande corticoterapia sistemică, cu toate că acest lucru poate avea efecte negative asupra apărării imune împotriva SARS‑CoV‑2. Aceste recomandări se aplică atât adulţilor, cât şi copiilor cu boli inflamatorii cronice ale căilor respiratorii, precum şi celor cu COVID‑19 sau cu suspiciunea de a avea infecţia. Contactul cu furnizorii de servicii medicale ar trebui să fie digital cât mai mult posibil.
Rinosinuzita cronică
Simptome ca obstrucţia nazală, rinoreea, presiunea facială şi anosmia sau hiposmia apar regulat în rinosinuzita cronică. Tratamentul acesteia se bazează pe corticosteroizi intranazali, corticosteroizi sistemici sau terapii antiinflamatorii specifice, orientate pe endotipul T2, în funcţie de severitatea bolii. Terapia cu corticosteroizi intranazali nu se întrerupe nici de către pacienţii infectaţi cu SARS‑CoV‑2. Tratamentele chirurgicale trebuie reduse la minimum, fiind indicate doar pacienţilor cu complicaţii locale şi celor pentru care nu există alte opţiuni de tratament. Corticosteroizii sistemici trebuie evitaţi pe cât posibil (Lee et al., 2021).
Dermatita atopică
Se recomandă continuarea tratamentului imunomodulator în dermatita atopică, deoarece exacerbările bolilor subiacente pot avea un impact negativ puternic asupra pacientului. Tratamentul cu imunosupresoare sistemice convenţionale precum ciclosporina poate interacţiona cu mecanismele de apărare împotriva bolilor virale, în timp ce dupilumab, care este înregistrat în multe ţări pentru tratamentul dermatitei atopice moderate până la severe, modulează selectiv inflamaţia de tip 2 şi, în general, nu este considerat a creşte riscul de infecţii virale. Se recomandă o procedură igienică atentă de spălare şi dezinfectare a mâinilor cu săpunuri neiritante, urmată de aplicarea de creme emoliente. În cazul pacienţilor cu dermatită atopică cu COVID‑19, este necesară efectuarea unui consult interdisciplinar de evaluare a acestora şi, în conformitate cu recomandările actuale privind infecţiile active şi terapia sistemică, terapia imunomodulatoare poate fi sau nu întreruptă (Miodońska et al., 2021). Dacă tratamentul sistemic este întrerupt, este importantă optimizarea tratamentului topic.
Urticaria
Infecţiile virale reprezintă un potenţial factor declanşator – şi uneori principalul agent etiologic – în urticaria acută sau cronică. Manifestările cutanate legate de infecţia cu SARS‑CoV‑2 sunt similare cu cele care apar în timpul infecţiilor virale obişnuite. Ca o consecinţă a acestor observaţii, urticaria acută ar putea fi o indicaţie pentru testarea pentru SARS‑CoV‑2 (Kaplona et al., 2021). Conform recomandărilor, antihistaminicele H1 de a doua generaţie stau la baza tratamentului urticariei şi trebuie continuate în timpul pandemiei. Dacă urticaria nu poate fi controlată cu antihistaminice în doze de patru ori mai mari decât cele din prospect, omalizumab este recomandat ca tratament suplimentar. Omalizumab este înregistrat pentru autoadministrare după ce pacienţii au fost instruiţi cu privire la tehnica injectării şi la evaluarea efectelor secundare alergice (Cruz-Teran et al., 2021). Doar primele două injecţii trebuie administrate în spital, din cauza riscului de anafilaxie. Prin urmare, mai ales în timpul pandemiei de COVID‑19, tratamentul la domiciliu este de preferat.
Vaccinarea anti-COVID‑19 la pacienţii cu boli alergice
Pe baza datelor din studiile actualizate, se poate concluziona că pentru pacienţii cu boli alergice (de exemplu, rinoconjunctivită alergică, astm alergic, alergii alimentare, alergii la veninul de insecte, alergii la medicamente) nu există o probabilitate crescută de reacţie anafilactică după vaccinarea anti-COVID‑19 (Hosoki et al., 2020). O treime din cazurile cu reacţii alergice observate nu prezintă istoric alergic. Majoritatea cazurilor în care reacţiile au avut loc în câteva minute după vaccinare au fost diagnosticate ca reacţii nonimunologice (cum ar fi sincopa vasovagală) (Sharma et al., 2020).
Pacienţii cu anafilaxie anterioară la vaccinare, anafilaxie idiopatică cunoscută, mastocitoză sistemică diagnosticată sau cu alergii confirmate la o mare varietate de medicamente din diferite clase pot fi observaţi o durată mai lungă postvaccinare (Varghese et al., 2021). Centrele de vaccinare ar trebui să fie echipate cu personal medical care poate administra tratament de urgenţă pentru reacţii potenţial severe. Medicamentele de urgenţă, inclusiv autoinjectoarele cu adrenalină, şi echipamentele de perfuzie şi intubaţie trebuie păstrate la îndemână, iar personalul trebuie instruit în resuscitare (Sampath et al., 2021).
Pacienţii care se află sub terapie antialergică (antihistaminice, antagonişti ai leucotrienelor, corticosteroizi topici şi sistemici), cei care se află sub imunoterapie alergenică sau cei care primesc terapie cu substanţe biologice pentru boala alergică (de exemplu, omalizumab, dupilumab, benralizumab, mepolizumab, reslizumab, reslizumab) pot fi vaccinaţi. În general, se recomandă ca imunoterapia alergenică subcutanată şi terapiile biologice să fie administrate cu una până la două săptămâni înainte sau după vaccinarea anti-COVID‑19. Imunoterapia alergenică sublinguală poate continua să fie luată ca de obicei, posibil cu o pauză în ziua vaccinării anti-COVID‑19 şi, eventual, una până la două zile după aceea, pentru a distinge posibilele reacţii adverse legate de vaccin de reacţiile la imunoterapie.
Conform cunoştinţelor actuale, reacţiile alergice sau anafilactice la noile vaccinuri COVID‑19 sunt foarte rare, dar de până la aproximativ zece ori mai frecvente decât la vaccinurile convenţionale (Shavit et al., 2021). Pacienţii cu atopii cunoscute şi boli alergice nu prezintă un risc crescut de reacţie alergică la vaccinare. Nanoparticulele lipidice din vaccinurile ARN (vaccinurile Pfizer şi Moderna) şi, în special, PEG conţinute în acestea sunt suspectate ca agent declanşator al reacţiilor de hipersensibilitate (Altrichter et al., 2021). În vaccinurile cu vectori virali (vaccinurile AstraZeneca şi Johnson & Johnson), polisorbatul 80 este un posibil alergen. Din păcate, procedurile de testare care permit predicţia reacţiilor de intoleranţă (pseudo-) alergică la vaccinările anti‑COVID‑19 sau le exclud sunt disponibile doar într-o măsură foarte limitată (Sampath et al., 2021).
Consideraţii sociopsihologice pentru pacienţii alergici şi îngrijirea optimă în timpul şi după pandemie
Răspunsurile alergice sunt afectate de factori psihologici precum stresul şi anxietatea şi pot fi modulate prin alte intervenţii decât terapia convenţională cu medicamente. Aceste mecanisme psihologice joacă un rol important în dezvoltarea, exacerbarea şi percepţia simptomelor. Reacţiile negative ale altor persoane la pacienţii care prezintă simptome respiratorii alergice în timpul pandemiei de COVID‑19 sunt amplificate. Aceste reacţii, împreună cu reglementările guvernamentale (de exemplu, distanţarea socială) pentru tratarea pandemiei, induc o stigmatizare suplimentară şi sporesc astfel stresul psihosocial pentru pacienţii alergici (Asselah et al., 2021).
Dezvoltarea simptomelor şi percepţia simptomelor sunt provocate doar parţial de mecanismele biologice ale alergiei şi mulţi pacienţi raportează simptome somatice care sunt dezvoltate în principal prin efecte psihologice (efecte nocebo). Mecanismele psihologice relevante pentru dezvoltarea simptomelor includ: aşteptări negative, creşterea autoobservării reacţiilor somatice, percepţia catastrofală a simptomelor (evaluare disfuncţională), precum şi temeri şi afectare negativă. Pentru mulţi pacienţi (şi, uneori, chiar şi pentru medicul lor), simptomele raportate sunt un conglomerat de potenţiale simptome alergice, potenţiale simptome ale COVID‑19 şi alte temeri care sunt aproape imposibil de separat. Aceste simptome nocebo pot fi prezente la până la 80% dintre pacienţii cu afecţiuni medicale (Owji et al., 2020).
În timpul pandemiei de COVID‑19, populaţia generală este extrem de sensibilă la percepţia persoanelor care prezintă simptome respiratorii. Acest lucru creşte riscul de stigmatizare a pacienţilor cu alergii, crescând în continuare stresul psihosocial al pacienţilor. Consecinţele neuroendocrine şi imunologice ale expunerii la stres sunt la rândul lor capabile să amplifice dezvoltarea simptomelor alergice. Efectele negative asupra disponibilităţii pacienţilor de a se expune acestor contacte (de exemplu, la locul de muncă, în reţelele sociale private) sunt în continuare consecinţe potenţiale cu impact negativ asupra condiţiilor de sănătate. Acest lucru este şi mai problematic, deoarece contactul social şi sprijinul social pot diminua efectele negative ale stresului şi pot reduce simptomele bolii.
Îngrijirea pacienţilor alergici: etapa preclinică şi trierea pacienţilor
Furnizarea nivelului adecvat de îngrijire medicală necesară pentru pacienţii cu boli alergice trebuie să se bazeze pe următoarele principii.
Amânarea consulturilor ambulatorii, care presupune:
evaluarea capacităţii şi a resurselor pacientului de a se adapta la monitorizarea la domiciliu;
selectarea pacienţilor care necesită consultaţie în persoană pe baza unor protocoale adecvate de screening (figura 2).
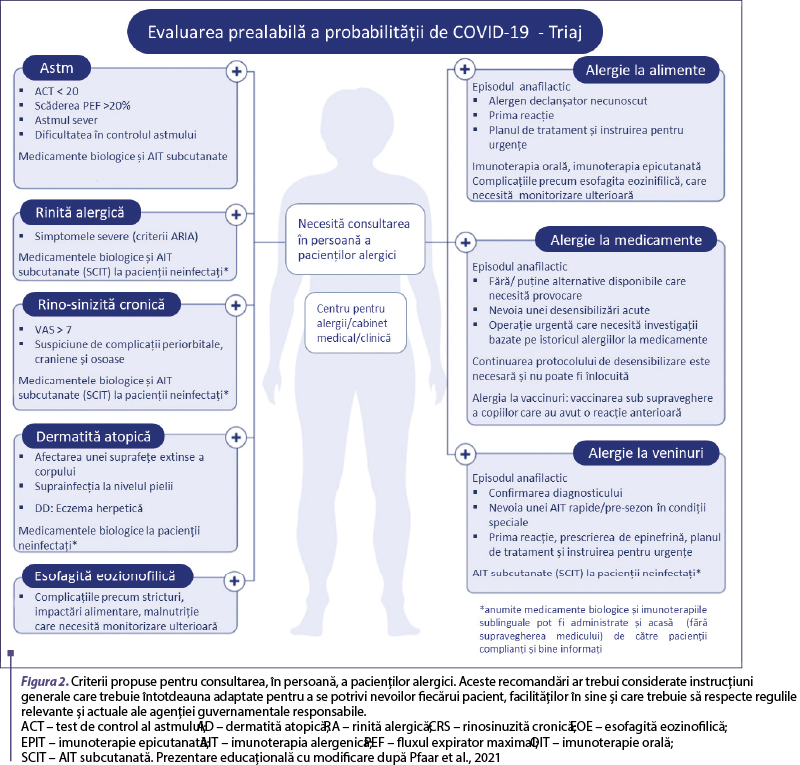
Reprogramarea oricăror proceduri neesenţiale care ar putea avea un impact asupra siguranţei pacientului şi a personalului medical (de exemplu, testarea funcţiei pulmonare, testele de provocare, rinoscopiile).
Implementarea instrumentelor de asistenţă medicală la distanţă (Waibel et al., 2019; Matricardi et al., 2020).
Multe clinici şi cabinete medicale folosesc deja aceste instrumente de îngrijire a sănătăţii la distanţă pentru triajul şi gestionarea pacienţilor ca parte a practicilor uzuale. Cu toate acestea, există mai multe proceduri de bază care trebuie luate în considerare. În primul rând, ar trebui identificat un număr suficient de furnizori de servicii medicale pentru a efectua interacţiuni telefonice şi de telesănătate cu pacienţii pentru a identifica simptomele de COVID‑19 (Asselah et al., 2021). De asemenea, trebuie diferenţiate simptomele de COVID‑19 de simptomele cauzate de virozele respiratorii comune, gripă, rinită alergică, rinosinuzită cronică şi astm alergic. În acest scop, telemedicina este un instrument util, dar ar trebui să fie furnizat de personal medical dedicat, respectând strict condiţiile generale ale tehnologiei informaţiei.
Triajul cazurilor urgente este extrem de important pentru a determina persoanele care au nevoie de proceduri de consultaţie şi diagnostic în persoană şi cele care pot fi gestionate eficient prin telemedicină sau programate pentru date ulterioare (Owji et al., 2020). Cu toate acestea, acest triaj important nu ar trebui să fie efectuat de un operator de centru de apel fără pregătire medicală. Cererile pentru testele alergologice in vivo trebuie evaluate individual de către medicii specialişti, pe baza efectuării unui istoric alergologic riguros. Tehnica documentării istoricului alergologic în telemedicină urmează principiile general acceptate ale conversaţiei medicale. Chestionarele standardizate şi validate pentru cuantificarea simptomelor pot facilita analiza istoricului; acestea pot fi completate de pacient înainte de consultarea prin telemedicină, documentându-se datele colectate şi facilitându-se evaluarea asistată de computer. Pacienţii cu o nevoie clară de consultare personală în clinică trebuie identificaţi, trimişi la clinică şi instruiţi cu privire la procedurile care trebuie urmate în clinică (Sharma et al., 2021).
În formele mai uşoare, pacienţilor trebuie să li se ofere soluţii alternative ori de câte ori este posibil pentru a evita orice riscuri inutile asociate cu o consultaţie din viaţa reală: de exemplu, livrarea de dispozitive electronice de monitorizare a inhalării, peak-flowmetre şi furnizarea de reţete pentru medicaţie. În special, pacienţii alergici cu simptome uşoare care frecventează în mod regulat ambulatoriul trebuie instruiţi să continue să-şi administreze medicamentele, inclusiv corticosteroizii inhalatori şi intranazali, imunoterapia alergenică şi terapiile biologice care vizează răspunsul imun T2, conform prescrierii (Suzaki et al., 2021). Ori de câte ori este posibil, administrarea la faţa locului în clinici a imunoterapiei şi a terapiilor biologice ar trebui înlocuită cu autoadministrarea la domiciliu, cu o monitorizare atentă, şi ar trebui furnizate suficiente medicamente pacienţilor. Organizaţiile comunitare locale şi serviciile de sănătate ar putea fi angajate pentru a ajuta pacienţii care sunt trataţi acasă şi care ar putea avea nevoie de servicii de sprijin pentru a asigura îngrijirea optimă. În plus, aceşti pacienţi ar trebui să fie bine instruiţi cu privire la măsurile de prevenire adecvate pentru controlul expunerii la alergene – de exemplu, folosind diferite aplicaţii, măsurători ale fluxului expirator maximal şi evitarea unor alimente (în special atunci când şi expedierilor online, în cazul în care nu este posibilă o selecţie individuală a alimentelor). Aceştia ar trebui, de asemenea, să fie motivaţi să îşi anunţe medicul curant sau medicul de familie în caz de exacerbare ori deteriorare a simptomelor care nu pot fi gestionate în mod adecvat acasă.
O atenţie specială trebuie acordată pacienţilor care se află în convalescenţă post-COVID‑19, mai ales în cazul formelor moderate sau severe de boală. Înainte de reînceperea administrării tratamentelor, care este posibil să fi fost întrerupte pe durata COVID‑19, inclusiv pe durata unei potenţiale spitalizări, este necesară evaluarea funcţiei pulmonare, cardiace, renale şi hepatice (figura 3).
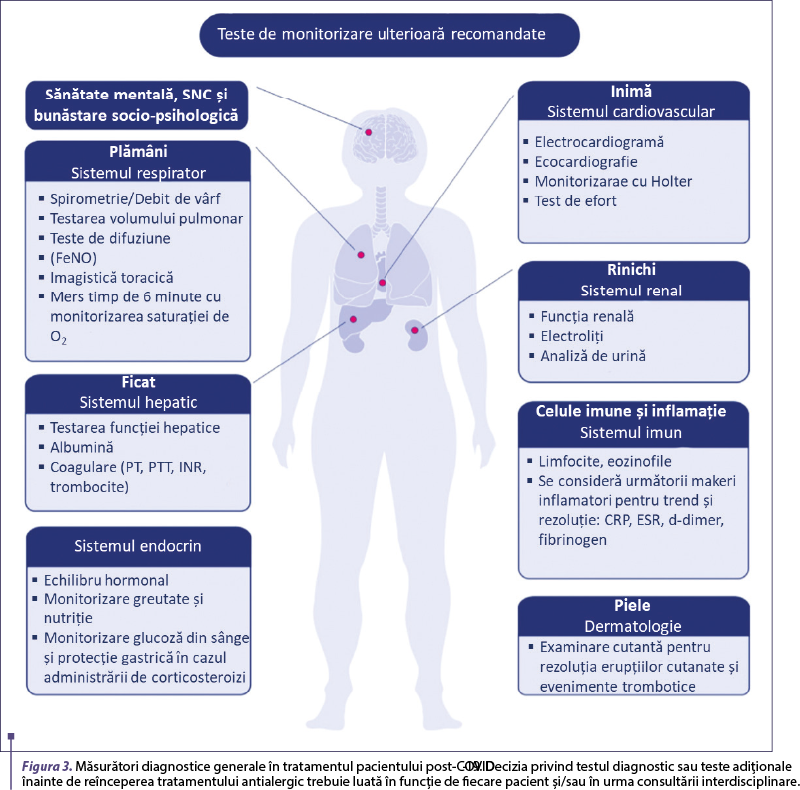
Consideraţii specifice pentru procedurile de diagnostic
la pacienţii alergici
Deoarece SARS‑CoV‑2 se răspândeşte în principal prin aerosoli respiratori, sunt afectate căile respiratorii, dar şi alte organe posibil afectate de alergie. Indicaţia şi urgenţa pentru proceduri de diagnostic în diferite boli alergice într-un cadru clinic în timpul pandemiei actuale ar trebui stabilite anterior, de exemplu printr-o vizită iniţială efectuată prin telemedicină. Acestea cuprind examenele ORL (inclusiv endoscopia), bronhoscopia, testele de provocare nazale şi bronşice, testele funcţiei pulmonare, testarea cutanată şi recoltarea probelor de sânge, testele de provocare la medicamente, provocările orale la alimente şi examenele esofagiene. În timpul vizitei iniţiale prin telemedicină pot fi clarificate contraindicaţiile pentru aceste teste, ceea ce poate ajuta la evitarea consultării inutile cu pacienţii în timpul pandemiei de COVID‑19.
Examinarea ORL şi testele
de provocare nazală
SARS‑CoV‑2 se răspândeşte în principal prin aerosoli respiratori şi s-au detectat încărcături virale mai mari în tampoanele nazale în comparaţie cu alte locuri (Sharma et al., 2021). Astfel, rinoscopia, endoscopia nazală, testele de provocare nazală, testarea mirosului şi gustului şi prelevarea de probe sunt proceduri cu risc ridicat (Van Gerven et al., 2020). Testele de provocare nazală trebuie evitate, în timp ce rinoscopia, endoscopia şi prelevarea de probe nazale trebuie limitate la pacienţii cu nevoie urgentă de examinare (Suzaki et al., 2021). Examinatorul trebuie să poarte echipamentul personal de protecţie adecvat: mască de faţă FFP2 sau FFP3, ochelari de protecţie sau scut de unică folosinţă care acoperă faţa şi părţile laterale ale feţei, mănuşi curate şi halat de izolare curat (Zou et al., 2020).
Testarea funcţiei pulmonare şi testele de bronhoprovocare
În timpul spirometriei, al testelor de bronhoprovocare, al măsurării oxidului nitric expirat fracţionat (FeNO) se pot genera aerosoli. Prin urmare, testarea de rutină a funcţiei pulmonare şi procedurile conexe trebuie suspendate în general în timpul pandemiei actuale (Pfaar et al., 2021). În caz de nevoie extremă, personalul trebuie să utilizeze echipament de protecţie individuală şi să respecte celelalte măsuri de siguranţă descrise anterior.
Testele cutanate şi recoltarea probelor de sânge pentru diagnostic
Testele cutanate ar trebui, în general, suspendate în timpul pandemiei actuale, deoarece presupun contact apropiat între medic şi pacient. Cu toate acestea, excepţiile pot fi luate în considerare după o evaluare atentă a raportului risc-beneficiu sau pot fi înlocuite cu teste de laborator. Când colectează probe biologice sau efectuează teste cutanate, personalul trebuie să utilizeze echipamentul personal de protecţie recomandat şi să respecte, de asemenea, măsurile de precauţie standard când manipulează probe clinice, toate acestea putând conţine materiale potenţial infecţioase. După colectare, probele trebuie plasate într-un recipient primar etanş şi introduse într-un ambalaj secundar etanş cu material absorbant. Acest pachet trebuie plasat într-un ambalaj exterior rigid cu etichetare adecvată. Prelucrarea probelor trebuie efectuată în conformitate cu practicile de nivel 2 de biosecuritate (BLS-2), standardul actual în laboratoarele clinice. Aerosolii pot proveni din centrifugare, pipetare, vortexare, amestecare, decantarea lichidelor, încărcarea şi vărsarea probelor sau curăţarea deversărilor. Suprafeţele şi echipamentele de lucru trebuie decontaminate în mod corespunzător, iar deşeurile de laborator ar trebui tratate ca agenţi periculoşi biologici. Inactivarea probelor de ser suspectate a fi contaminate cu SARS‑CoV‑2 trebuie efectuată urmând procedura recomandată de OMS pentru probele de ser (Pfaar et al., 2021).
Provocarea la medicamente
Tusea, strănutul sau rinoreea pot apărea în timpul testelor de provocare la medicamente. Prin urmare, aceste proceduri nu trebuie efectuate în general în timpul pandemiei actuale. Cu toate acestea, se pot lua în considerare excepţii după o evaluare adecvată a raportului risc-beneficiu, de exemplu chimioterapia la pacienţii oncologici, medicamentele perioperatorii sau mediile de radiocontrast la pacienţii care au nevoie de proceduri urgente sau antibioticele la persoanele infectate care nu primesc niciun alt medicament eficient (Aberer et al., 2003; Romano et al., 2020; Kowalski et al., 2019)
Provocarea orală la alimente şi examenul esofagian
Provocarea orală la alimente poate induce simptome respiratorii cu potenţial generator de aerosoli, împreună cu vărsături şi diaree. Important, virusul poate persista în lichide gastrointestinale pentru o perioadă mai lungă decât în probele respiratorii. Prin urmare, provocările la alimente pe cale orală ar trebui evitate în timpul pandemiei actuale, deoarece acestea nu sunt urgenţe. Diagnosticul de esofagită eozinofilă necesită o biopsie esofagiană ghidată de gastroscopie. Efectuarea unei gastroscopii nu este recomandată în timpul pandemiei actuale, din cauza posibilei persistenţe a virusului în fluidele biologice. În cazul unei nevoi extreme (de exemplu, impactarea frecventă a alimentelor), ar trebui efectuată o evaluare adecvată a raportului risc-beneficiu (Eiwegger et al., 2019; Chen et al., 2020; Pettersson et al., 2018).
Extinderea bruscă a pandemiei de COVID‑19 a impus modificări drastice ale practicii medicale, provocând dificultăţi în tratarea bolilor cronice pentru majoritatea pacienţilor. Deşi domeniul s-a adaptat pentru a rămâne operaţional în timpul acestei provocări semnificative, este important să se aplice lecţiile învăţate pentru a optimiza îngrijirile acordate pacienţilor, atât pe parcursul pandemiei, cât şi după terminarea acesteia.
Bibliografie
-
Aberer W, Bircher A, Romano A, et al. European Network for Drug Allergy (ENDA); EAACI interest group on drug hypersensitivity. Drug provocation testing in the diagnosis of drug hypersensitivity reactions: general considerations. Allergy. 2003;58(9):854-863. doi: 10.1034/j.1398-9995.2003.00279.x. PubMed PMID: 12911412
-
Altrichter S, Wöhrl S, Horak F, Idzko M, Jordakieva G, Untersmayr E, Szepfalusi Z, Zieglmayer P, Jensen-Jarolim E, Wiedermann U, Rosenkranz A. Answers to burning questions for clinical allergologists related to the new COVID-19 vaccines. Allergo Journal International. 2021 Jul 14:1-7. doi: 10.1007/s40629-021-00177-3. PubMed PMID: 34277326
-
Asselah T, Durantel D, Pasmant E, Lau G, SchinazI RF. COVID-19: Discovery, diagnostics and drug development. J Hepatol. 2021 Jan; 74(1): 168–184. doi: 10.1016/j.jhep.2020.09.031. PubMed PMID: 33038433
-
Chen Y, Chen L, Deng Q, et al. The presence of SARS-CoV-2 RNA in the feces of COVID-19 patients. J Med Virol. 2020;92(7):833-840. doi: 10.1002/jmv.25825. PubMed PMID: 32243607
-
Cruz-Teran C, Tiruthani K, McSweeney M, Ma A, Pickles R, Laia SK. Challenges and opportunities for antiviral monoclonal antibodies as COVID-19 therapy. Adv Drug Deliv Rev. 2021 Feb; 169: 100–117. doi: 10.1016/j.addr.2020.12.004. PubMed PMID: 33309815
-
Eiwegger T, Hung L, San Diego KE, O'Mahony L, Upton J. Recent developments and highlights in food allergy. Allergy. 2019;74(12):2355-2367. doi: 10.1111/all.14082. PubMed PMID: 31593325
-
Gaspar-Marques J, van Zeller M, Carreiro-Martins P, Chaves Loureiroe C. Severe asthma in the era of COVID-19: A narrative review. Pulmonology. 2021 Apr 30, doi: 10.1016/j.pulmoe.2021.04.001. PubMed PMID: 34053902
-
Hosoki K, Chakraborty A, Sur S. Molecular mechanisms and epidemiology of COVID-19 from an allergist’s perspective. J Allergy Clin Immunol. 2020 Aug; 146(2): 285–299. doi: 10.1016/j.jaci.2020.05.033. PubMed PMID: 32624257
-
Kaplona H, Reichert JM. Antibodies to watch in 2021. MAbs. 2021; 13(1): 1860476. doi: 10.1080/19420862.2020.1860476. PubMed PMID: 33459118
-
Kowalski ML, Agache I, Bavbek S, et al. Diagnosis and management of NSAID-Exacerbated Respiratory Disease (N-ERD)-a EAACI position paper. Allergy. 2019;74(1):28-39. doi: 10.1111/all.13599. PubMed PMID: 30216468
-
Lee SW, Kim SY, Yong Moon S, Yang, MD JM, Ha EK, Jee HM, Shin J, Cho SH, Yon DK, Suh DI. Estimating COVID-19 Infection and Severity Risks in Patients with Chronic Rhinosinusitis: A Korean Nationwide Cohort Study. J Allergy Clin Immunol Pract. 2021 Jun; 9(6): 2262–2271.e2. doi: 10.1016/j.jaip.2021.03.044. PubMed PMID: 33931377
-
Lombardi C, Gani F, Berti A, Comberiati P, Peroni D, Cottini M. Asthma and COVID-19: a dangerous liaison?. Asthma Research and Practice. 2021 Dec;7(1):1-4. doi: 10.1186/s40733-021-00075-z. PubMed PMID: 34261543
-
Matricardi PM, Dramburg S, Alvarez-Perea A, et al. The role of mobile health technologies in allergy care: An EAACI position paper. Allergy. 2020;75(2):259-272. doi: 10.1111/all.13953. PubMed PMID: 31230373
-
Miodońska M, Bogacz A, Mróz M, Mućka S, Bożek A. The Effect of SARS-CoV-2 Virus Infection on the Course of Atopic Dermatitis in Patients. Medicina (Kaunas). 2021 Jun; 57(6): 521. doi: 10.3390/medicina57060521. PubMed PMID: 34067403
-
Owji H, Negahdaripour M, Hajighahramanic N. Immunotherapeutic approaches to curtail COVID-19. Int Immunopharmacol. 2020 Nov; 88: 106924. doi: 10.1016/j.intimp.2020.106924. PubMed PMID: 32877828
-
Pettersson ME, Koppelman GH, Flokstra-de Blok BMJ, Kollen BJ, Dubois AEJ. Prediction of the severity of allergic reactions to foods. Allergy. 2018;73(7):1532-1540. doi: 10.1111/all.13423. PubMed PMID: 29380392
-
Pfaar O, Klimek L, Jutel M, Akdis CA, Bousquet J, Breiteneder H, Chinthrajah S, Diamant Z, Eiwegger T, Fokkens WJ, Fritsch HW. COVID‐19 pandemic: Practical considerations on the organization of an allergy clinic - An EAACI/ARIA Position Paper. Allergy. 2021 Mar;76(3):648-76. doi: 10.1111/all.14453. PubMed PMID: 32531110
-
Qiu H, Zheng R, Wang X, Chen Z, Feng P, Huang X, Zhou Y, Tao J, Dai M, Yuan L, Wang X, Zhang L, Yang Q. Using the Internet Big Data to Investigate the Epidemiological Characteristics of Allergic Rhinitis and Allergic Conjunctivitis. Risk Manag Healthc Policy. 2021; 14: 1833–1841. doi: 10.2147/RMHP.S307247. PubMed PMID: 33986620
-
Ramakrishna RK, Heialy SA, Hamid Q. Implications of preexisting asthma on COVID-19 pathogenesis. Am J Physiol Lung Cell Mol Physiol. 2021 May 1; 320(5): L880–L891. doi: 10.1152/ajplung.00547.2020. PubMed PMID: 33759572
-
Romano A, Atanaskovic-Markovic M, Barbaud A, et al. Towards a more precise diagnosis of hypersensitivity to beta-lactams – an EAACI position paper. Allergy. 2020;75(6):1300-1315. doi: 10.1111/all.14122. PubMed PMID: 31749148
-
Sampath V, Rabinowitz G, Shah M, Jain S, Diamant Z, Jesenak M, Rabin R, Vieths S, Agache I, Akdis M, Barber D. Vaccines and Allergic reactions: the past, the current COVID‐19 pandemic, and future perspectives. Allergy. 2021 Feb 9. doi: 10.1111/all.14840. PubMed PMID: 33811364
-
Sharma A, Farouk AA, Lal SK. COVID-19: A Review on the Novel Coronavirus Disease Evolution, Transmission, Detection, Control and Prevention. Viruses. 2021 Feb; 13(2): 202. doi: 10.3390/v13020202. PubMed PMID: 33572857
-
Sharma O, Sultan AA, Ding H, Triggle CR. A Review of the Progress and Challenges of Developing a Vaccine for COVID-19. Front Immunol. 2020; 11: 585354. doi: 10.3389/fimmu.2020.585354. PubMed PMID: 33163000
-
Shavit R, Maoz-Segal R, Iancovici-Kidon M, Offengenden I, Yahia SH, Maayan DM, Lifshitz-Tunitsky Y, Niznik S, Frizinsky S, Deutch M, Elbaz E. Prevalence of Allergic Reactions After Pfizer-BioNTech COVID-19 Vaccination Among Adults With High Allergy Risk. JAMA Network Open. 2021 Aug 2;4(8):e2122255-. doi: 10.1001/jamanetworkopen.2021.22255. PubMed PMID: 34463744
-
Suzaki I, Kobayashi H. Coronavirus Disease 2019 and Nasal Conditions: A Review of Current Evidence. In vivo. 2021 May 1;35(3):1409-17. doi: 10.21873/invivo.12393. PubMed PMID: 33910818
-
Van Gerven L, Hellings PW, Cox T, et al. Personal protection and delivery of rhinologic and endoscopic skull base procedures during the COVID-19 outbreak. Rhinology 2020;58(3):289-294. doi: 10.4193/Rhin20.119. PubMed PMID:
-
Varghese PM, Tsolaki AG, Yasmin H, Shastri A, Ferluga J, Vatish M, Madan T, Kishorea U. Host-pathogen interaction in COVID-19: Pathogenesis, potential therapeutics and vaccination strategies. Immunobiology. 2020 Nov; 225(6): 152008. doi: 10.1016/j.imbio.2020.152008. PubMed PMID: 33130519
-
Waibel KH, Bickel RA, Brown T. Outcomes From a Regional. Synchronous Tele-Allergy Service. J Allergy Clin Immunol Pract. 2019;7(3):1017-1021. doi: 10.1016/j.jaip.2018.10.026. PubMed PMID: 30385405
-
Zou L, Ruan F, Huang M, et al. SARS-CoV-2 Viral Load in Upper. Respiratory Specimens of Infected Patients. N Engl J Med. 2020;382(12):1177-1179. doi: 10.1056/NEJMc2001737. PubMed PMID: 32074444





