Creşterea incidenţei infecţiilor invazive cauzate de Streptococcus pyogenes în Europa
The increasing incidence of invasive infections caused by Streptococcus pyogenes in Europe
Abstract
At the end of the year 2022, it was reported in some European countries an increase in the incidence of invasive infection/disease caused by Streptococcus pyogenes (group A beta-hemolytic Streptococcus; GAS), especially in case of children younger than 10 years old, in which fatalities occurred. It is worth mentioning that the GAS strains isolated in these cases didn’t have special particularities, such as the emergence of a new strain, and an increase of GAS resistance to antibiotics wasn’t revealed, either. Through this article, we intend to issue a warning regarding the risks of invasive streptococcal infection, reviewing some important aspects on the etiology, diagnosis, treatment and prevention of these infections.Keywords
invasive streptococcal infection/diseaseStreptococcus pyogenes/group A beta-hemolytic StreptococcusRezumat
La sfârşitul anului 2022 a fost semnalată în câteva ţări din Europa o creştere a incidenţei bolii/infecţiei invazive cauzate de Streptococcus pyogenes (streptococul beta-hemolitic de grup A – SGA), cu deosebire în rândul copiilor cu vârsta sub 10 ani, la care s-au înregistrat şi decese. De subliniat faptul că tulpinile de SGA izolate la aceste cazuri nu au prezentat caractere speciale, în sensul apariţiei unei tulpini specifice sau noi şi nici nu s-a evidenţiat o creştere a rezistenţei la antibiotice a SGA. Prin acest articol, dorim să tragem un semnal de alarmă asupra riscurilor pe care le prezintă infecţiile streptococice invazive, trecând în revistă aspectele importante ale etiologiei, diagnosticului, tratamentului şi prevenirii acestora.Cuvinte Cheie
infecţie/boală invazivă streptococicăStreptococcus pyogenes/streptococ beta-hemolitic de grup AIntroducere
În decembrie 2022, Organizaţia Mondială a Sănătăţii (OMS) anunţa faptul că mai multe ţări europene, dintre care Franţa, Irlanda, Ţările de Jos, Spania, Suedia şi Regatul Unit, au raportat o creştere, în special din septembrie 2022, a numărului de cazuri de boală streptococică invazivă cauzată de Streptococcus pyogenes (streptococul beta-hemolitic de grup A – SGA), cu preponderenţă în rândul copiilor cu vârsta sub 10 ani, în această grupă de vârstă fiind raportate şi decese. În Franţa şi Regatul Unit s-a remarcat că numărul cazurilor de boală invazivă cauzată de SGA (SGAi), observată la copii, a fost de câteva ori mai mare comparativ cu nivelurile înregistrate în aceeaşi perioadă de dinainte de pandemie. În aceste ţări au mai fost semnalate, de asemenea, focare de scarlatină. Important de menţionat faptul că în aceeaşi perioadă a fost constatată şi o circulaţie timpurie crescută a virusurilor respiratorii, inclusiv virusul gripal sezonier şi virusul sinciţial respirator, dar şi virusul varicelic, ştiindu-se faptul că o eventuală coinfecţie virală-bacteriană (în cazul nostru, SGA) poate creşte riscul de apariţie a SGAi. În timpul pandemiei de COVID-19, incidenţa infecţiilor cu SGA (atât cele uşoare sau medii, cât şi cele severe sau invazive) a fost redusă, în perioada următoare, postpandemică, fiind raportată către OMS Europa şi Centrul European pentru Prevenirea şi Controlul Bolilor (ECDC) o creştere a incidenţei acestor infecţii. De remarcat faptul că infecţiile cu SGA, precum şi SGAi sunt boli notificabile doar într-un număr limitat de ţări europene. Astfel, este dificil de evaluat nivelul general de circulaţie al acestor infecţii în Regiunea Europeană. De asemenea, datele raportate sugerează faptul că creşterea cazurilor nu este legată de o tulpină specifică sau nouă şi nici de o creştere a rezistenţei la antibiotice a SGA. În aceste condiţii, OMS Europa şi ECDC evaluează în prezent un risc scăzut de SGAi pentru populaţia generală(1-5). Acest fenomen, semnalat în sezonul 2022-2023, ne-a determinat să facem o scurtă incursiune privind etiologia, aspectele clinice, diagnosticul şi tratamentul infecţiilor streptococice invazive, cu scopul de a creşte conştientizarea în rândul cadrelor medicale şi, pe această cale, şi al celor interesaţi şi, astfel, să se impună o supraveghere cât mai atentă a acestor afecţiuni, alături de instituirea măsurilor de prevenire şi protecţie.
Etiologie şi forme clinice ale infecţiilor cauzate de SGA
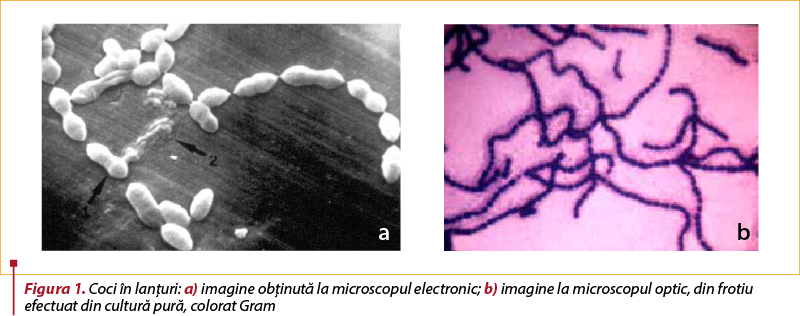
Agentul etiologic cel mai frecvent al bolii invazive streptococice este Streptococcus pyogenes sau streptococul de grup A (SGA) (conform sistemului de clasificare introdus de Rebeca Lancefield la începutul secolului XX, pe baza prezenţei antigenului specific de grup, polizaharidul C, din peretele celular)(6). Streptococii de grup A aparţin genului Streptococcus, familia Streptococcaceae, şi sunt germeni prin excelenţă patogeni pentru om. Sunt coci Gram-pozitivi, care cresc în lanţuri (figura 1). Pe mediile de cultură cu agar-sânge dezvoltă b-hemoliză (hemoliză completă) (figura 2), făcând parte din grupul streptococilor b-hemolitici, împreună cu streptococii de grup B, C şi G. Sunt imobili şi pretenţioşi nutritiv (au nevoie de medii de cultură bogat nutritive pentru dezvoltare).
SGA reprezintă cea mai frecventă cauză a faringitei bacteriene la copiii de vârstă şcolară. Infecţiile cu SGA provoacă, de obicei, afecţiuni uşoare/medii, precum: amigdalită, faringită, impetigo, celulită şi scarlatină. În Europa, incidenţa faringitei atinge, de obicei, vârfuri în lunile de iarnă şi la începutul primăverii, când sunt raportate frecvent focare în grădiniţe şi şcoli.
În cazuri rare, infecţia cu SGA poate conduce la afecţiuni severe – boala/infecţia invazivă cu SGA (SGAi), în anumite situaţii având o evoluţie fatală. Agentul etiologic al bolii invazive este izolat dintr-un situs al organismului – în mod normal steril (sânge, lichid cefalorahidian sau alte lichide ori fragmente de ţesuturi sau organe, obţinute prin aspirare sau printr-o procedură chirurgicală).
În cadrul SGAi sunt descrise trei mari sindroame clinice: i) fasciita necrozantă (FN); ii) sindromul de şoc toxic streptococic (SSTS); iii) infecţii caracterizate prin izolarea streptococului dintr-un situs normal steril la pacienţi care nu prezintă semne de SSTS sau FN. În acest grup sunt incluse bacteriemia fără un focar identificat sau bacteriemia cu un focar identificat, precum meningita, pneumonia, peritonita, osteomielita, artrita septică, febra puerperală, miozita, infecţii ale diferitelor răni etc(7).
Creşterea incidenţei bolii streptococice invazive, observată în Europa încă din septembrie 2022, poate fi explicată printr-un început timpuriu al sezonului de infecţii cu SGA, care coincide cu o creştere a circulaţiei virusurilor respiratorii şi cu o posibilă coinfecţie cauzată de un virus şi SGA. Copiii cu infecţii virale, în special varicela şi/sau gripa, prezintă un risc foarte mare de a dezvolta boala invazivă streptococică.
Transmitere
SGA se transmite de la un bolnav sau purtător (starea de purtător este definită de prezenţa streptococului la nivelul faringelui, fără a fi însoţit de manifestări clinice: febră, dureri în gât, stare generală modificată) la contacţii apropiaţi, prin tuse şi strănut, sau printr-o rană. Riscul de transmitere este mai mare în cazul bolnavilor decât al purtătorilor.
În cazul infecţiilor invazive, intrarea iniţială a SGA în organism poate avea loc pe mai multe căi. Boala poate apărea la pătrunderea bacteriei printr-o barieră compromisă (cum ar fi o leziune sau deteriorare a pielii – sunt prezentate frecvent aşa-zisele bătături cauzate cel mai adesea de încălţăminte, inclusiv răni chirurgicale), sau prin membranele mucoaselor faringiene ori vaginale. Din păcate, calea de intrare rămâne necunoscută în aproape 50% din cazuri. Bacteriile se răspândesc apoi în ţesuturile profunde şi, în cele din urmă, în fluxul sanguin.

Factori de risc pentru boala invazivă cu SGA
-
Riscul pentru SGAi este crescut în următoarele condiţii, legate de:
-
Vârsta gazdei, cei mai vulnerabili fiind cei din grupele de vârstă cu risc crescut (copiii mici şi vârstnicii).
-
Starea de sănătate a gazdei. Astfel, putem menţiona infecţia cu HIV, diabetul, diversele stări de malignitate, consumul de droguri injectabile şi alcool, tratamente imunosupresoare, bolile cardiace. Unele studii au sugerat o relaţie între medicamentele antiinflamatoare nesteroidiene (AINS) şi fasciita necrozantă(8). Se ştie că AINS afectează funcţia granulocitelor şi cresc producţia de citochine; în plus, aceste medicamente maschează semnele evoluţiei bolii (durerea, edemul, febra), întârziind diagnosticul, într-o fază mult avansată a infecţiei severe.
-
Factorii de mediu pot fi, de asemenea, asociaţi cu un risc crescut de boală invazivă streptococică. Astfel putem menţiona aglomerarea, care, măsurată prin numărul de persoane dintr-o casă, creşte riscul de îmbolnăvire în rândul adulţilor de peste 65 de ani. În aceste familii, copiii sunt cel mai probabil rezervoare de SGA pentru adulţi, transmiterea de la persoană la persoană fiind foarte facilă(9).
-
Varicela este, de asemenea, un factor de risc bine documentat în dezvoltarea bolii invazive cu SGA, în special în rândul copiilor, veziculele reprezentând o poartă de intrare a agentului patogen(10,11).
Patogenia bolii invazive cu SGA
Pe lângă proteina M, unul din factorii de virulenţă cei mai importanţi ai SGA, mai sunt descrise numeroase exotoxine streptococice pirogene, denumite şi superantigene, care au un rol important în patogenia infecţiilor severe cauzate de SGA. Producţia de către SGA a exotoxinelor şi factorilor de virulenţă în ţesuturile profunde şi în fluxul sanguin poate duce la inducerea cascadei de citochine, cu apariţia unui răspuns inflamator, contribuind la dezvoltarea şocului sau a insuficienţei organice. Astfel, au fost detectate niveluri ridicate ale citochinelor proinflamatorii în serul pacienţilor cu şoc septic şi s-a remarcat o corelaţie directă între răspunsul imun inflamator şi severitatea bolii. În infecţiile invazive severe, precum SSTS şi FN, au fost evidenţiate, cu o frecvenţă foarte mare, celulele producătoare de interleukine (IL-1ß, IL-2, IL-6) şi TNF-a (tumor necrosis factor), în comparaţie cu infecţiile mai puţin severe(12).
Manifestări clinice ale principalelor forme de boală invazivă cu SGA
I. Fasciita necrozantă (FN)
FN este o infecţie care progresează rapid, cu distrugerea ţesuturilor moi profunde, inclusiv fascia musculară şi grăsimea subcutanată. În cadrul acestei boli, SGA mai este cunoscut popular sub numele de „bacteria mâncătoare de carne”.
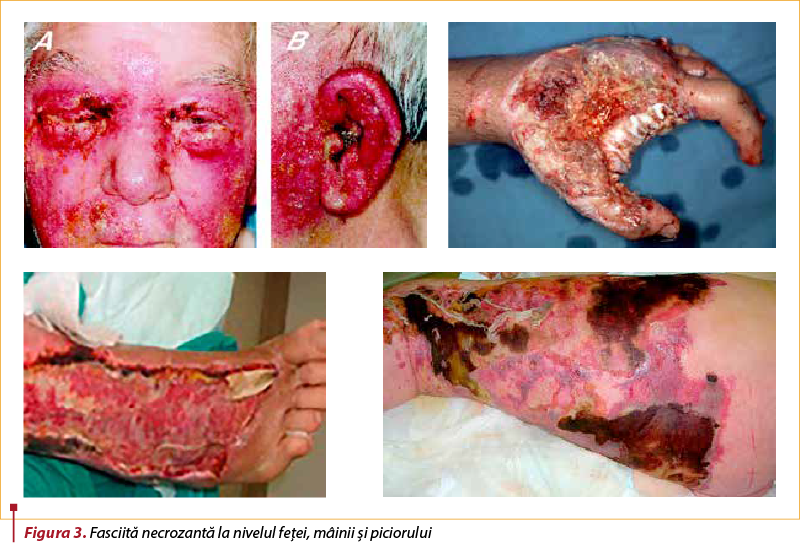
Această infecţie se poate dezvolta în orice zonă a corpului uman, dar cel mai frecvent la nivelul braţelor, picioarelor şi peretelui abdominal. Infecţia începe la nivelul unei leziuni cutanate, se dezvoltă în ţesuturile subcutanate şi se răspândeşte rapid de-a lungul planurilor fasciale (de exemplu, fascii musculare), determinând necroza ţesuturilor respective. FN începe cu o durere în zona afectată, însoţită de edem, eritem şi căldură. De obicei, durerea este disproporţionată cu semnele infecţiei cutanate locale: intensitatea durerii este foarte mare, nejustificată de aspectul relativ conservat al pielii de deasupra leziunilor subcutanate, cu absenţa limfadenitei şi limfangitei(13). Pe măsură ce se instalează cangrena, ţesuturile afectate îşi modifică progresiv culoarea de la roşu la violet, la albastru, apoi la negru. Se dezvoltă, de asemenea, ischemia cutanată; se formează bule umplute cu lichid de culoare galben pai, care se transformă progresiv în lichid hemoragic; la palparea zonei afectate, din cauza acumulării de gaze, se pot simţi crepitaţii. Pielea devine anesteziată din cauza distrugerii nervilor superficiali, apoi se desprinde, formându-se o escară necrotică, asemănătoare unei arsuri de gradul trei (figura 3).
Fasciita necrozantă este o afecţiune gravă, asociată adesea cu septicemie şi insuficienţă organică, reprezentând o urgenţă medicală, care, dacă nu este tratată prompt şi eficient, poate duce la deces (cu o rată de mortalitate între 11% şi 40% din cazuri) sau invaliditate (de multe ori necesită o debridare extinsă sau chiar amputări).
Diagnosticul fasciitei necrozante
-
Imagistica, respectiv tomografia computerizată (CT) sau rezonanţa magnetică nucleară (RMN), ne poate da informaţii utile încă de la începutul procesului, când durerea şi edemul sunt prezente fără modificări cutanate, putându-se detecta edem subcutanat şi fascial sau gaze tisulare.
-
Semnele clince: durere profundă, zone cu scăderea sensibilităţii, crepitaţii, bule, necroză a pielii.
-
Explorarea chirurgicală sau biopsia trebuie să se facă într-un stadiu cât mai timpuriu al bolii. Aceasta nu trebuie întârziată de explorarea imagistică.
-
Examenele de laborator, precum leucocitoza, trombocitopenia şi azotemia, sunt frecvente şi pot orienta rapid diagnosticul.
-
Coloraţia Gram şi cultura, realizate din lichidul de la nivelul leziunii şi ţesutul necrozat, ne pot da informaţii privind etiologia streptococică.
Tratamentul fasciitei necrozante
-
Se impune un tratament de urgenţă, care constă în:
-
Explorarea chirurgicală precoce şi agresivă, cu debridarea extensivă a ţesutului necrotic. Rana trebuie lăsată deschisă şi reinspectată după 24 de ore, pentru a asigura eliminarea adecvată a ţesutului necrotic.
-
Antibioterapia parenterală cu antibiotice cu spectru larg se va institui imediat. Odată cu confirmarea SGA ca agent etiologic, se va impune administrarea intravenoasă a unei asocieri de două antibiotice cu efect ţintit (a se vedea în continuare).
-
Imunoglobulina, administrată intravenos, poate fi luată în considerare în cazurile de FN severă, deşi eficacitatea nu a fost dovedită.
II. Sindromul de şoc toxic streptococic (SSTS)
Sindromul de şoc toxic streptococic este o boală definită ca o infecţie cauzată de Streptococcus pyogenes, care se caracterizează prin prezenţa şocului şi insuficienţă multiorganică, ce se instalează destul de repede în cursul bolii, iar rata de mortalitate poate depăşi 50% din cazuri.
Semnele clinice ale SSTS
SSTS începe adesea cu simptome asemănătoare cu ale gripei (febră, frisoane, mialgie, greaţă, vărsături), care progresează rapid spre septicemie – cu hipotensiune arterială, tahicardie, tahipnee, cu disfuncţia a cel puţin două organe, precum: insuficienţă renală, coagulopatie (prin scăderea trombocitelor), insuficienţă hepatică, sindrom de detresă respiratorie acută, erupţie eritematoasă generalizată cu descuamare, necroză tisulară, cu o rată crescută a letalităţii.
Diagnosticul SSTS
-
Se realizează pe baza:
-
semnelor clinice (amintite mai sus) şi
-
izolarea şi identificarea SGA prin culturi ale exsudatului faringian, culturi din puroi de la nivelul leziunilor cutanate şi/sau dintr-un situs în mod normal steril (de exemplu, sânge, LCR sau, mai puţin frecvent, lichid articular, pleural sau pericardic).
Tratamentul SSTS
-
Ca şi în cazul FN, tratamentul SSTS este unul de urgenţă:
-
Primul pas îl constituie tratamentul standard al şocului şi insuficienţei organice, cum ar fi resuscitarea cu lichide.
-
Terapia cu antibiotice este, de asemenea, esenţială şi trebuie introdusă rapid. Se recomandă, ca şi în cazul FN, administrarea intravenoasă a unei asocieri de două antibiotice cu acţiune ţintită pe agentul etiologic.
-
Unele studii au sugerat că tratamentul SSTS cu imunoglobuline administrate intravenos poate reduce rata mortalităţii. Explicaţia acestui fenomen ar fi faptul că imunoglobulinele administrate intravenos ar furniza anticorpi neutralizanţi sau protectori. S-a dovedit că plasma, recoltată de la pacienţii care au primit imunoglobuline intravenos, a inhibat producţia de citochine şi proliferarea celulelor T induse de superantigenele streptococice(14).
Antibioterapia în infecţiile invazive cu SGA
Trebuie subliniat faptul că toţi streptococii beta-hemolitici continuă să fie sensibili la penicilină (din fericire, nu a fost semnalată rezistenţa la beta-lactamine), deci tratamentul de elecţie în infecţiile streptococice este penicilina.
Pentru infecţiile invazive streptococice se recomandă asocierea a două antibiotice, cu administrare intravenoasă: o beta-lactamină (penicilină în principal, sau amoxicilină, ampicilină, ori o cefalosporină) şi un lincozamid (clindamicină) sau un glicopeptid (vancomicină).
La persoanele alergice la penicilină se recomandă înlocuirea beta-lactaminei cu un macrolid. Însă la macrolide sunt semnalate rate diferite de rezistenţă (aproximativ 5% pentru SGA), dar şi la clindamicină (aproximativ 1,5%), ceea ce impune, în aceste situaţii, testarea susceptibilităţii la aceste antibiotice(7,15-17).
Tratamentul cu antibiotice al infecţiilor invazive severe nu este întotdeauna eficient, depinzând şi de momentul administrării medicamentelor, rata mortalităţii putând fi crescută.
Prevenirea infecţiilor streptococice invazive
-
Presupune o serie de măsuri generale, dar şi specifice(18):
-
Măsuri generale de igienă (spălarea frecventă a mâinilor, izolarea la domiciliu, folosirea obiectelor proprii – săpun, prosoape, burete, cană etc., protejarea cu un şerveţel sau mânecă în timpul tusei ori strănutului). Şcolile şi alte unităţi educaţionale în care sunt raportate infecţii cu SGA ar trebui să urmeze instrucţiunile de curăţare şi dezinfecţie pentru obiecte şi suprafeţe atinse frecvent.
-
Alăptarea copiilor mici şi interzicerea fumatului de către persoanele de contact din casă pot fi măsuri preventive şi ar trebui încurajate.
-
În condiţiile actuale, OMS Europa şi ECDC recomandă o supraveghere mai atentă privind infecţiile streptococice, mai ales în perioadele când virusurile respiratorii circulă pe scară largă. În acest sens, trebuie sporită conştientizarea părinţilor asupra acestui risc: boala invazivă poate prezenta iniţial simptome nespecifice (febră, oboseală generală, pierderea poftei de mâncare), cu evoluţie rapidă spre o boală severă, în special la copii. Prin urmare, părinţii ar trebui să fie conştienţi de simptomele îngrijorătoare şi să solicite o evaluare clinică dacă starea de sănătate a copilului nu se îmbunătăţeşte.
-
Autorităţile de sănătate publică trebuie să se coordoneze cu laboratoarele pentru a obţine identificarea agentului patogen şi testarea sensibilităţii la antibiotice.
-
Nu există niciun vaccin streptococic de grup A; sunt cercetări în acest sens, dar prepararea unui vaccin s-a dovedit a fi foarte dificilă, din cauza existenţei a peste 120 de tipuri M ale tulpinilor de SGA circulante (clasificare realizată pe baza proteinei M – care stimulează producerea anticorpilor protectori) şi a dificultăţii de purificare a acestei proteine.
-
Ştiind că prevenirea bolilor virale poate fi foarte importantă în reducerea riscului de apariţie a bolii invazive streptococice, vaccinarea împotriva gripei sezoniere, a varicelei şi a COVID-19 ar trebui, de asemenea, promovată.
Concluzii
Infecţiile cu SGA şi SGAi sunt boli notificabile doar într-un număr limitat de ţări europene. Prin urmare, este dificil de evaluat în acest moment nivelul general de circulaţie în regiunea europeană.
Investigaţiile realizate în ţările europene, care au raportat creşterea incidenţei acestor boli, sugerează că în aceste cazuri nu a fost identificată o tulpină specifică sau nouă şi nu a fost detectată o creştere a rezistenţei la antibiotice a tulpinilor de Streptococcus pyogenes izolate.
Având în vedere faptul că creşterea actuală a cazurilor de SGAi este, în general, relativ scăzută, că aceste cazuri raportate nu sunt cauzate de o tulpină nouă şi că boala este uşor de tratat cu antibiotice, OMS Europa şi ECDC evaluează riscul prezentat de infecţia invazivă cu SGA ca fiind scăzut pentru populaţia generală. Însă, din cauza evoluţiei severe şi chiar fatale, se impune în continuare o supraveghere cât mai atentă a infecţiilor streptococice în general, alături de instituirea măsurilor de prevenire şi protecţie.
Conflict de interese: niciunul declarat
Suport financiar: niciunul declarat

Bibliografie
-
UK Health Security Agency. Group A streptococcal infections: report on seasonal activity in England, 2022 to 2023. Updated 12 January 2023.
-
Santé publique France. Invasive Group A Streptococcal Infection (IISGA). Update as of December 8, 2022.
-
Health Protection Surveillance Centre (hpsc.ie). News: Update on Group A streptococcus. Published: January 12, 2023.
-
WHO Europe (12 December 2022). Increase in invasive Group A streptococcal infections among children in Europe, including fatalities.
-
World Health Organization (15 December 2022). Disease Outbreak News; Increased incidence of scarlet fever and invasive Group A Streptococcus infection-multi-country. Available at: https://www.who.int/emergencies/disease-outbreak-news/item/2022-DON429.
-
Facklam R. What happened to the streptococci: overview of taxonomic and nomenclature changes. Clinical Microbiology Reviews. 2002;15(4):613–630.
-
Ungureanu V. Boli bacteriene invazive. Infecţiile invazive cauzate de streptococii beta-hemolitici. Infecţio.ro. 2015;2:35-39.
-
Rimailho A, Riou B, Richard C, Auzepy P. Fulminant necrotizing fasciitis and nonsteroidal anti-inflammatory drugs. J Infect Dis. 1987;155:143–146.
-
Factor SH, Levine OS, Schwartz B, Harrison LH, Farley MM, McGeer A, et al. Invasive group A streptococcal disease: risk factors for adults. Emerg Infect Dis. 2003;9:970–7. Medline.
-
Harper A, Fleiser GR. Group A beta-hemolytic streptococcal bacteremia: historical overview, changing incidence, and recent association with varicella. Pediatrics. 1995;96:428-33.
-
Factor SH, Levine OS, Harrison LH, et al. Risk factors for pediatric invasive group A streptococcal disease. Emerg Infect Dis. 2005;11(7):1062-1066.
-
Cunningham MW. Pathogenesis of group A streptococcal infections. Clin Microbiol Rev. 2000;13:470–511.
-
Committee on Infectious Diseases. Group A streptococcal infections. In: Kimberlin DW, Brady MT, Jackson MA, Long SS (Editors), 30th ed. Red Book (2015). Report of the Committee on Infectious Diseases. Elk Grove Village (II). American Academy of Pediatrics. 2015;732–44.
-
Nelson GE, Pondo T, Toews KA, et al. Epidemiology of invasive group A streptococcal infections in the United States, 2005–2012. Clin Infect Dis. 2016;63(4):478–86.
-
Efstratiou A. Group A streptococci in the 1990s. J Antimicrob Chemother. 2000;45: 3–12.
-
Ikebe T, Hirasawa K, Suzuki R, et al. Antimicrobial susceptibility survey of Streptococcus pyogenes isolated from severe invasive group A streptococcal infections in Japan. Antimicrob. Agents Chemoter. 2005;49:788-790.
-
Steer AC, Curtis N, Carapetis JR. Diagnosis and treatment of invasive group A streptococcal infections. Expert Opin Med Diagnostics. 2007;2:289–302.
-
Centers for Disease Control and Prevention. Prevention of Invasive Group A Streptococcal Infections Workshop Participants. Prevention of invasive group A streptococcal disease among household contacts of case patients and among postpartum and postsurgical patients. Clin Infect Dis. 2002;35(8):950–9. Erratum in: Clin Infect Dis. 2003;36(2):243.





