Langerhans’ cells histiocytosis represents a group of rare diseases produced by the aberrant proliferation of dendritic cells in any organs in the body. Lungs, bones, lymph nodes, hypophysis and skin are mostly affected. Etiology is unclear, but cigarettes smoking, genetic factors like those involved in cancer development and immune reactive processes are the main risk factors and may explain the pathophysiology of the disease. Pulmonary Langerhans’ cell histiocytosis (PLCH) affects smoking young age women more frequently than men, and has a very unpredictable natural history, from mild to severe respiratory function impairment. Cases of pregnant women with PLCH are rarely described in literature. We present the ante-, peri- and postnatal management of a 20-year-old primipara with PLCH.
Managementul ante-, peri- şi postnatal al unei gravide cu histiocitoză pulmonară cu celule Langerhans - prezentare de caz
Ante-, peri- and postnatal management of a pregnant woman with pulmonary Langerhans’ cell histiocytosis - case report
First published: 05 octombrie 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Gine.17.3.2017.1082
Abstract
Rezumat
Histiocitozele cu celule Langerhans sunt un grup de patologii rare produse prin proliferarea clonală a celulelor dendritice Langerhans, care pot afecta orice organ. Sunt afectate mai frecvent: plămânii, tegumentul, sistemul osos, hipofiza, nodulii limfatici. Etiologia bolii este necunoscută, însă se pare că fumatul, mutaţiile genetice asemănătoare celor din neoplazii, dar şi cauze imunologice, reactive, joacă un rol important în fiziopatologia acestei maladii. Histiocitoza pulmonară cu celule Langerhans (HPCL) are o incidenţă mai crescută la femeile tinere fumătoare şi are o evoluţie imprevizibilă. În literatura de specialitate există foarte puţine cazuri raportate de gravide cu HPCL. Prezentăm managementul ante-, peri- şi postnatal al unei gravide, primipare, în vârstă de 20 de ani, cu HPCL.
Introducere
Histiocitozele cu celule Langerhans sunt un grup de patologii rare produse prin proliferarea clonală a celulelor dendritice Langerhans, care pot afecta orice organ(1). Sunt afectate mai frecvent: plămânii, tegumentul, sistemul osos, hipofiza, nodulii limfatici. Afectarea poate fi a unui singur organ sau multisistemică. Incidenţa anuală estimată este de 0,5-5,4 la 1 milion de persoane(1,2). Aceste patologii sunt mai frecvente la copiii cu vârsta între 0-15 ani. Cazurile de histiocitoze ale adultului sunt în general mai greu de evaluat şi de tratat, deoarece studiile asupra diagnosticului şi terapiei se bazează pe populaţia pediatrică. Etiologia şi fiziopatologia bolii sunt neclare, cuprinzând mutaţii genetice asemănătoare celor din neoplazii, dar şi cauze imunologice, reactive(1).
În general, prognosticul histiocitozelor este foarte variabil, în funcţie de tipul bolii, mergând de la unul bun până la unul fatal, neexistând protocoale clare de diagnostic şi tratament.
O categorie aparte o reprezintă histiocitoza pulmonară cu celule Langerhans (HPCL), în care, alături de limfocite, bronhiolele şi ţesutul interstiţial, sunt invadate de celule plasmatice, neutrofile şi eozinofile(2). Boala este mai frecventă la adulţii tineri, între 30 şi 40 de ani, fumători. Femeile de vârstă fertilă, fumătoare, sunt mai des afectate, deşi unii autori raportează o incidenţă egală între bărbaţi şi femei(2).
Fiind o patologie rară, care poate atinge o femeie de vârstă reproductivă, implicând deci şi o sarcină, diagnosticul, tratamentul şi evoluţia sunt dificil de efectuat şi apreciat, cazurile individuale raportate având importanţă ştiinţifică. În acest sens, expunem experienţa noastră, prezentând un caz clinic al unei gravide cu HPCL.
Prezentare de caz
Raportăm cazul unei gravide, secundigestă, primipară, în vârstă de 20 de ani, diagnosticată în urmă cu doi ani cu histiocitoză cu celule Langerhans cu afectare pulmonară, care în săptămâna 33 de sarcină s-a prezentat la Camera de Gardă a Spitalului Universitar de Urgenţă Bucureşti pentru contracţii uterine dureroase. Pacienta, fostă fumătoare, 5PA, în curs de sevraj de aproximativ două luni, a fost diagnosticată în 2015 cu histiocitoză X în cadrul Institutului Naţional de Pneumoftiziologie „Marius Nasta”, însă ulterior nu a efectuat monitorizare medicală.
Sarcina a fost parţial investigată. La 29 de săptămâni de sarcină, pacienta acuză dispnee, pentru care se prezintă la Camera de Gardă a Institutului Naţional de Pneumoftiziologie „Marius Nasta”, unde se stabileşte diagnosticul de pneumotorax complet drept; pacienta este internată şi se practică drenaj pleural. După 7 zile, pacienta face pneumotorax apical stâng, pentru care, de asemenea, se practică drenaj pleural. Se efectuează radiografie de control, cu şorţ de protecţie din plumb, care evidenţiază că pneumotoraxul drept este parţial remis, iar pneumotoraxul stâng este total remis. Se decide renunţarea la drenajul pleural stâng şi păstrarea drenajului pleural drept permanent, până în momentul naşterii. Ulterior, pacienta este externată.
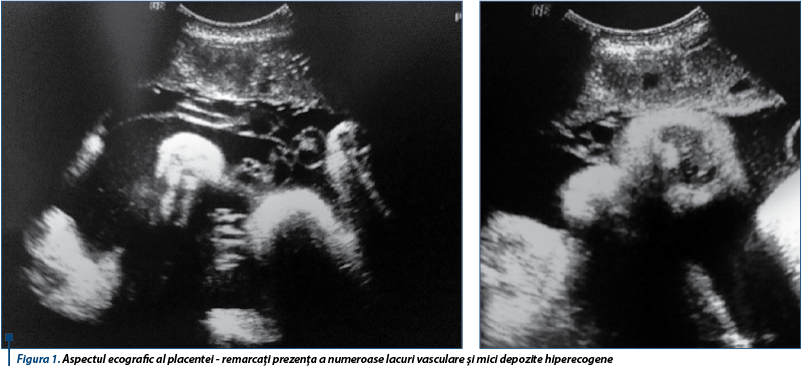
În cadrul Secţiei de Obstetrică-Ginecologie III a Spitalul Universitar de Urgenţă Bucureşti s-a efectuat un bilanţ obstetrical complet al gravidei. În cadrul evaluării ecografice s-a decelat o discretă întârziere de creştere intrauterină de aproximativ 2 săptămâni, în contextul unei insuficienţe placentare cronice (figura 1), însă cu raport cerebro-placentar supraunitar şi profil biofizic fetal normal. Paraclinic, s-a decelat anemie hipocromă microcitară uşoară. S-a instituit tratament tocolitic şi marţial, precum şi terapie cortizonică.
S-a efectuat radiografie pulmonară cu şorţ de plumb şi s-a decelat pneumotorax drept parţial remis şi pneumotorax stâng apical, pentru care s-a efectuat drenaj pleural stâng. La radiografia de control, pneumotoraxul stâng era remis, însă s-a decelat în continuare un viciu important de reexpansionare pulmonară dreaptă. Evoluţia este lent favorabilă, cu ameliorarea simptomatologiei, dar cu persistenţa pierderilor aeriene, motiv pentru care se decide montarea unor tuburi de dren pleural la valve unidirecţionale.
După un bilanţ obstetrical complet (examen clinic, evaluare ecografică şi cardiotocogramă) şi reevaluare chirurgie toracică, se decide externarea pacientei, aceasta având stare generală bună, fiind echilibrată hemodinamic şi respirator.
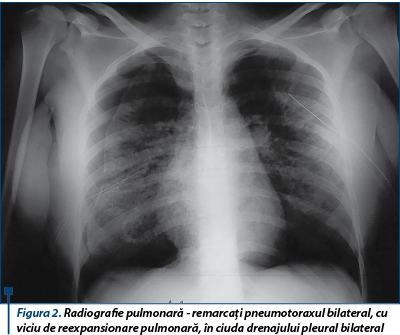
După trei zile, pacienta devine dispneică şi se prezintă la Camera de Gardă a Institutului Naţional de Pneumoftiziologie „Marius Nasta”, de unde este îndrumată către Spitalul Universitar de Urgenţă, unde este internată în Secţia de Chirurgie Toracică, pentru pneumotorax bilateral cu insuficienţă respiratorie (corectată sub oxigenoterapie) (figura 2).
Se decide extragerea de urgenţă a fătului prin operaţie cezariană, pentru suferinţă fetală cronică acutizată, în contextul insuficienţei respiratorii materne. Se extrage din prezentaţie pelviană un făt viu, de sex masculin, G - 2000 g, L - 44 cm, IA - 7. Fătul este admis în Secţia Terapie Intensivă Neonatală, unde se asigură suport ventilator prin CPAP timp de 72 de ore. Evoluţia ulterioară a nou-născutului este favorabilă, fără alte complicaţii, având curba de creştere în limite normale.
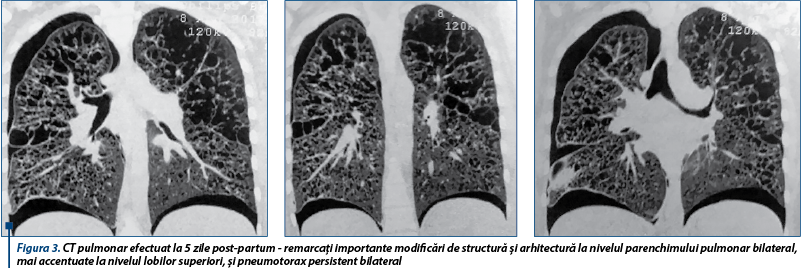
Imediat post-partum, lăuza este transferată în Secţia Terapie Intensivă, pentru monitorizare şi suport avansat al funcţiilor vitale, necesitând oxigenoterapie permanentă. Evoluţia este favorabilă şi, în ziua a treia postpartum, pacienta este transferată în Secţia Chirurgie Toracică. Se efectuează CT pulmonar (figura 3), care decelează importante modificări de structură şi arhitectură la nivelul parenchimului pulmonar bilateral, mai accentuate la nivelul lobilor superiori (modificări chistice cu tendinţă la confluare, rezultând voluminoase chisturi subpleurale); pneumotorax persistent bilateral (viciu important de expansiune).
Având în vedere patologia pulmonară preexistentă şi aspectul imagistic al parenchimului pulmonar, s-a considerat cu risc vital major şi beneficii minime (chiar în eventualitatea unei evoluţii favorabile intra- şi postoperator) o intervenţie chirurgicală (sub AG-IOT) de tratament al pneumotoraxului bilateral (aceasta presupunând toracotomie cu sutură pulmonară şi pleurodeză). Astfel, pacienta a fost propusă pentru transplant pulmonar.
Discuţii
Cele mai frecvente tipuri de histiocitoze sunt(3):
- boala Letterer-Siwe, care apare predominant la copiii sub 2 ani;
- boala Hand-Schuller-Christian şi forma cronică multifocală, care apar cu precădere la copiii între 2 şi 10 ani;
- granulomatoza eozinofilică localizată, care apare mai frecvent la copiii între 5 şi 15 ani;
- histiocitoza pulmonară cu celule Langerhans (HPCL), care este mai frecventă între 30 şi 40 de ani.
Etiologia HPCL este necunoscută, dar s-a observat că boala apare aproape în exclusivitate la rasa albă şi la fumători. Femeile şi bărbaţii par să fie afectaţi în mod egal, dar femeile dezvoltă boala ceva mai târziu, în funcţie şi de comportamentul de fumător/nefumător. Unii autori au raportat frecvenţa mai crescută a histiocitozelor în rândul populaţiei feminine. Incidenţa bolii este raportată ca fiind 5%(4). Noi raportăm cazul unei paciente în vârstă de 20 ani, fumătoare 5 PA, diagnosticată cu HPCL la vârstă de 18 ani.
Prezentarea clinică a pacientului cu HPCL cuprinde adesea tuse neproductivă sau dispnee, durere toracică, asociate cu simptome nespecifice de tipul fatigabilităţii, scăderii în greutate, transpiraţii nocturne, febră(5,6). Pacienta noastră s-a prezentat la spital în urmă cu doi ani pentru tuse neproductivă. Aproximativ 20% dintre pacienţi sunt iniţial asimptomatici sau se pot prezenta direct cu pneumotorax. Până în săptămâna a 29-a de sarcină, pacienta noastră a fost asimptomatică şi s-a prezentat la spital direct cu pneumotorax. Pentru evitarea unui tratament incomplet este important de diagnosticat dacă boala este una sistemică sau cu afectarea izolată a plămânilor(5,6).
Diagnosticul cuprinde radiografie pulmonară, tomografie de înaltă rezoluţie, probe ventilatorii, lavaj bronhoalveolar şi, în anumite cazuri, biopsie pulmonară(7).
Radiografia pulmonară prezintă un desen reticulo-micronodular, iar în cazurile severe se observă chisturi în infiltratele pulmonare, situate simetric în ambii plămâni, predominant în câmpurile pulmonare superioare şi mijlocii, cu evitarea unghiurilor costofrenice(5,8). CT-ul de înaltă rezoluţie este cea mai utilă investigaţie imagistică în HPCL. Desenul tipic cuprinde mici noduli sau noduli cavitari, care pot dispărea sau care, în cazurile avansate, evoluează către chisturi cu pereţi subţiri. Funcţia pulmonară este afectată prin scăderea capacităţii vitale şi creşterea volumului rezidual. În boala avansată apare bronhopatia obstructivă. Lavajul bronhoalveolar prezintă un număr crescut de macrofage alveolare, consecinţă a fumatului. Cauzele infecţioase trebuie de asemenea excluse. Biopsia pulmonară nu este utilă în diagnosticarea HPCL, dar este utilă în cazurile atipice. Procedurile invazive trebuie folosite cu discernământ în cazurile cu leziuni chistice extinse(8).
Evoluţia naturală a HPCL în cazul adulţilor este foarte variabilă şi imprevizibilă. Aproximativ 40-50% dintre pacienţi au evoluţie favorabilă, cu dispariţia semnelor radiologice sub tratament sau chiar spontan(9). Prima măsură esenţială este renunţarea la fumat(10). În cazurile simptomatice persistente este indicată corticoterapia sistemică (1 mg/kg/zi pentru o lună, apoi doze de întreţinere pentru mai multe luni)(11).
De asemenea, este importantă profilaxia infecţiilor respiratorii, care pot deteriora statusul pacientului cu HPCL. Cazurile progresive, neresponsive la corticoterapie, pot fi tratate cu 2-CDA. Cazurile de pneumotorax necesită drenaj, ţinând cont de riscul mare de recurenţă. Şi în cazul raportat de noi s-a optat pentru drenaj pleural bilateral permanent, având în vedere riscul crescut de recurenţă.
Transplantul pulmonar reprezintă o opţiune terapeutică pentru cazurile severe, cu insuficienţă respiratorie severă sau hipertensiune pulmonară importantă(12-16). Şi în cazul raportat de noi a fost stabilită indicaţia de transplant pulmonar, având în vedere că arhitectura şi structura parenchimului pulmonar erau foarte modificate şi o intervenţie chirurgicală fără viză curativă avea risc vital major şi beneficii minime(13-16).
HPCL în sarcină
În literatura de specialitate există foarte puţine cazuri de gravide cu HPCL, la care s-au raportat fie înrăutăţirea simptomelor, fie nicio schimbare din punctul de vedere al manifestărilor bolii pulmonare(17). Deteriorarea stării pacientelor se pare că s-a datorat mai degrabă diabetului insipid dezvoltat, nefiind însă clar dacă acesta ar fi fost cauzat direct de histiocitoză sau de scăderea vasopresinei prin intermediul vasopresinazei placentare, fapt observat şi la paciente fără histiocitoză(18,19). Restricţia de creştere intrauterină fetală poate fi explicată prin relaţia dintre fumat şi insuficienţa placentară(20).
Concluzii
Lipsa datelor din literatura de specialitate despre impactul sarcinii asupra evoluţiei HPCL şi a histiocitozelor, în general, face foarte dificilă evaluarea cazurilor. Managementul unei gravide diagnosticate cu HPCL necesită o abordare pluridisciplinară care să includă obstetrician, neonatolog, chirurg toracic, pneumolog şi specialist în anestezie şi terapie intensivă.
Bibliografie
2. Windebank K, Nanduri V. Langerhans cell histiocytosis. Archives of Disease in Childhood. 2009;94(11):904-8.
3. Vrijmoet-Wiersma C, Kooloos V, Koopman H, Kolk A, van der Laan I, Grootenhuis M. Health-related quality of life, cognitive functioning and behaviour problems in children with Langerhans cell histiocytosis. Pediatr Blood Cancer, 2009;52(1):116-22.
4. Tazi A. Adult pulmonary Langerhans' cell histiocytosis. Eur Respir J. 2006;27(6):1272-85.
5. Watanabe R, Tatsumi K, Hashimoto S, Tamakoshi A, Kuriyama T& Respiratory Failure Research Group of Japan. Clinico-epidemiological features of pulmonary histiocytosis X. Internal medicine, 2001;40(10):998-1003.
6. Vassallo R, Ryu J, Schroeder DR, Decker P, Limper A. Clinical outcomes of pulmonary Langerhans'cell histiocytosis in adults. New England Journal of Medicine, 2002;346(7):484-90.
7. Tazi A, Marc K, Dominique S, de Bazelaire C, Crestani B. Serial computed tomography and lung function testing in pulmonary Langerhans’ cell histiocytosis. Eur Respir J, 2012;40(4):905-12.
8. Auerswald U, Barth J, Magnussen H. Value of CD-1-positive cells in bronchoalveolar lavage fluid for the diagnosis of pulmonary histiocytosis X. Lung, 1991;169(1):305-9.
9. Lazor R, Etienne-Mastroianni B, Khouatra C. E, Tazi A, Cottin V, Cordier J. F. Progressive diffuse pulmonary Langerhans cell histiocytosis improved by cladribine chemotherapy. Thorax, 2009;64(3):274-5.
10. Lorillon G, Bergeron A, Detourmignies L, Jouneau S, Wallaert B, Frija J, Tazi A. Cladribine is effective against cystic pulmonary Langerhans cell histiocytosis. American journal of respiratory and critical care medicine, 2012;186(9): 930-.
11. Mendez JL, Nadrous HF, Vassallo R, Decker PA, Ryu, JH. Pneumothorax in pulmonary Langerhans cell histiocytosis. Chest, 2004;125(3):1028-32.
12. Dauriat G, Mal H, Thabut G, Mornex JF, Bertocchi M, Tronc F, Pison C. Lung transplantation for pulmonary langerhans' cell histiocytosis: a multicenter analysis. Transplantation, 2006;81(5):746-50.
13. Harari S, Torre O, King Jr TE, Moss J. Pulmonary Langerhans' Cell H istiocytosis. Elias JA, Fishman JA, Kotloff RM, Pack A, Senior RM, eds. Fishman's Pulmonary Diseases and Disorders. 5th ed. NY: McGraw-Hill; 2015; 919-27.
14. Alalawi R, Whelan T, Bajwa RS, Hodges TN. Lung transplantation and interstitial lung disease. Curr Opin Pulm Med. 2005;11(5):461-6.
15. DiCaprio MR, Roberts TT. Diagnosis and Management of Langerhans Cell Histiocytosis. J Am Acad Orthop Surg. 2014; 22(10):643-652.
16. Rădulescu IM, Rădulescu L, Cîrstiu MM, Cordoş I. Thoracic surgery in lung metastases of genital cancers. Brief review of literature. Ginecologia 2014;2(4):30-2.
17. Ananthakrishnan S. Diabetes insipidus in pregnancy: etiology, evaluation, and management. Endocr Pract, 2009;15(4):377-82.
18. DiMaggio LA, Lippes HA, Lee RV. Histiocytosis X and pregnancy. Obstet Gynecol, 1995;85(5):806-9.
19. Sharma R, Maplethorpe R, Wilson G. Effect of pregnancy on lung function in adult pulmonary Langerhans cell histiocytosis. J Matern Fetal Neonatal Med, 2006;19(1):67-8.
20. Bodean OM, Munteanu O, Secară DC, Cîrstoiu MM. Metabolic changes and the risk of preterm birth. Ginecologia.ro 2014;2(3):28-30.
Articole din ediţiile anterioare
Trombofilia ereditară şi complicaţiile obstetricale mediate de placentă
Trombofilia se referă la o predispoziţie către o stare de hipercoagulabilitate şi poate fi identificată în 30-50% din cazurile de tromboembolism ve...
Restaurarea coronară directă cu pivot din fibră de sticlă în sarcină - prezentare de caz
În cadrul tratamentelor dentare care sunt necesare în cursul perioadei de sarcină, situațiile clinice în care pacienta prezintă o distrucție corona...
Contracepţia la pacientele infectate HIV
Infecţia cu virusul HIV reprezintă apanajul vieţii moderne, de aceea contracepţia la femeia infectată HIV reprezintă un subiect controversat şi de ...
Hemangiom vertebral agresiv care determină afectare neurologică severă în al treilea trimestru de sarcină – prezentare de caz
Hemangiomas are benign vascular tumors characterized by endothelial cell proliferation, most commonly affecting the soft tissues, but they can al...