Incidentalom adrenal la o pacientă cu cancer endometrial şi sindrom metabolic
Adrenal incidentaloma in a patient with endometrial carcinoma and metabolic syndrome
Abstract
Introduction. Metabolic complications (MC) may be caused by an active adrenal tumor (AT) as Conn’s, Cushing’s syndrome; however a secondary site of a previous carcinoma may involve adrenals. Objective. We present endocrine panel of a menopausal woman with MC and cancer to whom differential diagnosis need to be clarified in front of a newly discovered AT. Material and method. Hormonal assays are detailed. Results. In 2015, a 64-year-old female is admitted for accidentally discovered AT (of 2.89/3.6/3.2 cm). In 2011 she was diagnosed with endometrial carcinoma and total hysterectomy with bilateral anexectomy was done with local radiotherapy added. She associated high-risk MC as: type 2 diabetes mellitus, high blood pressure, hyperlipemia, chronic ischemic heart disease, persistent atrial fibrillation, hyperuricemia, and an episode of stroke (complicated with left hemiplegy). On admission, the serum sodium and potassium were normal while the endocrine profile revealed non-secretor profile: plasma metanephrines = 10 pg/mL (Normal: 10-90 pg/mL), plasma normetanephrines = 20 pg/mL (Normal: 15-180 pg/mL), plasma baseline ACTH = 8.04 pg/mL (Normal: 3-66 pg/mL), baseline morning plasma cortisol = 14.97 µg/dL (Normal: 6.2-11.9 µg/dL), morning plasma cortisol after dexametasone suppression test =3 µg/dL (Normal: <1.8 µg/mL), chromogranin A = 20 ng/mL (Normal: 20-125 ng/mL). The patient was followed for one more year, and clinical, hormonal and imagery aspects were status quo. Conclusion. Adrenal incidentaloma may represent a challenge if metabolic complications are already diagnosed and a secretor pattern might be involved, and if a prior cancer is treated, the adrenal mass raises the question of a secondary spreading.Keywords
endometrial canceradrenal tumorhigh blood pressureobesityRezumat
Introducere. Factorii de risc metabolic şi cardiovascular diagnosticaţi la un pacient ar putea fi în esenţă datoraţi unei tumori suprarenale secretante similare cu cea cauzatoare de sindrom Conn sau Cushing; mai mult, adrenalele pot găzdui ca sediu secundar un carcinom. Obiectiv. Să introducem tabloul endocrin în menopauză al unei paciente care asociază atât tulburări metabolice, cât şi un istoric de neoplasm, context ce necesită un diagnostic diferenţial atent al tumorii adrenale. Material şi metodă. S-au utilizat pentru acest caz datele bazate pe dozările endocrine, ginecologice şi imagistice. Rezultate. O pacientă de 64 de ani este internată în 2015 pentru relevarea fortuită a unei tumori suprarenale (de 2,89/3,62/3,2 centimetri). În 2011, pacienta fusese diagnosticată cu un carcinom endometrial tratat prin histerectomie totală cu anexectomie bilaterală şi ulterior cu radioterapie locală. Doamna prezenta profil cardio-metabolic cu risc ridicat, dat de asocierea: diabet zaharat de tip 2, hipertensiune arterială, hiperlipemie, boală coronariană, fibrilaţie atrială permanentă, diateză urică, istoric de accident vascular. La internare, sodiul şi potasiul seric au fost normale, cu dozările următoare: metanefrine plasmatice de 10 pg/mL (normal între 10 şi 90 pg/mL), normetanefrine plasmatice de 20 pg/mL (normal între 15 şi 180 pg/mL), ACTH bazal matinal de 8,04 pg/mL (normal între 3 şi 66 pg/mL), cortizol plasmatic bazal matinal de 14,97 µg/dL (normal între 6,2 şi 11,9 µg/dL), cortizol plasmatic după testul de supresie la dexatemazonă de 3 µg/dL (normal sub 1,8 µg/dL), cromogranina A de 20 ng/mL (normal între 20 şi 125 ng/mL). Pacienta a fost urmărită un an, fără modificări semnificative clinice sau dozimetrice. Discuţii. Identificarea unei tumori adrenale în astfel de circumstanţe implică multiple specialităţi, de la oncologia ginecologică, cardiologie la endocrinologie. Concluzie. Incidentalomul adrenal ar putea asocia dificultăţi de confirmare a profilului specific dacă se asociază complicaţii metabolice sau, pentru pacienţii cu istoric oncologic, o masă adrenală poate ascunde o metastază.Cuvinte Cheie
cancer endometrialtumoră adrenalăhipertensiune arterialăobezitateIntroducere
Pacienţii cu istoric medical complex de tip profil cardio-metabolic de risc înalt pot avea un context primar (esenţial sau fără o cauză evidentă) ori pot asocia disfuncţii specifice endocrine care să perturbe balanţa cardiacă, precum tumori suprarenale secretante de tip sindrom Conn, sindrom Cushing (clinic sau subclinic) sau carcinom adrenal (Di Dalmazi şi col., 2015; Di Dalmazi şi col., 2014; Zografos şi col. 2014). Identificarea într-un context fortuit a unei tumori endocrine care în final se va dovedi non-secretantă, eveniment din ce în ce mai frecvent în ultimii ani, odată cu accesul la investigaţii din ce în ce mai performante, a dus la implementarea termenului de „incidentalom”, utilizat frecvent pentru adrenală şi hipofiză (Poiană şi col., 2013; Carsote şi col., 2009).
Excesul de glucocorticoizi acţionează pe augmentarea riscului cardiovascular prin intermediul insulinorezistenţei, ateromatozei, respectiv al diabetului zaharat, al insulinorezistenţei, hipertensiunii arteriale, bolii coronariene ischemice etc. (Nieman, 2015; Ferrau şi Korbonits, 2015; Santos şi col., 2015; Petramala şi col. 2015).
Actual, determinarea contextului de sindrom Cushing subclinic pentru cazurile mai puţin „zgomotoase” ca simptome nu este bine definită în practica uzuală, la fel ca decizia de intervenţie terapeutică radicală (Goddard şi col., 2015; Kaltsas şi col., 2012). Pe de altă parte, la un pacient cunoscut cu o malignitate anterior confirmată şi tratată, decelarea unei tumori adrenale necesită diferenţierea de o diseminare secundară, care, similar cu incidentaloamele adrenale în accepţiunea clasică a termenului, nu au tulburări endocrine (Glenn şi col., 2016; Ginzburg şi col. 2015; Gryn şi col. 2015). Diferenţa majoră nu este numai la prognostic (metastază versus incidentalom adrenal), dar mai ales la faptul că acesta este net îmbunătăţit dacă determinarea secundară este recunoscută şi rezecată în timp util (Kebew şi col. 2002; Moinzadeh şi Gill, 2005).
Obiectiv
Ne propunem să prezentăm tabloul endocrin şi caracteristicile evaluării ginecologice în menopauză la o pacientă care asociază atât tulburări metabolice, cât şi un istoric de neoplasm endometrial, context ce necesită realizarea unui diagnostic diferenţial detaliat odată cu identificarea unei tumori adrenale.
Material şi metodă
S-au utilizat pentru acest caz datele bazate pe dozările endocrine, ginecologice, imagistice, ca şi cele de istoric medical personal din diverse clinici din România. Consimţământul informat a fost semnat de către pacientă.
Rezultate
Context clinic
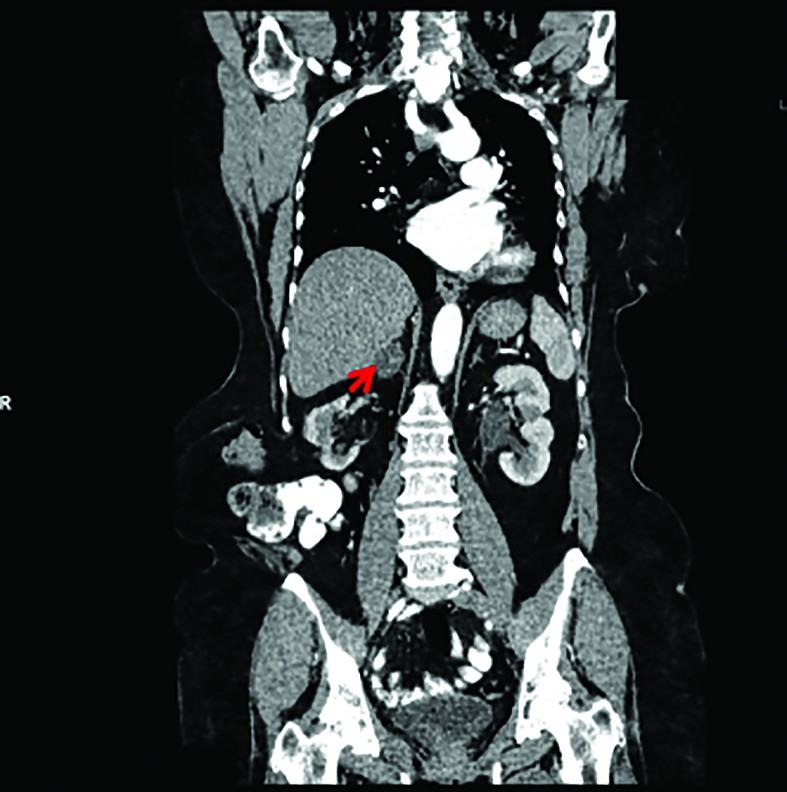
Pacienta, în prezent în vârstă de 64 de ani, a fost internată în 2015 pentru decelarea accidentală a unei tumori suprarenale (de 2,89 pe 3,6 pe 3,2 centimetri), iniţial ecografic (din 2012 la ecografii anuale, cu un diametru maxim de 3 cm) apoi confirmată computer tomografic (figura 1). Antecedentele familiale medicale ne arată: tată cu infarct miocardic la vârsta de 50 de ani, mama hipertensivă şi diabetică, un frate cu hipertensiune arterială şi litiază renală.
Istoric medical
Circumstanţele patologice anterioare internării reliefează faptul că în 2011 pacienta fusese diagnosticată cu un carcinom endometrial tratat prin histerectomie totală, cu anexectomie bilaterală şi ulterior cu radioterapie locală.
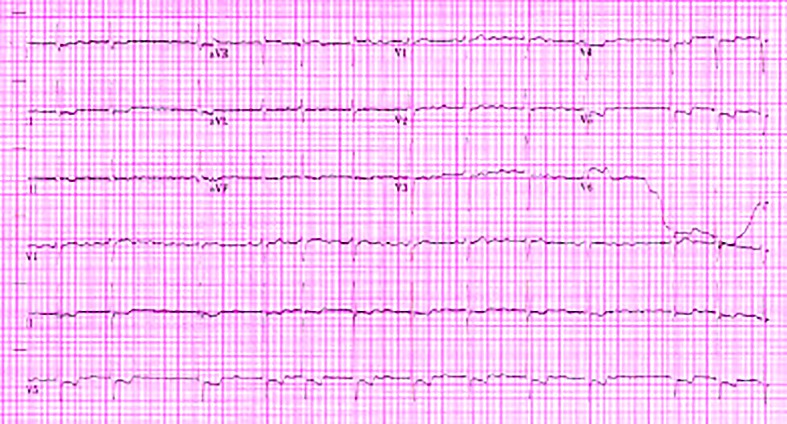
Subiectul mai prezintă un profil cardio-metabolic cu risc ridicat dat de asocierea următoarelor boli: diabet zaharat de tip 2 (din 2007), aflat sub terapie cu antidiabetice orale, hipertensiune arterială, hiperlipemie, boală coronariană ischemică, fibrilaţie atrială permanentă, diateză urică, istoric de accident vascular cerebral (în 2010; complicat cu hemiplegie stângă) (figura 2). De asemenea, în 2007 a suferit o intervenţie de colecistectomie clasică, iar în 1980, respectiv 1981, două intervenţii pentru litiază renală dreaptă pe fond normocalcemic. Pentru aceste comorbidităţi, în prezent urmează terapie cu digitalo-diuretic, betablocant, inhibitor de enzimă de conversie, blocant de calciu, statină, biguanid.
Bilanţul endocrin
La internarea în clinica de endocrinologie, examenul clinic a reliefat obezitate de grad 1 (indicele de masă corporală de 34,9 kg/m2); biochimia a fost normală, inclusiv sodiul şi potasiul seric. Dozările hormonale au fost următoarele: metanefrine plasmatice 10 pg/mL (valori normale între 10 şi 90 pg/mL), normetanefrine plasmatice de 20 pg/mL (normal, cu limitele între 15 şi 180 pg/mL), ACTH (Hormonul AdrenoCorticotrop) bazal matinal de 8,04 pg/mL (normal între 3 şi 66 pg/mL), cortizol plasmatic bazal matinal de 14,97 µg/dL (normal între 6,2 şi 22 µg/dL), cortizol plasmatic după testul de supresie la dexatemazonă de 3 µg/dL (normal se inhibă sub 1,8 µg/dL), cromogranina A serică de 20 ng/mL (normal între 20 şi 125 ng/mL).
Funcţia tiroidiană a fost normală. Bilanţul osos a indicat un deficit de vitamina D (25-hidroxivitamina D serică de 13 ng/mL, normal între 30 şi 100 ng/mL), dar cu markeri osoşi şi parahormon normali, iar examenul DXA central (Absorbţiometrie Duală cu raze X) a relevat densitate minerală osoasă (DMO) adecvată: DMO lombar de 1,295 g/cm2, scor T de 1 DS, scor Z de 1,16 DS, DMO col femural de 0,965 g/cm2, scor T de -0,5 DS, scor Z de 0,3 DS, DMO şold total de 1,091 g/cm2, scor T de 0,7 DS, scor Z de 1,2 DS, DMO de treime distală radius non-dominant de 0,671 g/cm2, scor T de -0,6 DS, scor Z de 0,7 DS.
S-a recomandat, pe lângă medicaţia de control cardiovascular, suplimentarea cu vitamină D.
Aceste date sunt sugestive pentru un profil endocrin adrenal non-secretor, potenţial un sindrom Cushing subclinic, conform cu anumite criterii.
Date fiind multiplele intervenţii chirurgicale anterioare şi riscul cardiovascular/anestezic prezent, s-a optat pentru monitorizare (ţinând cont şi de opţiunea pacientei), iar la un an nu au fost modificări semnificative clinice sau dozimetrice.
Având în vedere istoricul oncologic, riscul de a fi o metastază adrenală este posibil, dar mai puţin probabil dacă dimensiunile sunt statu quo la evaluarea în dinamică şi nu există un context metastatic pe alte organe sau de recidivă locală pelviană.
Discuţii
Observaţiile acestui caz se pot grupa pe mai multe aspecte particulare de multidisciplinaritate în faţa unei paciente cu istoric de patologie oncologică endocrină asociat cu boli cardiovasculare şi o tumoră endocrină.
Cancerul de endometru este cea mai frecventă malignitate din sfera ginecologică pentru populaţia din ţările dezvoltate (Lheureux şi Oza, 2016).
Odată cu creşterea incidenţei obezităţii la nivel mondial, se estimează că în paralel se va augmenta numărul de persoane confirmate cu acest tip de diagnostic oncologic (Laskey şi col., 2016).
Tipurile histopatologice variază, cel mai des fiind întâlnit adenocarcinomul endometrioid (ca în cazul de faţă) (Cetinkaya şi col., 2016).
Opţiunile terapeutice sunt limitate, cea mai modernă fiind cea biologică, încă insuficient implementată în practica uzuală (Kamal şi col., 2016).
Datele din istoricul medical al pacientei prezentate ne arată o evoluţie bună până la momentul actual, dar este de recomandat o monitorizare atentă.
Un alt aspect este legat de sindromul Cushing subclinic, despre care nu există date precise actuale ca definiţie şi atitudine terapeutică (Pisano şi col., 2015).
Legat de parametrii medicali expuşi mai sus, lipsa inhibiţiei la testul de supresie la dexametazonă, dar cu o scădere considerabilă a nivelului cortizolului plasmatic, ar putea sugera o astfel de entitate, mai ales având în vedere contextul metabolic.
Sindromul Cushing subclinic este descris în corelaţie cu tumori adrenale decelate accidental (incidentaloame), inclusiv bilaterale (Rossi şi col., 2000).
Suprarenalectomia unilaterală nu aduce după sine neapărat insuficienţă corticosuprarenală cum se întâlneşte în sindromul Cushing franc de cauză tumorală adrenală (Albu şi col., 2015; Carsote şi col., 2015).
Nu toţi autorii recomandă chirurgie pentru situaţii similare, motiv pentru care, având în vedere şi opţiunea pacientei, a fost monitorizată.
Decelarea unei tumori adrenale pe fondul unei boli cu potenţial metastastic aduce în discuţie diferenţierea unui incidentalom de o metastază (sugestivă în lipsa adrenalectomiei, prin creşterea dimensională în timp sau asocierea de noi sedii de determinări secundare) (Carsote şi col., 2015; Bartosch şi col. 2016).
Evaluarea osoasă în menopauză este de recomandat, dar în cazul de faţă s-a identificat DMO normal la DXA în context de deficit vitaminic D (Hernlund şi col., 2013).
Studiile pe populaţia din România aflată la menopauză ne arată o mare prevalenţă a hipovitaminozei D legată de alimentaţie, expunerea redusă la soare, boli cu malabsorbţie sau care induc apetit alimentar scăzut (precum cancerele) (Poiană şi col., 2015; Albu şi col., 2015; Capatina şi col., 2014).
Concluzie
Decelarea unei tumori adrenale la o pacientă cunoscută cu patologie oncologică ginecologică şi multiple complicaţii cardio-metabolice pune problema unui diagnostic diferenţial între metastază suprarenală şi incidentalom (dacă profilul este nesecretor), respectiv de sindrom Cushing (clinic sau subclinic), având în vedere riscul cardiovascular. Dacă adrenalectomia nu se poate efectua, monitorizarea atentă imagistică şi dozimetrică este de dorit.
Conflict de interese: Autorii nu au nici un conflict de interes de declarat.
Mulţumiri: Mulţumim echipei interdisciplinare de medici care au urmărit pacienta în diverse centre medicale din România. De asemenea, mulţumim pacientei.
Bibliografie
1. Di Dalmazi G, Pasquali R, Beuschlein F, Reincke M (2015). Subclinical hypercortisolism: a state, a syndrome, or a disease? Eur J Endocrinol, 173(4), M61-71. doi: 10.1530/EJE-15-0272.
2. Di Dalmazi G, Vicennati V, Garelli S, Casadio E, Rinaldi E, Giampalma E, Mosconi C, Golfieri R, Paccapelo A, Pagotto U, Pasquali R (2014). Cardiovascular events and mortality in patients with adrenal incidentalomas that are either non-secreting or associated with intermediate phenotype or subclinical Cushing’s syndrome: a 15-year retrospective study. Lancet Diabetes Endocrinol, 2(5), 396-405.
3. Zografos GN, Perysinakis I, Vassilatou E (2014). Subclinical Cushing’s syndrome: current concepts and trends. Hormones (Athens), 13(3), 323-37. doi: 10.14310/horm.2002.1506.
4. Poiană C, Chiriţă C, Carsote M, Hortopan D, Ioachim D, Corneci CM, Stănescu B (2013). Adrenal and pituitary incidentalomas in a case of Cushing’s syndrome. Chirurgia (Bucur), 108(6), 886-91.
5. Carsote M, Chirita C, Dumitrascu A, Hortopan D, Fica S, Poiana C (2009). Pituitary incidentalomas - how often is too often? J Med Life, 2(1), 92-7.
6. Nieman LK. (2015) Cushing’s syndrome: update on signs, symptoms and biochemical screening. Eur J Endocrinol, 173(4), M33-8. doi: 10.1530/EJE-15-0464.
7. Ferraù F, Korbonits M. (2015) Metabolic comorbidities in Cushing’s syndrome. Eur J Endocrinol,173(4), M133-57. doi: 10.1530/EJE-15-0354.
8. Santos A, Resmini E, Gómez-Ansón B, Crespo I, Granell E, Valassi E, Pires P, Vives-Gilabert Y, Martínez-Momblán MA, de Juan M, Mataró M, Webb SM. (2015) Cardiovascular risk and white matter lesions after endocrine control of Cushing’s syndrome. Eur J Endocrinol, 173(6), 765-75. doi: 10.1530/EJE-15-0600.
9. Petramala L, Lorenzo D, Iannucci G, Concistré A, Zinnamosca L, Marinelli C, De Vincentis G, Ciardi A, De Toma G, Letizia C (2015). Subclinical Atherosclerosis in Patients with Cushing Syndrome: Evaluation with Carotid Intima-Media Thickness and Ankle-Brachial Index. Endocrinol Metab (Seoul), 30(4), 488-93. doi: 10.3803/EnM.2015.30.4.488.
10. Goddard GM, Ravikumar A, Levine AC (2015). Adrenal mild hypercortisolism. Endocrinol Metab Clin North Am, 44(2), 371-9. doi: 10.1016/j.ecl.2015.02.009.
11. Kaltsas G, Chrisoulidou A, Piaditis G, Kassi E, Chrousos G (2012). Current status and controversies in adrenal incidentalomas. Trends Endocrinol Metab, 23(12), 602-9. doi: 10.1016/j.tem.2012.09.001.
12. Glenn JA, Kiernan CM, Yen TW, Solorzano CC, Carr AA, Evans DB, Wang TS (2016). Management of suspected adrenal metastases at 2 academic medical centers. Am J Surg, 211(4), 664-70. doi: 10.1016/j.amjsurg.2015.11.019.
13. Ginzburg S, Reddy M, Veloski C, Sigurdson E, Ridge JA, Azrilevich M, Kutikov A (2015). Papillary Thyroid Carcinoma Metastases Presenting as Ipsilateral Adrenal Mass and Renal Cyst. Urol Case Rep, 3(6), 221-2. doi: 10.1016/j.eucr.2015.08.007.
14. Gryn A, Peyronnet B, Manunta A, Beauval JB, Bounasr E, Nouhaud FX, Rioux-Leclercq N, Caron P, Thoulouzan M, Verhoest G, Soulie M, Bensalah K, Huyghe E (2015). Patient selection for laparoscopic excision of adrenal metastases: A multicenter cohort study. Int J Surg, 24(Pt A):75-80. doi: 10.1016/j.ijsu.2015.10.038.
15. Kebebew E, Siperstein AE, Clark OH, Duh QY (2002). Results of laparoscopic adrenalectomy for suspected and unsuspected malignant adrenal neoplasms. Arch Surg, 137(8), 948-51; discussion 952-3.
16. Moinzadeh A, Gill IS (2005). Laparoscopic radical adrenalectomy for malignancy in 31 patients. J Urol, 173(2), 519-25.
17. Lheureux S, Oza AM (2016). Endometrial cancer-targeted therapies - myth or reality? Review of current targeted treatments. Eur J Cancer, 59:99-108. doi: 10.1016/j.ejca.2016.02.016.
18. Laskey RA, McCarroll ML, von Gruenigen VE (2016). Obesity-related endometrial cancer: an update on survivorship approaches to reducing cardiovascular death. BJOG,123(2):293-8. doi: 10.1111/1471-0528.13684.
19. Cetinkaya K, Atalay F, Bacinoglu A, Dervisoglu H (2016). To what extent is risk grouping method successful in deciding surgical staging in endometrial cancer? Tumori, 30:0. doi: 10.5301/tj.5000497.
20. Kamal A, Tempest N, Parkes C, Alnafakh R, Makrydima S, Adishesh M, Hapangama DK (2016). Hormones and endometrial carcinogenesis. Horm Mol Biol Clin Investig, 25(2):129-48. doi: 10.1515/hmbci-2016-0005.
21. Pisano G, Calò PG, Erdas E, Pigliaru F, Piras S, Sanna S, Manca A, Dazzi C, Nicolosi A (2015). Adrenal incidentalomas and subclinical Cushing syndrome: indications to surgery and results in a series of 26 laparoscopic adrenalectomies. Ann Ital Chir, 86:406-12.
22. Rossi R, Tauchmanova L, Luciano A, Di Martino M, Battista C, Del Viscovo L, Nuzzo V, Lombardi G (2000). Subclinical Cushing’s syndrome in patients with adrenal incidentaloma: clinical and biochemical features. J Clin Endocrinol Metab, 5(4):1440-8.
23. Albu SE, Carsote M, Capatina C, Dumitrascu A, Ghemigian A (2015). Adrenal surgical approach in a woman with synchronous bilateral adrenal tumours. Journal of Surgical Sciences, 2(3):132-135.
24. M. Carsote, A. Ghemigian, A. Valea, A. Dumitrascu, C. Chirita, C. Poiana (2015). Sublinical Cushing’s syndrome with bilateral adrenal tumours in a patient with gallbladder multiple stone: therapeutical options. Ars Medica Tomitana, 3(21):124-127.
25. Carsote M, Valea A, Dumitraşcu A, Terzea D, Păun S, Poiană C (2015). The unilateral adrenal tumor in a patient with history of uterine cervix cancer: the radiological and endocrine profile related management. International Journal of Diagnosis Imaging, 2(2):90-95.
26. Bartosch C, Afonso M, Pires-Luís AS, Galaghar A, Guimarães M, Antunes L, Lopes JM. (2016) Distant Metastases in Uterine Leiomyosarcomas: The Wide Variety of Body Sites and Time Intervals to Metastatic Relapse. Int J Gynecol Pathol. 2016 Mar 24. [Epub ahead of print]
27. Hernlund E, Svedbom A, Ivergård M, Compston J, Cooper C, Stenmark J, McCloskey EV, Jönsson B, Kanis JA. (2013) Osteoporosis in the European Union: medical management, epidemiology and economic burden. A report prepared in collaboration with the International Osteoporosis Foundation (IOF) and the European Federation of Pharmaceutical Industry Associations (EFPIA). Arch Osteoporos. 8:136. doi: 10.1007/s11657-013-0136-1.
28. Poiana C, Carsote M, Capatina C, Radoi V, Ghemigian A. (2015) Vitamin D in menopause: a cross-sectional study on 471 women. Romanian Journal of Rheumatology, XXIV(1): 40-44.
29. Albu SE, Geleriu A, Carsote M, A Mihai, C. Vasiliu, C. Poiana. (2015) The vitamin D status in menopausal women. Archives of Balkan Medical Union, 50(2): 275-277.
30. Capatina C, Carsote M, Caragheorgheopol A, Poiana C, Berteanu M. (2014) Vitamin D deficiency in postmenopausal women – biological correlates. Maedica: a Journal of Clinical Medicine, 9(4): 316-322.


