De la ghiduri la practica clinică: recomandări actuale pentru abordarea pacientului cardiac cu patologie chirurgicală noncardiacă
From guidelines to clinical practice: current recommendations for the management of cardiac patients undergoing non-cardiac surgery
Abstract
Non-cardiac surgeries account for nearly 85% of the total 300 million surgeries that are performed annually worldwide, cardiovascular events representing the main source of perioperative morbidity and mortality. Considering that often patients suffering from cardiovascular (CV) diseases tend be clinically fragile, clear recommendations are needed to guide clinical decisions, in order to minimize their perioperative risk. The current ESC guideline maintains some of the classic indications, emphasizing the importance of preoperative risk assessment and clinical examination of the patients suffering from a CV disease. It also introduces new concepts regarding the preoperative use of biomarkers, the perioperative thromboprophylaxis and the management of patients newly diagnosed with murmurs, dyspnea, oedema or angina. Furthermore, other sections, approaching complex clinical situations, as peri-operative management of antiplatelet and anticoagulant therapies, have been revised, according to the latest studies. This review is meant to concisely present these new recommendations, in a simplified and more accessible manner.Keywords
non-cardiac surgerytherapeutic managementcardiovascular diseasesRezumat
Intervenţiile chirurgicale noncardiace (ICNC) reprezintă aproape 85% din totalul de 300 de milioane de intervenţii chirurgicale care sunt efectuate anual la nivel mondial, evenimentele cardiovasculare reprezentând principala sursă de morbiditate şi mortalitate perioperatorie. Având în vedere că majoritatea pacienţilor care suferă de boli cardiovasculare (CV) se caracterizează prin fragilitate, în practica clinică sunt necesare recomandări clare pentru a ghida deciziile terapeutice, în scopul de a minimiza riscul lor perioperatoriu. Actualul ghid al Societăţii Europene de Cardiologie (ESC) menţine unele dintre vechile indicaţii, subliniind importanţa evaluării riscului preoperatoriu şi a examinării clinice complete la toţi pacienţii care suferă de o patologie CV. De asemenea, s-au introdus noi concepte privind utilizarea preoperatorie a biomarkerilor, tromboprofilaxia perioperatorie şi managementul pacienţilor noudiagnosticaţi cu sufluri cardiace, dispnee, edeme sau angină pectorală. De asemenea, au fost revizuite şi alte secţiuni, care discută situaţii clinice complexe, precum managementul perioperatoriu al terapiilor antiplachetare şi anticoagulante, conform ultimelor studii din literatură. Această lucrare este menită să prezinte concis aceste noi recomandări, într-o manieră simplificată şi cât mai accesibilă tuturor specialiştilor din domeniu.Cuvinte Cheie
chirurgie noncardiacămanagement terapeuticboli cardiovasculareNoţiuni introductive
Intervenţiile chirurgicale noncardiace (ICNC) reprezintă aproape 85% din totalul de 300 de milioane de intervenţii chirurgicale care sunt efectuate anual la nivel mondial(1). Unele dintre principalele surse de morbiditate şi mortalitate asociate acestor proceduri invazive sunt evenimentele cardiovasculare (CV) perioperatorii, care complică 3% din spitalizări(2).
Cei doi principali determinanţi ai riscului de evenimente CV perioperatorii pot fi clasificaţi în:
-
factori de risc legaţi de pacient şi
-
factori de risc legaţi de intervenţia chirurgicală propriu-zisă.
Având în vedere că pacienţii care au nevoie de ICNC sunt în general persoane vârstnice şi ţinând cont că vârsta înaintată este per se un factor de risc important pentru bolile cardiovasculare (BCV), identificarea de soluţii viabile pentru a minimiza riscul de complicaţii CV perioperatorii reprezintă o provocare majoră în practica medicală curentă. Boala cardiacă ischemică, disfuncţia ventriculară stângă (VS), patologia valvulară şi aritmiile reprezintă entităţile patologice responsabile pentru majoritatea evenimentelor CV asociate cu ICNC.
Unul dintre principalele mecanisme aflate la originea acestor complicaţii CV este reprezentat de stresul hemodinamic asociat intervenţiei chirurgicale, care poate induce un dezechilibru dintre consumul şi, respectiv, aportul de oxigen de la nivel miocardic, putând astfel decompensa un VS deja disfuncţional. Eroziunea plăcii de aterom indusă de stresul operator, statusul proinflamator şi hipercoagulant sau necesitatea de a întrerupe administrarea terapiilor antiagregante plachetare sunt alte surse importante de complicaţii CV, fiind asociate în principal cu agravarea ischemiei miocardice(3).
Managementul preoperatoriu:
o abordare integrativă
În cel mai recent Ghid al Societăţii Europene de Cardiologie (ESC) privind evaluarea şi managementul cardiovascular al pacienţilor supuşi ICNC, se subliniază instrumentele utile pentru stratificarea riscului preoperatoriu al acestor pacienţi şi, de asemenea, pentru managementul lor perioperatoriu, având ca scop minimizarea riscului de morbi-mortalitate. După cum am menţionat anterior, riscul de evenimente CV legate de ICNC este influenţat atât de factori ce ţin de intervenţia chirurgicală (independenţi de pacient), cât şi de factori dependenţi de pacient, noul ghid ESC subliniind importanţa identificării adecvate a elementelor de risc din ambele categorii pentru a minimiza riscul perioperatoriu.
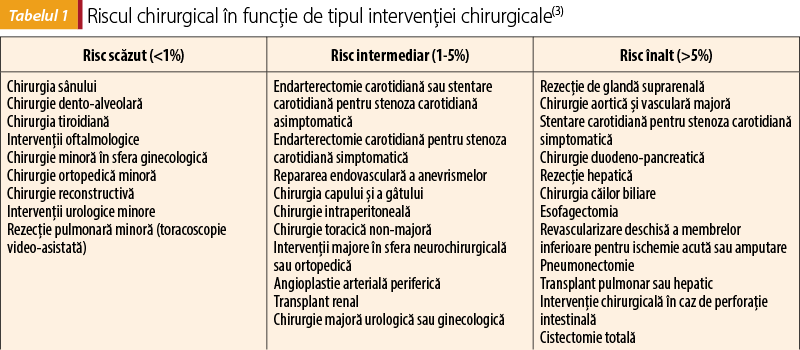
În ceea ce priveşte factorii legaţi de intervenţia chirurgicală, menţionăm că tipul, durata şi gradul de urgenţă al procedurilor reprezintă factori esenţiali care clasifică intervenţiile chirurgicale în trei clase principale de risc (tabelul 1). În general, principalele dileme gravitează în jurul alegerii momentului efectuării intervenţiei: „Procedura trebuie efectuată cât mai precoce, chiar în afara programului de lucru, sau poate aştepta până a doua zi?”, deoarece randamentul operatorului poate fi redus şi, în plus, anumite elemente suportive pot să nu fie disponibile în afara programului de lucru. Acesta este motivul pentru care noul ghid recomandă ca momentul optim să fie discutat de o echipă multidisciplinară.
În plus, Ghidul ESC 2022 face şi recomandări în ceea ce priveşte tipul de tehnică chirurgicală care ar trebui utilizată în funcţie de riscul CV. Prin urmare, procedurile vasculare şi endovasculare, precum şi ICNC asistate video ar trebui utilizate pentru pacienţii cu risc CV crescut (clasa a II-a), deoarece sunt asociate cu mortalitate şi morbiditate mai reduse. Pe de altă parte, la pacienţii cu BCV, laparoscopia nu reduce riscul de evenimente CV la toţi pacienţii, comparativ cu operaţia clasică, deschisă. O explicaţie pentru aceasta ar putea fi reprezentată de efectele hemodinamice ale pneumoperitoneului indus iatrogen şi ale poziţiei Trendelenburg. În consecinţă, ghidul actual recomandă laparoscopia doar în cazul pacienţilor atent selectaţi, în principal al celor vârstnici(4).
Anestezia este un alt factor de risc legat de intervenţia chirurgicală care influenţează semnificativ riscul CV perioperatoriu; modificările hemodinamice intraoperatorii şi managementul durerii postoperatorii sunt principalele probleme ce ar trebui abordate cu atenţie de către medicul anestezist, împreună cu chirurgul curant şi cu medicul cardiolog.
Relaţia dintre tensiunea arterială (TA) intraoperatorie şi morbi-mortalitatea postoperatorie a fost evaluată în numeroase studii, hipotensiunea arterială fiind o problemă importantă care a fost abordată în ultimul Ghid ESC. În ciuda faptului că nu există o valoare-prag universală care să caracterizeze hipotensiunea intraoperatorie, pentru a evita posibila disfuncţie de organ asociată intervenţiei chirurgicale se recomandă ferm evitarea unei scăderi a TA intraoperatorii cu peste 20% faţă de valoarea iniţială sau a unei TA sistolice sub 60-70 mmHg pentru o perioadă mai mare de 10 minute (recomandare clasa IA). În plus, durerea severă după ICNC este o problemă relativ frecventă (5-10% dintre pacienţi), care poate creşte marcant riscul de evenimente CV, în principal din cauza asocierii sale cu activarea simpatică exagerată. Acesta este motivul pentru care ghidul actual recomandă ameliorarea promptă a durerii acute după procedurile chirurgicale (recomandare clasa I), iar în ceea ce priveşte opţiunile terapeutice, nu recomandă medicamentele antiinflamatoare nesteroidiene (cu excepţia aspirinei) ca opţiuni de primă linie pentru pacienţii cu risc crescut de BCV (recomandare clasa III), diclofenacul fiind asociat cu cel mai mare risc CV(5).
După cum am precizat deja, riscul de evenimente CV perioperatorii este puternic influenţat şi de caracteristicile pacientului, precum vârsta şi starea sa preoperatorie. Din acest motiv, o examinare clinică atentă, precum şi o anamneză bine realizată sunt recomandate în cazul tuturor pacienţilor programaţi pentru ICNC. Pe baza acestora, pacienţii vor fi incluşi în diverse clase de risc, în funcţie de care se vor realiza alte explorări individualizate. Aşadar, conform ghidului actual, pacienţii cu vârsta sub 65 de ani, fără semne şi simptome evidente pentru patologii CV şi fără factori de risc CV, pot fi supuşi unor intervenţii chirurgicale din categoria celor cu risc scăzut sau intermediar, fără a fi necesară o evaluare preoperatorie mai amănunţită, explorarea ECG şi utilizarea biomarkerilor putând fi luate în considerare în cazul intervenţiilor chirurgicale cu risc înalt (clasa de recomandare IIA). Cu toate acestea, acei pacienţi care prezintă totuşi antecedente heredocolaterale de cardiomiopatii ar trebui, conform recomandărilor din ghid, să fie evaluaţi ecocardiografic, cu scopul de a exclude o astfel de patologie. Pe de altă parte, pacienţii cu vârsta de peste 65 de ani şi cei care prezintă factori de risc cardiovascular au un risc important de a avea o patologie CV nediagnosticată, precum şi un risc mai mare de a dezvolta complicaţii CV perioperatorii. Din acest motiv, ghidul recomandă efectuarea ECG, precum şi recoltarea de biomarkeri în cazul acelor pacienţi care efectuează intervenţii cu risc intermediar sau crescut (indicaţie de clasă I), testarea capacităţii funcţionale fiind o altă explorare care ar putea fi luată în considerare la aceşti pacienţi (indicaţie de clasă IIA).
O altă categorie de pacienţi discutată în acest ghid este reprezentată de acei bolnavi cu patologii CV deja diagnosticate. În cazul acestora, recomandările sunt asemănătoare cu cele din categoria de pacienţi anterior menţionată, cu precizarea că anterior efectuării intervenţiilor chirurgicale cu risc crescut este necesară o evaluare cardiologică prealabilă. Ultima situaţie clinică discutată este reprezentată de acei pacienţi fără patologie CV documentată, dar cu simptome sugestive recent instalate. În cazul unor sufluri cardiace nou obiectivate, ghidul recomandă efectuarea ecografiei transtoracice atât în cazul pacienţilor cu alte simptome supraadăugate (indicaţie de clasă I), cât şi în cazul celor asimptomatici (indicaţie de clasă IIA). Pacienţii care prezintă durere toracică sugestivă pentru angină pectorală, fără diagnostic de boală coronariană, ar trebui investigaţi suplimentar în vederea investigării etiologiei durerii toracice, atât în cazul unei intervenţii chirurgicale elective, cât şi în cazul uneia în urgenţă (indicaţie de clasă I). În vederea investigării originii dispneei şi a edemelor, în absenţa unei cauze noncardiace evidente, autorii recomandă efectuarea ECG, precum şi recoltarea NT-proBNP/BNP (indicaţie de clasa I), iar în cazul în care probele biologice sunt modificate, se recomandă investigarea ecocardiografică (indicaţie de clasă I)(3).
Un capitol important al noului ghid este dedicat măsurilor preoperatorii ce pot fi adoptate cu scopul de a reduce riscul de apariţie a complicaţiilor CV. Dintre aceste măsuri, controlul factorilor de risc CV, conform noului ghid, reprezintă o opţiune terapeutică uşor de aplicat şi cu rezultate promiţătoare. Astfel, în cazul pacienţilor fumători, oprirea fumatului cu cel puţin patru săptămâni înaintea efectuării unei ICNC elective reprezintă o recomandare de clasă I, studiile asociind această măsură cu o reducere a riscului de complicaţii de orice natură până la şase luni postoperatoriu, fiecare săptămână suplimentară de sevraj asociind o scădere a acestui risc cu până la 19%(6). O altă măsură nonfarmacologică disponibilă este exerciţiul fizic, principalele sale efecte, demonstrate deja de numeroase studii, fiind controlul unor factori de risc CV clasici, precum hipertensiunea arterială, tahicardia, obezitatea sau diabetul zaharat(7). Deşi în prezent există doar studii mici care au evaluat potenţialul recuperării cardiovasculare de a reduce riscul perioperatoriu, analize recente au arătat o reducere a complicaţiilor postoperatorii de până la 67% în cazul pacienţilor care au beneficiat de astfel de programe. Din acest motiv, ghidul precizează că această resursă terapeutică poate fi luată în considerare la pacienţii care sunt programaţi pentru ICNC majore sau complexe.
În privinţa măsurilor farmacologice, ghidul actual oferă câteva indicaţii care vizează principalele clase de medicamente utilizate în tratamentul pacienţilor cardiaci menite să reducă riscul hipotensiunii şi al bradicardiei perioperatorii, precum şi cel al decompensării unor patologii deja diagnosticate, aflate sub tratament cronic. Prima clasă terapeutică discutată este reprezentată de beta-blocante, iar una dintre dilemele dezbătute vizează iniţierea preoperatorie a acestei clase. Recomandările în acest sens diferă în funcţie de situaţia clinică şi de caracteristicile pacientului. Deşi ghidul actual nu recomandă iniţierea de rutină a beta-blocantelor (recomandare de clasă III), în cazul pacienţilor cu doi sau mai mulţi factori de risc CV, care urmează să efectueze o procedură cu risc ridicat, precum şi în cazul pacienţilor cu boală coronariană aterosclerotică documentată, acest lucru poate fi luat în considerare, cu scopul de a reduce incidenţa perioperatorie a infarctului miocardic (indicaţie de clasă IIB). În cazul pacienţilor sub tratament cronic cu beta-blocante, acestea ar trebui continuate perioperatoriu (indicaţie de clasă I), unele studii asociind sevrajul de peste două zile cu o dublare a riscului de fibrilaţie atrială (FiA)(8). În ceea ce priveşte tratamentul cu statine, rezultatele studiilor nu sunt foarte clare, motiv pentru care ghidul nu recomandă iniţierea de rutină a acestora, o excepţie fiind pacienţii ce urmează să efectueze o procedură cu risc înalt (indicaţie de clasă IIA). Totodată, pacienţii aflaţi deja sub terapie cu statine ar trebui să continue tratamentul inclusiv perioperatoriu (indicaţie de clasă I).
În cazul IECA, principalele probleme sunt legate de riscul de hipotensiune, studiile arătând că menţinerea acestora asociază o incidenţă mai mare a hipotensiunii periprocedurale şi a utilizării de medicaţie inotropă şi vasopresoare. Pe de altă parte, sevrajul asociază un risc crescut de hipertensiune postoperatorie şi de decompensare a insuficienţei cardiace (IC), motiv pentru care ghidul face următoarele recomandări: în cazul pacienţilor cu IC stabilă, menţinerea tratamentului cu IECA ar putea fi luată în considerare (indicaţie de clasă IIB), iar în cazul pacienţilor fără IC, administrarea IECA ar trebui temporizată în ziua intervenţiei şi reiniţiată ulterior (indicaţie de clasă IIA). Aceste recomandări se menţin şi în cazul blocantelor de calciu, cu precizarea că unele studii au asociat utilizarea dihidropiridinelor cu o incidenţă mai mare a mortalităţii perioperatorii, în cazul pacienţilor operaţi pentru anevrism aortic(3,9).
Diureticele sunt o altă clasă terapeutică abordată în ultimul ghid în vigoare, dată fiind utilizarea lor pe scară largă pentru tratamentul hipertensiunii arteriale. Şi în cazul acestora, recomandarea este să fie oprite în ziua intervenţiei chirurgicale (indicaţie de clasă IIA), cu acelaşi scop, de a scădea riscul de hipotensiune, o altă problemă legată de acestea fiind riscul de diselectrolitemii, ce pot fi agravate în contextul procedurilor invazive(3).
Nu în ultimul rând, ghidul actual recomandă oprirea inhibitorilor de SGLT-2 cu minimum trei zile anterior efectuării unei intervenţii chirurgicale (indicaţie de clasă IIA) cu risc intermediar sau înalt, scopul fiind acela de a evita cetoacidoza diabetică euglicemică(3).
Managementul terapiei antiagregante plachetare
Luând în considerare faptul că orice intervenţie chirurgicală asociază în mod inevitabil hemoragii de diverse severităţi, un bun management al terapiei antitrombotice şi anticoagulante reprezintă un subiect de mare interes al noului ghid. În ceea ce priveşte medicaţia antitrombotică, decizia continuării sau sistării acesteia este influenţată de raportul dintre riscul hemoragic şi, respectiv, cel trombotic, precum şi de caracteristicile farmacocinetice şi farmacodinamice ale medicamentelor. În cazul pacienţilor aflaţi sub terapie cu aspirină, pentru prevenţie primară, medicaţia antiagregantă poate fi sistată preoperatoriu, iar în cazul bolnavilor cu risc hemoragic crescut, aceasta poate fi oprită pe termen nedefinit, având în vedere riscul trombotic scăzut(3). Adevăratele semne de întrebare se pun în cazul pacienţilor cu istoric de angioplastie coronariană. În cazul acestora, prezenţa implantului coronarian creşte foarte mult riscul trombotic, motiv pentru care terapia antiagregantă devine esenţială. În aceste situaţii, decizia de a opri terapia dublu antiagregantă (DAPT) este influenţată de următorii factori: riscul hemoragic al intervenţiei chirurgicale, timpul scurs de la momentul implantării stentului, precum şi contextul în care a avut loc procedura de revascularizare coronariană (acut sau electiv). Astfel, conform ghidului, în cazul intervenţiilor chirurgicale care nu presupun un risc hemoragic important, terapia DAPT ar trebui continuată periprocedural. În cazul intervenţiilor chirurgicale ce presupun un risc hemoragic crescut, se recomandă oprirea DAPT şi menţinerea doar a antiagregării cu aspirină, însă acest lucru nu este posibil imediat după o procedură de revascularizare coronariană. Astfel, în cazul ICNC elective, ghidul contraindică oprirea DAPT în prima lună de la o procedură de revascularizare coronariană electivă, respectiv în primele trei luni de la o revascularizare pentru un sindrom coronarian acut (SCA). O astfel de procedură ar putea fi realizată după aceste perioade de timp (indicaţii de clasă IIA şi IIB), însă autorii ghidului recomandă menţinerea DAPT pentru minimum şase luni în cazul revascularizărilor elective, respectiv 12 luni în cazul celor acute (indicaţie de clasă I). În cazul ICNC dependente de timp, la un pacient revascularizat electiv în urmă cu mai puţin de o lună sau pentru un SCA debutat cu mai puţin de trei luni în urmă, ghidul oferă opţiunea terapiei de punte cu inhibitori de GpIIb/IIIa sau cangrelor, administraţi intravenos. Indiferent de situaţia la care ne referim, inhibitorii receptorilor pentru ADP (clopidogrel, ticagrelor sau prasugrel) ar trebui opriţi după cum urmează: ticagrelor cu 3-5 zile anterior intervenţiei, clopidogrel cu cinci zile anterior acesteia, iar prasugrel cu şapte zile anterior. Reintroducerea lor ar trebui să se realizeze cât mai precoce după intervenţia chirurgicală, în primele 48 de ore (indicaţie de clasă I)(3).
Managementul terapiei anticoagulante şi tromboprofilaxia trombozei venoase profunde
Gestionarea medicaţiei anticoagulante la pacienţii care urmează să efectueze o intervenţie chirurgicală reprezintă, de asemenea, o provocare pentru clinicieni, mai ales că 25% dintre pacienţii anticoagulaţi vor trece printr-o astfel de procedură(10). Ca şi în cazul terapiei antitrombotice, decizia opririi terapiei anticoagulante va fi luată în funcţie de raportul dintre riscul trombotic şi riscul de sângerare, raport ce este influenţat atât de factori care ţin de procedura chirurgicală (riscul hemoragic al procedurii şi caracterul său urgent sau electiv), cât şi de factori care ţin de pacient (vârstă, riscul trombotic individual, istoric de sângerări, funcţie renală, comorbidităţi sau tratamentul cronic)(3). Cele două clase principale de anticoagulante sunt antivitaminicele K (AVK) (warfarina, acenocumarolul şi fenprocumonul) şi anticoagulantele orale noi (DOAC) (apixaban, rivaroxaban, endoxaban şi dabigatran), acestea fiind tratate separat în ghidul actual, având în vedere caracteristicile lor farmacocinetice şi farmacodinamice diferite.
În cazul AVK, indicaţiile de management perioperatoriu diferă în funcţie de indicaţia pentru care a fost iniţiată terapia, aceasta influenţând riscul trombotic. Astfel, în cazul pacienţilor sub tratament cu AVK pentru proteză valvulară mecanică, menţinerea efectului anticoagulant este crucială, având în vedere riscul trombotic ridicat. În cazul intervenţiilor chirurgicale minore şi al celor în care sângerarea poate fi controlată cu uşurinţă, ghidul recomandă efectuarea lor fără întreruperea prealabilă a AVK, dar cu menţinerea INR la limita inferioară a intervalului terapeutic. În cazul procedurilor cu risc hemoragic crescut, decizia devine puţin mai dificilă, ghidul recomandând terapie de punte cu heparină nefracţionată (HNF) sau heparină cu greutate moleculară mică (indicaţie de clasă IIA), datele din literatură fiind limitate în această situaţie particulară. În cazul utilizării heparinei cu greutate moleculară mică, recomandarea este a se utiliza doze terapeutice, de două ori pe zi, cu monitorizarea activităţii antifactorului Xa, nivelul-ţintă fiind 0,5-1 U/mL. Pacienţii care se află sub tratament cu AVK pentru fibrilaţie atrială sau profilaxia secundară a trombembolismului venos (TEV) nu prezintă risc trombotic semnificativ, astfel încât terapia de punte se indică doar în cazul pacienţilor cu alţi factori care cresc riscul de tromboză. Bolnavii care au necesitat sistarea tratamentului cu AVK trebuie să reiniţieze administrarea medicaţiei în primele 12-24 de ore după procedura invazivă, doza recomandată fiind cea de întreţinere plus 50% pentru două zile. Pacienţii care au necesitat terapie de punte, conform ghidului, trebuie să reînceapă administrarea AVK împreună cu HNF la 24 de ore după procedură, până când INR revine în limite terapeutice.
Referitor la utilizarea tratamentului cu DOAC, se recomandă ca procedurile cu risc mic de sângerare să fie efectuate după 12-24 de ore de la ultima doză administrată, cu indicaţie de clasă IC. Pentru intervenţii cu risc foarte mare de sângerare, cum ar fi anestezia rahidiană sau epidurală, întreruperea tratamentului cu DOAC până la cinci zile (trei zile pentru inhibitorii F Xa sau 4-5 zile pentru dabigatran), cu reluarea ulterioară a DOAC la 24 de ore de la intervenţie (indicaţie de clasă IIA). Dacă există risc de sângerare cu reluarea dozei complete şi anticoagularea depăşeşte riscul de evenimente tromboembolice, amânarea tratamentului anticoagulant până la 48-72 de ore după procedură poate fi luată în considerare, folosind postoperatoriu tromboprofilaxie până la reluarea dozei de DOAC (indicaţie de clasă IIB). Astfel, utilizarea NOAC în doză redusă pentru a scădea riscul postoperatoriu de sângerare nu este recomandată. În privinţa tromboprofilaxiei perioperatorii, se recomandă ca deciziile să fie bazate pe riscul individual şi specific procedurii (indicaţie de clasă I). La pacienţii cu risc scăzut de sângerare perioperatorie, tromboprofilaxia trebuie luată în considerare pentru o durată de până la 14 sau 35 de zile, pentru intervenţiile la genunchi sau, respectiv, artroplastie de şold (indicaţie de clasă IIA). Administrarea de DOAC în doză de tromboprofilaxie poate fi luată în considerare ca tratament alternativ la HNF, după artroplastia totală de genunchi şi şold, cu risc crescut de TEV perioperatoriu.
Tromboprofilaxia trebuie iniţiată în timpul spitalizării până la 12 ore înainte de ICNC şi continuată postoperatoriu, în funcţie de pacient şi de evaluarea riscului de sângerare. În cele mai multe cazuri, tromboprofilaxia trebuie continuată până când pacientul se poate mobiliza sau până la externare (de obicei, până la 10 zile). Profilaxia TEV dincolo de externare nu este recomandată în mod obişnuit în majoritatea cazurilor; dintre acestea, un TEV anterior este cel mai puternic predictor de risc(3).
Situaţii specifice
În practica zilnică, de cele mai multe ori, pacienţii care necesită tratament chirurgical prezintă multiple alte comorbidităţi, de multe ori chiar CV, care cresc morbi-mortalitatea perioperatorie. Din acest motiv, o bună gestionare a tratamentului, precum şi a protocolului de monitorizare a acestora reprezintă un element important, necesar reducerii riscului de evenimente CV asociate intervenţiei invazive. Insuficienţa cardiacă (IC), o boală frecventă în populaţia generală, cu o prevalenţă în creştere chiar şi în rândul pacienţilor sub 65 de ani(11), reprezintă un factor de risc consacrat pentru mortalitatea postoperatorie. Dintre factorii determinanţi ai riscului asociat IC, fracţia de ejecţie şi gradul compensării hemodinamice sunt printre cei mai importanţi, ghidul nerecomandând efectuarea ICNC elective la pacienţii decompensaţi(3,12). Totodată, orice intervenţie chirurgicală, prin stresul hemodinamic asociat, reprezintă un factor de risc important pentru decompensarea IC, motiv pentru care este esenţială menţinerea tratamentului optimal al bolii, conform ghidurilor specifice, precum şi evaluarea cu regularitate a statusului volemic (indicaţie de clasă I). Pentru ICNC ce asociază risc intermediar sau înalt, monitorizarea invazivă a tensiunii arteriale poate reprezenta o opţiune pentru o mai bună gestionare a statusului hemodinamic al pacienţilor(3). În cazul decompensării postoperatorii a IC, ghidul recomandă înregistrarea ECG, dozarea markerilor de citoliză cardiacă, precum şi explorarea ecocardiografică, în vederea optimizării tratamentului de bază. În pofida existenţei unui panel extins de biomarkeri cu rol prognostic dovedit în ICA (ex.: ST2, GDF-15), actualmente aceştia nu sunt indicaţi în determinările de rutină, studii suplimentare fiind necesare în acest sens(13).
O altă patologie care influenţează considerabil prognosticul CV perioperatoriu este cea valvulară, riscul fiind cel mai ridicat în cazul bolilor obstructive (stenoza aortică şi cea mitrală)(14). Având în vedere acest lucru, orice pacient cunoscut sau la care suspicionează o astfel de patologie şi care este programat pentru o ICNC electivă ce asociază un risc intermediar sau crescut ar trebui evaluat clinic şi ecocardiografic, în vederea cuantificării severităţii valvulopatiei. Totodată, pacienţii cu boală valvulară uşoară sau moderată documentată prezintă indicaţie de reevaluare ecocardiografică dacă aceasta nu a fost realizată în ultimul an(3).
Pentru pacienţii cu stenoză aortică, managementul perioperatoriu este influenţat de următorii factori: prezenţa simptomelor, severitatea stenozei, precum şi coexistenţa altor boli cardiace. Aşadar, în cazul unei stenoze severe, din bilanţul preoperatoriu nu trebuie să lipsească evaluarea clinică, ECG, biomarkerii de injurie cardiacă, ecografia transtoracică şi cea transesofagiană în cazurile selectate (indicaţie de clasă I). De asemenea, pacientul trebuie să primească tratament medicamentos, conform ghidului, pentru a asigura o bună compensare a bolii (indicaţie de clasă I). În cazul pacienţilor simptomatici, programaţi la o procedură ce asociază un risc scăzut, aceasta poate fi realizată fără alte intervenţii terapeutice. În schimb, în cazul ICNC cu risc intermediar sau crescut, ghidul recomandă efectuarea înlocuirii valvulare (prin TAVI sau chirurgical), anterior efectuării procedurii, dacă riscul perioperatoriu permite acest lucru (indicaţie de clasă I). În cazul pacienţilor la risc înalt pentru înlocuirea de valvă sau al celor care necesită o ICNC dependentă de timp, alternativa oferită de ghid este plastia cu balon sau, dacă aceasta nu este posibilă, efectuarea procedurii sub monitorizare atentă (indicaţie de clasă IIB). Pentru pacienţii asimptomatici, funcţia sistolică la ventriculul stâng (VS) reprezintă un criteriu decizional important, pacienţii cu fracţie de ejecţie de peste 50% putând efectua procedura invazivă fără a fi necesare proceduri suplimentare. Doar pacienţii cu disfuncţie sistolică de VS, programaţi la o intervenţie cu risc crescut, prezintă indicaţie de înlocuire valvulară (indicaţie de clasă IIA)(3).
Conform ghidului, pacienţii cu stenoză mitrală uşoară sau chiar moderat-severă, dar cu tensiunea arterială pulmonară sistolică mai mică de 50 mmHg (PAPs), pot efectua ICNC, riscul asociat pentru complicaţii fiind relativ mic(15). Pe de altă parte, stenoza mitrală moderat-severă şi simptomatică sau cea asimptomatică, dar care asociază PAPs mai mare de 50 mmHg, prezintă indicaţie de comisurotomie preoperatorie, în cazul intervenţiilor la risc ridicat(3). Regurgitarea mitrală severă în sine nu reprezintă o contraindicaţie pentru o intervenţie chirurgicală. Totuşi, prezenţa simptomelor, în ciuda tratamentului corespunzător, ar putea pune în discuţie, în cazul procedurilor la risc intermediar sau înalt, cura chirurgicală preoperatorie a valvulopatiei mitrale (indicaţie de clasă IIA)(3).
Pentru regurgitarea aortică severă, ghidul recomandă adresarea chirurgicală a valvulopatiei, înaintea efectuării ICNC, doar în cazul procedurilor cu risc intermediar sau înalt, la pacienţii simptomatici sau asimptomatici, dar cu PAPs>50 mmHg, diametru telediastolic al VS>50 mm sau FEVS ≤50%. Aritmiile reprezintă un grup de patologii complexe şi relativ frecvente în rândul pacienţilor care suferă de boli cardiovasculare, iar potenţialele tulburări electrolitice produse de intervenţiile invazive pot complica aceste tulburări de ritm.
Fibrilaţia atrială, o aritmie supraventriculară, care uneori trece neobservată de către pacient, acesta fiind asimptomatic, poate fi o descoperire întâmplătoare în cazul bilanţului preoperatoriu. În această situaţie, managementul corespunzător constă în profilaxia tromboembolică şi controlul frecvenţei, controlul ritmului fiind indicat doar în cazul pacienţilor care rămân simptomatici, în ciuda unei frecvenţe cardiace mai mici de 100/min. Pentru controlul frecvenţei, ghidul recomandă utilizarea beta-blocantelor şi a blocantelor de calciu non-dihidropiridinice, digoxinul fiind ineficient în contextul unei încărcări adrenergice substanţiale, cum este cazul intervenţiilor chirurgicale. În cazul pacienţilor simptomatici, care necesită cardioversie, flecainida şi propafenona sunt principalele medicamente recomandate de ghid în cazul pacienţilor fără boală cardiacă structurală. Pentru pacienţii cu insuficienţă cardiacă cronică uşoară, autorii recomandă vernakalant intravenos, acesta fiind considerat medicamentul care permite cardioversia cea mai rapidă. În cazul pacienţilor instabili hemodinamic, indicaţia de clasă I este cardioversia electrică, în timp ce amiodarona poate fi utilizată pentru controlul acut al frecvenţei cardiace (indicaţie de clasă IIB).
Aritmiile ventriculare sunt o altă entitate clinică ce poate complica managementul perioperatoriu al pacienţilor. Dintre acestea, extrasistolele ventriculare (ESV) şi tahicardia ventriculară nesusţinută sunt cele mai frecvente. Deşi iniţial erau considerate benigne, studii recente au demonstrat că acestea ar putea asocia un prognostic prost, chiar şi la pacienţii fără o boală structurală cardiacă evidentă, mai ales atunci când au o frecvenţă mai mare de 10-20%. Acest tip de aritmii nu necesită tratament în cazul unor intervenţii urgente, atât timp cât nu sunt frecvente sau simptomatice, ba mai mult, în cazul ESV asimptomatice, este contraindicată iniţierea preoperatorie a tratamentului medicamentos (indicaţie de clasă III). În cazul intervenţiilor elective, mai ales atunci când sunt frecvente, simptomatice sau complexe, şi la pacienţii cu istoric familial de moarte cardiacă subită, ghidul indică realizarea unui bilanţ preoperatoriu pentru excluderea unei patologii cardiace subiacente. Tahicardia ventriculară (TV) susţinută şi fibrilaţia ventriculară (FV) necesită, conform ghidului, explorări suplimentare pentru excluderea unei disfuncţii ventriculare severe, precum şi a bolii coronariene aterosclerotice. În cazul TV monomorfe, pentru care s-a exclus o boală structurală sau o disfuncţie a sistemului excitoconductor, autorii nu recomandă tratament medicamentos, decât în cazul în care sunt simptomatice. Dacă bilanţul preoperatoriu obiectivează drept cauză a aritmiei o cicatrice cardiacă, iar TV este recurentă, în ciuda tratamentului medicamentos, indicaţia este de ablaţie preoperatorie (indicaţie de clasă I).
Nu doar tahiaritmiile reprezintă o problemă frecventă în practica zilnică, ci şi bradiaritmiile. În cazul unui pacient care suferă de o astfel de patologie, ce determină instabilitate hemodinamică neresponsivă la tratament medicamentos, ghidul recomandă pentru intervenţiile chirurgicale în urgenţă cardiostimularea temporară, în cazul celor elective fiind necesară temporizarea procedurii chirurgicale până după momentul implantării unui cardiostimulator permanent. Pacienţii cu bloc bifascicular se află la risc ridicat de bloc atrioventricular total. Cu toate acestea, ghidul nu recomandă cardiostimulare temporară profilactică, ci tratament medicamentos; totuşi, ICNC ar trebui realizată în prezenţa echipamentului necesar pentru cardiostimulare transcutanată.
Fiind un subiect de actualitate, dar, mai mult decât atât, un factor de risc CV important, ce poate decompensa o patologie CV preexistentă, noul ghid include o secţiune separată ce discută managementul pacientului diagnosticat preoperatoriu sau recent cu infecţie cu SARS-CoV-2. Conform unor studii recente, infecţia cu noul tip de coronavirus se asociază cu o mortalitate şi un risc perioperatoriu de TEV crescute, până la şapte săptămâni după diagnostic. Totodată, injuria miocardică asociată infecţiei, deşi cu un mecanism fiziopatologic încă neclar, ar putea creşte riscul intrinsec perioperatoriu de reacţii adverse CV(16,17). Deşi nu există încă un protocol specific de screening preoperatoriu la această categorie de pacienţi, ghidul recomandă, pe lângă investigaţiile perioperatorii de bază, evaluarea severităţii infecţiei, a istoricului complicaţiilor CV din timpul infecţiei, precum şi a capacităţii funcţionale, după recuperare. Toate aceste informaţii sunt menite să ajute clinicianul să stabilească momentul oportun al unei intervenţii cardiace elective. Conform unor ghiduri ale societăţilor americane, în cazul pacienţilor nevaccinaţi, intervenţia chirurgicală electivă ar trebui amânată timp de şapte săptămâni, cu scopul de a evita riscurile amintite(3).
Nu în ultimul rând, în ghidul din 2022 este abordată problema pacienţilor cu boală coronariană aterosclerotică. În cazul acestora, riscul perioperatoriu este influenţat de riscul CV de bază, de tipul intervenţiei chirurgicale şi de indicaţia intervenţiei (electivă sau în urgenţă). Pentru pacienţii cu sindrom coronarian cronic, ghidul recomandă, în primul rând, tratament medicamentos optimal (indicaţie de clasă I), în cazul ICNC ce asociază un risc scăzut nefiind necesare alte măsuri terapeutice, în măsura în care simptomele sunt controlate. Pentru intervenţiile cu risc intermediar sau crescut, bilanţul preoperatoriu ar trebui să includă examinare clinică, ECG, recoltarea biomarkerilor de citoliză cardiacă (indicaţie de clasă I), precum şi ecocardiografie. În cazul în care acestea sunt sugestive pentru ischemie miocardică sau în cazul în care pacientul este simptomatic, se indică efectuarea explorării coronarografice, preoperatoriu, şi discutarea necesităţii revascularizării leziunilor în cadrul unei echipe multidisciplinare. Pentru pacienţii care dezvoltă sindrom coronarian acut, preoperatoriu, indicaţia este de a urma recomandările ghidului specifice acestei patologii (indicaţie de clasă I)(3).
Concluzii
Managementul perioperatoriu al patologiilor cardiovasculare rămâne o provocare pentru practica zilnică, aceşti bolnavi având adesea un status clinic fragil. Patologiile care pun cele mai multe probleme sunt îndeosebi cele care implică tratamente precum anticoagulante sau antiagregante, ce cresc riscul periprocedural de hemoragie, în aceste cazuri decizia terapeutică fiind bazată pe punerea în balanţă a riscului trombotic şi, respectiv, a celui hemoragic. Noul ghid al Societăţii Europene de Cardiologie adresează aceste probleme, alături de multe altele, oferind totodată recomandări ce ajută clinicienii să personalizeze deciziile terapeutice perioperatorii, astfel încât pacientul să fie expus unui risc minim.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Weiser TG, Regenbogen SE, Thompson KD, Haynes AB, Lipsitz SR, Berry WR, Gawande AA. An estimation of the global volume of surgery: a modelling strategy based on available data. Lancet. 2008;372(9633):139-144.
- Smilowitz NR, Gupta N, Guo Y, Beckman JA, Bangalore S, Berger JS. Trends in cardiovascular risk factor and disease prevalence in patients undergoing non-cardiac surgery. Heart. 2018;104(14):1180-1186.
- Halvorsen S, Mehilli J, Cassese S, et al. 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery. Eur Heart J. 2022;43(39):3826-3924.
- Keus F, Gooszen HG, van Laarhoven CJ. Open, small-incision, or laparoscopic cholecystectomy for patients with symptomatic cholecystolithiasis. An overview of Cochrane Hepato-Biliary Group reviews. Cochrane Database Syst Rev. 2010, 2010:CD008318.
- Ray WA, Varas-Lorenzo C, Chung CP, Castellsague J, Murray KT, Stein CM,
- et al. Cardiovascular risks of nonsteroidal antiinflammatory drugs in patients after hospitalization for serious coronary heart disease. Circ Cardiovasc Qual Outcomes. 2009;2:155-163.
- Lee SM, Landry J, Jones PM, Buhrmann O, Morley-Forster P. Long-term quit rates after a perioperative smoking cessation randomized controlled trial. Anesth Analg. 2015;120, 582–587.
- Jigoranu RA, Mitu O, Oancea AF, Miftode RS, Timpau AS, Haba MSC, Gavril RS, Cumpat C, Mitu F. The Effects of Cardiac Rehabilitation on Resting Heart Rate and Blood Pressure In Heart Failure Patients. Med Surg J. 2022;126(3):36-342.
- Longrois D, Couffignal C, Ait-Hamou N, Amour J, Cholley B, Dilly M, et al. Indispensable optimisation de la réintroduction des bêtabloquants après chirurgie cardiaque. Résultats de l’étude Bêtabloquants Avant et Après Chirurgie Cardiaque (BBAACC). Anesthésie & Réanimation. 2015;1:A248.
- Kertai MD, Westerhout CM, Varga KS, Acsady G, Gal J. Dihydropiridine calcium-channel blockers and perioperative mortality in aorticaneurysm surgery. Br J Anaesth. 2008;101:458-465.
- Beyer-Westendorf J, Gelbricht V, Forster K, Ebertz F, Kohler C, Werth S, et al. Peri-interventional management of novel oral anticoagulants in daily care: results from the prospective Dresden NOAC registry. Eur Heart J. 2014;35:1888–1896.
- Robinson JG, Williams KJ, Gidding S, et al. Eradicating the Burden of Atherosclerotic Cardiovascular Disease by Lowering Apolipoprotein B Lipoproteins Earlier in Life. J Am Heart Assoc. 2018;7(20):e009778.
- Flu WJ, van Kuijk JP, Hoeks SE, Kuiper R, Schouten O, Goei D, et al. Prognostic implications of asymptomatic left ventricular dysfunction inpatients undergoing vascular surgery. Anesthesiology. 2010;112:1316–1324.
- Miftode RS, Constantinescu D, Cianga CM, Petris AO, Timpau AS, Crisan A, Costache II, Mitu O, Anton-Paduraru DT, Miftode IL, Pavel-Tanasa M, Cianga P, Serban IL. A Novel Paradigm Based on ST2 and Its Contribution towards a Multimarker Approach in the Diagnosis and Prognosis of Heart Failure: A Prospective Study during the Pandemic Storm. Life (Basel). 2021;11(10):1080.
- Agarwal S, Rajamanickam A, Bajaj NS, Griffin BP, Catacutan T, Svensson LG, et al. Impact of aortic stenosis on postoperative outcomes afternon cardiac surgeries. Circ Cardiovasc Qual Outcomes. 2013;6:193–200.
- Sohrabi B, Kazemi B, Mehryar A, Teimouri-Dereshki A, Toufan M, Aslanabadi N. Correlation between pulmonary artery pressure measured by echocardiography and right heart catheterization in patients with rheumatic mitral valve stenosis (a prospective study). Echocardiography. 2016;33:7-13.
- Guzik TJ, Mohiddin SA, Dimarco A, Patel V, Savvatis K, Marelli-Berg FM. COVID-19 and the cardiovascular system: implications for risk assessment, diagnosis, and treatment options. Cardiovasc Res. 2020;116:1666-1687.
- Timpau AS, Miftode RS, Leca D, Timpau R, Miftode IL, Petris AO, Costache II, Mitu O, Nicolae A, Oancea A, Jigoranu A, Tuchilus CG, Miftode EG. A Real Pandora’s Box in Pandemic Times: A Narrative Review on the Acute Cardiac Injury Due to COVID-19. Life (Basel). 2022;12(7):1085.


