Indicaţiile hemodializei intermitente și continue
Indications of intermittent and continuous hemodialysis
Abstract
Intermittent hemodialysis (HDI) is a useful and effective way of feasible improvement in dog and cat kidney analyzes that do not respond adequately to medical management Decision to choose hemodialysis in patients with acute or acute kidney disease with chronic tendency should be taken as soon as possible to improve the probability of a successful result. The goal of HDI is make dramatic changes in patient status in regarding uremia, acidosis and overloading withf luids for short periods of time. continue therapy by renal substitution (TCSR) is a more recently developed method of purifying blood. HDI can be considered appropriate when medical management does not manages to achieve the goals outlined above. Therefore, HDI is indicated in cases of significant uremia or even increasing, electrolyte imbalances or acidosis, who do not answer medical management. HDI is, also indicated in cases where oliguria and / or Anuria does not respond to adequate medical management with diuretics. TCSR can be used for patients with leptospirosis, tumor lysis syndrome, insolation, support pre- and postoperative ureteral obstruction, as well as in aminoglycoside and melamine poisoning. TCSR can be also used to remove from the body certain drugs and toxins. TCSR indications in dog include severe uremia with fluid overload, sepsis and other inflammatory syndromes. TCSR is a continuous process and, once the treatment is started, therapy continues to when renal function returns or the patient is transferred to intermittent dialysis. TCSR has several advantages significant compared to HDI. Slow and gradual nature of the technique provides better control of electrolytes and the like acid-base balance. This continuous process is approaching more than the functionality of a normal kidney. The use convection in TCSR confers a significant advantage in removing molecules larger than by diffusion.Keywords
hemodialysisdogscatsindicationsRezumat
Hemodializa intermitentă (HDI) este o modalitate utilă și fezabilă de îmbunătățire a analizelor la câinii și pisicile cu afecțiuni renale care nu răspund adecvat managementului medical. Decizia de a alege hemodializa la pacienții cu afecțiuni renale acute sau acute cu tendință de cronicizare trebuie luată cât mai repede posibil pentru a îmbunătăți probabilitatea unui rezultat reușit. Scopul HDI este de a realiza schimbări dramatice în statusul pacientului în ceea ce privește uremia, acidoza și supraîncărcarea cu fluide pe perioade scurte de timp. Terapia continuă de substituție renală (TCSR) este o metodă de purificare a sângelui mai recent dezvoltată. HDI poate fi considerată adecvată atunci când managementul medical nu reușește să atingă obiectivele expuse mai sus. Așadar, HDI este indicată în cazurile de uremie semnificativă sau chiar în creștere, dezechilibre electrolitice sau acidoză, care nu răspund managementului medical. HDI este, de asemenea, indicată în cazurile în care oliguria și/sau anuria nu răspund managementului medical adecvat cu diuretice. TCSR poate fi utilizată pentru pacienții cu leptospiroză, sindrom de liză tumorală, insolație, în suportul pre- și postoperator al obstrucțiilor ureterale, precum și în intoxicațiile cu aminoglicozide și melamină. TCSR poate fi, de asemenea, utilizată pentru a elimina din organism anumite medicamente și toxine. Indicațiile TCSR la câine includ uremie severă cu supraîncărcare cu fluide, sepsis și alte sindroame inflamatorii. TCSR este un proces continuu și, odată ce începe tratamentul, terapia continuă până când funcția renală revine sau pacientul este transferat la dializă intermitentă. TCSR are mai multe avantaje semnificative în comparație cu HDI. Natura lentă și treptată a tehnicii asigură un control mai bun al electroliților și al echilibrului acido-bazic. Acest proces continuu se apropie mai mult de funcționalitatea unui rinichi normal. Utilizarea convecției în TCSR conferă un avantaj semnificativ în îndepărtarea unor molecule mai mari decât prin difuzie.Cuvinte Cheie
hemodializacâinipisiciindicațiiHemodializa intermitentă și continuă
Hemodializa intermitentă (HDI) este o terapie de substituție renală, definită prin ședințe scurte și eficiente de hemodializă, cu scopul de a elimina toxinele endogene sau exogene din fluxul sangvin. Indicațiile frecvente pentru HDI includ ingestia de substanțe sau toxine, afecțiuni renale acute sau acute cu tendință de cronicizare și boalarenală cronică (BRC). Ședințele pot fi efectuate o singură dată, cum este des întâlnit în ingestia toxinelor, sau pot fi repetate zilnic ori în fiecare zi pentru câteva zile sau mai mult, așa cum se întâmplă adesea în cazul afecțiunilor renale acute (ARA). Ședințele de hemodializă pot fi planificate de două sau trei ori pe săptămână pe durata întregii vieți a pacientului, așa cum se procedează în bolile renale cronice (BRC). Durata ședințelor este în mod normal de una până la 6 ore, dar pot fi și mai lungi, în funcție de stabilitatea pacientului și de eficiența ședinței în sine. HDI este concepută ca fiind o terapie mai eficientă decât terapia continuă de substituție renală (TCSR), ceea ce înseamnă că ședințele de HDI elimină moleculele dializabile mici (inclusiv ureea din sânge [BUN], creatinina, fosforul, electroliții și anumite medicamente și toxine) mai rapid decât TCSR. Între ședințele de dializă, aceste molecule dializabile pot crește din nou în sânge.
Terapia continuă de substituție renală (TCSR) este o metodă de purificare a sângelui recent dezvoltată. TCSR este un proces continuu și, odată ce începe tratamentul, terapia continuă până când funcția renală revine sau pacientul este transferat către dializă intermitentă. TCSR este similară cu HDI, deoarece sângele pacientului trece prin mii de membrane semipermeabile conținute într-un dializor. Cu toate acestea, în timp ce HDI este în primul rând o terapie difuză, TCSR utilizează difuzia, convecția și, într-o măsură mai mică, adeziunea. TCSR are avantaje semnificative în comparație cu HDI. Natura lentă și treptată a tehnicii asigură un control mai bun al electroliților și al echilibrului acido-bazic. Acest proces continuu se apropie mai mult de funcția unui rinichi normal. Utilizarea convecției în TCSR conferă un avantaj semnificativ față de difuzie în îndepărtarea moleculelor mai mari. Aceste molecule mai mari sunt mai aproape de dimensiunea celor care sunt în mod normal filtrate de rinichi. Scopul HDI este de a aduce schimbări dramatice în statusul pacientului în ceea ce privește uremia, acidoza și supraîncărcarea cu fluide pe perioade scurte de timp, utilizând difuzia; așadar, cantități mari de soluție de dializat pur trebuie să fie produse la fața locului. Utilizarea eficientă a difuziei și a convecției în TCSR permite utilizarea de lichide sterile preambalate, iar aparatele de TCSR nu necesită mentenanță între tratamente.
Indicațiile hemodializei intermitente
Afecțiunea renală acută (ARA) sau afecțiunea renală acută cu tendință de cronicizare apare ca urmare a deteriorării acute a funcțiilor hemodinamice, de filtrare sau de excreție ale rinichiului. Scăderea bruscă a vitezei de filtrare glomerulară duce la acumularea de toxine uremice și deșeuri metabolice în fluxul sanguin, producând o dereglare a cantității de fluide, a electroliților și a echilibrului acido-bazic. Un algoritm de diagnostic care include următoarele criterii poate fi utilizat pentru a stabili gradul ARA. Principalele criterii pentru diagnosticarea ARA sunt debutul acut al semnelor clinice (<7 zile) și creșterea creatininei sau creșterea nivelului BUN, în ciuda fluidoterapiei corespunzătoare adaptate nevoilor electrolitice ale pacientului. Criteriile de susținere pentru diagnosticarea ARA sunt:
- valorile normale din ultima lună ale creatininei;
- ischemia recentă cunoscută;
- ingestia unor substanțe nefrotoxice;
- confirmarea morfologică a leziunilor renale acute și revenirea creatininei la valorile normale.
La câini, cele mai frecvente cauze ale ARA includ ischemia și ingestia toxinelor. Evenimentele ischemice pot fi cauzate de pancreatită, hipovolemie, sepsis, coagulare intravasculară diseminată (CID), anestezie generală sau alte cauze.
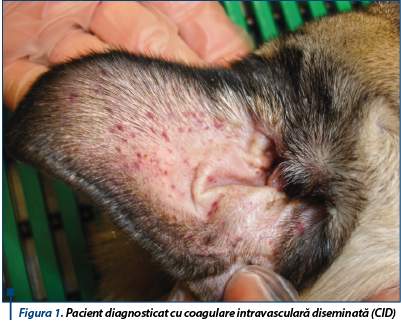
Cea mai frecventă substanță nefrotoxică ingerată de câini este etilenglicolul, deși ARA a fost raportată consecutiv mai multor toxine, inclusiv strugurii și stafidele, aminoglicozidele, agenții chimioterapeutici, cum ar fi cisplatina și ifosfamida, și medicamentele antiinflamatoare nesteroidiene (AINS). Leptospiroza este una dintre cele mai frecvente cauze ale ARA la câini, iar dializa peritoneală sau hemodializa poate să îmbunătățească rezultatul la câinii cu infecții severe. La pisici, cele mai frecvente cauze ale ARA sunt factorii toxici și ischemici. Cea mai frecventă plantă nefrotoxică ingerată de pisici este crinul din genurile Lilium și Hemerocallis, deși ARA mai poate fi cauzată și de etilenglicol, precum și de o varietate de medicamente, cum ar fi aminoglicozidicele, AINS și agenți chimioterapeutici. Obstrucția ureterală parțială sau completă poate duce la leziuni renale acute sau cronice, cel mai frecvent ca urmare a urolitiazei pe bază de calciu. Recent, s-a demonstrat că acești calculi solidificați din sânge pot provoca obstrucție ureterală la pisici. Unii clinicieni definesc obstrucția uretrei la pisici ca fiind o indicație clară pentru dializă.
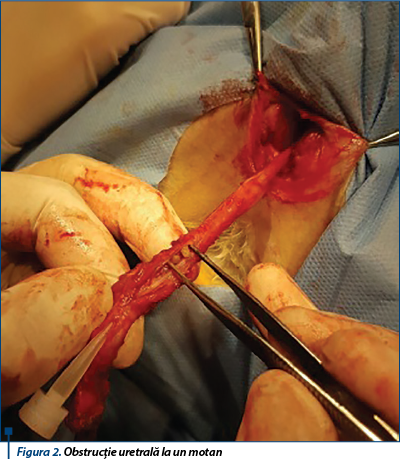
La câini, pielonefrita bacteriană, obstrucția ureterală și ruptura tractului urinar pot provoca ARA. Pielonefrita bacteriană este frecvent cauzată de infecția de la nivelul tractului urinar inferior, dar mai poate fi cauzată și de răspândirea hematogenă a acesteia. Obstrucția ureterală este foarte frecvent întâlnită la pisici și câini de talie mică, fiind cauzată de ureteroliți pe bază de calciu sau de traume ureterale, neoplazii sau inflamații. Distrugerea tractului urinar poate fi cauzată de traume, necroză de presiune consecutivă urolitiazei sau de intervenții chirurgicale.

Gestionarea inițială a leziunilor acute sau acute cu tendință de cronicizare include administrarea fluidoterapiei, corectarea hipovolemiei, corectarea dezechilibrelor minerale, electrolitice și acido-bazice, terapia simptomatică a uremiei și suportul nutrițional. Tratamentul include, de asemenea, și îndepărtarea cauzei inițiale a leziunii renale, dacă este posibil. Multe cauze ale ARA sunt potențial reversibile; pacienții pot deceda din cauza complicațiilor uremiei înainte de inițierea terapiei sau de apariția recuperării renale. HDI este indicată atunci când managementul medical nu reușește să atingă obiectivele expuse mai devreme. Așadar, HDI este indicată în cazurile de azotemie semnificativă sau în creștere, dezechilibre electrolitice sau acidoză, care nu răspund la managementul medical. HDI este, de asemenea, indicată și în cazurile de oligurie și anurie care nu răspund managementului medical adecvat cu diuretice.
Înainte de a recomanda HDI, trebuie luat în considerare dacă pacientul dumneavoastră este hidratat în mod adecvat, dacă hipovolemia și hipotensiunea sunt corectate prin intermediul fluidoterapiei și dacă pacientul a fost deja supus unei terapii cu diuretice în cazul oliguriei sau anuriei. Dacă toate problemele de mai sus au fost verificate și managementul medical nu reușește încă să îmbunătățească simptomatologia pacientului sau dacă severitatea bolii pune viața pacientului în pericol, se impune recomandarea HDI.
Indicațiile hemodializei continue
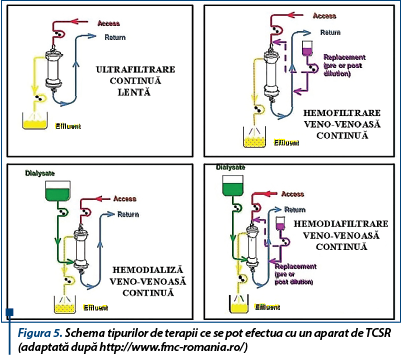
Terapia continuă de substituție renală (TCSR) este o formă continuă de înlocuire a funcției renale și este utilizată pentru a trata afecțiunile renale acute (ARA) la pacienții în stare critică. Terapiile ce se pot efectua cu un aparat de TCSR sunt:
- ultrafiltrare continuă lentă (SCUF);
- hemofiltrare veno-venoasă continuă (CVVH);
- hemodializa veno-venoasă continuă (CVVHD);
- hemodiafiltrare veno-venoasă continuă (CVVHDF).
Infuzarea continuă a fluidelor de substituție permite îndepărtarea fluidului fără contracția volumului intravascular și oferă o stabilitate hemodinamică mai bună, control metabolic la parametri aproape normali și eliminarea toxinelor și citokinelor de dimensiuni mari.
Cea mai frecventă indicație pentru TCSR este tratamentul ARA în cazurile în care este de așteptat ca funcția renală să revină în viitorul apropiat sau pentru pacienții care urmează să fie transferați la HDI. TCSR poate fi utilizată pentru pacienții cu leptospiroză, sindromul de liză tumorală, insolație, suportul pre- și postoperator al obstrucțiilor ureterale, precum și cu intoxicații cu aminoglicozide și melamină. TCSR poate fi, de asemenea, utilizată pentru a elimina anumite substanțe medicamentoase și toxine. Indicațiile TCSR la câini includ și îmbunătățirea azotemiei, acompaniată de supraîncărcare cu fluide.
Sepsisul și alte sindroame inflamatorii, cum ar fi sindromul de insuficiență respiratorie acută (SIRA), reprezintă cele mai frecvente indicații non-renale pentru TCSR. Ipoteza de bază este că hemofiltrarea îndepărtează mediatorii inflamatori din circulație și, prin urmare, atenuează răspunsul inflamator sistemic, păstrând în același timp efectele locale, care sunt considerate a fi benefice. În cazul insuficienței cardiace congestive (ICC), fluxul sangvin sistemic redus este perceput ca fiind un volum circulant redus în totalitate, având ca rezultat activarea mai multor sisteme neuroumorale, cum ar fi sistemul simpatic și sistemul renină-angiotensină-aldosteron, și eliberarea vasopresinei. Unii pacienți rămân refractari la tratamentul medical, iar la acești pacienți îndepărtarea lichidelor și a sodiului poate fi obținută prin ultrafiltrare simplă. Capacitatea oricărei terapii extracorporale de a îndepărta o substanță depinde de mărimea moleculei, de volumul său de distribuție, precum și de gradul de legare a acesteia la proteine. Moleculele mici, cu un volum minim de distribuție și cu o capacitate scăzută de legare la proteine, sunt cel mai ușor de îndepărtat.
Bibliografie
1. Adin C.A., Cowgill L.D., Treatment and outcome of dogs with leptospirosis: 36 cases (1990–1998), J Am Vet Med Assoc 2000;216(3):371-5.
2. Beckel N.F., O’Toole T.E., Rozanski E.A., et al., Peritoneal dialysis in the management of acute renal failure in 5 dogs with leptospirosis, J Vet Emerg Crit Care 2005; 15(3):201-5.
3. Behrend E.N., Grauer G.F., Mani I., et al., Hospital-acquired acute renal failure in dogs: 29 cases (1983-1993), J Am Vet Med Assoc 1996;208(4):537-41.
4. Bjorling D.E., Traumatic injuries of the urogenital system, Vet Clin North Am Small Anim Pract 1984;14(1):61-76.
5. Bloom C.A., Labato M.A., (2011), Intermittent hemodialysis for small animals, Veterinary Clinics of North America: Small Animal Practice, 41(1), 115-133.
6. Cerdá J., Ronco C., (2009), The Clinical Application of Crrt-Current Status: Modalities of Continuous Renal Replacement Therapy: Technical and Clinical Considerations, In Seminars in dialysis (Vol. 22, No. 2, pp. 114-122), Blackwell Publishing Ltd.
7. Cianciolo R.E., Bischoff K., Ebel J.G., et al., Clinicopathologic, histologic, and toxicologic findings in 70 cats inadvertently exposed to pet food contaminated with melamine and cyanuric acid, J Am Vet Med Assoc 2008;233(5):729-37.
8. Diehl S.H., Seshadri R., Use of continuous renal replacement therapy for treatment of dogs and cats with acute or acute-on-chronic renal failure: 33 cases (2002–2006), J Vet Emerg Crit Care 2008;18(4):370-82.
9. Eubig P.A., Brady M.S., Gwaltney-Brant S.M., et al., Acute renal failure in dogs after the ingestion of grapes or raisins: a retrospective evaluation of 43 dogs (1992–2002), J Vet Intern Med 2005;19(5):663-74.
10. Groman R., Apheresis in veterinary medicine: therapy in search of a disease in: Proceedings of the Advanced Renal Therapies Symposium. 2010. pp. 26-32.
11. Humes H.D., Buffington D.A., MacKay S.M., Funke A.J., Weitzel W.F., (1999), Replacement of renal function in uremic animals with a tissue-engineered kidney, Nature biotechnology, 17(5).
12. Langston C.E., Acute renal failure caused by lily ingestion in six cats, J Am Vet Med Assoc 2002;220(1):49–52.
13. Rumbeiha W.K., Agnew D., Maxie G., et al., Analysis of a survey database of pet food-induced poisoning in North America. J Med Toxicol 2010;6:172-84.
14. Schetz M., (1999), Non-renal indications for continuous renal replacement therapy, Kidney International, 56, S88-S94.
15. Stanley S.W., Langston C.E., Hemodialysis in a dog with acute renal failure from currant toxicity, Can Vet J 2008;49:63-6.
16. Ștefănescu Alina, Viţălaru B.A., Bîrţoiu I.A., (2017), Hemodialysis in veterinary medicine: review, Agriculture for life, life for agriculture, May 2017.
17. Stokes J.E., Bartges J.W., Causes of acute renal failure, Compend Contin Educ Pract Vet 2006;28:387-96.
18. Vaden S.L., Levine J., Breitschwerdt E.B., A retrospective case-control of acute renal failure in 99 dogs, J Vet Intern Med 1997;11(2):58-64.
19. Westropp J.L., Ruby A.L., Bailiff N.L., et al., Dried solidified blood calculi in the urinary tract of cats, J Vet Intern Med 2006;20:828-34.
20. Worwag S., Langston C.E., Acute intrinsic renal failure in cats: 32 cases (1997-2004), J Am Vet Med Assoc 2008;232(5):728-32.
21. www.fmc-romania.ro
