Antibiotics, in the broad sense of the word, are drugs that exhibit selective toxicity to certain bacteria. Because of this property, only bacteria can become resistant to antibiotics, not the macroorganism. Although they have selective toxicity against bacteria, antibiotics can also produce side effects in the macroorganism. In general, each antibiotic has certain target organs of its toxicity. There is no antibiotic that is toxic to all organs. The most typical adverse reactions of antibiotics are dysmicrobisms, which occur especially when taking broad-spectrum antibiotics, orally. For an antibiotic to be effective in the treatment of an infectious disease, it is necessary that the disease-causing microbe is susceptible to the antibiotic, and that antibiotic penetrates and produces active concentrations at the site of the infection. To avoid systemic adverse reactions, it is important that the target organs of antibiotic toxicity not to be already ill to the patient. In order to avoid dysmicrobrobisms, a narrow spectrum antibiotic is preferred. With some notorious exceptions, the prophylactic antibiotic treatment is not recommended.
Utilizarea raţională a antibioticelor
Rational use of antibiotics
First published: 24 mai 2019
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/FARM.188.3.2019.2411
Abstract
Rezumat
Antibioticele, în sensul larg la cuvântului, sunt medicamente care prezintă toxicitate selectivă faţă de anumite bacterii. Datorită acestei proprietăţi, numai bacteriile pot deveni rezistente la antibiotice, nu şi macroorganismul. Deşi au toxicitate selectivă faţă de bacterii, antibioticele pot produce şi reacţii adverse la nivelul macroorganismului. În general, fiecare antibiotic prezintă anumite organe-ţintă ale toxicităţii lui. Nu există niciun antibiotic care să fie toxic pentru toate organele. Cele mai caracteristice reacţii adverse ale antibioticelor sunt dismicrobismele care apar, în special, când se administrează antibiotice cu spectru larg, pe cale orală. Pentru ca un antibiotic să fie eficace în tratamentul unei boli infecţioase este necesar ca microbul cauzator al bolii să fie sensibil la antibioticul respectiv, iar acel antibiotic să pătrundă şi să realizeze concentraţii active la locul infecţiei. Pentru a se evita reacţiile adverse sistemice este bine ca organele-ţintă ale toxicităţii antibioticului să nu fie deja bolnave la pacientul respectiv. Pentru a se evita dismicrobismele este de preferat un antibiotic cu spectru îngust. Cu unele excepţii de notorietate, tratamentul profilactic cu antibiotice nu este recomandat.
Antibioticele sunt substanţe de origine naturală produse de microorganisme în procesul de antibioză, un fenomen în cadrul căruia o specie microbiană sintetizează şi eliberează în mediul înconjurător substanţe chimice cu toxicitate selectivă faţă de speciile microbiene concurente, substanţe numite antibiotice. Având toxicitate selectivă numai faţă de anumite specii microbiene, nu şi faţă de celulele macroorganismului, antibioticele pot fi – şi sunt – utilizate în tratamentul bolilor infecţioase produse de bacterii la om şi la animale. Cu puţin timp înaintea descoperirii antibioticelor fuseseră însă inventate şi unele substanţe chimice care, la fel ca antibioticele, prezintă toxicitate selectivă asupra anumitor specii microbiene şi pot fi utilizate astfel în tratamentul bolilor infecţioase la om şi la animale, substanţe numite chimioterapice de sinteză. Astăzi nu se mai face o foarte netă distincţie între antibiotice şi chimioterapice de sinteză. Unii autori le numesc pe toate chimioterapice antimicrobiene, alţi autori le numesc pe toate antibiotice. În fond, toate au aceeaşi proprietate esenţială – selectivitatea de acţiune faţă de bacterii. După cum spunea Paul Erlich, ele se comportă ca nişte gloanţe fermecate, trec pe lângă celulele macroorganismului fără să le afecteze, găsesc bacteriile şi numai pe acestea le omoară. În materialul de faţă, termenul de antibiotice este folosit în sensul său larg, adică atât cu sensul său strict de substanţe de origine naturală, cât şi cu sensul de chimioterapice de sinteză.
Antibioticele, în sensul larg al cuvântului, trebuie însă clar diferenţiate de alte substanţe antibacteriene numite antiseptice şi dezinfectante. Acestea nu au toxicitate selectivă faţă de bacterii. În paradigma lui Paul Erlich, ele nu sunt gloanţe fermecate, ci gloanţe obişnuite, adică distrug orice celulă întâlnită. Ele nu pot fi utilizate în tratamentul sistemic al infecţiilor. În general, se numesc antiseptice când se utilizează pentru distrugerea microbilor de pe suprafeţe vii (spălarea plăgilor cu apă oxigenată, spălarea mâinilor chirurgului etc.) şi se numesc dezinfectante când se utilizează pentru distrugerea microbilor de pe suprafeţe care nu sunt vii (spălarea instrumentarului medical, a pereţilor sălilor de operaţii etc.).
Din cele de mai sus rezultă cel puţin două aspecte importante în utilizarea raţională a antibioticelor.
În primul rând, antibioticele se adresează selectiv microbilor, nu macroorganismelor. Aceasta presupune că macroorganismul nu poate dezvolta toleranţă sau rezistenţă la antibiotice. Numai microbii pot dezvolta toleranţă sau rezistenţă la antibiotice. Dacă o persoană este infectată cu un microb sensibil la un anume antibiotic şi dacă antibioticul pătrunde la locul infecţiei, acel antibiotic este eficace în tratamentul infecţiei respective, indiferent de câte ori a mai fost tratată anterior respectiva persoană cu acel antibiotic. Afirmaţia „la mine antibioticele nu au efect” este un neadevăr.
În al doilea rând, antibioticele sunt eficace numai faţă de anumite specii microbiene. Nu există niciun antibiotic care să fie activ faţă de toţi microbii. Este în logica biologiei ca microbul care produce în procesul de antibioză un anume antibiotic să fie rezistent la antibioticul pe care îl produce. La această rezistenţă naturală se adaugă fenomenul de rezistenţă dobândită, în cadrul căruia anumite specii microbiene care erau iniţial sensibile sau chiar foarte sensibile la un anume antibiotic să devină ulterior rezistente la antibioticul respectiv.

Totalitatea speciilor microbiene sensibile la un anume antibiotic constituie spectrul de activitate antimicrobiană al antibioticului respectiv. Unele antibiotice sunt active pe un număr mic de specii microbiene şi se numesc antibiotice cu spectru îngust. Astfel sunt, de exemplu, penicilinele şi aminoglicozidele. Alte antibiotice sunt active faţă de un număr mare de specii microbiene şi se numesc antibiotice cu spectru larg. Astfel sunt, de exemplu, tetraciclinele şi cloramfenicolul.
La începuturile antibioterapiei au fost descrise trei mari spectre de activitate antimicrobiană. Primul din acestea este spectrul de tip penicilinic, care cuprinde bacili Gram-pozitivi (de exemplu bacilul cărbunos, clostridiile), coci Gram-pozitivi (de exemplu streptococul, pneumococul şi stafilococul) şi coci Gram-negativi (spre exemplu, meningococul şi gonococul). Al doilea este spectrul de tip aminoglicozidic, care cuprinde coci atât Gram-pozitivi, cât şi Gram-negativi şi bacili Gram-negativi (spre exemplu, Salmonella şi Shigella, Neiseria etc.). Al treilea spectru este aşa-numitul spectru larg, caracteristic pentru tetracicline şi cloramfenicol, care cuprinde, pe lângă bacili şi coci atât Gram-pozitivi, cât şi Gram-negativi, şi germenii de tranziţie (chlamidiile, rickettsiile, mycoplasmele). Ulterior, aceste spectre s-au îngustat prin apariţia rezistenţei dobândite. De pildă, stafilococul auriu, care, iniţial, era foarte sensibil la penicilina G, este astăzi rezistent la acest antibiotic în peste 90% dintre cazuri. De asemenea, multe antibiotice apărute ulterior nu se mai încadrează perfect în unul dintre cele trei spectre. De exemplu, ampicilina sau amoxicilina, două peniciline de semisinteză, pe lângă spectrul penicilinic clasic, sunt active şi pe unii bacili Gram-negativi. Un alt exemplu este cel al cefalosporinelor. Generaţia I de cefalosporine are un spectru de activitate antibacteriană de tip penicilinic, generaţiile ulterioare de cefalosporine au un spectru lărgit, cuprinzând şi alţi microbi, care nu intră în spectrul penicilinic.
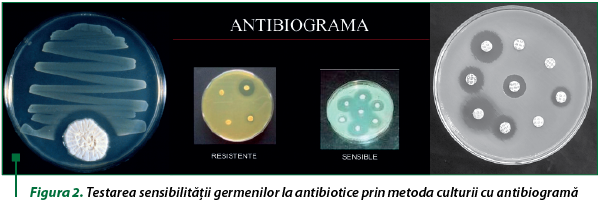
Din cele de mai sus rezultă că prima condiţie esenţială pentru ca un antibiotic să fie eficace în tratamentul unei boli infecţioase este ca microbul care produce respectiva boală să intre în spectrul de activitate antimicrobiană al acelui antibiotic, adică să fie sensibil la antibioticul respectiv. O metodă clasică de detectare a acestei condiţii este recoltarea microbului de la bolnav, cultivarea sa in vitro şi efectuarea unei antibiograme care precizează cu claritate la ce antibiotice este sensibil microbul izolat. Nu este nevoie însă întotdeauna de o asemenea determinare. Există multe situaţii de boli infecţioase care sunt precis determinate de un anume microb şi care au o simptomatologie atât de specifică, încât pot fi diagnosticate clinic. De exemplu, pneumonia francă lobară este întotdeauna determinată de pneumococ, erizipelul este întotdeauna determinat de streptococ, furunculul este întotdeauna determinat de stafilococul auriu, febra tifoidă este întotdeauna determinată de Salmonella tiphy etc., aceste boli putând fi diagnosticate clinic. În alte boli se procedează pe criterii statistice, de exemplu amigdalita roşie ca focul este produsă în cea mai mare parte a cazurilor de streptococ, meningita bacteriană este produsă în cea mai mare parte a cazurilor fie de streptococ, fie de meningococ. Dacă boala nu prezintă risc vital, se poate administra antibioticul care este cel mai probabil să fie activ. Dacă boala prezintă risc vital, se procedează la fel, numai că înaintea administrării antibioticului se recoltează probe biologice pentru izolarea ulterioară a microbului şi determinarea sensibilităţii acestuia la antibiotice.
Pentru ca un antibiotic să fie eficace în tratamentul unei boli infecţioase nu este însă suficient ca acel antibiotic să fie activ faţă de microbul care produce infecţia. Este imperios necesar, de asemenea, ca acel antibiotic să pătrundă şi să realizeze concentraţii active la locul infecţiei. Ca majoritatea medicamentelor, multe antibiotice se distribuie neuniform în organism, existând zone în care se concentrează preferenţial, concomitent cu zone în care antibioticul nu pătrunde. De exemplu, aminoglicozidele sunt foarte active faţă de microbii care produc în majoritatea cazurilor meningitele bacteriene, dar sunt ineficace în tratamentul meningitelor, deoarece nu traversează bariera hematoencefalică şi nu pătrund în lichidul cefalorahidian. Există, bineînţeles, şi situaţii inverse. De pildă, ampicilina realizează în bilă (fiere) concentraţii de 200 de ori mai mari decât în sânge, motiv pentru care ampicilina este, în general, foarte eficace în tratamentul colecistitelor infecţioase. Un alt exemplu este cel al cloramfenicolului, care se concentrează foarte mult în limfă, motiv pentru care este medicamentul de elecţie în tratamentul febrei tifoide, deoarece Salmonella tiphy se multiplică la nivelul ganglionilor limfatici.
Absorbţia digestivă poate constitui şi ea un criteriu în alegerea antibioticului optim. Unele antibiotice, cum este penicilina G, sunt distruse în tubul digestiv şi nu sunt eficace decât dacă se administrează injectabil. Alte antibiotice nu sunt distruse în tubul digestiv, dar nu se absorb dacă se administrează pe cale orală. Nici aceste antibiotice nu sunt eficace în infecţiile sistemice decât dacă se administrează injectabil. Dacă se administrează pe cale orală, aceste antibiotice pot fi însă foarte eficace în tratamentul infecţiilor digestive, deoarece, prin faptul că nu se absorb din tubul digestiv, realizează concentraţii mari la locul infecţiei (interiorul tubului digestiv). În plus, prin faptul că nu se absorb, aceste antibiotice administrate pe cale orală sunt lipsite de reacţii adverse sistemice. Este cazul aminoglicozidelor şi, mai nou, al vancomicinei.
Deşi antibioticele, după cum am amintit, au toxicitate selectivă faţă de bacterii, ele pot produce totuşi reacţii adverse la nivelul macroorganismului. În general, fiecare antibiotic are toxicitate selectivă faţă de unul sau mai multe organe, dar nu există niciun antibiotic care să fie toxic pentru toate organele. De exemplu, aminoglicozidele sunt toxice pentru rinichi şi pentru urechea internă, cloramfenicolul este toxic pentru măduva oaselor (poate produce extrem de rar o aplazie medulară), etambutolul poate fi toxic pentru ochi (poate produce o nevrită optică retrobulbară), tetraciclinele pot fi toxice pentru ficat etc. Este important să nu se administreze un antibiotic pentru tratamentul unei infecţii la un bolnav la care organul-ţintă al toxicităţii antibioticului respectiv este deja afectat de o boală. De exemplu, se vor evita aminoglicozidele în tratamentul unei infecţii la un bolnav hipoacuzic sau la un bolnav cu insuficienţă renală.
Cele mai caracteristice reacţii adverse ale antibioticelor sunt însă dismicrobismele. Acestea apar cel mai frecvent dacă se administrează antibiotice cu spectru larg pe cale orală. Având spectru larg, aceste antibiotice pot distruge flora saprofită a colonului. În urma acestei distrugeri, colonul urmează a fi repopulat cu alţi microbi. Dacă microbul care repopulează colonul este patogen, apare o altă boală infecţioasă decât cea tratată. Dacă repopularea colonului se face în mediu spitalicesc, există riscul ca această repopulare să se facă cu un microb polirezistent la antibiotice, cum este, de exemplu, Clostridium difficile. Pot să apară astfel infecţii extrem de severe şi foarte greu de tratat. O asemenea infecţie se tratează tot cu antibiotice, dar, bineînţeles, altele decât cele folosite iniţial. În principiu, cu cât spectrul de activitate antimicrobiană al unui antibiotic este mai îngust, cu atât şi riscul de apariţie a dismicrobismelor este mai mic.
Pe baza celor arătate mai sus, rezultă că, în esenţă, este optim ca în tratamentul unei infecţii să se aleagă un antibiotic care este activ faţă de bacteria care produce infecţia (antibioticele nu sunt active faţă de virusuri), care pătrunde şi realizează concentraţii active la locul infecţiei şi care nu este toxic pentru niciunul dintre organele care sunt bolnave la pacientul respectiv. Pentru evitarea riscului de dismicrobisme este de preferat ca acel antibiotic să aibă un spectru de activitate antimicrobiană îngust.
În principiu, se consideră că profilaxia cu antibiotice nu este bine-venită, deoarece un bolnav în tratament cu un antibiotic are risc crescut de a se suprainfecta cu un microb rezistent la acel antibiotic, poate chiar polirezistent, situaţie în care infecţia devine greu de tratat ulterior. Există însă numeroase excepţii de la această regulă. Profilaxia infecţiilor streptococice la bolnavii cu reumatism articular acut în antecedente sau profilaxia în cursul intervenţiilor chirurgicale pe organele interne abdominale sunt numai două exemple în acest sens.
Foarte rar, asocierea de antibiotice determină o creştere a eficacităţii tratamentului antibacterian. Este bine cunoscut, de exemplu, că asocierea sulfamidelor cu trimetoprimul sau asocierea penicilinelor cu aminoglicozidele conferă o eficacitate superioară faţă de antibioticul utilizat în monoterapie. În general, se utilizează asocieri de antibiotice când se doreşte o lărgire a spectrului de activitate antimicrobiană – de exemplu, asocierea penicilinelor cu aminoglicozidele este eficace pe toţi cocii şi pe toţi bacilii, atât Gram-pozitivi, cât şi Gram-negativi. Dacă la această asociere se adaugă şi un antibiotic activ pe microbii anaerobi, spectrul antibacterian al asocierii se lărgeşte şi mai mult. Uneori antibioticele se asociază pentru a se evita apariţia rezistenţei microbilor la antibioticele cu care se face tratamentul. Aceasta se practică în general în cazul tratamentului de lungă durată cu antibiotice, cum este, de exemplu, cazul tuberculozei. În această boală se asociază două sau mai multe antibiotice cu mecanisme de acţiune diferite. Dacă microbul dezvoltă rezistenţă la un antibiotic cu un anume mecanism de acţiune, el va fi distrus de celelalte antibiotice din asociere şi care acţionează prin alte mecanisme.
În concluzie, antibioticele trebuie utilizate pentru tratamentul infecţiilor bacteriene, iar alegerea ideală este probabil aceea în care microbul cauzator al bolii este sensibil la antibioticul ales, antibioticul pătrunde şi realizează concentraţii active la locul infecţiei, nu este toxic pentru niciunul dintre organele deja bolnave ale pacientului şi este un antibiotic cu spectru îngust.
Bibliografie
- Clark AM, Finkel R, Rey AJ, Whalen K. Lippincotts Illustrated Reviews, Pharmacology, 5th Edition. Ed. Wolters Kluwer/Lippincott Williams &Wilkins. 2012.
- Fulga I. Farmacologie, ediţia II-a revizuită şi adăugită. Ed. Med. Bucureşti. 2015.
- Fulga IG. Antibiotice, antibioză, antibioterapie, Ed. Med. Bucureşti. 1989.
- Golan DE, Armstrong J. Principles of Pharmacology. The pathophysiologic basis of drug therapy. 4th Edition, Wolters Kluwer. 2017.
- Brunton L, Chabner A, Knollman B. Goodman & Gilman’s The Pharmacological Basis of Therapeutics, Twelfth Edition. Ed. Mc Graw Hill Medical. 2011.
- Katzung BG, Trevor AJ. Basic and Clinical Pharmacology. 13th Edition, McGraw Hill Education, 2015.
- Bertram BG, Susan MB, Trevor AJ. Basic and Clinical Pharmacology, 11th Edition, Ed. Mc Graw Hill Medical, 2009.
- Waldman T. Pharmacology and Therapeutics Principles to Practice. Ed. Saunders Elsevier, 2009.
- Walker W. Clinical Pharmacy and Therapeutic. Fifth Edition, Ed. Churchill Livingstone. 2012.
Articole din ediţiile anterioare
Folosirea judicioasă antibioticelor şi chimioterapicelor antibacteriene (I)
Bolile infecţioase sunt printre cele mai frecvente motive ale prezentării la medic.Antibioticele sunt arme importante în arsenalul farmacoterapeuti...
Utilizarea preparatelor antibacteriene la pacienţii cu COVID-19
Strategiile de utilizare a preparatelor antimicrobiene în infecţia cu SARS-CoV-2 au evoluat odată cu pandemia, cunoscând controverse importante în ...
Farmacoterapia unor afecţiuni dermatologice frecvente. Iatrogenie cu manifestări cutanate
Tratarea leziunilor dermatologice este o artă-cu-ştiinţă. Complexitatea leziunilor, multitudinea lor, evoluţia lor spre vindecare sau agravarea lor...
Folosirea judicioasă a antibioticelor şi chimioterapicelor antibacteriene (III)
Antibioticele şi chimioterapicele antimicrobiene pot acţiona la nivelul peretelui celular, la nivelul membranei celulare, la nivelul ribozomilor cu...