The present paper constitutes an example for the clinician regarding babesiosis diagnostic workflow, parasitic load monitoring in correlation with specific treatment and therapeutic efficiency for disease, as well as infection removal. The results obtained, as standalone or in correlation with the symptomatology and paraclinical routine tests, are able to generate a high level of information, therefore allowing the clinician to have a correct approach for the two main objectives in disease management – patient’s recovery and removal of the specific cause.
Monitorizarea răspunsului terapeutic în babesioza canină – studiu de caz
Therapeutic response monitoring in canine babesiosis – case study
First published: 18 decembrie 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/PV.33.4.2018.2103
Abstract
Rezumat
Prezenta lucrare se constituie ca un exemplu pentru medicul clinician în ceea ce priveşte metodologia în diagnosticul babesiozei, monitorizarea încărcăturii parazitare, corelată cu administrarea tratamentului specific şi, nu în ultimul rând, eficienţa protocolului terapeutic atât în remiterea bolii, cât şi în sterilizarea organismului (remiterea infecţiei). Rezultatele obţinute ca atare şi în corelaţie cu simptomatologia şi examenele paraclinice de rutină reuşesc să genereze un nivel informaţional extrem de ridicat şi, în consecinţă, permit clinicianului o abordare judicioasă a celor două mari repere în managementul bolii, şi anume recuperarea pacientului şi îndepărtarea agentului cauzal.
Introducere
În prezent, babesioza ocupă unul dintre primele locuri în ceea ce priveşte cazuistica întâlnită la nivelul animalelor de companie şi în special la câine, fiind raportate numeroase îmbolnăviri. Aşa cum am arătat, boala în sine are un aspect clinic şi paraclinic extrem de heterogen, fapt deloc surprinzător dacă se ţine cont de cei doi actori implicaţi, şi anume organismul-gazdă (vârstă, rasă, existenţa unor afecţiuni colaterale atât de origine infecţioasă, cât şi de altă natură) şi specia de parazit care este implicată (până în prezent fiind descrise trei specii distincte care produc boala în România)(9).
În ceea ce priveşte tratamentul, a fost identificat un număr relativ restrâns de molecule cu eficienţă în tratament, în administrare unică sau sub formă de combinaţii(1,3,5,7,8,10). Totuşi, trebuie menţionat faptul că mecanismul specific de acţiune al multora dintre ele nu este pe deplin elucidat, fiind introduse în protocolul terapeutic în urma studiilor din teren(2,4,6,10). Mai mult, există particularităţi evidente în ceea ce priveşte specia de Babesia infectantă şi răspunsul terapeutic obţinut(5,7,9).
Prezentare caz
În data de 11.05.2018, pacientul (câine, Akita Inu, mascul, cu vârsta de 10 luni) s-a prezentat la clinica Facultăţii de Medicină Veterinară din Bucureşti. Anamneza a relevat diagnosticul de babesioză, în urmă cu câteva săptămâni, la o clinică privată, moment în care a fost instituit tratament cu dipropionat de imidocarb în administrare unică. Având în vedere vârsta pacientului, s-a considerat oportună administrarea unei doze reduse, de 3,3 mg/kg (aproximativ jumătate din doza uzual utilizată). Subsecvent administrării imidocarbului s-a recurs la administrarea per os a clindamicinei, în doză de 10 mg/kg/zi, timp de două săptămâni.
La examenul clinic s-au constatat următoarele: mucoase aparente uşor palide, timp de reumplere capilară <1,5 secunde, persistenţă pliu cutanat <1,5 secunde, uşoară abatere, fără sensibilitate abdominală la palpare, temperatura rectală în limite fiziologice.
Pentru confirmarea diagnosticului şi instituirea unui protocol terapeutic personalizat s-a recurs la recoltarea de probe biologice (sânge integral pe EDTA) pentru examen PCR în vederea stabilirii speciei infectante şi a încărcăturii parazitare. Rezultatul a fost pozitiv pentru Babesia canis, fiind identificată o încărcătură parazitară medie la nivel de probă biologică analizată (Ct=29,83 – crossing threshold) (figurile 1 şi 2).
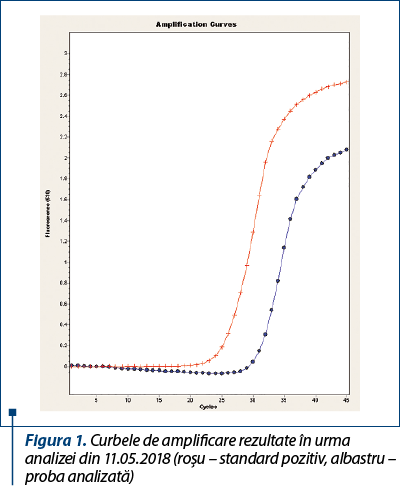
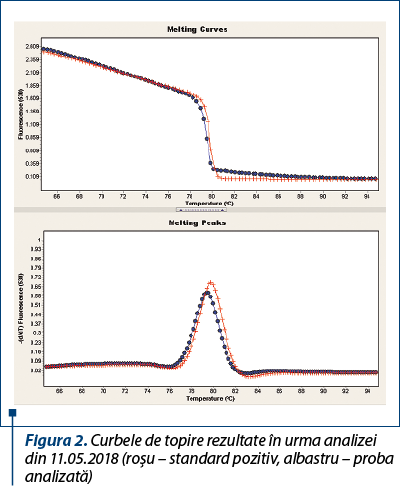
Consecutiv diagnosticului şi stabilirii încărcăturii parazitare, a fost instituit un tratament cu clindamicină, de data aceasta în doză crescută, de 15 mg/kg/zi, cu o durată estimată de 4 săptămâni.
În data de 16.05.2018 (după 5 zile de tratament) s-a recurs la reevaluarea pacientului prin examen hematologic, biochimic şi examen PCR. Rezultatele obţinute indică o hemoleucogramă compatibilă cu tipul de infecţie identificat (scăderea hematocritului şi a concentraţiei de hemoglobină, trombocitopenie – date disponibile la cerere), fără modificări pentru profilul biochimic şi cu un rezultat PCR pozitiv, dar cu o încărcătură parazitară semnificativ redusă (Ct>40 – crossing threshold) (figurile 3 şi 4). Din punct de vedere clinic, starea generală a fost foarte bună. S-a luat decizia continuării tratamentului şi reevaluării pacientului după aproximativ două săptămâni.
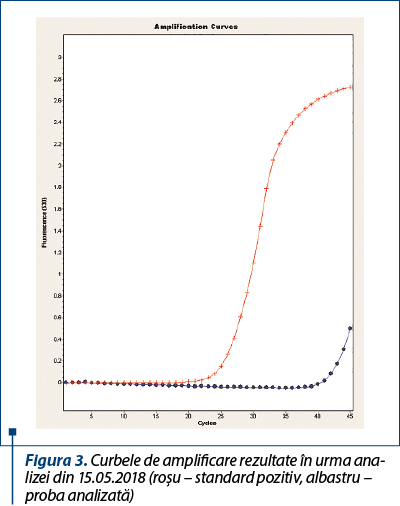
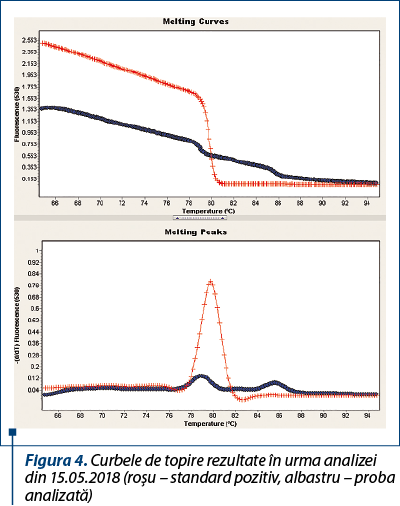
În data de 24.05.2018, pacientul s-a prezentat pentru reevaluare, astfel că s-a recurs la protocolul anterior prezentat – screening hematologic şi biochimic, evaluare încărcătură parazitară prin PCR. La examenul hematologic s-a constatat o revenire la normal a concentraţiei de hemoglobină şi a numărului de trombocite, cu un hematocrit încă sub limitele fiziologice, dar semnificativ îmbunătăţit faţă de determinările anterioare (date disponibile la cerere). Surprinzător însă, rezultatul pentru testul PCR a evidenţiat o încărcătură parazitară mai mare decât în determinarea anterioară (16.05.2018; Ct=34,59 – crossing threshold) (figurile 5 şi 6).

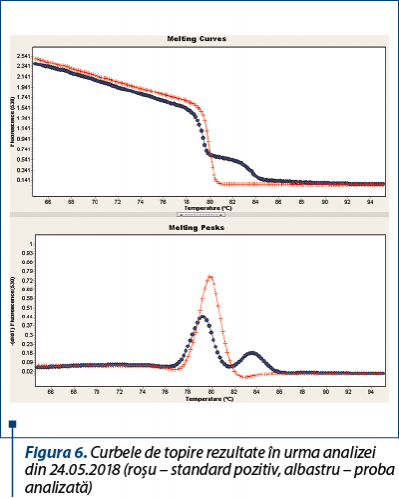
În urma discuţiei cu proprietarul a fost identificat motivul acestei schimbări – doza zilnică a fost modificată, în sensul reducerii la jumătate faţă de cea recomandată. În consecinţă, a fost reiterată importanţa administrării corecte a medicaţiei şi bineînţeles revenirea pentru monitorizare.
În data de 5.06.2018, pacientul s-a prezentat pentru reevaluare şi consecutiv s-au efectuat analizele hematologice şi testul PCR. Hemoleucograma a evidenţiat revenirea la normal a tuturor parametrilor anterior modificaţi, iar testul PCR a fost negativ. S-a considerat oportună continuarea tratamentului pentru toată perioada recomandată iniţial.
Discuţii
Testul PCR s-a dovedit a fi de un real ajutor atât în diagnosticul babesiozei (din experienţa acumulată, pentru această încărcătură parazitară examenul microscopic efectuat în cele mai bune condiţii a fost sistematic negativ, aşadar inutilizabil în astfel de situaţii).
Mai mult, prin efectuarea tehnicii PCR în timp real s-a reuşit monitorizarea încărcăturii parazitare pentru toate momentele în care a fost efectuată, fiind stabilită cu exactitate dinamica infecţiei. Aşadar, s-a putut determina o scădere dramatică a parazitemiei (de aproximativ 10.000 de ori) între prima determinare şi cea de-a doua, alături de o creştere a acesteia consecutiv subdozării tratamentului (de 100 de ori între cea de-a doua determinare şi a treia determinare) (tabelul 1).
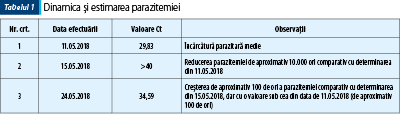
Şi în ceea ce priveşte tratamentul, testul PCR şi-a dovedit pe deplin utilitatea, fiind argumentat ştiinţific faptul că subdozarea medicaţiei conduce la rezultate inadecvate în ceea ce priveşte sterilizarea organismului, aşadar se recomandă respectarea cu stricteţe a posologiei indicate de producător.
Mai mult, testarea în dinamică poate semnaliza orice abatere de la rezultatul dorit, fiind în cazul de faţă identificată neconcordanţa dintre recomandările clinicianului şi administrarea de facto a medicaţiei. Bineînţeles, atunci când se exclud astfel de evenimente, o situaţie de acest gen poate fi generată de rezistenţa la tratament a patogenului, astfel că se poate ajunge în situaţia reevaluării medicaţiei administrate.
Nu în ultimul rând, testul PCR a contribuit decisiv la obţinerea dezideratului suprem, şi anume eliminarea din organism a patogenului, situaţie care până în prezent era aproape imposibil de monitorizat. Aşa cum am arătat, revenirea la normal a parametrilor hematologici (eventual şi a celor biochimici, dacă există modificări) şi însănătoşirea clinică a pacientului nu corespund cu sterilizarea organismului, fiind vorba doar de îndepărtarea condiţiei de boală, dar NU şi a infecţiei.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Beugnet F, Moreau Y. Babesiosis. Rev. Sci. Tech. 2015; 34; 627-639.
- Birkenheuer AJ, Levy MG, Breitschwerdt EB. Efficacy of combined atovaquone and azithromycin for therapy of chronic Babesia gibsoni (Asian genotype) infections in dogs. J. Vet. Intern. Med. 2004; 18, 494-498.
- Camacho AT, Pallas E, Gestal JJ et al. Infection of dogs in north-west Spain with a Babesia microti-like agent. Vet Rec. 2001; 149, pp. 552-555.
- Checa R, Montoya A, Ortega N, González-Fraga JL, Bartolomé A, Gálvez R, Marino V, Miró, G. Efficacy, safety and tolerance of imidocarb dipropionate versus atovaquone or buparvaquone plus azithromycin used to treat sick dogs naturally infected with the Babesia microti-like piroplasm. Parasit. 2017; Vectors 10, 145.
- Irwin PJ. Canine babesiosis: from molecular taxonomy to control. Parasit. 2009; Vectors 2 (Suppl 1), pp. 1-9.
- Lin EC, Chueh LL, Lin CN, Hsieh LE, Su BL. The therapeutic efficacy of two antibabesial strategies against Babesia gibsoni. Vet. Parasitol. 2012; 186, 159-164.
- Solano-Gallego L, Baneth G. Babesiosis in dogs and cats – expanding parasitological and clinical spectra. Vet. Parasitol. 2011; 181, 48-60.
- Solano-Gallego L, Trotta M, Carli E et al. Babesia canis canis and Babesia canis vogeli clinicopathological findings and DNA detection by means of PCR-RFLP in blood from Italian dogs suspected of tick-borne disease, Vet Parasitol. 2008; 157, pp. 211-221.
- Turcitu MA. Actualizarea protocolului de diagnostic în babesioza canină. Revista Practica Veterinară.ro. 2016; Anul VII, Nr. 24 (3).
- Vial HJ, Gorenflot A. Chemotherapy against babesiosis. Vet. Parasitol. 2006; 138, 147-160.
Articole din ediţiile anterioare
Resuscitarea cardiopulmonară
Iniţierea resuscitării cardiopulmonare (RCP) reprezintă primul gest salvator pentru pacientul aflat în stop cardiorespirator. Prin eforturile a pes...
Aplicaţiile testării potenţialelor auditive evocate de trunchi cerebral (BAER) în medicina veterinară
Patologia nervului statoacustic reprezintă una dintre cele mai frecvente afecţiuni ale nervilor cranieni întâlnite în practica veterinară. Ea se po...
Coordonate clinice și de diagnostic în principalele afecţiuni urologice la câine
Vezica urinară este un organ care se pretează foarte bine la examenul ecografic, deoarece urina anecogenă este un produs de contrast natural, favor...
Carcinomul scuamocelular la pisică − diagnostic diferenţial şi abordare terapeutică multimodală
Carcinomul scuamocelular la pisică este o afecţiune care poate fi tratată dacă este diagnosticată precoce. Din acest considerent sunt extrem de imp...