Impactul infecţiei HIV asupra dezvoltării cancerelor cutanate
The impact of HIV infection on the development of cutaneous cancers
Abstract
Human immunodeficiency virus (HIV) infection continues to be an important public health issue. Immunosuppression is responsible for the development of much comorbidity among HIV-infected patients. Of these, malignancies play an important role in the prognosis of the disease. Cancers diagnosed in HIV-infected patients can be divided into two main categories: AIDS-defining cancers and non-AIDS-defining cancers. In the second category, skin cancers represent an important subgroup, the most common being basal cell carcinoma, squamous cell carcinoma and melanoma.Keywords
HIVimmunosuppressionskin cancerRezumat
Infecţia cu virusul imunodeficienţei umane (HIV) continuă să reprezinte o importantă problemă de sănătate publică. Imunosupresia este responsabilă de dezvoltarea a numeroase comorbidităţi în rândul pacienţilor infectaţi HIV. Dintre acestea, un rol important în prognosticul bolii îl deţin neoplaziile. Cancerele diagnosticate la pacienţii infectaţi HIV se pot împărţi în două categorii principale: cancere care definesc SIDA şi cancere care nu definesc SIDA. În a doua categorie, un loc important îl deţin cancerele cutanate, cele mai frecvente fiind carcinomul bazocelular, carcinomul spinocelular şi melanomul.Cuvinte Cheie
HIVimunosupresiecancer cutanatIntroducere
Numărul cazurilor de infecţie cu virusul imunodeficienţei umane (HIV) este în creştere. Conform Organizaţiei Mondiale a Sănătăţii, la sfârşitul lui 2017 erau circa 36,9 milioane de indivizi infectaţi HIV, dintre care 25,7 milioane în Africa. În 2017 au fost raportate 1,8 milioane de cazuri noi(1). Principalele grupe de risc pentru contractarea infecţiei sunt homosexualii, bisexualii, cei care au relaţii sexuale neprotejate cu parteneri multipli, cei care au un partener infectat şi cei cu istoric de infecţii cu transmitere sexuală(1,2). Toţi cei care se încadrează în aceste grupe de risc trebuie testaţi de rutină pentru depistarea infecţiei HIV, precum şi pentru tuberculoză şi pentru infecţiile cu virusurile hepatitice B şi C(2).
În diagnosticarea infecţiei HIV un rol esenţial îl joacă anamneza, ceea ce presupune încadrarea pacientului într-o grupă de risc. Din punctul de vedere al tabloului clinic, iniţial se manifestă prin febră, transpiraţii sau scădere ponderală involuntară(3,4). Semnale de alarmă sunt şi limfadenopatia generalizată, candidoza vaginală recurentă sau ulceraţiile recurente ale mucoasei orale(3). Terapia antiretrovirală a fost aprobată în 1987, iar în 2017, 59% dintre adulţii infectaţi HIV erau trataţi cu terapie antiretrovirală(1,4). Au fost descrise cancere care definesc stadiul SIDA (precum sarcomul Kaposi, cancerul de col uterin etc.) şi cancere care nu definesc stadiul SIDA (precum cancerul pulmonar, hepatic, renal, cutanat etc.)(5). Cele mai frecvente cancere cutanate la pacienţii HIV-pozitivi care nu definesc stadiul SIDA sunt carcinomul bazocelular (CBC), carcinomul spinocelular (CSC) şi melanomul(6).
Zhao şi colab. au efectuat o metaanaliză, cu scopul de a observa riscul pacienţilor infectaţi HIV de a dezvolta cancere cutanate nonmelanocitare. Au fost analizate şase studii la care au participat 78794 de pacienţi infectaţi HIV şi s-a observat un risc mai crescut de a dezvolta cancere cutanate nonmelanocitare. În plus, s-a pus în evidenţă că tratamentul antiretroviral conduce la reducerea acestui risc(7). De asemenea, studiul lui Asgari şi colab., care a inclus 455 de subiecţi HIV-pozitivi şi 1945 HIV-negativi, a arătat un risc cu 15% mai mare de apariţie a cancerelor cutanate nonmelanocitare în rândul celor infectaţi faţă de cei neinfectaţi. Pacienţii au fost urmăriţi pe o perioadă de cinci ani. Riscul a fost mai mare în cazul celor cu un grad de imunosupresie mai avansat, riscul de CSC fiind de până la 222% mai mare faţă de cei HIV-negativi(8). Legătura dintre gradul de imunosupresie şi riscul de apariţie a cancerelor cutanate nu este bine stabilită în literatură, existând studii semnificative doar în cazul CSC(8,9). Datele actuale nu susţin corelarea agresivităţii tumorii din punct de vedere histopatologic cu gradul de imunosupresie(9).
Cancerele cutanate la pacienţii infectaţi HIV
Decesele pacienţilor HIV-pozitivi sunt rezultatul, în o treime din cazuri, evoluţiei unei neoplazii. Cei mai importanţi factori care participă la apariţia cancerelor la pacienţii infectaţi HIV sunt infecţiile cu virusuri oncogene, factorii imunologici şi de mediu. Printre virusurile cel mai frecvent întâlnite la pacienţii HIV-pozitivi şi care prezintă potenţial oncogen se numără virusul papiloma uman (HPV), virusul Epstein-Barr (EBV), virusul herpetic uman 8 (HHV8) şi virusurile hepatitice B şi C. De asemenea, imunosupresia este un bine cunoscut factor implicat în oncogeneză. Dintre factorii de mediu cei mai redutabili sunt fumatul şi expunerea cronică la radiaţiile solare(10). Grulich şi colab. au analizat studii disponibile în literatura medicală cu privire la incidenţa cancerelor la pacienţii HIV-pozitivi şi la cei transplantaţi, ambele grupuri având drept trăsătură comună imunosupresia. Studiul a pus în evidenţă rezultate similare între cele două grupuri analizate, concluzionând că imunosupresia joacă rolul definitoriu în dezvoltarea neoplaziei, iar alţi factori deţin doar un rol secundar. Cele mai frecvente cancere identificate în ambele grupuri au fost cele în care era implicat un agent infecţios(11).
Studiul realizat de Cianflone şi colab., care a inclus 4498 de pacienţi HIV-pozitivi, a analizat incidenţa cancerelor în funcţie de momentul introducerii terapiei antiretrovirale. Studiul concluzionează că există o scădere a numărului de cancere care definesc SIDA odată cu introducerea terapiei antiretrovirale. În schimb, rata cancerelor care nu definesc SIDA este în creştere, devenind tipurile de cancer dominante. Autorii ridică ipoteza conform căreia acest fapt ar putea fi rezultatul creşterii speranţei de viaţă la persoanele HIV-pozitive graţie terapiei antiretrovirale(12). Studiul realizat de Bedimo şi colab. a arătat că pacienţii cu cancere care nu definesc SIDA, în comparaţie cu cei cu cancere care definesc SIDA, au un număr semnificativ mai mare de limfocite CD4 (276,5 vs. 37,5 celule/µL)(13).
Studiile din ultimii 20 de ani arată o creştere a cancerelor cervico-faciale în rândul pacienţilor infectaţi HIV. Se observă o incidenţă mai mare în special a celor asociate cu o infecţie orală cu HPV, riscul unei infecţii orale cu HPV în rândul acestor subiecţi fiind de 2-3 ori mai mare decât în populaţia generală. Printre factorii de risc care contribuie la acest fapt se numără incidenţa crescută a fumătorilor şi a consumatorilor de alcool în rândul pacienţilor infectaţi HIV şi obiceiurile sexuale ale acestor indivizi(14). Spre exemplu, studiul realizat de Clifford şi colab. a pus în evidenţă o proporţie de 72% a fumătorilor în rândul pacienţilor infectaţi HIV analizaţi(15).
Carcinomul bazocelular
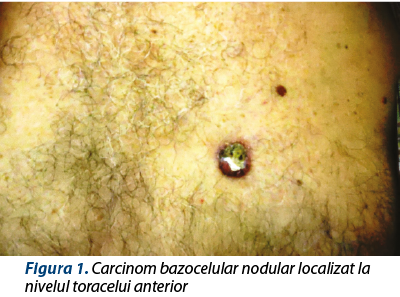
Carcinomul bazocelular este cel mai frecvent neoplasm. Afectează în special adulţii în decada a patra de viaţă. Factorul de risc major implicat în patogeneza sa este expunerea cronică la soare. Alţi factori de risc includ expunerea la arsenic, imunosupresia, prezenţa unor leziuni de tipul ulcerelor, cicatricelor sau arsurilor(16). Metastazează foarte rar, dar are efect distructiv local(17). Deşi încă mai există controverse asupra originii sale, cercetări recente arată că îşi are originea fie la nivelul epidermului interfolicular, fie la nivelul foliculului pilos. Din punct de vedere clinic, poate îmbrăca mai multe aspecte, cel mai comun fiind tipul nodular, care se prezintă sub forma unui nodul cu aspect perlat, cu telangiectazii pe suprafaţă şi contur elevat, care poate prezenta o ulceraţie centrală (figura 1)(18). În jur de 80% dintre CBC se localizează la nivelul regiunii cervicale(19). Diagnosticul se bazează pe aspecte clinice, dermatoscopice şi histologice. Terapiile disponibile sunt variate, de la terapii conservatoare (ex.: crioterapia, electrocauterizarea), excizie chirurgicală sau aplicare de chimioterapice (ex.: 5-fluorouracil) la terapii moderne, precum administrarea de agenţi imunomodulatori (ex.: imiquimod) sau agenţi biologici, indicaţi în special în cazurile metastazate(17,20).
Cancerele nonmelanocitare sunt cele mai frecvente tipuri de cancer. În jur de 80% sunt reprezentate de CBC şi 20% de CSC(21). Pacienţii infectaţi HIV au un risc de a dezvolta o formă de cancer nonmelanocitar de 3-5 ori mai mare decât populaţia generală. O observaţie interesantă este faptul că în rândul acestor pacienţi raportul CSC/CBC este de 1:7, iar în cazul celor care au suferit un transplant renal este de 1,8:1. Trebuie avut în vedere că, din punct de vedere clinic, nu există diferenţe între cei HIV-pozitivi şi cei HIV-negativi(22). Studiul lui Garlassi şi colab. nu a identificat diferenţe cu privire la vârsta, durata de evoluţie a infecţiei HIV şi gradul de imunosupresie între pacienţii diagnosticaţi cu CBC faţă de cei cu CSC(9).
Un studiu recent efectuat în Danemarca a inclus 4280 de indivizi infectaţi HIV şi aduce în atenţie o observaţie interesantă. În ceea ce priveşte riscul de dezvoltare a CBC, autorii au observat o corelaţie cu sursa infecţiei. Astfel, homosexualii au avut un risc mai crescut, în schimb în cazul celorlalte căi de contractare a HIV nu s-a identificat un risc mai mare faţă de populaţia generală(23).
Carcinomul spinocelular
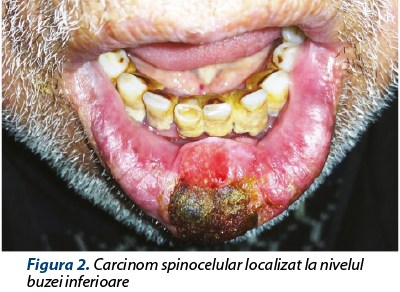
CSC afectează în special mucoasele. În cazul CSC, factorii de risc sunt similari cu cei asociaţi dezvoltării CBC, expunerea cronică la ultraviolete deţinând de asemenea un rol important(21). Rareori apare pe tegument sănătos. În cele mai multe cazuri se dezvoltă pe tegument agresat actinic sau cu diverse leziuni de tipul arsurilor, cicatricelor sau ulcerelor. Din punct de vedere clinic se prezintă sub forma unei papule sau a unei plăci, dar cel mai frecvent apare sub forma unui nodul cu suprafaţă netedă, scuamoasă sau verucoasă, care evoluează spre ulcerare (figura 2)(24). Spre deosebire de CBC, prezintă un risc semnificativ de metastazare. Strategiile terapeutice trebuie să aibă în vedere în primul rând o abordare radicală, iar opţiunile conservatoare să fie destinate pacienţilor care prezintă contraindicaţii(25).
În ceea ce priveşte CSC localizat în regiunea cervicală, se cunoaşte că este asociat cu precădere cu fumatul, dar s-a observat o incidenţă crescută la cei nefumători, dar care asociază infecţie HIV, aceştia având un risc de până la 4 ori mai mare decât populaţia generală, fapt care este cauzat şi de consumul de alcool, dar şi de infecţia cu HPV(26). O metaanaliză care a investigat pacienţi infectaţi HIV s-a focusat pe cancerele care nu definesc stadiul SIDA şi a analizat 18 studii la care au participat 625716 indivizi infectaţi HIV. Aceasta a evidenţiat o incidenţă crescută a cancerelor asociate cu infecţii, precum cancer anal (virusul HPV), hepatic (virusurile hepatitice), limfomul Hodgkin, dar şi cu fumatul – cancer pulmonar, renal şi laringian(27). Pacienţii HIV-pozitivi prezintă un risc crescut de dezvoltare a CSC genital. În rândul acestor pacienţi, cancerul anal este de 30 de ori mai frecvent decât în populaţia generală. În ceea ce priveşte cancerul vulvar şi penian, statisticile arată o incidenţă de 6, respectiv de 4 ori mai mare(6).
Un studiu recent a arătat o rată crescută a recurenţelor CSC nongenital în rândul pacienţilor HIV-pozitivi. Peste 90% dintre pacienţii incluşi în studiu, HIV-pozitivi, urmau terapie antiretrovirală, iar durata medie de evoluţie a infecţiei era de 11 ani. Modalităţile terapeutice au inclus în principal tehnici distructive sau tratamente topice, mai puţin de 50% beneficiind de un tratament chirurgical. Nu s-a observat o corelaţie cu numărul de limfocite CD4, sugerând că imunosupresia nu reprezintă factorul principal în apariţia recurenţelor(28). Totuşi Silverberg şi colab. au realizat un studiu de cohortă între 1996 şi 2008, care a inclus 6560 de indivizi HIV-pozitivi şi 36821 HIV-negativi. S-a observat o incidenţă mai crescută a cancerelor cutanate la cei cu un număr scăzut de limfocite CD4 în comparaţie cu cei neinfectaţi. S-a pus în evidenţă o incidenţă de două ori mai mare comparativ cu cei HIV-negativi şi o corelaţie cu imunosupresia doar în cazul CSC, nu şi al CBC(29).
Nguyen a analizat 10 pacienţi HIV-pozitivi diagnosticaţi cu CSC, o formă agresivă, definită pe baza dimensiunii (peste 1,5 cm), evoluţiei (creştere rapidă, recurenţe locale) şi prezenţei metastazelor. Toţi au urmat un tratament radical sau conservator, dar în jumătate din cazuri a survenit decesul. Cea mai bună evoluţie au avut-o cei la care încă de la început s-a efectuat excizie urmată de radioterapie. Autorii atrag atenţia asupra importanţei apelării la tratamentele radicale în cazul acestor pacienţi(30).
Studiul realizat de Yanik a evaluat răspunsul imun local la pacienţii HIV, având în vedere că aceştia nu au fost incluşi în studii asupra agenţilor de tipul checkpoint inhibitors, dat fiind gradul de imunosupresie. Autorii au observat că infecţia HIV nu influenţează infiltratul inflamator în cazul CSC anal şi nici expresia PDL-1, rezultate care deschid noi orizonturi în terapia biologică la pacienţii infectaţi HIV(31). De asemenea, Heppt a tratat nouă pacienţi cu checkpoint inhibitors şi nu a observat efecte importante asupra încărcăturii virale sau a numărului de limfocite CD4. Mai mult decât atât, s-a observat remisie totală în cazul pacientului cu cel mai mic număr de limfocite CD4 la începutul terapiei(32). Actualmente sunt disponibile mai multe studii în care s-au administrat checkpoint inhibitors la pacienţi infectaţi HIV şi s-au obţinut rezultate încurajatoare(33).
Melanomul
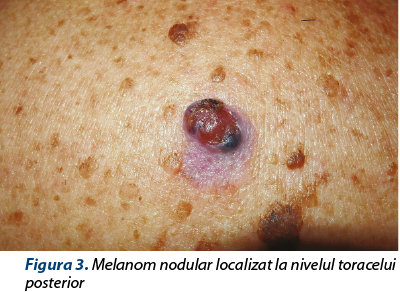
Cazurile de melanom reprezintă aproximativ 4% dintre cazurile de cancer cutanat, numărul fiind în creştere. Este o tumoră foarte agresivă, cu risc important de metastazare. Principalul factor de risc este expunerea la razele ultraviolete, care au efect direct sau indirect asupra ADN-ului, ceea conduce la carcinogeneză(34). Melanomul îşi are originea la nivelul melanocitelor când apare de novo, sau la nivelul nevocitelor, când se dezvoltă pe leziuni nevice preexistente. Forma cutanată este cea mai frecventă (figura 3), dar se poate localiza şi la nivelul mucoaselor sau uveal(35).
Datele despre riscul de a dezvolta melanom în rândul pacienţilor infectaţi HIV sunt destul de puţine. Se ştie că incidenţa este mai crescută în rândul celor transplantaţi, ceea ce arată un posibil rol al imunosupresiei în dezvoltarea melanomului(36). Studiul caz-control realizat de Lanoy şi colab., care a inclus 29956 de indivizi vârstnici (cu vârste peste 67 de ani) HIV-pozitivi sau care au suferit un transplant de organ şi au fost diagnosticaţi cu cancer cutanat, a evidenţiat că cel mai frecvent a fost înregistrat melanomul, cu menţiunea că nu au fost luate în calcul CBC şi CSC, datele referitoare la aceste tumori nefiind disponibile(37).
Studiul realizat de Yanik a inclus un număr important de pacienţi infectaţi HIV (33934) în rândul cărora au fost diagnosticate opt cazuri de melanom, incidenţa nefiind mai mare decât în populaţia generală(36). Rodrigues şi colab. au pus în evidenţă că pacienţii HIV-pozitivi au o evoluţie mai agresivă a melanomului, ceea ce implică un prognostic mai slab în comparaţie cu cei HIV-negativi(38). Astfel, Wilkins şi colab. recomandă screeningul pacienţilor diagnosticaţi cu melanom, pentru depistarea metastazelor, efectuarea anuală a unei radiografii toracice şi determinarea nivelului lactat-dehidrogenazei. În plus, autorii atrag atenţia asupra importanţei colaborării cu un oncolog(39).
Concluzii
În ciuda tuturor programelor de prevenţie implementate pentru a reduce numărul cazurilor de infecţie HIV, incidenţa este în creştere. Imunosupresia cauzată de infecţia HIV conduce la apariţia a diverse patologii. Astfel, au fost descrise cancere care definesc sau nu SIDA. Cele mai frecvente cancere cutanate care nu definesc SIDA sunt CBC, CSC şi melanomul. Conform mai multor studii, incidenţa lor este mai crescută în rândul acestor pacienţi comparativ cu populaţia generală, de aceea se recomandă acordarea unei atenţii sporite asupra depistării acestor neoplazii.
Conflict of interests: The authors declare no conflict of interest.
Bibliografie
- https://www.who.int/news-room/fact-sheets/detail/hiv-aids
- Feinberg J, Keeshin S. Management of Newly Diagnosed HIV Infection. Ann Intern Med. 2017;167(1):ITC1-ITC16.
- Khalsa AM. Preventive counseling, screening, and therapy for the patient with newly diagnosed HIV infection. Am Fam Physician. 2006;73(2):271-80.
- Kwong J, Gabler S. Counseling, screening, and therapy for newly-diagnosed HIV patients. Nurse Pract. 2015;40(10):34-43.
- Deeken JF, Tjen-A-Looi A, Rudek MA, et al. The rising challenge of non-AIDS-defining cancers in HIV-infected patients. Clin Infect Dis. 2012;55(9):1228-35.
- Chang AY, Doiron P, Maurer T. Cutaneous malignancies in HIV. Curr Opin HIV AIDS. 2017;12(1):57-62.
- Zhao H, Shu G, Wang S. The risk of non-melanoma skin cancer in HIV-infected patients: new data and meta-analysis. Int J STD AIDS. 2016;27(7):568-75.
- Asgari MM, Ray GT, Quesenberry CP Jr, et al. Association of Multiple Primary Skin Cancers With Human Immunodeficiency Virus Infection, CD4 Count, and Viral Load. JAMA Dermatol. 2017;153(9):892-896.
- Garlassi E, Harding V, Weir J, et al. Nonmelanoma skin cancers among HIV-infected persons in the HAART era. J Acquir Immune Defic Syndr. 2012;60(2):e63-5.
- Goncalves PH, Montezuma-Rusca JM, Yarchoan R, et al. Cancer prevention in HIV-infected populations. Semin Oncol. 2016;43(1):173-188.
- Grulich AE, van Leeuwen MT, Falster MO, et al. Incidence of cancers in people with HIV/AIDS compared with immunosuppressed transplant recipients: a meta-analysis. Lancet. 2007;370(9581):59-67.
- Crum-Cianflone N, Hullsiek KH, Marconi V, et al. Trends in the incidence of cancers among HIV-infected persons and the impact of antiretroviral therapy: a 20-year cohort study. AIDS. 2009;23(1):41-50.
- Bedimo R, Chen RY, Accortt NA, et al. Trends in AIDS-defining and non-AIDS-defining malignancies among HIV-infected patients: 1989-2002. Clin Infect Dis. 2004;39(9):1380-4.
- Ceccarelli M, Rullo EV, Facciolà A, et al. Head and neck squamous cell carcinoma and its correlation with human papillomavirus in people living with HIV: a systematic review. Oncotarget. 2018;9(24):17171-17180.
- Clifford GM, Polesel J, Rickenbach M, et al. Cancer risk in the Swiss HIV Cohort Study: associations with immunodeficiency, smoking, and highly active antiretroviral therapy. J Natl Cancer Inst. 2005;97(6):425-32.
- Crowson AN. Basal cell carcinoma: biology, morphology and clinical implications. Mod Pathol. 2006;19 Suppl 2:S127-47.
- Telfer NR, Colver GB, Morton CA, et al. Guidelines for the management of basal cell carcinoma. Br J Dermatol. 2008;159(1):35-48
- Marzuka AG, Book SE. Basal cell carcinoma: pathogenesis, epidemiology, clinical features, diagnosis, histopathology, and management. Yale J Biol Med. 2015;88(2):167-79.
- Wong CS, Strange RC, Lear JT. Basal cell carcinoma. BMJ. 2003;327(7418):794-8.
- Basset-Séguin N, Hauschild A, Kunstfeld R, et al. Vismodegib in patients with advanced basal cell carcinoma: Primary analysis of STEVIE, an international, open-label trial. Eur J Cancer. 2017;86:334-348.
- Alam M, Ratner D. Cutaneous squamous-cell carcinoma. New Engl J Med. 2001;344(13):975-83.
- Wilkins K, Turner R, Dolev JC, et al. Cutaneous malignancy and human immunodeficiency virus disease. J Am Acad Dermatol. 2006;54(2):189-206.
- Omland SH, Ahlström MG, Gerstoft J, et al. Risk of skin cancer in HIV infected patients: a Danish nationwide cohort study. J Am Acad Dermatol. 2018. doi: 10.1016/j.jaad.2018.03.024.
- Parekh V, Seykora JT. Cutaneous Squamous Cell Carcinoma. Clin Lab Med. 2017;37(3):503-525.
- Stratigos A, Garbe C, Lebbe C, et al. Diagnosis and treatment of invasive squamous cell carcinoma of the skin: European consensus-based interdisciplinary guideline. Eur J Cancer. 2015;51(14):1989-2007.
- Picard A, Arowas L, Piroth L, et al. Head and neck squamous cell carcinoma in people living with HIV in France. Med Mal Infect. 2018;48(8):503-508.
- Shiels MS, Cole SR, Kirk GD, Poole C. A meta-analysis of the incidence of non-AIDS cancers in HIV-infected individuals. J Acquir Immune Defic Syndr. 2009;52(5):611-22.
- Hausauer AK, Maurer T, Leslie KS, et al. Recurrence after treatment of cutaneous basal cell and squamous cell carcinomas in patients infected with human immunodeficiency virus. JAMA Dermatol. 2013 Feb;149(2):239-41.
- Silverberg MJ, Leyden W, Warton EM, et al. HIV infection status, immunodeficiency, and the incidence of non-melanoma skin cancer. J Natl Cancer Inst. 2013;105(5):350-60.
- Nguyen P, Vin-Christian K, Ming ME, et al. Aggressive squamous cell carcinomas in persons infected with the human immunodeficiency virus. Arch Dermatol. 2002;138(6):758-63.
- Yanik EL, Kaunitz GJ, Cottrell TR, et al. Association of HIV status with local immune response to anal squamous cell carcinoma: implications for immunotherapy. JAMA Oncol. 2017;3(7):974-978.
- Heppt MV, Schlaak M, Eigentler TK, et al. Checkpoint blockade for metastatic melanoma and Merkel cell carcinoma in HIV-positive patients. Ann Oncol. 2017;28(12):3104-3106.
- Marra A, Scognamiglio G, Peluso I, et al. Immune Checkpoint Inhibitors in Melanoma and HIV Infection. Open AIDS J. 2017;11:91-100.
- Sample A, He YY. Mechanisms and prevention of UV-induced melanoma. Photodermatol Photoimmunol Photomed. 2018 ;34(1):13-24.
- Ali Z, Yousaf N, Larkin J, et al. Melanoma epidemiology, biology and prognosis. EJC Suppl. 2013;11(2):81-91.
- Yanik EL, Hernández-Ramírez RU, Qin L, et al. Brief Report: Cutaneous Melanoma Risk Among People With HIV in the United States and Canada. J Acquir Immune Defic Syndr. 2018;78(5):499-504.
- Lanoy E, Costagliola D, Engels EA. Skin cancers associated with HIV infection and solid-organ transplantation among elderly adults. Int J Cancer. 2010;126(7):1724-31.
- Rodrigues LK, Klencke BJ, Vin-Christian K, et al. Altered clinical course of malignant melanoma in HIV-positive patients. Arch Dermatol. 2002;138(6):765-70.
- Wilkins K, Dolev JC, Turner R, et al. Approach to the treatment of cutaneous malignancy in HIV‐infected patients. Dermatol Ther. 2005;18(1):77-86.
