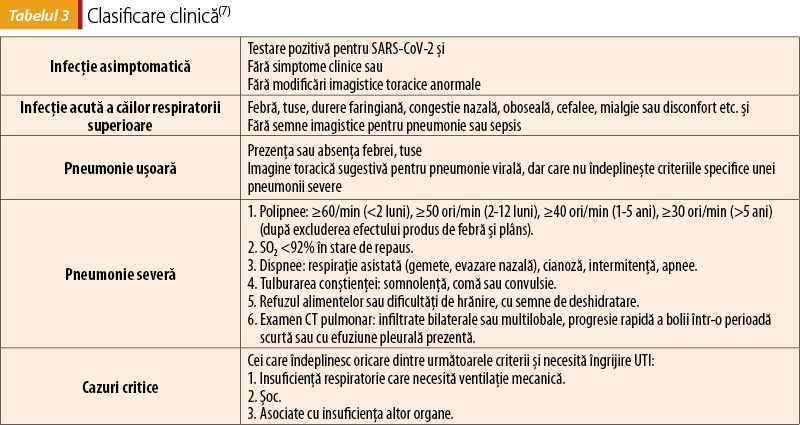
Infecţia cu SARS-CoV-2 în populaţia pediatrică
SARS-CoV-2 infection in the pediatric population
Abstract
Data from the Centers for Disease Control and Prevention (CDC) demonstrate a lower incidence of SARS-CoV-2 infection and severe disease in children than in adults. At this time, no public data have been identified on the incidence of COVID-19 in the pediatric population of Romania. In the current epidemiological context, the family doctor has a fundamental role in identifying and managing COVID-19 cases in Romania, despite the fact that he was deprived of guidance with specific recommendations to help him in the management of COVID-19 disease in children. The purpose of this paper is to provide recommendations to the family doctors who are taking care of children aged 1 month to 18 years old, with up-to-date information on children confirmed with COVID-19 as well as on child care during the pandemic. Materials and method. Systematic review of articles and studies published in virtual libraries (PubMed, Cochrane, BMJ, Elsevier, JAMA Network, The Lancet, New England Journal of Medicine, Springer Nature, Wiley) between December 2020 and March 2021, on SARS-CoV-2 infection in children. Discussion and conclusions. The incubation period of SARS-CoV-2 appears to be approximately the same for children as in adults, 2-14 days, with an average of 6 days. Infants under 3 months of age and children with underlying diseases (congenital heart and respiratory diseases, chronic heart and kidney diseases, malnutrition, hereditary metabolic diseases, immunodeficiency, tumors etc.) can become severe cases. Most children have relatively mild clinical symptoms without fever or pneumonia and recover within 1-2 weeks. The most common symptoms in children are cough and/or fever. Depending on the clinical elements corroborated with the imaging ones, COVID-19 cases can be classified into: asymptomatic infection, acute upper respiratory tract infection, mild pneumonia, severe pneumonia, critical cases. Severe pediatric cases present with obvious dyspnea and may progress rapidly to acute respiratory distress syndrome, septic shock, refractory metabolic acidosis, coagulation disorder, encephalopathy, and multiple organ failure. Those who progress to the severe form may have a low to moderate fever and may even be deprived of the fever characteristic of the disease. The multisystem inflammatory syndrome in children is a serious late complication of SARS-CoV-2 infection that can develop in a minority of children and young adults. Most children with mild or moderate illness can only be treated with supportive care which includes the prevention and management of complications.Keywords
SARS-CoV-2COVID-19managementchildrenprimary careRezumat
Datele de la Centrele pentru Controlul şi Prevenirea Bolilor (CDC) demonstrează o incidenţă mai mică a infecţiei cu SARS-CoV-2 şi a bolilor severe la copii decât la adulţi. În acest moment, nu au fost identificate date publice cu privire la incidenţa COVID-19 în populaţia pediatrică din România. În contextul epidemiologic actual, medicul de familie are un rol fundamental în identificarea şi gestionarea cazurilor de COVID-19 în România, în ciuda faptului că acesta a fost privat de o ghidare cu recomandări specifice care să-l ajute în managementul afecţiunii la copil. Scopul acestei lucrări este de a oferi recomandări medicilor de familie care îngrijesc copii cu vârsta cuprinsă între 1 lună şi 18 ani, cu informaţii actualizate despre copiii confirmaţi cu COVID-19, precum şi despre îngrijirea copiilor în timpul pandemiei. Materiale şi metodă. Revizuirea sistematică a articolelor şi studiilor publicate în bibliotecile virtuale (PubMed, Cochrane, BMJ, Elsevier, JAMA Network, The Lancet, New England Journal of Medicine, Springer Nature, Wiley) în perioada decembrie 2020 – martie 2021, privind infecţia cu SARS-CoV-2 la copii. Discuţie şi concluzii. Perioada de incubaţie a SARS-CoV-2 pare a fi aproximativ aceeaşi pentru copii, ca şi la adulţi, de 2-14 zile, cu o medie de 6 zile. Sugarii sub 3 luni şi copiii cu boli subiacente (afecţiuni congenitale cardiace şi de căi respiratorii, boli cronice ale inimii şi rinichilor, malnutriţie, boli metabolice ereditare, imunodeficienţă, tumori etc.) pot deveni cazuri severe. Majoritatea copiilor au simptome clinice relativ uşoare, fără febră sau pneumonie, şi se recuperează în decurs de 1-2 săptămâni. Cele mai frecvente simptome la copii sunt tusea şi/sau febra. În funcţie de elementele clinice, coroborate cu cele imagistice, cazurile de COVID-19 pot fi clasificate în: infecţie asimptomatică, infecţie acută a căilor respiratorii superioare, pneumonie uşoară, pneumonie severă, cazuri critice. Cazurile pediatrice severe prezintă dispnee evidentă şi pot evolua rapid către sindrom de detresă respiratorie acută, şoc septic, acidoză metabolică refractară, tulburare de coagulare, encefalopatie şi insuficienţă multiplă de organe. Cei care evoluează către forma gravă pot avea febră scăzută până la moderată şi chiar pot să nu prezinte febra caracteristică bolii. Sindromul inflamator multisistemic la copil este o complicaţie tardivă gravă a infecţiei cu SARS-CoV-2 care se poate dezvolta la o minoritate de copii şi adulţi tineri. Majoritatea copiilor cu boli uşoare sau moderate pot fi trataţi numai cu îngrijire de susţinere, care include prevenirea şi gestionarea complicaţiilor.Cuvinte Cheie
SARS-CoV-2COVID-19managementcopiiîngrijire primarăInfecţia cu SARS-CoV-2 în populaţia pediatrică
Aceste recomandări sunt destinate medicilor de familie care îngrijesc copii, definiţi ca având vârsta cuprinsă între 1 lună şi 18 ani, cu informaţii actualizate despre copiii suspectaţi sau confirmaţi pentru COVID-19, precum şi despre îngrijirea copiilor în timpul pandemiei(1).
Introducere
La sfârşitul anului 2019, un focar de pneumonie cu etiologie necunoscută a apărut în Wuhan, provincia Hubei, China, iar apoi agentul patogen a fost izolat şi denumit Noul Coronavirus 2019 (2019-nCoV), la 12 ianuarie 2020(2).
Coronavirusurile (CoV) sunt o familie numeroasă de virusuri despre care se ştie că provoacă boli, de la răceala obişnuită până la maladii mai severe. Virus ARN protejat de un înveliş proteic (capsidă), coronavirusul este omniprezent la om, la alte mamifere şi la păsări, putând provoca tulburări respiratorii, digestive, hepatice şi ale sistemului nervos(3). Până în prezent, şase virusuri CoV au fost cunoscute a provoca infecţii la om. Dintre acestea, două virusuri zoonotice, SARS-CoV şi MERS-CoV, au fost responsabile de focare grave, în China, în 2002-2003, respectiv în Orientul Mijlociu, în 2012. Un nou coronavirus a fost identificat la sfârşitul anului 2019, în Wuhan, China. Acesta este un nou tip de coronavirus care nu a fost identificat anterior la oameni. La 11 februarie 2020, Grupul de studiu Coronavirus al Comitetului Internaţional pentru Taxonomia virusurilor a denumit noul tip de coronavirus sindromul respirator acut sever coronavirus 2 (SARS-CoV-2; severe acute respiratory syndrome coronavirus 2). În aceeaşi zi, OMS a denumit boala cauzată de noul tip de coronavirus drept boala coronavirus-2019 (COVID-19). Virusul s-a răspândit foarte repede în Wuhan, iar mai târziu, ca urmare a desfăşurării Festivalului chinezesc de primăvară, odată cu adunarea unui număr mare de oameni, a făcut ca acesta să se răspândească rapid în toată ţara, iar apoi, în peste 100 de ţări(4). La 12 martie 2020, OMS a anunţat că boala COVID-19 a atins statutul de pandemie(5).
Epidemiologie
Datele de la Centrele pentru Controlul şi Prevenirea Bolilor (CDC) demonstrează o incidenţă mai mică a infecţiei cu SARS-CoV-2 şi a bolilor severe la copii decât la adulţi(1).
Coronavirusurile – atât SARS-CoV, cât şi SARS-CoV-2 – au apărut pentru prima dată în China. Acestea au anumite asemănări biologice, epidemiologice şi patologice. Până în prezent, cercetările au arătat că genele lor prezintă 79% din secvenţe identice, iar structura domeniului de legare a receptorilor este, de asemenea, foarte similară. Au fost efectuate cercetări ample asupra SARS; totuşi, înţelegerea impactului fiziopatologic al bolii coronavirus 2019 (COVID-19) este încă limitată(6).
Incidenţa COVID-19 la copii
Copiii de toate vârstele sunt susceptibili la infecţia cu SARS-CoV-2(7). În SUA şi la nivel global, au fost raportate mai puţine cazuri de COVID-19 la copii (cu vârsta cuprinsă între 0 şi 17 ani) comparativ cu adulţii. Adevărata incidenţă a infecţiei cu SARS-CoV-2 la copii nu este cunoscută, din cauza lipsei de testare pe scară largă şi a priorităţii de testare la adulţi şi la cei cu boli severe(1). Ratele de spitalizare la copii sunt semnificativ mai mici decât ratele de spitalizare de la adulţii cu COVID-19, sugerând că cei mici pot avea o boală mai puţin gravă comparativ cu adulţii(1). Copiii cu boli subiacente (afecţiuni congenitale cardiace şi de căi respiratorii, boli cronice ale inimii şi rinichilor, malnutriţie, boli metabolice ereditare, imunodeficienţă, tumori etc.) pot deveni cazuri severe(7), dar şi sugarii sub 3 luni(7).
Copiii care îndeplinesc oricare dintre criteriile prezentate în tabelul 1 sunt cu risc ridicat de a deveni cazuri severe sau critice(7).
CDC a raportat faptul că adolescenţii şi adulţii tineri, indienii americani hispanici, afro-americanii, indienii americani non-hispanici, nativii din Alaska şi persoanele cu afecţiuni medicale subiacente sunt reprezentaţi în mod disproporţionat printre decesele asociate cu SARS-CoV-2 la persoanele cu vârsta mai mică de 21 de ani. Sugarii, copiii, adolescenţii şi adulţii tineri, în special cei din grupurile minoritare rasiale şi etnice cu risc mai mare, cei cu afecţiuni medicale subiacente şi îngrijitorii lor au nevoie de mesaje de prevenire a COVID-19 clare, consistente şi adecvate din punct de vedere lingvistic şi cultural (de exemplu, legat de purtarea măştii, distanţarea fizică, igiena mâinilor). Pentru a asigura o supraveghere exactă, este important ca furnizorii de servicii medicale şi departamentele de sănătate să asigure urmărirea sugarilor, copiilor, adolescenţilor şi adulţilor tineri infectaţi sau expuşi la SARS-CoV-2 şi să documenteze şi să raporteze condiţiile medicale subiacente şi cauza decesului, legat de COVID-19(8).
O analiză Cochrane publicată în iunie 2020 şi care a identificat 45 de lucrări ştiinţifice relevante a arătat că până atunci copiii au reprezentat 1-5% din cazurile de COVID-19 diagnosticate, având adesea boli mai uşoare decât adulţii, iar decesele au fost extrem de rare(9).
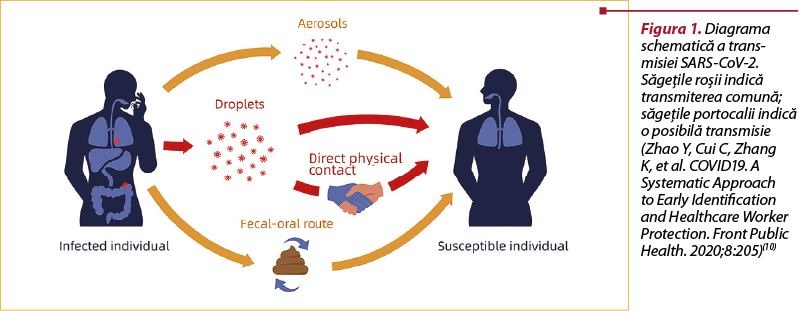
Transmisie
Picăturile respiratorii şi contactul apropiat sunt principalele căi de transmitere a infecţiei(9). Contactul strâns cu pacienţii infectaţi, cu sau fără simptome, este principala cale de transmitere a infecţiei cu SARS-CoV-2 la copii(9). Dovezi recente sugerează că, la fel ca adulţii, copiii au probabil sarcini virale similare în nazofaringe, rate similare de infecţii secundare şi pot răspândi virusul la alţii(1). În primele etape ale epidemiei, mulţi copii cu COVID-19 făceau parte din grupurile familiale cu boală(9). Datorită limitării de deplasare în comunitate şi închiderii şcolilor, transmiterea SARS-CoV-2 către şi între copii a fost redusă în Statele Unite în timpul pandemiei, în primăvara şi începutul verii anului 2020. Acest lucru poate explica incidenţa scăzută la copii în comparaţie cu cea de la adulţi. Compararea tendinţei infecţiei pediatrice înainte şi după revenirea în centrele de îngrijire a copiilor, şcoală, săli de sport pentru tineri sau pentru alte activităţi ne poate spori înţelegerea privind transmisia infecţiei cu SARS-CoV-2 la copii(1).
Particulele lichide sau solide cu un diametru mai mic de 5-10 µm sunt clasificate ca aerosoli şi rămân în suspensie în aer timp de secunde până la ore, în timp ce particulele sau picăturile cu diametru mai mare se depun rapid din aerul liniştit pe suprafeţe(11).
SARS-CoV-2 este emis sub formă de aerosoli în timpul respiraţiei normale, atât de persoanele asimptomatice, cât şi de cele simptomatice, rămânând viabil cu o perioadă de înjumătăţire de până la aproximativ o oră, timp în care mişcarea aerului îl poate duce la distanţe considerabile, deşi se dispersează simultan. Particulele de aerosoli care conţin SARS-CoV-2 se pot uni şi cu particule de poluare, iar rata de infecţie se corelează cu poluarea. Funcţionarea sistemelor de ventilaţie în clădirile publice şi transportul pot crea pericole de infecţie prin aerosoli, dar oferă oportunităţi de reducere a riscului de transmitere în moduri la fel de simple ca trecerea de la aerul recirculat la cel exterior(11). Există, de asemenea, oportunităţi de a inactiva SARS-CoV-2 sub formă de aerosoli cu lumina soarelui sau cu lămpi UV. Multe virusuri sunt sensibile la temperatură şi umiditate, dar efectele umidităţii asupra SARS-CoV-2 în aerosoli au fost considerate destul de slabe, spre deosebire de efectul său asupra viabilităţii reziduurilor de suprafaţă(11). Lumina puternică a soarelui reduce timpul de înjumătăţire în aerosoli la 2-3 minute, componenta UV a razelor solare fiind probabil cea responsabilă(11).
SARS-CoV-2 viu poate fi izolat din fecale şi urină la pacienţii infectaţi; clearance-ul acidului nucleic viral din fecale a fost identificat mai târziu decât în tampoanele nazofaringiene. Cu toate acestea, nu au fost detectate leziuni histopatologice sau antigenele SARS-CoV-2 în ţesuturile gastrointestinale(12). Cu alte cuvinte, ar trebui acordată atenţie atât transmiterii prin aerosoli, cât şi contactului cauzat de poluarea mediului cu fecale şi urină(7).
Nu există dovezi directe ale transmiterii verticale mamă-copil, dar nou-născuţii pot fi infectaţi prin contact strâns(9). Nou-născuţii au dezvoltat COVID-19 simptomatic, dar nu există dovezi ale transmiterii verticale intrauterine(9). O cohortă prospectivă din Marea Britanie, care a inclus 66 de nou-născuţi cu infecţie cu SARS-CoV-2, a constatat că 3% ar fi putut avea o posibilă infecţie dobândită pe cale verticală şi la 12% s-a suspectat o infecţie nosocomială(13). Un studiu de cohortă din Suedia (11 martie 2020 – 31 ianuarie 2021), care a cuprins 88159 de nou-născuţi (49% fete), 2323 (1,6%) fiind născuţi din 2286 de mame SARS-CoV-2 pozitive, a concluzionat că infecţia maternă cu SARS-CoV-2 în timpul sarcinii a fost semnificativ asociată cu creşteri mici ale unor morbidităţi neonatale. ARN-ul viral a fost detectat în placentă şi la nivelul membranelor, dar transmiterea intrauterină a SARS-CoV-2 de la mamă la făt a părut a fi rară(14).
Se sugerează că măsurile publice tradiţionale din pandemia de SARS-CoV nu sunt suficiente şi în pandemia de COVID-19. Colaborarea internaţională şi partajarea resurselor informaţionale pot ajuta la minimizarea dimensiunii focarului şi la reducerea deceselor la nivel mondial(9).
Patogenie
SARS-CoV-2 se leagă de ACE2, receptorul celulei-ţintă gazdă. Replicarea activă şi eliberarea virusului în celulele pulmonare duc la simptome nespecifice, precum febră, mialgie, cefalee şi simptome respiratorii. Virusul provoacă leziuni tranzitorii celulelor din epiteliul olfactiv, ducând la disfuncţie olfactivă, ceea ce poate explica pierderea temporară a gustului şi a mirosului, frecvent observate în COVID-19. Distribuţia receptorilor ACE2 în diferite ţesuturi poate explica situsurile infecţiei şi simptomele pacientului. De exemplu, receptorul ACE2 se găseşte pe epiteliul altor organe, cum ar fi intestinul şi celulele endoteliale din rinichi, alături de vasele de sânge, ceea ce poate explica simptomele gastrointestinale şi complicaţiile cardiovasculare. Endotelita limfocitară a fost observată la examinarea anatomopatologică post-mortem a plămânului, inimii, rinichilor şi ficatului, precum şi la necroza celulelor hepatice şi la infarctul miocardic la pacienţii care au murit de COVID-19. Aceste constatări indică faptul că virusul afectează în mod direct multe organe, aşa cum s-a văzut în SARS-CoV-1 şi influenza. Mai sunt şi alte necunoscute, astfel încât încă se mai caută răspunsuri la întrebarea dacă modificările patologice ale căilor respiratorii sau ale disfuncţiei endoteliale sunt rezultatul unei infecţii virale directe, furtunei de citokine, coagulopatiei sau sunt multifactoriale. Invazia virală directă sau coagulopatia contribuie direct la unele dintre complicaţiile ischemice, cum ar fi infarctele ischemice? Acestea ca şi multe alte necunoscute vor necesita studii suplimentare pentru elucidare(15).
Conform constatărilor patologice disponibile la pacienţii adulţi, sunt afectaţi în principal plămânii şi sistemul imunitar. Plămânii apar cu diferite grade de consolidare: cavitatea alveolară este invadată de lichid seros, exsudat de fibrină, cu formare de membrane; septul alveolar apare hiperemic şi edemaţiat, se pot observa infiltraţii cu celule mononucleare şi limfocite şi tromboză intravasculară; mucus, precum şi tampoane de mucus pot fi văzute în lumenul bronşic al plămânului(7).
SARS versus COVID-19
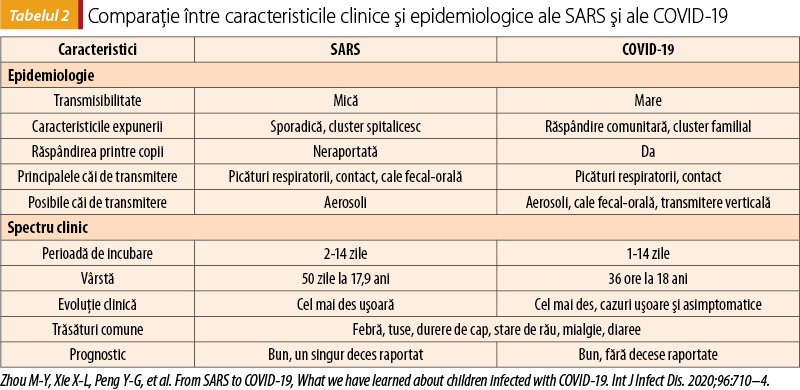
Coronavirusurile, atât SARS-CoV, cât şi SARS-CoV-2, au apărut pentru prima dată în China. Acestea au anumite asemănări biologice, epidemiologice şi clinice. Până în prezent, cercetările au arătat că genele lor prezintă 79% din secvenţe identice, iar structura domeniului de cuplare a receptorilor este, de asemenea, similară. Prin compararea acestor două boli, în cazul COVID-19 s-a constatat o transmisie mai rapidă şi mai largă, alături de o morbiditate şi mortalitate mai ridicată. Nou-născuţi, copii asimptomatici şi cazuri normale de imagistică a toracelui au apărut în literatura despre COVID-19. Copiii la care boala debutează cu simptome gastrointestinale pot evolua către afecţiuni severe, iar nou-născuţii ale căror mame sunt infectate cu SARS-CoV-2 ar putea avea complicaţii severe. Datele testelor de laborator au arătat că procentul de neutrofile şi nivelul de LDH sunt mai mari, iar numărul de celule CD4 T+ şi CD8 T+ este scăzut în cazurile de COVID-19 la copii(6).
Manifestările clinice ale COVID-19 la copii
Perioada de incubaţie a SARS-CoV-2 pare a fi aproximativ aceeaşi pentru copii ca şi la adulţi, de 2-14 zile, cu o medie de 6 zile(1).
O analiză Cochrane publicată în septembrie 2020, care a cuprins 737 de studii retrospective, cu excepţia unuia, şi care a înrolat 1614 pacienţi, majoritatea din China, cu excepţia a patru studii (Malaezia, Spania, Italia şi SUA), a estimat că 16% dintre copiii infectaţi cu SARS-CoV-2 sunt asimptomatici(16). O altă metaanaliză publicată în septembrie 2020 şi care a identificat studii asupra COVID-19 din 25 decembrie 2019 până la 30 aprilie 2020, cuprinzând 5829 de pacienţi pediatrici, a evidenţiat că proporţia pacienţilor asimptomatici de vârstă pediatrică a fost de 20%(17). Un alt studiu prospectiv, multicentric, efectuat în Franţa, care a colectat date din patru spitale din regiunea Parisului şi a înrolat 446 de pacienţi pediatrici în perioada 15 aprilie – 30 aprilie 2020, a sugerat că până la jumătate din infecţiile pediatrice pot fi asimptomatice, proporţia pacienţilor pediatrici pozitivi şi asimptomatici fiind de 35%(18). Alte dovezi evidenţiază că mai mult de jumătate din pacienţii de vârstă pediatrică infectaţi cu SARS-CoV-2 sunt asimptomatici(19).
Semnele şi simptomele COVID-19 la copii sunt similare cu cele ale altor infecţii şi procese neinfecţioase, inclusiv gripă, faringită streptococică şi rinită alergică. Lipsa specificităţii semnelor sau simptomelor şi proporţia semnificativă a infecţiilor asimptomatice fac ca screeningul bazat pe simptome pentru identificarea SARS-CoV-2 la copii să fie deosebit de dificil(18).
Semnele sau simptomele COVID-19 la copii includ(1):
- Febră
- Oboseală
- Durere de cap
- Mialgie
- Tuse
- Rinoree
- Pierderea recentă a gustului sau a mirosului
- Durere de gât
- Respiraţie scurtă sau dificultăţi de respiraţie
- Durere abdominală
- Diaree
- Greaţă sau vărsături
- Apetit diminuat
La unii copii, s-a semnalat şi prezenta wheezingului(9).
Copiii infectaţi cu SARS-CoV-2 pot avea mai multe dintre aceste simptome nespecifice sau doar câteva (cum ar fi doar simptomele respiratorii superioare sau numai simptomele gastrointestinale), sau pot fi asimptomatici. Cele mai frecvente simptome la copii sunt tusea şi/sau febra(1,17).
O analiză Cochrane publicată în februarie 2021, care a cuprins 44 de studii şi a inclus 26884 de participanţi, a concluzionat pe baza datelor disponibile în prezent că nici absenţa şi nici prezenţa semnelor sau simptomelor nu sunt suficient de precise pentru a exclude COVID‐19. Prezenţa anosmiei sau a ageuziei poate fi utilă ca semn de alarmă pentru COVID‐19. Prezenţa febrei sau a tusei, având în vedere sensibilitatea lor ridicată, poate fi, de asemenea, utilă pentru identificarea persoanelor cu indicaţie pentru testare, mai ales la populaţia pediatrică de vârstă şcolară(20).
Majoritatea copiilor au simptome clinice relativ uşoare, fără febră sau pneumonie, şi se recuperează în decurs de 1-2 săptămâni(7,21). O ipoteză atractivă pentru a explica boala mai puţin severă la copii în comparaţie cu adulţii este că vârsta pediatrică exprimă mai puţini receptori ai enzimei de conversie a angiotensinei 2 (ACE2) în epiteliul lor nazal, care explică o intrare virală mai redusă la copii şi, astfel, o infecţie mai uşoară(22). Dacă acest lucru este dovedit, atunci vizarea expresiei ACE2 în epiteliul nazal poate fi o abordare terapeutică potenţială pentru a reduce transmiterea SARS-CoV-2(22).
Cazurile pediatrice severe prezintă dispnee evidentă şi pot evolua rapid către sindrom de detresă respiratorie acută, şoc septic, acidoză metabolică refractară, tulburare de coagulare, encefalopatie şi insuficienţă multiplă de organe(1,7,9). Cei care evoluează către forma gravă pot avea febră scăzută până la moderată şi chiar poate lipsi febra caracteristică bolii(7).
Unii nou-născuţi au manifestat simptome gastrointestinale, cum ar fi vărsături, diaree şi dificultăţi în respiraţie(7). Incidenţa simptomelor critice şi a vărsăturilor a fost ridicată la copiii sub 1 an(17). Tratamentul sugerat a inclus furnizarea de oxigen, inhalări, suport nutriţional şi menţinerea echilibrelor de lichide şi electroliţi(9).
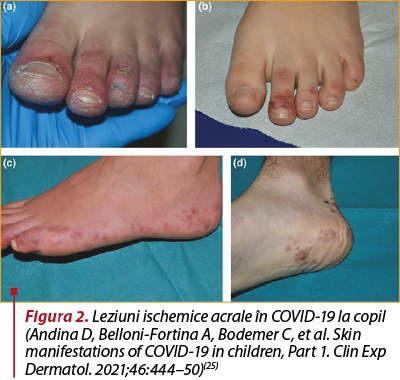
În mod similar, manifestările cutanate ale COVID-19 la copil diferă, de asemenea, de cele ale adulţilor. În timp ce manifestări precum urticarie, erupţie cutanată maculopapuloasă ori veziculară pot să apară la persoane de toate vârstele, anumite manifestări precum cele similare degerăturilor (19% din 375 de pacienţi cu manifestări cutanate de COVID-19(23)), eritemul multiform (EM) şi manifestări cutanate ale sindromului multisistemic inflamator pediatric asociat temporar cu SARS-CoV-2 (PIMS-TS) sunt mai frecvent observate la copii şi pacienţii tineri(24). Leziunile apar de obicei la copiii şi adolescenţii în stare bună de sănătate, rareori fiind observate la copii cu vârsta sub 10 ani. Apar pe picioare în 74-100% din cazuri, dar au fost descrise şi pe mâini şi degete. Leziunile sunt de obicei multiple, rotunde şi variază de la câţiva milimetri până la câţiva centimetri în dimensiune, afectând întregul deget de la picioare, cu o delimitare clară la nivelul metatarsofalangian (figura 2). Au fost observate pete şi umflături eritematoase, violacee sau purpurice, care pot apărea infiltrativ. Pielea periunghială şi subunghială este de obicei afectată. În evoluţia ulterioară, leziunile pot deveni veziculo-buloase sau pot prezenta cruste de culoare violet închis sau neagră. Pot fi implicate şi regiunea plantară, faţa laterală a picioarelor şi zona calcaneană, cu leziuni grosiere, echimotice şi infiltrative. Testarea SARS-CoV-2 prin PCR din probele nazofaringiene a fost negativă la aproape toţi copiii şi adolescenţii suspectaţi de COVID-19 (au fost raportate rezultate pozitive doar în 11% din cazuri); în plus, leziunile pot fi o manifestare tardivă atunci când ARN-ul viral nu mai este detectabil(25).
Lucrătorii din domeniul sănătăţii au un mare risc de contact cu pacienţi infectaţi şi au fost raportate mai multe grupuri de infecţie intraspitalicească, inclusiv în medii pediatrice, ameninţând atât lucrătorii din domeniul sănătăţii, cât şi pacienţii internaţi. În Italia, până la 20% dintre lucrătorii din domeniul sănătăţii ar fi putut fi infectaţi cu SARS-CoV-2. În contextul presiunii maxime aplicate asupra sistemelor de sănătate din multe ţări, protejarea lucrătorilor din domeniul sănătăţii şi lupta împotriva infecţiei nosocomiale cu SARS-CoV-2 sunt probleme majore. Pentru a limita riscul transmiterii intraspitaliceşti, sunt necesare strategii optime de screening pentru SARS-CoV-2 şi măsuri de prevenire(18).
Severitatea COVID-19 la copii
Dovezile actuale sugerează că pacienţii pediatrici cu anumite afecţiuni medicale subiacente şi sugarii (vârsta sub 1 an) ar putea fi expuşi unui risc crescut de forme severe de infecţie cu SARS-CoV-2(11,14). Dintre copiii care au dezvoltat boli severe din cauza COVID-19, majoritatea au avut afecţiuni medicale subiacente.
Există dovezi limitate despre condiţiile medicale care stau la baza creşterii riscului pentru forme severe. Dovezile actuale sugerează că pacienţii de vârstă pediatrică cu complexitate medicală, cu afecţiuni genetice, neurologice, metabolice sau cu boli cardiace congenitale ar putea prezenta un risc crescut de forme severe de COVID-19. Similar cu adulţii, copiii cu obezitate, diabet, astm sau boli pulmonare cronice, boli falciforme sau cu imunosupresie ar putea avea, de asemenea, un risc crescut de boală severă(1,7,22).
Se pare că majoritatea sugarilor şi copiilor cu anumite afecţiuni subiacente, precum cancer, care sunt infectaţi cu SARS-CoV-2 nu dezvoltă de obicei o formă severă de COVID-19, doar 5% necesitând spitalizare pentru simptome de COVID-19(26). Testarea a 120 de pacienţi pediatrici asimptomatici cu cancer a relevat doar o rată de 2,5% a pozitivităţii SARS-CoV-2. Prin comparaţie, s-a observat o rată de 14,7% a pozitivităţii SARS-CoV-2 la îngrijitorii lor asimptomatici (2,5%; IC 95%, 0,5-7,1% faţă de 14,7%; IC 95%, 7,3-25,4%; P=0,002)(26).
Copiii infectaţi cu SARS-CoV-2 sunt, de asemenea, expuşi riscului de a dezvolta sindromul inflamator multisistemic la copii (SIM-C)(1).
COVID-19 – analize paraclinice
Analize din sânge
Majoritatea pacienţilor prezintă markeri ai inflamaţiei uşor ridicaţi(1,7) (proteină C reactivă, VSH) şi uneori un nivel normal al procalcitoninei, deşi uneori aceasta poate fi normală(7). La unii pacienţi se pot remarca niveluri crescute ale markerilor hepatici şi ale lactat dehidrogenazei(1,7). Nivelul troponinei este crescut la unii pacienţi cu forme grave(1,7).
Pacienţii cu formă severă de boală prezintă niveluri crescute ale D-dimerilor şi feritinei şi scăderea progresivă a numărului de limfocite din sânge şi pot avea niveluri crescute ale factorilor inflamatori, cum ar fi IL-6, IL-4, IL-10 sau factorul de necroză tumorală (TNF-a)(7).
Examen radiologic
Imaginea radiologică toracică normală a apărut la 41% dintre pacienţii copii şi adolescenţi, în timp ce proporţia tomografiilor computerizate normale a fost de 35%(17).
Imaginile radiologice la copiii cu COVID-19 includ infiltratele unilaterale sau bilaterale pe radiografia toracică, iar la CT, opacităţi în sticlă mată şi consolidări cu halo înconjurător(1).
O analiză Cochrane publicată în martie 2021, care a inclus 51 de studii cu 19775 de participanţi, din care doar un singur copil, a evidenţiat că tomografia computerizată toracică (CT), radiografia toracică şi ultrasunetele oferă proporţii mai mari de rezultate pozitive la persoanele cu COVID-19 în comparaţie cu cele sănătoase. Pentru CT toracică, şansele de a obţine un rezultat pozitiv sunt de 87,9% la persoanele cu COVID-19 şi de 20% la cele sănătoase. Pentru radiografia toracică, şansele de a obţine un rezultat pozitiv sunt de 80,6% la persoanele cu COVID-19 şi de 28,5% la cele sănătoase. Pentru examinarea ecografică a plămânilor, şansele de a obţine un rezultat pozitiv sunt de 86,4% la persoanele cu COVID-19 şi 45,4% la cele sănătoase. Din cauza disponibilităţii limitate a datelor, estimările de precizie ale radiografiei toracice şi a examenului cu ultrasunete a plămânilor pentru diagnosticarea COVID-19 la participanţii suspectaţi trebuie interpretate cu atenţie(27). În comparaţie cu testarea RT-PCR, un potenţial avantaj major al imagisticii toracice este că rezultatele sunt disponibile mai repede şi că oferă o perspectivă mai bună asupra stării plămânilor. Cu toate acestea, imagistica CT toracică este de obicei disponibilă numai în unităţile de asistenţă medicală secundară şi terţiară, iar disponibilitatea variază între aceste unităţi(27).
Rolul examenului radiologic(27):
Imaginea toracică poate juca un rol integral în excluderea pneumoniei COVID-19 atunci când RT-PCR nu este disponibil, este în aşteptare sau este negativ ori când suspiciunea clinică este suficient de redusă pe baza altor semne, simptome şi teste de laborator de rutină.
Testarea simultană/combinată cu alte teste de diagnostic pentru a îmbunătăţi precizia diagnosticului. De exemplu, imagistica toracică ar putea fi utilizată în cazul suspiciunii unui RT-PCR fals negativ.
În îngrijirile primare, alternativele pentru diagnosticarea COVID-19 pot consta în semnele şi simptomele clinice şi testele rapide la punctul de îngrijire. În mod similar, ecografia la punctul de îngrijire poate fi utilizată, dacă resursele permit acest lucru. Avantajul testelor de laborator de rutină este că acestea pot aprecia gradul de severitate a bolii, valori peste cele de referinţă putând indica infecţii mai severe(28).
COVID-19 la copii: testare
Până în prezent, testul despre care se crede că este cel mai precis în detectarea SARS-CoV-2 este ARN viral SARS-CoV-2, care utilizează metoda Real Time-PCR (RT-PCR), evidenţiind virusul prin tehnici de amplificare a materialului genetic viral(28).
Copiii de vârstă şcoalară ar trebui să aibă prioritate pentru testarea virală dacă au:
Semne sau simptome ale COVID-19 şi
contact strâns (la o distanţă de sub 2 m de cineva pentru 15 minute sau mai mult) cu o persoană cu infecţie confirmată de laborator sau probabil infectată cu SARS-CoV-2 sau
probabilitate crescută de expunere (persoană care locuieşte sau călătoreşte într-o comunitate cu transmitere substanţială, aşa cum este definit de departamentul local de sănătate publică).
Nu există simptome, dar a avut un contact strâns (sub 2 m de cineva pentru 15 minute sau mai mult) cu o persoană cu infecţie confirmată de laborator sau probabil infectată cu SARS-CoV-2.
Copiii cu simptome ale unei boli infecţioase nu ar trebui să frecventeze şcoala, dar perioada de timp în care copilul ar trebui să rămână acasă depinde de etiologia cea mai probabilă a bolii (COVID-19 sau nu). Politicile de reîntoarcere la şcoală pentru copiii cu COVID-19 ar trebui să se bazeze pe recomandarea CDC de a întrerupe izolarea la domiciliu. Un test negativ sau o adeverinţă medicală nu ar trebui să fie necesare pentru întoarcerea la şcoală după terminarea celor 10 zile de izolare, cu ameliorarea simptomelor.
Dacă un copil are simptome de COVID-19, dar nu a avut un contact strâns (la o distanţă sub 2 metri de cineva timp de 15 minute sau mai mult) cu o persoană cu infecţie cu SARS-CoV-2 confirmată de laborator sau probabilă, copilul nu are o probabilitate crescută de expunere la SARS-CoV-2 şi ar trebui să fie evaluat pentru alte afecţiuni. Dacă un furnizor de asistenţă medicală decide că pacientul pediatric nu are COVID-19, acesta ar trebui să aibă voie să frecventeze şcoala în conformitate cu politicile şcolare existente pentru bolile non-COVID-19 (exemplu: afebrilitate fără antipiretice timp de 24 de ore pentru bolile virale non-COVID-19 sau după iniţierea antibioticelor pentru bolile bacteriene).
Dacă un copil are simptome de COVID-19 şi o probabilitate crescută de expunere (locuieşte sau s-a deplasat într-o comunitate cu transmitere substanţială), ar trebui să fie testat pentru infecţia cu SARS-CoV-2, dacă este posibil. Dacă rezultatul testului este negativ, copilul ar trebui să aibă voie să se întoarcă la şcoală odată ce simptomele bolii s-au îmbunătăţit, în concordanţă cu politicile de întoarcere non-COVID la şcoală. Dacă nu se poate face testare, copilul ar trebui să fie considerat un caz suspect pentru COVID-19 şi ar trebui izolat.
Dacă un copil a avut un contact strâns cu o persoană cu COVID-19, acesta ar trebui să fie testat pentru SARS-CoV-2.
Testele virale (acid nucleic sau antigen) sunt recomandate pentru a diagnostica infecţia acută cu SARS-CoV-2. Strategiile de testare, inclusiv criteriile clinice pentru luarea în considerare a testării şi tipul de specimen recomandat, sunt aceleaşi pentru copii şi adulţi.
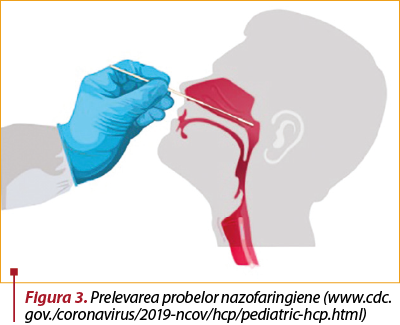
Prelevarea probelor(1)
A. Căile respiratorii superioare
Prelevarea probelor nazofaringiene (NF)/orofaringiene (gât) (OF) se va face numai de către un furnizor de asistenţă medicală instruit.
Utilizaţi numai tampoane din fibre sintetice cu arbori subţiri din plastic sau sârmă care au fost proiectate pentru prelevare de probe la nivelul mucoasei nazofaringiene. Nu utilizaţi tampoane de alginat de calciu sau tampoane cu arbori de lemn, deoarece acestea pot conţine substanţe care inactivează unele virusuri şi pot inhiba testele moleculare.
CDC recomandă colectarea numai a specimenului NF, deşi un specimen OF poate fi un tip de specimen acceptabil. Dacă sunt colectate atât specimenele NF, cât şi OP, se recomandă a se combina într-un singur tub pentru a maximiza sensibilitatea.
Tehnica recoltării
Instrucţiuni pentru prelevarea probelor din nazofaringe:
Înclinaţi capul pacientului înapoi cu 70 de grade.
Introduceţi uşor şi încet un tampon cu un ax flexibil (sârmă sau plastic) prin nară, paralel cu palatul (nu în sus) până când se întâlneşte rezistenţă sau distanţa este echivalentă cu cea de la ureche la nara pacientului, indicând contactul cu nazofaringele.
Frecaţi uşor şi rulaţi tamponul.
Lăsaţi tamponul în loc câteva secunde pentru a absorbi secreţiile.
Scoateţi încet tamponul în timp ce îl rotiţi. Exemplarele pot fi colectate din ambele părţi folosind acelaşi tampon, dar nu este necesar să se colecteze exemplarele din ambele părţi dacă minitipul este saturat cu lichid din prima colectare. Dacă un sept este deviat sau blocat şi creează dificultăţi în obţinerea specimenului dintr-o nară, utilizaţi acelaşi tampon pentru a obţine specimenul din cealaltă nară.
Introduceţi tamponul cu vârful mai întâi în tubul de transport furnizat.
Instrucţiuni pentru colectarea unui specimen OP (efectuat de un furnizor de asistenţă medicală instruit):
Introduceţi tamponul în zona faringelui posterior şi a amigdalelor.
Frecaţi tamponul peste ambii stâlpi amigdalieni şi pe orofaringele posterior şi evitaţi atingerea limbii, a dinţilor şi a gingiilor.
Aşezaţi tamponul, vârful mai întâi, în tubul de transport furnizat.
Pentru un ghid vizual, consultaţi pictograma infografică pentru paşii de colectare a specimenelor nazofaringiene.
Instrucţiuni pentru prelevarea probei din orofaringe(1):
Introduceţi tamponul în zona faringelui posterior şi a amigdalelor.
Frecaţi tamponul peste ambii stâlpi amigdalieni şi pe orofaringele posterior şi evitaţi atingerea limbii, a dinţilor şi a gingiilor.
Introduceţi tamponul cu vârful mai întâi în tubul de transport furnizat.
Prelevarea eşantionului din sângele capilar(1):
Eşantioanele de sânge sunt utilizate pentru teste de anticorpi (serologice); eşantioanele sunt colectate prin înţeparea pielii degetului cu un dispozitiv.
Dispozitivele de înţepare nu trebuie utilizate niciodată pentru mai mult de o persoană, din cauza riscului de contractare a altor boli infecţioase transmisibile din sânge.
Tehnică:
Spălaţi-vă mâinile cu apă caldă cu săpun şi uscaţi-vă bine mâinile sau efectuaţi igiena mâinilor folosind un dezinfectant pentru mâini pe bază de alcool!
Puneţi mănuşi pentru colectarea specimenului de sânge cu vârful degetelor!
Ţineţi mâna persoanei testate în poziţie descendentă şi masaţi mâna pentru a îmbunătăţi fluxul de sânge în degete!
Utilizaţi degetul mijlociu sau inelar pentru colectarea probelor! Localizaţi punctul de puncţie – partea laterală a vârfului degetului!
Curăţaţi locul puncţiei cu un tampon cu alcool izopropilic de 70% şi lăsaţi-l să se usuce la aer!
Utilizaţi dispozitivul de colectare furnizat de producător sau o lancetă de unică folosinţă, care se retrage la puncţie pentru efectuarea ei! Urmaţi instrucţiunile producătorului dacă utilizaţi dispozitivul de colectare!
Aruncaţi imediat dispozitivele pentru puncţionare într-un container aprobat pentru obiecte ascuţite!
Îndepărtaţi corect mănuşile şi aruncaţi-le în recipientele corespunzătoare!
Schimbaţi mănuşile între contactele cu fiecare persoană testată! Schimbaţi mănuşile care au atins obiecte potenţial contaminate cu sânge înainte de a atinge suprafeţe curate!
Spălaţi şi uscaţi bine mâinile sau efectuaţi igiena mâinilor imediat după îndepărtarea mănuşilor şi înainte de a atinge consumabilele medicale destinate utilizării altor persoane!
Managementul infecţiei cu SARS-CoV-2
în populaţia pediatrică
Furnizorii de asistenţă medicală pediatrică ar trebui să ia în considerare prezentarea clinică a copilului, cerinţa de îngrijire, condiţiile medicale subiacente şi capacitatea îngrijitorilor de a îngriji copilul la domiciliu(1):
Pacientul este suficient de stabil pentru a primi îngrijiri la domiciliu.
Îngrijitorii copilului sunt disponibili pentru îngrijiri la domiciliu.
Există un dormitor în care pacientul se poate recupera fără a împărţi spaţiul cu ceilalţi.
Există o baie separată pentru pacient. Dacă acest lucru nu este fezabil, trebuie avut grijă ca baia să fie dezinfectată după fiecare utilizare.
Sunt disponibile resurse pentru accesul la alimente şi alte necesităţi.
Pacientul şi ceilalţi membri ai gospodăriei sunt capabili să respecte precauţiile recomandate ca parte a îngrijirii la domiciliu sau a izolării. Aceasta include capacitatea pacientului de a purta o mască atunci când este indicat (această recomandare se bazează pe dovezile care atestă rolul picăturilor respiratorii în răspândirea virusului ce provoacă COVID-19, asociat cu dovezile emergente din studiile clinice şi de laborator care arată că măştile reduc pulverizarea picăturilor atunci când sunt purtate pe nas şi gură).
Îngrijitorul poate purta, de asemenea, o mască atunci când îngrijeşte o persoană bolnavă şi ar trebui să practice acţiuni preventive de zi cu zi pentru a evita îmbolnăvirea.
Persoanele cu risc crescut de boală severă (persoanele în vârstă; femeile gravide; adulţii cu condiţii medicale: cancer; boală cronică de rinichi; bolile cronice de plămâni care includ BPOC, astmul moderat şi sever, fibroză chistică, HTP; demenţa şi alte condiţii neurologice, cum ar fi accidentele vasculare cerebrale; sindromul Down; afecţiuni cardiace cronice care includ insuficienţă cardiacă, arteriopatiile coronariene, cardiomiopatia, HTA; infecţia cu HIV; statusul imunocompromis; afecţiunile hepatice, cum ar fi hepatita alcoolică, ciroza; obezitatea; talasemia şi anemia falciformă, transplantul de organ) nu ar trebui să aibă grijă de membrii gospodăriei care au COVID-19, dacă este posibil.
Oferiţi părinţilor suport informativ cu privire la semnele de alarmă care exprimă agravarea simptomelor, cu indicaţie pentru internare, în îngrijirile la domiciliu ale copilului infectat cu SARS-CoV-2(1)!
În prezent, nu există medicamente aprobate în mod specific de către Administraţia SUA pentru Alimente şi Medicamente (FDA) pentru tratamentul COVID-19 la copii(1).
Tratamentul COVID-19 rămâne în mare măsură de susţinere şi include prevenirea şi gestionarea complicaţiilor(1).
Infecţia cu SARS-CoV-2 este în general mai uşoară la copii decât la adulţi şi o proporţie substanţială a copiilor au infecţie asimptomatică.
Majoritatea copiilor infectaţi cu SARS-CoV-2 nu vor necesita nicio terapie specifică(29,30).
Terapia specifică
Majoritatea copiilor cu forme uşoare sau moderate pot fi trataţi numai cu îngrijire de susţinere (AIII)(29,30).
Remdesivir este un antiviral potenţial util pentru tratamentul COVID-19, care inhibă ARN polimeraza ARN-dependentă, blocând prematur transcripţia ARN(30). Eficienţa remdesivirului este ca a oricărei medicaţii antivirale, cu atât mai ridicată, cu cât se administrează mai precoce după debutul simptomatologiei; este mai eficient la pacienţi cu hipoxie cu necesar redus de oxigen suplimentar, faţă de cei care necesită un flux mare de oxigen, ventilaţie invazivă sau neinvazivă, ECMO(30). Are activitate in vitro împotriva coronavirusurilor, inclusiv împotriva SARS-CoV-2, şi este recomandat pentru(29):
Copiii spitalizaţi cu vârsta ≥12 ani cu COVID-19 care au factori de risc pentru boli severe şi au o nevoie emergentă sau crescândă de oxigen suplimentar(29).
Copiii spitalizaţi cu vârsta ≥16 ani cu COVID-19 care au o nevoie emergentă sau crescândă de oxigen suplimentar, indiferent dacă au factori de risc pentru boli severe(29).
În consultare cu un specialist în boli infecţioase pediatrice, remdesivirul poate fi luat în considerare pentru copiii spitalizaţi de toate vârstele cu COVID-19 care au o nevoie emergentă sau crescândă de oxigen suplimentar(29).
Doza de tratament: 200 mg/zi în ziua 1, apoi 100 mg/zi; copiii sub 40 kg şi >3,5 kg: 5 mg/kgc/zi în ziua 1, apoi 2,5 mg/kgc/zi; durata de tratament: 5 zile (10 zile la pacient IOT sau cu oxigenare cu membrană extracorporală ECMO)(30).
Grupul de experţi în tratamentul COVID-19 recomandă utilizarea dexametazonei pentru copiii spitalizaţi cu COVID-19 care necesită oxigen cu debit mare, ventilaţie neinvazivă, ventilaţie mecanică invazivă sau oxigenare cu membrană extracorporală(29,30).
Anticorpii monoclonali neutralizanţi au specificitate pentru proteina S a SARS-CoV-2; asemenea altor medicaţii antivirale, eficienţa depinde de administrarea cât mai precoce după debutul bolii, nu mai târziu de primele 10 zile, când de multe ori replicarea virală s-a diminuat semnificativ şi începe producerea de anticorpi specifici de către pacient(30). Nu există suficiente date pediatrice pentru ca grupul să recomande fie pentru, fie împotriva utilizării produselor de anticorpi monoclonali anti-SARS-CoV-2 pentru copiii cu COVID-19 care nu sunt spitalizaţi, dar care au factori de risc pentru boli severe(29). Pe baza studiilor la adulţi, bamlanivimab plus etesevimab sau casirivimab plus imdevimab pot fi luaţi în considerare de la caz la caz pentru copiii nespitalizaţi care îndeplinesc criteriile Autorizaţiei de utilizare în urgenţă (EUA) pentru risc crescut de boală severă, în special cei care îndeplinesc mai multe criterii sau au vârsta ≥12 ani (NIH ≥16 ani)(29,30). Grupul recomandă consultarea unui specialist în boli infecţioase pediatrice în astfel de cazuri(29).
Administrarea de plasmă de convalescent pleacă de la premisa că un pacient care nu are o imunodepresie va avea după infecţia cu SARS-CoV-2 un nivel suficient de anticorpi protectivi pentru a putea fi folosiţi în scopul limitării replicării virale la un pacient cu COVID-19. Totuşi, momentul optim al recoltării rămâne incert, având în vedere datele limitate privind dinamica anticorpilor, inclusiv scăderea rapidă a titrului IgG anti-SARS-CoV-2 în primele 2-3 luni după vindecare(30). Grupul nu recomandă utilizarea plasmei convalescente pentru copiii spitalizaţi cu COVID-19 care nu necesită ventilaţie mecanică (AIII)(29). Grupul nu recomandă utilizarea plasmei pentru pacienţii pediatrici cu COVID-19 care sunt ventilaţi mecanic(29). În consultare cu un specialist în boli infecţioase pediatrice, plasma de convalescent cu titru înalt poate fi luată în considerare de la caz la caz pentru copiii spitalizaţi care îndeplinesc criteriile EUA pentru utilizarea sa(29).
Favipiravir este un inhibitor al ARN-polimerazei care s-a utilizat pentru gripă şi infecţia cu virusul Ebola. Din cauza efectelor teratogene, utilizarea sa a fost autorizată doar pentru situaţii speciale, cum ar fi epidemii cu virusuri gripale noi. Nu este indicat la copii şi a fost folosit în China la paciente din grupe de vârstă fertilă doar dacă aveau testul de sarcină negativ şi întotdeauna asociat cu medicaţie contraceptivă pe durata tratamentului şi minimum 7 zile după oprirea acestuia; bărbaţilor li s-a recomandat, de asemenea, utilizarea de metode contraceptive pentru cel puţin o săptămână după încheierea tratamentului cu favipiravir(30).
Baricitinib este un inhibitor de Janus-kinază 1 şi 2, indicat în prezent în tratamentul poliartritei reumatoide şi al dermatitei atopice, care necesită tratament sistemic, fiind utilizat într-o doză standard de 4 mg/zi, doar ca alternativă de rezervă pentru corticosteroizi, în cazurile în care aceştia nu se pot administra(30). Nu există date suficiente pentru ca grupul să recomande fie pentru, fie împotriva utilizării baricitinibului în asociere cu remdesivir pentru tratamentul COVID-19 la copiii spitalizaţi la care corticosteroizii nu pot fi utilizaţi(29).
Tocilizumab este un antagonist de receptor de IL-6 folosit la un subgrup de pacienţi cu forme severe de COVID-19 la care există o activare excesivă a inflamaţiei („furtună de citokine”). Anterior, tocilizumab a mai fost utilizat în tratamentul sindromului de eliberare de citokine(30). Nu există date suficiente pentru ca grupul să recomande fie pentru, fie împotriva utilizării tocilizumabului la copiii spitalizaţi cu COVID-19 sau sindrom inflamator multisistemic la copii (SIM-C). Grupul nu recomandă împotriva utilizării sarilumabului pentru copiii spitalizaţi cu COVID-19 sau SIM-C(29). SIM-C este o complicaţie tardivă gravă a infecţiei cu SARS-CoV-2, care se poate dezvolta la unii copii şi adulţi tineri(29).
Se recomandă consultarea cu o echipă multidisciplinară atunci când se ia în considerare şi se administrează terapia imunomodulatoare pentru copiii cu SIM-C. Imunoglobulina intravenoasă şi/sau corticosteroizii sunt folosiţi în general ca terapie de primă linie, deşi antagoniştii interleukinei-1 au fost utilizaţi pentru cazuri refractare. Alegerea şi combinaţia optimă de terapii imunomodulatoare nu au fost stabilite definitiv(29).
Medicii de familie ar trebui să continue să utilizeze strategii de prevenire a infecţiilor, inclusiv(1):
Programarea vizitelor persoanelor bolnave şi a copiilor în diferite momente ale zilei.
Reducerea aglomeraţiei în sălile de aşteptare, cerând pacienţilor să rămână afară (de exemplu, să rămână în vehiculele lor, dacă este cazul) până când sunt chemaţi în unitate pentru programarea lor sau înfiinţarea de cabine de triaj pentru a examina pacienţii în siguranţă.
Luarea în considerare a telemedicinei pentru vizitele care nu implică vaccinare sau care nu necesită un examen fizic direct.
Sindromul inflamator multisistemic la copil
SIM-C este o complicaţie tardivă gravă a infecţiei cu SARS-CoV-2 care se poate dezvolta la unii copii şi adulţi tineri(29) (tabelul 4).
Prezentarea clinică a SIM-C
SIM-C poate debuta la câteva săptămâni după o infecţie cu SARS-CoV-2. Este posibil ca pacientul pediatric să fi fost infectat de un contact asimptomatic, fără ca aceştia să cunoască că au trecut prin infecţie(31).
Pacienţii cu SIM-C prezintă de obicei febră persistentă, dureri abdominale, vărsături, diaree, erupţii cutanate, leziuni mucocutanate şi, în cazuri severe, hipotensiune şi şoc(31).
Semnele şi simptomele includ febră persistentă, inflamaţie (pe baza rezultatelor testelor de laborator) şi dovezi ale disfuncţiei organelor sau şocului(31). Febra persistentă fără o sursă clinică clară este primul indiciu. Orice febră care este însoţită de simptome care afectează severitatea lor sau care coincide cu expunerea recentă la o persoană cu COVID-19 ar trebui să ridice suspiciunea pentru SIM-C(32).
Deşi au fost descrise diferite simptome, cele comune includ(22,31,32):
Caracteristici asemănătoare bolii Kawasaki (Kawasaki disease-like syndrome): conjunctivită, ochi roşu; mâini şi picioare roşii sau umflate; eczemă; buze roşii crăpate, adenopatii. La unii copii, au fost descrise dilataţii ale arterelor coronare şi/sau anevrisme. Unii copii care au prezentat sindrom asemănător bolii Kawasaki au avut predominant manifestări gastrointestinale (dureri abdominale sau diaree) şi neurologice (cefalee, meningită).
Simptome gastrointestinale, cum ar fi dureri abdominale, diaree, greaţă/vărsături (după infirmarea altor afecţiuni care se exprimă prin aceeaşi simptomatologie).
Caracteristici asemănătoare sindromului şocului toxic, cu instabilitate hemodinamică şi funcţie slabă a inimii.
Activarea furtunii de citokine/activarea macrofagelor sau caracteristici hiperinflamatorii.
Tromboză sau leziuni renale acute.
Respiraţia scurtă sugerează insuficienţă cardiacă congestivă sau embolie pulmonară.
Simptomele respiratorii raportate de obicei la adulţii cu COVID-19 pot să nu fie prezente la copiii şi adolescenţii cu SIM-C.
Rezultatele comune de laborator din rapoartele de caz au inclus(17,31,32):
Un nivel anormal de markeri inflamatori în sânge crecuţi, inclusiv VSH, CRP, feritină şi LDH.
Limfopenie <1000, trombocitopenie <150.000, neutrofilie.
Peptidă natriuretică de tip B crescută (BNP) sau NT-proBNP (pro-BNP), hiponatremie, creşterea D-dimerilor.

Evaluarea SIM-C
Examen de laborator:
Este indicată detectarea SARS-CoV-2 prin RT-PCR sau prin testul antigenic.
Unde este posibil, se sugerează testarea serologică SARS-CoV-2, chiar şi în prezenţa rezultatelor pozitive din testarea RT-PCR sau a antigenului. Orice testare serologică trebuie efectuată înainte de administrarea imunoglobulinei intravenoase (IVIG) sau a oricărui alt tratament anticorp exogen.
Alte evaluări
Având în vedere asocierea frecventă a SIM-C cu afectarea cardiacă, se recomandă: ecocardiogramă; electrocardiogramă; testarea enzimei cardiace sau a troponinei (conform standardelor de testare ale centrului) şi a peptidei natriuretice de tip B (BNP) sau NT-proBNP(31).
Alte teste pentru evaluarea implicării multisistemice trebuie să fie direcţionate în funcţie de semnele sau simptomele pacientului(31).
Tratamentul SIM-C
Nu există studii care să compare eficacitatea clinică a diferitelor opţiuni de tratament. Tratamentele au constat în primul rând în îngrijire de susţinere şi îngrijire îndreptată împotriva procesului inflamator de bază. Măsurile de susţinere au inclus:
resuscitarea fluidă;
suport inotrop;
suport respirator;
în cazuri rare, oxigenarea extracorporală arterio-venoasă cu membrană (ECMO).
Măsurile antiinflamatorii au inclus utilizarea frecventă a imunoglobulinelor intravenoase (IVIG) şi a steroizilor. Utilizarea altor medicamente antiinflamatorii şi utilizarea tratamentelor anticoagulante au fost variabile. Aspirina a fost folosită în mod obişnuit din cauza preocupărilor pentru implicarea arterei coronare, iar antibioticele sunt utilizate în mod obişnuit pentru a trata potenţialele sepsisuri, în aşteptarea culturilor bacteriene. Profilaxia trombotică este adesea utilizată, având în vedere starea de hipercoagulabilitate asociată în mod tipic cu SIM-C(31).
Pacienţii cu diagnostic de SIM-C ar trebui să urmeze un control ambulatoriu la interval scurt, inclusiv o monitorizare cardiologică pediatrică la 1-2 săptămâni după externare(31,32). Pacienţii diagnosticaţi cu leziuni miocardice trebuie să aibă restricţie pentru activităţi fizice(32).
Pacienţii care primesc terapie cu steroizi sau tratament cu substanţe biologice ar trebui să fie urmăriţi de reumatologul pediatric după externare(32).
Efectele lockdownului din pandemia
de COVID-19
Modificarea comportamentelor şi a stilului de viaţă la copiii cu obezitate
Un studiu observaţional longitudinal efectuat în Verona, Italia, care a inclus 41 de copii şi adolescenţi cu obezitate, a colectat date despre stilul de viaţă (inclusiv dietă, activitate fizică şi somn) la momentul iniţial şi la trei săptămâni de carantină. Rezultatele studiului au evidenţiat că nu au existat modificări în aportul de legume raportat, dar a crescut aportul de fructe; a crescut în schimb semnificativ consumul de chipsuri de cartofi, carne roşie şi băuturi îndulcite; timpul petrecut pentru activităţi sportive a scăzut cu 2,30 ore/săptămână, iar timpul de somn a crescut cu 0,65 oră/zi; timpul alocat ecranului a crescut cu 4,85 ore/zi. Concluzia studiului a fost că este necesar a recunoaşte aceste efecte colaterale adverse ale COVID-19 pentru a evita eşecul eforturilor în controlul menţinerii greutăţii în rândul tinerilor afectaţi de exces de adipozitate care, în funcţie de durata carantinării, pot avea un impact durabil asupra nivelului de adipozitate al unui copil sau adolescent(33).
Un sondaj naţional retrospectiv a fost condus în China (COINLICS), distribuit prin intermediul platformelor de socializare la începutul lunii mai 2020, unde 10082 de tineri participanţi (cu vârsta cuprinsă între 17,5 şi 24,7 ani, 71,7% femei, 63,2% trăind în zone nonurbane, 28% liceeni – majoritatea cu specializare în ştiinţe medicale, 69,6% studenţi – majoritatea specializaţi în ştiinţe sociale, 2,3% absolvenţi de studii superioare – majoritatea specializaţi în ştiinţe medicale) şi-au raportat în mod voluntar informaţiile sociodemografice de bază, privind greutatea şi stilul de viaţă în lunile anterioare şi în timpul carantinei induse de COVID‐19. Studiul a evaluat modificările în greutate şi tiparele de activitate în rândul tinerilor din China în timpul carantinei. Indicele mediu de masă corporală al tuturor tinerilor participanţi a crescut semnificativ (21,8-22,6) şi în toate subgrupele de educaţie în timpul carantinei. Creşteri au apărut, de asemenea, în prevalenţa supraponderalităţii/obezităţii (21,3-25,1%, P<0,001) şi a obezităţii (10,5% până la 12,9%, P<0,001) la tineri în general, în special la liceeni şi studenţi. Modelele lor de activitate s-au schimbat, de asemenea, în mod semnificativ, inclusiv în ceea ce priveşte frecvenţa scăzută a angajării pentru mers, treburile casnice de intensitate moderată/intensă, activitatea fizică cu intensitate moderată/intensă în timpul liber, precum şi sedentarismul crescut, somnul şi durata de utilizare a ecranelor(34).
Tulburări de sănătate mintală
Copiii şi adolescenţii sunt, probabil, mai susceptibili de a experimenta rate ridicate de depresie şi, cel mai probabil, anxietate în timpul şi după terminarea izolării forţate, iar acest lucru poate creşte pe măsură ce izolarea forţată continuă. Serviciile clinice ar trebui să ofere sprijin preventiv şi intervenţie timpurie acolo unde este posibil şi să fie pregătite pentru o creştere a problemelor de sănătate mintală. O metaanaliză a cercetat 80 de articole (80 de studii) publicate între 1 ianuarie 1946 şi 29 martie 2020, dintre acestea 63 de studii (un studiu a fost o investigaţie retrospectivă după o pandemie) raportând impactul izolării sociale şi al singurătăţii asupra sănătăţii mintale a copiilor şi adolescenţilor anterior sănătoşi (n=51.576; vârsta medie – 15,3 ani). Izolarea socială şi singurătatea au crescut riscul de depresie şi, eventual, anxietate în momentul în care singurătatea a fost măsurată şi între 0,25 şi 9 ani mai târziu. Această revizuire sistematică rapidă a 63 de studii cu 51.576 de participanţi a constatat o asociere clară între singurătate şi problemele de sănătate mintală la copii şi adolescenţi. Singurătatea a fost asociată cu viitoare probleme de sănătate mintală până la 9 ani mai târziu. Singurătatea a fost mai puternic asociată cu simptome crescute de depresie la fete şi cu anxietate socială crescută la băieţi. Durata singurătăţii pare a fi un predictor al viitoarelor probleme de sănătate mintală. Acest lucru are o relevanţă deosebită în contextul pandemiei de COVID-19, întrucât politicile din diferite ţări stabilesc durata în care şcolile ar trebui să rămână închise şi implementarea distanţării sociale în cadrul şcolilor(35).
Conflict of interests: The author declares no conflict of interests.
Bibliografie
- Centers for Disease Control and Prevention. COVID-19: information for pediatric healthcare providers 2020 Dec 30:https://www.cdc.gov/coronavirus/2019-ncov/hcp/pediatric-hcp.html.
- European Centre for Disease Prevention and Control. Risk assessment: Outbreak of acute respiratory syndrome associated with a novel coronavirus, China: first local transmission in the EU/EEA - third update.
- Weiss SR, Leibowitz JL. Coronavirus pathogenesis. Adv Virus Res. 2011;81:85–164.
- Su L, Ma X, Yu H, et al. The different clinical characteristics of corona virus disease cases between children and their families in China - the character of children with COVID-19. Emerg Microbes Infect. 2020;9:707–13.
- World Health Organization (WHO). WHO characterizes COVID‐19 as a pandemic [EB/OL].
- Zhou M-Y, Xie X-L, Peng Y-G, et al. From SARS to COVID-19, What we have learned about children infected with COVID-19. Int J Infect Dis. 2020;96:710–4.
- Shen K-L, Yang Y-H, Jiang R-M, et al. Updated diagnosis, treatment and prevention of COVID-19 in children, Experts’ consensus statement (condensed version of the second edition). World J Pediatr. 2020;16:232–9.
- Centers for Disease Control and Prevention. SARS-CoV-2–Associated Deaths Among Persons Aged <21 Years - United States, February 12–July 31, 2020.
- Ludvigsson JF. Systematic review of COVID-19 in children shows milder cases and a better prognosis than adults. Acta Paediatr. 2020;109:1088–95.
- Zhao Y, Cui C, Zhang K, et al. COVID19, A Systematic Approach to Early Identification and Healthcare Worker Protection. Front Public Health. 2020;8:205.
- Jarvis MC. Aerosol Transmission of SARS-CoV-2, Physical Principles and Implications. Front Public Health. 2020;8:590041.
- Centers for Disease Control and Prevention. Pathology and Pathogenesis of SARS-CoV-2 Associated with Fatal Coronavirus Disease, United States, Volume 26, Number 9-September 2020.
- Gale C, Quigley MA, Placzek A, et al. Characteristics and outcomes of neonatal SARS-CoV-2 infection in the UK, A prospective national cohort study using active surveillance. The Lancet Child & Adolescent Health. 2021;5:113–21.
- Norman M, Navér L, Söderling J, et al. Association of Maternal SARS-CoV-2 Infection in Pregnancy With Neonatal Outcomes. JAMA. 2021;325(20):2076-86.
- Samudrala PK, Kumar P, Choudhary K, et al. Virology, pathogenesis, diagnosis and in-line treatment of COVID-19. Eur J Pharmacol. 2020;883:173375.
- Assaker R, Colas A-E, Julien-Marsollier F, et al. Presenting symptoms of COVID-19 in children, A meta-analysis of published studies. Br J Anaesth. 2020;125:e330-e332.
- Cui X, Zhao Z, Zhang T, et al. A systematic review and meta-analysis of children with coronavirus disease 2019 (COVID-19). J Med Virol. 2021;93:1057–69.
- Poline J, Gaschignard J, Leblanc C, et al. Systematic SARS-CoV-2 screening at hospital admission in children:a French prospective multicenter study. Clin Infect Dis. 2020;72(12):2215-7.
- Maltezou HC, Magaziotou I, Dedoukou X, et al. Children and Adolescents With SARS-CoV-2 Infection, Epidemiology, Clinical Course and Viral Loads. Pediatr Infect Dis J. 2020;39:e388-e392.
- Struyf T, Deeks JJ, Dinnes J, et al. Signs and symptoms to determine if a patient presenting in primary care or hospital outpatient settings has COVID-19. Cochrane Database Syst Rev. 2021;2:CD013665.
- Mehta NS, Mytton OT, Mullins EWS, et al. SARS-CoV-2 (COVID-19), What Do We Know About Children? A Systematic Review. Clin Infect Dis. 2020;71:2469–79.
- Gallo Marin B, Aghagoli G, Lavine K, et al. Predictors of COVID-19 severity, A literature review. Rev Med Virol. 2021;31:1–10.
- Galván Casas C, Català A, Carretero Hernández G, et al. Classification of the cutaneous manifestations of COVID-19, A rapid prospective nationwide consensus study in Spain with 375 cases. Br J Dermatol. 2020;183:71–7.
- Andina D, Belloni-Fortina A, Bodemer C, et al. Skin manifestations of COVID-19 in children, Part 2. Clin Exp Dermatol. 2021;46:451–61.
- Andina D, Belloni-Fortina A, Bodemer C, et al. Skin manifestations of COVID-19 in children, Part 1. Clin Exp Dermatol. 2021;46:444–50.
- Boulad F, Kamboj M, Bouvier N, Mauguen A, Kung AL. COVID-19 in Children With Cancer in New York City. JAMA Oncol. 2020;6:1459–60.
- Islam N, Ebrahimzadeh S, Salameh J-P, et al. Thoracic imaging tests for the diagnosis of COVID-19. Cochrane Database Syst Rev. 2021;3:CD013639.
- Stegeman I, Ochodo EA, Guleid F, et al. Routine laboratory testing to determine if a patient has COVID-19. Cochrane Database Syst Rev. 2020;11:CD013787.
- National Institutes of Health NIH. Special Considerations in Children.
- Monitorul Oficial al României. Anul 189 (XXXIII)-Nr. 434, Vineri, 23 aprilie 2021, P A R T E A I LEGI, DECRETE, HOTĂRÂRI ŞI ALTE ACTE.
- Centers for Disease Control and Prevention. Information for Healthcare Providers about Multisystem Inflammatory Syndrome in Children (MIS-C).
- American Academy of Pediatrics. Multisystem Inflammatory Syndrome in Children (MIS-C) Interim Guidance, Critical Updates on COVID-19 / COVID-19 Interim Guidance/Multisystem Inflammatory Syndrome in Children (MIS-C) Interim Guidance.
- Pietrobelli A, Pecoraro L, Ferruzzi A, et al. Effects of COVID-19 Lockdown on Lifestyle Behaviors in Children with Obesity Living in Verona, Italy, A Longitudinal Study. Obesity (Silver Spring). 2020;28:1382–5.
- Yang S, Guo B, Ao L, et al. Obesity and activity patterns before and during COVID-19 lockdown among youths in China. Clin Obes. 2020;10:e12416.
- Loades ME, Chatburn E, Higson-Sweeney N, et al. Rapid Systematic Review, The Impact of Social Isolation and Loneliness on the Mental Health of Children and Adolescents in the Context of COVID-19. J Am Acad Child Adolesc Psychiatry. 2020;59:1218-1239.e3.




