Hipersensibilitatea imediată la inhibitori de pompă de protoni – discuţii pe marginea unui caz de anafilaxie la lansoprazol
Proton pump inhibitors immediate hypersensitivity – a lansoprazole anaphylaxis case discussion
Abstract
Proton pump inhibitors are a class of medication widely used in practice, both as prescription and self administered – over the counter (OTC), due to a high incidence of chronic gastritis and gastric ulcer, as well as Helicobacter pylori infection. They have a good therapeutic index and a low incidence of side effects. Though, a few anaphylactic reactions for omeprazole and derivates have been described – case reports or small series. The reported cases have been explored using prick skin tests and intradermic reaction – a specific and quite sensitive method. The literature mentions only two reports of in vitro positive tests – one FAST and one CAST. I present the case of an episode of anaphylaxis to lansoprazole, preceded by isolated dermographic urticaria after the same drug administration, explored with a positive CAST-ELISA test (the third positive in vitro report in the whole world literature) and revised the specific allergologic diagnostic management.Keywords
anaphylaxislansoprazoleprotone pump inhibitorsCASTimmediate drug hypersensitivityRezumat
Inhibitorii de pompă de protoni reprezintă o clasă de medicamente frecvent utilizată în practica clinică, atât sub formă de prescripţie medicală, cât şi autoadministrate (OTC), în condiţiile unei incidenţe mari a gastritei cronice şi a ulcerului gastric, respectiv a infecţiei cu Helicobacter pylori. Inhibitorii de pompă de protoni au un indice terapeutic bun şi o incidenţă redusă a evenimentelor adverse. Au fost însă înregistrate şi descrise câteva reacţii anafilactice la omeprazol şi alţi derivaţi din aceeaşi clasă – cazuri izolate sau serii mici de pacienţi. Cazurile raportate au fost frecvent explorate prin testare cutanată prick şi intradermoreacţie, metodă specifică şi destul de sensibilă; în literatură există doar două raportări de teste in vitro pozitive, unul de tip FAST şi altul CAST. Se descrie cazul unei paciente cu un episod de anafilaxie la lansoprazol, precedat de episoade de urticarie dermografică izolată după administrarea acestuia, obiectivată cu un test de eliberare de mediatori CAST-ELISA pozitiv (al treilea test in vitro pozitiv raportat în lume, conform literaturii consultate) şi se revede conduita diagnostică alergologică specifică.Cuvinte Cheie
anafilaxielansoprazolinhibitori de pompă de protoniCASThipersensibilitate imediată medicamentoasăIntroducere
Aproximativ 25% din reacţiile adverse medicamentoase sunt reacţii de hipersensibilitate, care pot fi cauzate de aproape toate clasele de medicamente, indiferent de structura chimică, complexitate sau calea de administrare(1).
Anafilaxia reprezintă cea mai severă manifestare imediată de hipersensibilitate medicamentoasă, cu potenţial letal. Într-o analiză a peste 4000 de cazuri de anafilaxie din Germania, Austria şi Elveţia, medicamentele se găseau pe locul al treilea în topul triggerilor (15,1% din cazuri, după veninul de insecte şi alimente)(2).
Incidenţa gastritei cronice şi a ulcerului gastric este de aproximativ 10% din populaţia globală, conform raportărilor la nivelul anilor 2000. Actualmente, incidenţa pare a fi revizuită în scădere, mai ales în ţările dezvoltate, în concordanţă cu nivelul de trai crescut al populaţiei. În acelaşi timp, infecţia cu Helicobacter pylori, responsabilă în mare parte de sindromul dispeptic de tip ulceros, are o incidenţă de până la 35-50% din populaţie (cu vârfuri în Asia şi America Centrală), incidenţă care creşte odată cu înaintarea în vârstă. Persistenţa infecţiei este asociată în 15% din cazuri cu ulcerul gastric, iar în 0,5-2% din cazuri, chiar cu adenocarcinom gastric şi limfom gastric MALT (mucosa-associated lymphoid tissue).
Ca urmare, inhibitorii de pompă de protoni (IPP) au o utilizare extrem de largă în cadrul populaţiei, atât sub prescripţie medicală, cât şi în autoadministrare. În SUA se găsesc în top 10 medicamente prescrise, iar în Danemarca sunt folosite de 7,4% din populaţia adultă.
Prezentare de caz
Este prezentat cazul unei paciente de 32 de ani, care a venit pentru o consultaţie alergologică a doua zi după o reacţie sistemică, incluzând prurit şi eritem generalizat, rinoree, obstrucţie nazală, eritem conjunctival, greaţă şi diaree, stare de slăbiciune/presincopă, apărute la ora 2 noaptea, la două ore după administrarea unui comprimat de lansoprazol pentru pirozis. Pacienta respectivă consumase cu 4 ore înainte masa de seară (salată de icre, pâine, struguri) şi neagă ingestia de alcool, efectuarea vreunui efort fizic sau administrarea unei alte medicaţii în decursul acelei zile. Văzând reacţia, şi-a autoadministrat un comprimat de loratadină şi un comprimat de metoclopramid şi a chemat un echipaj de Salvare, care i-a administrat suplimentar hemisuccinat de hidrocortizon 200 mg i.v. şi i-a recomandat să continue cu loratadină un comprimat pe zi şi dexametazonă o fiolă injectabilă i.m. pe zi pentru încă două zile.
Tratamentul cu lansoprazol a fost început în urmă cu 8 luni, iniţial 40 de zile încontinuu, apoi intermitent, la nevoie, în cazul senzaţiei de pirozis, aproximativ un comprimat la 1-2 luni, în cadrul indicaţiei gastroenterologice pentru o gastrită cronică obiectivată prin tranzit baritat. Ultima doză de lansoprazol înaintea zilei în care a apărut reacţia descrisă fusese administrată cu 2-3 săptămâni în urmă.
De câteva săptămâni, pacienta remarcase zile în care prezenta urticarie dermografică, pe care le-a identificat anamnestic ca fiind zilele în care lua, intermitent, câte un comprimat de lansoprazol.
Ca antecedente personale patologice, se notează episoade recurente de lucită polimorfă, un episod de pitiriazis rozat Gilbert şi o rinită persistentă uşoară, predominant obstructivă. Pe linia antecedentelor heredocolaterale marcante în sfera alergologică, pacienta a remarcat că tatăl său avea diagnostic de hipersensibilitate la AINS/pirazolonice (la aspirină).
Analizele uzuale sunt fără modificări la nivelul HLG, biochimiei, complementului C3, C4, triptazei bazale serice, dar cu o valoare crescută a IgE totale, 210,5 UI/ml. Se efectuează testare cutanată screening pentru aeroalergene uzuale, care reiese negativă, înclinând orientarea spre un diagnostic secundar de rinită persistentă uşoară, probabil nealergică.
Se pune diagnosticul prezumtiv de etapă de anafilaxie gradul II în observaţie postmedicamentoasă la lansoprazol şi se indică deocamdată evitarea clasei inhibitorilor de pompă de protoni.
Se recomandă reevaluare gastroenterologică şi se efectuează endoscopie digestivă superioară, care decelează modificări minime de reflux gastroesofagian, ceea ce pare a fi liniştitor pentru a continua abstinenţa medicaţiei din clasa inhibitorilor de pompă de protoni. Pacienta ia la nevoie în locul acestora şi tolerează un antihistaminic H2 (famotidină), al cărui nucleu este 2-guanidino-thiazolic (înlocuind nucleul imidazolic al cimetidinei).
La patru săptămâni de la reacţie se realizează testul seric de determinare in vitro a mediatorilor de reacţie imediată la lansoprazol CAST (Cellular Antigen Stimulation Test) – ELISA, care revine pozitiv: 333 pg/ml (cut-off 200pg/ml). Testul CAST presupune expunerea bazofilelor extrase din serul pacientului în contact cu IL3 şi cu alergenul, medicament sau altă substanţă chimică. Bazofilele sensibilizate la alergen eliberează sulfidoleucotriene, care sunt măsurate printr-un test ELISA. Se determină astfel eliberarea de leucotriene printr-un mecanism fie IgE dependent, fie non-IgE mediat(3).
Pacienta temporizează testarea cutanată şi nu se mai prezintă iniţial. Revine însă la un an, declarând că şi-a autoadministrat esomeprazol şi omeprazol, pe care le-a tolerat.
Discuţii
După apariţia omeprazolului, în 1989, urmat de lansoprazol, în 1995, clasa inhibitorilor de pompă de protoni a cunoscut o extindere rapidă în utilizarea clinică, şi datorită faptului că reacţiile adverse s-au dovedit a fi, în decursul anilor, puţine şi uşoare (la 1,5-3% dintre consumatori).
Recent, a crescut însă numărul raportărilor unor reacţii asociate cu un termen lung de utilizare a acestora (de exemplu, creşterea numărului fracturilor de şold, al pneumoniilor de aspiraţie, al enterocolitelor cu Clostridium difficile şi, recent, al bolilor renale şi insuficienţei renale cronice cu 33% faţă de populaţia generală la pacienţii care consumă continuu peste 1 an medicaţia de tip inhibitori de pompă de protoni). Este discutabil însă dacă unele sunt efecte ale acestei clase sau ale altor asocieri medicamentoase la IPP, cea mai frecventă fiind cu clasa AINS.
IPP sunt administraţi eficient în patologii gastroenterologice frecvente, precum ulcerul, boala de reflux gastroesofagian, gastrite, inclusiv cele provocate de AINS, sindromul Zollinger-Elison, precum şi în eradicarea infecţiei cu Helicobacter pylori, fiind asociaţi dublei antibioterapii, unde clasa de IPP se dovedeşte fundamentală. Modul de acţiune este prin inhibarea competitivă a pompei gastrice parietale H+/K+ ATP-aza şi prin creşterea pH-ului gastric.
Structural, IPP sunt benzimidazoli modificaţi cu câte un inel piridinic. Actualmente, sunt 7 molecule de IPP: omeprazol (OTC în SUA), lansoprazol, dexlansoprazol, esomeprazol, pantoprazol, rabeprazol şi ultimul membru, ilaprazol, dezvoltat pe piaţa asiatică, actualmente în curs de aprobare de către Food and Drug Administration (FDA).
Asemănările structurale îi împart în două subgrupe:
- lansoprazolul şi rabeprazolul (şi desrabeprazolul) au substituenţi diferiţi pe inelul piridinic (trifluoroetoxi şi, respectiv, metoxi-propoxi), dar nucleul lor benzimidazolic este identic;
- omeprazolul (şi esomeprazolul), pantoprazolul şi ilaprazolul au substituenţi diferiţi pe nucleul benzimidazolic (metoxi-, respectiv difluorometoxi şi -pirolic), având inelul piridinic identic.
- Conform acestor asemănări structurale, se identifică patru modele diferite de cross-reactivitate în cadrul reacţiilor alergice, atât imediate, cât şi tardive(4):
- Patternul A: pacienţi alergici la omeprazol, esomeprazol, pantoprazol şi ilaprazol, dar tolerând lansoprazolul şi rabeprazolul.
- Patternul B: pacienţi alergici la lansoprazol şi rabeprazol, dar tolerând omeprazolul, esomeprazolul şi pantoprazolul.
- Patternul C: pacienţi cu sensibilizare selectivă la un singur IPP, care tolerează toţi ceilalţi membri ai clasei IPP.
- Patternul D: pacienţi alergici la toate moleculele de IPP.
În literatură există, în afara cazului de faţă, 36 de raportări de cazuri de hipersensibilitate imediată la medicamente din clasa IPP, însumând un număr de 185 de pacienţi cu simptome de anafilaxie. Se poate observa, consultând tabelul 1, că majoritatea sunt raportări de unu sau două cazuri, existând doar două şiruri mari de 53 de cazuri (Bonadonna, 2012) şi de 65 de cazuri (Kepil Ozdemir, 2013)(4).
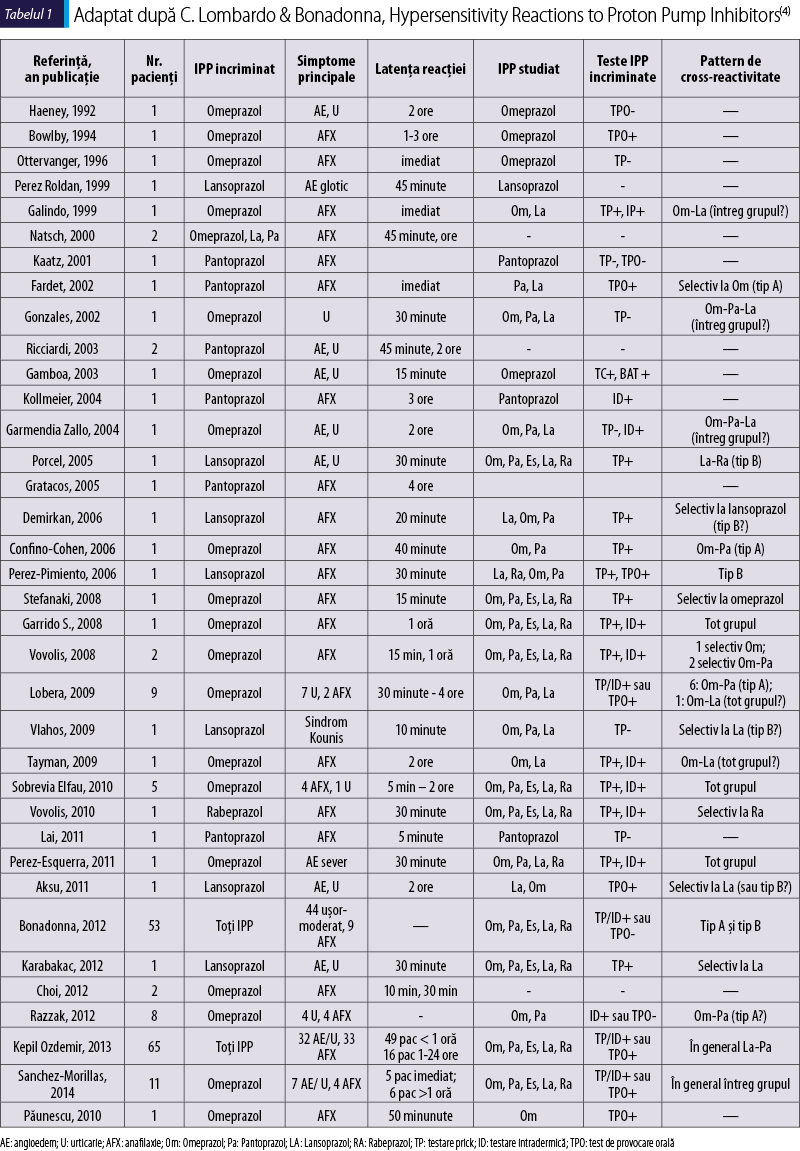
Cele două serii mai mari de cazuri raportează o frecvenţă a distribuţiei celor mai numeroase cazuri de anafilaxie uşor diferită: Bonadonna(5) raportează în 30% din cazuri ca agent etiologic esomeprazolul, 26,4% lansoprazolul şi 18,9% omeprazolul, pe când Kepil Ozdemir(6) raportează în 68,3% din cazuri ca agent cauzal lansoprazolul, 20% pantoprazolul, 10% esomeprazolul, 6,7% rabeprazolul şi omeprazolul în 1,5% din cazuri. Aceasta poate fi şi datorită unei prescripţii diferite a IPP în cele două regiuni.
Un alt aspect important al manifestărilor de hipersensibilitate la IPP este timpul de latenţă între momentul administrării dozei şi apariţia simptomelor. În general, acestea apar până într-o oră de la ingestie, dar există şi frecvente raportări (25% în seria raportată de Kepil Ozdemir(6)) în care simptomele debutează între 1 şi 24 de ore, uneori începând de la 3 ore. Acest fapt poate fi explicat prin formularea farmaceutică de tip eliberare prelungită, care protejază IPP de degradarea acidă în stomac, absorbţia având loc astfel în intestinul subţire proximal şi întârziind astfel declanşarea simptomatologiei. În plus, într-un caz cu anafilaxie tardivă recurentă la pantoprazol s-a formulat ipoteza variaţiei activităţii enzimelor citocromului P450, astfel încât metabolizatorii lenţi prezintă o acumulare a medicamentului şi o creştere a semivieţii plasmatice.
În 2013, Bose et al.(7) au publicat un review extensiv al cazurilor de hipersensibilitate la IPP şi au arătat că la 86% din 118 pacienţi erau imediate, toate la adulţi, cu vârsta medie de 46±13 ani, cu excepţia unui singur caz, la un adolescent cu simptome la două ore după administrarea omeprazolului.
Deşi iniţial păreau foarte rare, recent s-a publicat însă şi o serie de 69 de cazuri de reacţii de hipersensibilitate tardivă, analizată de un grup de autori din Taiwan, între 2003 şi 2016 (C.-y. Lin(8)).
Mecanismul molecular al hipersensibilităţilor imediate şi tardive la IPP este încă neclar. Majoritatea IPP sunt metabolizaţi prin intermediul sistemului citocromului P450, cu principalele izoenzime CYPC19 şi CYP3A4(8):
- omeprazolul şi esomeprazolul sunt metabolizaţi predominant prin CYP2C19 (80% din clearance);
- lansoprazolul şi rabeprazolul sunt metabolizaţi prin CYP2C19 şi CYP3A4.
- pantoprazolul este metabolizat în principal de o enzimă din afara sistemului CYP, o sulfotransferază.
Activitatea CYP2C19 variază destul de mult, în funcţie de etnie, fiind mai scăzută în populaţia asiatică; se poate face o legătură cu prevalenţa aparent mai mare a hipersensibilităţii tardive la IPP în zona asiatică.
Timpul de înjumătăţire plasmatică al omeprazolului, lansoprazolului şi rabeprazolului este scurt: 1-2 ore.
Teste de diagnostic
Conform recomandărilor recente (2016) publicate de Grupul de Interes pentru Medicamente din cadrul EAACI(9), diagnosticul hipersensibilităţii medicamentoase imediate se efectuează prin testare cutanată prick şi intradermică, teste serologice (IgE specific, teste de activare a bazofilelor), urmate de test de provocare orală în cazuri selecţionate.
Testarea cutanată a fost realizată în majoritatea cazurilor raportate ca reacţii de hipersensibilitate la IPP, din păcate nu şi în cazul pacientei noastre.
Recomandările din „Concentraţiile pentru testarea cutanată pentru medicaţia administrată sistemic – Position paper al grupului de interes în alergiile medicamentoase al EAACI/ENDA“(10) din 2013 privind concentraţiile non-iritante de testare ale IPP sunt:
- testare cutanată prick cu soluţiile de uz parenteral nediluate (în cazul omeprazolului, esomeprazolului, pantoprazolului) sau cu un comprimat sfărâmat şi dizolvat în 1 ml ser fiziologic (pentru lansoprazol şi rabeprazol, unde nu există formă farmaceutică pentru administrare parenterală);
- testare intradermică la concentraţie de 40 mg/ml cu soluţiile de uz parenteral.
Cu toate acestea, concentraţiile utilizate de diverşi autori pentru testarea intradermică variază destul de mult, conform tabelului 2.
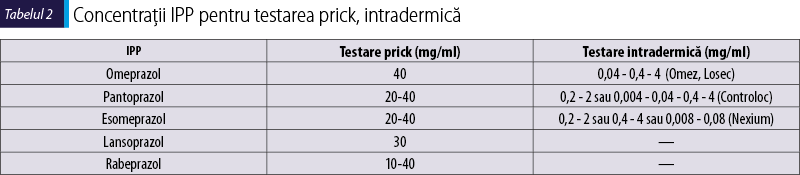
Testarea intradermică s-a efectuat, în funcţie şi de istoricul reacţiei, cu concentraţii variabile ale soluţiei de administrare parenterală – de la 0,002 sau 0,004 mg/ml până la 0,4 mg/ml, rar 4 mg/ml. Unii autori au folosit chiar soluţia rezultată prin diluţia unui comprimat sfărâmat în ser fiziologic şi pentru testare intradermică, dar în general procedura nu este recomandată şi poate genera reacţii falspozitive.
Testarea cutanată s-a dovedit a fi sigură, fără reacţii sistemice raportate.
Seriile mai mari de cazuri, precum cea a lui Kepir Ozdemir(6), raportează indici foarte buni în privinţa testelor cutanate raportate la corelarea cu testele de provocare: specificitate 100%, valoare predictivă pozitivă 100%, sensibilitate 58,3% şi valoare predictivă negativă 70,8%.
De asemenea, seria publicată de Bonadonna(4) concluzionează că există aceeaşi specificitate şi aceeaşi valoare predictivă pozitivă, de 100%, cu o sensibilitate de 61,3% şi o valoare predictivă negativă de 91,9%.
Un singur studiu aminteşte că probabilitatea ca testele cutanate să fie relevante pentru diagnostic descreşte în timp, ele fiind indicat a fi efectuate cât mai aproape de momentul reacţiei, începând cu 4-6 săptămâni şi până la 6-9 luni de la acesta.
Metode experimentale precum ELISA sau ImmunoCap/Phadia pentru determinarea IgE specifice la IPP (câteva la omeprazol) nu au dat rezultate satisfăcătoare, fiind negative(11,12).
Se raportează, în schimb, până în prezent, doar două cazuri în care testele de activare celulară, alternativă, in vitro, pentru evidenţierea hipersensibilităţii imediate, au fost pozitive:
CAST pozitiv pentru pantoprazol(13) (şi test de provocare orală de asemenea pozitiv, cu reacţie de anafilaxie);
BAT - FAST pozitiv pentru omeprazol, corelat cu o testare cutanată pozitivă la acesta(14).
Cazul de faţă raportează a treia ocazie în care o testare in vitro revine pozitivă într-un caz de anafilaxie la IPP (test CAST-ELISA) şi primul caz pentru lansoprazol.
Ca opţiuni de tratament în cazurile de anafilaxie la IPP şi indicaţie fermă de tratament antiacid, există:
- clasa antihistaminicelor H2;
- variante de alte molecule de IPP alese conform testării cutanate prick şi intradermice negative şi testate prin test de provocare orală controlată intraspitalicesc;
- desensibilizare, în caz de aparentă hipersensibilitate la toţi membrii clasei de IPP şi de indicaţie absolută a acestui tratament (frecvent pentru eradicarea Helicobacter pylori).
Există publicat un singur caz în care s-a realizat cu succes un protocol de desensibilizare la omeprazol(15). S-au utilizat granulele din capsulă de omeprazol diluate în soluţie de bicarbonat, începându-se de la concentraţia de 0,002 mg/ml, cu creşteri seriate de 18 ori la fiecare 20 de minute, pe parcursul a 5-6 ore, până la doza de 32,665 mg, pacientul tolerând ulterior omeprazolul 20 mg de două ori pe zi, timp de 14 zile (conform tabelului 3). Interesant este că s-au repetat testele cutanate a doua zi după desensibilizarea reuşită, acestea arătând dimensiuni mult scăzute ale papulei şi eritemului.

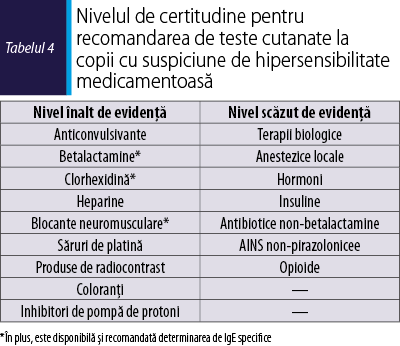
Un alt aspect de menţionat ar mai fi înscrierea clasei de IPP între recomandările grupului EAACI de interes pediatric privind hipersensibilitatea medicamentoasă pentru testare cutanată la copii, cu un nivel de evidenţă mai mare privind coeficienţii de performanţă a rezultatelor(16), conform tabelului 4.
Un alt subiect de discutat este posibila cross-reactivitate cu alte molecule cu structură asemănătoare, cu nucleu imidazolic sau benzimidazolic. Cele mai utilizate clase de medicamente cu această structură sunt:
- antiprotozoare (metronidazol, tinidazol, secnidazol, ornidazol);
- antihelmintice (albendazol, mebendazol= nitro-imidazol, tiabedazol, fenbendazol, oxenbendazol, oxibendazol, triclabendazol);
- antifungice (ketoconazol);
- antiemedice – domperidonă;
- neuroleptice – droperidol;
- antihistaminice H1 (mizolastină, astemizol);
- antihistaminice H2 (cimetidină).
M.A. Gonzalo-Garijo et al. au prezentat cazul unui pacient cu hipersensibilitate imediată la mizolastină, presupusă imunologică, dar fără a se putea demonstra mecanismul IgE-mediat, pacient care a tolerat ulterior omeprazolul(17).
Într-un alt caz, raportat de R. Gonzalez-Mendiola, omeprazolul a fost bine tolerat la o pacientă cu hipersensibilitate imediată la mebendazol şi albendazol(18).
M. Kaatz et al. nu au observat cross-reactivitate între omeprazol şi alţi derivaţi de benimidazol-ketoconazol sau derivaţi de imidazol-metronidazol ori cimetidină(13).
În cadrul acestor alte structuri benzimidazolice, se raportează cross-reactivitate patch între metronidazol, tinidazol, albendazol şi ketoconazol şi cross-reactivitate din punct de vedere al testării (provocării orale) între tinidazol, albendazol şi metronidazol.
Concluzii
Ţinând cont de acurateţea crescută a testelor cutanate în cadrul diagnosticului reacţiilor imediate la IPP, acestea se recomandă a fi executate la o gamă largă sau chiar la toţi IPP când aceştia se impun în tratament, pentru a creiona tabloul de cross-reactivitate în cadrul clasei de IPP pentru fiecare pacient.
Pot fi precedate de teste de activare celulară, precum testul de activare a bazofilelor cu determinare flowcitometrică (FAST) sau chiar de testul CAST, care par a se corela pozitiv cu reactivitatea imediată la IPP.
Ulterior, acestea sunt completate de teste de provocare orală cu alternative sau, mai rar, de protocoale de desensibilizare la IPP. Acestea se recomandă a fi în concordanţă cu ultimele recomandări formulate în 2014 de Position Paper „International Consensus on drug allergy“(19).
Bibliografie
- J Szebeni, S Fishbane, M Hedenus, S Howaldt, F Locatelli, S Patni, D Rampton, G Weiss and J Folkersen. Hypersensitivity to intravenous iron: classification, terminology, mechanisms and management. British Journal of Pharmacology (2015) 172 5025–5036.
- Worm Margitta et al. Triggers and Treatment of Anaphylaxis, An Analysis of 4000 Cases From Germany, Austria and Switzerland. Dtsch Arztebl Int. 2014 May; 111(21): 367–375.
- PC Potter. Clinical Indications and Interpretation of the CAST. Current Allergy & Clinical Immunology, March 2006 Vol 19, No. 1.
- Lombardo C & Bonadonna P. Hypersensitivity Reactions to Proton Pump Inhibitors. Curr Treat Options Allergy (2015) 2: 110.
- Bonadonna Patrizia et al. Hypersensitivity to proton pump inhibitors: Diagnostic accuracy of skin tests compared to oral provocation test. Journal of Allergy and Clinical Immunology, Volume 130, Issue 2 , 547–549.
- Kepil Özdemir S, Öner Erkekol F, Ünal D, Büyüköztürk S, Gelincik A, Dursun A, B, Karakaya G, Bavbek S. Management of Hypersensitivity Reactions to Proton Pump Inhibitors: A Retrospective Experience. Int Arch Allergy Immunol 2016; 171:54-60.
- S Bose. Evaluation and management of hypersensitivity to proton pump inhibitors. Annals of Allergy, Asthma & Immunology Volume 111, Issue 6, December 2013, Pages 452-457.
- Lin C-y, Wang C-W, Hui C-YR, et al. Delayed-type hypersensitivity reactions induced by proton pump inhibitors: A clinical and in vitro T-cell reactivity study. Allergy. 2018; 73:221–229.
- Mayorga C, Celik G, Rouzaire P, Whitaker P, Bonadonna P, Cernadas JR, Vultaggio A, Brockow K, Caubet JC, Makowska J, Nakonechna A, Romano A, Montañez MI, Laguna JJ, Zanoni G, Gueant JL, Oude Elberink H, Fernandez J, S Viel, Demoly P, Torres MJ. In vitro tests for drug hypersensitivity reactions: an ENDA/EAACI Drug Allergy Interest Group position paper on behalf of in vitro tests for Drug Allergy Task Force of EAACI Drug Interest Group. Allergy 2016; 71: 1103–1134.
- Brockow K, Garvey LH, Aberer W, Atanaskovic-Markovic M, Barbaud A, Bilo MB, Bircher A, Blanca M, Bonadonna B, Campi P, Castro E, Cernadas JR, Chiriac AM, Demoly P, Grosber M, Gooi J, Lombardo C, Mertes PM, Mosbech H, Nasser S, Pagani M, Ring J, Romano A, Scherer K, Schnyder B, Testi S, Torres M, Trautmann A, Terreehorst I, on behalf of the ENDA/EAACI Drug Allergy Interest Group. Skin test concentrations for systemically administered drugs – an ENDA/EAACI Drug Allergy Interest Group position paper. Allergy 2013; 68: 702–712.
- Vovolis V, Koutsostathis N, Stefanaki E. IgE-mediated anaphylaxis to proton pump inhibitors - cross-reacting study. Allergy. 2008 Sep; 63(9):1251-2.
- Por Javier Reyes Balaguer, Ángel Campos Andreua, Dolores Hernández Fernández de Rojas. Anafilaxia secundaria a inhibidores de la bomba de protons. Med Clin (Barc). 2007;128:799.
- Kaatz M, Bauer A, Hipler C, Elsner P. Nonallergic anaphylaxis to pantoprazole. Allergy. 2002 Feb; 57(2):184.
- Gamboa PM, Sanz ML, Urrutia I, Jáuregui I, Antépara I, Diéguez I, De Weck AL. CD63 expression by flow cytometry in the in vitro diagnosis of allergy to omeprazole. Allergy. 2003 Jun; 58(6):538-9.
- Confino-Cohen R, Goldberg. Anaphylaxis to omeprazole: diagnosis and desensitization protocol. A. Ann Allergy Asthma Immuno, 2006 Jan; 96(1):33-6.
- Gomes ER, Brockow K, Kuyucu S, Saretta F, Mori F, Blanca-Lopez N, Ott H, Atanaskovic-Markovic M, Kidon M, Caubet J-C, Terreehorst I on behalf of the ENDA/EAACI Drug Allergy Interest Group. Drug hypersensitivity in children: report from the pediatric task force of the EAACI Drug Allergy Interest Group. Allergy 2016; 71: 149–161.
- Gonzalo-Garijo MA, Jiménez-Ferrera G, Bobadilla-González P, Cordobés-Durán C. Hypersensitivity Reaction to Mizolastine: Study of Cross Reactions. J Investig Allergol Clin Immunol 2006; Vol. 16(6): 391-393.
- Gonzalez-Mendiola R, Martínez Borque N, Palomeque Rodríguez T, Torrecillas Toro M, Martínez Bohigas D. Type I allergic reaction to benzimidazole antihelmintics. Allergy. 2007 Jun; 62(6):713-4.
- Demoly P, Adkinson NF, Brockow K, Castells M, Chiriac AM, Greenberger PA, Khan DA, Lang DM, Park H-S, Pichler W, Sanchez-Borges M, Shiohara T, Thong BY-H. International Consensus on drug allergy. Allergy 2014; 69: 420–437.
